コンテンツ
ACE2のアップレギュレーション
クルクミン
www.ncbi.nlm.nih.gov/pmc/articles/PMC6153927/
レスベラトロール
高脂肪食の消費はマウスのACE2遺伝子発現を下方制御する。 オスマウスでのみ、高脂肪食が腎臓のACE2活性低下を引き起こした。 ラットへのレスベラトロール投与は、ACE2の増加を示しており、食事からのレスベラトロールは、高脂肪食によるACE2の影響を軽減する可能性がある。
journals.physiology.org/doi/abs/10.1152/ajpendo.00150.2020
スタチン
スタチンはACE2をアップレギュレートする。 COVID-19感染症の患者の、急性呼吸器疾患症候群(ARDS)による死亡リスクを下げるか?
過去の実験的研究で、ジェネリックのスタチンとARB併用投与がエボラ患者のARDSを改善している。
mbio.asm.org/content/11/2/e00398-20
アトルバスタチン
アトルバスタチン処理されたアテローム性動脈硬化症ウサギの心臓、腎臓で〜2倍のACE2タンパク質の増加が示された。
運動
運動は、SARS-CoV-2感染のより大きなリスクの一因となる可能性がある。[R]
スピロノラクトン
CHF患者の単球由来マクロファージでACE2活性を4〜196倍に増加させた。CHFでは心臓ACE2を有意に増加させることはできなかった。
[R]
PPARγアゴニスト
テルミサルタン
ロシグリタゾン
イルベサルタン
[R]
喫煙とニコチン
現喫煙者では、未喫煙者と比較して肺のACE2発現を25%増加させる。
TMRPSS2遺伝子発現は喫煙とは関連していなかった。
α7ニコチン性アセチルコリン受容体
喫煙は、α7-nAChRシグナル伝達によるSARS CoV-2の細胞取り込みメカニズムを促進する可能性があることを示唆する。in vitro
重度COVID-19の喫煙患者、COPD患者に特有の脆弱性を説明するかもしれない。
ニコチン
中国の予備的研究では、COVID-19入院患者の喫煙率が異常に低いことが観察された。(P <0.0001) 喫煙は保護的な役割の可能性を示唆しており、以前から知られているように、喫煙によるACE2発現のダウンレギュレーションと関連している可能性がある。
www.qeios.com/read/article/541
ニコチンは、ACE2をダウンレギュレートすることにより、ACE-アンジオテンシンII-AT1受容体軸をアップレギュレートし、RASのホメオスタシスを変えることを強く示唆する。
pubmed.ncbi.nlm.nih.gov/30088946/
遺伝子発現情報データベース(GEO)の分析 喫煙が肺内気道および口腔上皮細胞のACE2発現を増加させ、反対に長期間の禁煙はACE2発現を低下させることが確認された。 喫煙者はHCoV-19に対する感受性が高いことが示される。
www.preprints.org/manuscript/202003.0078/v1
参考記事
https://alzhacker.com/covid19-nicotini…olinergic-system/
ACE2発現の増加に関与する遺伝的変異体
rs4646127、rs2158082、rs5936011、rs6629110、rs4830983、rs5936029
東アジアの集団では95%以上が保有しており、ヨーロッパ集団では低い(52-65%)
www.nature.com/articles/s41421-020-0147-1
ACE2の阻害
アンジオテンシン変換酵素IIの阻害活性を有する生理活性化合物;COVID-19の管理と予防のためのスタート
www.sciencedirect.com/science/article/pii/S0306987720306952
これまでCOVID-19の治療法やワクチンは明らかにされていない[1]。COVID-19の標的となる可能性が高いアンジオテンシン変換酵素II(ACE-II)受容体は、ウイルスの肺胞細胞への伝達に重要な役割を果たしている[2]。したがって、ACE-II受容体を阻害または調節する可能性のある薬剤は、COVID-19の管理に有効である可能性がある[3]。
生理活性化合物は、このような感染症の薬剤開発やアジュバント治療に有用である。これらの化合物は、予防薬または治療促進剤として作用しうる。
- ナリンジン(COVID-19のACE-III受容体への結合を阻害する可能性を有するフラバノン-7-O-配糖体)、
- ナリンジンおよびヘスペレチン(フラバノン)、
- ヘスペリジン(フラバノン配糖体)、
- バイカリンおよびネオヘスペリジン(フラバノン配糖体)などが挙げられる。
- ノビレチン(O-メチル化フラボン)、
- スクテラリン(フラボン)、
- ニコチンアミン(非タンパク性アミノ酸)、
- グリチルリチン(サポニン)、
- エモジン(6-メチル-1,3,8-トリヒドロキシアントラキノン)
は、天然のACE-II阻害剤の中でも最も重要なものである[4], [5], [6]。
シクロオキシゲナーゼII、インターロイキン-6および-1β、一酸化窒素合成酵素などのプロ抑制性サイトカイン(COVID-19感染症で増加)に対するナリンジンの影響は相当なものである[5]。グリチルリチンは、COVID-19のSタンパク質のACE-II受容体への結合を阻害することができる[7]。生理活性抗ウイルス剤であるエモジンは、ACE-II受容体へのSタンパク質の結合を阻害する可能性がある。したがって、エモジンおよびおそらくアロエモジンは、ACE-IIとの結合においてS-タンパク質と競合することでCOVID-19の感染を食い止めることができると考えられる[7]。これらの化合物の豊富な供給源は、Rheum palmatum L.およびAloe vera (L.) Burm.f.である[8]。
このような見解に基づき(図1)、これらの化合物は、COVID-19の予防および管理に単独で、または従来の介入との併用で応用することができると考えられる。
SARS-CoV-2 3CLproとアンジオテンシン変換酵素Ⅱを標的としたCOVID-19に対する潜在的な漢方薬のIn Silicoスクリーニング
link.springer.com/article/10.1007%2Fs11655-020-3476-x
表1. SARS-CoV-2 3CL および ACE2 を有する代表的な成分と臨床的に推奨される薬剤の結合エネルギー 化合物式 MW 3CLpro (kJ/mol) ACE2 (kJ/mol)
- プエラリン C21H20O10 432.38 -33.47 -38.07
- ビククリン C20H20O10 432.38 -33.47 -38. 07
- ビクマリン C20H17NO6 367.40 -26.78 -41.42
- ルテオリン C15H10O6 286.24 -26.78 -36.82
- ケルセチン C15H10O7 302.24 -26.36 -36.40
- イソラムネチン C16H12O7 316.27 -25.95 -35.15
- イリソリドン C17H14O6 314.29 -25.53 -38.49
- ロピナビル C37H17NO6 367.40 -26.78 -41.42
- リトナビル C37H48N6O5S2 720.94 -24.69 -36.40
- レムデシビル C27H35N6O8P 602.58 -25.94 -36.40
- アルビドール C22H25BrN2O3S 531.89 -28.03 -30.54
- クロロキン C18H26ClN3 319.87 -24. 30 -27.20
- リバビリン C37H48N6O5S2 720.96 -25.52 -32.22
- ニタゾキサニド C12H9N3O5S 307.28 -23.85 -34.73
ACE阻害作用をもつ食品
ACE-1の阻害により増加したアンジオテンシンIは、ACE-2を上方制御する傾向がある。動物モデルの実験においては、ACE-1阻害剤とARBの両方が、心臓ACE-2の活性を増加させることが示されている。
www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.104.510461
ACE阻害薬は、COVID-19の重症化リスクを高める可能性がある。
academic.oup.com/jtm/advance-article/doi/10.1093/jtm/taaa041/5809509
味噌、大豆発酵食品、豆類
www.jstage.jst.go.jp/article/jbrewsocjapan/110/9/110_636/_pdf/-char/ja
www.sciencedirect.com/science/article/abs/pii/S0963996909002671
ソイプロテイン
pubmed.ncbi.nlm.nih.gov/11170618
豆腐よう(沖縄の豆腐を使った発酵食品)
www.jstage.jst.go.jp/article/nskkk/57/5/57_5_181/_article/-char/ja/
タンニン
南アフリカ伝統部族のヒーラーが高血圧の治療に使用している20の植物のうち7つがACE阻害活性を示した。
pubmed.ncbi.nlm.nih.gov/10624863
生姜
生姜抽出物は、in vitroにおいてラット心臓のACEを阻害する。
pubmed.ncbi.nlm.nih.gov/23875904
高コレステロール食を与えられたラットにおける2種類のショウガ(Zingiber Officinale)によるアンギオテンシン1変換酵素活性の阻害。in vivo
pubmed.ncbi.nlm.nih.gov/24433069
にんにく
Allium Ursinum、Allium Sativum
野生のニンニクの葉の水抽出物が最も高いACE阻害活性を示した。
pubmed.ncbi.nlm.nih.gov/1620734/
アンドログラフィス
Andrographis paniculataの水抽出物の循環ACE低下作用
pubmed.ncbi.nlm.nih.gov/8886488
イカ
europepmc.org/article/agr/ind44601560
スピルリナ・クロレラ
pubmed.ncbi.nlm.nih.gov/14961345
わかめ
ワカメ(Undaria pinnatifida)から、ACE阻害特性を持つ4つのテトラペプチドが単離された。
pubmed.ncbi.nlm.nih.gov/11091100
なまこ
+アミノ酸(プロリン)
www.ncbi.nlm.nih.gov/pmc/articles/PMC6117704/
バイカリン
アンジオテンシン変換酵素(ACE)を阻害
pubmed.ncbi.nlm.nih.gov/15305324/
pubmed.ncbi.nlm.nih.gov/22136493/
ACE阻害活性を有する6つの植物
www.ncbi.nlm.nih.gov/pmc/articles/PMC3896793/
ロサルタン
コロナウイルス誘発肺損傷に対するロサルタンの潜在的な保護的役割
いくつかの病理学的状態では、AT1の過剰活性化は、TGF-β発現の増加を介して、異なる臓器(例えば、肝臓や肺)の線維化などの有害事象につながる可能性がある。ロサルタンは、アルドステロンの放出を含むAngⅡの生理的作用を打ち消す。
ロサルタンは、レニンとAngIIの下流作用を中和し、最終的に血圧を低下させることができる。
ロサルタンは、AT1 受容体の選択的アンタゴニストであり、内臓線維化の分子経路として知られている。RAS 系における ACE-AngII-AT1 軸の阻害作用を示す。 このように、ロサルタンはCOVID-19による肺障害の予防薬として期待されている。また、ロサルタンは、TGF-β1 のダウンレギュレーションなど、他の分子機構を介して肺線維化を抑制する可能性がある。
腸内ACE2/アミノ酸・トリプトファン
ACE2は、RAASに依存しない機能を有する。腸内では、細胞性ACE2(循環していないACE2)がアミノ酸の吸収を調節し、腸内細菌のバランスを整えて腸内
炎症を調節する。
腸管上皮細胞におけるACE2は、中性アミノ酸トランスポーター
腸管上皮細胞におけるB0AT1の複合体の存在。ACE2-B0AT1複合体が存在しない場合、血清中の中性のアミノ酸のバリン(Val)、スレオニン(Thr)、チロシン(Tyr)、必須アミノ酸のトリプトファン(Trp)が著しく減少し、重度の腸内炎症と微生物のアンバランスをもたらした。
ACE2ノックアウトマウスにおいて Trpまたはニコチンアミド(Trpの代謝産物)との投与は、抗菌ペプチドα-デフェンシンの発現を増加させ、上述したような逆効果をもたらす可能性がある。
COVID-19重症・重症の解剖学的所見と病理学的所見によれば、小腸もSARS-CoV-2感染により重篤な損傷を受けたことが示唆されている。
仮説
SARS-CoV-2はTMPRSS2を介して肺や腸に侵入する。
免疫系がSARS-Cov2感染を克服できない場合、SARS-CoV-2は大量に複製され、細胞ACE2を占有することになる。宿主の細胞を破壊し Ang II-AT1 シグナルは不活性化することができない。 続いて腸の機能が破壊され炎症が悪化する。その結果、サイトカインストームが発生し、最終的には呼吸器系、循環器系、その他の臓器の機能を失う。
腸内ACE2を回復させる
腸内の細胞内ACE2/B0AT1はウイルスによって破壊される。
必須アミノ酸が吸収できず、抗菌ペプチドのが減少し、腸内マイクロバイオームの生態が損なわれる。これらの腸の変化は炎症を深化させる。その結果、サイトカインストームが起こり、最終的には多臓器不全を引き起こす。
必須アミノ酸の補給治療
トリプトファンまたはニコチンアミドの投与は、重度の腸管を逆転させる可能性があることが示されている。ACE2ノックアウトマウスでは炎症を抑制している。栄養増強剤として、トリプトファンとその代謝物は腸内細菌叢の維持、微生物代謝、宿主の免疫システム、腸内細菌叢の維持に重要な役割を果たしている。
宿主-マイクロバイオームインターフェース、および宿主免疫系-腸内細菌叢相互作用
トリプトファンまたはニコチンアミドの補給は、腸内マイクロバイオームを調節し、腸内細菌を増加させる可能性がある。抗菌ペプチドで腸内のSARS-CoV-2誘発病変を変換し、さらに改善するために全身性の条件である。
まとめると、ACE2はSARS-CoV-2細胞の侵入に必須の役割を果たしており、その影響はCOVID-19の重症・重症状態の経過と予後に関与する。ACE2関連の調節酵素やアミノ酸の摂取量を増やすことが疾患制御に望ましいと考えられる。
www.fox10phoenix.com/news/doctor-offers-coronavirus-protection-advice
組換えヒト(rh)ACE2の外因性サプリメント
erj.ersjournals.com/content/early/2020/05/07/13993003.01560-2020
組換えヒト(rh)ACE2の外因性サプリメントは、Covid-19の治療において素晴らしいアイデアかもしれない。可溶性ACE2は、可溶性受容体への結合がSARS-CoV-2の侵入をブロックすることが示されており、ウイルスの広がりに影響を与える可能性がある。
非常に驚くべきことに、Changeuxら[4]は、ニコチン受容体もまた、病態生理において重要な役割を果たしており、COVID-19感染症の予防と制御のための標的となりうると仮説を立てている。
繰り返しになるが、基本的なレベルでは、SARS-CoV-2ウイルスは、ニコチンと受容体を競合させるニコチン性物質であるという仮説です。この仮説のバックボーンは、制御された設定の下で、ニコチン剤(ニコチンパッチのような)は、Covid-19のような急性感染症に対して効率的な治療法を提供し得ることを提案している。
可溶性ACE2は、可溶性受容体への結合がSARS-CoV-2の侵入をブロックすることが示されているため、ウイルスの拡散に影響を与える可能性がある。Batlleら[6]は、適切な組換えACE2タンパク質として可溶性の形態で与えられた場合、これはCovid-19の拡散に対抗するための新たな手段を表すかもしれないと論じている。
同様に、Guoら[7]は、組換えヒト(rh)ACE2を外因性に補充することは、コビド-19の治療において素晴らしいアイデアであるかもしれないと考えている。
ここでは、可溶性ACE2は、SARS-CoV-2の表面上のスパイクタンパク質を中和するための餌として作用し、その結果、侵入を阻害する可能性がある。さらに、Guoらは、最近の研究で、rhACE2の融合タンパク質(Fcフラグメントを有する)がSARS-CoV-2の受容体結合ドメインに高い親和性で結合していることを示したことを参照している。
SARS-CoV-2感染を軽減するためのデコイとしての修飾アンジオテンシン変換酵素2(ACE2)の吸入投与
改変された組換えヒトACE2を吸入すると、SARS-CoV-2に結合し、肺障害を軽減する可能性がある。このおとり作戦は、有害な免疫反応を引き起こす可能性は低く、高リスク群における罹患率と死亡率を減少させる可能性がある。
pubmed.ncbi.nlm.nih.gov/32438383/
レニン・アンジオテンシン系
www.nature.com/articles/s41440-020-0476-3
ACE2のダウンレギュレーションはCOVID-19におけるレニン-アンジオテンシン系の過剰刺激を誘導する。
レニン-アンジオテンシン系をブロックすべきか?
レニン-アンジオテンシン系(RAS)は、血圧、血漿カリウム、肺上皮膜の安定性を調節する血行力学的・生物学的システムである(図1)[4]。この系では、2つの拮抗経路がバランスをとっている。
一つはアンジオテンシノーゲン経路で、アンジオテンシノーゲンが(レニンによって)アンジオテンシンIに変換された後、アンジオテンシン変換酵素(ACE)によってアンジオテンシンIIに変換される。アンジオテンシンIIはアンジオテンシンII 1型受容体(AT1R)に付着して活性化し、血管収縮、アルドステロン分泌刺激、低カリウム血症、肺上皮分解を誘導する[5]。
レニン-アンジオテンシン系(RAS)の調節
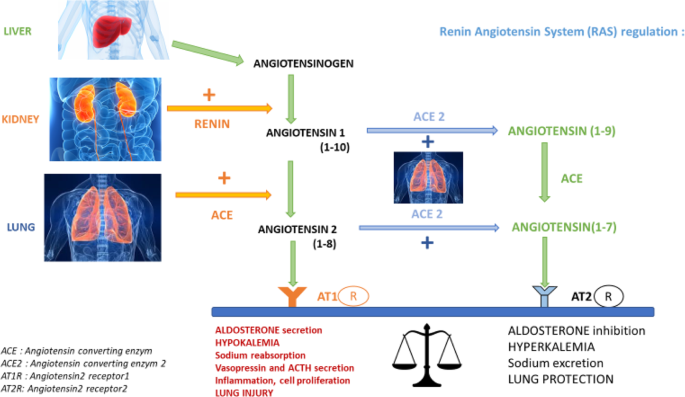
アンジオテンシン系がバランスをとる第二の方法は、第二のアンジオテンシン変換酵素(ACE2)[6, 7]を含む。この経路は、アンジオテンシンI [1,2,3,4,5,6,7,8,9,10]およびアンジオテンシンII [1,2,3,4,5,6,7,8]の一部を、そのAT1R受容体に付着する前に変換する。
アンジオテンシンIおよびIIのリン酸化産物は、アンジオテンシン1-9およびアンジオテンシン1-7である。これらはアンジオテンシンII型2型受容体レシーバーに付着し、AT1Rと比較してアンタゴニスト効果を誘導する[8]。
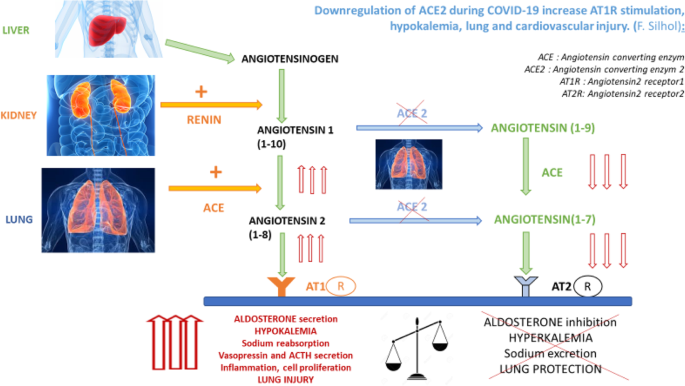
感染期(図2)では、COVID-19ウイルスはACE2の酵素受容体を利用して宿主細胞に侵入する[9、10]。
コロナウイルスがACE2と結合すると、ACE2のダウンレギュレーションをもたらすことが示されており[11]、ACE2の低下はアンジオテンシンのアンジオテンシン1-7血管拡張剤への変換の低下をもたらすため、ACEを介したアンジオテンシン2の増加に寄与することが示されている[12]。
ACE2のレベルが低いほど、アンジオテンシンI [1,2,3,4,5,6,7,8,9,10]およびアンジオテンシンII [1,2,3,4,5,6,7,8]が分解されにくくなる;したがって、それらの形質濃度は徐々に増加する。
アンジオテンシン1-10の増加とアンジオテンシン1-9の減少
米国の集中治療室では、アンジオテンシン1-10の増加とアンジオテンシン1-9(そのACE2処理産物)の減少がARDSの予後不良と相関していることが示されている[1]。
図2に示すように、ARDSの予後不良の原因となるアンギオテンシン1-10(ACE2の処理産物)の増加と減少は、ARDSの予後不良との相関があることが示されている。
COVID-19の間のACE2のダウンレギュレーションは、AT1R刺激、低カリウム血症、および肺および心血管障害を増加させる。このように、アンジオテンシンII濃度の上昇およびAT1Rの刺激は、肺内皮の安定性の低下および呼吸窮迫の悪化につながる[13, 14]。
低カリウム血症
その他の作用としては、アルドステロンの分泌増加、カリウレシスによる低カリウム血症、およびナトリウム再吸収の増加と炎症が挙げられる[15]。COVID-19の患者では低カリウム血症が頻繁にみられる。中国のあるチームは最近、低カリウム血症が不良な転帰と関連していることを報告した(武漢の経験)[16]。
RAS阻害剤
逆に、RASブロッカーはACE2を増加させ、潜在的に細胞内へのウイルス負荷を促進する可能性がある[17]。我々は、ACE2のダウンレギュレーションによって誘導されるRASの大きな不均衡が、COVID-19患者における好ましくない進行の必須要素であると考えている。この不均衡の生物学的マーカーは低カリウム血症であるように思われる。
ロサルタン
インフルエンザおよびエボラ肺感染症におけるいくつかの研究では、炎症およびサイトカインの減少を伴うAT1Rブロッカーの肺損傷に対する有益な役割が示されている[18,19,20,21]。2 つの動物実験では、ロサルタンは ACE2 発現の増加を示した[22, 23]。
ロサルタンは、ミネソタ大学が最近米国で開始した COVID-19 患者を対象とした 2 つの試験(clinical trials.gov NCT04311177 および NCT104312009)でも選択された分子である。治療評価(ISRA-COV)の前にCOVID+患者(SAR-COV)におけるRASのキネティクスを文書化するための予備的研究を開始した。
ACE阻害薬
COVID-19患者における慢性ACE阻害薬曝露と重症化率低下との関連性
Association Between Chronic ACE Inhibitor Exposure and Decreased Odds of Severe Disease in Patients With COVID-19
pubmed.ncbi.nlm.nih.gov/32628137/
方法
ACEi または ARB への曝露に関連した重症化(14 日以上の入院、集中治療室への入院、または死亡と定義)のオッズを特定することを目的としたレトロスペクティブ・コホート研究を実施した。2020年3月9日から5月11日の間にイスタンブール医学部コロナセンターに入院したCOVID-19の成人患者(年齢≧18歳)を対象とした。ACEi、ARB、または他の降圧薬の慢性使用者を、年齢、性別、入院前の病欠日数、併存疾患、喫煙、降圧レジメンの回数、ドキサゾシン使用、フロセミド使用、血清クレアチニン値に応じてマッチさせた。重症化した場合のオッズ比(OR)を算出した。
結果
COVID-19で入院した患者は合計611人で、逆転写酵素ポリメラーゼ連鎖反応またはコンピュータ断層撮影(CT)のいずれかで確認された。男性は363人で、年齢は18歳から98歳までで、平均年齢は57±15歳であった。このうち重症者は165人(死亡53人、症例死亡率8.7%)であった。
高血圧患者(n=249)では、統計的に有意ではなかったが、ARB曝露は重症化のオッズ低下(OR=0.60、95%CI:0.27-1.36、p=0.31)と相性があり、ACEi曝露は重症化のリスクを有意に低下させた(OR=0.37、95%CI:0.15-0.87、p=0.03)。
ACEi投与は、ベースラインCTで認められた浸潤の軽度化、C反応性蛋白質とフェリチンの低下、単球数の増加、入院期間の短縮、特定の経験的治療(favipiravirとmeropenem)の必要性の低下と関連していた。
結論。我々のデータは、COVID-19肺炎においてACEi薬への曝露が良好な効果をもたらす可能性を示唆している。

