COVID-19:神経放射線学者のための入門書
ACE2はヒトの脳全体に広く発現しており、主にグリア細胞に発現しているが、心肺系を制御する脳幹核、網状体活性化系、運動野にも発現している。
呼吸機能の変調に重要な役割を果たすソリタリウス核とアンビグス核に蓄積する傾向があり、重度の呼吸機能障害への寄与が研究上の関心事である。
SARS-Cov2ウイルスが中枢神経系内に入ると、ウイルスによって誘発された調節不能な宿主免疫応答が「サイトカインストーム」を引き起こすことが示されている。このサイトカインストームとウイルス粒子による直接的な細胞病的損傷は、感受性の高い人では脳炎、急性弛緩性麻痺、または急性壊死性脳症(ANE)などの神経疾患を引き起こす可能性がある。
link.springer.com/article/10.1007%2Fs00234-020-02437-5
神経系の関与によるCOVID-19の新たな証拠
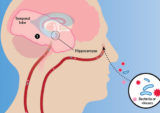
SARS-CoV-2ウイルスが中枢神経系に到達するには、血行性、転写性、およびニューロンの逆行性伝播経路が提案されている。 神経系への正確な経路は、これらの経路のいずれか、またはその組み合わせである可能性がある。
pubs.acs.org/doi/10.1021/acschemneuro.0c00181
SARS-CoV-2感染が神経変性疾患および神経精神疾患に及ぼす影響:遅発性パンデミックの一例
もう一つの全く知られていない点は、子供や青年における一見軽度の感染が、長期的には認知能力に変化をもたらし、精神疾患の出現を促進する可能性があるということです。ウイルスによる免疫系の変化は、小児期や思春期にシナプス/細胞の剪定の変化を引き起こし、成人期になって初めて明らかになる問題を引き起こす可能性がある。
老化との関連性
重度の新型コロナウイルス感染が、長期的には罹患組織だけでなく、脳を含む他の臓器でも、生存者の老化を加速させる可能性がある。
SARS-CoVは、宿主細胞のミトコンドリアとミトコンドリア機能を操作して、先天的な宿主免疫を回避する。
H1N1は、宿主のUPSを乗っ取る。
ウイルスによるオートファジー、HSP阻害、レドックスの不均衡、活性酸素種の増加、リソソームの機能不全など。
onlinelibrary.wiley.com/doi/abs/10.1002/mds.28084
COVID-19の長期的な影響
20%の低酸素/虚血性脳症
SARS-CoV-2の神経萎縮症の可能性 COVID-19が確認された患者では、重度の呼吸器合併症を発症する患者の併存疾患として脳血管疾患が挙げられる。例えば、ある研究では、死亡したCOVID-19患者113人のうち約20%の低酸素/虚血性脳症が報告されている。
最近の研究では、中国からCOVID-19と診断された214人の患者を評価し、36%が急性脳血管障害や意識障害を含む神経学的症状を呈していたことが明らかになった。急性出血性壊死性脳症の1例も報告されている。別の最近の研究(フランス)では、COVID-19患者64人中58人の神経学的特徴が報告されており、脳症、顕著な動揺と錯乱、皮質脊髄路徴候などが含まれている。
SARS患者のCSF中にSARS-CoV RNAが検出されたことが報告されている。前臨床研究では、動物性のCoVだけでなく、ヒト(例えば、HCoV-OC43)も中枢神経系に到達し、脳炎を引き起こすことがさらに示されている。
多発性硬化症
さらに、多発性硬化症(MS)患者のヒト脳組織およびCSFでは、CoV抗原およびRNAが検出されており、MSを含む中枢神経系自己免疫の病因因子として、CoVが示唆されている。また、神経変性疾患との関連性も示唆されている。 例えば、CoV-OC43およびCoV-229Eはパーキンソン病患者のCSFで発見されている。
特筆すべきは、脳の炎症は、少なくとも部分的には、ウエストナイル、ジカ、単純ヘルペスウイルスの感染に伴う中枢神経系の損傷の下敷きとなることが示されており、中枢神経系で長期的な炎症プロセスが発達していく条件となる。
さらに、ウイルス感染に関連した激しい全身性の炎症反応は、血液脳関門(BBB)の破壊を引き起こしうる。これにより、末梢性サイトカインが中枢神経系へのアクセスを可能にし、脳炎につながる神経炎症を誘発または悪化させる可能性がある 。
長期的な中枢神経系への影響の可能性
ヒトの神経変性疾患は、多くの場合、場合によっては数十年をかけて徐々に進行していく。現在、世界中で多数の若年成人が SARS-CoV-2 に感染しているか、近い将来に感染する予定である。
急性または慢性感染時に誘発される炎症反応は、神経変性疾患の初期段階の基礎となる初期および不顕性のメカニズムを誘発または加速させる可能性がある。
神経症状・神経変性疾患
さらに、神経変性疾患や他のウイルス感染症における知見は、全身性の炎症性メディエーターが中枢神経系にアクセスし、BBB機能の障害を介して損傷を誘発することを示唆しているため、SARS-CoV-2感染によって誘発された全身性の炎症は、神経炎症プロセスにさらに寄与し、神経症状への感受性を増加させる可能性がある。
このように、中枢神経系感染症は、すでにリスクを抱えている患者の神経変性疾患の発症を促進する可能性がある。
現在の理解では、感染者が数年後、数十年後に高齢化し、SARS-CoV-2感染によって誘発される全身性および/または脳の炎症反応により、神経変性疾患の発生率の広範な増加につながるメカニズムの引き金となるかもしれないと思われる。
重度のCOVID-19による脳損傷の明確な兆候
www.eurekalert.org/pub_releases/2020-06/uog-cso061820.php
コロナウイルス感染症(COVID-19)で病院で治療を受けている特定の患者は、脳損傷の臨床的および神経化学的徴候を示すことが、ヨーテボリ大学の研究で明らかになった。中等度のCOVID-19症例でも、脳損傷の血液ベースのバイオマーカーを見つけて測定することが可能であることが証明された。
コロナウイルスSARS-CoV-2に感染した人の中には、軽い風邪のような症状しか出ない人もいれば、重症化して病院での治療を必要とする人もいる。後者の中には、脳が本来の機能を発揮していないことが明らかになっている。これらのケースは一般的なものではないが、発生している。
アストロサイトの損傷
ヨーテボリ大学Sahlgrenskaアカデミーのプロジェクトでは、入院中に軽度、中等度、重度のCOVID-19を有する47人の患者から血液サンプルを採取した。これらのサンプルは、脳損傷の高感度バイオマーカーを用いて分析された。その結果は、年齢と性別を一致させた33人の健康な対照群と比較された。
この研究が『Neurology』誌に発表された今、バイオマーカーの1つが中等度のCOVID-19でも増加していることが明らかになった。GFAP(グリア線維性酸性タンパク質)として知られるこのマーカーは、通常、アストロサイト(脳内の星型神経細胞を支える細胞型)に存在するが、アストロサイトの損傷や過剰活性化の場合には漏出してしまう。
バイオマーカー NfL(ニューロフィラメント軽鎖タンパク質)
第二のバイオマーカーは、NfL(ニューロフィラメント軽鎖タンパク質)である。これは通常、脳の神経突起の内部に存在し、安定化の役割を果たしているが、損傷を受けると血液中に流出する。血漿中のNfL濃度の上昇は、人工呼吸器治療を必要とした患者のほとんどで認められ、その上昇の程度と重症度との間には顕著な相関関係があった。
「特に、時間経過に伴うNfL濃度の上昇は、集中治療に関連した研究で以前に見られたものよりも大きく、これはCOVID-19が実際に直接脳損傷をもたらす可能性があることを示唆している。これを引き起こしているのがウイルスなのか免疫システムなのかは現時点では不明であり、より多くの研究が必要です」
と、Sahlgrenskaアカデミーの研究チームが測定を行った教授であり、神経科学の教授でもあるヘンリックZetterberg氏は言う。
マグヌス Gisslén、Sahlgrenska アカデミーの感染症の教授と感染症科、Sahlgrenska 大学病院の主任医師は、COVID-19 に関するアカデミーの臨床研究をリードしている。
同氏の見解では、脳損傷に関連するバイオマーカーの血液検査は、中等度から重度のCOVID-19を持つ患者のモニタリングに利用され、脳損傷のリスクを軽減できる可能性があるという。
「現在提案されている新しいデキサメタゾン治療のような新しい治療法でNfLの増加を遅らせることができるかどうかを見ることは非常に興味深いことであろう 」とGisslén氏は言う。
関連記事