コンテンツ
pubmed.ncbi.nlm.nih.gov/37841274
オンライン公開 2023年9月29日 .
PMCID: PMC10570809
PMID:37841274
Stacie Z. Bergcorresponding author * and Jonathan Bergcorresponding author *
要旨
どこにでもある黒い色素であるメラニンは、紫外線吸収に反応して生成される活性酸素の消去、金属の吸収、熱調節、薬物の取り込み、自然免疫系機能、酸化還元、エネルギー伝達など、免疫系において重要な役割を果たしている。
脳、心臓、動脈、卵巣など、多くの種類の組織がメラニンを含んでいる。ほとんど全ての細胞がメラニンの前駆体を含んでいる。
メラニンおよび/または神経メラニンが失われる疾患の数は増えており、例えばアルツハイマー病(AD)、パーキンソン病(PD)、レビー小体型認知症(LBD)、白斑など、感染性の病因があると考えられるようになってきている。
AD、PD、LBD、白斑は、メラノソームに侵入してアポトーシスを引き起こすヘルペスウイルスや、腸内環境の異常や炎症と関連している。ヘルペスウイルスは、腸内細菌異常症や炎症とも関連している。
通常の健康な状態では、メラニンは電磁波から吸収したエネルギーの一部を保持し、それが細胞の燃料として使われ、ATPからのエネルギーがそのエネルギー供給を補完するために使われる、というのが我々の理論である。
私たちはさらに、メラニンが失われると細胞のエネルギー供給が減少し、AD、PD、LBDの場合、免疫系の防御が維持できなくなり、疾患に関連したプラークを除去することができなくなると推論している。
さらに、これらのプラークを除去しても認知や気分が改善しない理由や、これらの患者の認知や気分に波がある理由を説明するために、我々は、認知症状を引き起こすのはプラークではなく、むしろ病原体に対する免疫系の反応から生じる脳内の炎症であると仮定している。
メラニンに保持されたエネルギーは、ATPと逆相関で細胞を活性化するという我々の理論は、メラノーマ、白斑、健康な細胞において、メラニン量とATP産生の変化を示す研究によって支持されている。従って、メラニンレベルの変化は、多くの疾患の核心にあるのかもしれない。われわれは、メラニンレベルを調節することが、治療法開発の新たな道を開く可能性があることを提案する。
キーワードパーキンソン病、レビー小体型認知症、アルツハイマー病、メラニン、グリホサート、炎症、アミロイドプラーク、腸内マイクロバイオーム
AIキーワード解説
ユーメラニン
- 色: ユーメラニンは、茶色から黒色の色素です。
- 化学構造: ユーメラニンは、ポリマー構造を持ち、チロシンから生合成されます。チロシナーゼ酵素の作用により、チロシンがドーパキノンに変換され、さらに複雑なポリマーへと重合します。
- 機能: ユーメラニンは、紫外線を吸収し、皮膚や体内組織を紫外線によるダメージから保護する役割を持っています。また、色の濃淡によって個体の外見に影響を与えます。
フェオメラニン
- 色: フェオメラニンは、黄色から赤色の色素です。
- 化学構造: フェオメラニンもチロシンから生合成されますが、システインが組み込まれることで異なる化学構造を持ちます。このシステインの組み込みにより、フェオメラニンはユーメラニンとは異なる色と化学的特性を持ちます。
- 機能: フェオメラニンは紫外線をある程度吸収しますが、ユーメラニンほどの保護効果はありません。その代わり、フェオメラニンは皮膚や髪の色に明るい色調を与えることができます。
ニューロメラニン
- 存在場所: ニューロメラニンは主に人間や他の哺乳類の脳内、特に中脳の黒質(substantia nigra)や網膜に存在します。
- 機能: ニューロメラニンの正確な生物学的機能は完全には解明されていませんが、神経保護作用があると考えられています。また、パーキンソン病などの神経変性疾患との関連が研究されています。
- 化学構造: ニューロメラニンは、ユーメラニンやフェオメラニンとは異なる複雑な高分子であり、その構造は完全には解明されていません。ドーパミンなどのカテコラミンの酸化によって形成されると考えられています。
リソソームメラニン
- 存在場所: リソソームメラニンは、細胞のリソソーム内で見られるメラニン類似物質です。
- 機能: このタイプのメラニンは、細胞内での鉄イオンの過剰な蓄積を防ぐ役割を持つと考えられています。
- 化学構造: リソソームメラニンの詳細な化学構造はまだ完全には明らかにされていません。
これらのメラニン類似物質は、特定の生物学的環境や条件下でのみ生成され、特有の機能や役割を持っています。ニューロメラニンは特に興味深い研究対象であり、その機能や神経変性疾患との関連についての研究が進められています。しかし、これらのメラニン類似物質も、ユーメラニンやフェオメラニンと同様に、生物の保護、生理機能、および疾患との関連性を理解する上で重要な役割を果たしています。
1. はじめに
認知症は、認知障害、記憶喪失、判断力の低下、錯乱、興奮、無気力などを特徴とする(1)。アロイス・アルツハイマー(Alois Alzheimer)、そしてその少し後にフリッツ・ハインリッヒ・レヴィ(Fritz Heinrich Lewy)が、脳内の特徴的なプラークを認知症と結びつけ(2,3)、後にそれぞれアルツハイマー病(AD)、パーキンソン病(PD)として知られるようになった。これらのプラークを標的とする薬物やその他の治療法では、これらの疾患を適切に治療したり、進行を止めたり、治癒させたりすることは見つかっていないにもかかわらず、これらのプラークは一般に原因であると考えられ続けている。私たちは、神経変性疾患やその他の疾患の患者において何が起こっているのかについて、仮説に行き詰っている。AD、PD、レビー小体型認知症(LBD)が脳内のプラークによって引き起こされるのではないとすれば、これらの神経変性疾患は何によって引き起こされるのだろうか?
神経変性疾患やその他の疾患において見落とされているのは、メラニンの役割である。メラニンは主に、遺伝的に有害な紫外線(UV)を吸収し、熱として放出することで知られる色素であり、免疫系の一部である。一般的に濃い色をしており(ユーメラニンとニューロメラニン)、ニューロメラニンは加齢とともに増加するが(4)、AD、PD、LBD患者では著しい減少がみられる(5-7)。メラニンには抗酸化作用もあり、活性酸素種(ROS)を減少させる(8)。したがって、これらの神経変性疾患において見られる酸化ストレスの上昇は、メラニン/ノイロメラニンの消失と関連していると考えられる。これらの疾患ではミトコンドリア機能障害も見られ(9,10)、神経変性疾患で見られる酸化ストレスの上昇とミトコンドリア機能障害を関連付ける研究が増えている(11)。それは、メラニンには電子貯蔵・輸送能力があり、ミトコンドリアから供給されるエネルギーと逆の関係で細胞にエネルギーを供給しているように見えるということである。
微生物もまた、病因学的パズルの一部として一般には見過ごされてきた。しかし、AD、PD、LBD、多発性硬化症(MS)、筋萎縮性側索硬化症(ALS)など、認知に影響を及ぼすさまざまな脳疾患は感染と関連しており、AD、PD、LBDの脳のプラークにはこれらの病原体が封入されていることが判明している。したがって、プラークは病原体の存在に対する正常な免疫系の反応の一部である可能性があるが(12)、これらの疾患の患者の脳ではクリアーではない。これはなぜかという疑問につながる。
私たちは、脳の免疫システムがプラークを除去できないのは、メラニンの消失によるものだと理論化している。具体的には、メラニンのエネルギー貯蔵の役割に注目し、メラニンとその電子貯蔵・輸送能力が疾患の基盤にあると理論化する。ここでは、AD、PD、LBD、白斑、黒色腫をモデルとしているが、これらはすべて、メラニンレベルの減少(AD、PD、LBD、白斑)または増加(黒色腫)によって特徴づけられる。さらに最近では、腸内細菌叢とその結果生じる炎症との関連も、これらの神経変性疾患の一因として認識されるようになった(11)。重要なことは、先に述べたように、これらの神経変性疾患は病原体との関連がますます強まっているということである。これらの疾患に共通するのはヘルペスウイルス(13–18)である。興味深いことに、偶然の一致ではないが、メラニン欠乏を特徴とする白斑もヘルペスウイルス(19)、腸内細菌異常症(20)、認知症発症リスクの増加(21)と関連している。
まとめると、AD、PD、LBD、白斑はすべてメラニンの喪失と腸内細菌異常症と関連している(20-22)。ヘルペスウイルスも腸内細菌異常症、認知症(23)、白斑(メラニンの消失)と関連している(18)。腸内細菌異常症は免疫反応と炎症を引き起こす(24)。なぜなら、免疫細胞の70%から80%という大部分は腸に存在し、腸内細菌叢と局所粘膜免疫系は相互に作用しているからである。このような局所粘膜免疫反応に加えて、腸内細菌叢は全身性免疫にも影響を及ぼす(25)。
本稿の目的は、科学文献からメラニンレベルの変化と疾病との関連性を示す証拠を提示し、その変化がどのように起こりうるか、また疾病に及ぼす影響、さらには免疫系やその他の生物学的機能の燃料として細胞が使用するエネルギーの貯蔵分子としてのメラニンの役割の可能性を説明しようとするものである。メラニンは細胞エネルギーの供給において重要な役割を果たし、それが存在する体内のあらゆる疾患において重要な保護的役割を果たす可能性があるという考えを考慮すべきであり、これは疾病の統一理論を提供するものである、マスト細胞疾患、自己免疫疾患、結合組織障害、脂肪組織に関連する疾患、動脈、静脈、毛細血管、心臓、脳、肺、および/または筋肉を含む上皮細胞に関連する疾患、糖尿病、耳、目、鼻、および/または皮膚に関連する疾患、およびメラニンおよび/またはその前駆体、および/またはミトコンドリアに関連するその他の疾患、障害、状態 (表1).さらに我々の見解では、認知状態や気分症状の変化を引き起こすのは、神経変性疾患(32)に伴う炎症であり、感染に対する免疫系の反応のピークと衰退に反応して炎症が変動した結果であると考える。さらに、日没が見られる認知症患者では、日没とともに自然に起こり、午後10時頃まで続く気圧の低下(33)によって脳の炎症が亢進し、日没が引き起こされると考えられる。
表1 メラニンの既知および提案されている機能と、メラニンに関連する疾患
| メラニンの機能 | 著者らが提唱するメラニンの機能 | メラニンレベルの変化に関連する疾患 | 著者らがメラニンレベルの変化に関連すると提唱した疾患 | 参考文献 |
|---|---|---|---|---|
| 紫外線吸収、光保護、色素沈着、金属吸収、薬物の取り込みと保持、活性酸素種(ROS)消去/抗酸化、体温調節、自然免疫系の役割、エネルギーの伝達、酸化還元に関与する。 | 細胞プロセスに燃料を供給するため、細胞にエネルギーを供給する主要な供給源となる可能性がある。ミトコンドリアと逆の関係でエネルギーを供給する。 | 白斑、アルビニズム、パーキンソン病、アルツハイマー病、レビー小体型認知症、メラノーマ、その他 | 神経変性疾患、神経炎症性疾患、神経免疫疾患(AD、PD、LBD、MS、ALS、血管性認知症、外傷性脳損傷/慢性炎症性脳症、てんかん/発作を含むその他の脳疾患、神経系のその他の疾患、自己免疫疾患など)、消化管の疾患、糖尿病、癌、心臓病、脳卒中、深部静脈血栓症、慢性静脈不全を含む心血管系疾患、動脈、静脈、毛細血管、脳、心臓、肺、および/または筋肉を含む上皮細胞に関連する疾患、マスト細胞疾患、結合組織障害、脂肪組織に関連する疾患、急性およびLong-COVID-19およびその他の感染後自己免疫性脳症、うつ病、心的外傷後ストレス障害、気分障害、双極性障害、統合失調症およびその他の精神神経疾患を含む精神神経疾患、自閉症、注意欠陥多動性障害、ダウン症候群、およびその他の発達障害、不眠症、薬物中毒、耳、目、鼻、および/または皮膚に関する疾患、ならびにメラニンおよび/またはその前駆体および/またはミトコンドリアに関連または関与するその他の疾患、障害、および状態 | (4-8, 19, 26– 31) |
2. 感染とアミロイド斑の形成
30年以上にわたる研究により、AD患者の脳内のβアミロイド(β-amyloid/Aβ)斑には感染性微生物、特に単純ヘルペスウイルス1型(HSV1)が含まれていることが判明した。HSV1に加えて、他の病原体もADと関連していた:肺炎クラミジア、数種類のスピロヘータ、真菌感染である(34)。50万件の医療記録を対象とした最近の研究では、この研究をさらに発展させ、インフルエンザ、ヘルペスウイルス、エプスタイン・バーなどのウイルス感染が、AD、PD、MS、ALS、全般性痴呆、そして興味深いことに血管性痴呆と関連している(35)。
欧州の研究者たちがアルツハイマー病患者の脳で発見されたβアミロイド斑から微生物を分離していた頃、米国ではオーストラリアの研究者ロバート・モアが、ADの脳内のβアミロイド斑は免疫系が病原体を殺す残骸ではないかという考えを抱いていた。2016年、彼と彼の同僚たちは、抗菌剤としてのβアミロイドの役割に関する初の生体内モデルを発表した(36)。彼らはAβの抗菌活性が、いくつかの病原体に対してペニシリンの100倍も強力であることを発見したのである。ADにとって最も重要なことは、Aβが微生物の細胞表面にAβの塊を結合させ、アミロイド線維の形成を誘発することによって、病原菌を捕捉し殺すことをモアが発見したことである。アミロイド線維は微生物が宿主細胞に付着するのを妨げ、感染を防ぐ。成長するフィブリルは病原体を絡め取り、凝集構造へと引き込み、そこで病原体は一時的に無力化される。フィブリルは穴を開け、病原体の表面に孔を形成し、病原体細胞の内容物が漏れ出す。Aβからフィブリルが形成されると、タンパク質の銅イオンに対する親和性が10億倍になる。Aβは局所環境から銅イオンを引き込み、その金属を使って高レベルの次亜塩素酸イオン(漂白剤)を生成する化学反応を触媒する。それによって凝集体が殺菌され、架橋と呼ばれるプロセスでアミロイド線維が融合する。さらに、近くの脳組織への損傷を防ぐために、Aβがさらに漂白剤を生成するのを止め、線維を酵素分解に対して抵抗性にする。病原体はAβ線維を分解するために様々な酵素を分泌し、それによってAβ線維を逃がすので、これは重要である。しかし、脳の局所の清掃細胞はAβを容易に除去できず、凝集して何十年も残ることがある(12,37)。
Moirの発見以来、神経細胞内にAβが蓄積している証拠が見つかっている。このプロセスは、神経原線維のもつれ形成や細胞外Aβ(BayerとWirthsの総説)に先立って起こる(38)。われわれは、病原体に攻撃された神経細胞内でも、同じようにアミロイド線維のカプセル化と漂白のプロセスが起こるのではないかと考えている。この漂白は、ADや、PDやLBDのように漂白を生じるアミロイド斑が存在する他の神経変性疾患におけるニューロメラニニンの減少を説明しうる(39)。あるいは、病原体がメラニンを自分自身の目的のために利用している、おそらく自分自身の免疫系や宿主への攻撃を強化するため、あるいは増殖のためにエネルギーを利用するため、あるいは宿主に利用されるための貯蔵を枯渇させながらシェルターを建設し強化するため、といったことであろう。より具体的には、後者に関しては、細胞外マトリックスは免疫系の防御であり、細胞内マトリックスは病原体によって作られる。
神経変性患者では、病原体の侵入に対する正常な反応と思われるものを排除するエネルギーが、脳にはもはやないのだろうか。プラークや病原体、その他の残骸を除去するグリア細胞(40)にはメラニンが含まれているが(41)、メラニンが減少または枯渇しているため、その燃料となるメラニンが不足し、プラークや封入された病原体が残っている可能性がある。我々が非常に興味深く感じたことのひとつは、これらの認知症、特にPDとLBDの患者には、記憶にアクセスでき、認知能力が向上する時期があるということである。実際、認知能力や注意力の変動は症状の一部である(42)。また、ある種の薬剤を投与すると、ニロチニブの場合のように、時には即座に深い改善が見られることもある(43–45)。神経症状の浮き沈みは、免疫系反応の初期にピークと衰退を繰り返す炎症によって経路が阻害されていることを示唆している。しかし、罹患したニューロンは無傷のままであるが萎縮しており(46)、メラニンが欠乏していることを除けば、ADではそれ以外は健康である(6)。このことは、これらの神経変性疾患の真の根本原因を特定し、それを効果的に治療すれば、患者の神経機能を回復させることができるという希望を与えてくれる。
3. メラニン:病気の統一理論
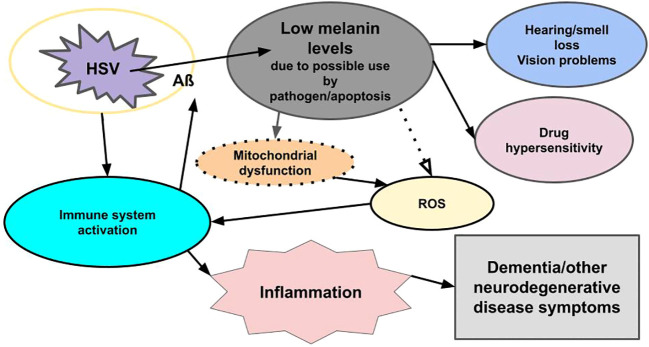
私たちは、神経変性疾患やその他の疾患の鍵はメラニン、特にメラニンが供給するエネルギーにあり、神経変性疾患で見られる神経メラニンの減少は、病原体を包み込んでいるプラークを脳が免疫系から除去できなくなる結果であると推論している(図1)。もしこれが本当なら、黒に近いメラニンが減少した脳の領域で、免疫系が「総出で」アプローチし、より高濃度のフェオメラニン(赤みを帯びた色素)を生成しても不思議ではない、なぜなら、フェオメラニンは、暗いユーメラニン/ノイロメラニンに比べて、より高い周波数、より高いエネルギーを持つ光スペクトルの短い波長をより多く吸収し、可視光線よりもかなり高エネルギーである紫外線(UV)光子を吸収するのに必要なフェオメラニンは、ユーメラニンに比べてより少ないからである(47)。2023年、Cai et al.(48)は、この疾患によって影響を受ける脳の領域であるパーキンソン病患者の黒質で、まさにそのことを発見した。さらに、ニロチニブは、2015年に患者の反応をビデオで撮影し(インターネット上ではもう入手できない)、研究者と患者の間でこの分野の興奮を引き起こした薬剤であるが、LBD、PD、AD患者の脳のプラークを除去するのに役立つことが示されただけでなく、血液脳関門を通過し(43–45)、メラニン生成を誘導する(49)。
図1 ウイルスに関連した神経炎症と神経変性。微生物(例えばHSV)の感染は免疫反応を引き起こし、その結果、カプセル化プラーク(Aß)が形成され、炎症が起こると同時に、アポトーシスや病原体による簒奪によってメラニン量が減少する。メラニンの減少はミトコンドリアの機能不全を引き起こし、活性酸素の増加を招き、これが免疫反応を引き起こし、炎症を誘発する。メラニンレベルの低下/アポトーシスはまた、聴覚/嗅覚障害、視力障害、薬物過敏症を引き起こす。メラニンの消失は皮膚にも見られることがある(図示せず)。病原体はまた、免疫反応においてマスト細胞の放出を誘発する(図示していない)。マスト細胞は脱顆粒し、ヒスタミンや他の免疫系炎症性化学物質を放出する。病原体とメラニンレベルの減少の両方に対する免疫反応は炎症を引き起こし、病原体はアポトーシスを誘発し、メラニンとドーパミンを減少させる(図示せず)。
もしメラニンが、脳や身体、特に免疫系が必要とするエネルギー、そして免疫系そのものが必要とするエネルギーを保持しているのだとしたら、それをどうやって知ることができるのだろうか?さらに、この病気の患者の脳でメラニンが減少している場合、PDの特徴である疲れるような震えを、エネルギーという観点からどのように説明できるのだろうか?第一に、健常者では加齢とともに神経メラニンが蓄積することが分かっている(4)。しかし、神経変性疾患の患者では、疾患によって脳の特定部位で暗色メラニンの消失が見られ、その消失は疾患の症状と相関する(50,51)。このことから、私たちは、PDの疲れるような安静時振戦を説明するという難問に行き着いた。もしメラニンにエネルギーが含まれているならば、エネルギーは疾患状態でも保存される必要があり、過剰に消費されることはないはずである。しかし、Amano et al.(52)は、PDでみられる安静時振戦やその他の運動行動が、実際には代謝的にエネルギー効率が高いことを示す理論的枠組みを提示している。彼らは、ニューロメラニン形成の前駆体であるドーパミンの役割と脳内のエネルギー代謝が関連していると仮定し、「ドーパミン病変はグルコース取り込みを減少させる」という研究結果でこの主張を支持した。彼らは、「PDにおけるドーパミンニューロンの喪失は、グルコース代謝の機能障害に関与している可能性が高い」と結論づけている。彼らはまた、ミトコンドリア機能障害がPDに多く、代謝機能障害を引き起こしていると主張する文献が増えていることにも言及している。私たちは、メラニンレベルとミトコンドリアのATP産生との間に逆相関があることを発見しました。実際、メラニンがエネルギーの主な供給源となり、ミトコンドリアが補助的なエネルギーを生産するという、相反する、しかし相補的な相互依存関係があるようです」
4. ATP産生はメラニンからのエネルギーを補完する
我々は、白斑細胞のミトコンドリアに関する文献を検討することで、細胞燃料の補給におけるメラニンの役割の可能性を示す証拠の探索を開始した。白斑細胞は色素沈着がないのが特徴である(53)。また、悪性黒色腫細胞についても調べた。悪性黒色腫細胞はメラノサイトの増殖を特徴とし、したがって一般的にメラニンが増加する。
Dell’Anna et al.(26)は、培養した表皮白斑メラノサイトを健常対照細胞と比較した。彼らは、正常細胞と比較して、表皮白斑メラノサイトはATP産生が低いことを発見した。この細胞は、グルコースの取り込みの増加、グルコースの代謝に使われる特定の酵素の産生の増加、ミトコンドリアの容積と質量の増加によって、低いエネルギーを補った。このことは、メラニンが健康な(白斑のない)細胞に供給していると考えられるエネルギーの損失を補うために、これらの細胞が実際にATP産生を増加させた可能性を示唆している。ミトコンドリアのサイズが大きくなったことで、ATPを産生する能力が高まり、グルコースの取り込みと酵素の増加が、通常メラニンから供給されるエネルギーがない場合のATP産生の燃料として使われる可能性がある。加えて、白斑では表皮メラノサイトがメラニン産生にエネルギーを消費しないため、実際にエネルギーが節約され、ATPの利用可能性が高まるはずである。
もし私たちの理論が正しければ、メラノーマ細胞は豊富なエネルギーを持つことになる。Hall et al.(27)は、メラノーマ細胞は酸化的リン酸化の機能不全の結果、エネルギー代謝が損なわれていることを突き止めた。正常細胞がATPのほとんどを酸化的リン酸化から得ているのに対し、悪性黒色腫細胞はATPの多くを解糖から得ていた。興味深いことに、これらの悪性黒色腫細胞で解糖を阻害しても、すべての悪性黒色腫細胞が死滅することはなかった。一方、正常なメラノサイトで酸化的リン酸化を阻害すると、すべての細胞が死滅した(27)。メラニンを豊富に持つ細胞だけが生き残ったことから、生き残った悪性黒色腫細胞は、解糖に加えて、別の供給源であるメラニンからもエネルギーを得ていた可能性が示唆される(表2)。加えて、悪性黒色腫細胞は、増殖するように遺伝的にプログラムされているため、より多くのエネルギーを必要とする。他のがんでは、酸化的リン酸化は障害されない。それどころか、ミトコンドリアの生合成とミトコンドリアの品質管理は、他のほとんどのがんでアップレギュレートされることが知られている(54)。したがって、悪性黒色腫細胞は豊富なメラニンからエネルギーを得ている可能性がある。
表2 メラニンとATP産生の逆相関説
| 白斑細胞 | メラノーマ細胞 | 参考文献 | |
|---|---|---|---|
| 既知の特徴 | グルコースの取り込みの増加、グルコースの代謝に使われる特定の酵素の産生の増加、ミトコンドリアの容積と質量の増加。 | 酸化的リン酸化が減少し、酸化的リン酸化よりも解糖から多くのATPを得る。 | (26,27) |
| 理論 | 白斑細胞はメラニンの欠乏の結果、ATP産生が増加しているのだと推測している。 | 我々は、メラノーマ細胞はメラニンからのエネルギーが増加した結果、ATP産生が減少したと仮定している。正常細胞とメラノーマ細胞でATP産生の主な源を阻害したところ、正常細胞はすべて死滅したが、メラノーマ細胞は死滅しなかった。 | (27) |
メラニンが細胞へのエネルギー供給に関与しているかもしれないというさらなる証拠は、ミトコンドリアによるATP産生の阻害とメラニン産生の増加との関連に見出すことができる。Williams et al.(28)は、melan-p1細胞においてメラニン産生を3倍以上に増加させる6つの低分子を同定した。これら6種類の低分子はすべて、ミトコンドリアのF1F0-ATP合成酵素(mtATPase)を阻害することがわかった。これら6種類の低分子を特定した後、mtATPaseを阻害することが知られているさらに2種類の低分子を試験したところ、驚くべきことに、メラニン産生を増加させることがわかった。研究者らは、これら8種類の低分子が、「mtATPaseを介したH+イオンの輸送を阻害する」ことによってメラニン産生を増加させ、それによってpHが変化し、pHの変化によって、メラニン生成の律速段階を触媒する酵素であるチロシナーゼとチロシン関連タンパク質-1(TRP-1)の適切な区画への輸送が修正されることによって、メラニン産生の増加につながった、と提唱した(図2A)。これは、ミトコンドリアのATP産生を阻害することでメラニン産生を増加させる方法の一つを示したもので、pHを変化させることで、メラニン生成過程に重要な特定のタンパク質の輸送を修正する。

図2 われわれは、メラニン量とATP産生には逆相関があると理論的に考えた。(A)ミトコンドリアのATP産生を阻害するmtATPaseの低分子阻害剤は、メラニン産生を3倍以上に増加させる。したがって、ATP経路が遮断されるとメラニン濃度が上昇する。発光装置が細胞のATPレベルを増加させるのは、メラニン/神経メラニンの利用可能性が増加した結果、それほど多くのATPが使用されなくなったからだと、私たちは推論している。光はATP産生の前駆物質ではないが、光はメラニン生成の前駆物質である。したがって、色素細胞が放出された光を浴びると、メラニン/ノイロメラニンが生成されたと推測される。したがって、メラニン/ノイロメラニンを生成する細胞が光にさらされると、ATPレベルが上昇するようだ。このことは、ATP産生とメラニン産生が反比例の関係にあることを示唆している。(B)ミトフシン-2の産生をアップレギュレートすると、ATP産生は増加するが、メラニン生成速度は減少し、ミトフシン-2の産生をダウンレギュレートすると、ATP産生は減少するが、メラニン生成速度は増加する。(C)プロヒビチンは、ミトコンドリア、核、細胞膜、細胞質に存在し、それらの間をシャトルするタンパク質である。私たちは、プロヒビチンがATPを産生するために、これらの細胞構成要素間でエネルギーの必要性を伝達し、ミトコンドリアの生合成とメラニン生成という既知の役割とバランスをとっていると推論している。
私たちは、メラニン量とATP産生量の間に逆相関があるのは、メラニンが細胞にエネルギーを供給しているからだと考えている。もしメラニンが細胞にエネルギーを供給するのであれば、メラニンを増やすと、細胞がメラニンから得るエネルギーの量が増えることになる。したがって、メラニンを基準値より大幅に増加させ、細胞に余分なエネルギーを供給するような分子は、ミトコンドリアのATP産生を制限し、ATPが浪費されるような進化を遂げたということになる。ATPは水中での安定性が低いため、ごく短期間を除いては細胞内に貯蔵することができない(55)。多くの研究で、発光装置を使用すると細胞のATPレベルが上昇することがわかっている。なぜこのようなことが起こるのかは、まだ解明されていない(56)。しかし、これらの研究では細胞ATPレベルを測定したのであって、細胞ATP産生を測定したのではないことに注意することが重要である。われわれは、メラニンが放出された光の一部をエネルギーに変換し、細胞がATPの代わりにこのエネルギーを利用できるようになったと理論的に考えている。したがって、想定されていたようなATP産生の増加はなく、ミトコンドリアでの反応も起こらなかったと推論する。その代わりに、細胞内のATPレベルが増加したのは、光を吸収した結果、メラニンによって産生されたエネルギーが増加したため、ATPの使用量が減少し、細胞がそれを利用してATPを節約したためだと考えられる(図2A)。このことはまた、メラニンからのエネルギーが、多くの細胞経路にとってエネルギーの第一選択であるという我々の結論を指し示し、メラニンレベルとミトコンドリアATP産生レベルの間の逆相関をさらに説明するものである。先に述べたように、ATPは水中での安定性が低いため、細胞内に短時間しか貯蔵できない(55)。従って、メラニンからのエネルギーが多くの経路で最初に選択されるのであれば、ミトコンドリアのATP産生があまり減少しなければ、これらの研究で見られるように、細胞内にATPが過剰に存在することになる。このATPの多くは分解され、無駄になってしまう。このことは、メラニンが増加するとミトコンドリアのATP産生が減少するという進化的な利点を説明している。
我々は、ミトコンドリアのATP産生とメラニン生成の間に逆相関があることを示す、さらなる証拠を発見した。Pich et al.(57)は、ミトフシン-2(Mfn2)をダウンレギュレーションすると、ピルビン酸、グルコース、脂肪酸の酸化が阻害され、ミトコンドリア膜電位が低下する一方、Mfn2をアップレギュレーションすると、グルコースの酸化とミトコンドリア膜電位が上昇することを見出した。このことは、Tanwar et al.(58)は、Mfn2をダウンレギュレートするとメラニン生成速度が増加し、アップレギュレートするとメラニン生成速度が減少することを見出した。さらに彼らは、色素沈着が強いヒト初代メラノサイトは、色素沈着が弱いヒト初代メラノサイトに比べて、Mfn2の発現が少ないことも見出した(59)。このことは、メラニン産生とミトコンドリアのATP産生との間に逆相関があることを示唆している。Mfn2の発現低下により酸化的リン酸化が減少し、メラニン産生が増加する一方、Mfn2の発現上昇により酸化的リン酸化が増加し、メラニン産生が減少するためであり、メラニンが細胞にエネルギーを供給しているという我々の考えを裏付けている(図2B)。さらに、Bach et al.(59)は、肥満者ではMfn2の発現が低下していることを発見した。脂肪組織にはメラニンが含まれ、肥満者の脂肪組織には痩せた人の脂肪組織よりも多くのメラニンが含まれ(60)、肥満者の脂肪組織にはミトコンドリア機能障害があることが知られているからである(61)。さらに、PD動物モデルで蓄積したドーパミン作動性ニューロンの神経メラニンが閾値を超えると、他の細胞プロセスとともにミトコンドリア機能を阻害した。具体的には、ミトコンドリアが消費する酸素が減少し、これはわれわれのモデルでは予測可能であった(4)。
次に、ミトコンドリア、核、細胞膜、細胞質に存在するタンパク質、プロビンチン(PHB)に注目した。PHBは細胞のある部分から別の部分へと移動することが知られている(62)。その機能には、ミトコンドリアの生合成や、ミトコンドリア内での他の重要な機能(63)、メラニン生成の律速酵素であるチロシナーゼをコードする遺伝子の転写速度に影響を与えることによるメラニン生成(64)などがある。細胞はミトコンドリアと細胞質でATPを産生し、ミトコンドリアは核とエネルギーの必要性について連絡を取り合い(65)、核では転写が行われ、細胞膜のタンパク質がATP産生に必要なグルコースを含む物質の出入りを行っていることを考えると興味深い。このように、PHBが存在し、その間を行き来する細胞内の4つの部分は、すべてエネルギー生産に関わっている(図2C)。また、Williamsら(28)が色素沈着を増加させると決定した8つの低分子化合物も興味深い。(28)が色素沈着を3倍以上増加させることを決定した8つの低分子もまた、チロシナーゼに影響を与え、これらの場合はチロシナーゼの経路を変えている。我々は、PHBシグナル伝達が、必要に応じてメラニン産生の引き金に使われている可能性があると考えている。
私たちはメラニンがATP産生を補うという考えで探索を始めたが、最終的にはその逆であることに気づいた。
4.1.神経変性疾患におけるメラニン産生とATP産生の関係
詳細は明らかではないが、コレステロールはトリグリセリドと同様にADと関係があるようだ。例えば、Moser et al.(66)は、貯蔵エネルギーである総コレステロールおよびトリグリセリドの変動と、ADおよび他の認知症の発症率との間に関連があることを発見した。このことは、メラニン生成とATP産生の関係をさらに裏付けるもの:1.コレステロールは時間および用量依存的にメラニン生成を調節する(67)。トリグリセリド(脂質)の分解は、脂肪分解と呼ばれるプロセスでATPを形成する(68)。
アルコールもエネルギーの一種である(69)。研究者らは最近、マウスモデルにおいて、アルコールの過剰摂取がADの進行を促進する可能性があることを発見した(70)。ヒトでは、慢性的なアルコール摂取はATP合成の障害(71)や色素沈着(72)と関連している。
神経変性疾患では、ATPレベルが低い(73)。しかし、これはATP産生が低いことを意味しない。われわれは、神経変性疾患ではメラニン産生とそれに関連するエネルギーのレベルが低い結果、ATPがより急速に使用されていると推測している。このことから、神経変性疾患に関して、ATP産生とメラニンとの間に逆相関があるかどうかを調査することになった。Delijewski et al.(74)は、メラノサイトを様々な濃度のニコチンで24時間処理した。最低濃度のニコチンはメラニン生成に影響を与えなかった。しかし、中間の濃度で処理した細胞では、メラニン濃度は26%と15%増加し、濃度が高くなるにつれて減少した。最高濃度では、メラニン含量は約16%減少した。次に、同じく様々な濃度のニコチンで24時間処理したメラノサイトの細胞チロシナーゼ活性を調べたところ、メラニン生成への影響と相関関係があることがわかった。最も低いニコチン濃度では影響はなかった。中間の濃度では、チロシナーゼ活性はそれぞれ約26%と16%上昇し、濃度が上がるにつれて減少した。最高濃度では、チロシナーゼ活性は14%減少した。ATP産生、メラニン産生、ニコチンを明確に調べた研究はないが、メラニン産生が低ければATPが増加し、高ければATPが減少すると予想される。タバコの煙に暴露されると、ミトコンドリアの複合体Iと複合体IIが用量依存的に阻害され、ミトコンドリアの呼吸とATP産生が減少したのである(75)。別の研究では、タバコの煙にさらされると、ミトコンドリアの呼吸が減少し、その結果、用量依存的にATPレベルが低下し、酸化物質の産生が増加することが示された(Fettermanによる総説)(76)。ATP産生レベルが低下すると、電子伝達体の酸化が少なくなり、その結果、活性酸素の主要種であるスーパーオキシドが生成される(77)。メラニンがベースラインより減少すると、活性酸素を消去するメラニンが少なくなるため、活性酸素が増加し(8,77)、メラニンがベースラインより増加すると、メラニンの産生が活性酸素を作り出すため、活性酸素も増加する(78)。メラニンが増加するとATP産生が減少し、これによっても活性酸素が増加することは、先に詳述した通りである(77)。
ニコチンはある濃度でメラニンを増加させるので、我々の理論によれば、その濃度でニコチンを増加させれば、PDやADの発症を予防したり遅らせたりすることができ、潜在的には治療することができることになる。実際、70以上の研究が、タバコの使用がPDの発症リスクを低下させることを示している(ニコラトスによる総説)(79)。AD発症リスクは、発症前に1日に喫煙するタバコの本数が増えるにつれて減少したが、これはニコチンによるものであると研究者らは推論している(80)。ニコチンは神経保護の主要なメディエーターであると考えられており(81)、この知見はNicholatosらによってさらに解明された(79)。タバコによるPDリスクの軽減は、使用期間と強度に依存する(82)。ニコチン投与はADでは認知機能障害を改善し、PDではジスキネジアと記憶を改善し(Alhowailに総説あり)(83)、歩行を改善し転倒を減少させる(84)。ニコチンはメラニンを含む細胞に蓄積するようで、メラニン合成を増加させる可能性がある(85)。このことは、脳への入り口が複数あることから、免疫系やメラニンとエネルギーに関する理解を深める上で重要な意味を持つのではないかと考えている。
4.2.電荷と電磁合成
心臓を鼓動させる電気刺激から、電気信号が電波を通して細胞間に情報を伝達するまで、電流は絶えず人体中を流れている。見過ごされているのは、メラニンが電気の流れに果たす役割である。メラニン分子は通常、鎖状に結合している。この構造が電子の流れを可能にする(86)。メラニンはまた、電子を蓄え(45)、それによって電子の銀行として働き、電気を流す(85,87)。
電気という形でエネルギーを伝導、貯蔵、放出する能力(86,88)に加え、メラニンには双安定なスイッチングを示す能力がある。メラニンは、以前考えられていたような非晶質の有機半導体ではなく、電子イオン性のハイブリッド伝導体であり(87)、異なる電圧の下でオン・オフを繰り返すことができる(86)。このオン・オフスイッチは、ミトコンドリアが生産するエネルギーとの関係で使われるメカニズムかもしれない。
後述するように、メラニンが免疫系に不可欠なエネルギーの供給源であることはわかったが、メラニンがどこに存在し、そこでどのような働きをしているのかを知る必要がある。目、毛髪、皮膚、卵巣、心臓、動脈(心臓につながるものも含む)に加え、肝臓、内耳、肺、結合組織、脾臓、腎臓、精巣、腹膜、筋肉、脈絡膜、松果体、そしてもちろん脳(ドーパミン作動性ニューロン、ノルアドレナリン作動性ニューロン、脳を覆う髄膜、グリア細胞)など、他の臓器や組織にもメラニンは存在する(41,89)。実際、メラニンは全身に存在する可能性がある。GeneCardsデータベースを検索したところ、メラニン生合成経路の酵素であるチロシナーゼ、TRP-1、ドーパクロム互変異性化酵素(TRP-2)をコードする遺伝子が、ほぼすべての種類の臓器組織で発現していることがわかった。したがって、すべての細胞がメラニンを生成する能力を持っているのかもしれない。体全体の電気の流れを見るもう一つの方法は、病気である。電気の量が不規則になったり、急増したりすると、不整脈やてんかんのような病気の状態になる。そして、電子の流れが劇的に減少し、その結果、エネルギーが著しく失われると、神経変性疾患が発症する。ニューロメラニンは脳にエネルギーを供給しており、エネルギーが不足すると、病原体が存在する場合に神経変性疾患が発症するのである。
実際、このことは別の臓器である心臓やてんかんの脳でも実証されている。Levin et al.(90)は、TRP-2を欠損させた心筋メラノサイト様細胞を持つマウスの心臓は、対照マウスの心臓に比べて色素沈着が少なく、異常な電気活動を起こしやすいことを発見した。さらに、マウス心筋メラノサイト様細胞は隣接する心筋細胞と電気的に結合していることを発見し(90)、これはメラニンが心筋にエネルギー源を供給していることを示唆している。先に、血管性痴呆が感染症とも関連していることを述べた(35)。血管性痴呆はAD、PD、LBDと類似した特徴をもっている:動脈にはプラークが存在し、動脈、静脈、毛細血管の上皮細胞内膜はメラニンで色素沈着している(91,92)。血管性痴呆患者の上皮細胞が、脳および/または心臓の血管系において、あるいは深部静脈血栓症や他の心臓イベントが起こったと思われる領域において、メラニンレベルが低下しているかどうか、脂質が増加しているかどうか、ミトコンドリア機能障害があるかどうかを研究者が調べることを提案する。
フェニルアラニン水酸化酵素は、フェニルアラニンのチロシンへの変換を触媒する。食事とタンパク質の異化から得られるフェニルアラニンの約75%がチロシンに変換される(93)。チロシン、ひいてはフェニルアラニンはメラニンの前駆体であり(94)、フェニルアラニン水酸化酵素欠損症の症状は、パーキンソン様症状、かび臭さ(95)、知的障害(認知障害)など、PDと同様にメラニンレベルの低下に関係しているように思われる。また、皮膚や毛髪の色素沈着も見られるが、これはメラニンレベルが低いことの明らかな徴候である。また、流産を繰り返したり、奇形児が生まれたりする女性もいるが、これは妊娠を維持し、胎児を完全に形成するのに十分なエネルギーがないことを意味しているのかもしれない。電気波を伴うてんかんもまた、フェニルアラニン水酸化酵素欠損症(96)に関連しており、したがってメラニンレベルが異常に低い。我々のモデルでは、このような低レベルのメラニンによってATPが大量に生産され、ミトコンドリアの機能不全の結果として電気活動(発作)が急増すると予測する。実際、てんかんでは酸化ストレス(97)と同様にミトコンドリアの機能障害があり、活性酸素を消去するのに十分なメラニンがない場合に起こると予測され、てんかん発作ではATP濃度が劇的に上昇する(98)ことから、我々の仮説が支持される(図3)。
図3 メラニンには、エネルギーを伝導、貯蔵、放出する能力がある。メラニン:病気の統一理論は、ATP産生と逆相関のある、細胞への主要なエネルギー供給源としてのメラニンの役割に関する新しい理解を述べ、神経変性疾患やその他の疾患の病態に関する新しい理論を提供する。神経変性疾患では、メラニン/ノイロメラニンの喪失が脳の細胞エネルギーを減少させ、迷走神経を経由して腸から、嗅神経を経由して鼻から、あるいはその他の経路で移動してきたと思われる微生物を内包するプラークを除去する免疫系の能力を妨害する、というのが我々の提案である。メラニンが失われると、電気インパルスが阻害され、不整脈や発作を引き起こす可能性もある。過剰なメラニン生成は、メラノーマのような病気を誘発する。
5. メラニンの性質
末梢メラニンは皮膚の表皮層で生成される。メラニンは、紫外線に反応して形成される活性酸素を消去し(29)、金属を吸収し、体温調節を行い、薬物の取り込みに関与し、自然免疫系の一部であり、エネルギーを伝達し(Koike et al.に総説あり)(30)、酸化還元に関与している。この他にも、まだ同定されていない多くの機能や性質があると予想されている(29)。細菌や真菌を含む病原微生物は、感染した宿主の防御機構から身を守るためにメラニンを利用する(99)。
メラニンはポリマーである。メラニンの生成は紫外線によって誘発される。メラニンは、メラノサイト内のメラノソームと呼ばれる小器官で生成される(100)。メラノソームはその後ケラチノサイトに運ばれ、核の周りに集まってDNAを紫外線から守る(30)。メラノサイトはいくつかのシステムと相互作用している。したがって、メラニン生成は免疫系、内分泌系、炎症系、中枢神経系によって制御されている。メラノサイトの活性は、前述のように紫外線やある種の薬物などの外因性因子によっても制御されている(100)。
私たちの仮説の最も基本的な側面のひとつは、光が光子、つまり大きさを持たないエネルギーの塊(101)からできているという事実にある。したがって、骨に守られた臓器組織であっても、光子の観点から見れば、その経路は広く開かれている。したがって、皮膚のメラニンが太陽からの紫外線を吸収するように、脳の神経メラニンを含む全身のメラニンも吸収するのであり、このことは、神経変性疾患の将来の治療に関して最も重要なことであろうというのが、我々の理論である。
5.1.メラニン生成経路
メラニンの正確な組成は不明である。その化学構造は多様で複雑である(29,87)。メラニン生成はメラノソームで起こり、L-フェニルアラニンヒドロキシラーゼがフェニルアラニンをアミノ酸チロシンに変換する反応を触媒することから始まる(94)。チロシンは酵素チロシナーゼによってドーパキノンに変換される。ドーパキノンはL-3,4-ジヒドロキシフェニルアラニン(L-DOPA)に変換される。L-DOPAは、チロシナーゼとの2回目の反応によってドーパキノンに戻すことができる。ドーパキノンはユーメラニンとフェオメラニンの前駆体である。ドーパキノンはロイコドパクロムに変換される。ロイコドパクロムはL-DOPA分子を生成し、再びドーパキノンに変換される。ロイコドパクロムはドーパクロムに変換される。ドーパクロムは脱炭酸して5,6-ジヒドロキシインドールを生成し、これがチロシナーゼと反応してユーメラニンを生成する。ドーパクロムは酵素TRP-2と相互作用する。これによりドーパクロムはDHICA(5,6-ジヒドロキシインドール-2-カルボン酸)に変換される。5,6-ジヒドロキシインドールとDHICA分子は一緒に重合する。これらのモノマーの重合はTRP-1によって触媒され、ユーメラニンとなる。フェオメラニンのメラニン生成はチロシンから始まり、チロシンはL-DOPAに変換される。L-DOPAは5-システインドパに変換され、5-システインドパはフェオメラニンに変換される(29,87,102– 104)(図4)。ニューロメラニンの構造と合成経路は、ほとんど未知のままである(105)。フェオメラニン(97)を核とするニューロメラニンは、神経細胞で産生され、カテコールアミン作動性ニューロン、特にドーパミン作動性ニューロンとノルアドレナリン作動性ニューロン、およびグリア細胞の両方に蓄積される(105)。したがって、オイメル酸はドーパミンまたはノルエピネフリンに由来する。したがって、ユーメラニン、ニューロメラニン、フェオメラニンの生成にはL-DOPAが関与している。L-DOPAはドーパミンの前駆体である。ドーパミンはPD(106)、LBD(107)、AD(108)で主要な役割を果たしている。
図4 Raper-Masonメラニン生成経路。ユーメラニン、フェオメラニン、ニューロメラニンにはL-DOPAが関与している。L-DOPAはドーパミンの前駆体である。ドーパミンはPD、LBD、ADにおいて主要な役割を果たしている
6. メラニンと病原性
特定の病原体は、特定の理由で特定の細胞タイプを攻撃することが知られている。例えば、ヘリコバクター・ピロリは胃の上皮細胞をコロニー化し、増殖できるように免疫系をコントロールする(109)。したがって、ある種の病原体がなぜメラニンを含む細胞を攻撃するのかを考えることは興味深い。われわれは2つの仮説を立てた:1.メラニンはヒトの免疫系に不可欠なものであり、細胞からメラニンを取り除くことは宿主を弱体化させる。2.病原菌は宿主のメラニンを盗んで、自らの防御力を高めているのではないか。病原体のメラニン化は、その病原性と関連している。感染性微生物に含まれる色素は、宿主の免疫クリアランス機構を妨害したり、炎症促進作用や細胞毒性作用を起こしたりすることで、病原性を高めることが多い。例えば、メラニンはクリプトコッカス・ネオフォルマンス(Cryptococcus neoformans)やアスペルギルス・フミガータス(Aspergillus fumigatus)に存在し、免疫力が低下した患者に重篤な日和見感染を引き起こすことがある(110)。メラニンは負電荷を帯びるため、C. ネオフォルマンス感染症の治療に使われる内因性の抗菌ペプチドや抗真菌薬の作用や効果を阻害する(111)。したがって、微生物が宿主のDNAを改変してメラニンをより多く産生することは、微生物にとって有益である。メラノーマはPDのリスクを4倍に高め、PDはメラノーマのリスクを4倍に高めることは興味深い(112)。ある研究では、メラノーマサンプル中の41種類の細菌が同定された(113)。我々は、両疾患が罹患者において同じ病原体によって引き起こされることを示唆している。
病原体におけるメラニン化が病原体の病原性と関連しているのに対し(110)、メラニン化を阻害すると病原体の病原性が低下する(114)。微生物についても同様で、メラニンが少ないほど活性酸素や紫外線によって死滅しやすくなることがわかった(115)。例えば、C. neoformansのメラニン欠乏変異体は病原性が低いことが示された(116,117)。さらに、メラニン欠損変異体は試験管内試験での貪食細胞による殺傷に抵抗する能力が低いことがわかった(118)。メラニンはT細胞を介して炎症反応をも制御している可能性がある。メラニン色素の多いC. neoformans株は、色素の少ない株に比べてT細胞免疫応答を抑制した(119)。
ある種のウイルスは、ヒト宿主の感染組織において、メラノサイトを死滅させるか無力化することにより、メラニン生成を阻害する。ヘルペスウイルス(120)、サイトメガロウイルス(121)、ヒト免疫不全ウイルス(HIV)、慢性C型肝炎ウイルス(122)、B型肝炎ウイルス(123)は白斑と関連している。Koike et al.(30)は、ウイルス感染によるtoll-like receptor-3(TLR-3)の活性化(メラノソームの移動と細胞外への放出を促進する)が、メラノサイトのアポトーシスとメラノサイトの機能不全の結果としてのメラニン合成の抑制の両方によって、白斑の病態形成に寄与している可能性を示唆している。TLRは微生物の分子パターンを認識する受容体である。インターロイキン-1受容体として分類される(124)。ヘルペスウイルスの一種である水痘・帯状疱疹ウイルスもまた、メラノサイトの色素脱失を引き起こす可能性がある(125)。Harsonらによる研究(126)では(126)は、尋常性白斑における水痘・帯状疱疹ウイルス感染の初期段階における皮膚におけるウイルス複製の主要部位はメラノサイトであり、ウイルスが細胞内の色素形成機構をハイジャックしてウイルス複製を行う可能性があることを示した。メラニンの免疫系特性から逃れるだけでなく、病原体が宿主のメラニンを利用して自らの供給源を強化することもあるようだ。私たちは、白斑と同様に、病原体が神経メラニンを含む細胞のアポトーシスを誘発するのではないかと考えている。メラニンの免疫系特性から逃れることに加えて、病原体は宿主のメラニンを破壊して免疫系の防御を弱めたり、宿主のメラニンを使って自分自身の免疫系を強化したりしているのかもしれない。
PDとLBDの場合、薬物過敏症、耳鳴り、嗅覚の喪失はすべてメラニンを含む組織で生じる。嗅覚が、LBDやADの認知症の症状に先立って低下することは興味深い。ADでは、Itzhaki(34)が述べているように、鼻から感染性の微生物が侵入し、嗅神経を移動し、脳内に移動するためと考えられているが、この経路がPDとLBDで同じであると考えるのはあながち間違いではない。我々は、病原体の複製は鼻、そしておそらく耳のメラノソームで起こり、そこでアポトーシスが起こると考えている。神経メラニンの消失はAD、PD、LBDで認められる(5-7)。さらに、LBDは皮膚メラニンの減少とも関連していると考えられている(127)。興味深いことに、白斑はあらゆる認知症の発症リスクを高める(21)。先に述べたように、ヘルペスウイルスは白斑と関連している(120)。ヘルペスウイルスはメラノサイトのアポトーシスを誘導する(128)。嗅覚の低下と聴覚の喪失は、これらのメラニン化した細胞のアポトーシスに起因し、解明されていないメカニズムによって、これらの感覚の出口を減衰させるというのが我々の理論である。
病原菌は嗅神経や耳だけでなく、目にも入りやすい。不潔な手で目をこする人は珍しくないからだ。従って、病原体が目から入る可能性はある。同様に、病原体がその部位に内部移行することもある。いずれにせよ、認知症ではしばしば著しい視覚障害がみられる。AD、PD、LBDはすべて視覚障害と関連している。PDにおける視知覚障害には、顔や顔の感情認識、色識別、コントラスト感受性、重なり合った物体の識別などの問題がある(129)。これらの認知症はすべて後皮質の萎縮と関連しており、視空間および視知覚能力、識字能力、構音能力の低下を示す神経変性症候群である(130)。また、網膜内層の菲薄化、網膜ドーパミン作動性の欠乏、後皮質の皮質菲薄化も見られる(129,131)。さらに、ぶどう膜路のメラニンは光を吸収して視力を改善すると考えられている(41)。これらのメラニン化領域のいずれかにメラニンの消失があれば、視覚障害や識字能力・失行能力の低下を説明するのに役立つであろう。実際、PDの網膜ではドーパミン作動性細胞の減少が報告されている(132)。ドーパミン作動性細胞にはニューロメラニンが含まれている(41,105)。ニューロメラニンは大脳皮質でも確認されている(133)。また、我々の見解では、視覚や読み書き、運動能力の変化の一部は、エーラス・ダンロス症候群の斜視にみられるように、マスト細胞によるぶどう膜などの結合組織の問題に起因している可能性もある(134)。輻輳不全に関係する斜視は、PDのドーパミン補充療法に反応する(135)。メラニンの喪失はドーパミンの喪失を意味する。
7. グリホサート、腸、メラニン消失の影響
神経変性疾患やその他の神経免疫疾患におけるメラニンの効果を示すもう一つの方法は、除草剤グリホサートの影響を見ることである。グリホサートはヒトでも病原菌でもメラニン生成を阻害する(136)。メラニンと疾患におけるその役割についてここで紹介したことを踏まえると、グリホサートがPDやADと関連していることは驚くべきことではないだろう(137)。
グリホサートはヒトのメラニン生成を阻害するだけでなく、ある種のヒト腸内細菌叢が必要とする植物上の微生物を、これらの微生物のシカ酸経路を阻害することによって死滅させる。Puigbò et al.(138)は、シキミ酸代謝経路はヒトの一般的な腸内細菌の54%に存在し、従ってそれらはグリホサートに対して本質的に感受性が高いことを発見した。BarnettとGibson(139)は、日和見病原体は常在菌に比べてグリホサートに対してより耐性があることを指摘している。グリホサート誘発性ディスバイオシスは炎症と関連している(140,141)。Zhangらは、可溶性メラニンやメラニン化した細菌が腸の炎症や腸内細菌異常症を予防する可能性を示唆している(142)。
シキメート経路は、タンパク質合成に使われる3つの芳香族アミノ酸であるチロシン、フェニルアラニン、トリプトファンの生成を担っている。これらのアミノ酸は、色素化合物を含む他の重要な生物学的分子の上流にある。これらの芳香族アミノ酸経路に由来する代謝産物は、神経信号伝達に関与し、脳内の活性酸素を鎮める。ヒトや他の動物にはシキメイト経路はない。しかし、腸内環境の異常とその結果を防ぐために、植物と微生物の両方を含む食事に頼っている(143)。
フェニルアラニンとチロシンはメラニン合成の前駆体であり(93)、食事から得られる芳香族アミノ酸は神経伝達物質の生合成の上流にあることに注意することが重要である。フェニルアラニンとチロシンは、L-DOPA、ドーパミン、ノルエピネフリン、エピネフリンの生合成の前駆体でもある。トリプトファンは、もう一つの神経伝達物質であるセロトニンや、メラトニン(神経ホルモン)、ナイアシン(ビタミン)、神経保護物質であるキヌレニン、NAD+およびNADP+(酵素の補酵素)の合成の前駆体であり(143)、これらのほとんどは神経変性疾患で影響を受ける。
昆虫においても、グリホサートはメラニンの合成を阻害することが示されている。Smith et al.(144)は、グリホサートへの曝露は、メラニン阻害と免疫系障害の結果として、昆虫の病原体に対する感受性を高める可能性があると結論づけている。
メラニンの喪失が神経変性疾患の症状の要であるならば、メラニンを増やすことが新たな治療法になるかもしれない。メラニン生成はまた、論理的には症状を改善し、あるいは病気を根絶することになる。先に述べたように、抗癌剤であるニロチニブはメラニン生成を誘導する(145)。AD、PD、LBD患者にニロチニブを投与すると、認知症状や運動症状の軽減が認められた(43–45)。ある投与量でメラニンを増加させるニコチンと認知症状についても同様である(74,75,84)。
8. メラニン、ヒスタミン、免疫系
神経変性疾患ではメラニンが失われるため、体がメラニンを合成しようとすることでそれを補おうとしているのではないかと推測している。研究によると、パーキンソン病患者ではヒスタミン濃度が有意に上昇していることがわかった(146)。ヒスタミンはチロシナーゼを活性化し、メラニン生成を誘発する(147)。ヒスタミン濃度の増加はパーキンソン病患者の大脳基底核でも認められている(148)。ヒスタミンは神経炎症も引き起こす(149)。ADでは、神経細胞のヒスタミン作動系の変化が認知機能の低下を予測し、ヒスタミン3受容体(H3R)拮抗薬が認知症状を緩和する(150)。レビー小体型認知症およびアルツハイマー病患者では、皮質および基底核構造におけるH3Rレベルの上昇が認められた。淡蒼球におけるH3Rの増加は妄想や幻覚と関連していた(151)。我々は、ヒスタミン高値による炎症が認知症の根本的な原因であると推論している。重要なことは、Kawamoto et al.(152)は、メラニンがマスト細胞の脱顆粒を強力に抑制することを発見した。ヒスタミンはマスト細胞で産生され、貯蔵される。ニューロメラニンが失われれば、ヒスタミンレベルが上昇することになる。Rocha et al.(153)は、ヒスタミンがミクログリアの活性化とドーパミン作動性細胞死を誘導することを発見した。アレルギー反応に対するメラニン治療の効果は、フマル酸ケトチフェンとほぼ同等であり、細胞毒性の証拠はなかった。この研究は、ホモジナイズしたメラニンをマスト細胞(152)が関与する疾患の治療薬として使用できる可能性を示すものであり、われわれの理論をさらに支持するものである。
興味深いことに、食品から摂取されたメラニンは免疫系に影響を与える。ElObeid et al.(31)は、IgAやインターロイキン-1の放出、サイトカイン産生、抗体産生の増加、その他の免疫系反応の活性化、抗炎症作用、抗酸化作用、その他の保護作用など、メラニンの摂取による免疫系の増強と調節についてレビューしている。
9. 薬物有害反応とメラニン
もう一つの疑問は、神経変性疾患と薬物過敏症との間にどのような関係があるのか、そしてそれはメラニンと関係があるのか、ということである。認知症患者では中枢神経系に作用する薬物の副作用のリスクが高いが(154)、ある種の薬物はメラニンを含む組織との結合能が高いため(155)、神経変性疾患におけるメラニンの消失がこうした薬物過敏症を引き起こしているのではないかと考えられる。実際、Bridelli et al.(156)のデータは、メラニンの薬物結合能が薬用活性炭に匹敵することを示している。メラニンと神経メラニンは、細胞を保護するために薬物や金属を保持し、その後ゆっくりと放出するのかもしれないが、蓄積と放出は毒性を引き起こすかもしれない(31)。内耳、目、皮膚の色素組織に薬剤が滞留すると、細胞にダメージを与える。例えば、クロロキンは真皮のメラノサイトや毛包に蓄積し、耳鳴り、難聴、めまいを引き起こすことがある(156)。さらに、皮膚の光毒性を引き起こす薬剤もある(157)。高い神経メラニン親和性は、中枢神経系における薬物有害反応やPDの病因に関与しているようである(158)。
10. 光が神経変性疾患を改善するという証拠
もし我々の理論が正しければ、神経メラニンが不足している脳の領域に光子を照射すれば、神経変性疾患やその他の疾患を効果的に治療できることになる。フォトバイオモジュレーションは、光を治療的に用いて身体を癒す技術である。脳疾患の治療には経頭蓋的に使用される。光バイオモジュレーションのメカニズムはよくわかっていない。ミトコンドリア内の発色団が光子を吸収すると考えられている。これらの発色団には、シトクロムCオキシダーゼ、オプシン、熱ゲートイオンチャネル、シトクロム/フラボタンパク質などが含まれる。しかし、これらの発色団のどれもが光線を大量に吸収するという強い証拠はなく、シトクロムCオキシダーゼが光線吸収に関与しているという証拠もない。ともあれ、光バイオモジュレーションは、プラークを除去し、炎症を抑え、ミトコンドリア機能を回復させることにより、神経変性疾患を含む様々な脳疾患の治療に有効であることが示されている(Hamlinの総説)(159)。われわれは、光がメラニンによって吸収されていると理論的に考えている。
興味深いことに、次のセクションでさらに詳しく述べるが、ミクログリアにはさまざまな表現型がある。神経炎症は、M1表現型のミクログリアが活性化することによって起こる。ミクログリアは、貪食機能を低下させながら、炎症性サイトカインを放出する。これらのミクログリアは病原体、プラーク、損傷したニューロンを除去する。ミクログリアは光バイオモジュレーションによってM1表現型からM2表現型に移行することができ、プラークを除去し、抗炎症作用と抗酸化作用を発揮する。光バイオモジュレーションはまた、神経新生を刺激し、シナプス形成を促進することが示されており、これは神経変性疾患だけでなく、外傷性脳損傷、脳卒中、気分障害の治療にも不可欠である(Hamblinの総説)(159)。
11. 幹細胞は色素性ニューロンとミトコンドリア機能を回復させる
もし私たちの理論が正しく、神経変性疾患の根底にある問題が、神経細胞への病原体の侵入と、それに続く炎症を含む免疫反応、しかし病原体を除去するエネルギー不足にあるとすれば、新しい健康な細胞が病気を治療することになる。実際、幹細胞に関する研究は、それが事実であることを示す重要な証拠を提供している。ヒト子宮内膜由来幹細胞を免疫不全PDモデルマウスに移植すると、ドーパミン産生が回復した(160)。これは、メラニンを含むドーパミン作動性細胞への形成を示唆している(41,105)。臍帯、骨髄、脂肪組織由来の間葉系幹細胞は、ADマウスモデルにおいてミクログリアの活性化を誘導し、Aβ沈着、タウの過剰リン酸化、神経炎症を抑制し、認知機能の改善をもたらした(161–164)。ヒト月経血由来幹細胞(MenSC)をADモデルマウスの脳に脳内移植したところ、ミクログリアが活性化され、それまでの炎症性サイトカインではなく、抗炎症性サイトカインが発現するようになった。これらの新しく形成されたミクログリアはAβ斑を除去した(165)。Moir et al.(12)は、これらのプラークがどのように病原体を包み込んで殺すかを示している。われわれは、MenSCsによってもたらされた新しい健康な細胞は、メラニンから正常なエネルギー供給を受けた結果、病原体を除去し、非炎症性ミクログリアの誘導は病原体の根絶から生じたのではないかと推論している。さらにADでは、タウが神経細胞で高リン酸化され、微小管からタウが剥離する。この剥離により、ミトコンドリアが軸索に運ばれなくなる。MenSCsは、タウがもはや過リン酸化されないようにし(165)、軸索へのミトコンドリアの輸送を可能にし、ミトコンドリア機能を回復させたと予測された。
12. 理論の検証
神経変性疾患におけるメラニンの役割を調査し、新しい治療法や治療プロトコルを開発するために、私たちは、より即効性のある解決策を提供するために、すでに他の適応症での使用が承認されている薬剤や技術を再利用することを想定している。有効性と安全性の研究が必要である。一つのアプローチとして、以下のようなものが考えられる:
- 1.血液検査で病原体に対する免疫反応を調べる。すべての感染症がこのような測定に現れるとは限らないことに注意すること。
- 2.血液脳関門を通過するが、メラニン/メラニン生成に影響を与えない抗炎症剤を投与する。
- 3.細胞外および細胞内のプラークやマトリックスを、この目的ですでに市販されている薬剤で除去する。
- 4.血液脳関門を通過し、マトリックスや線維の残骸に浸透できる適切な細胞内抗菌剤で病原体を殺す。
その強力さとバイオフィルムを破壊する能力から、将来使用するために調査する価値があると思われる抗菌剤のひとつが、ハダカデバネズミ由来の高分子ヒアルロン酸である。興味深いことに、ハダカデバネズミは脳や他の組織で質量6-12 MDaの高分子ヒアルロン酸を大量に合成しており、ハダカデバネズミの脳にはプラークは形成されない。この高分子ヒアルロン酸は、ヒトが合成する高分子ヒアルロン酸(1-2 MDa)よりかなり重い(166–168)。5.神経メラニンレベルを改善するには、ニコチン、特に経口暴露を避けるためのパッチ、ニロチニブ、同じくメラニンを増加させるサリチルアミドなどの薬物(169,170)や、ホモジナイズしたメラニン、あるいは高濃度の食品由来のメラニンを試す。
サリチルアミドはB16F1黒色腫細胞のメラニン合成を促進する
白斑は、世界人口の0.5~1%が罹患していると推定される、最も一般的な色素脱失性疾患の一つである(Ezzedineet al.)この疾患の原因を説明するためにいくつかの仮説が提唱されており、最も顕著なものは酸化ストレスの蓄積、自己免疫疾患、遺伝的側面である(Alikhanet al.)現在までに、いくつかの化合物や植物抽出物がメラニン合成を刺激することが報告されている。例えば、Kimら(2020)は、Polygonum multiflorumThunb.(ツルドクダミ)の根のエタノール抽出物が、B16F10メラノーマ細胞においてMitf発現を誘導することにより、メラニン合成を刺激することを報告した。Ullahら(2020)は、抗生物質であるホスホマイシンが、Mitfの制御に関与するc-Jun N-末端キナーゼとp38経路のアップレギュレーションを通じてメラニン生成を促進することを示した。現在、白斑の一般的な治療法はUVBを皮膚に照射することである(Sherschunら、2001)。しかし、UVは皮膚に有害である。従って、抗白斑作用を有する新規化合物のスクリーニングは非常に重要である。
結論として、サリチルアミドは主にMitf転写を介してチロシナーゼ発現をアップレギュレートすることにより、メラニン合成を速やかに誘導できることが示された。従って、本研究は、サリチルアミドが化粧品(白髪用を含む)または色素沈着性疾患の内科的治療において有用なメラニン生成誘導剤となり得ることを示している。[R]
シンシナティ小児疾患院がNICU用に開発したもの(171)を強化し、メラニン/ノイロメラニン/フェオメラニン産生を誘発するのに適切な光スペクトルの波長を分散させるように再構成したような光技術、あるいは、メラニン/ノイロメラニン/フェオメラニン産生を誘発する適切な光波長を放射するように開発または変更できる外部ライトボックスやその他の装置や方法論を用いた光バイオモジュレーションも検討すべきである。
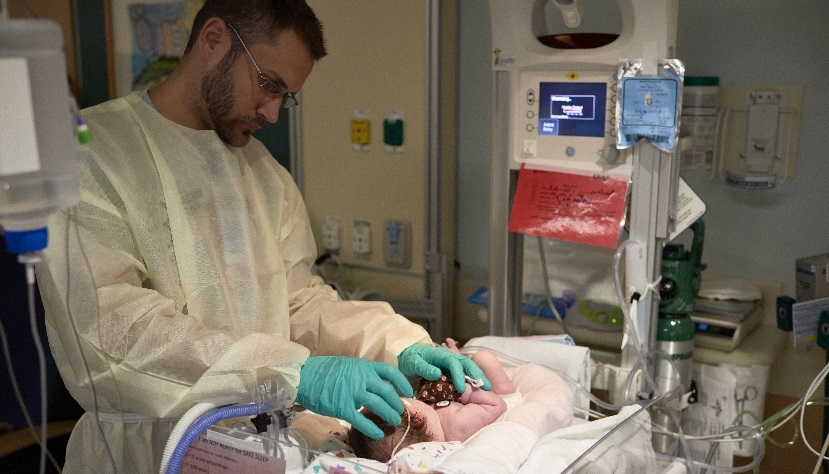
この発見は、 NICUの人工照明下で育てられた早産児の多くが正常な眼の発達を遂げない理由を部分的に説明するものである。
ラング氏はシンシナティ小児科に勤める妊婦たちに、発育途中の子供たちに日光浴をさせるため、定期的に外に出るよう日常的にアドバイスしていたという。
2020年1月、ラングは『Cell Reports』誌で、脂肪細胞内の光を感知するオプシンが代謝に影響を与えることを報告した。2020年9月、ラングの研究チームは再び『ネイチャー』誌に発表し、脳の奥深くにあるオプシンが、太陽光にはあるが人工照明にはない特定の波長の光を直接感知することを報告した。[R]
さらに、メラニン-p1細胞でメラニンを増加させる8種類の低分子化合物(28)や、メラノサイトの修復および/またはメラニン生成を促進する他の新規戦略も研究すべきである。最後に、AD、PD、LBDの予測やモニタリングのためだけでなく、メラニンが関与している可能性のあるすべての疾患や病態、および/またはミトコンドリア機能障害を伴う疾患について、メラニンレベルの正常と異常を判定する検査を開発すべきである。
ミトコンドリアのATP合成酵素を阻害することが知られている低分子化合物であるオリゴマイシンとオーロバーチンBは、アルビノのメラノサイトにおいて、トリアジン系化合物と細胞標的を競合し、色素沈着とチロシナーゼの経路変更に同様の効果を与えることが示された。これは、ミトコンドリアATP合成酵素がアルビノメラノサイトの色素沈着を回復させるための潜在的な治療標的であることを示した初めての例である。[R]
柑橘類ヘスペレチンは成人ヒト表皮メラノサイトにおいてメラニン産生を誘導する[R]
ブドウ抽出物はB16F10黒色腫細胞においてα-MSH誘導性メラニン生成を促進し、レスベラトロールとは逆効果であった[R]
食事からのチロシン摂取量の増加は、成犬の黒毛和種の毛におけるメラニン沈着を増加させる。[R]
12.1.注意書き
なぜなら、メラニンの増加は、病原性のプロセスを助長する可能性があるからである。
13. 結論
1.正常な健康状態では、メラニンは光から吸収したエネルギーの一部を保持し、細胞によって使用されるこのエネルギーは、ATPによって供給されるエネルギーと逆の関係で補充される。
2.メラニン、感染症、神経変性疾患には因果関係がある。神経変性疾患における神経メラニンの消失は、細胞外のß-アミロイドで起こるのと同じアミロイド線維の漂白プロセスによるか、あるいは宿主のメラニンを自らの免疫系を強化するため、あるいは他の支出のために利用する病原体によるメラニンの取り込みによる可能性がある。
私たちは、メラニンの効果や意義が、取り上げた病気に限定されるとは考えていない。事実、私たちはメラニンが疾患の根底にある統一的な要因であると理論化している。今後の研究では、この関連性をさらに調査し、これらの疾患や他の疾患に対する理解をより洗練されたモデルに発展させる必要がある。これによって、新たな洞察が得られ、病気や免疫系に対する理解が深まり、病原体がどのように宿主の免疫系を利用しているのか、侵入するためだけでなく、攻撃を強化するためかもしれないこと、そして病気の新たな治療法が見つかるかもしれない。
略語
AD、アルツハイマー病;Aβ、βアミロイド;ATP、アデノシン5′-三リン酸;MtATPase、F1F0-ATP合成酵素;L-DOPA、L-3,4-デヒドロキシフェニルアラニン;LBD、レビー小体型認知症;Mfn2、ミトフシン-2;NADH、ニコチンアミドアダミンジヌクレオチド水素;PD、パーキンソン病;PHB、プロビンチン;ROS、活性酸素種;UV、紫外線。
利益相反
著者のSBとJBはウィリアム・エドワーズLLCという会社に勤めていた。