Contents
関連記事
概要
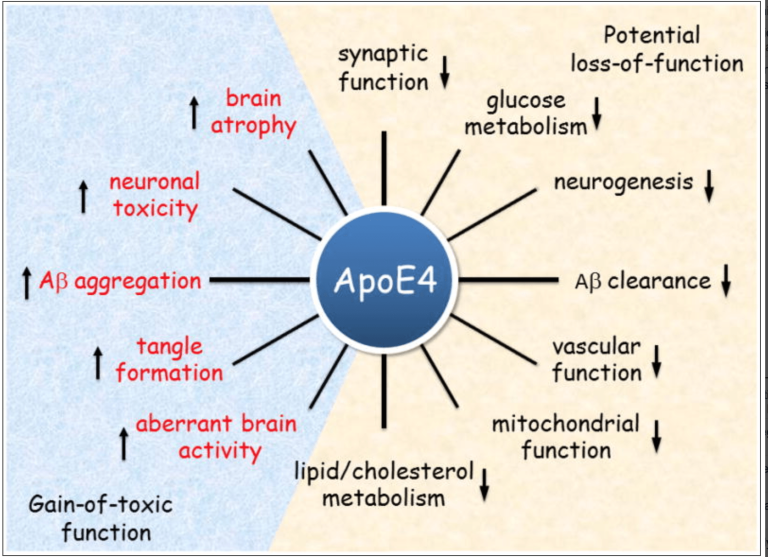
ApoE4の機能
ApoEは末梢コレステロール代謝を調節するために、カイロミクロンおよび中密度リポタンパク質と結合するアポリポタンパクの一種。
他のリポタンパク質は主に肝臓で産生されるが、ApoEは中枢神経、おもにアストロサイトにおいて大量に産生され脳内のコレステロールの運搬の役割を担う。
ヒトのApoEには3つの多型(ApoE2、ApoE3、ApoE4)が存在し、それぞれアミノ酸が数個だけ異なるが、構造的、機能的特徴は大きく異なり、生物学的に大きな影響をおよぼす。
ApoE4遺伝子保有者
ApoE4は、少なくとも一つのApoE4対立遺伝子を人口の約14%(日本人は約10%)が保有しており、アルツハイマー病患者のうち65~80%が同様に一つ以上のApoE4を保有している。
アルツハイマー病発症リスクを増加させる遺伝子は数多くあるが、その中でも、ApoE4は最も強い危険遺伝子として知られている。
ApoE遺伝子型別 アルツハイマー病発症リスク

www.ncbi.nlm.nih.gov/pmc/articles/PMC5605187/
ApoE4とアルツハイマー病
ApoE4とアルツハイマー病の関連性は1993年に発見されたが、現在でもアルツハイマー病研究はアミロイドβに焦点が向けられており、未だApoE4はアルツハイマー病治療の主要な標的とはなっていない。
現在のアルツハイマー病の治療研究はあまりにも狭く、アルツハイマー病患者の異種性に対してすべてに適応できるような「一発必中の魔法の弾」は機能しないという証拠が増えてきている。
ApoE4の標的
ApoE4が認知症・アルツハイマー病の発症リスクに影響を与える経路は非常に多彩であることから、ApoE4の構造的欠陥を修正することで、多面性をもつアルツハイマー病の広範囲にわたる下流シグナル伝達に対抗できる可能性がある。
一部の研究者の間ではApoE4の作用を妨げるアプローチが検討されており、RXRアゴニスト、ABCA1アゴニスト、VEGFの補正、抗ApoE4モノクローナル抗体、などが候補としてあがっている。
ApoE4キャリアの危険因子
ひとまず網羅的に危険因子、治療標的候補などをとりあげ、後に現実的に採用可能な方法を中心に書いていきたい。

アミロイドβクリアランス低下
ApoE4マウスのアミロイドβクリアランス速度は、ApoE3と比較して2~3倍遅い。
www.ncbi.nlm.nih.gov/pubmed/19033669/
アミロイドβの分泌増加
ApoE2<ApoE3<ApoE4の順番でAPP転写を大きく誘導する。in vitro
ApoE4はsAPPαの分泌を低下させる。
www.ncbi.nlm.nih.gov/pmc/articles/PMC3831497/
アミロイドβの凝集
ApoE4はアミロイド蓄積の増加と関連しており、ApoEが病理学的な分子シャペロンとして機能していることを示唆する。
www.ncbi.nlm.nih.gov/pubmed/1625800
脳から単離されたApoE4は、より大きくアミロイドβのオリゴマー化を増加させる。(E2 <E3 <E4
www.ncbi.nlm.nih.gov/pubmed/23100439
www.ncbi.nlm.nih.gov/pubmed/23430745
糖代謝の悪化
ApoE4を発現するヒトの脳ではグルコース取り込み代謝にもっとも不十分なプロファイルを示した。
ApoEのアイソフォームにより、ニューロンへの取り込みを媒介するグルコース輸送体およびグルコース代謝の「ゲートウェイ酵素」として作用するヘキソキナーゼにおいて有意に異なっていた。
興味深いことに、ケトンの取り込みと代謝においてApoE2とApoE4は似たような堅牢性を示したが、ApoE3の脳では不十分なプロファイルを示した。
www.ncbi.nlm.nih.gov/pubmed/29967007
IGF1・IDE・Irs・Glut4
ApoE2脳と比較して、ApoE3、ApoE4の脳は両方とも、IGF1、インスリン受容体基質(Irs)、グルコース輸送体(Glut4)レベルが低下し、グルコース取り込みの減少を示した。
ApoE4脳は、PPARγおよびインスリン分解酵素(IDE)の有意な減少を示し、さらなるグルコース代謝とアミロイドβの調節異常を示した。
www.ncbi.nlm.nih.gov/pubmed/26402005

www.ncbi.nlm.nih.gov/pmc/articles/PMC5485924/
血管機能の低下
ApoE遺伝子型は、脳血流、ニューロン、血管の結合、BBBの完全性に影響を及ぼし、アストロサイト、周皮細胞、平滑筋細胞、脳内皮細胞におけるシグナル伝達、および抹消及び中枢経路の機能不全を誘発する可能性がある。
www.ncbi.nlm.nih.gov/pubmed/26884068/
アミロイド血管障害
ApoE2は高脂血症と関連した血管の変化により微小出血を誘導するが、対照的にApoE4では脳アミロイド血管障害の増加により微小出血を引き起こす可能性がある。
血液脳関門を破壊
ApoE4は外傷性脳損傷後のBBB修復を損なう。
www.ncbi.nlm.nih.gov/pubmed/29618365
jem.rupress.org/content/early/2017/10/20/jem.20171406
アルツハイマー病患者では一般的にBBBの完全性は破壊されると考えられており、ApoE4キャリアにおいてもBBBが損なわれると信じられている。しかしApoE4ノックインマウスでは広範囲のBBB破壊は示さなかった。
www.ncbi.nlm.nih.gov/pubmed/26494278/
シクロフィリンA
シクロフィリンAがApoE4媒介性の神経血管損傷によって生じるニューロンの機能不全および変性を治療するための重要な標的
www.ncbi.nlm.nih.gov/pubmed/22622580/
ミトコンドリア機能(PGC-1α)の低下
PPARγ/PGC-1αシグナル伝達経路はApoE2の脳で活性化され、ApoE4の脳においては阻害される可能性があることを見出した。
注目すべきことに、PGC-1αの過剰発現は解糖系およびミトコンドリア呼吸におけるApoE4誘導性の欠損を改善した。
グルコース代謝の中間体、例えばピルビン酸の提供により細胞質ゾルのグルコース代謝の欠陥を回避する治療アプローチは、ApoE4キャリアに利益をもたらす可能性がある。
www.ncbi.nlm.nih.gov/pubmed/29967007
PPARγの不活性
肝臓X受容体(LXR)およびペルオキシソーム増殖因子受容体γ(PPARγ)の併用治療
www.ncbi.nlm.nih.gov/pubmed/26163517
ApoE4脳は、PPARγおよびインスリン分解酵素(IDE)の有意な減少を示し、さらなるグルコース代謝とアミロイドβの調節異常を示した。
www.ncbi.nlm.nih.gov/pubmed/26402005

www.ncbi.nlm.nih.gov/pmc/articles/PMC5485924/figure/F5/
ApoEの転写制御
ApoE4はDNAに高親和性で結合される。結合部位は、ニューロトロフィン、プログラム細胞死、シナプス機能、サーチュインおよび老化およびインスリン抵抗性に関連する遺伝子を含む1700のプロモーター領域を含む。
これらのプロモーターに関連する遺伝子は、栄養サポート、プログラムされた細胞死、微小管分解、シナプス機能、老化、およびインスリン抵抗性に関連する遺伝子を含む。ApoE4は、NF-κB、IL-6、IL-8を上昇させSirt1の酵素活性を減少させる。
www.ncbi.nlm.nih.gov/pubmed/26791201/
<動画> デール・E・ブレデセン ApoE4のメカニズム
ApoE4は、ヒト神経芽腫におけるヒストンデアセチラーゼ(HDAC)の核移行を増加させ、それによって脳由来の神経栄養因子NDBFの発現を減少させる。アミロイドβオリゴマーも、ApoE4と同様の効果を引き起こす。対照的に、ApoE3はプロテインキナーゼCεの発現を上昇させることにより細胞質ゾル中のHDACを保持する。
PKCε(プロテインキナーゼCイプシロンタイプ/PRKCE)活性化はまた、AβオリゴマーおよびApoE4誘導性HDACの核輸入を逆転させ、BDNFの喪失を防止する。
www.ncbi.nlm.nih.gov/pubmed/25972179/
PKCε活性化剤
ブリオスタチン(フサコケムシ)
www.news-medical.net/news/2009/04/22/80/Japanese.aspx
チャボタイゲキ/Euphorbia peplus
神経可塑性の低下
ほとんどの研究はapoE3がシナプス可塑性を増加させ、apoE4と比較して神経保護効果をより大きく有することを報告したが、apoE4の効果は研究間で一致しなかった。抗LRP1抗体または受容体関連タンパク質(RAP)による神経突起伸長に対するapoEの効果の減弱について、LRP1関与の強力な証拠が存在する。
apoEはApoER2へのリーリン結合を妨げることが知られている
apoE3は、apoEのN末端ドメインとタウの微小管結合リピート領域との間の直接的な相互作用を介してアポE3に熱心に結合するが、アポE4はタウと強く相互作用しない
www.ncbi.nlm.nih.gov/pubmed/25358504/
細胞を老化させる補体C1qの蓄積量は、APOE対立遺伝子に大きく依存する。ApoE4はC1qに覆われたシナプスの蓄積速度を加速化させ、シナプスの脆弱性を増強する。
これはアストロサイトの食作用能力の欠陥を介することを示唆する。
www.ncbi.nlm.nih.gov/pubmed/27559087/
ApoE4は、海馬歯状回におけるGABA作動性介在ニューロンの学習および記憶障害の変性を年齢依存的に引き起こす。これは海馬における低周波数ガンマ波の破壊に起因していた。
www.ncbi.nlm.nih.gov/pubmed/27161522/
BDNF低値
ApoE4がメスのADマウス脳のBDNFシグナル伝達にネガティブな作用を及ぼす可能性がある。エストロゲン受容体β活性の増強が、ApoE4キャリアよりもノンApoE4キャリアに大きな治療上の利益があるかもしれない。
www.ncbi.nlm.nih.gov/pubmed/28934977
Sirt1活性の低下
Sirt1と対抗するSirT2のアップレギュレーションは神経細胞に有毒である。ApoEのアイソフォームはSirt2、Sirt6のタンパク質レベルには影響を与えないが、ApoE4はSirT2タンパク質翻訳速度を増加させる可能性がある。
ApoE3はSirT2 / T1比を変化させない。
www.ncbi.nlm.nih.gov/pmc/articles/PMC3831497/
GSK-3βの活性
ApoE4はGSK3βをアップレギュレートし、タウのリン酸化を増強させる。
www.ncbi.nlm.nih.gov/pubmed/27435766
www.ncbi.nlm.nih.gov/pubmed/28900205
GSK-3β仮説
www.ncbi.nlm.nih.gov/pmc/articles/PMC3073119/
酸化ストレスへの脆弱性
アポリポタンパク質Eの抗酸化活性の強さ順 E2> E3> E4 in vitro
www.ncbi.nlm.nih.gov/pubmed/8782820/
www.ncbi.nlm.nih.gov/pubmed/8024602/
Nrf2
ApoE4マウスでの低いNrf2遺伝子発現
www.ncbi.nlm.nih.gov/pubmed/21626108/
メタロチオネイン
ApoE4ではMT遺伝子発現が損なわれる可能性がある。
ApoE4マウスではMT1およびMT2遺伝子発現の減少を部分的にしか補正できなかった。
www.ncbi.nlm.nih.gov/pubmed/22328270/
ApoE4のメリット
ApoE4遺伝子型は、人類祖先を含む霊長類にのみ存在していることが明らかになっており、ApoE4の維持が選択的利点をもたらしている可能性がある。
www.ncbi.nlm.nih.gov/pubmed/23112842
免疫応答
ミトコンドリア関連の小胞体膜(MAM)機能の活性
ApoE4は、ヒト進化の過程で病原体からの耐性力を有し、高レベルの感染症に曝された集団においては生存価値を有する。
www.ncbi.nlm.nih.gov/pubmed/17430245/
病原体は脂質ラフトより宿主細胞に侵入する。ApoE4はMAM活性をアップレギュレートすることによる自然免疫応答を介して感染性を緩和する可能性。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4718413/
www.ncbi.nlm.nih.gov/pmc/articles/PMC2782461/
ウイルス感染防御
ApoE3はC型ウイルス感染と関連し、ApoE2、ApoE4キャリアでは慢性感染の減少と関連しており、持続的なウイルス感染からの防御を果たす可能性を示す。
www.ncbi.nlm.nih.gov/pubmed/16299033
www.ncbi.nlm.nih.gov/pubmed/12143056/
マラリアからの保護
ApoE4遺伝子の頻度は、サハラ以南のアフリカおよび流行性マラリアを示す他の孤立したパプアニューギニアなどの地域で最も高い。ApoE4は、例えば、熱帯熱マラリア原虫などの感染症からの保護として、選択的利点を提供し得る。
www.ncbi.nlm.nih.gov/pubmed/24241262/
ApoE2は感染の危険因子となる可能性を示唆する。
www.ncbi.nlm.nih.gov/pubmed/12746397
環境因子の影響
ナイジェリアに住むヨルバ人ではApoE4対立遺伝子の保有がアルツハイマー病や認知症リスクの増加と関連していなかった。
ヨルバ人では高脂肪食および血管疾患が一般的に見られないことから、ApoE4対立遺伝子による認知症発症リスクの増加は遺伝的因子と環境的因子の混合によるものである可能性がある。
www.ncbi.nlm.nih.gov/pmc/articles/PMC2855121/
自然流産・周産期死亡を防ぐ
ApoE4遺伝子保有者では、自然流産の頻度が有意に低く、ApoE3では有意に増加した。ApoE4が胚形成中に保護効果を有することを示唆する。
www.ncbi.nlm.nih.gov/pubmed/21626108/
スコットランド人ApoE2遺伝子保有者では周産期死亡の罹患率が有意に上昇した。
www.ncbi.nlm.nih.gov/pubmed/16183800
栄養失調による認知機能低下への保護的役割
発展途上国の貧困地域に住むApoE4遺伝子陽性の小児たちは、重症の下痢・栄養不良による認知的、身体的発達の低下に対する耐性を有していた。
www.ncbi.nlm.nih.gov/pubmed/15611352/
www.ncbi.nlm.nih.gov/pubmed/20401432/
ApoE4治療標的
ApoEアップレギュレーション
肝X受容体/Liver X receptor(LXR)
肝臓X受容体(LXR)およびペルオキシソーム増殖因子受容体γ(PPARγ)の併用治療
PPARγアゴニストの併用により、LXR処置の副作用である血漿トリグリセリド濃度の上昇を打ち消すことができる。
www.ncbi.nlm.nih.gov/pubmed/26163517
レチノイドX受容体/retinoid X receptor(RXR)
エストロゲン
ApoE4マウスへの17βエストラジオール投与は、ミクログリア及びマクロファージの応答を変化させ、ApoE3マウスと比べて有意に炎症応答活性を低下させる。
www.ncbi.nlm.nih.gov/pubmed/17553597
6年間の観察研究
ApoE4陰性の女性のエストロゲン投与では認知低下の速度を半分に低下させたが、ApoE4陽性の女性では認知低下速度は対照群と同様であった。
www.ncbi.nlm.nih.gov/pubmed/10822435
www.alzdiscovery.org/cognitive-vitality/ratings/estrogen
ABCA1/ATP-binding cassette protein A1
ABCA1は末梢細胞からの脂質の除去や HDL 形成に関与するなど、コレステロールホメオスタシスに関わるタンパク質。
ABCA1は、脳のApoE脂質化を介して間接的にアミロイドβクリアランスを促進する。
ABCA1は、核内転写因子LXR/RXRを介して発現が誘導される。
www.ncbi.nlm.nih.gov/pubmed/24844148/
ニューロンにおいて、ApoE4は優先的なタンパク質分解切断を受け、神経毒性フラグメントを生成する。
www.ncbi.nlm.nih.gov/pubmed/24675880/
ApoE媒介のアミロイドβクリアランス LDLR
www.ncbi.nlm.nih.gov/pubmed/25956321/
ABCA1との発現増加とADマウス海馬の認知症重篤度は高度に相関する。
ABCA1は脂質分布に影響を与えコレステロールの細胞からの流出を促進するだけでなく、膜ラフトを破壊し、膜状の脂質構造と構造の物理化学的性質を強力に制御することができる。
www.ncbi.nlm.nih.gov/pmc/articles/PMC2826590/
cAMP
www.ncbi.nlm.nih.gov/pubmed/12454270
TREM2
TREM2は、受容体のIgスーパーファミリーのメンバー
TREM2の変異体は、アルツハイマー病リスクを2~4倍増加させる。
正常なTREM2はApoEタンパク質と結合し、ミクログリアに取り込まれる。
TREM2変異を有するキャリアでは、ミクログリアによるアミロイドβリポタンパク質複合体の取り込みが減少する。
www.ncbi.nlm.nih.gov/pubmed/27477018/
ApoE4は、ApoE3と比較してより低いTREM2発現をもたらす。
このことにより、TREM2媒介性のアミロイドβクリアランスを損なう可能性がある。
www.ncbi.nlm.nih.gov/pubmed/25593125/
アポリポタンパク模倣ペプチド
www.ncbi.nlm.nih.gov/pubmed/21172387
www.ncbi.nlm.nih.gov/pubmed/23603398
www.ncbi.nlm.nih.gov/pubmed/22326991
www.ncbi.nlm.nih.gov/pmc/articles/PMC3897976/
DLK・MKK7・ERK1/2
シナプトヤニン1/Synaptojanin 1
シナプトヤニンは、ニューロンにおける小胞の被覆を伴わないタンパク質であり、脂質ホスファターゼを調節する重要な役割をもつ。
シナプトヤニン/SYNJ1遺伝子の突然変異は、早期発症進行性パーキンソニズムと関連する。
アルツハイマー病の3つの形態(家族性、散発性およびDS / AD)すべてに関与する唯一の他のタンパク質はAPPであるが、SYNJ1レベルの変異も3つのアルツハイマー病で観察される記憶障害の共通する特徴であり得る。
ApoE3はSYNJ1の分解を素早く行うが(半減期2時間)、ApoE4においてはそうではない。(半減期16時間)
www.cell.com/cell-reports/pdf/S2211-1247(18)30744-7.pdf
シナプトヤニン阻害剤 イノシトール-5-ホスファターゼ
pubs.acs.org/doi/pdf/10.1021/cb500161z
サイクリックAMP(cAMP)の活性化により、SHIP1のリン酸化を介してイノシトールホスファターゼ活性を刺激する。
エフリン
エフリン(ephrin)は軸索伸長を反発させる効果をもつ軸索誘導因子として知られている。
シナプトヤニンはエフリンの影響を受ける。
www.ncbi.nlm.nih.gov/pubmed/21113149
エフリンとエフリン受容体
エフリン受容体及びエフリンは、外傷性または虚血性の神経系損傷後の修復プロセスに悪影響を与える。エフリンA4および、他のエフリン受容体の阻害は、損傷した神経の再生及び機能回復を促進するために有用であるかもしれない。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4388660/
エフリンB2レベルを増加させることによって、エフリンBの神経保護作用を促進する可能性がある。
www.ncbi.nlm.nih.gov/pmc/articles/PMC3030448/
ApoE4治療候補 食品・ハーブ類
DHA
高齢化とApoEステータスはDHAホメオスタシスを変化させ、加齢に伴う認知低下と関連する。
www.ncbi.nlm.nih.gov/pubmed/24103099
年齢、性別、BMI、およびAPOE遺伝子などの個人差により、オメガ3多価不飽和脂肪酸の投与の影響が変動する。
www.ncbi.nlm.nih.gov/pubmed/23689286
DHA投与によるApoE4マウスの脳へのDHA取り込みはApoE2マウスよりも低い。
www.ncbi.nlm.nih.gov/pubmed/24345162
血管リスクとApoE4対立遺伝子の相互影響が認知障害と関連する証拠が増えてきている。
www.ncbi.nlm.nih.gov/pmc/articles/PMC3849195/
www.ncbi.nlm.nih.gov/pubmed/27358067
ビタミンC
高齢者の栄養・食事習慣に関する前向き縦断研究。
- APOE E4陽性女性の認知機能低下(認知症またはMCI)のリスク低下と血中ビタミンC値は有意に関連している。
- APOE E4陰性男性の認知機能低下(認知症またはMCI)のリスク低下と血中ビタミンE値は、潜在的な交絡因子をコントロールしているにもかかわらず有意に関連している。
抗酸化サプリメントの投与はまれであったため、患者の血中ビタミンC濃度が高いのは、食事によるビタミンCの多量摂取に起因すると考えられている。このことから、ビタミンCを豊富に含む食事が認知機能の低下を抑制する可能性が示唆された。
www.amed.go.jp/news/release_20180523.html
ビタミンE
ビタミンE投与によるビタミンE濃度の増加はApoE4アルツハイマー病患者において消失しており、酸化ストレスが関与している。
ApoEはそれぞれ異なる経路で、脂質とビタミンEの生物学的利用能に影響を与える可能性がある。
www.karger.com/Article/PDF/90868
αトコフェロールが、アセチルコリンエステラーゼ阻害剤を服用していた軽度から中等度のアルツハイマー病患者の日常生活活動(ADCS-ADL)をプラセボ群と比べて有意に改善した。2000 IU / 日
メマンチンとαトコフェロールの併用療法では臨床的利益を示さなかった。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4109898/
Sirt1活性
- cAMP
- 寒冷曝露
- 運動
- 日光浴
- フルクトース
- オリーブオイル
- フィセチン
- HMB
- ゴツコラ
- アスピリン
- DHA
- EGCG
- 亜鉛
- PQQ
- クルクミン
- フォルスコリン
- αリポ酸
- ニコチンアミドリボシド
- ビタミンD
- ベルベリン
肝X受容体(LXR)アゴニスト
核内受容体肝臓X受容体(LXR)はコレステロール恒常性を調節する重要な因子
レチノイドX受容体/retinoid X receptor(RXR)
DHA
www.ncbi.nlm.nih.gov/pubmed/15073272/
www.ncbi.nlm.nih.gov/pubmed/10835357
アラキドン酸・オレイン酸
www.ncbi.nlm.nih.gov/pubmed/15073272/
Rhein(漢方薬 大黄の根)
www.ncbi.nlm.nih.gov/pubmed/21613212
ABCA1増加
アリシン/Allicin(にんにく・にら、ネギ)
www.ncbi.nlm.nih.gov/pmc/articles/PMC5428973/
ヘスペレチン(レモン、オレンジジュース)
nutrition.merschat.com/foods-by-nutrient.cgi?Nutr_No=759
www.ncbi.nlm.nih.gov/pubmed/22429094
ピペリン(黒胡椒)
ピペリンがABCA1の分解を妨害しABCA1のアップレギュレーションを促進
www.ncbi.nlm.nih.gov/pubmed/27862930
ホノキオール
LXRβの活性化を介在してABCA1発現レベルを増加させる。
www.ncbi.nlm.nih.gov/pubmed/20606297
シリマリン(ミルクシスル)
www.ncbi.nlm.nih.gov/pmc/articles/PMC4748397/
アピゲニン
www.karger.com/Article/FullText/491528
バイカレイン
www.tandfonline.com/doi/full/10.1080/13880200802179584
レスベラトロール
www.atherosclerosis-journal.com/article/S0021-9150(09)00412-2/references
サルビアノール酸B
www.ncbi.nlm.nih.gov/pubmed/25956064
アストラガルス
www.ncbi.nlm.nih.gov/pubmed/19653192
レオヌリン/Herba leonuri
www.karger.com/Article/FullText/484031
テトラメチルピラジン(Ligusticum wallichii Franchat)
www.ncbi.nlm.nih.gov/pubmed/28791414
ApoE4治療候補 その他
運動
回帰分析では、ApoE4キャリアの高い身体活動が反応時間の速さと関連していたが、ノンApoE4キャリアではなかった。
MEG分析では、身体活動によりApoE4キャリアの右下側頭葉の活性化を示したが、ノンApoE4キャリアではその活性化を示さなかった。
www.ncbi.nlm.nih.gov/pubmed/18395955
高齢の女性の有酸素運動への適応は、ApoE4ホモでより有意な認知テスト結果(聴覚言語学習テスト(AVLT)、複合図テスト(CFT)聴覚連続加算タスク(PASAT))と関連していた。
www.ncbi.nlm.nih.gov/pubmed/17218903
中年期の身体活動は、認知症、アルツハイマー病発症リスクの低下と関連しており、特にApoE4遺伝子型では大きなリスクの低下を示し、認知症およびアルツハイマー病の発症を遅らせる可能性がある。
www.ncbi.nlm.nih.gov/pubmed/16239176
一日の身体活動時間が1時間未満の被験者は、認知低下リスクが2倍増加した。ApoE4対立遺伝子キャリアにおいては3.7倍リスクが増加した。
www.ncbi.nlm.nih.gov/pubmed/11323547
運動によるApoE4の安定化は、高齢に伴う神経血管機能不全および補体誘導を防止する。
www.ncbi.nlm.nih.gov/pubmed/26512759
www.ncbi.nlm.nih.gov/pmc/articles/PMC4105011/
食事戦略
ApoE4患者向けダイエット by Gundry博士
優先順位
- 高品質の脂肪、特定のオイル、アブラナ科の野菜
- 半日断食
- ナッツ、小麦粉の代替品、レクチンフリー穀物
- レジスタントスターチ
- 野生の海産物
- 平飼いの家禽、オメガ3含有卵(一般人では平飼いの家禽はOK、しかしApoeE4保有者では非推奨)
- 季節のフルーツ
- 南欧で育てられた牛乳、ヤギの乳、羊の牛乳、バッファローミルク(一般人は少量であればOK、ApoE4患者では禁止)
- 牧草飼育の肉(一般人ではOK、ApoE4保有者では完全禁止)
- 赤ワイン、シャンパン、褐色のお酒
高脂肪食+LXRアゴニスト
マウスの海馬ApoEへの高脂肪食の効果は認知障害を増加させるが、LXRアゴニストによる治療によって症状が逆転し、ApoEレベルの安定性が増加する。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4734705/
ApoE4治療候補 医薬
スタチン
スタチン療法はApoE4対立遺伝子を一つ以上を保有する参加者のアルツハイマー病発症リスクに対して有意差はつかなったのものの、わずかに保護効果を有する。
www.ncbi.nlm.nih.gov/pubmed/15534246
スタチン投与は、高コレステロールレベル、ベースラインの高い認知スコア、ApoE4対立遺伝子を有するアルツハイマー病患者において認知的利益が認められた。
www.ncbi.nlm.nih.gov/pubmed/25004278
www.alzdiscovery.org/cognitive-vitality/ratings/statins
ニコチン
ApoEステータスとニコチン感受性の相互作用と差異
www.ncbi.nlm.nih.gov/pubmed/23958867
ニコチンを摂取するApoE4対立遺伝子保有者での選択的な認知増強(右海馬形成の活性)
www.ncbi.nlm.nih.gov/pubmed/23232444
若いApoE4対立遺伝子保有者ではニコチンによる刺激に対して大きな認知的利益を示す。
www.ncbi.nlm.nih.gov/pubmed/20072115
小規模の臨床試験で認知機能を改善したニコチン用量 5~15mg
高用量では、副作用として睡眠を妨げるリスクとなる可能性が高い。
www.alzdiscovery.org/cognitive-vitality/ratings/nicotine
セレブロリシン
BDNFを増強
軽度から中等度のアルツハイマー病患者へのセレブロリシン投与は脳由来の血清BDNFを増加させた。ドネペジルと併用した場合BDNFの増加は相乗的に増強された。
BDNFの増加は、ApoE4患者でより大きく上昇し、良好な認知改善および併用療法と関連していた。
www.ncbi.nlm.nih.gov/pubmed/27207906
www.alzdiscovery.org/cognitive-vitality/ratings/cerebrolysin
イブプロフェン
ランダム化二重盲検プラセボ対照試験 軽度、中等度のアルツハイマー病患者へ400mg×2回/日投与イブプロフェンを投与されたApoE4キャリアの患者のグループのみ認知低下を抑制した。
www.ncbi.nlm.nih.gov/pubmed/19448381
レチノイドX受容体/retinoid X receptor(RXR)
ベキサロテン
www.ncbi.nlm.nih.gov/pubmed/24849361
www.ncbi.nlm.nih.gov/pubmed/26822146
非ステロイド系抗炎症剤
www.ncbi.nlm.nih.gov/pubmed/15699354/
www.ncbi.nlm.nih.gov/pubmed/20541701/
ロシグリタゾン
www.ncbi.nlm.nih.gov/pubmed/19644018/
ApoE4構造補正剤
www.sciencedaily.com/releases/2018/04/180409112559.htm
ApoE4の高リスク要因
喫煙
ApoE4キャリアの喫煙者は、非ApoE4キャリアの喫煙者よりも皮質のアミロイド沈着が大きい。
www.ncbi.nlm.nih.gov/pubmed/25847292
メタアナリシス 冠状動脈性心疾患リスクはApoE遺伝子型とは関連しない。
www.atherosclerosis-journal.com/article/S0021-9150(14)01348-3/fulltext
飲酒
N2a細胞において、高濃度のエタノール誘発性の神経毒性はApoE3と比べてApoE4タンパク質において有意に増大する。
www.ncbi.nlm.nih.gov/pubmed/29174637
中年での頻繁のアルコール消費は、後の認知障害リスクと関連している。
しかし、頻繁な飲酒が認知症リスクを上昇は、ApoE4対立遺伝子を保持している対象者において生じている可能性がある。
www.ncbi.nlm.nih.gov/pmc/articles/PMC516103/
身体の不活動、高脂肪食(飽和脂肪酸)摂取、アルコールの飲酒および喫煙が、特にApoE4対立遺伝子を保有する人々で、認知症およびアルツハイマー病のリスク上昇と関連していた。
www.ncbi.nlm.nih.gov/pmc/articles/PMC3828889/

飽和脂肪酸
飽和脂肪酸の摂取量上位25%のApoE4を保有しない人では、1.13倍(0.18-6.93)のリスクであったが、ApoE4保有者では発症リスクが11.29倍(0.82-155.94)であった。オッズ比(96%信頼区間)
www.ncbi.nlm.nih.gov/pmc/articles/PMC3828889/
無作為化臨床試験
www.ncbi.nlm.nih.gov/pubmed/23779114/
高血圧
一つ以上のApoE4対立遺伝子保有する高血圧の患者は、その他の危険因子をもたないか一つしかもたない保有者よりも大きなアミロイド蓄積を示した。
www.ncbi.nlm.nih.gov/pubmed/23553344
スウェーデン 6年間の観察研究
ApoE4対立遺伝子、高収縮期血圧(140mmHg以上)、低拡張期血圧(<70mmHg)はアルツハイマー病発症リスクの上昇と関連していた。
高血圧治療はApoE4の状態と関係なく、アルツハイマー病のリスクを有意に低下させた。。
www.ncbi.nlm.nih.gov/pubmed/12963757
メタアナリシス
高血圧治療は、薬剤の種類と関係なく全体の認知機能に利益がある。
アンギオテンシンII受容体拮抗薬(ARB)は、全体の認知に対してプラセボより大きな効果を示した。
www.ncbi.nlm.nih.gov/pubmed/23552124
高血圧治療薬による認知症予防 ジヒドロピリジン、チアジド
www.ncbi.nlm.nih.gov/pubmed/19769454
www.alzdiscovery.org/cognitive-vitality/blog/manage-hypertension-prevent-dementia
水銀
ApoE4キャリアと、慢性水銀中毒、アルツハイマー病、双極性障害およびうつ病症状との間の強い相関関係が、アマルガムによって水銀を暴露した集団において見られた。
ApoE4の存在は水銀中毒のリスクを増加させる可能性を有するが、ApoE2保有者では最も低いリスクを示す可能性がある。
www.bioscience.org/2018/v10e/af/819/2.htm
www.ncbi.nlm.nih.gov/pmc/articles/PMC5295343/
有機塩素系殺虫剤
www.ncbi.nlm.nih.gov/pmc/articles/PMC4132934/
この研究では、有機塩素系殺虫剤DDTの代謝物であるDDEの血清レベルが、MMSEによって評価されるアルツハイマー病診断およびアルツハイマー病重症度と関連していることを示した。さらに、第3位までの血清DDE濃度とAPOE ε4対立遺伝子の存在は、さらに大きな認知障害をもたらした。
他の 2 つの研究では、DDT の散布に従事した労働者が認知機能障害を示すことが明らかになったが、いずれの研究でも DDT または DDE の測定値は得られなかった25,26 。同様に、大規模なコミュニティベースの研究では、有機塩素系殺虫剤への職業的曝露が認知症および アルツハイマー病 と関連していることが明らかになった5。
インドで行われた最近の研究では、DDEに加えて、ジルドリンとβ-ヘキサクロロシクロヘキサンがAD患者の血清サンプル中で上昇していることが明らかになった28。7 我々のコホートのAD患者(86人中17人)の中にはDDEが検出されなかった者もいたが、対照者はDDEレベルの上位3分の1に位置していた。このことは、DDEへの曝露がADの一因となるのは、一部の症例(おそらくDDT/DDE曝露に対してより感受性の高い遺伝的多型を有する症例)のみであることを示唆している。
結論
我々の知見は、有機塩素系農薬への職業的曝露と アルツハイマー病 の関連性を報告している疫学研究5,28,29 を支持し、米国の臨床集団において アルツハイマー病 に関連する特定の有機塩素系農薬として DDT/DDE を特定することで、これらの研究を拡張した。実際、血清DDEレベルの上昇とアルツハイマー病との関連性のオッズ比は、APOEおよび最近報告されたTREM2.3,30,31と同程度に高い。DDEレベルの上昇はMMSEパフォーマンスの有意な悪化と関連しており、APOE ε4対立遺伝子の存在によって悪化するため、APOE遺伝子タイピングを伴う血清DDEレベルの測定は、アルツハイマー病のリスクが高まる可能性のある個人を特定するための有用な臨床指標となるかもしれない。DDTとDDEが細胞内のAPPレベルを上昇させるという知見は、これらの暴露とアルツハイマー病との間の関連性の機序的な妥当性を提供している。
ApoE4のデメリット
弱いプラセボ効果
ドネペジル投与のApoE4キャリアとノンキャリアでは効果に差はなかった。
対照的にプラセボグループではApoE4キャリアよりもApoE4ノンキャリアで有意に大きな改善を示した。
www.ncbi.nlm.nih.gov/pubmed/26402762
セレニウム欠乏
ApoE4キャリアのアルツハイマー病患者は脳内の低いセレニウム濃度と関連する。
pubs.acs.org/doi/abs/10.1021/acschemneuro.7b00014?src=recsys&journalCode=acncdm
チキンエキス
チキンエキスはタンパク質、アミノ酸、ペプチドに豊富に含まれており、カルノシン(β-アラニル-l-ヒスチジン)やその誘導体であるアンセリン(β-アラニル-1-メチル-l-ヒスチジン)などの生理活性ペプチドを含む。カルノシンは、血液脳関門(BBB)を通過することができ、94 ラットにおけるLTP(長期増強)と認知パフォーマンスを向上させる。
チキンエキス(鶏の抽出物)は、ApoE3細胞におけるERK / CREBリン酸化を増強したが、ApoE4細胞においてはこの経路がダウンレギュレーションされた。
以上のことから、本研究では、チキンエキスがApoEアイソフォーム特異的なERK/CREBシグナル伝達の変化を誘発することが示された。チキンエキスは記憶機能を向上させることが報告されている4,6が、この有益な効果はApoEアイソフォームに依存している可能性が示唆された。
www.ncbi.nlm.nih.gov/pubmed/25080220
投薬の副作用リスク・薬剤効果の非効率性
ApoE4遺伝子型をもつ一般集団のグループではスタチン治療を中止する可能性がより高い。
www.ncbi.nlm.nih.gov/pubmed/12668918
ApoE4を保有するパーキンソン病患者への薬物投与は、視覚的な幻覚を発症するリスクが高い。
www.ncbi.nlm.nih.gov/pubmed/10442253
ApoE状態によって早期発症乳がん患者へのホルモン補充に対する応答に差異が生じる。
www.ncbi.nlm.nih.gov/pubmed/20697532/
www.ncbi.nlm.nih.gov/pubmed/18855536
ケトン、中鎖脂肪酸補給の限定的効果