Contents
Chronic inflammation in the etiology of disease across the life span
www.ncbi.nlm.nih.gov/pmc/articles/PMC7147972/
要旨
近年の研究により、ある種の社会的・環境的・生活的要因が全身性慢性炎症(SCI)/systemic chronic inflammationを促進することが明らかになってきた。SCIは、心血管疾患、がん、糖尿病、慢性腎臓病、非アルコール性脂肪肝、自己免疫疾患、神経変性疾患など、世界的に障害や死亡の主要原因となっているいくつかの疾患につながる可能性がある。本論文では、SCIの根底にあるマルチレベルのメカニズムと、この健康を害する表現型を促進するいくつかの危険因子(感染症、運動不足、食生活の乱れ、環境・産業毒物、心理的ストレスなど)について述べる。さらに、SCIの早期診断、予防、治療を進めるための潜在的な戦略を提案する。
過去20年間の最も重要な医学的発見の1つは、免疫系と炎症プロセスが、一部の特定の疾患だけでなく、今日の罹患率と死亡率を世界中で支配している多種多様な精神的・肉体的健康問題に関与しているということである1-4。実際、慢性炎症性疾患は、今日の世界における最も重要な死因として認識されており、全死亡者数の50%以上が、虚血性心疾患、脳卒中、がん、糖尿病、慢性腎臓病、非アルコール性脂肪性肝疾患(NAFLD)自己免疫疾患、神経変性疾患などの炎症関連疾患に起因している。慢性炎症の発症リスクは発育初期にまで遡ることができるという証拠が出てきており、その影響は生涯を通じて持続し、成人期の健康や死亡リスクに影響を及ぼすことがわかっている6-8。本展望では、これらの影響を説明し、今後の研究と介入のための有望な手段をいくつか紹介する。
炎症
炎症は、進化的に保存されたプロセスであり、免疫細胞および非免疫細胞の活性化を特徴とする。これらの細胞は、病原体を排除し、組織の修復と回復を促進することにより、細菌、ウイルス、毒素、感染症から宿主を保護する2,9。炎症反応が全身的なものか局所的なものかなど、その程度や程度に応じて、代謝エネルギーを節約し、活性化した免疫系により多くの栄養素を配分するために、代謝や神経内分泌の変化が起こる9-。炎症が生体に及ぼす具体的な影響としては、悲しみ、快感消失、疲労、性欲や食事量の減少、睡眠の変化、社会行動の引きこもり、さらには血圧上昇、インスリン抵抗性、脂質異常症など、一般的に「疾病行動」として知られる一連の省エネ行動が挙げられる10,13。
正常な炎症反応は、脅威が存在するときに起こる、時間的に制限された炎症活性のアップレギュレーションによって特徴づけられ、脅威が過ぎ去ると解消される9,13,15。しかし、ある種の社会的、心理的、環境的、生物学的要因の存在は、急性炎症の解決を妨げ、ひいては、急性免疫反応時とは異なる免疫成分の活性化を特徴とする、低悪性度で非感染性の(すなわち、「無菌」の)全身性慢性炎症(SCI)の状態を促進することに関連している13,16。
炎症反応が短期から長期に移行すると、免疫寛容の破綻を引き起こし9,15,すべての組織や臓器、正常な細胞生理に大きな変化をもたらし、若年者と高齢者の両方において様々な非伝染性疾患のリスクを高める可能性がある1,9-11,15,17-21。また、SCIは正常な免疫機能を損ない、感染症や腫瘍に対する感受性が高まり、ワクチンに対する反応が悪くなることがある22-。さらに、妊娠中および小児期のSCIは、生涯にわたる非伝染性疾患のリスクを高めるなど、深刻な発達上の影響を及ぼす可能性がある7,8,26,27。
全身性慢性炎症と非伝染性疾患のリスク
両者には共通のメカニズムがあるが、急性炎症反応はSCIとは異なる(表1)。最も特筆すべきことは、急性炎症反応は通常、感染時に自然免疫細胞に発現するパターン認識受容体と病原体上の進化的に保存された構造(病原体関連分子パターン(PAMPs)と呼ばれる)との相互作用を介して開始されることである。急性炎症反応は、細胞のストレスや損傷時に物理的、化学的、代謝的な有害刺激、すなわち「無菌的」な物質に反応して放出される損傷関連分子パターン(DAMPs)によっても活性化される2。感染後は、リポキシン、レゾルビン、マレシン、プロテリンなどの分子が産生され、炎症の収束に寄与する28,29。
表1 急性炎症と全身性慢性炎症の比較
| 急性炎症 | 全身性慢性炎症 | |
|---|---|---|
| 引き金 | PAMP(感染)、DAMP(細胞ストレス、外傷) | DAMP(「エクスポソーム」、代謝機能障害、組織損傷) |
| デュレーション | 短期 | 永続的、非解決 |
| マグニチュード | 高級 | 低品位 |
| 結果 | 治癒、引き金の除去、組織の修復 | 巻き添え被害 |
| 加齢に伴う | 番号 | はい |
| バイオマーカー | IL-6、TNF-α、IL-1β、CRP | サイレント-標準的な標準バイオマーカーはありません |
DAMPはdamage-associated molecular pattern、PAMPはpathogen-associated molecular patternを意味する。
対照的に、SCIは急性感染症やPAMPの活性化がなくても、典型的にはDAMPによって引き起こされる30-32。高齢者では、サイトカイン、ケモカイン、急性期タンパク質の循環レベルが高く、炎症に関与する遺伝子の発現が多いことを示す研究が示すように、SCIはしばしば年齢とともに増加する30。さらに、SCIは(その名が示すように)低悪性度で 持続的であり、最終的には酸化ストレスを誘発するなど、時 間の経過とともに組織や臓器に付随的な損傷を引き起こす1,4,9,19。
SCIによる損傷の臨床的影響は深刻で、高血圧、高血糖、脂質異常症の3つの要素を含むメタボリックシンドローム33,34,2型糖尿病33,NAFLD33,35,高血圧1,心血管疾患(心血管疾患)18,19,慢性腎臓病19,様々な種類の癌17,うつ病21,神経変性疾患および自己免疫疾患4,12,20,骨粗鬆症11,36,サルコペニア19のリスクの増加などがある(図1)。疾患の発症や進行に炎症が関与していることを示す実証的な証拠は、メタボリックシンドローム、2型糖尿病、心血管疾患について最も強い。実際、全身性の炎症を特徴とする関節リウマチなどの自己免疫疾患患者は、インスリン抵抗性、脂質異常症、高血圧を有し、メタボリックシンドローム、2型糖尿病、心血管疾患(特に虚血性心疾患とストロンチウム)の発症率が高いことが古くから知られている10,12,37-39。さらに、炎症性バイオマーカーである高感度C反応性タンパク質(CRP)は、男女ともに心血管イベントの予測因子となっている40。54件の長期前向き研究で得られた16万人以上のデータを対象とした最近のメタアナリシスでは、循環器系CRPの値が高いほど、冠動脈心疾患と心血管疾患死亡率の両方のリスクが相対的に高まることが示された41。
図1 症状 低悪性度全身性慢性炎症の原因と結果
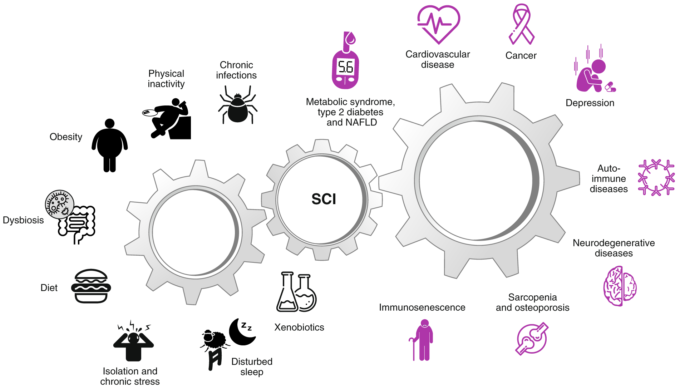
低悪性度全身性慢性炎症(SCI)の原因とその結果がいくつか特定されている。左に示すように、SCIの最も一般的な誘因(反時計回り)は、慢性感染症、運動不足、(内臓)肥満、腸内細菌異常、食生活、社会的孤立、心理的ストレス、睡眠障害と概日リズムの乱れ、大気汚染物質、有害廃棄物、工業化学物質、タバコの喫煙などの異質物質への暴露などである。
右図に示すように、SCIの結果(時計回り)としては、メタボリックシンドローム、2型糖尿病、非アルコール性脂肪性肝疾患(NAFLD)心血管疾患、癌、うつ病、自己免疫疾患、神経変性疾患、サルコペニア、骨粗鬆症、免疫老化などが挙げられる。
SCIと疾患リスクの関連性を示す最も説得力のある証拠は、インターロイキン(IL)-1βや腫瘍壊死因子(TNF)-αなどの特定の炎症性サイトカインを標的とした薬剤や生物製剤を試験した無作為化比較試験(RCT)から得られている。260名の参加者を含む8つのRCTを対象とした最近のメタアナリシスでは、抗TNF-α阻害剤による治療は、関節リウマチ患者のインスリン抵抗性を有意に低下させ、インスリン感受性を改善することが明らかになった42。また、TNF-α阻害剤であるエタネルセプトを投与した関節リウマチ患者さんでは、アルツハイマー病の発症リスクが有意に低下した43。さらに、IL-1β阻害剤であるカナキヌマブの最近の二重盲検RCTでは、心筋梗塞の既往があり、循環CRP値が上昇している1万人以上の成人を対象とし、カナキヌマブを3カ月ごとに皮下投与した患者は、心血管疾患の危険因子であるLDLコレステロールに変化がなかったにもかかわらず、プラセボを投与した患者と比較して、非致死性心筋梗塞、非致死性脳卒中、心血管疾患死亡の発生率が低下した。この試験では、canakinumabを投与された患者は、緊急の血行再建術につながる不安定狭心症の可能性も低かった44。
同様に、北グラスゴーの160,000人以上を対象とした最近の研究では、炎症マーカーである
- CRP(10 mg/L以上、HR 2.71,P < 0.001)
- アルブミン(35 mg/L以上、HR 3.68,P < 0.001)
- 好中球数(HR 2.18,P < 0.001)
の組み合わせが、がん、心血管疾患、脳血管疾患による死亡率に加え、8年間の全死亡を予測することがわかった45。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4346265/
全身性慢性炎症のバイオマーカー
SCIと疾病リスクおよび死亡率とを関連付ける証拠があるにもかかわらず45,現在のところ、健康を害する慢性炎症の存在を示す標準的なバイオマーカーは存在しない。急性炎症の代表的なバイオマーカーは、横断的研究と縦断的研究の両方で罹患率と死亡率を予測することが研究で示されており、したがって加齢性SCIの指標として使用できるかもしれない46。しかし、このアプローチには顕著な限界がある。例えば、Roubenoffらの初期の研究では、歩行者の単球において、IL-6とIL-1Ra(IL-1βやTNF-αは含まない)のレベルが加齢とともに増加することが示された47。しかし、高齢者の健康状態を厳密にコントロールした場合、若年者と高齢者の間でIL-1およびIL-6の発現量に差がないことがわかっている48,49。
さらに、最近の研究では、年齢の異なる41人の健康なボランティアを対象に、18種類の内因性炎症マーカーと生体外で刺激された炎症マーカーのレベルを調べた。その結果、女性ではIL-12p70,男性ではCRPの刺激を受けていないレベルが年齢と関連していることが明らかになったが、IL-1β、IFN-α、TNF-αには影響が見られなかった50。したがって、炎症活性の増大が高齢化と関連しているという証拠があるが、これはすべての炎症マーカーに当てはまるわけではなく、これらの関連は、生物学的な加齢そのものではなく、加齢に伴う慢性疾患や虚弱体質の増加に少なくとも一部が起因している可能性があると考えられる。
少数の炎症性バイオマーカーのみの評価では限界があるため、多数の炎症性マーカーを測定し、これらのマーカーを組み合わせて、炎症活性の高まりを表すより堅牢な指標を作成するという多次元的なアプローチを採用している研究者もいる。このような研究では、主成分分析を用いて、死亡率に加えて、複数の慢性疾患(心血管疾患、腎臓病、糖尿病)のリスクを有意に予測するプロ・アンチ炎症マーカーと自然免疫反応を特定した51。
さらに最近では、SCIと疾患リスクの関連性を調べるために、マルチオミクスの手法が適用されている。この研究者らは、135人の成人を縦断的に追跡し、トランスクリプトームと呼ばれる全血の遺伝子発現、サイトカインやケモカインなどの免疫タンパク質、イミュノームと呼ばれる免疫細胞、CD8+ T細胞サブセット、単球、ナチュラルキラー(NK)細胞、B細胞、CD4+などの細胞サブセット頻度など、詳細な分子プロファイリングを行った52。しかし、この研究はまだ初期段階にあり、加齢に伴う疾患リスクを定量化するために最も有用で予測可能な情報を得るために、SCI関連バイオマーカーの選択と分析のベストプラクティスを明らかにするためには、さらに多くの研究が必要である。
全身性慢性炎症の原因
高齢者のSCI状態は、細胞老化と呼ばれる複雑なプロセスが一因であると考えられている。このプロセスは、細胞増殖の停止と多面的な老化関連分泌表現型(SASP)の発現を特徴としている53。この表現型の顕著な特徴は、炎症性サイトカイン、ケモカイン、その他の炎症性分子の細胞からの分泌が増加することである53。この表現型を持つ老化細胞は、インスリン抵抗性、心血管疾患、肺動脈性肺高血圧症、慢性閉塞性肺疾患、肺気腫、アルツハイマー病、パーキンソン病、黄斑変性症、変形性関節症、がんなど、多くの慢性的な健康状態や疾患を促進する54,55。
老化細胞がSASPを獲得するメカニズムは完全には解明されていないが、既存の研究では、内因性および非内因性の社会的、環境的、生活習慣的な危険因子が組み合わさっていることが指摘されている。この表現型の内因性の原因としては、DNA損傷、テロメアの機能不全、エピゲノムの乱れ、有糸分裂シグナル、酸化ストレスなどが知られている56。非内因性の原因としては、慢性感染症57,生活習慣に起因する肥満58,マイクロバイオームの異常59,食生活60,社会的・文化的変化61,62,環境・工業用毒物63などが考えられている。高齢者のSCI52,64の程度に差があるという事実は、これらの危険因子とSCIとの間の個人内の関連性を記録した研究は限られているが、これらの危険因子および他の関連する炎症性因子への暴露における個人間の差を示していると考えられている。
それにもかかわらず、SCIに関連する非伝染性疾患の違いは、 文化や国によって明らかになっている。最も顕著なのは、SCI関連疾患の罹患率が、西洋的なライフスタイルを送る先進国に住む高齢者と若年者の両方で劇的に増加していることであるが、人類の進化の大部分の時期に存在したものに近い食生活、ライフスタイルおよび生態的ニッチを遵守する非西洋化集団の人々では比較的まれである65-71。さらに、食生活や生活習慣、さまざまな汚染物質への曝露は、酸化ストレスを増大させ、分裂促進シグナル伝達経路をアップレギュレートし、ゲノムやエピゲノムの摂動を引き起こす可能性がある8,60,,
慢性的な感染症
サイトメガロウイルス、エプスタインバーウイルス、C型肝炎ウイルスなどの感染症による生涯にわたる感染がSCIや免疫調節異常に及ぼす影響については、依然として議論の余地がある74-78。加齢に関しては、サイトメガロウイルスの慢性感染は、いくつかの縦断的研究において早期死亡を予測する、いわゆる免疫リスク表現型と関連している79。さらに、HIVの慢性感染は、免疫系の早期老化を引き起こし、早期の心血管や骨格の変化と関連している57。このような影響は、炎症性メディエーターを増加させる老化したCD8+T細胞の蓄積に大きく起因していると考えられている80。
慢性感染症と自己免疫疾患、特定のがん、神経変性疾患、心血管疾患との関連性を報告した研究はいくつかあるが、慢性感染症は環境因子や遺伝因子と相乗的に作用して、これらの健康状態に影響を与えているようだ76,77,81。実際、人間は様々なウイルス、細菌、その他の微生物と 共存しており82 、慢性感染症はSCIの一因となっているようだが、 主たる要因ではないと思われる。例えば、エクアドル・アマゾンのシュアール狩猟採集民83,84,ボリビアのツィマネ採集園芸民68,タンザニアのハドザ狩猟採集民67,ガーナの農村部の自給自足農耕民83,84などの狩猟採集民やその他の既存の非工業化社会の集団がある。ガーナ農村部の自給自足農業従事者85,キタバ(パプアニューギニア)の伝統的園芸農業従事者86など、工業化された環境への曝露は少ないが、さまざまな微生物への曝露は多い人々は、炎症に関連した慢性疾患の発生率が非常に低く、炎症マーカーの変動も大きく、年齢とともに増加することはない65,67,68,83,86。
ライフスタイル、社会的および物理的環境
上述した集団の個人は平均寿命が比較的短いため、一部の人は高度な老化の兆候を示す前に死亡している。しかし、これらの集団にSCI関連の健康問題が相対的にないのは、遺伝や寿命が短いことではなく、むしろ生活習慣の要因やその人たちが住む社会的・物理的環境に起因している66。例えば、これらの人々のライフスタイルは、
- より高いレベルの身体活動67,71,87,
- 主に新鮮な食材または加工度の低い食材で構成された食生活66,88,89,
- 環境汚染物質への曝露が少ないこと
を特徴としている66。さらに、これらの環境に住む人々の概日リズムは、
- 日中の太陽光照射量の変動とより密接に同期
しており90,経験する社会的ストレス要因は、工業化された環境で一般的に見られるものとは異なる91。
このような社会的・環境的特徴は、産業化が進むまでのヒトの進化の歴史の大半で見られたと考えられている66,82,89。工業化は、社会の安定、身体的外傷の減少、近代的医療技術の利用、衛生・検疫・予防接種などの公衆衛生対策の向上など、多くの恩恵をもたらし、乳幼児死亡率の低下や平均寿命の延長に大きく貢献した66。しかし、最近になって、これらの変化は食生活やライフスタイルの急激な変化も引き起こし、進化の大半で人間の生理を形成してきた環境とは大きく異なる生活環境になった。このことが、生態的ニッチからの離脱を特徴とする進化上のミスマッチを人間にもたらしたと考えられており、このミスマッチがSCI65,66,82,89,92の主な原因であるという仮説が立てられている。
身体活動
工業化は身体活動の著しい全体的減少を引き起こしたと考えられている。ある研究によると、全世界で31%の人が身体的不活 動をしていると考えられている。これは、定期的な身体活 動に関する国際的な最低推奨値を満たしていないこと を意味し、不活動のレベルは低中所得国よりも高所得国 の方が高い93。米国では、この数字はさらに高く、米国の成人の約50%が身体活動をしていないと考えられている94。
骨格筋は、ミオカインと呼ばれるサイトカインやその他の低分子タンパク質を産生し、血流に放出する内分泌器官である。これは特に筋肉の収縮時に起こり、全身の炎症を抑制する効果がある95。したがって、低い身体活動は、健康な人97だけでなく、乳がん生存者98や2型糖尿病患者99においても、同化抵抗96やCRPおよび炎症性サイトカインレベルの上昇に直接関係していることがわかっている。これらの影響は、インスリン抵抗性、脂質異常症、内皮機能障害、高血圧、筋肉量の減少(サルコペニア)100など、炎症に関連した病態生理学的変化を促進し、慢性的に運動不足の状態にある人では、心血管疾患、2型糖尿病、NAFLD、骨粗しょう症、各種がん、うつ病、認知症、アルツハイマー病など、さまざまな疾患のリスクが高まることがわかっている95,100。
これらの効果と一致して、身体活動の低下と加齢性疾患および死亡率のリスクの増加との関連性を示す強い証拠がある。欧州、米国、その他の地域のコホートを対象とした研究で、1,683,693人の参加者を対象とした最近のメタアナリシスでは、平均12.8年の追跡期間において、身体活動がない状態から推奨される中強度の有酸素運動を週に150分行うようになると、心血管疾患死亡率が23%、心血管疾患発症率が17%、2型糖尿病発症率が26%低下することが示された101。さらに、いくつかの前向きコホート研究で144万人の参加者から得られたデータもある。 さらに、いくつかの前向きコホート研究で得られた144万人の参加者のデータによると、余暇の身体活動量が多い人(90パーセンタイル以上)と比べて、身体活動量が少ない人(10パーセンタイル以下)は、脂肪率や喫煙状況などの複数の主要な危険因子を調整した後でも、食道腺がん、肝臓がん、肺がん、腎臓がん、胃心筋がん、子宮内膜がん、骨髄性白血病など、いくつかのがんの発症リスクが高い(20%以上)ことが明らかになった(肺がんを除く)102。同様に、10件の研究と23,345人の高齢者(70〜80歳)を3.9〜31年間追跡調査したメタアナリシスによると、国際的な身体活動の最低推奨値を満たしている人は、身体活動をしていない人に比べて、アルツハイマー病のリスクが40%低いことがわかった103。
最後に、身体活動不足は、肥満100,特に炎症の重要な引き金となる過剰な内臓脂肪組織(VAT)と関連しているため、様々な非伝染性疾患のリスクを高める可能性がある104-106。付加価値は、様々な細胞(常駐するマクロファージなどの免疫細胞を含む)で構成された内分泌・免疫・代謝の活発な器官であり、主に脂肪細胞の肥大によって膨張し、低酸素領域や細胞死に至ることもあり、その結果、低酸素誘導因子-1αの活性化、活性酸素種の産生増加、DAMPs(例えば、無細胞DNA)の放出などが起こる。これらの事象は、脂肪細胞、内皮細胞、および脂肪組織に常駐する免疫細胞(例えば、マクロファージ)によるアディポカイン、サイトカイン(例えば、IL-1β、IL-6,TNF-α)およびケモカイン(特に、単球化学吸引性タンパク質-1)を含む多数の炎症性分子の分泌を誘発する105-108。これにより、単球、好中球、樹状細胞、B細胞、T細胞、NKリンパ球などの様々な免疫細胞が付加価値税に浸潤し、T制御細胞が減少することで、炎症が増幅され、最終的には個人によっては長期化・全身化することもある106-109。
さらに、TNF-αなどの分子は、脂肪細胞のインスリン抵抗性を引き起こし、脂肪分解を亢進させ、その結果、脂質が膵臓や肝臓などの他の臓器に流出し、β細胞の機能障害、肝インスリン抵抗性、脂肪肝の原因となる106。したがって、内臓脂肪型肥満は老化を促進し、心血管疾患、神経変性疾患、自己免疫疾患、さらには数種類の癌のリスクを高める19,104,106,110-112。これらの動態は、成人でも発生し、加齢に伴う疾患リスクを促進することが知られているが、最初に現れるのは小児期である26。したがって、小児肥満のパンデミックは、世界中で炎症や加齢性疾患のリスクを促進する上で重要な役割を果たしている可能性がある113。
マイクロバイオームの異常
肥満は、腸内細菌を介したメカニズムでSCIにつながる可能性もある114。例えば、糖尿病のない中程度の肥満のデンマーク人115や重度の肥満のフランス人女性116を対象に行われた研究では、腸内細菌叢の組成や微生物遺伝子の豊富さの変化が、脂肪量の増加、炎症性バイオマーカー、インスリン抵抗性と相関していることがわかった。さらに、高齢者では、腸内細菌叢の変化が複数の炎症経路の結果に影響を与えているようである59。
腸内細菌叢の変化と強く関連する肥満は、腸管の副細胞伝染性の増加やエンドトキシン血症とも関連している114,117。さらに、エンドトキシン血症は、免疫細胞におけるToll様受容体などのパターン認識受容体の活性化を介した炎症や、インスリン抵抗性などの炎症を介した代謝状態の原因となることが疑われている118。興味深いことに、腸管伝染性を高めるタンパク質であるゾヌリンの血清濃度は、肥満の子供や大人117,119,2型糖尿病118,NAFLD、冠状動脈性心臓病、多嚢胞性卵巣症候群、自己免疫疾患、癌の患者で上昇しているようである117。さらに最近では、血清ゾヌリン濃度の上昇が、炎症や身体的弱さを予測することがわかっている120。
より広く言えば、腸内生態系には複雑なバランスが存在し、それが崩れると機能と整合性が損なわれ、ひいては低悪性度SCI59の原因になるという仮説が立てられている。したがって、腸内細菌叢の乱れと腸管の過透磁 率を引き起こす可能性のある要因を特定することが重 要である。その要因としては、抗生物質、非ステロイド性 抗炎症薬、プロトンポンプ阻害剤の多用121,122,過度の 衛生管理と動物や自然の土壌との接触の減少による微 生物への曝露不足(これは人類の進化の歴史の中で もごく最近の現象である)82,123,および食生活123(以 下参照)が考えられる。
食事
過去40年間に多くの国で広く採用されてきた典型的な食生活は、果物、野菜、その他の食物繊維やプレバイオティクスを豊富に含む食品66,123-125が比較的少なく、精製された穀物124,アルコール126,超加工食品125,特に乳化剤を含む食品127が多くなっている。これらの食事要因は、腸内細菌叢の組成と機能を変化させ123,127-130,腸管伝染性の亢進129-131や免疫系のエピジェネティックな変化129と関連し、最終的に低悪性度エンドトキシン血症やSCI129-131を引き起こす。しかし、炎症に対する食事の影響は、このような影響にとどまらない。例えば、食品の加工時や、高温・低湿度の環境下で調理した際に生成される経口吸収型の高度糖化・脂質酸化最終生成物は、食欲を増進させ、栄養過多、ひいては肥満や炎症につながる132。さらに、ほとんどの超加工食品に共通する成分である分離糖や精製穀物などの高グリセミック負荷食品は、炎症遺伝子を活性化させる酸化ストレスの増加を引き起こす可能性がある133。
炎症に影響を与えると考えられている他の食事成分には、トランス脂肪酸134と食塩がある。例えば、食塩は、ナイーブなCD4+ T細胞を炎症性の高いTヘルパー(TH)-17細胞に分化させ、T制御細胞の発現や抗炎症活性を低下させることで、マクロファージを炎症性表現型に偏らせることがわかっている135。さらに、塩分を多く摂取すると、腸内細菌叢の構成に悪影響を及ぼす可能性がある。その例として、高塩分食を摂取した動物やヒトでは、乳酸菌の数が減少していることが挙げられる135。この乳酸菌群は、T17細胞を制御し、腸上皮バリアの健全性を高めることで、全身の炎症を抑制するため、健康には欠かせない135。トランス脂肪酸と塩分を多く含む食品を摂取すると、健康に悪影響を及ぼすことが予想されるが、フランスの成人44,551人を中央値で7.1年間追跡調査した最近のコホート研究では、超加工食品の摂取割合が10%増加すると、全死亡リスクが14%増加することがわかった136。
他のいくつかの栄養因子も炎症を促進し、SCIの発症に寄与する可能性がある。これらの要因には、亜鉛137やマグネシウム138などの微量栄養素の欠乏が含まれ、これはビタミンやミネラルが少ない加工食品や精製食品を食べることによって引き起こされる。また、オメガ3レベル139が最適でないことは、炎症の解決段階に影響を与える。長鎖オメガ3脂肪酸、特にエイコサペンタエン酸とドコサヘキサエン酸は、代謝と炎症に関わる遺伝子の発現を調節する139。さらに重要なことに、これらの脂肪酸は、レゾルビン、マレシン、プロテリンなど、炎症の解決に関与する分子の前駆体でもある28,。世界的にオメガ3脂肪酸の摂取量が少なくなっている主な原因は、魚の摂取量が少ないことと、細胞膜のリン脂質に含まれるオメガ3脂肪酸を置換するリノール酸を多く含む植物油の摂取量が多いことである140,141。また、オメガ3脂肪酸を補給すると炎症が抑えられることが様々なRCTで示されており142-144,従って健康増進効果があると考えられる141-144。
食事と死亡率を関連付ける証拠は強固である。例えば、米国の国民代表健康調査とNational Center for Health Statisticsの疾患別死亡率統計を分析した結果 2005年の米国成人の死亡率が最も高かった食事の危険因子は、トランス脂肪酸の多い食事、オメガ3脂肪酸の少ない食事、塩分の多い食事であった145。また、195カ国の食事データを対象とした最近の系統的な分析では 2017年の死亡の主なリスク要因は食生活の乱れであり、食生活に起因する死亡の半分以上はナトリウムの過剰摂取が原因であるとされている146。
最後に、身体活動の低下と相まって、脂肪、糖分、塩分、香料添加物147を多く含む嗜好性の高い加工食品を摂取すると、細胞の代謝に大きな変化が生じ、ミトコンドリアなどの機能不全の小器官の産生増加(および廃棄不良)や、内因性分子の誤配置、ミスフォールド、酸化などを引き起こす30,60,148。これらの変化した分子は、加齢とともに増加し19,30,自然免疫細胞によってDAMPsとして認識され、その結果、インフラマソーム機構が活性化され、炎症反応が増幅され1,30,60,人生の後半に起こる「自然免疫系の慢性的な生理的刺激の長期的な結果」と定義される「炎症老化」と呼ばれる生物学的状態の原因となる30。提唱されているように、炎症老化は、脳、腸、肝臓、腎臓、脂肪組織、筋肉などの多くの器官系の変化を伴い、ストレスへの適応、エピジェネティクス、炎症、高分子損傷、代謝、プロテオスタシス、幹細胞と再生など、「老化の7つの柱」55と呼ばれる様々な分子老化関連メカニズムによって引き起こされる。
社会的・文化的変化
運動不足や食生活に加えて、産業革命と現代は、社会的交流や睡眠の質59,91に変化をもたらし、SCI149,150やインスリン抵抗性151を促進し、肥満、2型糖尿病、心血管疾患、全死亡のリスクを高めている150-154。さらに、仕事への要求が高く、管理能力が低いという特徴を持つ現代の職場環境に持続的に存在する心理的ストレス要因は、生理的変化155を引き起こす可能性があり、コルチゾールの慢性的な上昇による感受性の低下により、グルココルチコイドが炎症活動を効果的に抑制する能力が阻害され、結果的にSCIや不健康につながる156。
人類の進化の歴史の中でごく最近起こった現代社会のもう一つの中核的特徴は、生物学的に非典型的な時期に人工光、特に青色スペクトルにさらされる機会が増えたことである157-159。特に日没後のブルーライトへの曝露は、夜間の覚醒と注意力を高めるため、概日リズムの乱れを引き起こし158,159,その結果、炎症160が促進され、複数の炎症関連疾患のリスクとなる157,159。一例として、夜勤業務はメタボリックシンドロームのリスクを高めることがわかっており、肥満、2型糖尿病、心血管疾患のほか、乳がん、卵巣がん、前立腺がん、大腸がん、膵臓がんなどの原因となることが疑われている157。
環境・工業毒物
過去200年間の都市化の急速な進展8に伴い、大気汚染物質、有害廃棄物、SCIを促進する工業化学物質など、様々な異生物に人間がさらされる機会がかつてないほど増加した8,161。毎年、推定2,000種類の新しい化学物質が、食品、パーソナルケア製品、処方薬、家庭用洗剤、芝生の手入れ用品など、個人が日常的に使用または摂取するものに導入されている(https://ntp.niehs.nih.gov 参照)。これに伴い、環境中の化学物質がヒトの疾病に与える影響の推定値が増加している162。そのため、米国連邦政府のTox21プログラムのような取り組みによってサポートされている、産業用毒物の細胞経路への影響を調べるためのハイスループットスクリーニングを用いたデータ作成や、化学物質がヒトの健康や疾病の結果にどのように影響するかをよりよく理解するために、多様なデータストリームを統合するトランスレーショナル・システムトキシコロジーのアプローチの採用へとシフトしている163。Tox21プログラムでは、1,600以上のアッセイを用いて9,000以上の化学物質を試験し、人々が日常的にさらされている多くの化学物質が、炎症や炎症に関連する疾患のリスクの根底にある分子シグナル伝達経路を大きく変化させることを実証している164。これらの化学物質には、フタル酸エステル類、パーフルオロアルキルおよびポリフルオロアルキル物質、ビスフェノール類、多環芳香族炭化水素類、難燃剤などが含まれる165。
これらの化合物やその他の化合物は、複数のメカニズムで炎症活動を促進する。例えば、細胞毒性8,162,酸化ストレス、内分泌かく乱物質として、胎児期から作用する可能性がある8。そのため、これらの化学物質は、ホルモン依存性のがん、メタボリックシンドローム、2型糖尿病、高血圧、心血管疾患、アレルギーや喘息、自己免疫疾患や神経変性疾患などの原因となっていることが疑われている8,162,166。世界的な健康問題となっているタバコの喫煙は、様々な炎症関連疾患と関連している異性物質のもう一つの供給源である167。
全身性慢性炎症の発生的起源
SCIの起源は、発生学的な観点からも見ることができる。例えば、幼少期の環境が後年の代謝および免疫反応に大きな影響を与え、それが成人期のSCIを促進することはよく知られている8,26,27,168,169。例えば、幼少期の肥満は、脂肪組織の大きな変化や代謝機能障害と強く関連しており、代謝関連SCI、いわゆるメタ炎症を引き起こす26。肥満の子供が思春期や成人になって肥満になることが多いため26,子供の頃に肥満だった人は成人になっても炎症表現型を発症するリスクが持続することが多いのである。
SCIが幼少期の環境に影響されるもう一つの例として、乳児期に微生物に触れる機会が多いと、衛生仮説(「古い友人」仮説)82で予測されるように、成人期の慢性炎症のリスクが低下することを示す疫学研究がある。さらに、虐待、ネグレクト、マルトリートメント、いじめ、社会経済的に低い環境での生活など、人生の早い段階で心理的ストレスにさらされると、脅威に対する神経反応が高まり、炎症活性170をアップレギュレートしたり、免疫力を変化させたりして、ライフサイクルを通してSCIにつながるという証拠がある27,169。
さらに発達過程を遡ると、免疫系は出生前にプログラムされ171 、子宮内での母親の環境曝露(例えば、感染因子、食生活、心理的ストレス、異生物)によるエピジェネティックな変化の影響を受け、父親の因子もエピジェネティックな影響を与える可能性がある妊娠前でさえも影響を受けることを示すデータがある26,128,171。これらの影響が相まって、SCIのリスクが世代間で伝達される可能性がある。このモデル(図2)では、SCIと疾病リスクは世代を超えて永続すると仮定されている。つまり、妊娠中の母親の炎症172,173は、エピジェネティックな修飾を介して子孫に炎症の「コード」を伝えると考えられている。子孫は、小児期および成人期にSCIのリスク上昇を示し、その結果、肥満7,心血管疾患7,癌174,神経疾患175などを含む様々な炎症関連の健康問題に悩まされる可能性が高くなり、このリスクを再び自分の子孫に伝えることになるのである。
図2 母性型エクスポソーム
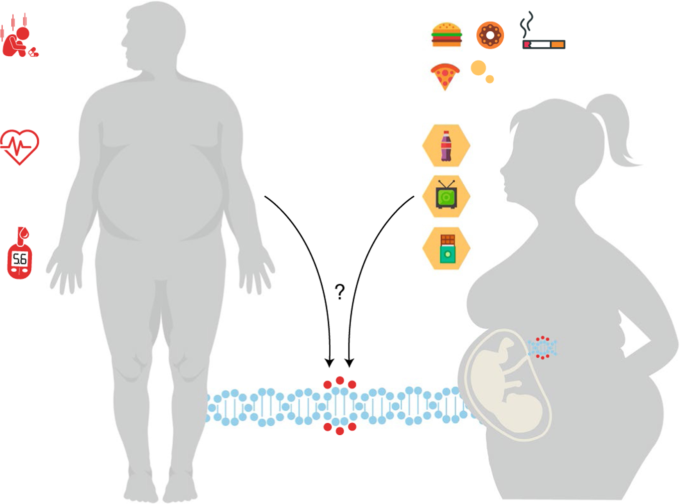
母親のエクスポソームと低悪性度全身性慢性炎症
母親の生活習慣や環境への曝露(エクスポソーム)には、食生活、身体活動、心理的ストレス、子宮内での汚染物質や喫煙などの様々な異質物質への曝露が含まれる。これらの要因は、子孫の免疫系のプログラムに影響を与え、後に炎症性の表現型を引き起こす可能性がある。健康的な食品へのアクセスの悪さ、住居の不安定さ、心理的ストレス、汚染された空気などの環境要因を含む関連因子は、母親がエピジェネティックな痕跡を持つ胎児を出産することにつながり、その胎児が思春期や成人期に肥満、低級SCI、およびそれに関連した結果を引き起こすリスクを高めることになる。
慢性炎症と急性疾患に対する免疫反応
SCIは一般的に年齢とともに増加するという観察結果にもかかわらず、高齢者の大部分は、ウイルス感染症に対する感受性の増加やワクチンに対する反応の弱化につながる免疫反応の構成要素のダウンレギュレーションを経験している。この明らかなパラドックス(Fig.3)は、いくつかのメカニズムで説明できる。
図3 炎症モデル
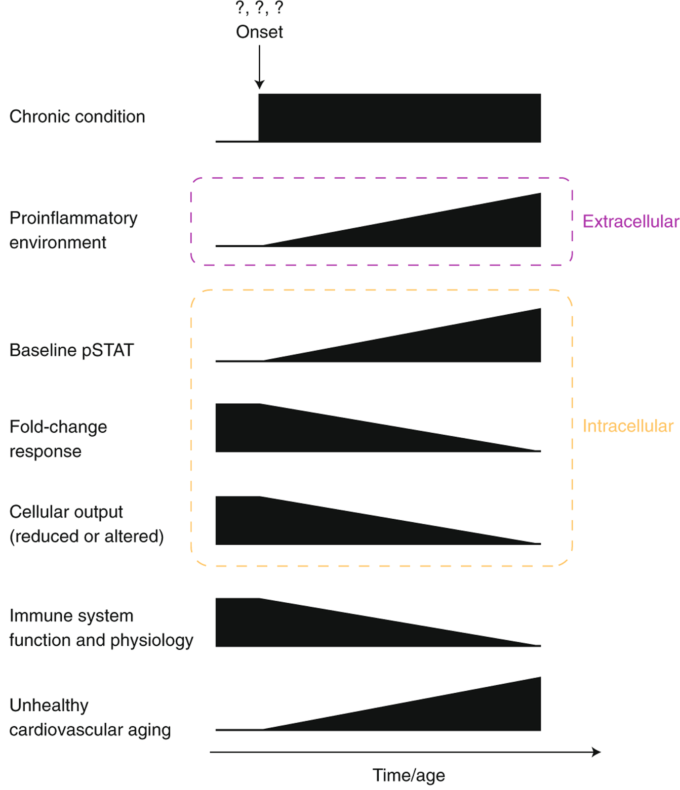
免疫老化と慢性疾患の炎症性モデル。
このモデルは、ベースラインのリン酸化シグナル伝達タンパク質(例えば、リン酸化STAT(pSTAT)レベル)の上昇を、細胞の無反応性や慢性的な炎症活性の上昇と関連付けるものである。このモデルでは、ベースラインのpSTATレベルの上昇と、免疫老化の特徴的な現象、炎症性環境の増加、反応しない細胞、免疫反応の臨床的影響との関連が示されている。(参考文献22,Elsevierから許可を得て引用している)。
具体的には、SCIの上昇は、白血球のヤヌスキナーゼ/シグナル伝達物質と転写活性化物質(JAK-STAT)系などの様々なシグナル伝達経路の基礎的な低レベルの構成的活性化につながり、その結果、慢性炎症を持つ高齢者の免疫細胞では、細胞刺激後のこれらのタンパク質のリン酸化レベルの倍数増加が減少するため、複数の刺激に対する急性応答が弱くなる22。また、SCIの上昇は、ヒトにおけるB型肝炎ワクチンへの反応性低下を予測することが示されている24。さらに、CRPなどの特定の炎症性バイオマーカーは、帯状疱疹ワクチンなどの他のワクチンに対する高齢者の反応と逆相関しているという証拠がある23。興味深いことに、これは若年層にも当てはまるようである。例えば、腸チフスワクチンの接種によく反応した青年は、成人になってからも、反応しなかった人に比べてCRPの濃度が低いことがわかっている25。以上のことから、今回の研究は、加齢に伴って生じる炎症誘発性/抗ウイルス性の偏りを説明するのに役立つ。また、人生の早い段階で炎症環境にさらされることが、大人になってからの免疫表現型のさまざまな側面を決定する重要な要因であることも示唆している。
今後の方向性
これらの研究を総合すると、SCIは、現在世界中の罹患率と死亡率の大半を占め、膨大な人間の苦しみを引き起こす様々な慢性疾患の発症リスクの増加と関連しているという収束的な証拠が得られる。同時に、この研究を強化し、人類の健康を改善するための効果的な戦略に結びつけるために、追求できるいくつかの重要な手段がある。
第一に、SCIに影響を与える複数の因子に関するデータを収集して、異なる分析レベルで特定された曝露と経験がどのように組み合わされてSCIと炎症関連疾患のリスクに影響を与えるかについて、より包括的なイメージを形成するために、SCIに影響を与える複数の因子に関するデータを収集する追加研究が明らかに必要である。第二に、この分野では、急性炎症の代表的なバイオマーカ ーをいくつか組み合わせるだけでなく、SCIの強固な統合的 バイオマーカーを切実に必要としている。既存のバイオマーカーには、主にCRP、IL-1β、IL-6,TNF-αなどがあり、炎症活動が病気や死亡リスクに関係していることを示すのに有用であったが、これらのマーカーは(炎症反応が非常に複雑であることを考慮すると)限られたメカニズム情報しか提供しておらず、炎症関連疾患リスクに影響を与える可能性のある抗炎症制御経路にも対応していない。したがって、今後の研究では、CD8+T細胞サブセット、単球、NK細胞、B細胞、CD4+T細胞サブセットなど、個人間でかなりのばらつきがあることがわかっている追加のバイオマーカーに注目すべきである176。この作業には、現在までに限られた方法でしか検討されていないSCIの分子、転写およびプロテオミクスのマーカーも含めるべきである177。また、マルチオミクス・アプローチ、計算モデル、人工知能を応用して、SCIに関連するメカニズムがどのように変化し、生涯にわたる個人の臨床状態の変化を予測するかを研究することも有用であろう178。
第三に、炎症に影響を与える食事、睡眠、ストレスレベルなどの要因を実験的に操作することは困難であるため、これまでに実施された研究の大半は、免疫系に負担をかけない基礎的な状態で炎症性バイオマーカーのデータを収集している。これは賢明な出発点ではあるが、このような研究では、炎症に関連する疾患リスクの個人差を理解する上で最終的に最も有用と思われる、生物学的反応性や回復(例えば、感染症や心理的・生理的ストレスからの回復)に関する情報は得られない3,179。最後に、ここまで述べてきたSCI促進因子の多くは、運動不足、食生活の乱れ、夜間の青色光への暴露、タバコの喫煙、環境および工業用毒物への暴露、心理的ストレスなど、少なくとも部分的には修正可能であるが、これらの危険因子を標的にしてSCIレベルの対応する減少を示すことに成功した研究の数は限られている。これは、炎症と慢性疾患との関連性が現在広く認識されており、SCIに関連する慢性健康問題で大きな負担を強いられている世界中の人々を治療するための莫大な費用のために、医療制度が崩壊しているにもかかわらず、起こっている。したがって、子供と大人の両方におけるSCI関連疾患のリスクをどのように予防し、治療するかを真剣に研究し始める時が来ている。
結論として、SCIが疾病リスク、生物学的老化および死亡率に果たす役割を完全に理解するまでには、長い道のりがある。例えば、これまでの研究では、胎内から始まり(例えば、母親の曝露、出産の種類、初期の栄養状態を測定することによって)成人期に至るまで(例えば、社会的・文化的プロセス、異種生物の曝露、個人の生活習慣、生涯にわたる抗生物質の使用、予防接種、感染症、社会的・心理的ストレス要因を評価することによって)発達の軌跡全体にわたってヒトのエクスポソーム全体を評価したものはない。さらに、SCIに関連するプロセスを修正することがどのように人間の健康や長寿に役立つかを調査した研究はわずかしかない。その結果、SCIは原理的には非常に修正可能なプロセスではあるが、炎症を標的にして人間の健康を改善することに関連した潜在的な利益を完全に実現するには、さらなる研究、イニシアチブ、投資が必要であると考えられる。