コンテンツ
www.ncbi.nlm.nih.gov/pmc/articles/PMC4221920/
デール・E・ブレデセン1、2
要旨
本報告書は、アルツハイマー病の根本的な病態に基づき、神経変性の代謝促進(MEND)を達成するために設計された複数のモダリティを含む、新規の包括的で個別化された治療プログラムについて述べている。
このプログラムを利用した最初の10人の患者は、アルツハイマー病(AD)、無症候性軽度認知障害(aMCI)、主観的認知障害(SCI)に伴う記憶障害を有する患者である。10例中9例は3~6ヶ月以内に主観的または客観的な認知機能の改善を示したが、1例は非常に末期のアルツハイマー病患者であった。
患者のうち6人は、提示時に仕事を中断しなければならなかったか、仕事に苦労していたが、全員が仕事に復帰したり、パフォーマンスを改善して仕事を続けたりすることができた。改善は持続しており、現時点での最長患者の追跡調査は、最初の治療から2年半で、持続的で顕著な改善が見られた。
これらの結果は、この治療プログラムのより大規模で大規模な試験が必要であることを示唆している。この結果はまた、少なくとも初期の段階では、認知機能の低下の大部分は代謝過程によって引き起こされている可能性があることを示唆している。
さらに、これまでのAD治療薬の単剤治療の失敗を考えると、このような治療システムは、単剤治療では失敗するであろう薬剤が、治療システムの重要な構成要素として成功するためのプラットフォームとして有用である可能性を示唆している。
キーワード
アルツハイマー病、認知症、軽度認知障害、神経行動障害、神経炎症、神経変性、システムバイオロジー
はじめに
問題の大きさ
認知機能の低下は高齢化社会の大きな懸念事項であり、アルツハイマー病は加齢に伴う認知機能低下の主な原因であり、米国人患者は約540万人、世界的には3000万人が罹患しているとされている[1]。効果的な予防と治療法がない場合、2050年にはアメリカ人が1、300万人、世界的には1億6000万人になると予測されており、メディケアシステムの破綻につながる可能性があることから、将来の見通しは非常に懸念されている。他の慢性疾患とは異なり、アルツハイマー病の有病率は増加傾向にあり、効果的な予防と治療法の開発がますます急務となっている。最近の推計によると、アルツハイマー病は心血管疾患、癌に次いで米国における第3位の死亡原因となっている[2]。さらに、最近では、アルツハイマー病のパンデミックの震源地が女性であることが指摘されており、患者の65%、介護者の60%が女性であるとされている[3]。実際、女性がアルツハイマー病を発症する確率は、乳がんを発症する確率よりも高くなっている[4]。
単剤治療の失敗
神経変性疾患治療薬は、間違いなく、生物医学的治療薬開発の中で最も失敗した分野である。感染症などの急性疾患、あるいは心血管疾患、骨粗鬆症、ヒト免疫不全ウイルス感染症、さらには癌などの慢性疾患を有する患者は、ADやレビー小体型認知症、前頭側頭葉変性症、筋萎縮性側索硬化症などの他の神経変性疾患を有する患者よりも、より効果的な治療法の選択肢を得ることができる。アルツハイマー型認知症の場合には、症状の改善効果がほとんどない、病気の進行にほとんど影響を与えない治療法はしかない。さらに、過去10年間だけでも、何百もの臨床試験が、数十億ドルの総費用で、ADのために行われていたが、成功することはなかった。これは、ADのための医薬品開発に取られたアプローチが最適なものであるかどうかに疑問を持っている。
心血管疾患、がん、HIVなどの他の慢性疾患は、併用療法の使用により治療の成功率が向上している[5]。ADとその前身である軽度認知障害(MCI)および自覚的認知障害(SCI)の場合、包括的な併用療法は探索されていない。しかし、過去数十年の遺伝学的・生化学的研究により、ADの発症に関与する分子間相互作用の広範なネットワークが明らかになり、単一の標的ベースのアプローチではなく、ネットワークベースの治療アプローチが、アルツハイマー病による認知機能低下の治療に実現可能であり、より効果的である可能性があることが示唆されている。
前臨床試験
数多くの研究室からの広範な前臨床研究により、潜在的な介入のための複数の病原性標的が同定されている。これらには、アミロイドβ(Aβ)オリゴマーおよびタウに加えて、炎症性メディエーター、アポリポタンパク質および脂質代謝因子、ホルモン性メディエーター、栄養因子およびそれらの受容体、カルシウム調節経路、軸索輸送機械、神経伝達物質およびそれらの受容体、プリオンタンパク、および他の潜在的標的のホストが含まれる。しかし、これらの前臨床研究の欠点の一つは、多くの研究が単一の経路に関連しており、1つの経路を標的とすることで大きな効果を示しているのに対し、ヒトの研究ではそのようなアプローチは実証されていないことである。このような矛盾した結果からは、いくつかの推論が考えられる:
第一に、症状や病態の改善をもたらすためには、複数の経路を同時にターゲットにする必要がある可能性がある。第二に、単一の経路を標的とすることで十分であるが、より早期の介入が必要となる可能性がある。第三に、これらの一見バラバラに見える経路のすべてが、単一の重要な経路に収束する可能性があり、単一の標的治療またはマルチコンポーネント、マルチターゲットアプローチのいずれかが有効であるかもしれない。そして第四に、もちろん、これら2種類のアプローチのいずれも十分ではない可能性がある。しかし、注目に値するのは、ADの病態生理の基礎となるネットワーク内の複数のターゲットに対処することは、各ターゲットが比較的控えめな方法で影響を受けている場合でも成功する可能性があるということである。
我々は、試験管内試験(in vitro)と生体内試験(in vivo)の研究の組み合わせに基づいて、ADが内因性可塑性シグナル伝達のアンバランスに起因するというモデルを進めてきた(図1)、5-9、そして、βアミロイド前駆体タンパク質(APP)がそのような可塑性関連シグナル伝達のメディエーターであるというモデルを構築した。このモデルは、ADが癌、骨粗鬆症、動脈硬化などの慢性疾患に類似していることを示唆している。骨粗鬆症では、骨芽細胞性シグナル伝達が破骨細胞性シグナル伝達によって慢性的に亢進し、結果として骨の喪失を特徴とする加齢に伴う慢性疾患を引き起こす。アルツハイマー病では、可塑性を媒介する動的に対立する生理学的プロセス間の基本的な、年齢に関連した不均衡、すなわち、シナプス可塑性とシナプス破砕活性の間がある。このシグナル伝達には、APP、その誘導体ペプチド、ApoE、タウなどのシナプス形成、維持、修復、リモデリングの生理的メディエーターが関与しており、アルツハイマー病に関連する多くの異種因子のすべてによって調節されている。さらに、新生物の場合と同様に、正のフィードバックが病気のプロセスを選択し、増幅させる。
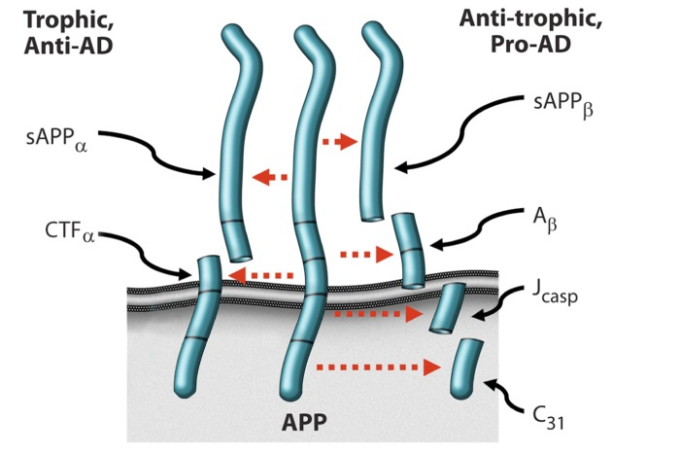
図1 APPの代替処理、およびAPPによるシグナリング。[5].
このモデルの裏付けとして、βアミロイド前駆体タンパク質(APP)のアミロイド生成処理に由来する4つのペプチド-sAPPβ、Aβ、Jcasp、およびC31-は、神経細胞の退縮、シナプス阻害、カスパーゼ活性化、およびプログラムされた細胞死を媒介することが示されている[6、 10-12]。一方、APP-sAPPαおよびαCTFの非アミロイド性処理に由来する2つのペプチドは、神経細胞の伸長を促進し、Aβ産生、カスパーゼ活性化、およびプログラムされた細胞死を阻害することが示されている13-15。このように、APPは可塑性に関連したプロセスを媒介する分子スイッチとして機能しているようであり、ADは因果関係があるのか偶発的なものなのかにかかわらず、ニューライト拡張ペプチドに対するニューライト退縮性ペプチドの比率の増加と関連している。この比率を減少させることは、BACE(βサイトAPP切断酵素)に影響を与えるか、APPの他の切断に影響を与えるかにかかわらず、ADの重症度を緩和するようである [7、 16、 17]。
慢性的なシナプス可塑性:シナプス細胞性アンバランスを修正することを目標とした治療プログラムの開発にとって特に興味深いのは、フィードバック機構である:一方、ホメオスタティック(負の)フィードバックは、単一の目標の結果(例えば、血清pH)を持つ生物学的システムによって利用されており、必要とされていない。一方、プリオニックループ(正)フィードバックは、複数の目標を持ち、迅速な増幅を必要とする生物学的システム(例えば、血栓形成や潜在的にシナプスの変調)で利用され、そのようなシステムは分子スイッチとして機能する[9]。これらの後者のシステムでは、システムの正のフィードバック機能により、関与する分子メディエーターまたはそのサブセットが、それ自身をより多く産生するか、またはそれ自身の活動を増強することが指示される。したがって、このような増幅系はプリオン性であり、感染性の程度は関与する分子種の安定性に依存する。APPシグナル伝達の場合、netrin-1のような栄養リガンドの結合は、相補的なフラグメントであるαCTFがγ-セクレターゼ切断を阻害するγ-セクレターゼ切断を阻害し、BACE切断を阻害するsAPPα[18] [19]の産生を増加させる[14]。同様に、Aβを産生するためのβサイトおよびγサイトでの開裂は、APP-C31産生を増加させるために積極的にフィードバックされ[20]、このようにしてAPPのプロ-AD、抗萎縮性処理を有利にする。さらに、Aβ自体がプリオン性を示すことが示されている[21]が、そのメカニズムは明らかにされていない。
このように、APPの処理は正のフィードバックを示すため、APPとその誘導体ペプチドは分子スイッチとして機能する。このことは、しきい値効果が起こるメカニズムを提供するため、治療法の開発にとって重要な意味を持っている。我々は、この現象を利用して、抗AD、栄養性APPシグナルを増加させる一方で、プロAD、抗栄養性APPシグナルを減少させ[22]、認知力を向上させる薬剤候補を開発してきた[23]。
遺伝的にも薬理学的にも、APP由来のペプチドバランスを媒介または反映する可塑性バランスの操作が、学習および記憶に対する予測可能な効果をもたらすことを見出した(図1)、1)。Asp664のカスパーゼ部位の変異は、ADのPDAPPトランスジェニックマウスモデルで他の方法で発生するシナプス損失、記憶障害、歯状回萎縮を抑制する[7、 17、 24-26]。さらに、野生型マウスD664Aのノックイン研究は、APPが本当に可塑性に根本的に関与しているという考えを支持している。(Kane、 et al、 未発表データ、 2014)
ADのシステム生物学とシステム治療
トランスジェニックマウスの研究は、APPシグナル伝達を操作してADの病態生理を抑制することができることを示唆している。しかし、マウスモデルは、APPまたはプレセニリン-1などの他の家族性AD関連遺伝子の変異を特徴としているが、アルツハイマー病患者の大多数は、APPまたはPS1の変異を伴わない散発性ADに苦しんでいる(大多数はApoEのε4対立遺伝子を発現しているが)。ヒトのAPPシグナルバランスへの多くの入力(例えば、エストロゲン、netrin-1、Aβなど)、および多くの潜在的に治療薬(例えば、エストロゲン、メラトニン、運動、ビタミンD、クルクミン、アシュワガンダなど)のそれぞれで最小限の成功を考えると、ADの病理学は、単一のターゲットとされたエージェントではなく、システムやプログラムを指示する。心血管疾患、新生物、および HIV などの他の慢性疾患での成功は、複数のコンポーネント システムの有効性をサポートする。私の同僚と私は最近、ADのためのそのようなシステムを記述した[5]。このような包括的な治療システムの基本的な考え方は以下の通りである。
- 動脈硬化性心血管疾患などの他の慢性疾患と同様に、目標は単に代謝パラメータを正常化することではなく、むしろそれらを最適化することである。例として、12μmol/lの血清ホモシステインレベルは正常範囲内であると考えられているが、亜最適であることはよく知られている[27]。同様の引数は、他の多くの代謝パラメータについて行うことができる。
- ADは広範な可塑性ネットワークのアンバランスに起因するという仮説に基づいて、治療は、組み合わせが多くの単剤治療薬の効果の合計以上の効果を作成することができるという考えで、可能な限り多くのネットワークコンポーネントに対処する必要がある[5]。
- 骨粗鬆症、癌、心血管疾患などの他の慢性疾患と同様に、基礎となるネットワークには閾値効果があり、ネットワークの構成要素が十分に影響を受けると、病原性のプロセスが停止または逆転する。したがって、ほとんどの患者がプロトコルのすべてのステップに従うことができるとは予想されないとしても、閾値を超えるのに十分なステップが続く限り、それは十分であるべきである。
- このアプローチは、可塑性ネットワークに影響を与える実験値に基づいて個別化されており、多くの生理学的データポイントが分析され、相互に依存するネットワーク構成要素の状態が評価され、治療プログラムを決定するために多くの介入が優先順位付けされるため、計算量が多い。
- プログラムは反復的に行われるため、時間の経過とともに最適化が継続的に行われる。
- それぞれのネットワークコンポーネントについては、生理学的な方法で、可能な限り上流で対処することを目標としている。
結果
ケーススタディ
患者1:病歴
67歳の女性が2年間の進行性の記憶喪失を呈した。彼女は分析報告書の作成や出張などの過酷な仕事をしていたが、データの分析や報告書の作成ができなくなり、仕事を辞めることを考えざるを得なくなった。読書をしていても、読んだ内容が思い出せないため、ページの下の方にたどり着くまでに、もう一度上から読み始めなければならないことを指摘した。彼女はもはや数字を覚えることができなくなり、それらを覚えるために偶数4桁の数字を書き留めなければならなかった。また、道に迷うようになり、見慣れた道でも、どこに出入りするのか分からなくなってしまう。また、ペットの名前を間違えたり、何年も前から家の中にあった電気のスイッチがどこにあるか忘れてしまったりすることにも気づいた。
母親は60代前半から同様の進行性の認知機能低下を発症し、重度の痴呆状態になり、老人ホームに入所し、約80歳で亡くなった。患者が自分の問題について主治医に相談したところ、母親と同じような問題を抱えており、主治医にはどうすることもできないと言われた。カルテに「記憶力の問題」と書いていたため、介護の申請を断られた。
母と同じ問題を抱えていたことを知らされた後、母が老人ホームで衰えていった長年のことを思い出した。有効な治療法がないことを知り、介護を購入できなくなることを知り、自殺を決意した。彼女は同情するために友人に電話をしたが、友人は彼女が飛行機に乗って訪問することを提案し、評価のために彼女を紹介した。
彼女はシステム1.0(表(表1)、1)を開始し、プロトコルの構成要素のいくつかを遵守することができたが、すべてではなかった。それにもかかわらず、3ヶ月後、彼女はすべての症状が軽減していることに気づいた:彼女は問題なく移動することができ、問題なく電話番号を覚え、報告書を作成し、すべての仕事を難なくこなすことができ、情報を読んで保持し、全体的に無症状になった。彼女は、記憶力が長年の間にあったものよりも良くなっていることを指摘していた。ある時、彼女は急性のウイルス性疾患を発症し、プログラムを中止した後、その衰えに気付き、プログラムを再開したところ、回復した。それから2年半後、現在70歳の彼女は今も無症状でフルタイムで仕事を続けている。
表1 治療システム1.0
| 目標 | アプローチ | 根拠・参考文献 |
|---|---|---|
| 食事の最適化:単純なCHOを最小限にし、炎症を最小限に抑える。 | 低血糖、低炎症、低穀物食を数種類から選択できるようにした。 | 炎症を最小限に抑え、インスリン抵抗性を最小限に抑える。 |
| オートファジー、ケトジェネシスの促進 | 就寝の3時間前を含め、毎晩12時間絶食する。 | インスリンレベルを下げ、Aβを減らす。 |
| ストレスを軽減する | ヨガや瞑想、音楽など、個人に合わせたもの。 | コルチゾール、CRF、ストレス軸の低減。 |
| 睡眠の最適化 | 睡眠時間は8時間、メラトニン0.5mgを1週間に1回投与、Trp500mgを3週間に1回投与(覚醒時)。睡眠時無呼吸症候群は除外する。 | [36] |
| エクササイズ | 30〜60′/日、4〜6日/週 | [37,38] |
| 脳への刺激 | 役職者または関係者 | [39] |
| ホモシステイン <7 | Me-B12、MTHF、P5P; 必要に応じてTMG。 | [40] |
| 血清B12 >500 | メB12 | [41] |
| crp <1.0; a/g >1.5 | 抗炎症食、クルクミン、DHA/EPA、衛生状態の最適化 | ADにおける炎症の重要な役割 |
| 空腹時インスリン<7、HgbA1c<5.5 | 同上の食事 | II型糖尿病とADの関係 |
| ホルモンバランス | fT3、fT4、E2、T、プロゲステロン、プレグネノロン、コルチゾールを最適化する。 | [5 , 42] |
| GIヘルス | 必要に応じて補修する;プレバイオティクス、プロバイオティクス | 炎症、自己免疫の回避 |
| A-βの低減 | クルクミン、アシュワガンダ | 43-45 |
| 認知機能向上 | Bacopa monniera, MgT | [46,47] |
| 25OH-D3 = 50-100ng/ml | ビタミンD3、K2 | [48] |
| NGFの増加 | H. erinaceusまたはALCAR | [49,50] |
| シナプスの構造部品を提供する | シチコリン、DHA | [51]. |
| 抗酸化物質の最適化 | ミックストコフェロール&トコトリエノール、Se、ブルーベリー、NAC、アスコルビン酸塩、α-リポ酸 | [52] |
| Zn:fCuの比率の最適化 | 得られる値による | [53] |
| 夜間酸素補給の確保 | 睡眠時無呼吸症候群の除外または治療 | [54] |
| ミトコンドリア機能を最適化する | CoQまたはユビキノール、α-リポ酸、PQQ、NAC、ALCAR、Se、Zn、レスベラトロール、アスコルビン酸、Ti(チアミン | [55] |
| 集中力を高める | パントテン酸 | アセチルコリン合成の必要条件 |
| SirT1の機能を高める | レスベラトロール | [32] |
| 重金属毒性を除く | Hg, Pb, Cdの評価;適応があればキレート化合物 | 重金属の中枢神経系への影響 |
| MCTの効果 | ココナッツオイルまたはアクソナ | [56] |
略語
CHO、炭水化物、Hg、水銀、Pb、鉛、Cd、カドミウム、MCT、中鎖トリグリセリド、PQQ、ポリキノリンキノン、NAC、N-アセチルシステイン、CoQ、コエンザイムQ、ALCAR、アセチル-L-カルニチン、DHA、ドコサヘキサエン酸。MgT、スレオネートマグネシウム;fT3、遊離トリヨードサイロニン;fT4、遊離チロキシン;E2、エストラジオール;T、テストステロン;Me-B12、メチルコバラミン;MTHF、メチルテトラヒドロ葉酸;P5P、ピリドキサール-5-リン酸;TMG、トリメチルグリシン;Trp、トリプトファン
患者1:治療プログラム
上述したように,治療プログラムの構成要素についての長い議論の後,患者はいくつかのシステムを始めたが,すべてを始めたわけではなかった。(1) 彼女はすべての単純な炭水化物を排除し、20ポンドの体重減少につながった; (2) 彼女は彼女の食事からグルテンと加工食品を排除し、野菜、果物、非養殖魚を増やした; (3) ストレスを軽減するために、彼女はヨガを始め、最終的にはヨガのインストラクターになった; (4) 彼女は仕事のストレスを軽減するための第二の対策として、彼女は1日2回20分間の瞑想を始めた; (5) 彼女はメラトニンを服用している0. 5)メラトニン0.5mg po qhs、(6)睡眠時間を毎晩4~5時間から7~8時間に増やし、(7)メチルコバラミン1mgを毎日服用、(8)ビタミンD3を毎日2000IU、(9)魚油を毎日2000mg、(10)CoQ10を毎日200mg、(11)電動フロッサーと電動歯ブラシを使用して口腔衛生を最適化した。(12)プライマリケア提供者との話し合いの結果、2002年のWHI報告後に中止されていたHRT(ホルモン補充療法)を再開した。
患者2:病歴
69歳の企業家・専門職の男性は、11年間にわたって徐々に進行した記憶喪失を呈し、それは1~2年前から加速していた。2002年、58歳の時にロッカーの鍵の組み合わせを思い出せなくなり、自分でも異常だと感じていた。2003年にFDG-PET(フルオロデオキシグルコース陽電子放射断層撮影)を受けたところ、初期のアルツハイマー病に典型的なパターンを示し、両側の頭頂側頭葉と左>右側頭葉ではブドウ糖の利用率が低下しているが、前頭葉、後頭皮質、大脳基底核では利用率が保たれていることが読み取られた。2003年、2007年、2013年に定量的神経心理学的検査を受けたところ、CVLT(カリフォルニア言語学習テスト)が84%ileから1%ile、ストループ色テストが16%ile、聴覚遅延記憶が13%ileに低下していた。2013年、彼はApoE4(3/4)のヘテロ接合体であることが判明した。彼は、仕事中に顔を認識することが困難になってきたことを指摘していた(前突症)、毎日のスケジュールを助手に促さなければならなかった。また、以前に読んだ本であることにようやく気づくまでに、本の数章を読んでいたという出来事もあったという。さらに、彼は人生のほとんどの時間をかけて持っていた能力を失った。
彼は18μmol/lのホモシステイン、CRP <0.5mg/l、25-OHコレカルシフェロール28ng/ml、ヘモグロビンA1c 5.4%、血清亜鉛78mcg/dl、血清銅120mcg/dl、セルロプラスミン25mg/dl、プレグネノロン6ng/dl、テストステロン610ng/dl、アルブミン:グロブリン比1の3、コレステロール165mg/dl、テストステロン610ng/dl、アルブミン:グロブリン比1。 3、コレステロール165mg/dl(リピトール)、HDL 92、LDL 64、トリグリセリド47、AMコルチゾール14mcg/dl、フリーT3 3.02pg/ml、フリーT4 1.27ng/l、TSH 0.58mIU/l、BMI 24.9。
彼は治療的なプログラムで始まり、6ヶ月後に、彼の妻、同僚、および彼はすべての改善を指摘した。彼は10ポンド痩せました。以前とは違って職場での顔を認識できるようになり、毎日のスケジュールを覚え、職場でも問題なく仕事ができるようになった。また、返事が早くなったことも指摘されていた。認知機能の低下が進行している間に失っていた頭の中の数字の列を素早く足していく能力が、生涯にわたって戻ってきていた。彼の妻は、明らかに改善が見られたが、より顕著な効果は、その前の1、2年で衰えが加速していたのが、完全に止まってしまったことだと指摘していた。
患者2:治療プログラム
この患者は、全体的な治療システムの以下の部分から始めた。(1)夕食から就寝までの間に最低3時間、夕食から朝食までの間に最低12時間の断食を行い、(2)食事から単純な炭水化物と加工食品を排除した。(3) 野菜と果物の消費量を増やし、魚の消費量を非農家のものに制限し、肉は牧草飼育された牛肉や有機鶏肉を時々食べるようにした。 5mgのQQを服用し、スケジュールが許す限り一晩8時間近く眠るようにしていた。 8mg、ピリドキシン-5-リン酸50mgを毎日服用していた;(10)シチコリン500mg po bidを服用していた;(11)ビタミンC 1g/日、ビタミンD3 5000IU/日、ビタミンE 400IU/日、CoQ10 200mg/日、ピコリン酸Zn 50mg/日、α-リポ酸100mg/日を服用していた;(12)DHA(ドコサヘキサエン酸)320mg、EPA(エイコサペンタエン酸)180mg/日を服用していた;(12)DHA(ドコサヘキサエン酸)320mg、EPA(エイコサペンタエン酸)180mg/日を服用していた。
患者3:病歴
55歳の弁護士は、4年間に渡って重度の記憶喪失に悩まされていた。家を出たときに誤ってコンロをつけっぱなしにしてしまったことが何度もあり、帰ってきてから再びコンロをつけっぱなしにしてしまったことに愕然とした。打ち合わせを忘れてしまい、複数の打ち合わせに同時に同意してしまう。遅れても何も覚えていないため、会話を録音したり、iPadを持ち歩いて大量のメモを取ったりしていた(iPadのロックを解除するパスワードを忘れた)。彼女は仕事の一環としてスペイン語を学ぼうとしていたが、ほとんど新しいことを覚えることができなかった。彼女は彼女の仕事を実行することができないであった、と彼女は彼女の子供たちに説明するために座って、彼らはもはや彼女の貧しい記憶力を利用することはできないであった、その代わりに、彼らは彼女の記憶喪失が深刻な問題であることを理解しなければならないこと。彼女の子供たちは、彼女が頻繁に文の途中で迷子になること、彼女は応答が遅いこと、そして彼女は頻繁に彼女が彼らに頼んだと思っていたことのフォローアップをしたかどうかを尋ねたが、実際には彼女が言及したタスクをするように彼らに頼んだことがないことを指摘した。
彼女のホモシステインは9.8μmol/l、CRP 0.16mg/l、25-OHコレカルシフェロール46ng/ml、ヘモグロビンA1c 5.3%、プレグネノロン84ng/dl、DHEA 169ng/dl、エストラジオール275pg/ml、プロゲステロン0. 4ng/ml、インスリン2.7μIU/ml、AMコルチゾール16.3mcg/dl、遊離T3 3.02pg/ml、遊離T4 1.32ng/l、TSH 2.04mIU/l。
治療プログラムの5ヶ月後、彼女はもはやメモのためにiPadを必要とせず、会話を録音する必要もないことを指摘した。彼女は再び働くことができ,スペイン語を学ぶことができ,新しい法律の専門分野を学び始めた。彼女の子供たちは、彼女がもはや文の途中で迷子になることもなく、自分が頼んでもいないことを頼まれたと思うこともなく、質問にも普通の速さと記憶力で答えていたことを指摘した。
患者3:治療プログラム
彼女は以下のような治療法を始めた。(1)夕食から就寝までの間に最低3時間、夕食から朝食までの間に最低12時間の断食、(2)単純な炭水化物と加工食品の除去、(3)野菜と果物の消費量の増加、魚の消費量を非農家のものに限定、肉を食べない、(4)週に4~5回の運動、(5)メラトニン0.5mg po qhsの服用、(6)瞑想でストレスを軽減しようとした生活、(7)睡眠時間を8時間に近づけようとした生活、(8)瞑想でストレスを軽減しようとした生活、(8)瞑想でストレスを軽減しようとした生活、(8)瞑想でストレスを軽減しようとした生活、(8)瞑想でストレスを軽減しようとした生活。 (5)メラトニン0.5mg po qhsを服用し、スケジュールに合わせて夜8時間近く眠るようにしていた。(9) 彼女はビタミンD3 2000IU/日とCoQ10 200mg/日を服用していた;(10) 彼女はDHA 700mgとEPA 500mg/日を服用していた;(11) 彼女の主治医はバイオアイデンティカル・エストラジオールとエストラジオール(BIEST)とプロゲステロンを処方した;(12) 彼女の主治医はブプロピオンを150mg/日から150mg/週3回に減らすように彼女の主治医と協力していた;(11) 彼女の主治医はブプロピオンを150mg/日から150mg/週3回に減らした。
10人の患者全員を表2にまとめた。
表2 治療システムで治療された患者の概要
| ペイシェント | 歴史、評価 | 診断名 | ステータス |
|---|---|---|---|
| 67F 3/3 | 2yrメモリ⇓;FH+。 | エーエムシーアイ | ノーマル×2.5年、ワーキング |
| 69M 4/3 | 12歳 記憶力 ⇓ FDG-PET+、NPsych+。 | 西暦前期 | “明らかに改善された; “作業 |
| 70M 4/3 | 4年目の記憶力⇓、NPsych+、MemTrax失敗 | 西暦 | 改善され、MemTraxは合格 |
| 75M 3/3 | 1年メモリ ⇓(1年分 | SCI | 改善され、機能している |
| 75F C677T | 1年メモリ ⇓(1年分 | aMCI/早期AD | 改良型 |
| 55F 3/3 | 4yrメモリ ⇓。 | aMCI/早期AD | 通常時;動作中 |
| 72M 3/3 | 7yrメモリ ⇓。 | エーエムシーアイ | 改善され、機能している |
| 55M 4/3 | 2年メモリ ⇓(2年分 | SCI | 通常時;動作中 |
| 63F 4/3 | FH認知症、軽度記憶力⇓。 | SCI | 正常、アミロイドPET陰性、作業中 |
| 60F 4/3 | 4年間急速に低下、MoCA 6、アミロイドPET+。 | 西暦後期 | 減少 |
略語
F、女性、M、男性、3/3、ApoE 3/3、4/3、ApoE 4/3、C677T、メチレンテトラヒドロ葉酸還元酵素(MTHFR)のC677T変異、FH、家族歴、aMCI、無症候性軽度認知障害、SCI、主観的認知障害、FDG-PET+、アルツハイマー病の典型的な解釈として解釈されるフルオロデオキシグルコースポジトロン断層撮影。アミロイドPET+、アミロイドPETスキャンで異常と判定され、アミロイドの蓄積を示す;NPsych+、ADの典型的な異常を示す神経心理学的定量検査;MoCA、モントリオール認知評価;MemTrax、記憶力を定量的に測定するiPhoneアプリケーション。
考察
ここで報告された10人の患者の結果は、主観的認知障害、軽度認知障害、少なくともアルツハイマー病の初期段階にある患者の記憶喪失が、ここで述べられた治療プログラムによって逆転し、改善が持続する可能性があることを示唆している。これは、そのような最初の実証である。しかし、現時点での結果は逸話的なものであり、より大規模な対照臨床試験が必要である。
ここで報告された結果は、代謝状態が可塑性の重要な、そして容易に操作可能な、決定因子を表し、特にSCI、MCI、および初期のADで示された可塑性の異常なバランスの概念と互換性がある。さらに、ビタミンD3のような単一の代謝パラメータを正常化しても、発症にはわずかな影響しかないが、機能的ネットワークを形成する包括的なパラメータの最適化は、発症およびその結果、機能にはるかに大きな影響を及ぼす可能性がある。
本報告書に記載されている治療システムは、可塑性におけるAPPシグナル伝達とプロテオライシスの役割と、アルツハイマー病で再現性のあるこの受容体プロテオライシスのアンバランスについての基礎研究から得られたものである。このバランスには、ホルモン[28、 29]、栄養因子[18]、グルコース代謝[30]、炎症性メディエーター[31]、ApoE遺伝的状態[32]、睡眠関連因子[33]、運動関連因子[34]など、多くの生理的パラメータが関与している;したがって、治療システムは、アルツハイマー病の病態生理を媒介すると仮定している自己強化的(すなわち、プリオニック的)なシグナル伝達のアンバランスを逆転させるように設計されている[8]。
この研究から得られた潜在的に重要な結果の一つは、治療プログラムが様々な患者の効果的な作業能力に与える影響である。10人の患者のうち6人は発症時に仕事を中断しなければならなかったか、仕事に悩んでいたが、全員が仕事に復帰したり、仕事を続けたりすることができ、パフォーマンスが向上した。さらに1名の患者は、提示時に仕事に支障をきたしておらず、問題なく仕事を続けている。他の3名の患者さんは何年も仕事をしておらず、治療後も仕事を再開していないであった。認知機能の低下で苦労した後に効果的に働くために必要な機能の改善は、成功した治療システムの重要な成果であり、最終的にはバイオマーカーの効果や検査成績よりも患者にとって重要なものである。
ここに記載されているシステムは、初期のシステムであり、最適化の恩恵を受ける可能性が高いシステムであることが認識されている。このシステムは、複数の主要な病原性メカニズムに対処するように設計されているが、主要な病原性メカニズムの大部分は、この初期システムによって亜最適化された影響を受けている。これは、複数の潜在的な治療標的を浮き彫りにしており、これらの標的のそれぞれに対する治療薬の最適化は、現在進行中の研究開発の目標である。
この治療システムの主な副作用は、健康状態の改善および最適なBMI(ボディマス指数)であり、これは単剤治療とは対照的な結果であることは注目に値する。しかし、このプログラムは簡単ではなく、患者の誰一人として、すべてのプロトコルに従った者はいなかった。食事やライフスタイルの変化が大きく、毎日複数の錠剤を必要とすることは、患者の2つの最も一般的な不満であった。しかし、これらの不満は、すべての患者が予後が悪く、認知機能の低下が本質的に治療不可能であることを、医師やメディアを通じて以前から知らされていたという事実であり、軽減されている。
本書に記載された治療プログラムの潜在的に重要な応用の一つは、このような治療システムが、単剤治療では失敗するであろう薬剤が、治療システムの重要な構成要素として成功するためのプラットフォームとして有用であるということである。併用療法は、HIVや癌などの複数の慢性疾患において成功していることが証明されている[5]。
ここで報告された肯定的な結果は、治療プログラムが動脈硬化性心血管疾患、HIV、および癌などの複数の慢性疾患において単剤治療薬よりも効果的であることが証明されていることを考えると、おそらく驚くべきことではない[5、 35]。確かに、慢性疾患は単剤治療よりも治療系の方が従順であるかもしれない。しかし、現在の逸話的な結果は、ここで報告された結果を確認または反論するためだけでなく、日常的に達成できる改善の程度、認知機能低下の反転はどの程度遅くまで効果があるのか、そのようなアプローチが家族性アルツハイマー病患者に有効かどうか、改善はどの程度の期間持続するのかといった重要な疑問に対処するために、より大規模な試験を必要としている。
まとめ
- アルツハイマー病の根本的な病態に基づいた、新規で包括的な個別化された治療システムが記載されている。また、このシステムを開発するための基本的な考え方も述べられている。
- アルツハイマー病(AD)、無症候性軽度認知障害(aMCI)、主観的認知障害(SCI)に伴う記憶喪失を有する患者を含む、このプログラムを利用した最初の10人の患者のうち、9人が主観的または客観的な改善を示した。
- 重要な結果として、認知機能の低下が仕事のパフォーマンスに大きな影響を与えていた6人の患者のすべてが、仕事に復帰したり、仕事を継続したりすることができたことが挙げられる。
- これらの逸話的な結果は、治療プログラムの対照臨床試験の必要性を示唆している。
