Contents

マイケル・パーマー医学博士
スチャリット・バクディ(Sucharit Bhakdi)医学博士
マーゴット・デボア(Margot DesBois)学士
ブライアン・フッカー(Brian Hooker)博士
デイヴィッド・ラスニック(David Rasnick)博士
メアリー・ホランド(Mary Holland)法学博士(タートルズ・オール・ザ・ウェイ・ダウンの編集者)
キャサリン・オースティン・フィッツ(Catherine Austin Fitts)
mRNAワクチンの毒性 D4CE.org
文と図版:マイケル・パーマー医学博士、以下からの寄稿による。
この作品はクリエイティブ・コモンズ 表示-非営利-継承 4.0 国際ライセンス(CC BY-NC-SA 4.0)の下でライセンスされている。これは、非営利目的に限り、この本を共有し、内容を翻案し、再利用することが自由であることを意味する。そのような場合、あなたはこの出典への適切なクレジットを示し、ライセンスへのリンクを提供し、再利用された素材に変更が加えられたかどうかを示さなければならない。他の言語への翻訳を含む商業的な翻案については、著者に連絡すること。
これらの要件から免除されるのは、フェアユースに相当する本作品の小部分の再利用である。また、本作品に含まれる画像や引用文は、他の様々な作品から引用されたものである。著者らは、本書におけるこれらの素材の使用は、フェアユースのルールのもとで許されるものと考えている。
詳細はこちらを参照のこと:
creativecommons.org/licenses/by-nc-sa/4.0/。
これはバージョン1.0(2023年7月28日)である。この文書の更新版を確認するには、ホームページを参照のこと:
d4ce.org/mRNA-vaccine-toxicity/ 印刷版はhttps://tinyurl.com/mRNA-vaccine-toxicity。
コメント、質問、訂正については、mRNA-vaccine-toxicity@posteo.net まで電子メールをお送りいただきたい。
表紙のグラフィックは、ソラーリ・レポート(https://home.solari.com/)のために jermwarfare.com/ のジェレミー・ネルが作成し、許可を得て使用している。
アルネ・ブルクハルト医学博士を偲ぶ
1944 – 2023
アルネは熟練した病理学者であったが、2021年、遺伝子ベースのCOVIDワクチンによって引き起こされた傷害と死亡を調査するために、十分に稼いだ引退生活から抜け出した。
アルネの精力的で専門的な研究により、ワクチンが血管やすべての主要臓器に誘発した炎症が明確に証明された。アルネは死の直前、ブリュッセルの欧州議会で研究結果を発表した。
私たちはアルネの献身と勇気、そして優しさに深く感謝している。彼は永遠に私たちの心の中にいることだろう。
目次
- 巻頭言
- 献辞
- 図のリスト
- 表のリスト .
- メアリー・ホランドによる序文
- 序文
- 1 はじめに
- 1.1 mRNAワクチンは原理的に危険なのか、それとも観察された害は偶発的なのか?
- 1.2 COVID-19ワクチンは決してあなたの健康のためではなかった
- 1.3 緊急使用許可の誤用と規制当局のセーフガードの崩壊
- 1.4 本書が書かれた理由
- 2 ウイルス学と免疫学のいくつかの要素
- 2.1 ウイルスのライフサイクル
- 2.2 ウイルスに対する免疫 .
- 2.3 非常に多様なT細胞とB細胞のリザーバーはどのようにして生まれるのか?
- 2.4 免疫学的記憶
- 2.5 交差免疫 .
- 2.6 ウイルス感染を本当に制御しているのは誰か:抗体か、細胞傷害性T細胞か?
- 2.7 呼吸器ウイルスに対する免疫:全身性免疫と粘膜免疫
- 2.8 ワクチン戦略
- 2.9 付録:ファイザー社の臨床試験における不正の証拠
- 3 mRNAワクチンによる害の免疫学的メカニズム
- 3.1 mRNAワクチンは全身に分布する 特に血管に影響を及ぼす
- 3.2 スパイクタンパク質の体内発現は広範囲で長期間持続する
- 3.3 mRNAワクチンLNPは免疫系のレーダーをかいくぐる
- 3.4 自己免疫疾患の誘発
- 3.5 ワクチンによる免疫抑制
- 3.6 mRNAワクチンによる害の基本的メカニズムは完全に一般的である
- 4 mRNAワクチンによる免疫学的危害の病理学的証拠
- 4.1 組織病理学で使用される主な技術
- 4.2 証拠のソース
- 4.3 mRNAワクチン接種によって誘発される血管炎
- 4.4 臓器特異的細胞や組織に対する免疫攻撃
- 5 mRNAワクチンの薬物動態と脂質毒性
- 5.1 脂質ナノ粒子の構造と機能
- 5.2 mRNAワクチンの薬物動態
- 5.3 脂質ナノ粒子の毒性
- 5.4 付録 規格外製造の証拠
- 6 mRNAワクチンの遺伝毒性
- 6.1 合成カチオン性脂質の遺伝毒性
- 6.2 ワクチンmRNA配列のDNAへの逆転写DNA
- 6.3 ファイザーとモデナのmRNAワクチンにおけるプラスミドDNAの混入
- 6.4 非自己遺伝子のDNAコピーがもたらす既知の、そしてもっともらしいリスク
- 7 COVID-19 mRNAワクチンの有害事象の疫学
Margot DesBois, B.A.およびBrian S. Hooker, Ph.D.- 7.1 はじめに
- 7.2 一般的有害事象、重篤な有害事象、死亡、入院、生命を脅かす事象
- 7.3 心イベント
- 7.4 血栓性事象
- 7.5 神経学的事象
- 7.6 免疫学的事象
- 7.7 生殖に関する事象
- 7.8 結論
- 8 エイズとHIV: 医学倒錯の青写真
デビッド・ラスニック博士- 8.1 AIDSは新奇な伝染病のようには振る舞わない
- 8.2 エイズと薬物乱用
- 8.3 ピーター・デュースバーグのHIV/AIDS仮説に対する科学的批判
- 8.4 HIVは性感染症ではない
- 8.5 HIVがエイズを引き起こすという証拠を求めるカリー・マリスの探求
- 8.6 反体制派の磔刑
- 8.7 アフリカにおけるエイズ
- 8.8 タボ・ムベキによるエイズの真相究明への不運な試み
- 8.9 エイズの正統性に異議を唱えるいくつかの証拠
- 9 まとめと結論
- 9.1 mRNAワクチン毒性の重要なメカニズム
- 9.2 害の免疫学的メカニズムは完全に一般的である
- 9.3 適正製造規範に戻れば、mRNAワクチンの毒性はなくなるのか?
- 9.4 mRNAワクチンが本質的に危険なものであるならば、なぜ私たちに接種が促され、強要されるのか?
- 9.5 私たちに何ができるのか?
- あとがき キャサリン・オースティン・フィッツ
- 参考文献
図表一覧
- 1.1 フランスにおける2018年、2019年、2020年の3月から6月までの日別全死因死亡率. . . . . . . .
- 2.4 抗ウイルス免疫エフェクター機構 .
- 2.6 MHC1結合タンパク質断片と細胞傷害性T細胞のT細胞受容体とのロック&キー相互作用 .
- 2.7 抗体産生の活性化 .
- 2.8 Tリンパ球のクローン選択 . . . . . . . . . . . .
- 2.10 COVID-19患者の血清中のSARS-CoV-2抗体 .
- 患者の血清中のSARS-CoV-2抗体 .2.12 遺伝子ベースのワクチンの作用機序 .
- 3.2 mRNAワクチンは免疫系のレーダーをかいくぐる
- 4.2 免疫組織化学の模式図 .
- 4.4 小血管および大血管の血管炎 .
- 4.6 mRNAワクチン接種後のIgA腎症 .
- 4.10 脳炎の病理組織像 .
- 4.11 mRNA ワクチン接種後の自己免疫様肝炎 .
- 5.1 mRNA脂質ナノ粒子の構造 .
- 5.2 ファイザーおよびModerna COVID-19ワクチンに含まれる合成脂質の分子構造 . . . . .
- 5.3 ワクチン脂質ナノ粒子はどのようにして「生体分子コロナ」を獲得するのか .
- 5.5 mRNAワクチン粒子の細胞内運命 . . . . .
- 5.6 DNA/脂質ナノ粒子とエンドソーム膜の融合 .
- 5.8 ファイザーのCOVID-19ワクチンに含まれる2種類の合成脂質の肝組織レベルの時間経過 .
- 5.9 有害事象発生率のバッチ間変動性
- 6.1 LINE-1レトロトランスポゾンはどのようにしてワクチンmRNAをDNAにコピーし、宿主細胞ゲノムに挿入するのか?
- 6.2 ファイザーワクチンがコードするスパイクタンパク質遺伝子のコピーがヒト肝細胞株の細胞DNA内に検出される
- 7.1 2020年12月から2021年8月までにVAERSに報告されたCOVID-19 mRNAワクチン接種後の心筋炎症例
- 8.1 急性伝染病のFarrの法則、米国人口におけるHIV感染の長期的傾向
- 8.2 HIV陽性者がダーバンを行進する、南アフリカ
- 8.3 南アフリカにおけるHIVと梅毒の有病率の負の相関関係
表の一覧
- 7.1 インフルエンザワクチンと比較したCOVID-19
- ワクチンとインフルエンザワクチンとの比較
序文
メアリー・S・ホランド、チルドレンズ・ヘルス・ディフェンス社長兼法律顧問(休職中
COVIDの閉鎖、恐怖の煽動、マスキング、検査、検閲、効果的な治療法の抑制、遺伝子ベースの実験的注射の強要、そして蔓延する傷害と死亡。恐怖の3年間が過ぎれば、このことを過去のことにして忘れたいと思うのが人間というものだ。しかし本書は、そうすることは私たち自身の危険と隣り合わせであることを明確に示している。人類に対するこの宣言されていない戦争は終わっておらず、我々は知識で武装しなければならない。
本書の目的は、COVID-19 mRNAワクチンの毒性が将来のmRNAワクチンにとって何を意味するかを説明することである。(1)脂質ナノ粒子の毒性、(2)ワクチン誘発スパイクタンパク質の毒性、(3)それらに対する免疫系の反応である。本書は、スパイクタンパク質に対する免疫系の反応が最も重要な毒性要因であると結論付けている。なぜなら、それは炎症と免疫系の損傷という剖検所見と一致し、理論的な害のメカニズムと一致するからである。
この本の結論は暗い: 「将来のすべてのmRNAワクチンは、標的とする特定の微生物に関連した、独自の特異的抗原を産生するように我々の細胞を誘導するだろう。したがって、そのようなワクチンは、COVID-19に対するワクチンと同じような規模の免疫学的損傷を引き起こすと予想しなければならない。インフルエンザ、RSV、HIV、マラリア、ガン、アレルギー、心臓病などに対して、無数のmRNAワクチンが開発中であるか、すでに市販されている。」
この本は警告している: 「何よりもまず、私たちは政府から狙われていることを受け入れなければならない。だから、彼らの裏切りや悪意に満ちた指導を鵜呑みにするのではなく、自分自身や愛する人のために気を配り、自分で調べ、科学や医学の既成の場であろうとなかろうと、どこででも正直な健康アドバイスを探し求めなければならない」。
あなたの手には、欠かすことのできない入門書がある。本書は包括的で、発表された科学文献を幅広く引用しており、本文156ページ、引用文献20ページと非常に読みやすく、ウイルス学、免疫学、毒物学の必読書となっている。引用文献、ウイルスと免疫機構の図解、COVID-19注射で死亡した人の染色組織写真も充実している。
COVID-19 mRNAワクチンの有害事象の疫学に関する章は、現在までの莫大な被害について示唆に富んでいる。COVIDワクチンは世界中で130億回接種されている。アメリカでは6億5000万回接種され、数百万件の有害事象が発生した。心筋炎、全身の血液凝固、神経学的、免疫学的、生殖学的障害などである。それにもかかわらず、CDCはワクチンを “安全 “と呼び、6ヶ月以上のすべての人に少なくとも年1回の接種を推奨するという大胆さを持っている。
デイビッド・ラスニックによる最終章は、エイズとHIVがいかにして「医学の倒錯の青写真」となったかを描いている。1980年代、トニー・ファウチ博士は「プレスリリースによる科学」を開始し、まったく証明されていないエイズについての物語を宣言し、強要した。ラズニックは、エイズの正統性は誤りであり、40年の歳月と数十億ドルの投資にもかかわらず、証明されたことは一度もない、と冷静に説明している。彼はこう書いている:
信じられないように聞こえるかもしれないが、エイズ、あるいはHIVが性行為によって感染するかどうかを決定するために計画され、実施された科学的研究は一つもない。. . .
第二次世界大戦以来、しかし特にここ数十年、アメリカでは事実上すべての主要な科学分野において、議論の封じ込めと異論者の迫害が定着している。いわゆる生物医学の分野では特にその傾向が強い。. . .
アイゼンハワー大統領が1961年に警告した政府、大企業、学会の結合が、いまや世界を支配している。. . . COVID-19の詐欺は、エイズ詐欺の典型である。. . .
われわれは世界的な全体主義的買収の真っ只中におり、この先数カ月で事態はさらに悪化するだろう。
この本の全体的な結論はラズニックと同じである:
当局の行動を “正直な間違い”と解釈することはできない。遺伝子ベースのCOVID-19ワクチンの背後にある邪悪な意図を明確に指し示すことが、あまりにも多く起こっている。必要性のない急ぎの承認、明白な脅迫と強制、正直な科学に対する組織的検閲、多数の死亡または重傷を負ったワクチン被害者に関する真実の抑圧は、すべて意図と目的について疑いを持つことを許すには、あまりにも長い間続いてきた。この戦争は何十年も続いており、今後も続き、エスカレートしていくことを予期しなければならない。
このような根拠のある情報は憂慮すべきものであり、憂鬱なものであるが、知識は力である。mRNAワクチンによる過去と未来の危害は意図的であり必然的であるという現実を理解すれば、私たちは自分自身と愛する人々を守ることができる。備えあれば憂いなしである。本書を読み、世界史におけるこの暗黒の章のページをめくるまで、参考資料として手元に置いておこう。
序文
本書の目的は、COVID-19 mRNAワクチンによる被害を検証し理解すること、そしてこの分析から、一般的な感染症に対するmRNAワクチンの使用に関する正しい教訓を引き出すことである。私たちは、メディアや科学的権威の多くにおける沈黙と検閲の陰謀にもかかわらず、COVID-19 mRNAワクチンによってもたらされた損害は、今や疑いの余地なく明らかであることを主張する。この評価は、統計的証拠とワクチン被害者の剖検・生検資料の病理学的所見によって裏付けられている。統計的側面については、Children’s Health Defenseの研究者であるマーゴット・デボアとブライアン・フッカーが第7章に寄稿している。病理学に関する第4章は、査読を経た文献に基づく部分もあるが、ドイツの上級病理学者であるアルネ・ブルクハルトの研究にも大きく依存している。彼は、多数のワクチン被害者の剖検資料について、まだ未発表の所見を我々に提供してくれた。残念なことに、アルネは2023年5月30日に予期せぬ死を遂げ、私たちから、そして現在進行中の仕事から引き離されてしまった。私たちは深い悲しみを覚えると同時に、彼の傑出した極めて重要な貢献に深く感謝している。
統計データと病理学的所見の両方を分析した結果、私たちは、これらのワクチンで経験したことは、特定の微生物抗原やそれがコードする抗原に関係なく、将来のmRNAワクチンでも同程度の危険と被害をもたらすと推測している。専門家でなくても理解できるように、免疫学の基本的な側面(第2章)と、mRNAワクチンと免疫系との相互作用(第3章)を紹介した上で、エビデンスの探求を始めた。
過去3年間の最も印象的な教訓のひとつは、医学、臨床医学、公衆衛生といったあらゆる側面における医学の腐敗と破壊の度合いである。このカテゴリーにおける最近の出来事については、ここでも議論する必要があっただろう。しかし、このテーマについては、すでに他の人々によって多くのことが語られている。そこで、第8章のAIDSとHIVに関するデイビッド・ラスニックの論文という形で、歴史的な視点を提供することにした。デイビッドは、私たちがCOVIDで見てきたような操作は、数十年前にすでに、欠陥のある科学と真っ赤な嘘を無防備な一般大衆に強要するために、そしてこの致命的と思われるウイルス感染症のキャリアと宣言された人々に有害な治療を強要するために使用されていたことを強く主張している。
戦争では真実が最初の犠牲者になるとよく言われる。COVIDの時代、私たちの多くは、欺瞞に満ちた科学と有害な “公衆衛生 “手段を使って行われている人々への戦争に目覚めている。デイビッドの章は、この戦争が長い間続いていることを明らかにしている。従って、我々はこの戦争が続くことを期待しなければならない。本書は、このような計画的な攻撃からあなた自身とあなたの大切な人たちを守るための一助となれば幸いである。
1. はじめに
COVID-19 mRNAワクチンは、感染症に対する予防接種を目的とした、mRNA技術の最初の応用であった。しかし、他の多くの感染性病原体に対するmRNAワクチンは、すでに実用化されている[1]。本書の目的は、そのような未来のワクチンがあなたの健康に及ぼすであろう影響を理解する手助けをすることである。入手可能な証拠は今のところCOVID-19ワクチンに限られているが、これらのワクチンで観察された傷害のパターンは、他の病原体に対する将来のmRNAでも再発すると予想される根本的な問題を示唆している。
1.1 mRNAワクチンは原理的に危険なのか、それとも観察された危害は偶発的なのか?
本書で示された事実から、COVID-19 mRNAワクチンが非常に重大な害をもたらしたことは明らかであろう。この被害は、これらのワクチンが意図したとおりに作用したためなのか、それともむしろ未申告の成分や汚染物質が原因なのか、疑問に思うかもしれない。この疑問を頭から否定することはできない。さらに、同じCOVID-19ワクチンのバッチ間で有害事象の発生率に異常に大きなばらつきがあり、これは少なくともこれらのワクチンが一貫した基準で製造されていないことを示している(セクション5.4参照)。これらの各要因は毒性に影響を及ぼす可能性がある。しかしながら、観察された重篤な危害のほとんどは、これらのワクチンが設計されたとおりのことを行っているという点で最もよく理解できる。
1.2 COVID-19ワクチンは決してあなたの健康のためではなかった
COVID-19の「パンデミック」に関する公式のストーリーは、非科学的なナンセンスと全くの嘘からなる驚くべき作り話である[2]。これは、SARS-CoV-2ウイルスの自然起源とされる話から始まっているが、中国のウイルス学者リ-メン・ヤンらがウイルスゲノムの詳細な分析を発表し、実験室での操作の痕跡が明らかになった時点で、通用しなくなった[3, 4]。このキメラ・ウイルスの作成に誰が関与したのか、あるいは関与していないのか、まだはっきりとはわかっていないが、この問題はそれほど重要ではない。WHOと世界のほとんどの国の政府によって迅速かつ足並みを揃えて課された、不合理で予想通り有害な「対応措置」は、ウイルスとこれらの措置が同じ意図の一部であることを明確かつ早期に明らかにした。すでに2020年初頭、クラウス・シュワブとティエリー・マレレは、その著書『COVID-19:グレート・リセット』[5]の中で明言している:
コロナウイルスのパンデミックによって引き起こされた世界的な危機は、……途方もない規模の経済的混乱をもたらしつつある。本稿執筆時点(2020年6月)で、パンデミックは世界的に悪化し続けている。私たちの多くは、事態がいつ正常に戻るかについて頭を悩ませている。簡潔に答えれば、「決して戻らない」である。
2020年6月の時点で「パンデミックは悪化の一途をたどっている」という著者の明らかな虚偽の主張は、例えば図1.1を参照されたい: 世界経済フォーラムのクラウス・シュワブとその取り巻きは、COVID-19を棍棒として、彼らの計画した「途方もない規模の経済混乱」を世界にもたらし、彼らのディストピア的な「新常態」を到来させようとしているのだ。中小企業、学校、礼拝所の閉鎖といった初期の措置は、私たちの生活と生活の質に重大な損害をもたらした。
しかし、遺伝子ベースのCOVID-19ワクチンの導入により、さらに悪いことが起こることになった。現在では、これらの製品による重大な傷害と死亡の圧倒的な証拠がある(第4章と第7章参照)が、この証拠はまだゆっくりとしか一般的な認識には浸透していない。これらのリスクは、単に容認されただけでなく、意図されたものであったということができる。開発と承認の全過程は、危険性を隠蔽し、これらの有害なワクチンの上市を急がせるように設計されていたようである。
1.3 緊急使用認可の悪用と規制上のセーフガードの崩壊
最初の緊急使用承認(EUA)は、2020年12月にFDAによって承認され、ファイザーのワクチンに関するものであった。他のワクチンの承認や、他の管轄地域の規制当局による承認もすぐに続いた。
しかし、これらの性急な承認は本当に正当化されたのだろうか?答えはノーである:
- 1. 承認される前から、私たちは本当の緊急事態が存在しないことを知っていた。2020年半ばから後半にかけて、COVID-19の感染致死率はすべての年齢層で0.15%から0.2%程度であり、合併症を持つ高齢者に非常に強い偏りがあることを示す疫学研究がいくつか発表されていた[7-9]。この感染致死率は、一般的なワクチン接種が不要とされる、毎年繰り返されるインフルエンザの流行で一般的に観察される範囲を超えていない。
- 2. COVID-19は治療可能である。このような治療に関するガイドラインは、経験豊富な医師たちによって共同開発され、すでに2020年に発表されている[10]。治療の選択肢は、ウイルスの複製を阻害することに重点を置く初期段階と、抗炎症治療が最も重要な後期段階の両方に用意されている[11]。ヒドロキシクロロキンとイベルメクチンの2つの薬剤は、初期段階でうまく使用されている。
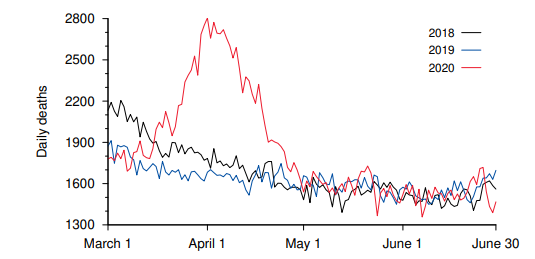
図1.1 フランス(海外領土を含む)における2018年、2019年、2020年の3月から6月までの日別全死因死亡率。
図はRancourtらの研究[6]から引用したもので、3月と4月にピークがあったのは、WHOがCOVID-19を “パンデミック “と宣言した直後に政府が隔離措置をとったためであるとしている。
イベルメクチンはオンコセルカ症(河川盲目症)などの熱帯寄生虫病の治療にも広く使われており、そのためWHOの必須医薬品リストにも入っている。しかし、COVID-19に関しては、WHOはこのよく知られた安全な薬剤を臨床試験以外で使用しないよう警告した[12]。このような方針は合理的に正当化されるはずもなく、国や地域の保健当局によって適切に無効化され、世界中の個々の医師によって無視されてきた。ヒドロキシクロロキンについても、状況は類似している。
COVID-19に対するワクチンの緊急使用の根拠は、ウイルス性疾患の重症度が限定的であること、効果的な治療法が利用可能であることであった。しかし、このようなEUAを検討する正当な根拠がなかっただけでなく、製造業者から提供された不完全で明らかに不正な文書に基づいて発行されたのである。このような不正は規制当局によって摘発されるべきだったが、どうやら摘発されなかったようである。
メーカー、規制当局、保健当局の冷笑的で無謀な行為は、その後も続いている。簡略化された場当たり的な臨床試験から除外された妊婦や授乳中の母親は、それにもかかわらず、EUAが投与された直後にワクチンを接種するよう勧められ、その結果、妊孕性や乳児の健康に許容できないリスクが生じることになった(7.7節参照)。このリスクは、ワクチン接種後間もなく授乳中の母親の母乳からワクチンmRNAが検出されたことからも明らかである[13]。さらに、VAERSやその他の主要なデータベースで重篤な有害事象の報告が急増しているにもかかわらず、EUAはその後ますます低年齢層に拡大され、現在では乳幼児にまで適用されている。
第三者による調査(5.4節参照)によって、多くの製造バッチで検出された様々な汚染は、ワクチンの品質と製造基準を誰も守っていないという考えを補強している。したがって、FDAをはじめとする国内外の規制当局が、もはや従来の倫理的・専門的基準を遵守していないことは明らかである。
1.4 本書が書かれた理由
COVID-19ワクチンによるリスクと顕在化した被害を一般大衆に知らせることが必要かつ緊急であることに変わりはないが、本書を執筆した主な理由は別のところにある。この原稿を書いている時点で、サイトメガロウイルス、エプスタイン・バーウイルス、呼吸器合胞体ウイルス、その他いくつかの病原体に対するワクチンの臨床試験がすでに進行中である[14]。本書の目的は、これらの将来のmRNAワクチンが、COVID-19に対するワクチンと同じような重大な危害を引き起こし、同じような方法でそうなることを予期しなければならないことを示すことである。私たちは、この害がmRNA技術に組み込まれていること、そして、薬に見せかけた未来の毒物から子どもたちやあなた自身を守るために、できる限りのことをしなければならないことを理解してもらいたいのである。
2. ウイルス学と免疫学のいくつかの要素
本書の中心的なテーゼは、COVID-19 mRNAワクチンで見られた危険性と顕在化した危害は、免疫学の第一原理から予測可能であったということであり、さらに他のウイルスや非ウイルス病原体に対する将来のmRNAワクチンでも同様の危害が予想されるということである。このケースを説明するために、まずウイルスがどのように増殖するのか、そして免疫システムがどのようにウイルス感染と戦い、最終的に克服するのかを簡単に説明する。この章での議論は包括的なものではなく、本書の論旨を評価する上で重要かつ不可欠な要素のみを簡略化して紹介する。より詳細な解説については、適切な標準的著作 [15, 16] を参照されたい。
2.1 ウイルスのライフサイクル
ウイルス粒子は細胞ではない。ウイルス粒子は核酸ゲノム(RNAまたはDNA)から構成されているだけであり、そのゲノムはタンパク質と、場合によっては脂質(脂肪のような分子)から構成される殻に包まれている。ウイルスにはエネルギー代謝やタンパク質合成のための細胞機構がないため、増殖には他の生物の細胞を利用しなければならない。そのためには、ウイルス粒子(ビリオン)が宿主生物の細胞に入り込み、その細胞に子孫のビリオンを作らせなければならない。これには少なくとも次のようなステップが必要である(図2.1):
- 1. ビリオンは宿主細胞表面のタンパク質レセプターに結合する。これがビリオンの細胞内への取り込みの引き金となる。
- 2. ビリオンはコーティングを解除する。これによりウイルス核酸ゲノムは放出され、ウイルスタンパク質の新しいコピーの合成を指示できるようになる。
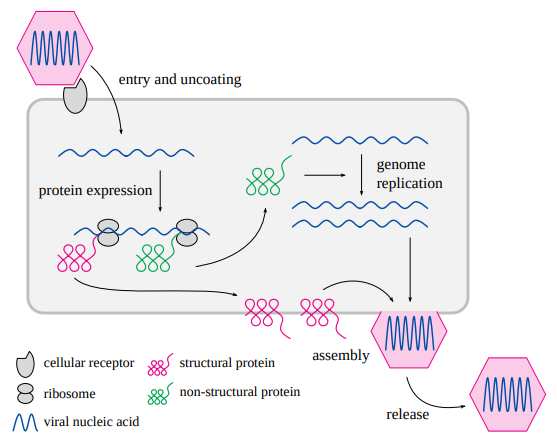
図2.1 ウイルス増殖とタンパク質発現の概要(簡略化)
ウイルス粒子は、ウイルス・タンパク質(マゼンタ)で囲まれた核酸ゲノム(DNAまたはRNA、青)から構成されている。これらは核酸を保護すると同時に、宿主細胞のレセプターへの結合を仲介し、宿主細胞への侵入を容易にする。細胞内に入ると、核酸は被覆を解かれ、ウイルスタンパク質の新しいコピーの合成を指示する。非構造ウイルスタンパク質はこの細胞内段階でのみ存在し、ウイルス核酸の複製などの機能を果たす。これらの新しいゲノムのコピーは、構造タンパク質とともに新しいビリオンに集合し、細胞から放出されて他の細胞に感染する。
- 3. すべてのウイルスタンパク質が娘ビリオンに組み込まれるわけではない。ビリオンに含まれないタンパク質は非構造タンパク質と呼ばれ、感染細胞内にのみ存在し、ウイルスゲノムのコピーを作るなど、ウイルス増殖において様々な役割を果たす。ウイルス粒子に組み込まれるタンパク質は構造タンパク質と呼ばれる。
- 4. ウイルスの新しいコピーは、細胞表面、または時には細胞内コンパートメント内で集合し、その後細胞から放出される。これらの子孫ウイルスは、他の体細胞に感染することができる。
2.1.1 細胞とウイルスのゲノム構造とタンパク質発現
図2.1は、ウイルス粒子に含まれる核酸の性質について意図的に曖昧にしたものである
ウイルス核酸はDNAであったりRNAであったり、また一本鎖であったり二本鎖であったりする。この多様性の意味するところは非常に興味深いが、ここでは長く論じない。代わりに、RNAウイルスはDNAウイルスよりも突然変異率が高い傾向があり、一本鎖ゲノムを持つウイルスは二本鎖ゲノムを持つウイルスよりも突然変異率が高いということだけを述べておこう。したがって、コロナウイルスやポリオウイルスなどの一本鎖RNAウイルスは、突然変異率が最も高い傾向にある。このことはワクチン開発を困難にする。というのも、循環しているウイルスは、変異によって免疫の対象となる分子的特徴を変えたり失ったりすることで、ワクチン誘導免疫を回避する可能性があるからである1。
図2.2は細胞自身の遺伝子とコロナウイルスの遺伝子の機能様式を対比したものである
細胞遺伝子の発現は、ゲノムDNAからメッセンジャーRNA(mRNA)への転写、そしてタンパク質への翻訳という規則的なパターンに従っている。対照的に、コロナウイルスは一本鎖のRNAゲノムを持ち、タンパク質の発現と自身の複製の両方の鋳型となる。複製には二本鎖RNA(dsRNA)中間体が関与するが、これは宿主細胞内にのみ存在し、ウイルス粒子にパッケージされることはない。これらのステップを実行するRNA依存性RNAポリメラーゼは、コロナウイルスゲノム内の非構造遺伝子の一つによってコードされている。
図が示唆するように、dsRNA分子は細胞の遺伝子発現には関与しない。従って、dsRNAが細胞内に存在することは、ウイルス感染と進行中のウイルス複製を意味する。驚くべきことに、我々の体細胞はdsRNAの存在を検出するレセプターを持ち、問題のウイルスに対して非特異的免疫反応と適応的免疫反応を起こす(セクション2.2.2.1参照)。
1ウイルスがこのような免疫学的逃避を起こしやすいかどうかは、その変異率だけでなく、ヒト宿主への適応度にもよる。例えば、インフルエンザウイルスも麻疹ウイルスも一本鎖RNAウイルスであり、突然変異率が高いが、この2つのうちインフルエンザウイルスだけが突然変異による急速な「抗原ドリフト」を起こしやすい。しかし、SARS-CoV-2はインフルエンザのパラダイムに従っているようである。実験室で最近製造されたため、ヒト宿主への徹底的な進化的適応ができなかったことから予想されたことである。(インフルエンザウイルスには、”抗原シフト “として知られる遺伝的変異の別の原因がある。これは原理的には非常に重要であるが、本書の趣旨からは外れる)。
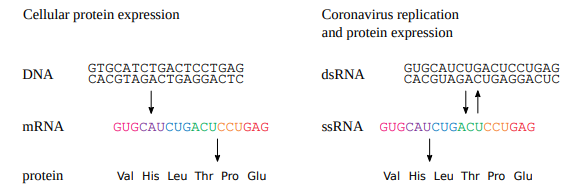
図2.2 細胞mRNAと比較したコロナウイルスRNAゲノムの機能
左:細胞の遺伝子はDNAからmRNAへの転写によって発現し、その後タンパク質に翻訳される。右:コロナウイルス粒子に含まれる一本鎖RNAもタンパク質合成を促進するが、同時に二本鎖RNAの中間体を含む自身の複製の鋳型としても機能する。
2.1.2 ウイルス増殖における細胞レセプタータンパク質の役割
ウイルスの侵入と増殖の第一段階は、細胞レセプター・タンパク質へのビリオンの結合である。もちろん、これらの細胞性タンパク質はウイルスの侵入を促進するために存在しているわけではない。その代わりに、細胞や生物の生理学において様々な役割を果たしている。例えば、SARS-CoV-2の侵入を促進する細胞性タンパク質であるアンジオテンシン変換酵素2(ACE2)は、アンジオテンシンIIを分解する役割を果たしている。これは血圧を上昇させるペプチド(小タンパク質)メディエーターである。ウイルスがレセプターに結合することで、そのレセプターの生理学的機能が阻害され、感染の臨床症状の一部が引き起こされる可能性がある。
ウイルスが細胞に感染するためには、特定の細胞表面分子を必要とするため、ほとんどのウイルスの宿主細胞の範囲が制限される。このように宿主細胞の範囲が限定されているため、ウイルス感染の重症度が緩和される傾向にある。
2.1.3 いくつかのウイルスは膜で包まれている
図2.1では、ウイルス粒子を核酸とタンパク質の殻(カプシド)のみからなるものとして描いた。多くのウイルス(ポリオウイルスやアデノウイルスなど)は確かにこの2つの要素だけで構成されているが、他のウイルスはさらにエンベロープに囲まれている。エンベロープの組成は細胞膜に似ており、脂質と埋め込まれた膜タンパク質で構成されている。この場合、細胞レセプターに結合するのはこれらの膜タンパク質である。これらはしばしばスパイクまたはスパイクタンパク質と呼ばれる。
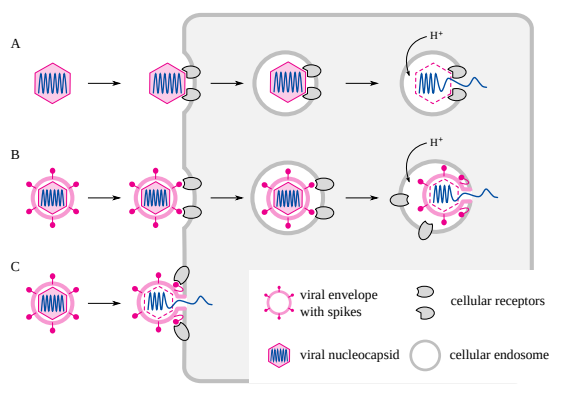
図2.3 非エンベロープ型ウイルスとエンベロープ型ウイルスの細胞内侵入と被覆解除。
A: 多くの非エンベロープウイルス(アデノウイルスなど)はエンドサイトーシスによって取り込まれる。エンドソームの酸性化(すなわち、エンドソーム内にH+イオンが蓄積すること)は、ウイルスゲノムのアンコーティングと細胞質への移行を引き起こす。B: 多くのエンベロープウイルス(例:インフルエンザウイルス)もエンドソーム経路をたどる。ゲノムの細胞質への移行は、ウイルスエンベロープがエンドソーム膜と融合するときに起こる。この段階はウイルスのスパイクタンパク質の分子形状の変化によって引き起こされるが、通常は酸性化によっても引き起こされる。C: エンベロープウイルスの中には、細胞表面で直接融合するものもある。BとCの両方の経路がコロナウイルスで起こることが示唆されている[15]。
細胞表面のレセプターに結合することに加えて、スパイクはウイルスエンベロープの細胞膜への融合を仲介する。この融合は、ウイルス核酸がウイルス粒子からサイトゾル(細胞の主要区画)へ移行するのに不可欠なステップである。ごく一般的に、このステップはエンドソーム、すなわちエンドサイトーシス後にウイルス粒子を含む膜コンパートメントの酸性化によって推進される(図2.3の経路Bを参照)。
コロナウイルスはエンベロープしている。COVID-19の原因ウイルスであるSARS-CoV-2の話題のスパイク・タンパク質は、このウイルスの受容体結合と膜融合の両方を仲介している。膜融合を起こすためには、スパイク・タンパク質は分子形状(「コンフォメーション」)を変えなければならない。
クロロキンやヒドロキシクロロキンはエンドソームの酸性化を阻害することが知られている。したがって、ヒドロキシクロロキンがCOVID-19に対して臨床的に有効であることは驚くべきことではない[17]。
2.2 ウイルスに対する免疫
われわれの免疫系は多くの武器を持っており、その多くは細菌、ウイルス、その他の特定のタイプの病原体に特化したものである。ここでは、ウイルス感染に関連する防御機構に焦点を当てる。COVID-19に対するような抗ウイルスワクチンだけでなく、結核やマラリア、その他の非ウイルス感染症に対する防御を目的とした将来のmRNAワクチンも同様である。
我々は2つの中心的な問題を提起することによって、抗ウイルス免疫の探求を開始する:
- 1. 進行中のウイルス感染をチェックし排除するために、免疫系が展開するエフェクター機構とは何か?
- 2. 免疫系は経験から学習し、多くの場合、同じウイルスに一度だけ罹患すると、その後は一生そのウイルスに対する免疫を維持する。この学習はどのように行われるのか?
2.2.1 抗ウイルス免疫エフェクター機構。私たちの免疫システムは、2つの重要な戦略を使ってウイルス感染と闘っている:
- 1. ウイルス粒子が私たちの体細胞に感染する前に阻止する。
- 2.すでに感染し、子孫ビリオンを生産している体細胞を破壊する。
これらの戦略はいずれも、問題のウイルスの抗原(タンパク質)を特異的に認識し、結合する分子と細胞が関与している(図2.4)。感染細胞の殺傷は、主にTキラー細胞としても知られる細胞傷害性Tリンパ球によってもたらされる。図2.4はこれらがどのように活性化されるかを示している。感染細胞はウイルスゲノムの指示に従ってウイルスタンパク質を発現するが、その過程でタンパク質分子のいくつかを小さな断片に切り刻む。そして、これらのタンパク質断片(ペプチド)を、特定のキャリアタンパク質(MHC1)と結合させて細胞表面に露出させる。タンパク質が合成されるときはいつでも、この作業を行う。この一般的なメカニズムは、免疫監視を可能にするために極めて重要である。免疫系は細胞表面のペプチド断片を検査し、その細胞が健康な状態にあるのか、それともウイルスに乗っ取られてウイルスタンパク質を生産しているのかを判断することができる。この監視は細胞傷害性Tリンパ球によって行われる。これらの細胞はT細胞レセプターと呼ばれる特異的な表面タンパク質を持ち、MHC1分子によって提示された個々のウイルス由来ペプチドを特異的に認識する。
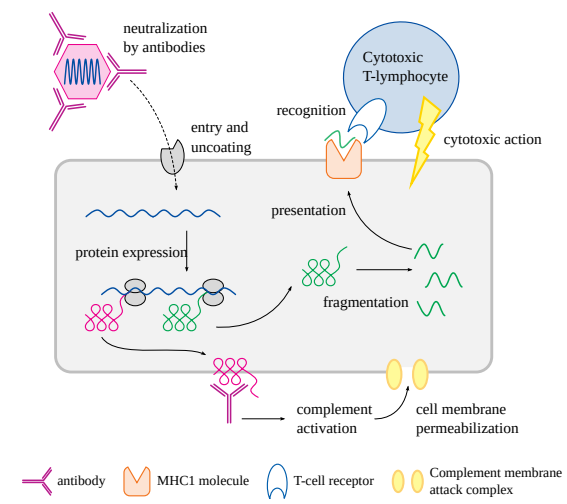
図2.4 抗ウイルス免疫エフェクター機構
この漫画は、私たちの免疫系がウイルス感染と闘い、根絶する3つのメカニズムを示している。抗体はウイルス粒子と結合し、中和することができる。また、細胞表面に現れたウイルスタンパク質に結合し、補体を活性化することもできる。補体は細胞外タンパク質のカスケードで、ウイルスに感染した細胞に膜貫通孔を形成させる。細胞内に残ったウイルスタンパク質は断片化され、特殊なキャリアタンパク質(MHC1)と結合して細胞表面に露出する。MHC1に結合した断片をTキラーリンパ球が認識すると、Tキラーリンパ球が活性化し、ウイルス感染細胞にいくつかの細胞傷害性タンパク質を放出する。
さまざまなT細胞レセプターを持つT細胞のレパートリーは非常に多く、その中でウイルス由来のペプチドに結合するのは1つまたは数個、あるいは全く結合しない場合もあることを理解することが重要である。T細胞レセプターがそのようなペプチドと結合する細胞傷害性T細胞は、そのペプチドを提示した細胞を攻撃するように誘導される。この認識イベントはまた、細胞傷害性T細胞の分裂と増殖を刺激する(これについては後述する)。
ウイルス粒子との結合と遮断-中和-は、形質細胞によって合成・分泌される細胞外タンパク質である抗体によって媒介される。これらの細胞はBリンパ球の子孫であり、Bリンパ球もまた、同族ウイルス抗原に遭遇することにより、増殖と成熟を誘導される(図2.7参照)。T細胞の場合と同様に、B細胞にはさまざまな表面レセプターを持つ非常に多くの細胞が存在し、そのうちのごく一部の細胞だけが特定の抗原を認識し、活性化を受ける。
抗体は様々な方法でウイルス感染細胞の殺傷に貢献する。図2.4はそのようなメカニズムの一つを示したものである。これは、血漿タンパク質からなる補体系が関与している。補体系はプロテアーゼ(タンパク質切断酵素)の自己増幅カスケードである。微生物細胞の表面や、ウイルス感染の場合は私たち自身の体細胞上に存在する抗原を認識し、結合した抗体によって活性化される。補体の活性化は膜攻撃複合体の生成で頂点に達する。膜攻撃複合体は複数のタンパク質分子からなるリング状の大きな構造で、細胞膜に穴を開ける。
図2.5は、補体系の作用様式に関する代表的な論文[18]から引用したもので、補体系が細胞を完全に破壊できることを示している。ご覧のように、抗体と補体にさらされた細胞は穴だらけになっている。穴は細胞膜のバリア機能を破壊し、細胞は死滅する。
細胞膜の透過化もまた、細胞傷害性T細胞が展開するエフェクター・メカニズムの一つである。問題の孔形成タンパク質であるパーフォリンは、補体孔の主成分(C9)と構造的に似ている。この効果は、T細胞からの破壊的酵素の放出によって増強され、その酵素はパーフォリン孔を通って感染標的細胞に侵入することができる。さらに、細胞傷害性T細胞は標的細胞をアポトーシス-生得的な細胞自殺プログラム-に誘導するメディエーターを放出する。
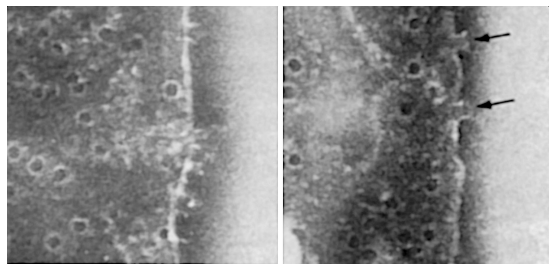
図2.5 赤血球上に孔を形成する補体膜攻撃複合体
補体タンパク質を供給するヒト血清の存在下で、ヒツジ赤血球に対する抗体をこのような細胞に結合させた[19]。ほとんどの膜攻撃複合体は上から見ている。矢印は、細胞の端に位置する個々の複合体を強調している。それらは横向きに描かれており、細胞表面から突出しているのがわかる。
抗体とT細胞レセプターは構造的に類似しており、前述のようにどちらも特異的に抗原を認識することができる。しかし、両者には以下のような違いがあることに注意すべきである:
- 1.抗体は無傷の抗原分子を認識するが、T細胞レセプターは断片としてのみ認識する;
- 2.抗体は結合のために抗原そのもののみを必要とするが、T細胞レセプターはMHC分子によって提示された場合にのみ、その同族ペプチド(タンパク質断片)を認識する。
抗体はそれ自身が細胞外タンパク質であるため、細胞表面か細胞外腔に抗原が存在する場合にのみ抗原と出会う。このような抗原では、抗体は非常に有効である。一方、図2.4に示した断片化とMHC1依存性の提示機構により、細胞傷害性T細胞は細胞内抗原に効果的に反応することができる。このように、抗体と細胞傷害性T細胞は明らかに相補的な機能をもっている。
2.2.2 抗ウイルス免疫応答の活性化
細胞傷害性T細胞もB細胞も、その同族抗原との接触によって活性化され、増殖が誘導されること、そして問題のT細胞やB細胞は、異なる抗原特異性を持つ細胞の大規模な既存のプールから引き出されることを前述した。T細胞やB細胞の活性化には、確かに特異的抗原の認識が必要であるが、それが全てではない。全ての特異的免疫応答は、免疫系の生得的な非特異的要素の活性化から始まるのである。
2.2.2.1 特異的免疫応答は、非特異的免疫系によって開始される
汚染された傷口が炎症を起こし、赤く腫れ上がり、痛みを伴うことがあるのは、経験的にご存知だろう。この迅速な反応は、まだ特異的な免疫反応によるものではない。その代わりに、感染微生物(このシナリオではほとんどが細菌である)が、最初に私たちの非特異的免疫系または自然免疫系を活性化させる。これは2つの方法で起こる:
- 1.微生物細胞そのものが引き金となる;
- 2.バクテリアの毒性または侵入性が、私たちの体細胞の一部を死滅させる。腐敗した体細胞から放出される分子の一部は、炎症を促進する。
補体系は、抗体の助けがなくても、細菌の細胞表面によって活性化される。補体の活性化は細菌細胞を透過させるだけでなく、マクロファージや好中球顆粒球による破壊の目印となる。これら2種類の細胞は貪食に特化しており、つまり専門的に微生物を食べて殺す。第三の貪食細胞は樹状細胞である。樹状細胞はマクロファージと関連しているが、後者とは対照的に、主に “戦士 “としてではなく、”メッセンジャー “として機能する。樹状細胞は、摂取・分解した病原体に対する抗体反応を引き起こすのに重要な役割を果たす(セクション2.2.2.3参照)。
死滅した細菌細胞から放出された分子(主に細胞壁成分だが、細菌のDNAなども含む)は、私たち自身の体細胞内にある様々なパターン認識受容体(PRR)によって認識される。これらのPRRは大規模かつ構造的に多様なタンパク質群であり、よく知られているサブクラスはToll様受容体(TLR)である。これらの様々なPRRが活性化されると、サイトカインやケモカインと総称される様々な炎症性メディエーターが放出される。これらのメディエーターの重要な作用には、以下のようなものがある。
- 1. 血管透過性の亢進。これにより、抗体や補体を含む血漿タンパク質が感染組織に流入する;
- 2. 貪食細胞や他の免疫細胞を感染巣に引き寄せ、活性化する。
- 3. 感染部位で遭遇した微生物抗原に対する特異的T細胞およびB細胞応答の活性化。
ウイルス感染症はそれぞれに適したPRRを活性化する。2本鎖DNAはもちろんヒト細胞にも存在するが、通常は細胞質には存在しない。二本鎖DNAはもちろんヒト細胞にも存在するが、通常は細胞質には存在しない。したがって、細胞質に存在する二本鎖DNAはDNAウイルス感染のシグナルとなる。
さらに他のタイプのPRRは、通常は健康な体細胞内にしか存在しないが、死滅した細胞から放出される可能性のある分子に反応する。微生物感染においては、このような「隠れた自己」シグナルは免疫反応を増幅させるのに有用である。自己免疫が自らの体細胞を破壊できる閾値を超えると、破壊された細胞から放出される隠れ自己シグナルが、自己免疫の攻撃性をさらに煽り、持続させる。
2.2.2.2 細胞傷害性T細胞の活性化
感染に対する非特異的な反応が一段落すると、今度は特異的な免疫反応が始まる。ここでは、細胞傷害性T細胞から始めて、適切な抗原特異的T細胞とB細胞クローンがどのように選択的に活性化されるかを考えてみたい。
2PRRの中には、エンドソーム内の一本鎖RNAを検出するものがあり、そこから感染ウイルスが侵入することが多い(図2.3参照)。mRNAワクチンもエンドソーム経由で取り込まれるため、これらのレセプターを活性化する可能性がある。この作用は、RNAのメチル-シュードウリジン修飾 [20]によって抑制することができ、ModernaワクチンとファイザーCOVID-19ワクチンで使用されている(セクション2.8.3.2参照)。
私たちは、細胞がタンパク質を産生するときはいつも、そのタンパク質分子のサンプルが小さな断片に切り刻まれ、細胞表面に運ばれ、そこで細胞傷害性T細胞と相互作用し、認識されやすくなることを見てきた。細胞傷害性T細胞と提示されたタンパク質断片の相互作用を、錠前と鍵のようなものと考えてみよう(図2.6)。細胞傷害性T細胞の貯蔵庫には無数の異なる鍵(T細胞レセプター)があり、事実上無限の鍵(断片)に適合することができる。しかし、どのウイルスのタンパク質も、限られた数のキーしか生み出さない。キーは、利用可能なすべての細胞傷害性T細胞のうち、対応する限られたサブセットにしか結合せず、活性化しない。
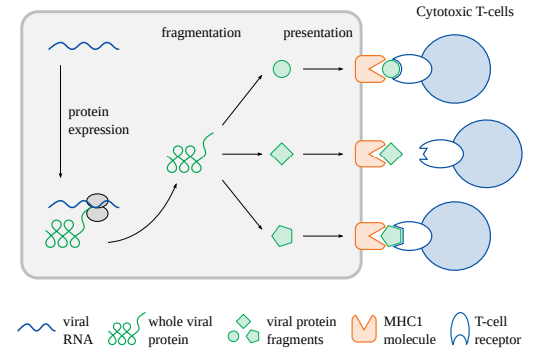
図2.6 MHC1に結合したタンパク質断片と細胞傷害性T細胞のT細胞レセプターの鍵と錠の相互作用
私たちの体内のTリンパ球上のT細胞レセプターは、総体として非常に広い抗原特異性のスペクトルをカバーしているが、個々のT細胞上のレセプター分子はすべて同一であり、同じ抗原に結合する。細胞表面のMHC1分子が提示するタンパク質断片のひとつと結合するT細胞だけが、結合して活性化することができる。
活性化されたT細胞の数は、利用可能な抗原特異性のリザーバー全体から見ればわずかであるが、それでも絶対数から見れば相当なものである。新しいウイルス変異体は、1つか数個の新しいタンパク質断片を作り出すかもしれないが、その他の断片の大部分は変化せず、したがって我々のTリンパ球によって認識され続ける。同様に、あるウイルスファミリーの異なるメンバー間には、ある程度の細胞傷害性T細胞ベースの交差反応性と交差防御が存在するのが普通である(セクション2.5も参照)。従って、SARS-CoV-2の変異の出現に対抗しなければならない、また、すべての「懸念される変異型」を特注ワクチンの開発によって追い詰めなければならないというシナリオは、最初から馬鹿げていたのである。
2.2.2.3 抗体産生の活性化 先に述べたように、抗体は形質細胞から分泌される細胞外タンパク質であり、形質細胞はBリンパ球、略してB細胞に由来する
T細胞と同様、B細胞は抗原特異性が多様な表面レセプターを持っているが、一つのB細胞のレセプターはすべて同じである。しかし、T細胞レセプターとは異なり、B細胞レセプターは実際には抗体である。B細胞が適切な抗原に出会い、その受容体である抗体を介して抗原と結合すると、このB細胞は活性化される:分裂を開始し、娘細胞は最終的に形質細胞に変化し、可溶性抗体を産生し始める。私たちの体内の血漿細胞によって産生される抗体の量は、感染症がないときでもかなり多い。私たちの血漿には1リットルあたり10~12グラムの抗体が含まれており、その半分は約3週間ごとに入れ替わる。
B細胞の中には抗原との結合だけで活性化するものもあるが、ほとんどのB細胞はT-ヘルパーリンパ球によるさらなる刺激を必要とする。全過程の概略を図2.7に示す。まず、樹状細胞やマクロファージなどの抗原提示細胞(APC)が抗原を取り込む。APCの内部で抗原は断片化され、細胞表面に提示される。このプロセスは、他の体細胞における細胞内抗原の提示と似ている(図2.4参照)が、抗原提示細胞は異なるタイプのMHC分子を用いていることに注意されたい。細胞内抗原の細胞傷害性T細胞への提示にはMHCクラスI分子(MHC1)が関与しているが、特殊な抗原提示細胞による本来の細胞外抗原の提示にはクラスII分子(MHC2)が関与している。これらのMHC2分子は、細胞傷害性T細胞よりもむしろTヘルパー細胞と選択的に相互作用する。
抗原を捕捉したB細胞は、APCと同じように抗原を処理してTヘルパー細胞をリクルートする。したがって、B細胞はAPCと同じようにMHC2と抗原由来のペプチドとの複合体を作り、同じT細胞レセプターと相互作用することができる。T-ヘルパーが抗原ペプチドを提示するB細胞と結合すると、そのB細胞の活性化が完了する。
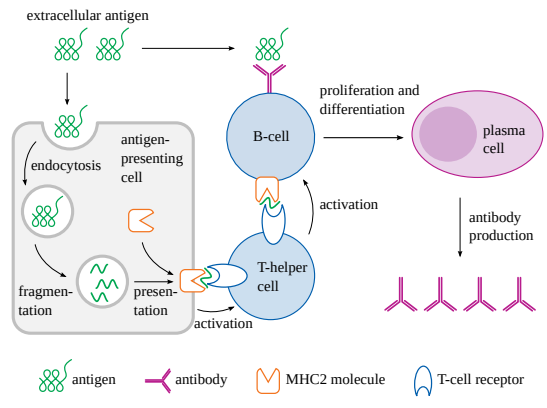
図2.7 抗体産生の活性化
細胞外抗原はB細胞表面の抗体と結合し、抗原提示細胞(APC;通常は樹状細胞)とも結合する。APC内で抗原は断片化され、MHCクラス2分子と結合して細胞表面に提示される。この複合体はTヘルパー細胞によって認識され、活性化される。T細胞は次にB細胞を活性化し、B細胞はAPCと同じ抗原プロセッシングと提示のステップを行う。無傷の抗原とTヘルパー細胞による二重の活性化に応答して、B細胞は分裂を開始する。その子孫は形質細胞に変化し、元のB細胞と同じ抗原特異性を持つ抗体を合成・分泌する。
要するに、B細胞の活性化には、抗原提示細胞とTヘルパー細胞の両方からの「許可」が必要なのである。このやや複雑な取り決めが、特に自己抗原に対する早すぎる過剰な抗体反応を防ぐ役割を果たしている。このやや複雑な仕組みが、特に自己抗原に対する早すぎる過剰な抗体反応を防いでいるのである。しかし、このような安全装置が機能しないこともあり、その結果、自己免疫疾患を引き起こすこともある。
図2.4をもう一度振り返ってみると、細胞表面には存在するが、細胞外には存在しないウイルスタンパク質に抗体が結合していることがわかる。このような細胞表面タンパク質は、どのようにして抗原提示のMHC2経路に入るのだろうか?例えば、細胞傷害性T細胞がウイルス感染細胞を殺した後などである。その後、その細胞の残骸はマクロファージや他の抗原提示細胞によって分散・除去される。残骸の一部は、B細胞を活性化するために、B細胞の表面レセプターに結合しなければならない。
2.2.2.4 抗体クラススイッチ
新しく形成された形質細胞が、最初は免疫グロブリンM(IgM)と呼ばれる特定の抗体クラスを産生することは注目に値する。IgM産生の一過性という性質は、診断上有用である。ある抗原に対する抗体反応のほとんどがIgMである場合、それは最近始まった一次反応に違いない。一方、ほとんどがIgMでない場合、それはしばらくの間続いており、免疫系が以前にすでに遭遇した抗原に対する二次反応または「記憶」反応である可能性が高い(セクション2.4参照)。
従って、IgGまたはIgAは、最初に形成されたIgMと同じ抗原と結合し続ける3。
2.3 非常に多様なT細胞とB細胞のリザーバーはどのようにして生まれるのか?
上述したように、T細胞とそのレセプターのリザーバーを無数の「鍵」に例えたが、これらの鍵はどんな抗原の「鍵」にも適合する。そしてBリンパ球も同様である。現在では、本当に驚くほど多様な鍵が、胎児の発育中にすでに生じていることが知られている。これはどのようにして起こるのだろうか?発育中に現れるタンパク質断片(キー)に反応して、ロックが形成されるのだろうか?しかしそれでは、T細胞は「自己」のタンパク質断片を認識するレセプターだけを備えていることになる。というのも、子宮内の胎児は通常、感染症から守られているため、発育中のT細胞を訓練するために、いかなる感染因子に由来するペプチドも利用できないからである。これでは有用な目的を果たせるはずがない。一方、もし多様なロックが自然発生的に、ランダムに、指示するキーやテンプレートを必要とせずに生じるとしたら、「非自己」抗原、すなわちウイルスタンパク質を含む外来病原体由来の抗原を認識するリンパ球が何十億個も生成されるかもしれない。
3成熟したB細胞の抗原特異性は原理的には変わらないが、抗体の抗原に対する結合親和性は時間とともに増加する。この “親和性成熟 “は、遺伝子の点突然変異によって引き起こされる。
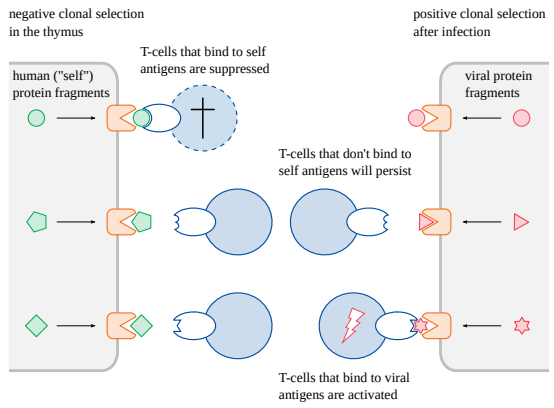
図2.8 Tリンパ球のクローン選択
T細胞レセプターの多様性は、最初はランダムに生成される。つまり、多くのT細胞が自己抗原に結合するレセプターを持つことになる。胸腺では、そのようなT細胞はその抗原を発現する細胞によって “餌付け “され、破壊されるか抑制される。自己抗原に結合しないT細胞は持続し、後日ウイルス感染に反応して活性化され、増殖を誘導されることがある。
興味深いことに、現在では後者であることが知られている。しかし、T細胞レセプターのランダムな生成ということは、多くのT細胞が「自己」抗原を認識するということでもある。不思議なことに、”自己 “を認識するこれらのリンパ球は、生涯を通じてサイレンシングされるか、抑制されている(図2.8)。この制御機構に時折誤作動が起こり、自己免疫疾患につながることがある。肝細胞に発現する抗原に反応するT細胞が、自己免疫性肝炎を引き起こす。T細胞が膵臓のインスリン産生細胞に対して反応するようになると、自己免疫性糖尿病になる。
しかしその一方で、基本的にすべての非自己タンパク質に反応する免疫細胞は、生まれながらにして存在し、何か挑戦的なことが起きればいつでも行動を起こす準備ができている。従来の予防接種が乳幼児期に成功するのも、新生児がすでにウイルス感染に耐え、克服できるのも、まさにこのためである。このように、コロナウイルスがやってくると、T細胞の抗コロナチームが立ち上がり、インフルエンザがやってくると、抗インフルエンザチームが立ち上がる。同じウイルス株、あるいはより一般的には関連したウイルス株で再感染するたびに、このチームは強化され、ウイルスをより迅速に封じ込め、感染をより効果的に終息させることができるようになる。
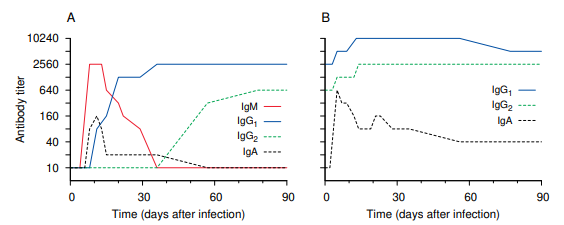
図2.9 一次および二次ウイルス感染に対する血清抗体反応
この実験では、子牛を同じウイルス(牛呼吸器合胞体ウイルス)に2回感染させ、異なるクラスの血清抗体濃度を経時的に測定した。A:最初の感染でIgM抗体が一過性に上昇し、その後IgGに取って代わられる。B: 再感染によりIgGはさらに急速に上昇するが、IgMは再上昇しない。IgAは最初の感染で一過性に上昇するが、2回目の感染ではより高く、より持続的に上昇する。Y軸が対数になっていることに注意。21]の図1より引用した。
2.4 免疫学的記憶
急性感染症に対する免疫応答は一過性である。感染が克服されると、上述したT細胞、B細胞、形質細胞など、活性化された炎症細胞のほとんどはもはや必要とされないため、除去される。このため、問題の病原菌に対する循環抗体のレベルも時間とともに低下する。しかし、一定数のT細胞やB細胞は、いわゆるメモリー細胞として、多くの場合、生涯にわたって存続し、同じ病原体に再びさらされたときに、迅速かつ強固な二次免疫反応を起こすことができる。
一次抗体反応と二次抗体反応の違いを図2.9に示す。描かれている実験は、初乳を与えずに、つまり母体抗体を一切摂取せずに育てた子牛で行われた。これは、観察された抗体が子牛自身の、最初はナイーブな免疫系によって産生されたものであることを確認するためである。
子牛は意図的に同じウイルスに2回感染させた。最初の感染では抗体の上昇がやや遅れた。当初、これらの抗体はすべてIgMクラスであった。その後、IgMはIgG抗体に取って代わられた。IgG抗体はこの実験の時間スケールでは持続的に高値を維持したが、さらに数ヵ月後には徐々に減少すると予想される。わずかな一過性のIgA反応も見られた。
2回目の感染では、初期の遅滞期が短くなった後、IgGがさらに増加した。注目すべきは、この時IgM抗体が全く出現しなかったことである。2回目の感染に対する反応からIgMが検出されなかったことは、新しいB細胞クローンが活性化されなかったことを証明している。その代わりに、抗体反応は、すでにIgMからIgGへ、あるいはIgAへのクラス転換を経験していたメモリーB細胞の増殖によって完全に駆動された。
二次的なT細胞反応も、一次的なものより迅速で強力である。二次免疫反応の臨床的相関は通常免疫であり、同じウイルスの再感染は臨床的に顕在化する前に食い止められる。その最たる例が、麻疹や風疹のような古典的な小児疾患である。天然痘もかつては小児科の病気と考えられ、終生免疫を残していた。
二次免疫反応の有効性を高めることは、もちろんワクチン接種のすべての理論的根拠である。効果の低い一次反応は、病原体である細菌の(理想的には)無害な派生物で誘発されるため、病原体そのものは最初の接触でも二次反応と出会うことになる。天然痘ワクチン接種後、記憶B細胞と記憶T細胞が実質的に終生持続することが報告されているが [22]、他のウイルス、例えば麻疹や流行性耳下腺炎では、ワクチンによる免疫の持続性は低いかもしれない [23, 24]。
2.5 交差免疫
われわれにとって新しいウイルスでありながら、以前に遭遇したウイルスと関連しているウイルスに感染した場合、われわれの免疫系は、古いウイルスから慣れ親しんだ新しいウイルスの分子的特徴を認識し、これらに対する二次的な反応を起こすことができる。同時に、免疫系は新しいウイルスに特有の、つまり新奇な特徴に対しても一次反応を起こす。このことは図2.10のような所見を説明する。このグラフは、COVID-19患者のうち、当初は抗体検査で陰性であったグループにおけるSARS-CoV-2に対する抗体の発現を追跡したものである。IgMとIgGの両方が上昇しているが、IgGの方がより速く上昇している。この急激な上昇は典型的な記憶による反応である。一方、すべての患者が最終的にIgMも発現しており、これは一次反応が起こっていることを示している。このように、IgGの初期の上昇は交差免疫によるものであり、その後のIgMの上昇はSARS-CoV-2の新規で特異的な抗原性特徴に対する一次反応である。
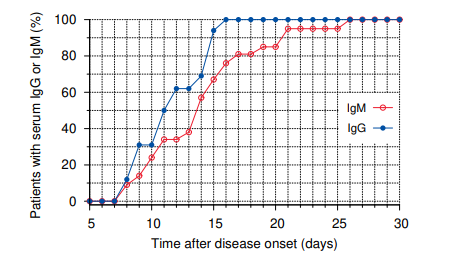
図2.10 COVID-19患者の血清中のSARS-CoV-2抗体
COVID-19患者の毎日の採血でIgGとIgMを別々に測定した。一次免疫反応で予想されるように、すべての患者は最終的にIgM抗体を獲得するが、IgGはIgMより先に上昇することから、免疫反応は二次的なものであり、交差免疫によるものであることがわかる。データは[25]の図1AとBによる。
SARS-CoV-2感染に対する記憶型反応の基礎を築いたと考えられる特異的ウイルスは、図2.11のデータから明らかである。この研究では、COVID-19患者の血清検体を用いて、SARS-CoV-1、MERS、HKU1、OC43の4種類のヒト・コロナウイルスのスパイク蛋白と交差反応する抗体について検査した。いずれの場合も、SARS-CoV-2感染は、SARS-CoV-2に感染していない対照群で観察された抗体レベルに対して有意に抗体レベルを上昇させた。しかし、HKU1およびOC43では、陰性対照群でもかなり高い抗体価が認められた。このような免疫を持っている人がSARS-CoV-2に感染した場合、HKU1やOC43で誘導された交差反応性メモリーB細胞が再活性化し、再び抗体を産生することになる。このような交差反応性抗体の存在は、COVID-19の臨床的重症度の低下と相関していることは注目に値する[27]。
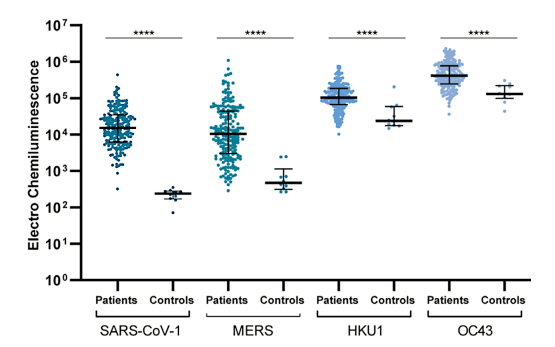
図2.11 SARS-CoV-2感染によって誘発された交差反応性IgG抗体
SARS-CoV-2感染を示す203人の血清検体と陰性対照群の血清検体を用いて、ヒトコロナウイルスSARS-CoV-1、MERS、HKU1、OC43のスパイク蛋白に対する抗体量を測定した。4つの抗原すべてにおいて、抗体価は対照群よりも感染群で高く、SARS-CoV-2のスパイクに対する抗体が他のコロナウイルスのスパイクと交差反応することを示していた。図は[26]から引用した。
SARS-CoV-1(オリジナルのSARSウイルス)とMERSでは、対照群の抗体レベルは低かった。これらのケースでは、COVID-19患者の交差反応性抗体レベルの強い上昇は、SARS-CoV-2そのものによって誘導されたに違いない。したがって、回復したCOVID-19患者は、SARSやMERSのどちらかのウイルスが、例えば別の “高セキュリティ “生物兵器研究所から逃げ出すなどしてカムバックした場合、SARSやMERSから一応の交差防御を享受できると予想される。
SARS-CoV-2と他のコロナウイルスとの間の交差免疫は、Tリンパ球に関しても証明されている [28, 29]。ほとんどの患者においてCOVID-19の臨床経過が穏やかなのは、T細胞とB細胞の交差免疫が広く存在するからであろう。
2.6 ウイルス感染を本当に制御しているのは誰か:抗体か、細胞傷害性T細胞か?
ウイルス感染は抗体形成とT細胞反応の両方を引き起こすことがわかった。ウイルス感染を制御し、克服するために、それぞれ何が重要なのだろうか?答えは「場合による」である。
2.6.1 一次免疫反応と二次免疫反応
あるウイルスに初めて感染した場合(そして交差免疫がない場合)、ウイルス粒子が体細胞に侵入する前に結合して中和する抗体は存在しない。したがって、免疫反応が起こるまでに、かなりの数の細胞が感染している可能性がある。この仕事は主に細胞傷害性T細胞が担うが、抗体依存性細胞傷害メカニズムも貢献している(図2.4参照)。一方、感染ウイルスに以前遭遇したことがあり、抗体レベルがまだ十分であるか、または短期間で上昇させることができる場合、これらの抗体はウイルスの拡散を効果的に制限することができ、したがって支配的な役割を持つ [16, p. 358]。
2.6.2 抗体依存性の増強
答えはウイルスの正体にもよる。すべてのウイルスが特異的抗体を誘導する一方で、一部のウイルスは抗体によって効果的に中和されない。これは、免疫系のある種の細胞が抗体-抗原複合体を取り込み、それを破壊することになっているからである。抗体が結合したウイルス粒子がそのような細胞に取り込まれ、破壊を免れた場合、そのウイルス粒子はその免疫細胞内で増殖し始める可能性がある。全体として、抗体は細胞をウイルスから守る代わりに、ウイルスの複製を促進し、病気を悪化させることになる。この作用は抗体依存性増強(ADE)と呼ばれる。臨床的には、ADEは炎症亢進反応(「サイトカインストーム」)を引き起こし、肺、肝臓、その他の臓器へのダメージを増幅させる。
デング熱は自然なウイルス感染症であるが、抗体依存性の増強によってしばしば合併症を起こす。ADEはデングウイルス、呼吸器合胞体ウイルス(RSV)、麻疹に対するワクチン接種後にも観察されている。コロナウイルスもワクチン誘発性ADEを起こしやすく、オリジナルのSARSウイルス(SARS-CoV-1)、MERSウイルス、ネココロナウイルスで報告されている [30, 31]。これらはすべてSARS-CoV-2に近縁である。特にSARS-CoV-1はSARSCoV-2と相同性が高く、ゲノムレベルで82%の配列同一性があり、両者の宿主細胞上のウイルスレセプターはACE2である。COVID-19感染とワクチン接種に関連した抗体依存性亢進のリスクは、遺伝子ベースのCOVID-19ワクチンが展開される前に文献で明確に認識されていた[32-35]が、非常に短期間の臨床試験中に厳密に評価されることはなかった。
2.6.3 ウイルスによるT細胞細胞傷害の回避
ADEによって抗体を介した中和を回避できるウイルスがある一方で、図2.4に概説したMHC1依存性の抗原プロセシングと提示経路を妨害することによって、細胞傷害性T細胞の活性化を妨げるウイルスもある。よく知られている例としては、ヘルペスウイルスやポックスウイルスがある。
私たちの免疫系には、ナチュラルキラー(NK)細胞という答えがある。NK細胞は特殊な表面レセプターを持つリンパ球で、体内の他の細胞にMHC1分子がないことを検出することができる。それによってNK細胞は、それらの細胞を殺すために活性化される。NK細胞は、感染細胞表面のウイルスタンパク質に結合した抗体によっても活性化される4。
まとめると、細胞傷害性T細胞は一次感染やADEを誘発するウイルスに対して最も重要であり、抗体は二次感染や細胞傷害性T細胞の作用を回避できるウイルスに対して支配的な役割を果たす。
2.7 呼吸器ウイルスに対する免疫:全身性免疫と粘膜性免疫
COVID-19を含む多くのワクチンは、主に呼吸器粘膜に感染し、その後血流にのって他の臓器に感染するウイルスを対象としている。その際、呼吸器(および消化器、泌尿生殖器)の粘膜内や粘膜下に存在する免疫系の細胞は、体内を守る免疫細胞とはやや独立して機能していることに注意しなければならない。
4抗体とNK細胞の複合作用は、「抗体依存性細胞媒介性細胞傷害」(ADCC)と呼ばれる。さらにNK細胞は、ウイルス核酸や一部のウイルスタンパク質に対するパターン認識受容体も備えている。このため、本格的な適応免疫応答が始まる前であっても、NK細胞はウイルス感染と闘うことができるのであり、NK細胞は自然免疫応答と適応免疫応答の両方に関与しているのである。
粘膜免疫と全身性免疫の機能的区別の重要な特徴の一つは、体内に存在する抗体の2つの主要カテゴリーである。第一のカテゴリーの抗体は、粘膜の最上層の細胞層(上皮)の直下にある形質細胞によって産生される。これらの抗体-分泌性免疫グロブリンA(sIgA)-は粘膜表面に分泌される。分泌型免疫グロブリンA(sIgA)は粘膜の表面に分泌されるため、空気感染(あるいは食物感染)したウイルスと接触し、ウイルスの結合や粘膜内の細胞への感染を防ぐことができる。
第二のカテゴリーに属する抗体-IgGと循環IgAは血流中に存在する。これらの抗体は、例えば粘膜免疫が気道の感染を撃退できなかったり、粘膜の細胞だけにウイルスを閉じ込めることができなかった場合に、血流を介したウイルスの拡散に対抗できる可能性がある。
重要なことは、筋肉、すなわち体の内部に注射されるワクチンは、IgGと循環IgAのみを誘導するが、分泌IgAは誘導しないことである。したがって、このようなワクチンによって誘導された抗体は、空気感染するウイルスによる感染から呼吸器の細胞を効果的に保護することはできないし、保護することもできない[37, 38]。この認識は、議論の余地があるわけでも、特に新しいわけでもない。30年前でさえ、McGheeら [38]はこう結論付けている:
現在、一般的な粘膜免疫系についての理解が進んでいるにもかかわらず、現在のワクチンのほとんどすべてが非経口経路[すなわち注射]でヒトに投与されていることは驚くべきことである。全身的な予防接種は粘膜免疫応答の誘導には本質的に効果がない。感染性微生物の大部分は粘膜表面で遭遇するため、粘膜組織における防御抗体やT細胞応答の誘導を考慮することは論理的である。
COVID-19と同様、起源が疑わしいコロナウイルスによって引き起こされる中東呼吸器症候群(MERS)[39]に関する最近の研究で、筋肉内注射による分泌型IgAの誘導に失敗することが再び確認された。この研究で使用された実験的ワクチンは、現在COVID-19に対して展開されている主要なワクチンと同様、遺伝子ベースであった。ファイザー社のCOVID-19ワクチンでは、粘膜抗体の誘導は弱く短時間しか検出されていない[40, 41]。分泌性IgAがほとんど、あるいは全くないため、ワクチン接種が粘膜内でのウイルスの複製を効果的に阻害することを期待する理由はない。従って、SARS-CoV-2コロナウイルスによる上気道感染を予防するワクチンの失敗、つまりウイルスの蔓延が顕在化することを予期しなければならなかった[42, 43]。
分泌型IgA抗体(sIgA)を効果的に誘導する唯一のものは、自然に起こる気道感染か、あるいはおそらく経鼻的に適用されるワクチンであるが、これは今のところ実験的なものである [39]5 。しかし、これらの抗体の感染予防能力には限界があり、そのため空気感染ウイルスによる感染が生涯にわたって繰り返し起こるのである。
分泌型IgAが全身性のウイルス感染症に対抗する上で従属的な役割を果たすことは、sIgAを産生できないごく一般的な遺伝的欠陥(選択的sIgA欠損症)を持つ人が、重症の呼吸器感染症に対する感受性が劇的に上昇することはないという事実からも明らかである。呼吸器粘膜を越えて広がる重症感染症は、身体の内部を保護する免疫システムの全身的な部分に遭遇する。この部分には血液中に存在する抗体、すなわちIgGや循環IgAが含まれる。
2.8 ワクチン接種戦略
次に、抗ウイルスワクチンの種類を、従来のものから検討していく。これらは本書の焦点ではないが、簡単に説明することで、mRNAワクチンの評価に役立つ背景が得られるだろう。
従来の抗ウイルスワクチンでは、感染性ウイルスワクチンと非感染性ウイルスワクチンとに大別される。どちらのタイプも広く使われており、それぞれの長所と短所がある。
2.8.1 「死菌」ワクチン
これらのワクチンは、複製できないウイルス由来の抗原で構成されている。このようなワクチンを調製するための伝統的な方法は、化学的不活化である。問題のウイルスを卵または適切な細胞培養で増殖させ、その後、ウイルス粒子と反応する化学物質で処理することにより、細胞に感染し複製する能力を破壊する。適切な手順は、不活化COVID-19ワクチンの開発に関する最近の報告に記載されている[44]。現在中国のシノバック社が販売しているワクチンはこの種のものである。もう1つの重要な例は、ポリオに対するソークワクチンで、後者の安全性が著しく損なわれたため、セービン生ポリオワクチンからトップの座を奪還した(セクション2.8.2.3参照)。
5生物学的に適切な方法で接種されたワクチンのひとつが、ポリオに対するセービン生ワクチンである。しかし、安全性に関する重大な懸念(下記参照)により、このワクチンは現在では時代遅れとなっている。
従来の死菌ワクチンの潜在的なリスクは、感染性粒子の一部が化学的不活化プロセスで生き残る可能性があることである。組換えDNA技術の出現により実現可能となったサブユニットワクチンでは、このリスクはない。その好例がB型肝炎ワクチンである。B型肝炎ワクチンの唯一の抗原成分はウイルス粒子の表面抗原であり、これは試験管内で組換え発現される。
化学的不活化も組換えサブユニット発現も、ウイルスの感染性だけでなく、そのウイルスタンパク質の毒性活性を低下させたり、あるいは消失させたりする可能性があるが、後者は絶対的なものではない。SARS-CoV-2のスパイクタンパク質を唯一の抗原として含む「ノババックス」サブユニットワクチンは、心筋炎の症例に関連している。
免疫系はこれらの死滅したワクチンにどのように反応するのだろうか?細胞外抗原として処理され、抗原提示細胞によって取り込まれ処理され、同族Tヘルパー細胞やB細胞の活性化を誘導し、抗体産生につながる(セクション2.2.2.3参照)。対照的に、細胞傷害性T細胞の活性化は起こらないか、ほとんど起こらない。さらに、これらのワクチンは皮下または筋肉内に注射されるため、粘膜免疫の誘導は弱いか、ない6。
2.8.2 生ウイルスワクチン
これらのワクチンは、問題となっている病原ウイルスを弱毒化した実際のウイルスであるか、あるいは病原体とは異なるが病原体に近縁の天然ウイルスである。後者の場合、エドワード・ジェンナーが天然痘の予防接種に天然の牛痘ウイルスを用いることを発明したことが最もよく示されている。この方法は交差免疫の優れた例でもある(セクション2.5参照)。20世紀に天然痘の予防接種に用いられたワクチニアウイルス株は、起源がやや不明確な他の天然痘ウイルスに由来するものである [51]。
6粘膜免疫による感染からの部分的な防御は、不活化ポリオワクチンなどで報告されている [48]。ある程度の細胞傷害性T細胞の活性化は、交差提示、すなわちMHC2経路からMHC1経路への抗原の「スピルオーバー」による抗原提示とT細胞の活性化によって可能である[49, 50]。しかし、ポリオの場合、主な目的は粘膜感染を抑制することではなく、むしろ血流を通じて中枢神経系への感染拡大を抑制することであることに留意すべきである(セクション2.8.4参照)。ソーク・ワクチンはこれを容易に達成した。
対照的に、セービンポリオワクチンと麻疹ワクチンは、実験室でヒト以外の細胞培養で連続継代して得られた生ワクチンである。減衰の原理は、単にウイルスがヒト以外の宿主細胞環境に適応するよう「促す」ことである。非ヒト細胞でウイルスの増殖を助ける自然突然変異の少なくとも一部は、ヒト宿主での増殖能力を低下させる。従って、その後ウイルスがヒトに導入された場合、軽度の感染しか起こさない傾向があるが、それでも防御免疫反応を誘導するには十分である。
生ウイルスワクチンは実際のウイルスであるため、抗体反応と細胞傷害性T細胞反応の両方を誘導する傾向がある。このような点から、死菌ワクチンよりも生ワクチンの方が有利であるが、それでも生ワクチ ンには特有の欠点がある。
2.8.2.1感受性の強い個体における非典型的な重症感染
ワクチンウイルスの毒性は、健康な被接種者にとっては十分に低いかもしれないが、免疫障害や皮膚疾患などの素因を持つ人は、接種後に重症化する可能性がある。例えば、天然痘ワクチン接種は、アトピー性湿疹(神経皮膚炎)のある人には禁忌である。アトピー性湿疹(神経皮膚炎)のある人は、ワクチンウイルスがワクチン性湿疹として知られる全身性の皮膚病を引き起こす可能性があるからである[52]。天然痘ワクチン接種は、素因が認められない被接種者においても、心筋炎や脳炎、すなわち心臓や脳への感染を引き起こし、しばしば重篤で時に致命的な結果をもたらす。
2.8.2.2 ヒト集団におけるワクチンウイルスの伝播
ワクチンは生きたウイルスであるため、ワクチン接種者から傍観者へ、そして傍観者からヒト集団全体へ伝播する可能性がある。表面的な検討では、このような伝播は生ワクチンの有効性を高める良い方法であると思われるかもしれないが[53, 54]、以下の理由から、受け入れがたいリスクがある:ワクチンによって重症化するリスクのある人に伝播する可能性がある(上記参照)。残念ながら、後者のリスクは単なる仮定の話ではない。
2.8.2.3 減衰したウイルス株がヒトに対して完全な病原性に戻る
減弱のプロセスは、ヒト以外の細胞でのウイルスの連続継代に依存しており、これらの細胞培養では増殖が促進されるが、同時にヒトに対する病原性が低下するランダムな変異が選択されることになることは前述した。逆に、このような弱毒化ウイルスをヒトに接種すると、ヒト細胞での継代継代が開始され、減弱させる変異を復帰させるか補う変異が選択されることになる。この効果は、ワクチンを接種した人から接種していない人へウイルスが感染すれば、さらに大きくなる。
このようなワクチン由来の復帰型の発生は経口ポリオワクチンでよく報告されており、これらの復帰型の一部はヒト集団で大規模なアウトブレイクを引き起こしている。ナイジェリアで発生したこのような集団感染に関する詳細な研究では、403例の麻痺性疾患と推定70万人の感染者が記録されている。さらに、この研究では、これらの集団発生中に復帰型ウイルス株が複数回出現したことが示唆されている[55]。この例は、問題の深刻さを説明するのに十分であろう。このことが、世界がより安全な死滅型ポリオワクチンに切り替えた理由である。
2.8.3 遺伝子ベースのワクチン アストラゼネカ社とジョンソン・エンド・ジョンソン社が製造しているアデノウイルスベースのワクチンと、ファイザー社とModerna社が製造しているmRNAワクチンである
このテーマには他にも実験的なバリエーションがあるが、ここではこの2種類に限定して議論する。
2.8.3.1 アデノウイルスベースのワクチン
アデノウイルス粒子は二本鎖DNAゲノムを持ち、宿主細胞内に放出する。感染細胞はまずウイルスゲノムをmRNAに転写し、そこからウイルスタンパク質を翻訳する(図2.12参照)。アデノウイルスベースのワクチンでは、天然のアデノウイルスゲノムのいくつかの遺伝子が、問題のワクチン抗原をコードする遺伝子に置き換えられている。アデノウイルスベースのCOVID-19ワクチンの場合、これはSARS-CoV-2スパイクタンパク質をコードする遺伝子である。
このような組換えアデノウイルス粒子に感染した細胞は、SARS-CoV-2スパイクタンパク質と、遺伝子が組換えゲノムの一部であるアデノウイルスキャリア(「ベクター」)のタンパク質の両方を産生することは注目に値する。従って、これらの蛋白質すべてに対して免疫応答が惹起される。初回注射後にアデノウイルスタンパク質に対して上昇した抗体の一部は組換えウイルス粒子を中和することができるので、ブースター注射の効果を低下させることになる。
さらに、組換えゲノムから天然に存在するアデノウイルス遺伝子の一部を欠失させると、このワクチンウイルスは “不自由な “状態になる-ヒト細胞に感染し、細胞内でタンパク質合成を誘導することはできるが、複製することができず、子孫ビリオンを生成することができない。つまり、免疫反応を刺激するのに必要なウイルス粒子の全量を、自然ウイルス感染や従来の生ウイルスワクチンのように生体内で徐々に構築するのではなく、一度に注射しなければならない。このような大量のウイルス物質の注入は、有害事象を悪化させる可能性がある。
2.8.3.2 mRNAワクチン
mRNAワクチン粒子には合成mRNAが含まれており、このmRNAは様々な種類の脂質からなるシェル、脂質ナノ粒子(LNP)に包まれている。これらの脂質は細胞外空間でRNAを保護し、宿主細胞への取り込みを促進する。この取り込みは基本的に細胞の種類に制限されない。どの細胞でもこのmRNA/脂質ナノ粒子を取り込むことができるが、特定の臓器、例えば肝臓、脾臓、卵巣の細胞は、セクション5.2.1で説明する理由により、特に多量に蓄積する。
細胞内に入ると、合成mRNAは脂質の殻を脱ぎ、天然のmRNAのように機能して、コードするタンパク質の合成を誘導する。COVID-19 mRNAワクチンでは、これもSARS-CoV-2スパイクタンパク質である。天然mRNAに含まれる4つのヌクレオシドのうちの1つ、すなわちウリジンが、1-メチルシュードウリジンに人工的に置き換えられているのである。
すなわち、スパイクタンパク質の融合前のコンフォメーションを安定化させる2つの戦略的点変異、すなわち、通常ウイルスエンベロープと細胞膜の融合に伴うスパイクタンパク質の分子形状の変化を抑制する2つの戦略的点変異である(図2.3参照)。
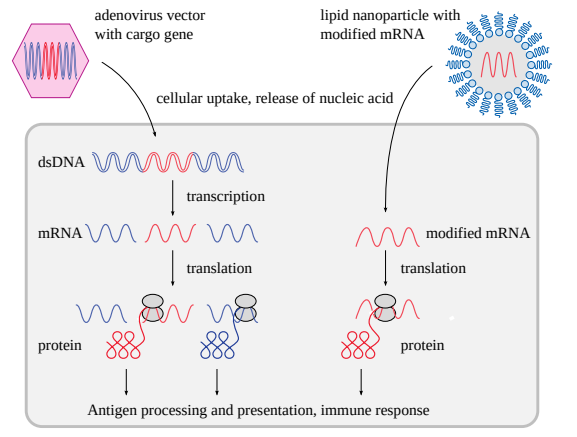
図2.12 遺伝子ベースのワクチンの作用機序
左:アデノウイルスベースのワクチンは、組換え二本鎖DNAゲノム内にカーゴ遺伝子(赤)を含み、細胞内遺伝子と同様に細胞内で発現する。右:mRNAワクチンは、改変されたmRNAを脂質の殻に包んだもので、mRNAの宿主細胞への取り込みを促進する。その後、mRNAは抗原タンパク質に直接翻訳される。抗原のプロセシングと提示は、図2.4と2.7に示すように進行する。
アデノウイルスベースのワクチンとは対照的に、mRNAワクチンの機能には、合成mRNAはスパイク以外のタンパク質をコードしていない。mRNAは宿主細胞内で複製されないため8、必要な量のタンパク質抗原を産生するのに必要な核酸の全量を一度に注射しなければならない。
8これは、少なくとも公式には、一般に供給されているCOVID-19ワクチンに当てはまる。しかし、ファイザー社は、追加のウイルス遺伝子をコードする自己増幅型mRNAワクチンを開発し、臨床試験を行っている。このようなワク チンは、限定的な臨床試験以外ではまだ導入されていない。
2.8.3.3 遺伝子ベースのワクチンにより誘導される免疫応答
どちらの遺伝子ベースのワクチンも、抗原タンパク質の細胞内産生を誘導するため、原理的には MHC1を介した強固な細胞傷害性T細胞応答の誘導に適しているはずである(図2.4参照)。しかし、すべての遺伝子ベースのCOVID-19ワクチンでコードされるスパイクタンパク質は細胞表面に輸送されるため、抗原提示のMHC2経路の大部分を占めることになる。したがって、Tヘルパー細胞の優先的活性化と強い抗体反応は期待できるが、細胞傷害性T細胞の誘導はかなり弱いと考えられる。入手可能な限られた証拠によると、これは実際にそうである [58] 。
遺伝子ベースのワクチンは、表面的には天然ウイルスや生ウイルスワクチンに似ているかもしれないが、悪魔は細部に宿る。これについてはセクション3.3で述べる。
2.8.4 ワクチンによる免疫の程度とワクチン接種の根拠
ワクチン接種の理想的な結果は不妊免疫、すなわち、問題のウイルスがワクチン接種者に感染できなくなることである。これにより、被接種者は臨床疾患から守られるだけでなく、ウイルスが増殖する機会もなくなる。もし集団の十分な割合がこのようなワクチンを接種していれば、その結果、群れ免疫となるはずである。各感染症例が別の感染症例を生む可能性(基本繁殖数)が1以下に低下するため、感染症は集団全体を引き裂くのではなく、一過性に終息することになる。理論的には、被接種者の感染を抑えるだけで、完全になくすわけではないワクチンでも群衆免疫は可能である。
感染を抑制しないワクチンでも、重大な臨床疾患を予防することはできる。例えば、ポリオウイルスは最初に腸の粘膜に感染し、そこからウイルスが排出され増殖する。しかし、この腸管感染は下痢程度のものである。特徴的な麻痺性疾患は、ウイルスがこの最初の増殖部位からまず血流に広がり、次に中枢神経系に広がった場合にのみ起こる。セクション2.7で述べたように、筋肉内投与されたワクチンは粘膜免疫を効果的に誘導することはなく、実際にポリオウイルスはワクチン接種者の多くで依然として伝播する可能性がある[48]。しかし、死菌ポリオワクチンの筋肉内注射は、血流中を循環する抗体を効果的に誘導し、中枢神経系に感染して麻痺性疾患を引き起こす前に、ウイルスを確実に中和する。
9これに反する明らかな例として、スパイク蛋白そのものではなく、スパイクに対する細胞傷害性Tリンパ球が肝臓内で検出された臨床例を取り上げた4.4.6節を参照されたい。
しかし、少なくともウイルスの領域では、現実的な例を見つけるのは困難である。細菌性疾患に関しては、弱毒生ワクチンであるオリジナルの結核ワクチンが有効な例であろう。
集団免疫の興味深い利点は、ワクチン接種者だけでなく、ワクチン接種が望ましくない人を含む非接種者も保護することである。しかし、集団免疫が実際に実現可能である場合にのみ、脆弱な少数の人々を守るために健康な大多数に強制的なワクチン接種を課すことができることは自明である。冷酷な強制力によって国民に押し付けられたCOVID-19ワクチンは、この要件を満たすには至っていない。
2.9 付録:ファイザー社の臨床試験における不正の証拠
抗ウイルス免疫反応の基本的な事柄を説明したところで、ファイザー社が緊急使用許可を申請する際に規制当局に提出した臨床試験データのいくつかを批判的に評価する準備が整った。FDAの報告書[59]とEMAの報告書[60]には、ワクチン接種群とプラセボ群のCOVID-19の累積発症率を比較した重要な図が掲載されている。このグラフはEMAの報告書では図9として示されているが、ここでは図2.13Aに示す。初回注射後12日目までは、両群の累積罹患率は互いに密接に追跡している。しかし、12日目以降、プラセボ群だけが安定したペースで新たな症例を積み重ね続けているのに対し、ワクチン群ではグラフの傾きが突然ほぼゼロになった。
この驚くべき観察結果は、ワクチン接種群ではまさに12日目に免疫が突然、一様に発現したことを示唆している。2回目の注射は1回目の注射から19日以上経ってから行われたので、これは1回目の注射で完全な免疫が確立されることを意味する。しかし、この結論は述べられておらず、実際ファイザー社は1回しか注射を受けなかった被検者に関するデータを全く報告していない。
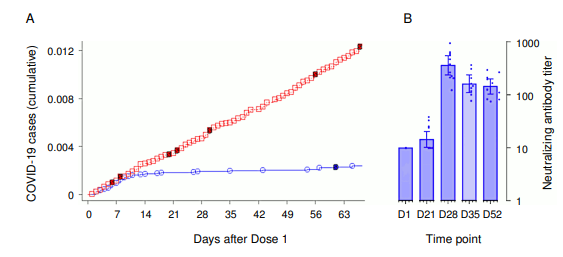
図2.13 ファイザー社の臨床試験における不正の証拠
EMA評価報告書[60]の図9(A;ワクチン接種群およびプラセボ群におけるCOVID-19の累積発生率)および図7(B;初回注射日[D1]およびその後のさまざまな日における中和抗体価)の一部複製。BのY軸が対数になっていることに注意されたい。
問題の微生物やワクチンに初めて曝露した後、12日目に突然完全な免疫が発現するというのは、生物学的にまったくありえない結果である。試験参加者のほとんどはCOVID-19に感染した形跡がないと言われている。多くの人がある程度の交差免疫を持っていたであろうが、本格的な特異的免疫反応はもっと徐々にゆっくりと始まったであろう(図2.10を比較)。図2.13Bは、EMA報告書の図7にあるように、まさにこのようなパターンが、このまったく同じ臨床試験で、このまったく同じワクチンについて報告されている。この図はSARS-CoV-2に対するワクチンの初回注射前とその後の各時点での中和抗体の増加を示している。
以上のことから、中和抗体の血中濃度はウイルスに対する臨床的免疫の程度を反映していると考えられる。しかし、図2.13Bに見られるようなことは全くない。最初の注射から21日目、つまり図2.13Aから明らかなように、突然完全な臨床免疫が発現してから丸9日後、血中の中和抗体量はバックグラウンドレベルをぎりぎり超えて上昇している。中和抗体のレベルが最大になるのは1回目の注射から28日目であり、このときほとんどの被検者はすでに2回目の注射を受けているはずである。細胞性(T細胞)免疫の時間経過は報告されていないが、反対の証明がない限り、抗体反応と類似していると考えられる。
要約すると、1回目の注射後12日目に突然完全な臨床免疫が発現するというのは、表面上は非常にあり得ないことであり、この主張の信憑性は、同じ試験の一部として行われた抗体研究によってさらに損なわれている。従って、この主張は詐欺的と見なさざるを得ない。この文脈で、臨床試験でファイザーのために契約業務を遂行した複数の人物が、これらの試験で発生した不正についてBritish Medical Journal誌に語ったことにも注目したい。その中には、不十分な検査室管理、データ入力の遅れや意図的な改ざん、症状のある患者のフォローアップ検査の完全な欠落などが含まれていた[61]。そのうちの一人は次のようにまとめている: 「クリーンなデータではなかったと思う。. . めちゃくちゃだ」。
Modernaの臨床試験では、状況はそれ以上良くない。両メーカーによるデータ不正の証拠については、Palmerら[62]を参照のこと。
3. mRNAワクチンによる害の免疫学的メカニズム
前章で、「非自己」抗原を発現する細胞は免疫系に攻撃され、破壊されることを見てきた。ウイルス感染では、これは必要悪であり、罹患した細胞を排除することにつながるからだ。緩和される状況としては、ほとんどのウイルスが標的とする組織や細胞の種類は限られており、ほとんどの組織は再生可能であるため、傷はその後治るということである。
mRNAワクチンの支持者は一般に、これらの薬剤は実際のウイルス感染で起こることを模倣しているに過ぎないと主張する。そのため、外来タンパク質の発現は短期間であり、主に筋肉内注射部位に限定されると主張する。したがって、重篤な副作用は予想されない。しかし、これほど誤解を招き、真実からかけ離れたものはない。
3.1 mRNAワクチンは全身に分布し、特に血管に影響を及ぼす
mRNA/脂質ナノ粒子が注射部位に留まるという主張は、現在ではあからさまな事実無根であることが広く知られている。これらのワクチンは、注射部位から局所のリンパ節や血液循環へと急速に広がる(セクション5.2.1参照)。さらに、ほとんどのウイルスとは対照的に、mRNAワクチンのナノ粒子は、血管の最も内側の細胞層を形成する内皮を含む、あらゆるタイプの細胞に取り込まれる可能性がある。
内皮が関与していることは、mRNAワクチン接種がほとんどの自然発生感染と直ちに異なる点である。セクション2.1では、ウイルスは宿主細胞表面の特異的レセプター分子に依存するため、感染できる細胞や組織の範囲が限定されることを述べた。内皮細胞を標的とするウイルスは非常に少ないが、危険な出血熱を引き起こすことがある。デングウイルス、エボラウイルス、マールブルグウイルスなどがその例だ。血管内皮に感染する細胞内細菌もまた、生命を脅かす疾患を引き起こす(チフスやロッキー山紅斑熱など)。これらの病原体によって引き起こされる臨床疾患は出血を特徴とし、しばしば血栓塞栓合併症を併発するが、これはCOVID-19 mRNAワクチンに対する主な急性副反応の一部と酷似している。
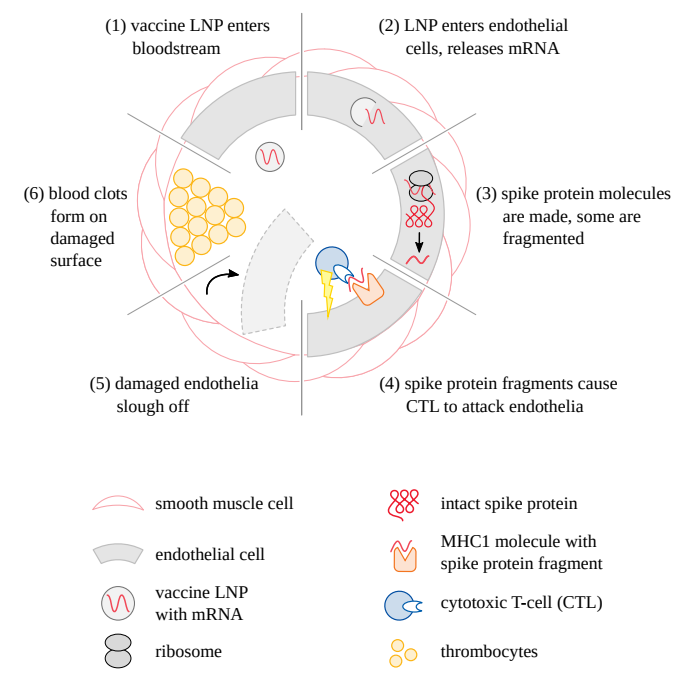
図31 mRNAワクチンがどのように血管を傷つけ、凝固を引き起こすか
ワクチンの脂質ナノ粒子が循環に入った後(1)、内皮細胞に取り込まれ、mRNAが放出される(2)。その後、抗原タンパク質(例えばSARS-CoV-2スパイクプロテイン)が発現し(3)、細胞表面に運ばれ、抗体や補体、あるいは細胞傷害性T細胞による細胞に対する免疫攻撃を引き起こす(4)。損傷した内皮細胞は剥がれ落ち(5)、ワクチン粒子が隣接組織に漏出する。また、血管壁の深層が血液にさらされ、血小板凝集(6)と血液凝固が誘発される。
「非自己」抗原を発現する内皮細胞は免疫系から攻撃を受ける(図31)。先に述べたように、この免疫攻撃には抗体を介した補体活性化、細胞傷害性T細胞、その他のエフェクター機構が様々な割合で関与している。内皮傷害の後に形成される血栓は循環障害を引き起こし、時には心臓発作や脳卒中のような重大で不可逆的な結果をもたらす。この点に関する証拠は明白である-血管の細胞におけるスパイクプロテインの発現、これらの細胞に対するそれに続く免疫攻撃、血栓の誘発はすべて、生検や剖検の組織サンプルではっきりと確認できる(セクション4.3参照)。
3.2 スパイクプロテインの体内での発現は広範囲かつ長期間持続する
モデルmRNAワクチンの研究から、脂質ナノ粒子は筋肉内注射後、速やかに血流に入ることが示された。その後、肝臓、脾臓、卵巣など特定の臓器に優先的に蓄積される。様々な臓器におけるワクチン粒子の蓄積に影響する因子については後述する(セクション5.1参照)。しかし、少なくとも血管自体はすべての臓器と組織でワクチンに曝されており、そこから外来抗原の広範な発現を期待せざるを得ない。COVID-19 mRNAワクチンでは、そのような広範な発現が実際に直接証明されている。
もう一つの重要な検討事項は、抗原がどの程度で発現し、発現がどの程度持続するかである。緒方ら [63]は、SARS-CoV-2スパイクプロテインの発現を、注射当日でも血液サンプルで検出した。スパイクプロテインはタンパク質分解酵素(プロテアーゼ)によって切断される可能性がある。これによってS1とS2と呼ばれる2つの断片が生じる。S2断片は細胞表面に固定されたままだが、S1断片は放出される。緒方らの血液サンプルで検出されたのはこの断片である。しかし、このように検出される期間が短かったのは、おそらく循環抗体のレベルが同時に上昇したためであろう。これらの抗体は抗原と結合し、特異的抗体による抗原の捕捉に依存する検出法を妨害したのであろう。
Bansalら[64]は、血液検体から検出可能なスパイクプロテインの時間経過に関する別の研究を報告している。緒方らとは対照的に、彼らは最初のワクチン注射から2週間後にのみ上昇を検出した。最高レベルは2回目の注射後2週間で検出された。しかし、2回目の注射から4カ月後でも、Bansalらはかなりのレベルを検出した。第一に、抗原は緒方らの報告よりはるかに長い期間後に検出されたこと、第二に、Bansalらは緒方らの初期のピークを見なかったことである。
これら2つの相違は、2つの研究で用いられたサンプリングおよびアッセイ方法の違いによって説明できるかもしれない。緒方らは、抗体捕捉アッセイを、事前の処理をしていない通常の血清サンプルに適用した。対照的に、Bansalらはまずエクソソームと呼ばれる細胞由来の膜小胞を血清から単離し、ウェスタンブロット、すなわちSDSゲル電気泳動によるタンパク質の分離、次いで抗体によるスパイクプロテインの同定を行った。
スパイクプロテインの早期発現に関しては、エクソソームに結合しなかったスパイクプロテインの画分を廃棄していないため、緒方らの報告データを支持する理由がある。一方、後期発現に関しては、SDSゲル電気泳動を用いたBansalらの研究が望ましい。なぜなら、彼らの研究ではスパイクプロテインの検出における血清抗体の干渉が取り除かれているはずだからだ。
結局のところ、緒方らによって報告された初期発現とBansalらによって報告された後期発現の両方が信用できるということである。両研究についてのより広範な考察は、別の文献 [65]に記載されている。mRNAワクチン接種後のスパイクのかなり長期にわたる発現はRöltgenらによっても報告されており[66]、彼らは2回目の注射から60日後もリンパ節でスパイクプロテインを検出し、この同じ時点でスパイクをコードするmRNAの継続的な存在も示した。同様に、Magenら[67]はワクチン接種1カ月後にも強いスパイクプロテインの発現とRNAの継続的な存在を検出した。彼らの研究は、ワクチン誘発性筋炎(筋炎症)の患者に関するもので、組織サンプルは注射部位から離れた骨格筋から採取された。
mRNAのこのような長期持続性、したがって抗原発現の持続性は、コードされた抗原の同一性とは無関係であると考えなければならない。むしろ、デリバリー技術全般の特性である可能性が高い。この抗原発現が長期間続くことによる災難な結果については、後述する。
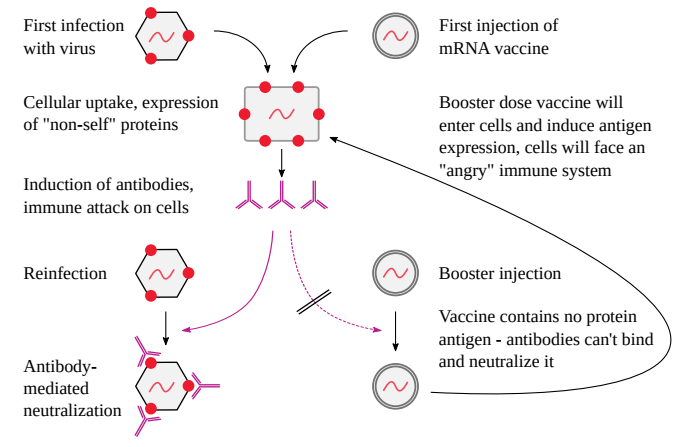
図32 mRNAワクチンは免疫システムのレーダーをかいくぐる
左:適切なウイルスの粒子は、ウイルスゲノムがコードするタンパク質の一部で装飾されている。その結果、ウイルスは最初に感染したときだけ効率よく細胞内に侵入し、それ以降は最初の感染後に誘導された抗体がウイルスを中和する。右:対照的に、mRNAワクチン粒子はタンパク質抗原を含まない。したがって、コード化されたタンパク質抗原に対する抗体は、粒子が私たちの体細胞に侵入し、免疫攻撃にさらされるのを防ぐことはできない。
3.3 mRNAワクチンLNPは免疫システムのレーダーをかいくぐる
本物のウイルスとmRNAワクチンのもう一つの決定的な違いは、後者ではなく前者の粒子が、粒子に含まれる核酸によってコードされたタンパク質分子のコピーで装飾されていることである。この違いがもたらす結果を図32に示す。
ウイルスが重大な病気を引き起こすのは、一般的に一度だけ、つまり、私たちがウイルスに初めて感染したときだけだ。しかし、最初の感染後、私たちはメモリーB細胞を持つようになり、迅速な抗体応答で繰り返し感染に対応できるようになる。
抗体がウイルス粒子と結合し、中和する。この抗体を介した中和が機能するためには、ウイルスの粒子が、そのウイルスによってコードされた抗原の少なくとも一部を含み、露出していなければならない。実際のウイルスはすべてそうだ。対照的に、mRNAワクチンの粒子は、有効な抗原ではない脂質分子の殻に包まれているだけである1。したがって、ワクチンを最初に注射すると、コード化された抗原に対する抗体が誘導されるにもかかわらず、その抗体は、別のワクチンを注射しても、ワクチン粒子を認識して中和することができない。そのため、ワクチンは私たちの体細胞内に衰えることなく入り込むことになる。抗原が発現し、その細胞の表面に現れたときに初めて、抗体はそれを認識し、免疫系の全破壊力をその細胞に対して向けることになる。
上記は、抗原が無傷の状態で細胞表面に現れることを前提としている。これはCOVID-19スパイクプロテインの場合だが、細胞内に残る別の抗原をコードする将来のmRNAワクチンでは当てはまらないかもしれない。しかしこの場合、抗原は処理され、MHC1関連ペプチドの形で提示されると予想される。したがって、記憶反応がB細胞とT細胞のどちらに支配されているかに関係なく、mRNAワクチンによってコードされた抗原に対する先行免疫は、その抗原に繰り返し暴露されることによって引き起こされる障害を悪化させるということである。この理論的予測に沿って、2回目のmRNAワクチン接種後のワクチン誘発性心筋炎のリスクは、1回目のそれを上回ると報告されている(セクション7.3だけでなく、Liら[71]も参照)。
一言で言えば、特異的免疫はウイルスの反復感染による疾病を軽減あるいは完全に予防するが、mRNAワクチンの反復注射による弊害を悪化させるということである。以下のことを述べておく。
1実際に、脂質の一部、特にポリエチレングリコール(PEG)を含む脂質に対する抗体をあらかじめ持っている人もいる。このような抗体はワクチンに対するアレルギー反応を引き起こす可能性がある[68-70]。
このような先行免疫は、先行ワクチン注射によって誘導されたものである必要はなく、問題のウイルスに感染したことのある人が初めてmRNAワクチンの注射を受けた場合でも、効果はほとんど同じだ。したがって、COVID-19ワクチン接種の文脈では、当局がこのような自然免疫を持つ人をワクチン義務から除外することを拒否したために、重篤な有害事象の数が大幅に増加した可能性が高い。
また、アデノウイルスベクターベースの遺伝子ワクチンでは、ここで論じた問題はそれほど深刻ではないことに注意したい。これらのワクチンでも、関心のある抗原は感染性粒子の一部ではないが、アデノウイルスベクターのタンパク質に対して引き起こされる抗体反応は、繰り返し注射することでワクチンウイルス粒子を中和する傾向がある。COVID-19に対するウイルスベースのワクチンは、mRNAワクチンと同規模の重篤な有害事象を引き起こしている[72]。
3.4 自己免疫疾患の誘発
3.4.1 背景
前章で、自己免疫疾患は「自己」抗原を異常に認識するTリンパ球やBリンパ球の出現と増殖によって引き起こされることを述べた。自己免疫疾患は通常、様々な程度の細胞や組織の破壊を伴うが、それはウイルス感染細胞を排除するために存在するのと同じエフェクター機構によってもたらされる。しかし、場合によっては、重症筋無力症における神経細胞から筋肉細胞への信号伝達の阻害や、バセドウ病における甲状腺内の成長やホルモン産生の過剰な活性化など、自己抗体がより微妙な機能障害を引き起こすこともある。さらに別のパラダイムでは、一過性の自己免疫疾患は、長期化する可能性はあるが、それでも臓器機能に不可逆的なダメージを与える。その好例が、膵島のインスリン産生β細胞に対する自己免疫性攻撃であり、その結果、生涯続く1型糖尿病となる。
上記の例が示唆するように、自己免疫疾患の標的である自己抗原はしばしば臓器特異的である。もう一つの例は、甲状腺にのみ存在するサイログロブリンというタンパク質であり、橋本甲状腺炎として知られる自己免疫疾患によるこの臓器の破壊に関与する重要な自己抗原である。血液細胞も自己免疫疾患の標的になりうる。例えば、自己抗体の中には、血液凝固に不可欠な血小板(血小板)を破壊するものがある。その結果、「血小板減少性紫斑病」、すなわち皮下やその他の場所での自然出血が起こる。他の自己抗体が血小板細胞を活性化することもあり、その場合は血栓が観察される。これらの自己抗体が不必要に過剰に活性化されると、血小板が枯渇し、臨床像は血栓と出血が混在するようになる。後者はCOVID-19ワクチン接種後に観察され、「ワクチン誘発性血栓性血小板減少症」(VITT)と呼ばれている。
しかし、すべての自己免疫疾患が臓器特異的というわけではない。自己抗原が全身に存在し、それに対する自己免疫攻撃によって様々な臓器が侵されるものもある。その好例が全身性エリテマトーデス(SLE)である。SLEに特徴的なのは、DNAやリン脂質に対する抗体であり、これらはすべての細胞や組織に偏在している。複数の臓器が侵されることから予想されるように、SLEは非常に重篤な疾患である。
3.4.2 感染症による自己免疫疾患
ほとんどの自己免疫疾患は遺伝的要素を強く持っているが、一方で、ほとんどすべての自己免疫疾患は、発症するために何らかの引き金を必要とする。そのような引き金は感染症である。一例として、急性リウマチ熱の原因となるA群溶血性連鎖球菌が挙げられる。この自己免疫疾患もまた一過性だが、心臓に不可逆的な損傷を与えることがある。
急性リウマチ熱や他のいくつかの自己免疫疾患では、中心的なメカニズムは分子模倣であると考えられている[73, 74]。この発症メカニズムでは、感染因子の非自己抗原が身体の自己抗原のひとつに酷似しているため、受容体がこの2つのどちらかを認識するT細胞クローンまたはB細胞クローンは、もう一方も認識するようになる。このような交差反応性リンパ球クローンは、感染が起こる前にすでに存在している。しかし、この段階では活性化していない。その代わり、自己抗原を発現している体細胞を守るために、他の制御性Tリンパ球から押し付けられた休眠状態にある。
このやや不安定な自己寛容の状態は、感染症が発生し、交差反応性の微生物抗原が飛び込んできたときに崩れることがある。感染は炎症を引き起こし、これが免疫反応を開始させる非特異的な原動力となる(セクション2.2.2.1参照)。この反応によってリクルートされ活性化される様々なT細胞やB細胞クローンの中には、交差反応性微生物抗原を認識した休眠細胞がある。そして、微生物だけでなく、対応する自己抗原を発現している体細胞をも攻撃する。適応免疫反応には遅れが伴うため、自己免疫疾患は通常、感染から数週間後に再燃する。例えば、急性リウマチ熱は、通常は些細な連鎖球菌感染症が引き金となって発症してから1〜5週間後に診断される。
分子模倣もまた、1型糖尿病の発症に関与していると広く信じられている。コクサッキーウイルス、サイトメガロウイルス、ロタウイルスなどいくつかのウイルスが関与している。しかし、他の原因機序、特に膵島細胞が当該ウイルスに持続感染することも、依然として検討されている[75]。
COVID-19感染やワクチン接種後に様々な自己免疫現象や疾患が報告されており[76, 77]、分子模倣が重要なメカニズムであることが示唆されている[76, 78]。このような因果関係は原理的には考えられるが、SARS-CoV-2のスパイクプロテインのアミノ酸配列をヒトのタンパク質の配列と比較することによって予測できる抗原決定基の数は、他のコロナウイルスのスパイクプロテインで得られた数と非常によく似ている。
3.4.3 死亡細胞から放出された自己抗原のクリアランス不全
セクション2.2.1で、ライフサイクル全体を通して私たちの体細胞内にとどまっている抗原は、MHC1表面分子によって断片化され、提示された後にのみ免疫系に遭遇する。これらの抗原を、抗体を産生する細胞から遠ざけることは、自己寛容の重要な側面である。この分離を維持するためには、崩壊した体細胞は速やかに整然と取り除かれなければならない。
SARS-CoV-2のスパイクプロテインは、動物のタンパク質よりもヒトのタンパク質の方が、はるかに高い配列類似性を持っており、したがって免疫学的交差反応の可能性が大きいとする計算機研究が発表された。[79]。しかし、これらの知見は、ヒトに非常に近縁なチンパンジーにも及んでいる。SARS-CoV-2のスパイクプロテインは、チンパンジーの蛋白質よりもヒトの蛋白質との配列類似性が高く、また他のいくつかのコロナウイルスのスパイクプロテインとの類似性を上回るものでもない。従って、SARS-CoV-2が自己免疫を引き起こす傾向が異常に高いことは、予測可能な交差反応性エピトープの数では説明できない。
細胞の残骸を整然と処理するための重要なメカニズムがアポトーシスである。例えば細胞傷害性T細胞の作用の結果、細胞がプログラムされた細胞死を起こすと、細胞片は分子マーカーを露出し、貪食細胞に自己由来であることを識別させる。貪食細胞は、病原性微生物を摂取したときと同じように反応することはなく、したがってヘルパーT細胞細胞を活性化して抗体反応を誘導することもない。
この整然としたクリアランス機構に負荷がかかりすぎ、細胞残屑が除去される前に「腐敗」したまま放置されると、もはや自己由来とは認識されなくなる可能性がある。すると食細胞は、残渣に含まれる「隠れた自己」抗原に対する抗体産生を開始する可能性がある(セクション2.2.2.1参照)。これらの自己抗体はさらに炎症を促進し、さらに多くの細胞を破壊し、さらに多くの細胞の残骸を放出する。この悪循環の最終結果は、本格的な自己免疫疾患であろう。このメカニズムに沿って、食細胞クリアランス経路を阻害する多くの遺伝子異常がSLEの発症を促進する[80]。
原理的には、どのような組織障害でも、この自己免疫経路を起動させる可能性がある。これには、感染症、ワクチン接種、そして明らかに身体的外傷さえも含まれる[81, 82]。この観点から、COVID-19 mRNAワクチンの臨床試験参加者の多くが高熱を経験したことに注目したい[83, 84]。細胞破壊の免疫学的メカニズムと脂質ナノ粒子の毒性活性[85]の両方が、これらの発熱反応の根底にある炎症に寄与している可能性がある。このような知見から、ワクチン接種後の自己免疫現象は一般的であると予想される。
3.4.4 COVID-19ワクチンによって誘発される自己免疫疾患
医学文献には、COVID-19 mRNAワクチンによって誘発された自己免疫疾患の症例報告が多数ある。臓器別の例については[86-89]を、一般的な概要については[77]を参照のこと。診断名には、1型糖尿病、甲状腺炎、ギランバレー症候群、肝炎、全身性エリテマトーデス(SLE)、血小板減少性紫斑病(抗体が介在する血小板破壊)、その他多数が含まれる。具体的な例については第4章で述べる。
3.5 ワクチンによる免疫抑制
3.5.1 COVID-19ワクチン接種後の免疫抑制の発現
COVID-19ワクチンによって引き起こされた自己免疫現象は医学文献の主流になったが、もう一つの潜在的な結果、すなわち免疫抑制についてはまだそうではない。免疫抑制の最も明確な兆候は、ワクチン接種直後に発症した帯状疱疹の数多くの症例報告である。帯状疱疹は、水痘帯状疱疹ウイルス(VZV)の再活性化によって生じる。このウイルスの初感染は水痘を引き起こす。この病気は臨床的には全身に広がるが、自己限定性であり、ウイルスは脊髄近くの知覚神経節(神経節)に残る。ほとんどの人の免疫システムは、ウイルスを永久に抑え込み、再び水疱瘡が現れるのを防いでいる。しかし、一部の人、典型的な中高年では、ウイルスが再び表に出て帯状疱疹を引き起こすことがある。皮膚病変は水疱瘡に似ているが、その広がりは通常1つの皮膚分節、すなわち1つの知覚神経節に対応する皮膚領域に限られる。帯状疱疹は、免疫系を低下させる全身性の基礎疾患の存在を示唆することがあるため、すべての帯状疱疹患者にそのような疾患のさらなる徴候がないか検査することが望ましい。
COVID-19ワクチン接種後には、帯状疱疹のほかに、しばしば消化管を含む細菌感染症も報告されている[91-93]。このような症例も免疫抑制が原因である可能性があるが、血栓や患部の灌流障害が関与している可能性もある。
COVID-19ワクチン接種の開始以来、症例数が増加し、癌の悪性度が増加していることについて、何人かの経験豊富な病理学者が見解を述べている(例えば[94]を参照)。このような症例の多くは、治癒したと考えられていた癌が、時には数十年後に再活性化しているようだ。がん細胞を抑える細胞性免疫のメカニズムは、基本的にウイルス感染を制御し、それに対抗するメカニズムと同じだ。したがって、これらの報告も、ワクチン接種後の著しい免疫抑制を示唆している。
3.5.2 考えられるメカニズム
上述したように、免疫抑制はCOVID-19ワクチン接種によって引き起こされる重大な問題としてまだ一般には認められておらず、その因果関係の問題に取り組む実験的研究が発表されていることも知らない。しかし、いくつかの原因メカニズムはもっともらしい(そして相互に排他的ではない)。
3.5.2.1 飽和帯域幅
免疫系は、その活性化の程度をグローバルに制限されている。もし免疫系が、ワクチンによって誘導された外来抗原の体内の複数の組織や器官における持続的な発現に注意を集中すれば、たまたま同時に侵入してきた実際の病原体との闘いからリソースを逸らしてしまうことになる。
3.5.2.2 リンパ球の餓死
ワクチンでコードされたmRNA外来抗原を発現する体細胞は、細胞傷害性T細胞やその他の細胞傷害性免疫エフェクター機構によって攻撃されることは先に述べた。リンパ球自体も例外ではない。もしmRNAワクチンを取り込めば、他のリンパ球の標的になる。このようにして、免疫システムは自滅する。病理学者のアルネ・ブルクハルトは、リンパ節や脾臓(体内で最大のリンパ器官)で高レベルのスパイクプロテインの発現を観察した。この所見は、免疫抑制の重要なメカニズムとしてリンパ球の餓死を支持している。
3.5.2.3 脂質ナノ粒子による免疫抑制
脂質ナノ粒子の免疫抑制効果は、Qinらによって実証されている[95]。この著者らは、インフルエンザウイルス抗原をコードする実験的mRNAワクチンに対するリンパ球活性化と抗体反応を測定した。この実験的に誘導された免疫応答は、脂質ナノ粒子単独(および別の実験的mRNAワクチン)の先行注射によって抑制された。興味深いことに、この免疫抑制効果は、両方の注射を同じ部位に行った場合に顕著であり、最初の注射による局所リンパ節へのダメージが一因であることが示唆された。しかし、免疫反応のパターンの変化は、2回目の注射を別の部位に行った場合にも観察され、驚くべきことに、LNPを注射したマウスの子孫にまで受け継がれた。
リンパ球は、アポトーシス刺激に対して並外れた感受性を持つことで注目されている。例えば、非常に低線量の電離放射線でプログラムされた細胞死に追い込むことができる。セクション5.3.3.1で述べるように、カチオン性脂質の毒性は活性酸素種によって媒介される。したがって、リンパ球は他の細胞よりも容易に脂質ナノ粒子の毒性に屈する可能性がある。
この文脈で、カチオン性脂質は特異的免疫を抑制するにもかかわらず、同時に非特異的炎症を促進することにも注目したい(セクション5.3.2参照)。この発見は、秦らによって記録された免疫制御の遺伝的変化と同様に、LNPの話には単にリンパ球を殺す以上のものがあることを示している。
3.6 mRNAワクチンによる害の基本的メカニズムは完全に一般的である
この章で取り上げた有害性の証拠はすべてCOVID-19 mRNAワクチンに関するものなので、他の病原性微生物に対する将来のmRNAワクチンには何を期待すべきなのか疑問に思うかもしれない。COVID-19ワクチンの毒性は、それがコードする特定の抗原のせいだと決めつけるべきなのだろうか、それともこのような重大な害はmRNA技術に固有のものなのだろうか?
私たちの考えでは、どのようなmRNAワクチンでも、結果はCOVID-19ワクチンとほぼ同じだ。スパイクプロテインそのものが、免疫系の助けを借りずに血液凝固や炎症を促進することは事実である[96]。とはいえ、第4章で示される証拠は、組織や血管に対する重大で広範かつ持続的な傷害は、ほとんどがスパイクプロテインを産生する細胞に対する免疫攻撃によって引き起こされることを示している。この攻撃は、単にスパイクプロテインが非自己抗原であるために起こるのであり、他のどのmRNAワクチンも、それが標的とする特定の微生物に由来する非自己抗原を必ずコードしているので、同じメカニズムで同じ程度の害をもたらすと予想しなければならない。
4. mRNAワクチンによる免疫学的危害の病理学的証拠
病理学者は病気の原因を特定するために、死亡した患者の臓器や組織、生きている患者の組織標本(生検)を検査する。肺塞栓症や心筋梗塞のような死因を診断するためには、剖検による臓器の巨視的検査が重要であり、通常はそれで十分である。顕微鏡検査は生化学的、免疫学的手法と組み合わせることで、疾患の特定の分子マーカーの発生と分布を検出することができる。病理組織学は死後の研究だけでなく、生検、つまり生きている患者から採取した組織標本でも有用である。COVID-19ワクチン接種の有害事象で苦しんだり死亡したりした患者の病理学的研究が医学文献に載るのは遅かったが、現在では疾病の発生メカニズムに光を当てる証拠がかなり出てきている。後述するように、免疫による体自身の細胞や組織への攻撃は、繰り返される主要なテーマである。
4.1 組織病理学で用いられる主な技術
組織サンプルを顕微鏡で観察するためには、まず組織を均一な厚さの繊細なスライスに切断する必要がある。このステップの準備として、組織サンプルは通常、まず固定剤(多くの場合ホルムアルデヒド)で処理され、次にパラフィンに包埋される。固定剤は試料の化学的・構造的劣化を防ぎ、パラフィンは切片化のために固める。
4.1.1 化学染色
もう一つの重要な考慮点は、視覚的コントラストである。
ほとんどの細胞や細胞内構造は無色であり、顕微鏡下で細部まで容易に識別することはできない。コントラストを高めるために、組織サンプルは一般的に化学染料の混合物で染色される。これらの色素分子は、そのイオン電荷やその他の性質に基づいて、異なる細胞内・細胞外構造に優先的に結合する。
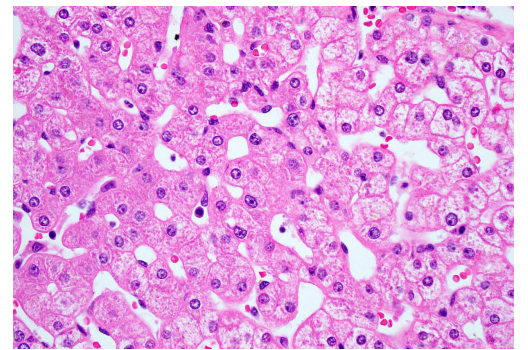
図41 正常肝組織(HE染色)
細胞核は紫色で、細胞の残りの部分(細胞質)はピンク色である。この画像では、ほとんどの細胞の輪郭を見ることができる。常に見えるわけではないが、核は常に見える。点在する小さな明るい赤色の点は赤血球である。これらは肝臓の洞房と呼ばれる空洞の中にある。しかしこのサンプルでは、ほとんどの血液が洗い流されている。画像は[97]から引用した。
広く用いられているHE染色法は、ヘマトキシリンとエオシンという2つの色素を用いる。前者は青みを帯び、核酸やその他の負に帯電した分子に優先的に結合するのに対し、後者は赤色でタンパク質に優先的に結合する。通常、大量のDNAを含む細胞核は青色または紫色に染まるが、それ以外の大部分は主に赤色に染まる(図41)。脂肪の沈着や飛沫は染色されない。HE法は日常的な病理組織検査に有用だが、特定の生理的・病理的な細胞や組織構造をより明瞭にする、興味深い特殊目的の化学染色も数多くある。
4.1.2 免疫組織化学
病理組織学の威力を大幅に増強する重要な技術が免疫組織化学である。免疫組織化学は、抗体の特異性を利用して、目的の特定の分子を含む細胞を選択的に染色する。例えば、すべてのリンパ球が
目的分子を含まない細胞
CD3細胞表面抗原を免疫組織化学的に検出すると、Tリンパ球は強調されるが、Bリンパ球は強調されない。CD4とCD8をそれぞれ検出すれば、T-ヘルパーと細胞傷害性T-リンパ球をさらに区別することができる。後述するように、SARS-CoV-2スパイクプロテインのようなウイルス抗原の発現も観察できる。
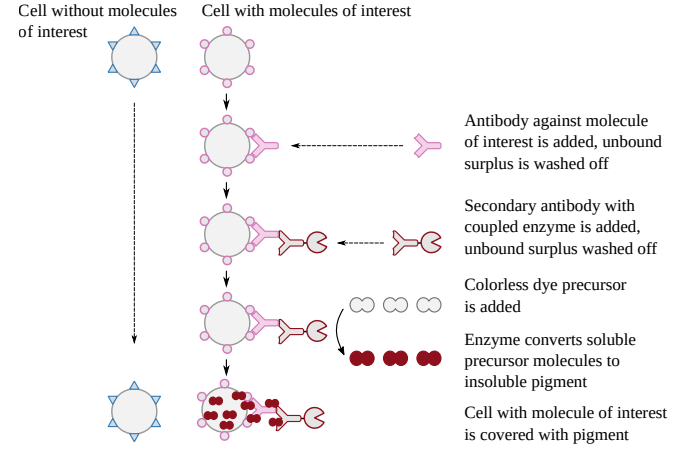
図42 免疫組織化学の模式図
特定の抗体を用いて、組織サンプル中の特定の目的分子を選択的に検出する方法である。詳細は本文を参照。
図42にこの方法の重要なステップを示す。まず組織スライスを、目的の分子を特異的に認識する抗体にさらす。結合が起こるまでしばらく時間をおいた後、結合していない余剰の抗体を洗い落とす。次に一次抗体を認識する二次抗体を加え、結合させた後、未結合の余剰抗体を再び洗い流す。この二次抗体は、無色で可溶性の前駆体分子(多くの場合、ジアミノベンジジン)をその場で沈着する不溶性の色素に変換できる酵素(触媒タンパク質)と化学的に結合している。
1なぜ酵素を抗原特異的一次抗体に直接結合させるのではなく、二次抗体に化学結合させるのか不思議に思うかもしれない。しかし、酵素を二次抗体に結合させる方が便利である。なぜなら、このような結合体は、非常に多くの異なる抗原特異的一次抗体に使用することができ、それ自体は化学修飾する必要がないからだ。例えば、ヘルパーT細胞細胞ではなく細胞傷害性T細胞を検出するには、CD4特異的一次抗体をCD8を認識するものに置き換えるだけでよい。
4.2 証拠のソース
以下では、ほとんどの場合、査読付き医学文献の症例報告や総説に頼ることにする。加えて、病理学の名誉教授であるアルネ・ブルクハルト医学博士が、数人の同僚の協力を得て実施した一連の剖検検査を繰り返し参照する。ブルクハルトの結果はまだ査読付き学術誌の論文として発表されてはいないが、他の病理学者や医学博士たちによって実証され、吟味されたものであり、本章の筆者も入手することができた。
ブルクハルトの発見のほとんどは、査読付き論文に記載されたものと定性的に確認されたものだが、彼の研究は貴重な定量的視点を加えている。この原稿を書いている時点で、ブルクハルトは1回以上のCOVID-19ワクチン注射を受けた後に死亡した43人の患者の剖検資料を評価している。これらのケースはすべて、死亡診断書にそのワクチンに関する記述はなかったが、遺族はブルクハルトにセカンドオピニオンを求めていた。徹底的な調査の結果、ブルクハルトは22症例でワクチンとの因果関係が確実または可能性が高いと結論づけ、さらに7症例で可能性があるとした。彼は3症例で因果関係を否定したが、残りの11症例では決定的な判断ができなかったか、まだできなかった。
死亡した43人の患者のうち、29人はmRNAワクチンの注射を1回以上受けているが、それ以外は受けていない。この中でブルクハルトは、14症例でワクチン接種による死亡が確実あるいは可能性が高いと判断した。このような図は、重篤な有害事象は「極めてまれ」であるという主流派の説をこれまで受け入れてきた人々に一考を促すものである。
4.3 mRNAワクチン接種による血管炎
セクション3.1では、ワクチンはまず血流にのって分布するため、ワクチン障害によって血管が顕著な影響を受けると述べた。血管内皮(血管壁の最内層)の細胞は、次にワクチン脂質ナノ粒子を取り込み、スパイクプロテインの発現を開始する。このセクションでは、いくつかの裏付けとなる証拠について考察する。
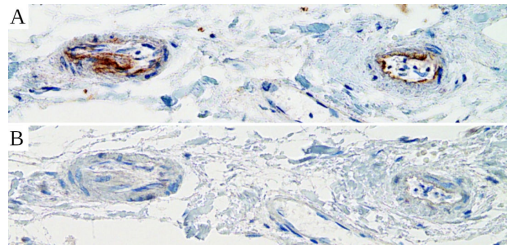
図43 大きな血管(冠動脈)の壁の中にある2つの小さな血管の断面図
SARS-CoV-2のスパイクプロテイン(A)とヌクレオカプシド(B)の免疫組織化学検査。スパイクプロテインのみが検出され、その発現はウイルス感染によるものではなく、ワクチンによるものであることがわかる。提供:Michael Mörz医学博士。
4.3.1ワクチンによって誘導された血管内皮におけるスパイクプロテインの発現
図43は大きな血管(冠動脈)の壁の中にある2つの小さな血管の内皮におけるスパイクプロテインの発現を示している。図のパネルAに見られる褐色の色素はスパイクプロテインを表す。パネルBでは、SARS-CoV-2ウイルスのヌクレオカプシドを検出するために免疫組織化学が用いられた。褐色の色素がないことは、ヌクレオカプシドが発現していないことを示している。
ウイルス感染では、スパイクプロテインとヌクレオカプシドの両方を含め、ウイルスがコードするすべてのタンパク質が発現し、一緒になっているはずだ。一方、遺伝子ベースのCOVID-19ワクチンはスパイクプロテインのみをコードしている。従って、スパイクプロテインのみが検出されたことは、その発現がウイルスへの未診断感染によるものではなく、ワクチン接種によるものであることを裏付けている。
4.3.2 血管炎、血栓、解離:剖検所見の例
図44はCOVID-19ワクチン接種後に死亡した人の小血管と大血管のHE染色組織切片である。パネルAは正常な動脈の断面である。頑丈でコンパクトな筋肉層が見られ、周囲の結合組織よりも強い赤色を呈している。隣のパネルBでは、血管炎に罹患したやや太めの動脈の壁断面が見える。一部の筋組織は左下に無傷のまま残っているが、組織の大部分はリンパ球を含む炎症細胞によって浸潤され、崩壊している。パネルCは同様に冒された小血管を示す。高倍率で見ると、リンパ球、顆粒球、組織球による浸潤が認められる。壁面の破壊はパネルBほど進行していないが、大きな血栓を形成し、内腔を完全に閉塞している。
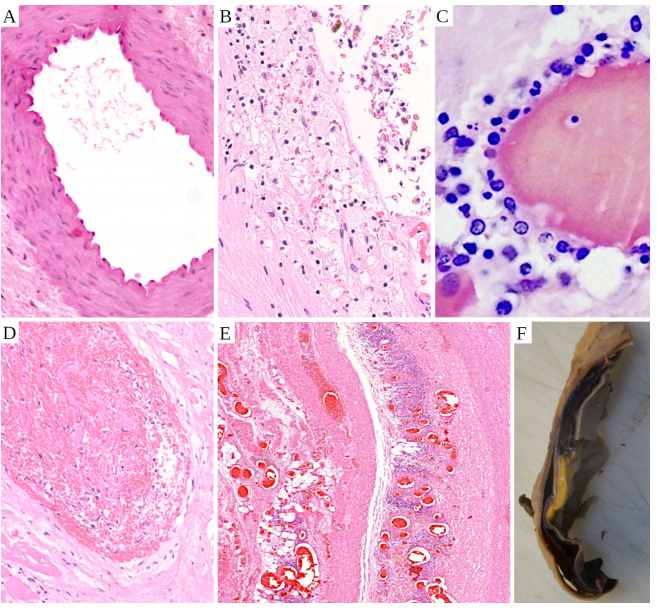
図44 小血管と大血管の血管炎
正常血管の断面(A)、小血管(C)および大血管(B、D、E、F)におけるCOVID-19ワクチン接種後の血管炎の症状。顕微鏡切片はすべてHE染色した。A:コンパクトで規則正しい筋層をもつ正常動脈。内表面は切れ目がなく、明瞭だ。波状の形状は死後の人工物である。B:血管炎を起こした動脈の壁。リンパ球(暗色の丸い点)とマクロファージに侵されている。C: より細い血管の血管炎(高倍率で撮影)。血管壁にはリンパ球と顆粒球が浸潤している。D:太い血管の血管炎は血栓を引き起こし、内腔を満たしている。E:大動脈壁の断面を低倍率で示す。浸潤リンパ球は小さな青い斑点の雲として見える。最も大きな青い雲の左側には、組織を縦に貫く亀裂がある。F:大動脈解離患者の大動脈壁の切除標本にも、マクロ的に亀裂が見える。亀裂内の暗色物質は凝固した血液である。さらなる説明は本文を参照。画像クレジット:パネルAは[97]、BとDはUte Krüger博士、CはMichael Möerz博士、EとFはアルネ・ブルクハルト博士による。
パネルEはワクチン接種者の大動脈の壁切片である。低倍率で撮影したため、浸潤リンパ球は小さな青い斑点の雲として写っている。炎症組織を横切る亀裂が見える。亀裂は図のパネルFにも巨視的に見えるが、これはEと同じ血管を示している。この臨床像は大動脈解離として知られている。
4.3.3 大動脈解離と破裂
解離は他の動脈にも起こりうるが、多くの場合、体内で最大の血管である大動脈に起こる。大動脈は、最も強力な心臓の部屋(左心室)から噴出される高圧の血液を受けているため、強い機械的ストレスにさらされている。大動脈の壁が炎症で弱くなっていると、この負担で破れることがある。破綻は血管の内層(内膜)の破裂から始まる。加圧された血液はその亀裂に押し込まれ、そこから下層の筋肉層である中膜に流れ込む。押し進められると、血液は血管壁を2つのスリーブに分ける。この分離域は大動脈の全長に沿って広がり、さらにその先には枝分かれしている。損傷した血管の外側のスリーブが持ちこたえれば、迅速な外科的治療で患者を救えるかもしれないが、破裂すれば、それに続く内出血は直ちに致命的となる。
大動脈解離は以前、他の型の血管炎に関連して報告されており、[98, 99]、最近ではCOVID-19感染にも関連して報告されている[100, 101]。大動脈解離や大動脈破裂は通常非常にまれだが、ブルクハルト教授はmRNAワクチン接種後に死亡した29人の患者のうち3人の症例を発見した。(この3例の死亡は直近の注射から7日から25日の間に起こっている)。これらの症例のうち1例は免疫組織化学的にも検討され、スパイクプロテインが大動脈壁の剥離セグメント内に検出された。日本の病理学者グループもこのような症例を報告している[102]。
小動脈の解離と破裂は、時に既存の血管奇形によって促進されることがあるが、COVID-19 mRNAワクチンを接種した複数の患者でも報告されている[103-107]。Burkhardt教授も、一連の剖検でそのような症例をいくつか発見している。
4.3.4 血栓
mRNAワクチンによって誘発される血管炎は、大小あらゆる血管に影響を及ぼすことが判明している。図44Dは太い血管の血栓である。図45はRoncatiら[108]の症例報告から引用したもので、肺の組織切片を示している。図45には、Roncatiら[108]の症例報告から引用した、肺の組織切片が示されている。図の右のパネルには、肺組織自体の中にリンパ球の大きな集団も見られる。同様の観察はブルクハルト教授も行っている。
Ayeら[109]は、COVID-19ワクチン接種後に心筋梗塞を発症した35例を調査した。これらの症例のほとんどは注射後24時間以内に発症していた。Sungら [110]が報告した2症例も同様で、両症例ともモデルナワクチンの接種を受けていた。Kawamuraら[111]はファイザー社のワクチンに関連した別の症例を報告している。VAERSデータベース [112]が収集したデータでも早期発現が明らかだ。これがどの程度早期症例が優先的に報告されることによるものかは現在のところ不明である。心筋梗塞は、多くの場合、冠動脈の炎症に関連しており、ブルクハルト教授が検討した剖検例でもよく観察された。
Kolahchiら [113] は、COVID-19ワクチン接種に関連した急性虚血性脳卒中、すなわち脳動脈の閉塞による脳卒中に関するレビューを発表した。彼らの報告に含まれる43人の患者の大多数はアデノウイルスベクターワクチンを接種されていたが、mRNAワクチンを接種された患者が8人いた。注目すべきは、これら8人の患者のうち5人が最初のワクチン接種後にすでに脳卒中を発症していたことで、これは既存の自然免疫によって促進された可能性が高い(3.3節参照)。
動脈ではなく太い静脈が血栓によって閉塞される。虚血性脳卒中と同様、この疾患はウイルスベクターワクチンでより一般的に観察されるが、mRNAワクチン接種後の症例報告もある[114-117]。
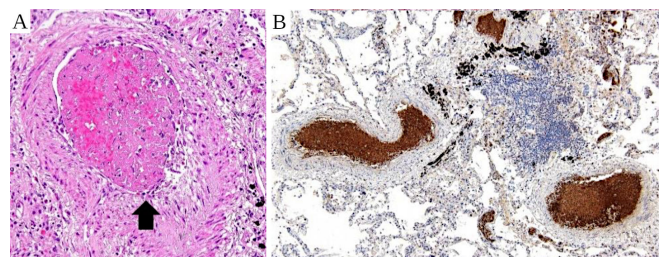
図45 肺組織の血栓。A:血栓が肺の小動脈を閉塞している
血管壁には血管炎の徴候がみられる。B:血栓により閉塞した肺血管。褐色の色素は免疫組織化学によって生じたもので、血小板因子4が検出され、血栓に血小板(血小板細胞)が豊富に含まれていることを示している。中央右の青い雲は大きなリンパ球浸潤である。図はRoncatiら[108]から引用した。
動脈および静脈の閉塞は、他の多くの解剖学的部位でも報告されている。例えば、Ahnら [118] は、モデルナ mRNAワクチンを接種した若年患者において、肺塞栓症を伴う下大静脈の血栓症の症例を報告している。Scendoniら[119]は、ファイザーのワクチン接種後に同様の症状を呈した高齢だが健康な女性の例を報告している。消化管内の多発性動脈閉塞の劇的で、最終的には致命的な症例がLeeらによって報告された。[120]。Burkhardt教授の一連の剖検においても、重篤な結果を伴う動脈閉塞と静脈閉塞の複数の症例が発見されている。
4.3.5 血管炎の多様性
前述したように、炎症が血管の内層に影響を及ぼし、特に血栓を引き起こしやすい例や、大動脈の筋肉質の中間層(中膜)に影響を及ぼし、解離や破裂を引き起こす例をみてきた。また、血管の一番外側の層(外膜)に炎症が集中する場合もある。一人の患者で3つの血管層すべてが異なる部位で侵されることもある。ブルクハルトは、mRNAワクチンのみを注射された患者29人中24人の死亡患者と、遺伝子ワクチンを接種された患者43人中37人の死亡患者で、1つ以上の血管層に血管炎を認めた。
血管炎を誘発する根本的な病態機序もまた、やや多様である。免疫攻撃はリンパ球によって主に行われる場合もあれば、抗体と補体が支配的な場合もある。後者の場合、好中球や好酸球の顆粒球やマクロファージ(組織球)の浸潤が顕著にみられることもある。これらすべての炎症細胞を含む混合浸潤も珍しくない。
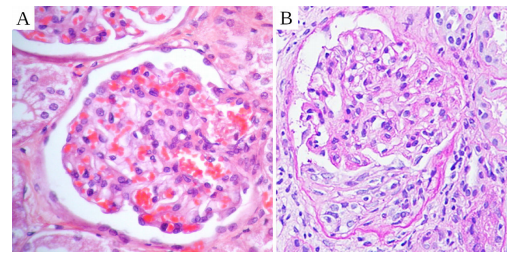
図46 mRNAワクチン接種後のIgA腎症。A:正常な糸球体 [97]
糸球体はコイル状の細動脈からなり、その壁は限外濾過膜として機能する。濾液はボーマン嚢に囲まれた周囲の空隙に取り込まれる。B:mRNAワクチン接種後のIgA腎症における糸球体[122]。ボーマン嚢の下3分の1は炎症の結果、増殖細胞で満たされている。
IgA血管炎も考えられる。これは自己免疫疾患の特殊な形態で、主要な抗体変異体(セクション2.7を参照)の一つである免疫グロブリンAが自己抗原として機能する。遺伝的にこの病気になりやすい人では、IgAに対する自己抗体の形成は、微生物感染やワクチン接種によって誘発されることがある[121]。IgAとそれに対する自己抗体からなる循環免疫複合体は、腎臓、特に尿産生の第一段階として血漿の側方流濾過を行う腎糸球体内に沈着する可能性がある。その結果がIgA腎症である。各糸球体を取り囲む、通常は液体で満たされた空間内に異常な細胞増殖が見られる(図46参照)。その結果、濾過装置の機能障害が生じ、尿中に血球や血漿蛋白が出現することがある。
IgA血管炎のもう一つの症状として、単独で、あるいは腎症とともに、損傷した細い血管から皮膚の結合組織層に血液がしみ出す特徴的な皮疹が現れる。mRNAワクチン接種後に発症したこのような症例は、中谷ら[122]と杉田ら[123]により2例報告されている。
4.3.6 血管炎と凝固におけるスパイクプロテイン毒性の役割
ここまでは、スパイクプロテインを外来抗原とする免疫反応に焦点をあてて病態を考察してきた。しかしながら、スパイクプロテインには固有の毒性が備わっている。例えば、血液脳関門の障害 [124, 125]やDNA修復の阻害 [126]など、驚くほど多様な毒性活性がスパイクプロテインには認められている。このような結合は、ACE2自体の酵素活性を阻害し、血液凝固を促進し、おそらく炎症も引き起こすであろう。[96]。
セクション3.2で述べたように、スパイクプロテインのS1フラグメントは、mRNAワクチン接種後数日間は血流中に循環して検出される。おそらくこれらの抗体は、循環しているスパイクプロテインの検出だけでなく、その活性も阻害すると考えられる。従って、ワクチン接種後数日以内に発生する有害事象、特に初めてワクチンを接種した患者や既存の自然免疫のない患者では、スパイクプロテインの直接的な毒性が原因である可能性が最も高い。この時期には心臓発作や脳卒中が特に多い。スパイクプロテインに対する免疫応答が始まった後に発現する有害事象は、主にこの免疫応答に起因する可能性が高い。
4.4 臓器特異的細胞・組織に対する免疫攻撃
血管炎と血液凝固はあらゆる臓器にダメージを与える可能性があるが、臓器特異的細胞により直接的なダメージを与えるという証拠もある。心臓や骨格筋の筋肉細胞、脾臓のリンパ球、脳のグリア細胞などがその例だ。しかし、mRNAワクチンで傷害を受けた患者の組織サンプルからスパイクプロテインを検出しようとした症例報告は、今のところごくわずかしか発表されていない。
2引用されたJiangとMeiの研究[126]は、掲載されたVirus誌のウェブサイト上では「撤回」とされている。しかし、この「撤回」の科学的理由は説得力に欠け、水面下で政治的圧力が働いた可能性が高い。COVID関連論文の科学的根拠のない「撤回」については、同様の事例がいくつかある[127-130]。
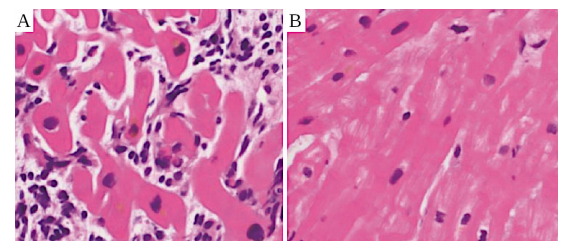
図47 mRNAワクチン接種後の心筋炎症例の心筋生検
A:急性期(ワクチン接種8日後)には、心筋細胞の間にリンパ球やその他の炎症細胞が見られる。B:ワクチン接種58日後、炎症は引いている。画像はKoiwayaら[132]から引用した。
したがって、ほとんどの臓器において、臓器特異的細胞がどの程度スパイクプロテインを発現しているかは現在のところ不明である。血管炎と同様に、ワクチン誘発性炎症によって引き起こされる真の自己免疫は、臓器障害の代替あるいは一因となるメカニズムである。
以下では、その関与が繰り返し観察されている臓器について、いくつかの重要で有益な病理学的研究について述べる。
4.4.1 心筋炎
COVID-19ワクチン接種後の心筋細胞におけるスパイクプロテインの発現は、Baumeierらによって心筋炎患者の心臓生検で証明されている[133]。報告された症例には、mRNAワクチンとアデノウイルスベースのワクチンの両方が含まれていた。Burkhardtらは、Baumeierらの報告よりも広範囲で、明らかに強い発現を、まだ未発表の心筋炎の致死的症例の組織サンプルで検出した。ここではヌクレオカプシドの発現も調べられたが陰性であり、スパイクの発現はワクチン接種によるものであることが確認された。
血管炎と同様、心筋炎の病理組織像はかなり多様である。筋組織に浸潤する炎症細胞は一般的に多形態からなるが、リンパ球が優勢な症例もあれば(図47参照)、顆粒球や組織球が主体である症例もある(図48参照)。好酸球顆粒球が強く存在する症例もいくつか報告されている[134, 135]。
リンパ球が存在する場合は、主にT細胞である。これらの細胞のうち、細胞傷害性T細胞が少なくとも1例で優勢であり、これらの細胞に典型的なCD8細胞表面抗原の発現から推測される[47]。顆粒球と組織球が優勢である炎症性浸潤は、主に抗体と補体によって駆動される免疫反応に適合する。この解釈に沿うように、Choiらによって報告された症例 [136] では、炎症細胞だけでなく、組織球も観察された。
[136]が報告した症例では、好中球顆粒球と組織球に富む炎症浸潤だけでなく、損傷した心筋細胞表面への補体タンパク質の活性化と沈着も認められた(図48C)。
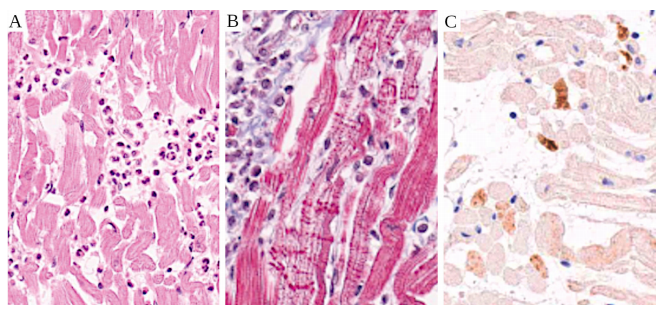
図48 mRNAワクチン接種後に急速に致死的心筋炎を発症した症例(剖検後の病理組織像)
A:心筋組織に浸潤した好中球顆粒球と組織球(マクロファージ)。B: 赤い横縞は心筋細胞の細胞死(収縮帯壊死)を示す。マッソン三色染色。C:心筋細胞上の補体因子C4の沈着(免疫組織化学)。すべての画像はChoiら[136]から引用した。
この所見の最も単純な説明は、これらの細胞がスパイクプロテインを発現しており、スパイク分子に結合した抗体が補体の活性化を引き起こしたというものである。この文脈において、補体膜攻撃複合体によって形成された孔が細胞外カルシウムを細胞内に取り込むことは注目に値する。細胞内カルシウム過剰は収縮帯壊死の原因として認められており、これはChoiらの発表した病理組織学で顕著な特徴であった(図48B参照)。しかしながら、Choiらはこの機序を実証しようとしなかったし、補体の活性化がどのように起こったかという問題についてもコメントしていないことに注意しなければならない。
同様のパターンの炎症が、mRNAワクチン接種後に心筋炎を発症した致死的な2症例において、Gillら [137]によって報告されている。これらの著者は、その所見が心臓に対する「カテコールアミン傷害に似ている」と示唆している。「カテコールアミン」とは、エピネフリン、ノルエピネフリン、ドーパミンを指す。カテコールアミンが過剰に放出される疾患状態、特にエピネフリンとノルエピネフリンを産生する副腎の腫瘍は、確かに心臓に障害を引き起こす可能性があるが、ギルらが示唆した関連性は、それまで健康であった2人の若者の致命的な転帰を考えると、微妙だ。私たちは、Gillらによって報告された病理学的所見は、スパイクを発現している心筋細胞に対する抗体を介した免疫攻撃によってより容易に説明できることを提案する。この疑問は、今後の病理組織学的研究において、より詳細に解明されるに値する。
最近報告された脳炎と心筋炎を併発した症例では、心臓の炎症性変化はほとんどが小血管に集中しており、小血管もスパイクプロテインを発現していることが示された[138]。しかし、これらの小血管が閉塞していないところでも、収縮帯(図48B参照)を伴う損傷した筋細胞が見られた。このことは、血管炎と臓器特異的細胞への直接的な炎症性損傷は、相互に排他的なものではないことを示している。
結論として、ワクチン誘発心筋炎の病理組織像はかなり多様である。リンパ球性炎症はウイルスによる心筋炎に最も類似しており、遺伝子ベースのワクチンが登場する以前はウイルスがこの疾患の主な原因であった。補体活性化によって引き寄せられる顆粒球や他のタイプの細胞による浸潤が優勢な炎症は、スパイクプロテイン発現に対する抗体を介した免疫反応に適合する。これまでに得られている細胞および臓器障害の証拠は、セクション2.2.1で概説した主要な免疫エフェクター機構と一致しているように思われる。しかし、様々なパターンの炎症の根底にある免疫学的メカニズムを完全に解明するためには、より詳細な調査が必要である。
4.4.2 肺の炎症(肺炎)
肺はCOVID-19の重症例 [11]だけでなく、ワクチン接種後の有害事象でも顕著に影響を受ける。前者はSARS-CoV-2が呼吸器ウイルスであることから当然である。ワクチン接種で肺が頻繁に侵される理由のひとつは、ワクチン粒子が血流に入った後に最初に遭遇する毛細血管床が肺であることであろう。さらに、末梢の太い静脈内に形成された血栓が剥離すると、血流に乗って肺に運ばれ、そこで詰まってしまう。
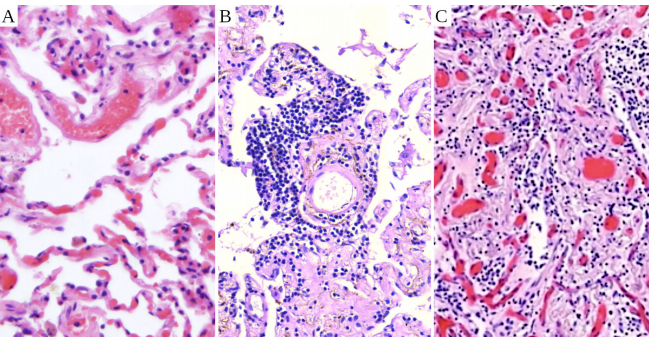
図49 mRNAワクチン接種(モデルナ)後の正常肺組織(A)と肺胞炎(B、C)
Aでは、空気で満たされた空間(肺胞)が見え、繊細な肺胞隔膜によって区切られ、血液で満たされた毛細血管が埋め込まれている。やや太めの血管もいくつか見える。Bでは、密集したリンパ球浸潤が見られる。隔膜は線維化(瘢痕組織)によって肥厚している。パネルCでは線維化がさらに進行し、空隙はほとんど消失している。パネルAは[97]より、パネルBとCはBurkhardt教授提供。
Burkhardt教授は、mRNAワクチン接種患者29人中17人に何らかの肺病変があることを認めた。これらの症例のいくつかは、確かに塞栓症や血管炎の局所症状によるものであったが、11例ではリンパ球による浸潤や肺組織自体の炎症が認められた。感染症によらない炎症性肺疾患は肺炎と呼ばれ、肺胞に炎症がある場合は肺胞炎と呼ばれる。
上の図45Bはすでにリンパ球が浸潤した肺組織の例を示した。ブルクハルトの症例のひとつを図に示す。
4.9. この患者は80歳の女性で、死の40日前に2回接種されたモデルナワクチンの2回目を接種した。肺の炎症に加え、この女性は心筋炎にも罹患していた。図では、肺にリンパ球が豊富に浸潤しているのがわかる。また、線維化、すなわち炎症によって誘発された瘢痕組織の形成が見られ、肺胞と肺胞の間の隔壁が厚くなり、肺胞と肺胞の間にはほとんど空気が残っていない。
mRNAワクチンによって誘発された肺炎で、肺生検での組織病理学的所見は類似しているが、やや重症度は低い症例がSoらによって報告された。[139]。重要なことは、その患者が副腎皮質ステロイドによる治療後に生存し回復したことである。清水ら [140] は、臨床的に類似した3症例を報告しているが、生検は行っていない。
mRNAワクチン接種後に数回報告されている特殊な肺病変は、放射線想起性肺炎として知られている[141-143]。これは、以前に肺の放射線治療を受けた患者に起こるまれな症状である。高線量での放射線照射は肺炎の引き金としては十分だが、通常はある程度の線維化を伴って治癒する。このような患者がその後ある種の薬剤を投与されると、以前に放射線が照射された部位で炎症が再燃することがある。
これまでのところ、このような状態を引き起こす薬剤として知られているのは、ほとんどが細胞毒性の抗癌剤である。このテーマの新しいバリエーションとして、がん細胞に対する免疫反応を増強するために治療的に使用されるある種のモノクローナル抗体の使用後に発生するものがある[144]。COVID-19 mRNAワクチンがこの驚くべき反応を引き起こす機序はまだ解明されていないが、この効果は、免疫系とこれらのワクチンの相互作用を示唆しており、その性質はまだ解明されていない。
4.4.3 脳の炎症(脳炎)
脳組織には、ニューロン(神経細胞)とグリア細胞という2つの主要な細胞タイプがある。神経細胞はもちろん脳機能の中心だが、グリア細胞は異種の集まりであり、多くの必要不可欠な補助機能を果たしている。そのひとつが血液脳関門(BBB)の形成で、血管内皮と共同でその役割を果たしている。BBBは血流によって運ばれる多くの毒物から脳を守っている。しかし、mRNAワクチン・ナノ粒子に関連したBBBの重要性は、おそらく同じではない。COVID-19ワクチン接種後に観察される脳へのダメージの形態は、他の臓器でも見られるものと似ている。血管の炎症と閉塞、直接的な免疫攻撃、自己免疫疾患などである。ここでは後者の2つの発症メカニズムに焦点を当てる。
4.4.3.1 スパイクプロテインに対する免疫反応による脳炎
ワクチン粒子が血管を出て周囲の脳組織の細胞に取り込まれた場合、免疫系がその細胞を攻撃し破壊することが予想される。ある脳炎の症例でこのようなことが起こったことを証明するにはどうすればよいのだろうか?次のような基準があれば、少なくともその可能性は高い:
- 1. ワクチン注射後数日から数週間以内に臨床症状が現れる;
- 2.脳組織内にリンパ球やその他の炎症細胞が検出される;
- 3.炎症巣内でのスパイクプロテインの検出。
基準2と3は病理組織学的検査によってのみ満たされることに注意すべきである。脳の場合、この臓器の生検は特に不安定であるため、病理組織学的検査は通常、剖検後にのみ行われる。
このメカニズムが非常に重要である可能性は高いが、病理学者がそれを探してこなかったため、これまでのところ裏付けとなる証拠は乏しい。しかし、上記の条件をすべて満たす初めての症例報告が最近発表された。[138]。所見の一部を図410に示す。この非常に綿密な研究では、4.3.1節で述べたヌクレオカプシド陰性対照を用いることで、検出されたスパイクプロテインの発現がワクチン接種によるものではなく、ウイルス自体の感染によるものであることを除外している。
この患者は最初にアストラゼネカのアデノウイルスベースのワクチンを1回注射され、その後ファイザーのmRNAワクチンを2回注射された。最後の注射は最初の注射から7カ月後、死亡の3週間前に行われた。スパイクプロテインの顕著な発現は、おそらく直近のmRNAワクチン投与によるものと思われるが、脳毛細血管とその周囲のグリア細胞の一部で検出された。注意しなければならないのは、神経細胞は細胞死を起こしたにもかかわらず、スパイクを直接発現していなかったことである。考えられる説明は3つある:
- 1.神経細胞はスパイクプロテインを発現していたため、免疫系に直接攻撃されたが、その死がスパイクの検出を妨げた;
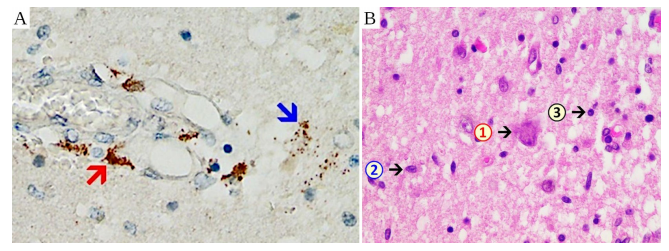
図410 脳炎の病理組織像 A:免疫組織化学的にSARS-CoV-2スパイクプロテインが小血管の壁(赤矢印)と周囲の脳組織の数個のグリア細胞(青矢印)内に検出された。B:脳炎焦点(HE染色)。1:壊死した神経細胞;細胞核は消失している。2:ミクログリア細胞;この細胞型は通常より多い。3:リンパ球。画像はMörzによる症例報告[138]から引用した。
- 2. ニューロンはスパイクプロテインを発現していたが、表面上の抗原発現はほとんどがMHC1関連プロセシングペプチドの形であった
- 3.ニューロンはスパイクプロテインを発現しておらず、直接攻撃されたのではなく、炎症の一般的な騒ぎの中で傍観者として殺された。
- 2つ目の選択肢は作為的と思われるかもしれないが、肝臓組織に関する研究によって、原理的には立証されている(下記セクション4.4.6参照)。更なる研究によって、脳組織での妥当性を確認する価値はあると思われる。
4.4.3.2 自己免疫性脳炎
この発症メカニズムでは、脳炎とワクチン接種の関連はそれほど直接的なものではない。ワクチンはまず炎症を引き起こすが、これは脳に直接作用する必要はないかもしれない。この炎症の中で、免疫反応はスパイクプロテインだけでなく、体内の1つ以上の蛋白質や他の生体分子(自己抗原;セクション3.4参照)に対しても引き起こされる。免疫系は次に、当初は影響を受けなかった標的臓器(脳を含む)内の同じ自己抗原を攻撃し、ここでも炎症を引き起こすことがある。
臨床症状や、定型的な方法で得られる剖検所見は、スパイクに対する直接的な免疫反応と非常によく似ている。従って、脳炎がスパイクプロテインによって引き起こされたのか、それとも自己抗原によって引き起こされたのかをどのように判断すればよいのだろうか?真の自己免疫性脳炎では、以下のような所見が予想される:
- 1. 問題の自己抗原に対する自己抗体が血液検体から検出可能である;
- 2. スパイクプロテインは炎症病変では検出されない;
- 3.自己抗原は体内で恒常的に産生されるため、ワクチン接種との時間的な関連性は低いかもしれない。
Jariusら[145]は、最初にアストラゼネカのアデノウイルスベースのワクチンを2回接種し、その後ファイザーのmRNAワクチンを1回接種した患者に自己抗体陽性の脳炎が発生した症例を報告している。この患者の自己抗原は脳内ミエリンオリゴデンドロサイト糖タンパク質(MOG)であった。これらの著者らは、同じ自己抗原を含む20例の既報告症例の概要も示した。これらの症例のうち3例ではmRNAワクチンが使用されていたが、残りの17例ではアストラゼネカのワクチンが使用されていた。これらの症例はいずれも致死的ではなかったため、炎症性脳病変におけるスパイクプロテイン発現の病理組織学的証拠は陽性も陰性も得られなかった。
Asioliら [146] は、LGI1蛋白に対する自己抗体が検出された4例の脳炎を報告した。これらの症例のうち3例は、すべて同じイタリアの都市(ボローニャ)で、mRNAワクチンを注射した後に発症した。脳の炎症を伴う特に顕著な症例は、Poliらによって報告された[147]。この患者は3つの異なる自己免疫疾患、すなわち脱髄性脳炎、重症筋無力症、甲状腺炎を同時に発症した。しかし、この症例の脳炎を説明しうる特異的な自己抗体は検出されなかった。
4.4.3.3 抗体陰性自己免疫性脳炎
この診断は、mRNAワクチン注射後の脳炎に関するいくつかの症例報告でなされている[148-150]。このような症例の中には、未同定の自己抗原によって引き起こされた可能性があると考えることは確かに妥当である。一方、病理組織学的検査を行わなければ、ある症例が未知の自己抗原に対する免疫反応によって引き起こされたのか、それともワクチンにコードされたスパイクプロテインに対する免疫反応によって引き起こされたのかを判断できないことが多い。
全体として、スパイクプロテインに対する直接的な免疫反応と真の自己免疫の両方がワクチン接種後脳炎の原因として立証されているが、入手可能な限られた証拠からは、この疾患の全体的な発生率に対するそれぞれの寄与を見分けることはできない。
4.4.4 肝炎(肝炎)
他の多くの臓器と比較して、肝臓は感染性または非感染性の原因による炎症に頻繁に冒される。mRNAワクチンによって誘発される肝炎のエビデンスを判断するために、様々な形態を簡単に概説することは有用な背景となるであろう。
4.4.4.1 ウイルス性肝炎
いくつかの肝炎ウイルスがあり、経口経路(最も一般的なのはA型肝炎ウイルス)または汚染された血液や注射針を介して感染する(B型肝炎ウイルスとC型肝炎ウイルス)。A型肝炎は典型的には急性で、自己限定性である。B型肝炎とC型肝炎も一過性だが、患者によっては慢性経過をとり、肝硬変や臓器不全にまで進行することがある。
4.4.4.2 毒性肝炎
肝臓は薬物や毒物の代謝分解において中心的な役割を担っている。これらの分解経路で生じる中間体は化学的に非常に反応性が高く、中毒性肝炎を引き起こすことがある。最も一般的な例はアルコールによる中毒性肝炎であり、その分解により反応性中間体としてアセトアルデヒドが生じる。中毒性肝炎の初期段階では、原因となる化学物質を中止すれば、通常、可逆的である。
4.4.4.3 自己免疫性肝炎
この型の肝炎は、肝組織に発生する自己抗原に対する免疫反応によって引き起こされる。通常、複数の自己抗原が関与しており、これらの自己抗原に対する抗体が血液中に認められる。自己抗原の多くは肝臓だけでなく他の組織にも存在する。それにもかかわらず、この疾患は典型的には肝臓にのみ発症する。これは、遺伝的あるいは外因的な何らかの付加的要因によるものでなければならない。
真の自己免疫性肝炎の特徴は、臨床経過が長引くことである-炎症は、除去される可能性のあるウイルスによっても、中止される可能性のある薬剤によっても引き起こされないため、疾患は長引き、再発する傾向がある。
4.4.4.4 ウイルス性肝炎と中毒性肝炎における自己免疫
理論的には、上記の肝炎の病型は原因によってきれいに分類できるが、実際にはかなりの重複がある。このことは、C型肝炎ウイルス(HCV)が発見された直後に行われたいくつかの研究によく示されている。それまで自己免疫性肝炎と診断されていた患者のかなりの割合が、HCVを保有していることが判明し、多くの場合、HCVがこの疾患の原因と考えられたのである[151-153]。
感染性病原体が組織損傷と抗原の交差反応によって自己免疫疾患を促進することは、すでに述べた(3.4.2節)。組織損傷はウイルス性肝炎でも起こる。上述のように、毒性肝炎は反応性の薬物分解中間体によって引き起こされ、これもまた細胞や組織に損傷を与える。さらに、このような中間体は自己抗原に付着することがあり、それによって自己抗原は変化し、免疫系にとっては非自己のように見える。その結果、化学的に変化した抗原に対する免疫反応が起こるが、その免疫反応は変化していない自己抗原の前駆体にも及ぶことがある。したがって、ウイルス性肝炎や中毒性肝炎の多くの症例では、何らかの自己抗体も存在する。
したがって、自己抗体の検出だけでは、真の自己免疫性肝炎とウイルス性肝炎や薬剤性肝炎を確実に見分けることはできない。さらに、肝細胞に対する免疫攻撃は、それが自己抗原、修飾自己抗原、真性非自己抗原のいずれによって引き起こされたとしても、同様の病理組織学的効果をもたらす。
4.4.5 mRNAワクチンで肝臓にどのような影響を期待すべきか?第5章では、mRNAワクチンを筋肉注射した後、体内でどのように分布するかについて議論する
今のところ、すべての臓器の中で、注射部位そのものを除けば、肝臓が単位組織重量当たりに最も多くのワクチン粒子を蓄積することを簡単に述べておく。このような高い組織濃度では、ワクチンナノ粒子に含まれる合成カチオン性脂質が何らかの細胞・組織障害を引き起こす可能性が高い。ファイザー社[60, p.55]とモデルナ社[154, p.49]の両社による動物実験では、実際に肝細胞障害が観察され、欧州医薬品庁[60]の報告書によれば、ファイザー社の専門家は、その原因が同社独自の未試験のカチオン性脂質にあることを明言している。
効果的な免疫反応を引き起こすには、非特異的な「危険」シグナルと特異的抗原の両方が必要であることは前述した(セクション2.2.2.1参照)。カチオン性脂質の細胞毒性作用は、非特異的シグナルを提供できる[85]。mRNAがスパイクプロテインに翻訳されれば、もちろん有効な標的抗原となる。これら2つの刺激により、肝細胞を攻撃する旺盛な免疫反応の舞台が整う。続く炎症は組織損傷を増幅し、自己抗原に対する二次的な免疫反応、すなわち自己免疫を促進する。したがって、少なくとも臨床例の一部には自己抗体が存在すると考えられる。
問題は罹病期間である。ワクチンのmRNA発現が数日間しか持続しないという製造業者や規制当局の保証は楽観的すぎたが(3.2節参照)、発現は確かに一過性であるはずだ。従って、中毒性肝炎のように、その原因となった薬剤を中止すれば炎症はおさまるが、ワクチンによる炎症もmRNAの発現がおさまるにつれておさまるはずだ。さらに、中毒性肝炎の場合と同様に、副腎皮質ステロイドによる免疫抑制治療に炎症が反応することも予想されるし、ワクチンによって誘発された脳炎や肺炎の報告例もある(上記参照)。
4.4.6 ワクチン接種後の肝炎におけるワクチンmRNAとその発現の証拠
ワクチン接種後の肝炎について発表された症例報告数はかなり多いが、これらの研究のほとんどは、発症機序を推測できるような分子的な詳細を示していない。この点で際立っているのは2つの症例報告である。最初のものは、Martin-Navarroらによって発表されたもので、in situハイブリダイゼーションによる肝生検でのワクチンmRNAの検出について述べている[155]。mRNAは検査された組織標本全体にわたって豊富に検出された。この研究では、検出されたRNAからスパイクプロテインへの翻訳を測定することは試みられていない。
この研究では、スパイクそのものではなく、むしろこのタンパク質に特異的な細胞傷害性Tリンパ球(CTL)、より正確には、スパイクプロテインの細胞内断片化によって生じる特定の小さなペプチドに特異的な細胞傷害性Tリンパ球(CTL)の存在を示している(セクション2.2.2.2参照)。著者らは免疫組織化学でも無傷のスパイクプロテインの存在を検出しようとしたが、結果は陰性であった。同様の所見は、正式には発表されていないが、以前ブルクハルト教授の発表でも共有されており、彼は肝細胞内でスパイクの発現がせいぜい弱い陽性シグナルであることを観察していた。これらの知見を総合すると、肝細胞は無傷のスパイクプロテインを高レベルで発現しているわけではなく、発現している量の断片が特異的CTLを引きつけ活性化するのに十分であることが示唆される。従って、本書が提唱するmRNAワクチンによるワクチン誘発免疫細胞・組織傷害の重要なメカニズムは、この証拠によって支持されることになる。
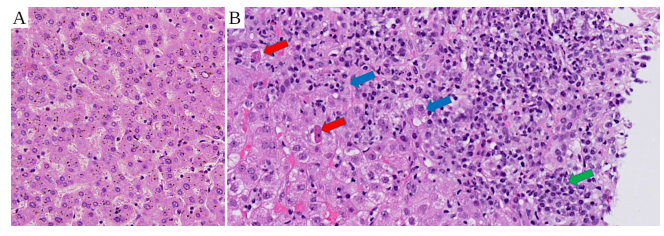
図411 mRNAワクチン接種後の自己免疫様肝炎
A:参考までに正常肝組織の切片([97]から引用)。B:ワクチン誘発肝炎。上端と右端にリンパ球と形質細胞が多い。赤矢印:細胞死(アポトーシス)を起こしている肝細胞。緑矢印:形質細胞(例)。青い矢印:肝細胞のロゼット(炎症の形態学的マーカー)。画像はVuille-Lessardら [157]から引用した。
4.4.7 mRNAワクチン誘発肝炎の臨床例報告
COVID-19ワクチン接種後の肝炎に関する症例報告は非常に多い;このような症例の総説は[158-161]を参照。これらの報告の多くは病理組織学的所見を示しているが、全体的にかなり規則的で類似している。浸潤炎症細胞には、リンパ球、形質細胞、時には好酸球顆粒球が含まれる。浸潤は通常、腸から肝臓に向かって血液を排出する門脈の枝の周囲に集中している。代表例を図411に示す。
ほとんどの報告は、所見を「自己免疫性肝炎」と断定しているが、これらの症例の多くでは、自己抗体がほとんど認められないか、全く認められない。例えば、Izagirreら [160] は、1つの病院から5つの症例を報告しているが、そのうち自己抗体を全く認めなかった症例は1例のみである。Fimianoら [162] は、SARS-CoV-2に対する抗体が非常に高値であったが、甲状腺にのみ存在し肝臓には存在しないタンパク質であるサイログロブリンに対する抗体以外には自己抗体を認めなかった1例を報告している。仮診断は自己免疫性肝炎であり、おそらく薬剤性であろうが、最も可能性の高い原因は自己免疫ではなく、肝細胞が発現するスパイクプロテインに対する免疫攻撃である。これに反する証拠がない限り、この説明は自己抗体陰性肝炎の他のほとんどの症例にも当てはまり、おそらく自己抗体の狭いスペクトルしか示さない多くの症例にも当てはまるものと思われる。
Efeら[163]は、複数の臨床施設でCOVID-19ワクチン接種後に肝炎を発症した87例の概要を報告している。このうち34例は自己抗体を示さなかった。これらの症例の臨床経過は、自己免疫の証拠がある症例よりもいくぶん軽度であったが、それ以外の臨床所見および病理所見のスペクトルは同様であった。著者らは、副腎皮質ステロイド治療に対する良好な反応と良好な長期経過を認めている。Efeらによって報告された症例のほとんどはmRNAワクチンによるものであったが、23%はアストラゼネカ社製のアデノウイルスベースのワクチンによるものであった。
発症機序に関する議論は全般的に曖昧なままだが、自己抗体を示す症例であっても、ほとんどの報告はワクチン接種との関連を認めている。ワクチンとの因果関係が、繰り返し注射を受けた後に肝炎発作を繰り返すことで裏付けられている例もある;例えば[156, 164, 165]を参照。したがって、ワクチン誘発性肝疾患に関する利用可能な症例報告から得られたエビデンスは、上述した予想と密接に一致しており、それは、mRNAワクチンの作用機序が認められていることと、肝細胞に強く蓄積することが知られていることに由来する。
4.4.8 腎臓病
図46にIgA腎症の症例を示したが、これは糸球体腎炎、すなわち腎糸球体を中心とした炎症で、自己免疫によって引き起こされる炎症の一形態である。腎臓の炎症の2番目の主なものは間質性腎炎であり、Tanら[166]はアストラゼネカのアデノウイルスワクチン後に発症した症例を、Miraら[167]はファイザーのワクチンに関連して発症した症例を紹介している。
Fenoglioら [168] は、COVID-19ワクチン接種後に糸球体腎炎、間質性腎炎、その他の腎症が生検で証明された17例を報告している。このうち13例はmRNAワクチンを接種した患者で発生した。この研究では腎臓病に関する他の多くの症例報告も紹介している。Schaubschlagerらによって、別の臨床センターから6例の症例が報告されている[169]。個々の病院からのこのような大規模な症例シリーズは、ワクチン接種後の腎臓病がまれではないことを示唆している。
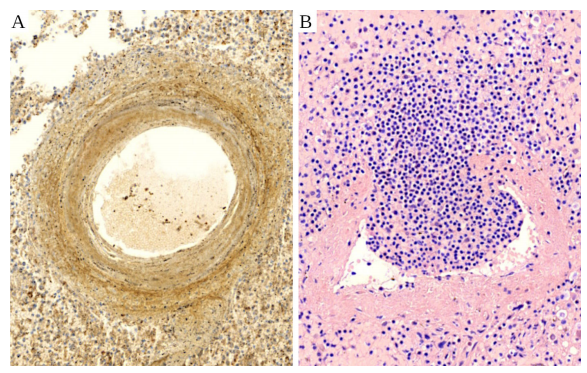
図412 ワクチンによる脾臓の血管炎。脾動脈の断面
A:スパイクプロテインの免疫組織化学検査。強い発現が観察されるが、血管壁の同心円状の層間では多少の差があり、それによって「オニオンスキン」パターンを形成している。周囲のリンパ組織にも強い発現が認められる。B: HE染色。大きなリンパ球浸潤が動脈壁を破って内腔を閉塞している。
4.4.9 脾臓への浸潤
本稿執筆時点で、PubMedはワクチン接種後の脾臓梗塞に関する単一の症例報告[170]と、脾臓の摘出を必要とした重篤な溶血性貧血または血小板減少症に関するいくつかの報告を見つけるだけで、脾臓自体の炎症性疾患に関する報告はない。しかし、ブルクハルト教授は、脾臓の血管炎に類似した非常に顕著な症状を示すいくつかの症例を発見しており、そのうちの1例を図412に示した。従って、ワクチン関連死の剖検において、脾臓の十分な詳細な検査が行われた例がどれだけあるのかという疑問が生じる。
4.4.10 皮膚症状
COVID-19 mRNAワクチン接種後の皮膚の様々な障害が報告されている。Kroumpouzosら[171]は、病理組織学的データのない臨床観察を包括的にレビューしている。組織病理学を含む研究では、血管炎のいくつかの型 [122, 172]、皮膚の最上層である表皮および結合組織からなる皮膚の支持層である真皮への炎症性浸潤がみられた。[173-175]。
天疱瘡 [171, 176]は、表皮と真皮を接着している重要な蛋白に対する自己免疫反応であり、この蛋白が破壊されると水疱が生じる。類天疱瘡はしばしば薬物によって誘発されるが、これはおそらく、中毒性肝炎との関連で前述したように、反応性薬物代謝物と問題の自己抗原との反応によるものであろう(セクション4.4.4.2参照)。
報告された皮膚症状のほとんどは一過性であり、重篤なものではなかったが、それでも診断上注意を要するものであった。生検は最小限のリスクと労力で皮膚から採取できる。このような検体で免疫組織化学的にスパイクプロテインの発現を、また通常の染色で血管炎を検出することは、ワクチンによって悪影響を受ける可能性のある他の臓器に関する診断上の考察に影響を与えるはずだ。例えば、全身性エリテマトーデス(SLE)では通常皮膚が侵されるが、これはmRNAワクチンやアデノウイルスベクターワクチンの接種後に繰り返し観察されている[177-179]。SLEは一般的に糸球体腎炎を引き起こすが、腎臓以外の臓器も侵すことがある。
4.4.11 その他の臓器
上記以外の臓器の病理組織学的報告は比較的まれである。これは、これらの臓器が頻繁に侵されないという意味ではない。
[180]は、シンガポールの一つのクリニックから甲状腺の自己免疫疾患であるバセドウ病の12症例を報告した。同様に、Caron [87]は甲状腺疾患に関する相当数の症例報告をレビューしている。
5. mRNAワクチンの薬物動態と脂質毒性
これまでの章では、mRNAワクチンが疾病を誘発する免疫学的メカニズムに焦点を当ててきた。これらのメカニズムは異なる臓器でも本質的に同じであり、血管が顕著に影響されるため、どの臓器でも発病する可能性があることは明らかだ。とはいえ、ワクチン毒性をよりよく理解するためには、ワクチン粒子が体内のどこに最も多く蓄積し、どのくらいの期間そこに留まるかを考えることが重要である。この種の問題は、本章で検討する薬物動態学の主題である。さらに、mRNAの発現以外の要因から生じるmRNAワクチンの毒性メカニズムについても考察する。
mRNAワクチンの薬物動態と化学毒性は、いずれも脂質ナノ粒子の特性と密接に関係している。従って、ここから検討を開始する。
5.1 脂質ナノ粒子の構造と機能
mRNAワクチンの脂質ナノ粒子の構成を図51に示す。このような粒子には4種類の脂質成分が含まれており、2種類の天然脂質(コレステロールとホスファチジルコリン)と2種類の合成脂質がある(図52参照)。最も少ない脂質は合成脂質で、水溶性ポリマーであるポリエチレングリコール(PEG)と結合し、粒子表面を装飾している。他の3つの脂質は粒子内部に存在する。コレステロールとホスファチジルコリンは粒子を安定化させる役割を果たす。番目の合成脂質はイオン化可能であり、2つの電荷の状態で存在することができる。細胞外腔や細胞質に多く存在する中性に近いpHでは、ほとんどが帯電していない。一方、酸性環境では、脂質分子は水素イオン(H+)と結合し、正電荷を帯びる。相互の静電反発によって脂質ナノ粒子は崩壊し、mRNAは細胞内に放出される(後述)1。
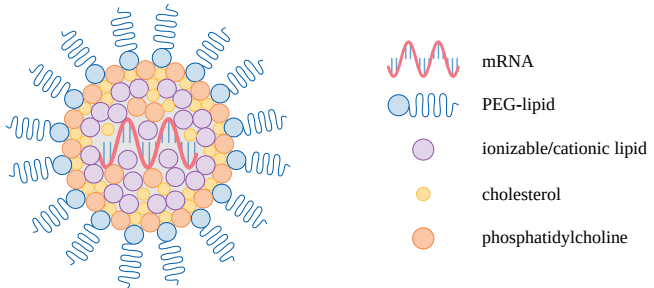
図51 mRNA脂質ナノ粒子の構造
粒子の表面は、親水性(水溶性)ポリマーであるポリエチレングリコール(PEG)と結合した合成脂質で覆われている。マイナスに荷電したmRNAは、主に第二の合成脂質と相互作用する。この合成脂質はプロトン化(すなわちH+イオンと結合)するとプラスに荷電する。コレステロールとホスファチジルコリンは天然に存在する脂質で、安定性のために添加される。
5.1.1 生体分子コロナ
ワクチン脂質ナノ粒子の重要な特徴のひとつは、「生体分子コロナ」を獲得することである。このプロセスは、最初に粒子表面を覆うPEG結合合成脂質分子によって促進される。この脂質種は他の脂質種よりも水溶性が高く、粒子から剥離し、より疎水性の脂質のパッチ、すなわちより「脂っぽい」、あるいは撥水性の脂質のパッチが露出する。このような疎水性のパッチは、同様に疎水性の表面特徴を持つタンパク質分子を引き寄せる(図53)。
このような状況に自然に適合するのがアポリポタンパク質である。これらのタンパク質分子は通常、体内の脂質輸送粒子であるリポタンパク質の表面に存在する(図54A)。しかし、アルブミン、抗体、補体因子C3などの他の血漿タンパク質も、人工リポソームや脂質ナノ粒子の表面で見つかっている[181]。
1脂質粒子内のマイナスに帯電したmRNAと直接相互作用するイオン化可能な脂質分子は、中性pHでもプラスに帯電している可能性が高い。
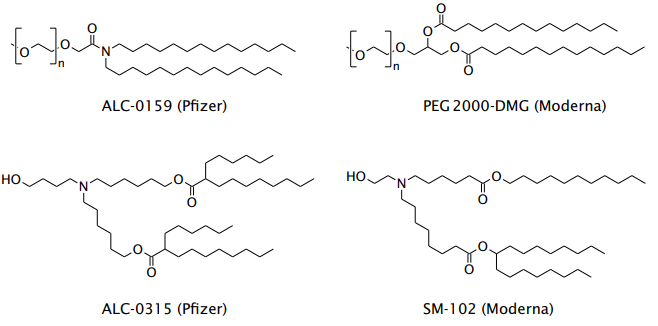
図52 ファイザーおよびモデルナ COVID-19ワクチンに含まれる合成脂質の分子構造
無印の角は水素で飽和した炭素原子を示す。このような原子が多いため、これらの分子は「脂っぽい」特徴を持つ。上:PEG結合脂質。PEGは高分子のエチレングリコール部分からなり、親水性である。このような部位の1つを括弧内に示す。文字nは、このような単位が約45個繰り返されていることを示す。下:カチオン性脂質。窒素(N)原子は水素イオン(H+)と結合することができ、それによって正電荷を帯びる。
アポリポ蛋白質や血漿蛋白質のワクチン脂質ナノ粒子への吸着は単なる好奇心ではない。アポリポタンパク質の生理的機能は、リポタンパク質粒子の「住所タグ」として機能することであり、リポタンパク質の細胞内への輸送や血管内皮のような細胞バリアを越える輸送を指示する。従って、ワクチン脂質ナノ粒子がこのようなアドレスタグと結合すると、体内の天然リポタンパク質と同様に認識され輸送されることになる。
5.1.2 受容体を介したリポ蛋白のエンドサイトーシスとトランスサイトーシス
天然のリポタンパク質の目的は、組織や細胞に脂肪とコレステロールを供給することである。脂肪やコレステロールを必要とする細胞は、受容体を介したエンドサイトーシスによってリポタンパク質粒子を取り込み、その後完全に分解する(図54B)。脂肪とコレステロールは細胞の必要に応じて利用され、アポリポタンパク質はアミノ酸に分解され、新しいタンパク質の合成に再利用される。
図54はまた、エンドサイトーシスによって取り込まれた粒子が、エキソサイトーシスによって再び放出される場合もあることを示している。エンドサイトーシスとエキソサイトーシスが細胞の反対側で起こると、その効果はトランスサイトーシスとなる。これが、リポ蛋白粒子が血管内皮細胞を通過し、循環と組織や臓器の血管外コンパートメントの間を移動するメカニズムである。これは毛細血管に限ったことではなく、動脈でも起こりうるようである[182-184]。
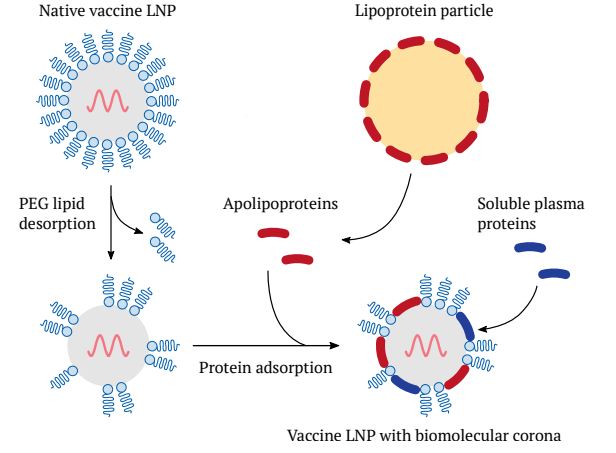
図53 ワクチン脂質ナノ粒子が「生体分子コロナ」を獲得する仕組み
表面に位置するPEG脂質は、粒子から脱離する可能性がある。これにより他のタイプの脂質が露出し、血漿中に存在する様々なタンパク質と結合する可能性がある。アポリポタンパク質は、通常、体内の脂質輸送粒子であるリポタンパク質と結合している。
5.1.3 脂質ナノ粒子による血管障壁の通過
同じ挙動は、表面にアポリポタンパク質を持つナノ粒子でも観察される。Kucharzら[185]は、脂質ナノ粒子が脳内の血管壁を通過し、脳組織内に到達することを報告している2。彼らの研究では、最大の移動は、毛細血管や動脈ではなく、静脈、つまり細い静脈で検出された。同様に、Hartlら[186]は、高分子ナノ粒子の表面は、毛細血管や動脈ではなく、静脈、すなわち小静脈に移動することを報告している。
2Kucharzらはアポリポタンパク質の役割については報告していないが、使用された粒子は生体内で生体分子コロナの獲得を誘導するような組成であった。
ある特定のアポリポタンパク質(ApoE)と共有結合した粒子もまた、循環から脳組織に出ることができた。
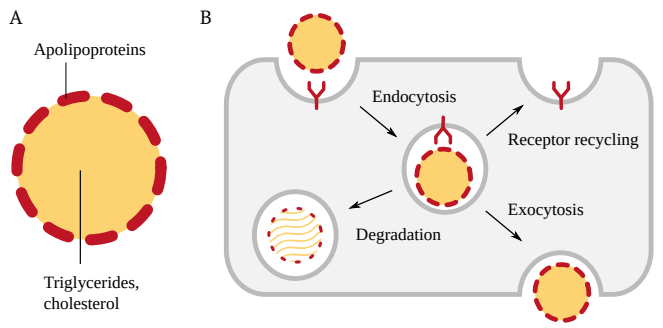
図54 受容体を介したリポ蛋白質のエンドサイトーシス
A:リポ蛋白質粒子の構造 コアは脂肪滴で、トリアシルグリセロール、コレステロール、その他の脂質を様々な割合で含んでいる。表面は様々なアポリポタンパク質で装飾されている。B: アポリポ蛋白質は細胞表面の受容体分子によって認識される。この認識により、細胞は粒子を飲み込み、その後分解されるか、あるいはエキソサイトーシスにより再び放出される。
KucharzらやHartlらが報告したような観察は、脳の血管が他の臓器に比べて溶質や粒子に対して一般的に寛容でないことを考えると、むしろ注目に値する。血管から脳組織への物質輸送を制限する解剖学的・生化学的特徴は、総称して血液脳関門と呼ばれている[187, 188]。生体内における脂質ナノ粒子の挙動に関する実験的研究のうち、血液脳関門を通過する薬物の送達に焦点が当てられているのは不釣り合いであり、このような粒子の他の臓器の組織への輸送はあまり注目されていない。しかし、その逆の証拠がなければ、体内の他のほとんどの臓器において、このような粒子が血管障壁を横切って輸送されることは、少なくとも脳内と同じくらい容易であろうと推測できる。これには胎盤内の母体循環と胎児循環の間の障壁も含まれる可能性が高いが、この疑問はまだ実験的に適切に扱われていない。
5.1.4 mRNAの細胞内放出
ワクチン脂質ナノ粒子の生体分子コロナが受容体を介した細胞への取り込みを促進する一方で、これだけでは中に含まれるmRNA分子がうまく放出・発現される保証はない。Schlichら[189]は、エンドソームコンパートメントから脱出し、タンパク質に翻訳されるmRNA分子は全体のごく一部であることを示すいくつかの実験的研究をレビューしている。これらの知見は、COVID-19 mRNAワクチンに使用されたものと組成は似ているが同一ではない脂質ナノ粒子に関するものである。
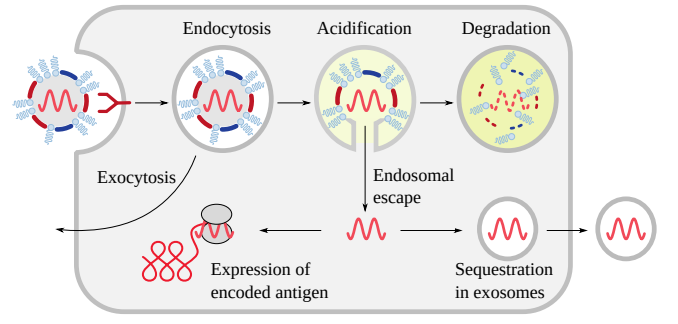
図55 mRNAワクチン粒子の細胞内運命
細胞内に取り込まれたワクチン粒子は、エキソサイトーシスによって再び放出されるか、あるいはエンドソームに捕捉されたまま完全な分解を受ける。このようなエンドソームは他の細胞に取り込まれ、抗原を発現する。
図55にワクチンmRNAの様々な別の運命を示す
最初にmRNAを包んでいたコンパートメント(エンドソーム)からのmRNAの脱出は、酸性化によって引き起こされる。胃粘膜内のある種の細胞が胃に酸を送り込むのと同じように、細胞はエンドソームに酸を送り込む。酸の水素イオンは脂質ナノ粒子のイオン化可能な脂質分子に結合し、プラスに帯電する。これにより、これらの脂質は分散し、エンドソームを包む脂質膜と混ざり合い、mRNAの細胞質への逃げ道ができる(図56)。一方、酸はエンドソーム内の脂質とmRNAの分解も促進する。分解は放出と競合する。
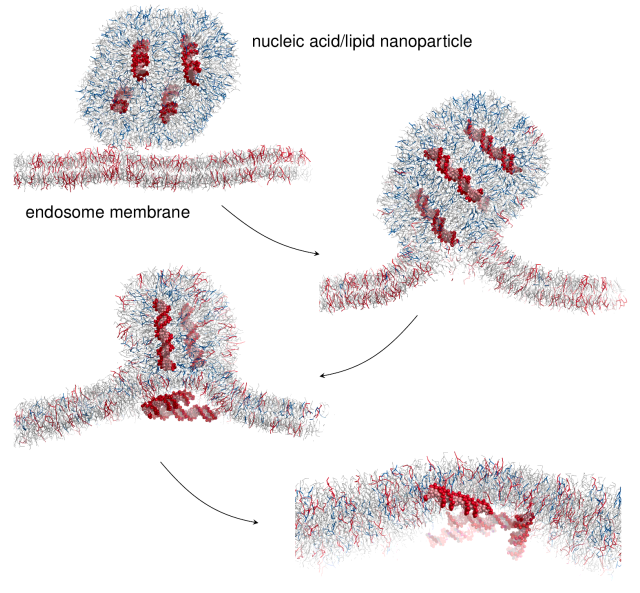
図56 脂質分子間の静電気力によるDNA/脂質ナノ粒子とエンドソーム膜の融合(コンピューターシミュレーション)
LNP上のプラスに帯電した脂質(青)は互いに反発するが、エンドソーム膜のマイナスに帯電した脂質(赤)には引き寄せられる。LNPが膜と結合すると、らせん状の核酸分子(赤)は細胞質に放出される。Bart Bruininks [190]の好意により提供された座標をPymolでレンダリングした。
エンドソームから無傷で脱出できたmRNA分子も、エクソソームにパッケージされることで流され、細胞外に放出される可能性がある。これは、mRNAが細胞内で翻訳される前、あるいは翻訳された後に起こる可能性がある。さらに、エクソソームは他の細胞と合体し、mRNAを他の細胞に送り込む可能性もある。したがって、エクソソームは、LNPの脂質が分散、分解、または排泄された後でも、mRNAの体内での持続と拡散を促進する可能性がある。エクソソームは、COVID-19 mRNAワクチンを接種した人に観察されたスパイクプロテインの長期発現において重要である可能性がある3。
5.2 mRNAワクチンの薬物動態
上記で検討した脂質ナノ粒子の特性は、人体内での輸送とその運命に強い影響を及ぼす。
5.2.1 モデルmRNAワクチンの臓器分布
ワクチンの脂質ナノ粒子の輸送は、細胞に脂肪やコレステロールを供給するリポタンパク質と似ている可能性があることはすでに述べた。すべての細胞はある程度のコレステロールを必要とし、ほとんどの細胞タイプは脂肪を燃焼することができる。とはいえ、リポタンパク質粒子が取り込まれ、回転する量は、異なる臓器の細胞間で大きく異なる。以下の臓器は特に多く取り込まれる:
- 1. 肝臓はリポ蛋白代謝の中心的役割を担っている。肝臓は全身のリポ蛋白の大部分を合成し、余剰のリポ蛋白粒子を再利用する
- 2. ステロイドホルモンを分泌する内分泌腺。このような内分泌腺は、ホルモン合成の前駆体としてコレステロールを使用する。精巣、卵巣、副腎などが含まれる
- 3. 胎盤。胎盤は、胎児への供給と、妊娠を維持するために必要な黄体ホルモンの産生のために、リポ蛋白を必要とする
- 4. 乳腺。乳腺はリポタンパク質から脂肪とコレステロールを獲得し、母乳に放出するためにそれらを再包装する
このことを念頭に置けば、mRNAワクチンの体内分布に関するいくつかの観察結果を理解することができる。この問題に関して入手可能なデータはかなり少ないが、ファイザー社が実施し、各国の保健当局に提出した関連動物実験がある4。この実験では、SARS-CoV-2のスパイクプロテインではなく、タンパク質酵素であるルシフェラーゼをコードするモデルmRNAワクチンをラットに筋肉注射した。このワクチンの体内での動きを追跡するため、脂質ナノ粒子に含まれるコレステロールを放射性物質とした。注射後さまざまな時点で動物を犠牲にし、この放射能を測定することによって、血漿中およびさまざまな臓器内のワクチンの量を決定した3。
3私たちは先に、mRNA中のウリジンをメチルシュードウリジンに置き換えることによって、タンパク質の発現レベルが大幅に増加することを指摘した(セクション2.8.3.2参照)。これは一般に分解に対する抵抗性という観点から説明されるが、発現の速度論 [56, 57]が観察されたことから、別の説明、すなわちメチルシュードウリジン修飾mRNAがエンドソームから細胞質により効率よく脱出することが示唆される。
図57はこの研究から得られた最も重要な知見をまとめたものである
注射後15分もすると、ワクチンは血中に検出される。血中濃度は最初の2時間上昇し、その後低下する。それに伴い、ワクチンは様々な臓器に蓄積される。ほとんどの臓器において、この蓄積は注射後48時間で最高レベルに達する。
組織レベルが最も高い臓器のうち、肝臓、副腎、卵巣はリポ蛋白の回転率が高い臓器である。精巣のホルモン産生細胞であるライディッヒ細胞は臓器組織のごく一部しか占めていないからだ。
一方、脾臓の組織中濃度が高いのは、この臓器がリポ蛋白代謝において顕著な役割を果たしているからとは容易に説明できない。おそらく、アポリポタンパク質以外のLNP生体分子コロナ要素がこの観察に関与しているのであろう。脾臓組織はマクロファージやリンパ球を含む免疫細胞が非常に豊富である。これらの細胞の多くは、抗体や補体系のタンパク質に対するレセプターを持っている。これらのレセプターによって、免疫細胞は、抗体や補体因子が結合した抗原タンパク質、ウイルス粒子、微生物細胞を摂取することができる。抗体や補体因子が確かにLNPに結合する可能性があることはすでに述べたとおりであり、この解釈と一致する。
このワクチンに関するEMAの報告書[58]によると、モデルナはモデルワクチンの動物データも提出している。このモデルワクチンにはSARS-CoV-2とは無関係の抗原をコードする6種類のmRNAが含まれていた。この研究では、脂質ではなくmRNAのレベルが測定された。モデルナの研究結果は報告書に不完全に記載されているが、47ページにはこうある:
4日本とオーストラリアの規制当局はその後、これらのデータの一部を公開した[191-193]。FDAとEMAは公開しなかったが、ファイザーのワクチンに関する評価報告書[59, 60]から、彼らもこの研究結果を目にしていたことは明らかだ。
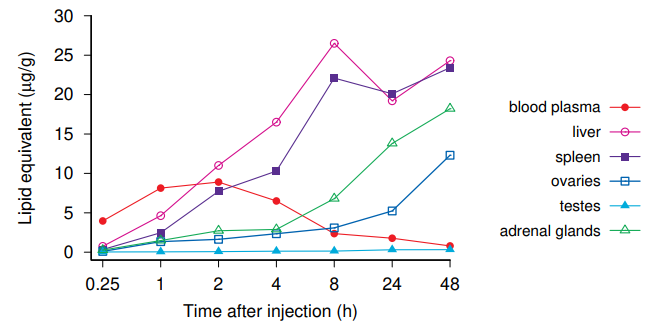
図57 ファイザー/バイオエヌテックワクチンと同じ脂質組成のモデルmRNAワクチンのラットにおける臓器分布
191]の表26.5.5Bから作成したプロット。血漿中濃度は注射後すぐに上昇し、その後ワクチンが様々な臓器に蓄積するにつれて低下する。ワクチンは、放射性標識コレステロール誘導体を用いて測定された(非標識コレステロールは、ワクチン脂質ナノ粒子の通常の成分である)。データは、組織1グラムまたは血漿1ミリリットルあたりのワクチン脂質のマイクログラム単位でのワクチン含有量を表している。肝臓、脾臓、副腎、卵巣の濃度が高いことに注意。
mRNA濃度が(血漿レベルと比較して)高いのは脾臓と眼であった。腎臓を除くすべての組織で低レベルのmRNAが検出された。この中には心臓、肺、精巣、そして脳組織も含まれていた。mRNA-1647の肝臓での分布も本研究で明らかになった。肝臓がLNPの一般的な標的臓器であるという文献報告と一致している。
脾臓と肝臓への蓄積はファイザー社の研究と一致している。卵巣と副腎については特に言及されていないが、これらの組織にはファイザーのものと同程度にはモデルナのモデルワクチンが蓄積しなかったことを示唆する表現である。
私たちは、特定の臓器の組織レベルにかかわらず、少なくとも血管とその内皮は、それぞれの臓器でワクチン粒子にさらされることに注意する。したがって、血管炎や血栓塞栓症はすべての臓器で発生する可能性がある程度高い。
さらに、蓄積レベルの高い臓器では、組織特異的な病理学的変化が予想される。しかし、後述するように、これらの動物実験の結果は、実際のmRNAワクチン分布の全体像を示していない可能性が高い。
5.2.2 モデルワクチンの臓器分布と病理組織学的所見との相関
4.4.7節で見たように、文献にはワクチン誘発性肝炎の症例報告が多数ある。ブルクハルト教授により脾臓の病変が数例報告されているが(4.4.9節参照)、卵巣や副腎はあまり精査されていないようだ。ワクチンに関連した流産や死産の症例における胎盤に関する病理組織学的な症例報告は、これまでのところ文献からも見つかっていない。
一方、心筋(4.4.1節)および脳(4.4.3節)では、ファイザー社およびモデルナ社の動物実験において、これらの臓器がモデルワクチンを比較的低濃度または中程度しか蓄積していないにもかかわらず、炎症およびワクチン誘発性のスパイクプロテイン発現の証拠が確認されている。観察された炎症は、血液脳関門によって保護されているはずの脳に関して特に顕著である。この文脈では、2つの重要な注意点に注意しなければならない:
1. 脳組織が炎症に罹患すると、血液脳関門は破壊される。したがって、mRNAワクチンの初回注射によって誘発された脳内の血管炎は、血液脳関門を軟化させ、その後のブースター注射で送達されたワクチン粒子の侵入を容易にするかもしれない。したがって、初回注射後だけでなく、1回以上の反復注射後にもワクチンの臓器分布を調べることが重要であった。しかし、ファイザー社とモデルナ社の動物実験ではこのようなことは行われなかった。
2. SARS-CoV-2のスパイクプロテインは血液脳関門の完全性を損なうことがいくつかの研究で示されている[124, 125, 194, 195]。他の場所で発現していても血流を通じて脳に到達するスパイクプロテインは、ワクチン粒子の脳への浸透を促進する可能性がある。対照的に、ファイザーのモデルワクチンはルシフェラーゼをコードしており、この点では不活性であると推定される。モデルナのモデルワクチンはサイトメガロウイルスのタンパク質をいくつかコードしている;
これらのタンパク質が血液脳関門の完全性に直接影響するという情報はないようだ。
これらの考察は、病理組織学的所見や上記5.1.3節で議論された実験的研究と相まって、mRNAワクチンは、ファイザー社やモデルナ社のモデルワクチンに関する非常に限定された動物実験が示すよりも、より広範囲かつ効果的に分布することを強く示唆している。
5.2.3 除去の時間経過と活性持続時間
セクション5.1.4で、mRNAはワクチンナノ粒子が細胞内に取り込まれた後、脂質から分離する可能性があることを示した。従って、両成分の排除は別々に考える必要がある。
5.2.3.1 mRNAの排除の時間経過
ファイザー社は、同社のCOVID-19ワクチンに含まれるmRNAの排除、あるいはmRNAワクチンのモデルに関するデータを全く提供していないようだ。彼らの動物実験[192]で適切なデータは、そのモデルワクチンによってコードされたタンパク質であるホタルルシフェラーゼによって誘導される発光の測定だけだ。報告によると、肝臓内の発光は注射後2日以内に沈静化したが、注射部位の筋肉組織は9日間検出可能な発光を示した。このことは、mRNA自体が同様の期間内に不活化されたことを示唆しているが、証明はしていない。
EMAの報告書[58]に記載されたモデルナのモデルワクチン研究の要約によると、消失の半減期、すなわちmRNAのレベルが半分に低下するのに必要な時間間隔は、注射部位で15時間、脾臓で63時間であった。また、モデルmRNAの混合物は血漿から速やかにクリアランスされ、半減期は約3時間であったとしている。
これらの結果は、全体として合成mRNAのクリアランスがかなり速いことを示唆しているが、これらの研究のどれもがCOVID-19ワクチンに配備されたmRNAを使用しておらず、さらにすべての研究がげっ歯類で行われたことを強調しなければならない。したがって、これらの結果を現在のmRNAワクチンやヒト患者への使用に直接適用することはできない。セクション3.2で述べたように、COVID-19ワクチンのmRNAは、注射後60日目にリンパ節で検出され[66]、30日目には注射した手足以外の筋肉組織で検出されている[67]。最近、Fertigらによって、注射を受けた患者の血漿サンプル中にワクチンmRNAが長期間残存していることが報告された[196]。この著者らによると、すべての患者が注射後15日目でも陽性であり、この時点が最も新しい時点であったようだ。同様に、Castruitaら[197]は、注射後28日目までの血液サンプルからワクチンmRNAを検出した。これらのヒトを対象とした研究を総合すると、ワクチンmRNAはファイザー社やモデルナ社の動物実験が示唆するよりもはるかに長く持続する可能性がある。
5.2.3.2 脂質排泄の時間経過
ファイザー社のワクチンには、人体に天然に存在する2種類の脂質と2種類の合成脂質が含まれている(図52参照)。ファイザー独自のデータ [192]によると、同社独自のカチオン性脂質(ALC-0315)の60%が静脈注射後に肝臓に蓄積する。このレベルは注射後2週間たっても著しく高く、分解が非常に遅いことを示している(図58)。PEG修飾脂質(ALC-0159)の肝臓への蓄積はより少ないが、これはおそらく、粒子が肝臓に到達する前に、循環系で脂質ナノ粒子から放出されることを反映している。
報告書によると、両脂質とも尿中では検出されなかった。しかし、PEG-脂質の半分は未変化体のまま糞便中に排泄された。これは肝細胞によって胆汁中に分泌されたためと考えられる。一方、カチオン性脂質はわずか1%しか糞便中に認められなかった。したがって、PEG-脂質の約半分とカチオン性脂質の大部分は代謝分解を受けている可能性が高い。いくつかの脂質の代謝物は、in-vitroの実験で実際に特徴づけられたが、in-vivoの研究はないようだ。
EMAの報告書[58]によると、モデルナはCOVID- 19 mRNAワクチンに含まれる2種類の合成脂質の除去に関するデータを提出していない。EMAの報告書には、モデルナ独自のカチオン性脂質であるSM-102の「近い構造類似体」に関する知見が簡潔にまとめられており、この類似体の注射後1週間を超える持続性は動物実験で観察されなかったと記載されている。モデルナのPEG結合脂質の構造式を考慮すると、かなり迅速な分解が考えられるが、証拠は示されていない。
EMAは、体内での脂質の蓄積は考えにくいと断言しているが、以下の点に注意しなければならない。
- 1.提供された情報は、医薬品開発と承認の通常の基準からするとまったく不十分である。
- 2.脂質の蓄積がないことは、累積毒性がないことを意味しない。これについては5.3.3.2節で後述する。
-
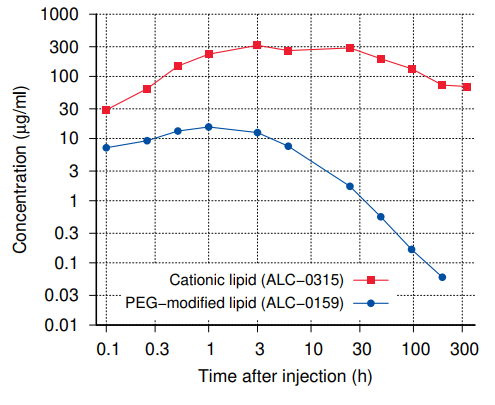
図58 ファイザーのCOVID-19ワクチンに含まれる2種類の合成脂質の静脈注射後の肝組織レベルの時間経過
データは[192]による。x軸とy軸はともに対数である。
5.2.4 偶発的な血管内注射
5.2.3.2節で、静脈内注射された実験動物では、ワクチンの非常に大きな割合が肝臓に到達することを見た。おそらく他の臓器にも、筋肉内注射よりも静脈内注射の方がより多量のワクチンが投与されるであろう。
ヒトの患者はCOVID-19ワクチンを筋肉注射されるが、注射が意図したとおりに機能すれば、注射された物質の多くは、少なくとも最初は確かに筋肉組織に保持される。しかし、看護師や医師であれば誰でも知っているように、筋肉内注射の注意深い手技、すなわち事前の吸引 [198-200]があっても、ボーラスが誤って直接血流に送り込まれることがある。Middletonら [201] は、テストステロン3000本以上の注射のうち、1.5~2%で部分的または完全な血流への注入が起こることを発見した。この割合は、COVID-19ワクチンでも同程度か、訓練を受けていない補助要員が投与することがあったことを考慮すると、さらに高い可能性がある。このような場合、注射されたワクチンの大部分、あるいは全部が全身に行き渡ることになる。
動物実験では、mRNAワクチンによる心筋炎は、筋肉内注射よりも静脈内注射の方が重篤であることが示されている[202]。ヒトや他の臓器への損傷についても、同じことが想定される。最も重篤な急性ワクチン副作用の多くが、このような偶発的な静脈内注射に関連している可能性は十分にある。
5.3 脂質ナノ粒子の毒性
ここでも2種類の合成脂質に限定して議論する。PEG結合脂質は、この2種の中では量が少なく、記録されている唯一の有害作用のメカニズムは、これらの脂質に対するアレルギー反応である。対照的に、カチオン性脂質はワクチンLNPに含まれる全脂質のほぼ半分を占めており、適応免疫系からの「助け」を得ることなく、そのまま毒性を発揮する可能性がある。
5.3.1 PEG結合脂質によるアレルギー反応
ポリエチレングリコール(PEG)結合脂質は、化学的反応性や細胞構造の物理的破壊によって重大な毒性を引き起こすことは知られていない。しかし、血漿中にPEGに対する抗体が存在する場合には、アレルギー反応を引き起こす可能性がある。このような抗体は、mRNAワクチンの初回注射に反応して生じた可能性があり、その後、同じまたは別のmRNAワクチンを注射した後にアレルギーが臨床的に顕在化する可能性がある。しかし、mRNAワクチンや他のPEG含有医薬品の注射を受けたことのない患者の血液サンプルからも、PEGに対する抗体が検出されている[203]。このような患者では、PEGを含む下剤や化粧品によって抗体が誘導された可能性があるが、他の化学物質との免疫学的交差反応も考えられる。
PEGアレルギーは、アナフィラキシーとして臨床的に現れる。皮膚に膨疹ができ、患者によってはアナフィラキシーショック [204]、すなわち循環不全を起こす。これはハチやスズメバチに刺されたときのアレルギーに類似しており、毒が直接血流に乗った場合に最も危険である。mRNAワクチンに反応するアナフィラキシーショックも、誤って静脈内に注射してしまう可能性がある。
アナフィラキシーは、炎症細胞、特にマスト細胞から特定の炎症メディエーター(ヒスタミン、血小板凝集因子、ロイコトリエン)が放出されることによって起こる。この放出の最も単純な引き金は抗原特異的免疫グロブリンE(IgE)である。しかし、他の機序、特に補体の活性化も関与している可能性があり、これはより一般的で豊富なIgG
やIgM抗体によって誘導される。PEGに対するIgGとIgMは、PEGアレルギーの臨床例で証明されている[205]。このような症例でPEG特異的IgEが生じるかどうかは、まだ明らかにされていない。
PEG結合医薬品への抗体の結合とそれに続く補体の活性化は、食細胞による循環からこれらの医薬品の除去も促進する[206]。mRNAワクチンの場合、このようなクリアランスの促進により、コード化された抗原に対する免疫応答が変化する可能性がある。
5.3.2 カチオン性脂質による炎症シグナル伝達
ファイザーおよびモデルナ COVID-19ワクチンに使用されているものと同様のカチオン性脂質が、強い炎症反応を引き起こすことが、いくつかの実験的研究で示されている。関与する細胞シグナル伝達経路のスペクトルはかなり広く、脂質種によって多少異なるLonezら[207]。Ndeupenらによる最近の研究 [85]では、RNAの有無にかかわらず、合成脂質ナノ粒子に対する強い炎症反応が示された。この研究で使用されたカチオン性脂質は独自のもので、その化学構造は特定されていないが、COVID-19ワクチンに使用された2種類のカチオン性脂質に類似している可能性が高い(図52参照)。このことは、COVID-19ワクチン接種者の間で局所的、全身的炎症反応が頻繁に観察されていることと一致する。しかし、このような臨床観察だけでは、炎症に対するmRNAと脂質のそれぞれの寄与を見分けることはできない。
セクション2.2.2で、特異的な免疫反応の誘導には非特異的な防御機構の活性化が必要であり、その活性化は組織の損傷によって、あるいは様々なパターン認識レセプターの刺激によって起こることがわかった。従来のワクチンに含まれるタンパク質抗原は、通常、それ自体ではどちらの刺激も与えない。そのため、このようなワクチンには、いわゆるアジュバント、すなわち、足りない非特異的免疫活性化をもたらす天然または合成物質が添加されている。カチオン性脂質は、その炎症促進作用と同様に、アジュバントとして働くことが示されている[208, 209]。COVID-19 mRNAワクチンに含まれるカチオン性脂質は、mRNAの細胞内放出における重要な役割に加えて、このような働きもすると考えられる。
5.3.3 カチオン性脂質の化学毒性
カチオン性脂質がエンドソームコンパートメントからワクチンmRNAを放出する能力は、その正電荷に大きく依存する。細胞膜を形成する天然脂質はすべて中性か負電荷(陰イオン)を帯びている。
様々な種類のカチオン性分子は、負に帯電した細胞膜に強く引き付けられ、細胞膜を不安定にし、破壊する傾向がある(図56参照)。このテーマには多くのバリエーションがある。例えば
- – 私たちの食細胞は陽イオン性ペプチドを産生し、病原微生物の細胞膜を破壊するのに使っている[210];
- – タンパク質は正電荷を帯びたペプチドモチーフを持ち、それが膜を通過するのを促進する[211]。
- – 陽イオン性洗剤は微生物の細胞膜を破壊し、効果的な殺菌剤となる傾向がある[212]。
現在のCOVID-19ワクチンに使用されているようなイオン化可能な脂質は、細胞質内、すなわちエンドソームの外側の細胞内全般で優勢なH+イオン濃度(またはpH値)でのみ部分的に帯電する。これは、pHに関係なく常に正電荷を帯びている前世代のカチオン性脂質よりも改善された点である。とはいえ、このようなイオン化可能な脂質であっても、細胞質内ではある程度帯電したままであるため、細胞膜を破壊することができる。
5.3.3.1 陽イオン性脂質は活性酸素種を誘導する
カチオン性脂質による細胞膜破壊の下流で起こる重要な作用は、活性酸素種(ROS)の産生である。活性酸素の生成には、NADPHオキシダーゼやミトコンドリア電子輸送鎖など、いくつかの膜関連酵素系が関与していると考えられる[213]。生成の正確なメカニズムに関わらず、これらの活性酸素は、膜脂質やDNAを含む細胞内の様々な敏感な標的を攻撃する[214]。ミトコンドリアの膜損傷は、活性酸素の産生を増幅させる可能性が高い。ミトコンドリアや細胞のDNAへの損傷は、アポトーシスを誘発する。
FilionとPhillips [216]は、マクロファージがカチオン性脂質の細胞毒性作用に対してより感受性が高いことを見出したが、彼らはかなり異なる脂質混合物を使用しており、COVID-19ワクチンに含まれる脂質では感受性プロファイルが異なる可能性があることに注意しなければならない。免疫組織化学的には、COVID-19
5特にアデノシンデアミナーゼ欠損症の例を参照されたい。アデノシンデアミナーゼ欠損症は、全身の細胞に遺伝毒性ストレスを与える代謝性疾患だが、リンパ球を選択的に駆逐する。これにより重症複合免疫不全症(SCID)が引き起こされる[215]。
このことは、リンパ球が脂質ナノ粒子の化学的毒性をも受ける可能性を示唆している。リンパ球は適応免疫系のバックボーンであるため、カチオン性脂質の毒性は免疫抑制を引き起こすと予想される。
活性酸素種は通常の細胞代謝でも発生するが、それに応じて私たちの体細胞は活性酸素種を消去し、ダメージを軽減する能力を持っている。活性酸素とその様々な毒性変換産物に対する重要なスカベンジャーは、チオール化合物のグルタチオン(G – SH)である。例えば、HazeltonとLang [217]は、ラットのG – SHレベルは腎臓で心臓の3倍、肝臓でさらに3倍高いと報告している。このように、肝臓は脂質ナノ粒子を強く蓄積する傾向がある一方で、脂質毒性に対処するための代謝予備能が最も高い。G-SH予備能が低い他の臓器は、LNPの組織レベルが低いにもかかわらず、肝臓よりも深刻なダメージを受ける可能性がある。これは、COVID-19ワクチンの前臨床安全性試験において、解決されるべきであったが、解決されなかった多くの疑問の一つである。
5.3.3.2 DNA損傷は累積する
大まかに言えば、薬物の影響は可逆的なものと不可逆的なものがある。
アルコールは、可逆的な作用と不可逆的な作用の両方を持ちうる薬物の好例だ。気分や警戒心に及ぼすアルコールの影響は、代謝によって不活性化されると治まるが、アルコールによって誘発された肝臓の炎症は化膿し、肝硬変になる可能性があり、これは薬物を完全にやめた後でも永続的である。
可逆的な薬物作用が累積毒性を引き起こすのは、薬物そのものが体内に蓄積される場合、つまり、以前の投与量が完全に除去される前に繰り返し投与される場合に限られる。しかし、肝硬変の例が示すように、不可逆的な薬物作用の場合はそうではない。DNA損傷はその性質上不可逆的だが、たとえ細胞のDNA修復システムによってDNA損傷の一部がうまく修復されるとしてもである。カチオン性脂質によって誘導される活性酸素がこのようなDNA損傷を引き起こすことから、これらの脂質は、それ自体の蓄積とは関係なく、累積毒性という問題を引き起こすと考えなければならない。
5.3.3.3 実験中または承認済みのLNP薬剤やワクチンの毒性
LNPベースの薬剤の毒性に関して最も好意的な報告は、通常の承認プロセスを経た薬剤に関するものである。
この薬剤(パティシラン、オンパトロ®)に含まれるRNAはmRNAではなく、外来抗原の発現を誘導するのではなく、むしろ「自己」のタンパク質の発現を抑える(「沈黙させる」)ように設計されている。このタンパク質であるトランスサイレトリンは肝臓で産生されるため、パティシランに含まれる脂質ナノ粒子は、この臓器に集積するように最適化されている6。
この薬に使われているLNPの組成は、モデルナ社やファイザー社のCOVID-19ワクチンに使われているものとかなり似ている。しかし、パティシランはCOVID-19ワクチンよりもはるかに高用量で使用されていることに注意しなければならない。したがって、その安全性に関する一様に良好な評価[218-220]は非常に注目に値する。この表向き肯定的な経験を考慮すると、肝臓に関する別の代謝性疾患、すなわちクリグラー・ナジャール症候群を治療する試みにおいて、なぜ同じ脂質ナノ粒子システムがモデルナ社によって使用されなかったのか疑問に思うかもしれない。動物におけるこの治療法の「概念実証」研究は発表されているが[221]、乗り越えられない毒性問題が、同社がこの取り組みを断念し、代わりにワクチンに切り替える決断をした理由であると伝えられている[222, 223]。
ファイザーとモデルナのCOVID-19ワクチンに含まれるカチオン性脂質の毒性に関する前臨床データは、ヒトにおける毒性の程度について明確な結論を出すには、あまりにもまばらである。しかし、モデルナワクチンのEMA報告書に簡潔にまとめられている、測定可能なレベルのDNA損傷を指摘するいくつかの結果については、第6章で議論する。
5.4 付録:COVID-19 mRNAワクチンの製造品質が基準以下である証拠
医薬品やワクチンと人体との相互作用の研究では、製品の品質が非常に安定していることが暗黙の前提であり、異なる製造ロットで得られたデータは確かに比較可能である。しかし、COVID-19 mRNAワクチンでは、この仮定が崩れることが証明されている。
6トランサイレトリンは血漿中を循環し、主要な甲状腺ホルモン(サイロキシン、T4)を輸送する。まれに、トランスサイレトリン分子が異常に折り畳まれて沈着物(「アミロイド」)を形成し、心臓や末梢神経の機能を損傷する患者がいる。パチシランを用いてこのタンパク質の発現を抑えることで、臨床転帰が改善すると報告されている[218]。
5.4.1 mRNAワクチンから検出される汚染物質
少なくとも2種類の汚染、すなわち金属粒子とプラスミドDNAが明確に記録されている。
5.4.1.1 金属粒子
上級研究者グループによる徹底的な顕微鏡および分光学的調査により、ファイザーとモデルナの両mRNAワクチンに金属粒子が含まれている明確な証拠が得られた。これらは遷移金属(コバルト、鉄、クロム、チタン)、希土類金属(セリウム、ガドリニウム)、その他様々な元素で構成されている[224]。これらの粒子の大きさは1 µmから0.1 mmで、肉眼で見える大きさのものもある。
このような粒子は、ワクチン製造に使用される装置のポンプやバルブからの研磨屑である可能性がある。通常、このような破片は最終ろ過工程で医薬品から除去される。最終製品であるワクチンにこのような異物が混入していることは、製造に手抜きがあったことを示している。これらの汚染物質による健康への影響については、まだ解明されていない。
5.4.1.2 プラスミドDNA
ワクチンに含まれるmRNAは、いわゆるプラスミド(細菌細胞内で複製可能なDNA分子)の一部であるDNAを鋳型として作られる。この鋳型DNAは、mRNAが脂質と結合してmRNA/脂質ナノ粒子になる前に、反応混合物から完全に除去されなければならない。しかし、今回もまた手抜きが行われたようで、少なくともいくつかのワクチンバッチは驚くほど多量のプラスミドDNAで汚染されていた[225]。起こりうる結果についてはセクション6.3で議論する。
5.4.1.3 その他の汚染物質
ワクチン中のその他の汚染物質、特にグラフェンや酸化グラフェンの存在が指摘されている。しかし、これに関する確かな実験的証拠は得られていない。
5.4.1.4 脂質不純物
mRNAワクチンのナノ粒子には2種類の非天然脂質が含まれていることは前述した(セクション5.1参照)。2つのメーカーは多少異なる合成脂質を採用しているが、これらの脂質には共通して、未知の量の未知の不純物が含まれている。欧州医薬品庁(EMA)は、ファイザーのワクチンに関する評価報告書の中で、ファイザーのカチオン性脂質ALC-0315 [60, p.24]に関して、次のように述べている:
脂質関連の不純物は、最近製造されたいくつかの完成品バッチで観察されており、ALC-0315脂質のバッチと相関している。ALC-0315の賦形剤の品質は、入手可能なデータに基づき、最終製品に含まれる特定の不純物をさらに評価することを条件に、許容可能であると考えられる。
同様に、モデルナワクチンに関するEMAの報告書は次のように述べている[58, p.23]:
特定および非特定の不純物に関する数値限界は、承認後のPEG2000-DMG規格に含まれる予定である。現在の不純物の報告は容認できない。「含有量不明」で報告されている不純物の特性データは、承認後に提供されるべきである。
モデルナのカチオン性脂質SM-102に関して、同報告書は次のようにコメントしている:
CQA(重要品質特性)、CPP(管理工程パラメータ)、SM-102の製造に使用される材料の重要な特性が欠落している。
このような脂質不純物の性質や量が正確に決定される前に、EMAや他の規制当局が「積極的に」承認を与えたことは、非常に驚くべきことである。
5.4.1.5 意味合い
既知の汚染物質はすべて、メーカーや規制当局とは無関係の研究者によって発見されたものであることに注意しなければならない。メーカーも規制当局も重大な過失で行動したという結論は避けられない。この推論は、EMAや他の規制当局が、両メーカーの新規脂質に関する品質情報の欠如に対する懸念を一蹴し、承認に踏み切った無謀なやり方によって補強されている。
5.4.2 有害事象報告のバッチ間ばらつき
コンタミネーションの検出は別として、COVID-19 mRNAワクチンの製造基準が一貫していないことを証明する第二の証拠は、製造バッチ間で報告された有害事象の数に大きなばらつきがあることである。これは図59Aでファイザーのワクチンについて明確に示されている。図59Aはデンマークからの有害事象報告を示しており、そのほとんどが2021年からのものである[226]。バッチは、それぞれ有害事象発生率が非常に高い、中程度、低い3つのクラスターに分けることができる。
ワクチンのロットは、ロット番号の英数字の並びである。
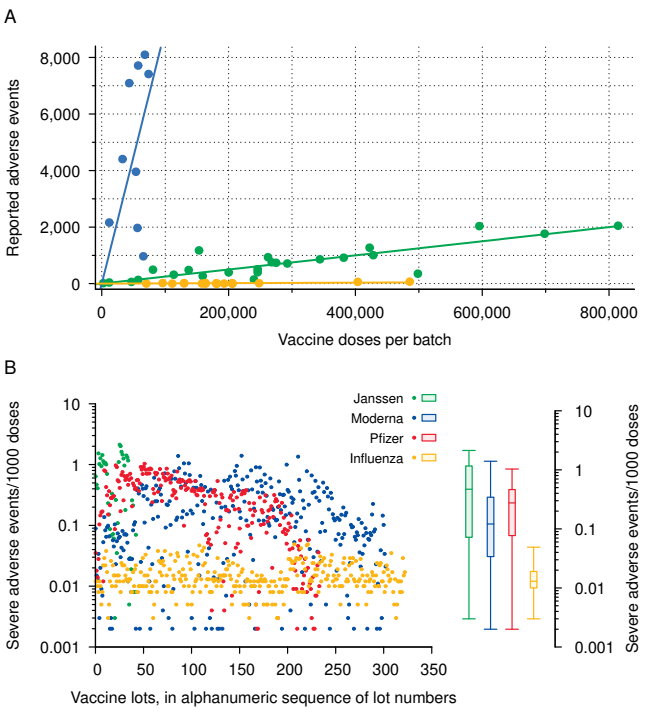
図59 有害事象発生率のバッチ間変動
A:Pfizer- BioNTech mRNA ワクチン接種後に報告された有害事象数のバッチ間変動。投与量および有害事象の報告はデンマークのみに関連する。報告期間: 報告期間:2020年12月27日~2022年1月11日。各点は1つのワクチンバッチを表す。バッチは3つのクラスターに分類され、それぞれ異なる色と別々の線形回帰線を用いて識別されている。Schmelingら[226]の図1の再掲である。B:VAERSに報告された重篤な有害事象をバッチ別に、3種類のCOVID-19ワクチンと数種類のブランドのインフルエンザワクチンについて示す。データは合計約600のCOVID-19ワクチンバッチと323のインフルエンザワクチンバッチからなり、後者の報告は2019年に提出された。Y軸が対数になっていることに注意されたい。箱ひげ図では、各ワクチンの箱は中央値と上下の四分位数を示し、ひげは全データ範囲にわたっている。Sasha Latypova、Craig Paardekooper、Jason Morphettの研究に基づく。
有害事象報告数にバッチ間で大きなばらつきがあることは、VAERSシステムのデータからも明らかであり、米国で使用された3種類の遺伝子組換えCOVID-19ワクチンすべてについて同様である。図59Bは、これらのワクチンのバッチごとの重篤な有害事象報告の発生率をインフルエンザワクチンと比較したものである。3種類のCOVID-19ワクチンの発生率は平均して非常に高いだけでなく、インフルエンザワクチンに比べて変動が大きい。この高いばらつきは、製品の品質がバッチ間でかなり一貫していないことを示している。
6. mRNAワクチンの遺伝毒性
遺伝毒性とは、遺伝子、つまりDNAに対する有害な損傷を意味する。生殖細胞(卵巣の卵母細胞や精巣の精子産生細胞など)に影響を及ぼすこともあれば、体細胞(生殖細胞以外の全身の細胞)に影響を及ぼすこともある。遺伝毒性は治療目的で用いられることもある。電離放射線や、シクロホスファミドやシスプラチンなどの細胞毒性抗がん剤の効果は、ほとんどDNA損傷によるものである。このような治療の目的は、がん細胞をアポトーシスに追い込むことである。アポトーシスはがん細胞だけにとどまらず、例えば骨髄や毛根の健康な細胞にも影響を及ぼし、あらゆる種類の血液細胞の減少や脱毛を引き起こす。生存しているがん細胞に突然変異が誘発されると、長期的にはがんの増殖が促進され、以前は健康だった細胞に突然変異が誘発されると、新たな二次的悪性腫瘍が発生する可能性がある。低強度であれば、DNA損傷は完全な細胞死を引き起こさないため、急性の臨床症状はないが、それでも変異のリスク、つまりがんを誘発するリスクはある。
mRNAワクチンは、細胞内に取り込まれた後、3つの異なる経路で遺伝毒性を引き起こす可能性がある:
- 1. 脂質ナノ粒子に含まれるカチオン性脂質が活性酸素種(ROS)の形成を誘導し、DNAと反応する可能性がある;
- 2. mRNAそのものがDNAへの逆転写を受け、染色体DNAに挿入される。その結果、細胞遺伝子が破壊されたり、制御不能になったりする可能性がある;
- 3. mRNAワクチンにコンタミネーションとして存在するDNAが、染色体DNAにも挿入される可能性がある。
最初の2つのメカニズムは技術に内在するものであり、現在の知識では避けることはできないと考えられるが、3番目のメカニズムは原則的に避けることができるはずである。しかしながら、最近のデータによると、少なくともファイザーとモデルナのmRNAワク チンの製造ロットによっては、高レベルの汚染DNAが存在している(セクション6.3参照)。
6.1 合成カチオン性脂質の遺伝毒性
我々はセクション5.3.3で、カチオン性脂質が活性酸素種(ROS)を誘発し、それがDNA損傷を 引き起こす可能性があることを述べた。このような薬剤の使用が完全に安全である閾値が存在するのだろうか。この疑問に答える直接的な証拠はない。しかし、電離放射線の例は、その影響が同様に活性酸素によって媒介されることから、安全な閾値が存在しないことを示唆している。X線診断に使われるような低線量の放射線を出生前に浴びると、小児がんや白血病の発生率が測定可能なほど上昇する。1956年にStewartらによって初めて報告され[227]1、当初は懐疑的な見方が広まったが、後に英国[228]と米国[229]で行われた2つの独立した大規模研究で確認された。リスクの正確な大きさについてはまだ議論が続いているが、一般的には、子宮外生殖で最も感受性の高い時期である生後10年間と同様に高いと考えられている [230]。電離放射線の線量調整発がんリスクは、年齢が高くなるにつれて減少するとはいえ、ゼロになるわけではない。カチオン性脂質を含む化学物質によるDNA損傷についても、同じことが予想される。
しかし、COVID-19 mRNAワクチンに含まれる脂質によるDNA損傷の実際の証拠はあるのだろうか?ファイザー/バイオエンテックワクチンのEMA評価報告書[60]によると、このメーカーは、自社の混合脂質の潜在的な細胞毒性に関する実験データを提供していない(そして、EMAはそれを放置した)。これとは対照的に、モデナはEMAへの申請において、動物実験によるデータをいくつか提出している。これらのデータは、多色性を示す赤血球(RBC)と小核を持つ赤血球に関するものであった。
6.1.1 多色性赤血球の増加
多色性赤血球とは、骨髄内で分化を終えたばかりの赤血球で、成熟の最終段階として細胞核を排出したものである。この段階では、細胞質内にリボソームRNAが残っているため、ギムザ染色では赤ではなく青っぽく見える。
1当時の画像診断に使用されたX線線量は、現在使用されているものよりもかなり高かったが、それでも当時や現在の治療照射に必要な線量よりもはるかに低かった。
多色性を示す赤血球の割合の変化は、赤血球の成熟速度の変化を示している。遺伝毒性物質はこのパラメーターを低下させるか [231] 、増加させる [232] 。同社独自のカチオン性脂質であるSM-102を含むモデルワクチンに暴露された動物において、Modernaは多色性赤血球のレベルが有意に減少していることを発見した [58, p. 50]。しかし、この効果は雄ラットでのみ観察された。この予想外のジェンダー差は、Modernaの研究の統計的検出力に疑問を投げかけるものである。
6.1.2 小核の増加
モデルmRNAは異なるが、SM-102を含む同じ脂質混合物を用いて、Modernaは次のことを発見した[58, p.50]。
小核化赤血球が統計的に有意に増加した。
…男女ともである。
いわゆる小核とは、赤血球前駆細胞内の染色体損傷によって生じた染色体断片のことで、主核が排出される際に細胞質内に取り残されたものである[232, 233]。小核を持つ赤血球を数えることは、in vivoでの遺伝毒性を検出するための簡単で広く用いられている検査である [233]。
Modernaワクチンに関するEMAの報告書は、同社が提出した研究を引用し、観察された小核を持つ赤血球の増加は、遺伝毒性によるものではなく、むしろこれらの細胞の血流からのクリアランスが阻害されたことによるものではないかと提案している。このクリアランスの阻害は、傷ついた赤血球や期限切れの赤血球を分解する臓器である脾臓に対するワクチンの毒性のせいだという。しかし、このかなり図々しい主張の証拠は示されていない。EMAの報告書にはさらに、雄ラットの最高用量投与群で、最終投与48時間後に分子開始事象の強い増加が観察された、と書かれている。
観察された事象の正確な性質についての詳細は記載されていないが、「分子開始事象の増加」という表現は、単にクリアランスが減少したのではなく、遺伝的に損傷を受けた細胞の形成率が実際に上昇したことを明らかに示唆している。
6.1.3 結論 Moderna社の実験所見に関する利用可能な記述はかなり不完全であるが、同社のCOVID-19ワクチンに含まれるSM-102脂質が実際にDNA損傷を引き起こすことを強く示唆している
このことは、例えばInglutら[234]がレビューしている、同様のカチオン性脂質を含むリポソームに関連した遺伝毒性に関する先行研究と一致している。反対の証拠がない限り、ファイザーの構造的に類似したALC-0315脂質も同じであると考えなければならない。
遺伝毒性はどのような形であれ、どのような投与量であれ、癌や白血病の一定のリスクを意味することを再度強調しておく。したがって、COVIDの “ブースターショット “を頻繁に繰り返したり、mRNA技術を他の病原体や非感染性疾患に対するワクチンにまで拡大することは、公衆衛生上の重大なリスクを想起させる。
6.2 ワクチンmRNA配列のDNAへの逆転写
mRNAワクチンがもたらす遺伝毒性の第二の主要リスクは、mRNA成分そのものに起因する。COVID-19のmRNAワクチンの緊急使用承認に関連して、このリスクはEMAや他の規制当局によって全く無視された。しかし、この軽率なアプローチが科学的に不当であったことは、以下で明らかになる。
6.2.1 組み換えRNAの遺伝毒性リスクは、時代遅れの科学に基づいて否定された
ファイザーのワクチンに関するEMAの評価報告書には、次のような簡潔な記述がある[60, p.50]:
遺伝毒性試験は行われていない。ワクチン製剤の成分は脂質とRNAであり、遺伝毒性の可能性は期待できないので、これは容認できる。
どうやらEMAの専門家は、一般的にRNAは宿主細胞ゲノムの完全性に影響を与えないという印象を持っていたようだ。この規則の最初の例外は、1970年にがん原性レトロウイルスが逆転写酵素活性を持つことが発見されて以来知られている。この酵素はウイルスRNAゲノムをDNAにコピーし、宿主細胞ゲノムに挿入する[235, 236]。真核細胞そのものが同様の逆転写酵素活性を持つことがわかったのは、それから数年後のことであったが [237]、2020年の時点ではほとんど目新しいこととは考えられなかった。
6.2.2 細胞内逆転写酵素活性によるRNAウイルスのゲノム挿入
レトロウイルスではないRNAウイルスに由来する哺乳類DNA配列の染色体挿入を実証した最初の研究は、1997年にKlenermanらによって報告された[238]。問題のウイルスは、マウスに感染するリンパ球性絨毛膜炎ウイルスであった。このウイルス自身は逆転写酵素をコードしていないので、観察されたウイルスRNAゲノムの部分的DNAコピーは、細胞内酵素による逆転写によって作られたものでなければならなかった。この分子メカニズムは、後に同じ研究室の科学者によって詳細に解明された[239]。その結果、レトロトランスポゾンがウイルスRNAの逆転写とDNAコピーの細胞ゲノムへの挿入の両方を成し遂げていることが判明した。
6.2.3 細胞レトロトランスポゾンの生物学的役割 レトロトランスポゾンは細胞ゲノムの移動性遺伝要素であり、自身のコピーをさらに生成するための完全なタンパク質装置をコードしている
ほとんどの場合、DNAにコピーされて挿入されるのはレトロトランスポゾンのmRNAそのものである。しかし、レトロトランスポゾンタンパク質は時折、鋳型の入れ替わりを起こすことがある。つまり、自分自身のmRNA鋳型を失い、代わりに別のRNA分子を拾い、それがDNAへの逆転写を受けて細胞ゲノムに挿入されるのである(図6.1)。
レトロトランスポゾンにはいくつかの相同ファミリーがあり、その中でヒトにおいて最も活発で重要なものはLINE-1ファミリーである[240- 242]。ゲノム内の新しい挿入の位置はほとんどランダムであるため [243]、生物学的な結果は非常に多様である。挿入が機能的遺伝子内で起こった場合、その遺伝子は破壊されるかもしれない。挿入が機能的遺伝子の近傍で起こった場合、後者の活性は上方または下方へ制御されるかもしれない(セクション6.4.2参照)。影響を受けた遺伝子の特定の役割に応じて、細胞の挙動が変化し、癌やその他の疾病が生じる可能性がある [244, 245]。
レトロトランスポゾンの活性は私たちの体細胞の種類や機能状態によって異なるが、分裂している細胞でも分裂していない細胞でも活性があり [246]、また卵母細胞でも活性があることは注目に値する [247]。したがって、ウイルスやその他の外来RNAがレトロトランスポゾンによって体細胞のゲノムに挿入され、それによって癌が発生する可能性があるだけでなく、生殖細胞にも挿入され、ヒト集団内で増殖する可能性がある。
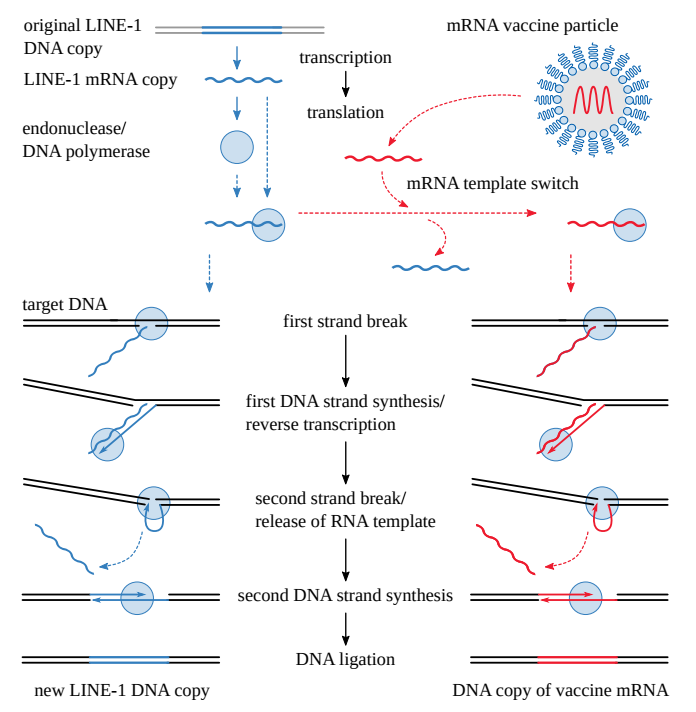
図6.1 LINE-1レトロトランスポゾンがワクチンmRNAをDNAにコピーし、宿主細胞ゲノムに挿入する過程
このプロセスは、既存のLINE-1インスタンスがmRNAコピーに転写されることから始まる。このmRNAが翻訳されると2つのタンパク質が生成されるが、そのうちの1つはエンドヌクレアーゼ/DNAポリメラーゼの2つの機能を持つもので、DNAを切断することも合成することもできる。この分子はLINE-1 mRNAに結合し、新しいDNA標的部位を見つける。最初のDNA鎖を切断する。そして逆転写によって、mRNAのDNAコピーで自由末端の一方を延長する。このステップが完了すると、標的DNAの2本目の鎖が切断され、新しいLINE-1のコピーの2本目の鎖が1本目の鎖に沿って合成される。このプロセスは、ワクチンmRNAのような別のmRNA分子によって早い段階で簒奪され、LINE-1 mRNAをエンドヌクレアーゼ/ポリメラーゼから外すことができる。このようなテンプレートスイッチにより、代用RNAのDNAコピーが挿入されることになる。
6.2.4 非レトロウイルスRNAウイルス由来のゲノムDNA配列
レトロウイルス以外の多くのRNAウイルスが、哺乳類や他の脊椎動物のゲノムに見られる部分的なDNAコピーを生み出している[248-251]。真菌類、植物、原生動物などの他の真核生物でも同様の発見がなされている[252-254]。これらのウイルス由来の配列はすべて、何らかのレトロトランスポジション機構によって生じたに違いない。このことは、レトロトランスポジションがこれらすべての種の生殖細胞で起こりうるという上記の点を明らかに立証している。
ここで引用した観察はすべてRNAウイルス由来の配列に関するものであるが、LINE-1によるレトロトランスポジションは配列特異的ではなく[255]、他のRNA配列、例えばPfizerやModernaのmRNAワクチンの配列が同じメカニズムに従う可能性を排除する理由はなかった。
6.2.5 感染細胞におけるSARS-CoV-2配列のゲノム挿入
すでに2021年に、SARS-CoV-2ウイルスのゲノムRNAの部分DNAコピーが、細胞培養でもウイルス感染患者でも、感染細胞の細胞DNAに挿入できることが証明されている[256]。これはmRNAワクチンとは直接関係ないとはいえ、SARS-CoV-2由来のRNA配列が一般的なメカニズムから除外されていないことを示している。さらに、この研究は、挿入がLINE-1レトロトランスポゾンによって媒介されていることを示した。
6.2.6 ワクチン暴露細胞におけるスパイク遺伝子DNAコピーの検出
より重要で、より直接的な関連性を持つのは、Aldénら[257]による、ファイザーのワクチンに暴露したヒト由来の肝細胞株に関する最近の研究である。著者らはこれらの細胞内でスパイクタンパク質遺伝子のDNAコピーを検出し(図6.2参照)、これを逆転写の証拠とした。この最初の研究で報告された結果は、この明らかな逆転写現象にLINE-1が関与していることを示唆しているが、厳密な証明にはなっていない。しかし、ヒトゲノム内の活性型レトロトランスポゾンは全て、いわゆる非LTRクラス[258]に属し、図6.1にLINE-1について示したように、RNAのDNAへの逆転写はDNAへの挿入と表裏一体の関係にある。したがって、ワクチン配列のDNAコピーが本当にLINE-1によって生成されたのかどうか、絶対的な確証を得ることはできないが、この疑問は決定的なものではない。
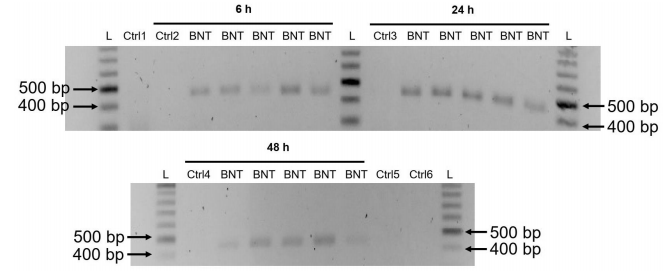
図6.2 ヒト肝細胞株の細胞DNA内にファイザーワクチンがコードするスパイクタンパク質遺伝子のコピーが検出された([257]の図5から引用)。細胞は示された時間だけワクチンに暴露された。その後、細胞DNAを単離し、長さ444塩基対(bp)の断片のPCR増幅によってワクチンmRNAのDNAコピーを検出した。BNT」と表示されたサンプルはすべてワクチンで処理されていた。それぞれのサンプルは、DNA断片長標準(’L’)との比較から明らかなように、期待される長さのPCR産物を示している。Ctrl n’の付いたサンプルはコントロールである: Ctrl 1-4はワクチンとインキュベートしていない細胞からのDNA、Ctrl 5はワクチン処理した細胞からのRNA(DNAではない)、Ctrl 6は同じであるがRNAseで追加処理したものである。予想通り、いずれのコントロール・サンプルからもPCR産物は得られなかった。
6.2.7 スパイクタンパク質をコードする細胞内DNAの検出は、レトロトランスポジションと直接トランスフェクションを区別しない
それは、細胞内で検出されたDNAコピーがワクチン中に含まれており、細胞内でのDNAコピーの出現は、単にそのような既存のDNAコピーの細胞内取り込み(「トランスフェクション」)を反映したものであるという可能性を考慮していないことである。アルデンの研究で使用されたワクチンバッチが本当にそのような汚染DNAを含んでいたとすれば、その細胞内への取り込みはmRNAと同様に脂質ナノ粒子によって促進された可能性が高い。最近報告された知見は、この可能性を真剣に考慮しなければならないことを示している(セクション6.3参照)。
6.2.8 結論
これまでに報告されたCOVID- 19 mRNAワクチンの知見から、ワクチンmRNAの逆転写とin vivoでのゲノム挿入が確実に証明されたわけではないが、このリスクを手放しで否定できないことを示す十分な状況証拠がある。後者はまた、他の病原微生物に対する将来的なmRNAワクチンにも当てはまる。
6.3 ファイザーとモデナのmRNAワクチンにおけるプラスミドDNAの混入
mRNAワクチンにとって、mRNAそのものとカチオン性脂質は必要な成分であるが、そのようなワクチ ンには汚染DNAがないことが理想的である。しかし、ワクチンmRNAの大量生産にはDNAが必要である。ファイザーとModernaのCOVID- 19ワクチンでは、スパイク蛋白遺伝子のDNAコピーがmRNAの酵素合成の鋳型となり、大腸菌ファージT7由来のRNAポリメラーゼによって合成される。このDNAコピーはプラスミド、すなわち細菌細胞内で持続的に増殖できるリング状のDNA分子上に運ばれる。大量のプラスミドDNAは、問題のプラスミドを含むバクテリアの液体培養物から簡単に得ることができる。
DNAはRNAと化学的によく似ているため、mRNAを封じ込めた脂質混合物はDNA分子も同じように封じ込める。したがって、mRNAワクチンの製造に使われた鋳型DNAによる汚染を防ぐためには、mRNAを脂質と結合させる前にDNAを除去する必要がある。これは原理的には可能であるが、ファイザー社とモデルナ社が用いた精製方法は非常に信頼性に欠けるものであったようだ。注目すべきことに、EMAは両社が精製ステップの有効性を十分に証明していないと批判した[58, 60]が、それにもかかわらず、この状況を改善するよう強制することなく、両社に認可を与えるよう勧告した。さらに、いったんワクチン製造が開始されると、mRNAワクチン中の残存DNA量に関する工程品質管理データは、製造業者からEMAやその他の規制当局に要求されることも提出されることもなかったか、少なくともそのようなデータは公開されていないようである。
以上のことから、mRNAワクチンのDNA含有量が、EMAが設定した制限値、すなわち「DNAはワクチンに含まれる全核酸の3030分の1以下であるべき」という制限値を超えていたとしても、それほど驚かないかもしれない。しかし、一部のワクチンバッチに含まれる過剰なDNAの量には驚かされる。有名な分子生物学者でありDNA配列決定法のパイオニアであるケビン・マッカーナンは、いくつかのバッチが20-35%もの残存プラスミドDNAで汚染されていることを発見した[225]。
この汚染がもたらす生物学的・医学的リスクについては、別のところで詳しく論じられている[259]。それらは、mRNA自体の逆転写と挿入が意味するものと本質的に同じである。このコンタミネーションは原理的に回避可能なはずであり、他のウイルスや病原性微生物に対する将来のmRNAワクチンでは、実際に回避できる可能性があることを再度強調しておく。しかし、ファイザーとモデナの両製品にこのコンタミネーションが存在することは、現在のところ、この問題が大規模生産に関して効果的に解決されていないことを示唆している。
6.4 非自己遺伝子のDNAコピーがもたらす既知の、そしてもっともらしいリスク
上記6.2節と6.3節は、mRNAワクチン粒子を取り込んだ細胞が、mRNAそのものだけでなく、ワクチンにコードされた非自己遺伝子のDNAコピー(COVID-19 mRNAワクチンの場合はスパイクタンパク質遺伝子を意味する)とも闘わなければならない可能性があることを示唆している。これまで見てきたように、このようなDNAコピーは細胞内での逆転写によって生じるか、ワクチ ン自体にプロセス関連の汚染としてすでに含まれている可能性がある。
6.4.1 非自己遺伝子の染色体への組み込み
mRNAのコピーがDNAにコピーされ、同時に細胞の染色体DNAに挿入されるメカニズムについては、6.2.3節で述べた。
6.2.3. プラスミドDNAも染色体DNAに挿入されることがあり[260]、この効果はトランスジェニック細胞や生物の作製に広く利用されてきた。しかし、より一般的には、体細胞に取り込まれたプラスミドDNAは、その細胞内で独立して存続し、細胞が分裂すると失われることが多い。とはいえ、非常に多くの人々がmRNAワクチンの接種を受けており、そのワクチンに は相当量のプラスミドDNAが混入していることが明らかであることから、少なくともいくつかのケー スでは挿入現象が起きていると推定される(下記6.4.2.3項も参照)。
6.4.2 DNA挿入の生物学的結果
LINE-1[243]、そしておそらく他のレトロトランスポゾンでも同様に、DNAの挿入はランダムな場所で起こるが、不活性遺伝子のDNAはヒストンタンパク質との複合体に密に詰め込まれ、アクセスが悪くなるため、転写活性のある遺伝子内かその近傍で優先的に起こる。プラスミドDNAの挿入も、ランダムな場所で起こるようである[261, 262]。このようなランダム挿入は、宿主細胞のゲノムに異なる機能的効果をもたらす可能性がある。
6.4.2.1 遺伝子の不活性化
挿入は遺伝子内で起こり、その遺伝子を破壊する可能性がある。これにより、重要な細胞内遺伝子産物(すなわち、タンパク質)が失われ、その結果、癌を含む疾患の発症につながる可能性がある[244, 245]。挿入はまた、大きな遺伝子断片の欠失を伴うこともある [263]。
6.4.2.2 遺伝子の制御
転写およびエピジェネティックな調節機構が影響を受け、タンパク質発現 レベルを上方または下方に調節し、予測できない望ましくない結果を もたらす可能性がある。間接的な制御作用は、DNAメチル化の変化を介することで、他の染色体上にある離れた遺伝子にも影響を及ぼす可能性がある [264]。
6.4.2.3 がん遺伝子の活性化
これは前述した点の特殊なケースであるが、別に強調すべき重要な点である。SCID-X1(重症複合免疫不全症)の小児の遺伝的治療のためのレトロウイルスベクターを用いた臨床試験において、DNAの統合とがん促進遺伝子(がん遺伝子)の活性化による悪性腫瘍の発生が証明されている [265]。これらの悪性腫瘍は通常、治療終了後数年経ってから顕在化する [266] 。したがって、有効なベネフィット・リスク分析のためには、前臨床試験でも臨床試験でも、染色体統合による遺伝毒性作用の可能性を長期にわたって監視することが絶対不可欠である。
レトロウイルスベクターは、宿主細胞ゲノムに効率よく組み込まれるように特に設計されている。なぜなら、そのような安定した組み込みのみが、問題の遺伝子欠損を永久に修復するからである。プラスミドベクターの場合、挿入率は通常数桁低くなる。とはいえ、プラスミドDNAの染色体挿入はin vivoで証明されている[262]。後者の研究では、プラスミドDNAの筋肉内注射に続いてエレクトロポレーションが行われた。エレクトロポレーションは、注入されたDNAの細胞内への取り込みを、「裸の」DNAのみの注入に比べて増加させたが、mRNAワクチンに含まれる脂質ナノ粒子に比べると、この点でははるかに効果が低かったと思われる。したがって、生体内、つまり私たち自身の体内の細胞内で、汚染されたプラスミドDNAの染色体統合がある程度進むことを期待しなければならない。
6.4.3 プラスミドDNAは細胞培養を不死化する可能性がある
健康なヒトや動物の臓器から細胞を分離し、細胞培養で増殖させると、細胞は限られた世代数だけ分裂し、その後死滅する。対照的に、悪性腫瘍や白血病に由来する細胞は無限に増殖できる。健康な体細胞をがん化させるのと同様の変化が培養細胞にも起こる可能性があり、それによって不死化し、典型的には由来組織に特徴的な特徴を失う。この形質転換は、がん原性ウイルスに感染させることで最も容易に誘導される。しかしながら、特異的な癌化活性を持たないプラスミドでも起こることが報告されている [267, 268]。これらの症例は、増殖制御に関与する細胞遺伝子の破壊や調節異常から生じたに違いない。このような破壊の根底にあるものと類似した分子現象は、ワクチン由来のDNAが私たち自身の体細胞内で起こることも予想される。従って、結論として、ワクチン接種を受けた集団が十分に多い場合には、ワクチン由来のDNAが染色体DNAに挿入されることによる悪性腫瘍のリスクを真剣に考慮しなければならない。
6.4.3.1 挿入された遺伝子の発現
スパイクタンパク質遺伝子が宿主細胞に組み込まれると、その遺伝子が恒常的に発現する可能性がある。その結果については別途後述する。
6.4.3.2 生殖細胞系列への組み込み
ファイザー社自身の動物データから、卵巣へのワクチン蓄積のレベルが高いことがわかった(セクション5.2.1参照)。さらに、LINE-1や他のレトロトランスポゾンは活性があり、ヒトの卵子においてゲノム挿入現象を引き起こす[247]。これらの知見を総合すると、mRNA遺伝子配列は卵子のDNAに組み込まれ、ヒト生殖細胞系列に組み込まれる可能性がある。ワクチンに含まれる混入DNA配列についても、同様の可能性がある。セクション5.2.1で議論した動物実験では、精巣へのワクチンの蓄積は卵巣よりも有意に少なかったが、男性の生殖細胞への挿入も否定できない。
ワクチン接種を受けた人の生殖系列細胞がトランスジェニック化された場合、トランスジェニック児を生むリスクはその人だけにとどまらず、その人の現在の配偶者や将来の配偶者も共有することになる。事実上、将来の親の世代全体がこのリスクにさらされることになる。
6.4.4 外来抗原の持続的発現
ワクチン mRNA だけでコードされた抗原の発現を促進するには十分であるが、この発現は短期間であるべきである。In-vitro のデータによると、メチルシュードウリジンによる修飾は、mRNA が持続している間に産生されるコード化抗原の量を大幅に増加させるにもかかわらず、その発現期間を有意には延長しないことが示唆されている[56, 57]。
余分な組換えDNAを含むDNAは、mRNAよりもはるかに寿命が長い。凝固第IX因子(血漿蛋白質)を発現するように設計されたプラスミドは、実験動物の肝細胞内で安定したレベルで1.5年まで持続することが分かっている[269, 270]。注目すべきは、この発現にはプラスミドが細胞DNAに組み込まれる必要はないということである。プラスミドは、細胞分裂が誘導されると急速に失われる可能性はあるが、細胞分裂が起こらない限り細胞内に持続する傾向がある[271]。
現在使用されているCOVID-19 mRNAワクチンでプラスミドによる発現が起こったと仮定する理由はあるのだろうか?これらのワクチンの製造に使用されているin vitro転写は、T7 RNAポリメラーゼを用いて行われていることは先に述べた。このポリメラーゼが、ポリメラーゼによって認識され活性化されるDNA配列モチーフであるT7プロモーターと結合すると、転写が開始される。我々の体細胞では、mRNA合成は別の酵素(RNAポリメラーゼII)によって行われる。しかし、T7プロモーターもこの細胞内酵素と結合し、これが哺乳類細胞内で転写を引き起こすことが実験的に確認されている [272]。
もう一つの証拠は、ワクチン接種後に観察されるスパイクタンパク質の発現期間に関するものである。ワクチン接種者を対象とした複数の研究から明らかなように、スパイクタンパク質自体もそれをコードする核酸も、注射後数週間から数カ月にわたって血流中やさまざまな臓器で検出される(セクション5.2.3.1参照)。このin vitroとin vivoの研究の食い違いを理解することは、これまで困難であった。プラスミドDNAが長期間持続し、そこからスパイクタンパク質が発現することは、これらの所見をもっともらしく説明するものである。
長期発現は、染色体挿入されたプラスミド由来のDNAでも可能である。mRNAの逆転写と染色体挿入も、持続的発現をもたらすかもしれない。しかし、mRNAにはT7プロモーターや、DNAコピーの転写を促進する他のプロモーターのコピーが含まれていないことに注意されたい。したがってこの場合、プロモーターは挿入された遺伝子の近傍の染色体DNAから供給されなければならない。これは不可能ではないが、ワクチンに含まれるコンタミDNAコピーからの発現に比べると、実際に起こる可能性は低いと思われる。第4章では、スパイクタンパク質の発現が、問題の細胞や組織に対する破壊的な自己免疫様炎症と相関することを見てきた。したがって、遺伝子のDNAコピーによるスパイクタンパク質の発現が長期化すると、そのような炎症の持続時間が延長され、累積的な破壊的影響が増大することになる。
7. COVID-19 mRNAワクチンの有害事象の疫学
Margot DesBois, B.A.およびBrian S. Hooker, Ph.D.1
7.1 はじめに
FDAは2020年12月にSARS-CoV-2 mRNAワクチンの緊急使用許可を初めて承認した[273]。それから2022年12月までの間に、mRNA COVID-19ワクチンは米国で6億5,000万回以上、世界中で130億回近く接種された[274]。このワクチン接種プログラムの展開以来、個人や医療従事者は、新規のファイザー・バイオNTechおよびModerna mRNA COVID-19ワクチンの接種後に数百万件の有害事象を報告している。これらのワクチンは事実上すべての子供と成人に安全であると政府保健機関が繰り返し主張しているにもかかわらず、多くの疫学調査により、米国および世界中でこれらのワクチン接種後に重篤な健康問題の発生率が著しく増加していることが明らかになった。この査読を受けた研究には、臨床試験データ、受動的サーベイランスデータ、前向きおよび後ろ向きコホートデータの解析が含まれ、その多くはワクチン接種群と非接種群を直接比較している。研究集団には、無作為化試験参加者、病院患者、政府医療登録者、および市、医療制度、国、および国際的データベースからの一般市民ボランティアが含まれる。
7.2 一般的有害事象、重篤な有害事象、死亡、入院、生命を脅かす事象
7.2.1 臨床試験データの解析
複数の研究グループが、ファイザーBNT162b2およびモデナmRNA-1273 SARS-CoV-2両mRNAワクチンの無作為化プラセボ対照試験のデータを解析し、ワクチン接種群の有害事象発生率がワクチン未接種群より有意に高いことを明らかにした。
1Margot DesBoisはChildren’s Health Defenseの科学フェローである。Brian Hookerはシンプソン大学の生物学教授で、Children’s Health Defenseの最高科学責任者である。
Chengらは、異なるCOVID-19ワクチンに関する第III相臨床試験データを評価するために、複数の文献を検討した[275]。8つの研究、7つのCOVID-19ワクチン、150,000人以上の被験者を分析した結果、mRNAワクチンはワクチン未接種の対照と比較して有害事象のリスクが最も高く、1回目と2回目の接種後にそれぞれ1.83倍(95%信頼区間1.80-1.86)、2.16倍(95%信頼区間2.11-2.20)有害事象のリスクが増加することがわかった。
KouhpayehとAnsariは、ワクチン群と対照群でそれぞれ60,000人近くを対象とした5つのmRNAワクチン研究を含む、公表されている臨床試験データもレビューした[276]。その結果、mRNAワクチンの接種は、未接種群に比べて全身性の有害事象のリスクが1.53倍(95%信頼区間1.08-2.16)高いことが判明した。最も多く報告された全身反応の種類は、発熱、疲労、頭痛であった。
Fraimanらは、ファイザーのBNT162b2ワクチンとModerna mRNA-1273ワクチンの第III相臨床試験データにおいて、重篤な有害事象(SAE)と重篤な有害事象(AESI)を評価した[277]。AESIは、ブライトン共同計画によって作成され、世界保健機関(WHO)によって承認された有害事象の優先リストから導き出された。SAEは、死亡、事象発生時に生命を脅かすもの、入院または既存の入院の延長、持続的または重大な障害/能力障害、先天異常/出生異常、医学的判断に基づく医学的に重要な事象と定義された。
2つのmRNAワクチンを組み合わせた場合、AESIの過剰リスクはワクチン接種者1万人あたり12.5人であった(95%CI 2.1~22.9)。どちらかのワクチンを接種された試験参加者は、対照群と比較してAESIのリスクが43%高かった(リスク比1.43;95%CI 1.07~1.92)。
ワクチンを接種されたファイザーの試験参加者は、対照群よりもSAEのリスクが36%高かった(リスク比1.36、95%CI 1.02~1.83、リスク差18.0/10,000ワクチン接種、95%CI 1.2~34.9)が、SAEは「治療群間でバランスがとれていた」というFDAの結論とは対照的であった[277, 278]。この不一致の理由として考えられるのは、FDAが異なる解析集団を使用したこと、追跡期間が短かったことなどである。また、FDAは何らかのSAEを経験した参加者の総数を分析したのに対し、FraimanらはSAEの総数に基づいて分析した。Fraimanらは、ファイザーとModernaの両試験において、最大の過剰リスクはBrighton分類の凝固障害で発生することを発見した。
Fraimanらはまた、両ワクチンのリスク-ベネフィット評価を行い、ファイザーのBNT162b2ワクチンは、プラセボ群と比較して、重篤なAESIの過剰リスクがワクチン接種者1万人あたり10.1人である一方、COVID-19による入院をワクチン接種者1万人あたり2.3人で予防することを明らかにした。Moderna mRNA-1273ワクチンは、プラセボ群と比較して、COVID-19による入院を1万人あたり6.4人予防する一方で、重篤なAESIの過剰リスクは1万人あたり15.1人であった[277]。
7.2.2 市販後サーベイランスデータの解析
研究者らは、ワクチンの一般への展開後の数ヶ月間に収集されたファーマコビジランスデータの解析を通じて、特定の有害事象の発生率が高いことも発見した。
WongらによるFDA後援の前向き研究では、2020年12月から2022年1月までの65歳以上の患者3,000万人以上の米国メディケイド請求データを評価した[279]。研究者らは、COVID-19ワクチンを少なくとも1回接種した患者において観察された14種類の転帰の数を、パンデミック前の同様のCOVID-19ワクチン未接種集団における背景率に基づく予想数と比較した。毎週の逐次検査により、ファイザー社製BNT162b2ワクチン接種後に統計的シグナルの閾値を満たす4つの転帰が明らかになった:肺塞栓症(PE、率比1.54、ワクチン接種後1~28日)、急性心筋梗塞(AMI、率比1.42、1~28日)、播種性血管内凝固症候群(DIC、率比1.91、1~28日)、免疫性血小板減少症(ITP、率比1.44、1~42日)。バックグラウンド率の月ごとの変動を調整した後でも、PEの率比のみが依然としてシグナルの統計的閾値を満たしていた[279]。
2020年12月から2022年12月の間に、ワクチン有害事象報告システム(VAERS)はCOVID-19ワクチンに関連する250万件以上の報告を受け処理したが、これは1万回接種あたり約42件の報告率であった[280, 281]。この中には、mRNA COVID-19ワクチンに関連した死亡報告40,883件が含まれており、投与量10万回あたり約6件の死亡に相当する。これは、1990年以降のすべてのインフルエンザワクチンで報告された死亡率の45倍以上である。
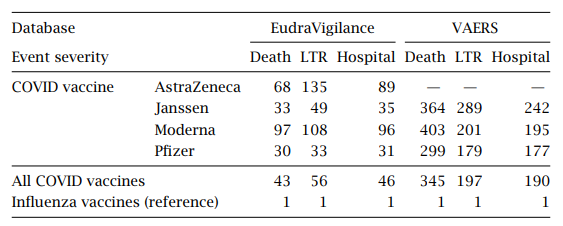
表7.1 2020年12月から2021年10月までの期間について、4つの主要な遺伝子ベースのCOVID-19ワクチンそれぞれに関連する死亡、生命を脅かす反応(LTR)、入院の相対リスクを、すべてのインフルエンザワクチンを合わせたものと比較した。データはMontano [282]の表1による。アストラゼネカのワクチンは米国では使用されていないため、VAERSのデータからは欠落している。
EudraVigilance(The European Database of Suspected Adverse Drug Reactions)とVAERSの2020年から2021年10月のロールアウト後のサーベイランスデータ分析において、MontanoはCOVID-19ワクチンの有害事象報告率とインフルエンザワクチンの有害事象報告率を比較した[282]。彼は、欧州疾病予防管理センター(ECDC)、欧州統計局(Eurostat)、米国疾病予防管理センター(CDC)の欧州と米国のワクチン接種率データを用いて、各種ワクチンの総投与数を推定した。COVID-19ワクチン(アストラゼネカ、ヤンセン、モデナ、ファイザーを含む)の接種単位あたりの死亡、入院、生命を脅かす反応の報告は、インフルエンザワクチンのそれをはるかに凌ぐものであった。EudraVigilanceとVAERSでは、死亡報告数はそれぞれ42.53倍(95%CI 33.49-54.01)、345.42倍(95%CI 224.61531.20)、入院報告数は45. 71倍(95%CI 41.26-50.65)、189.65倍(95%CI 163.85-219.53)、生命を脅かす反応の報告数は56.13倍(95%CI 44.51-70.78)、196.72倍(95%CI 147.04-263.19)であった。表7.1にこれらの所見をまとめた。
すべてのCOVID-19ワクチンは、インフルエンザワクチンに関連する有害事象のリスクを大きく上回っていたが、それでも両ワクチン間にはいくつかの違いがあった。EudraVigilanceでは、Modernaワクチン単独はヤンセンワクチンと比較して、死亡の報告頻度が2.99倍(95% CI 2.69-3.32)、入院の報告頻度が2.77倍(95% CI 2.65-2.89)、生命を脅かす反応の報告頻度が2.20倍(95% CI 2.02-2.39)であった。しかし、この顕著な差はVAERSでは明らかではなかった。インフルエンザワクチンと比較してCOVID-19ワクチンの相対リスクが最も大きかったのは、アレルギー反応、不整脈、一般心血管系イベント、凝固、出血、胃腸反応、眼反応、性器反応、血栓症であった。
7.2.3 ワクチン接種群と非接種群の比較
他の研究者が市販後の臨床において有害事象の増加を認めた。Bardaらのレトロスペクティブ・コホート研究では、イスラエルの大規模医療機関のワクチン接種患者と未接種患者約80万人をマッチングさせた。その結果、ワクチン未接種患者と比較して、2020年12月から2021年5月までにファイザー社製BNT162b2ワクチンの接種を受けた患者では、心筋炎(リスク比3.24、95% CI 1.55-12.44、リスク差2.7イベント/10万人、95% CI 1.0-4.6)、リンパ節腫脹(リスク比2.43、95% CI 2.05-2.78、リスク差2.7イベント/10万人、95% CI 1.0-4.6)のリスクが高かった。 05-2.78;リスク差78.4イベント/10万人;95%CI 64.1-89.3)、虫垂炎(リスク比1.40 95%CI 1.02-2.01;リスク差5.0イベント/10万人;95%CI 0.3-9.9)、帯状疱疹感染(リスク比1.43;95%CI 1.20-1.73;リスク差15.8イベント/10万人;95%CI 8.2-24.2)であった[283]。
7.2.4 まとめ
COVID-19 mRNAワクチン接種後の有害事象の範囲を調査している研究者らは、65歳以上の高齢者において、一般的な有害事象;凝固障害、肺塞栓症、急性心筋梗塞、播種性血管内凝固、免疫性血小板減少症を含む重篤な有害事象の発生率が増加することを見出している; アレルギー反応;不整脈;一般的心血管系イベント;凝固;出血;胃腸反応;眼反応;性器反応;血栓症;心筋炎;リンパ節腫脹;虫垂炎;帯状疱疹感染;入院;生命を脅かす反応;および死亡。
7.3 心臓疾患
炎症性心疾患は、受動的サーベイランス、能動的サーベイランス、医療システムのコホートデータの多くの分析において、mRNA COVID-19ワクチン接種と強く関連している。
7.3.1 サーベイランスデータの解析
心筋炎とmRNA COVID-19ワクチンを関連付けた初期の文献は、2021年6月に発表された米 国防総省の研究で、2021年1月から4月にかけての米軍サービス要員における23症例を詳述し ている[284]。2021年2月19日の週までに、VAERSは、若年男性における心筋炎がCOVID-19ワクチンと因果関係があると95%以上の信頼度で示唆するのに十分な重篤な有害事象報告を受け取っていた[285]。このような利用可能な有害性の証拠にもかかわらず、5月10日、FDAはファイザー-バイオンテックワクチンのEUAを拡大し、12歳から15歳のアメリカ人1,400万人を対象とした[286]。CDCはその2日後、この年齢層にこのワクチンを承認し推奨した[287]。5月27日、CDCはワクチン接種による心臓の有害反応を認め、ウェブサイトに「mRNA COVID-19ワクチン接種後の心筋炎と心膜炎」というウェブページを作成し、こう述べた[288]:
2021年4月以降、ワクチン有害事象報告システム(VAERS)への心臓の炎症症例の報告が増加している。
2020年12月から2022年12月にかけて、COVID-19ワクチンについて提出されたVAERS報告のうち、4,000件以上(~0.16%)が心筋炎の報告であり、ワクチン1用量あたり、インフルエンザの100倍の件数が報告されている[280, 281]。
2020年12月から2021年8月までのmRNAワクチン接種後の心筋炎に関するVAERS報告のOsterらの記述的分析では、心筋炎の症例定義を満たす報告が1,626件あった[289]。リスクは、16~17歳の思春期男性では2回目の接種後に最も高く(ファイザーBNT162b2ワクチンの100万回接種あたり105.9[95%CI 91.65-122.27])、12~15歳の思春期男性では(70.7[95%CI 61.88-81.11])であった。 11])、18~24歳の若年男性(ファイザーBNT162b2ワクチンおよびModerna mRNA-1273ワクチンそれぞれ100万回接種あたり52.4[95%CI 45.56-60.33]および56.3[95%CI 47.08-67.34])であった。図7.1にこの研究で得られた主な知見を示す。
同じ観察期間(2020年12月~2021年8月)を用いたLiらによるいずれかのCOVID-19ワクチン接種後の心筋炎および心膜炎に関するVAERS分析では、投与100万回当たりの発生率は5.98例(95%CI 5.73-6.24)と低かった[290]。発症率は12~17歳の青年で最も高く、100万回投与あたり20.94例(95%CI 19.01-23.01)であった。mRNAワクチンの2回目投与後の報告は、1回目投与後よりも多かった。全体として、VAERSに登録されている他のすべてのワクチンと比較して、2つのmRNA COVID-19ワクチンは心筋炎/心膜炎のオッズ増加と関連しており、報告オッズ比はModerna mRNA-1273で2.91(95%CI 2.21-3.83)、Pfizer BNT162b2で5.37(95%CI 4.10-7.04)であった。
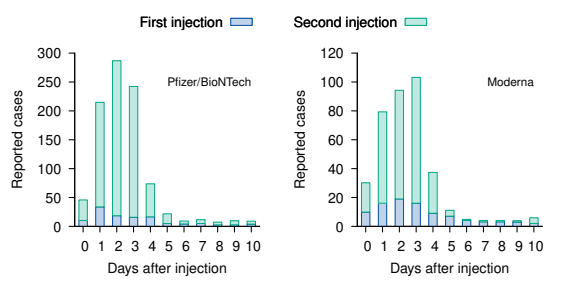
図7.1 2020年12月から2021年8月までにVAERSに報告されたCOVID-19 mRNAワクチン接種後の心筋炎症例(ワクチン接種後の発症日別、メーカー別)。[289]の図2の再掲。
Strausらによる2020年12月から2022年2月までのModernaグローバル安全性データベースの市販後調査分析では、Modernaワクチン接種後の心筋炎の発生率は40歳未満の男性、特に18~24歳で最も高く(10万人年当たり53.76人)、これは米国Premier Healthcare Databaseからの集団ベースのデータ推定値から予想される発生率の3.10倍(95%CI 2.68~3.58)であった[291]。
Witbergらの大規模なイスラエルの医療システムにおける250万人以上のワクチン接種患者のレトロスペクティブコホート解析によると、ファイザーのBNT162b2 mRNAワクチンを少なくとも1回接種した患者のうち、心筋炎の推定発生率は10万人あたり2.13例(95%CI 1.56-2.70)であった [292] 。最も発生率が高かったのは16~29歳の男性患者であり(10万人当たり10.69例;95%CI 6.93~14.46)、Osterらの所見と同等であった。
KrugらのVAERSデータを用いたリスク・ベネフィット解析によると、COVID-19感染歴があり合併症のない男児では、2021年のデルタ波では、ファイザーBNT162b2ワクチンを1回接種しても、COVID-19による入院に対するベネフィットよりも心筋炎/心膜炎のリスクの方が高いことが国際的な推計により判明した[293]。
Chuaらの2021年6月から9月までを対象としたレトロスペクティブ集団コホート研究[294]では、12~17歳の中国人男子青年におけるファイザーComirnatyの2回目接種後の急性心筋炎/心膜炎の発生率は、接種者10万人当たり37.32人であった(95%信頼区間26.98~51.25)。
KimらによるWHO VigiBaseデータベースのサーベイランス分析[295]では、2020年1月から2021年1月までに報告されたmRNA COVID-19ワクチンによる心臓有害事象とインフルエンザワクチンによる心臓有害事象を比較した。COVID-19 mRNAワクチンの接種者は、高血圧クリーゼ(12.72倍;95%CI 2.47-65.54)および上室性頻拍(7.94倍;95%CI 2.62-24.00)の心臓有害事象の報告オッズが、インフルエンザワクチンと比較して、投与1回あたり有意に高かった。
Sunらによるイスラエルの国立救急医療サービス(EMS)のデータセットの分析では、2021年1月~5月の16~39歳の集団における心停止と急性冠症候群の救急要請が、2019~2020年の年と比較して25%以上増加していた[296]。毎週の救急出動件数は、この年齢層に接種されたワクチンの1回目と2回目の接種率と有意な相関があったが、COVID-19感染率とは関連がなかった。
7.3.2 ワクチン接種と未接種のコホート解析
Karlstadらは、2020年12月から2021年10月までの期間にワクチン接種後28日以内の12歳以上の参加者を評価した4つの国内コホート研究のメタ解析において、mRNAワクチン2回目接種後の16歳から24歳の男性で心筋炎のリスクが最も高いことを観察した: ワクチン未接種者と比較して、ファイザーでは5.31倍(95% CI 3.68-7.68)、モデナでは13.83倍(95% CI 8.08-23.68)高かった[297]。
イスラエル保健省のデータを用いたMevorachらのレトロスペクティブ・コホート研究では、ファイザーのBNT162b2 mRNAワクチンの2回目接種後30日以内の心筋炎の発生率は、未接種者に比べて2.35倍(95%CI 1.10-5.02)高かった[298]。率比は16歳から数歳の男性接種者で最も高く、8.96倍(95%CI 4.50-17.83)で、このグループの発生率は6,637人に1人であった。これは、研究者らがワクチン未接種の一般集団で計算した心筋炎の発生率(10,857人に1人)の1.64倍である。2回目のワクチン接種を受けてから30日以内の心筋炎の発生率は、イスラエル国立病院退院データベース(2017-2019年)の過去のデータに基づく予想発生率の5.34倍(95%信頼区間4.48-6.40)であった。ここでも、リスクは16~19歳の男性レシピエントで最も高く、13.60倍(95%CI 9.30~19.20)であり、予想症例2.35例に対して32例が観察された。
Laiらによる香港の医療データベースに登録された12~18歳の青少年を対象としたレトロスペクティブ・コホート研究では、20万人以上の患者を対象として、ファイザーのBNT162b2ワクチン接種後28日以内の有害事象の発生率が評価された[299]。ワクチンの初回接種を受けた参加者は、ワクチン未接種の青少年と比較して心筋炎のリスクが9.15倍(95%CI 1.14-73.16)高く、2回目の接種を受けた参加者はリスクが29.61倍(95%CI 4.04-217.07)高かった。さらに、2回目の接種後、ワクチン接種を受けた青少年は、ワクチン接種を受けていない青少年と比較して、睡眠障害/障害のリスクが2.06倍(95%CI 1.01-4.24)高かった。
2021年2月から8月までの香港の入院患者を対象としたLaiらの症例対照研究では、心筋炎でトロポニン値が上昇した患者160人と対照患者1,533人を評価した[300]。心血管疾患のリスク因子をコントロールした多変量解析では、ファイザー社製BNT162b2ワクチンの接種者は、未接種患者に比べて心筋炎のオッズが3.57倍(95%CI 1.93-6.60)高かった。男性ワクチン接種者では、オッズは4.68倍(95%CI 2.25-9.71)であった。リスクはBNT162b2の2回目接種後の方が1回目よりも高かった。
7.3.3 その他のコホート解析 Goddardらは、CDCのVaccine Safety Datalinkデータベースを用いて、8つの統合医療提供システムを対象としたレトロスペクティブ解析を行った[301]
この研究は、CDCの予防接種安全対策室長のTom Shimabukuro博士とCDCの同僚のEric Weintraub博士とMatthew Oster博士の共著である。その結果、2020年12月から2022年1月までの期間において、18歳から39歳の参加者がファイザーワクチンまたはモデナCOVID-19ワクチンの1回目または2回目の接種を受けてから7日以内に心筋炎または心膜炎を発症するリスクが、22日から42日前に接種を受けた参加者と比較して有意に高いことが判明した。ファイザーワクチンでは、初回接種後に3.02倍(95%信頼区間1.03-8.33)、2回目接種後に14.30倍(95%信頼区間6.45-34.85)、Modernaワクチンでは、初回接種後に3.46倍(95%信頼区間1.12-11.07)、2回目接種後に18.75倍(95%信頼区間6.73-64.94)であった。
Simoneらのレトロスペクティブ・コホート研究は、Kaiser Permanente Southern Californiaのデータベース内で、2020年12月から2022年2月の間にmRNA COVID-19ワクチンを1~3回接種した患者を対象としたもので、総計300万人以上であった[302]。7日以内または2回目のワクチン接種後の心筋炎リスクは、接種日の2年前の365日のベースライン期間と比較して10.23倍(95%CI 6.09-16.4)高かった。3回目のワクチン(ブースター)接種後7日以内の心筋炎リスクは6.08倍(95%CI 2.34-13.3)高かった。この研究では、最初に受けたmRNAワクチンに関連する統計的に有意なリスクはなかった。
2020年12月から2021年9月までのイタリアの国立病院データを用いたMassariらの自己対照症例シリーズ研究では、12~39歳の男性がModernaワクチンを接種した場合、1回目または2回目のワクチン接種後0~21日の間隔を除いたベースライン期間と比較して、1回目接種後7日以内に心筋炎または心膜炎と診断されるリスクが12.28倍(95%CI 4.09~36.83)、2回目接種後11.91倍(95%CI 3.88~36.53)高かった[303]。
Patoneらの自己対照ケースシリーズ研究では、2020年12月から2021年12月までの間にイングランドで13歳以上の人を対象に心筋炎の診断を検討した[304]。男性は、ワクチン接種前29日と接種後29日にわたるウィンドウ外のベースライン期間と比較して、Modernaワクチンの1回目(2.35倍;95%CI 1.09-5.08)、2回目(14.98倍;95%CI 8.61-26.07)、3回目(3.57倍;95%CI 1.48-8.64)接種後28日以内にリスクの上昇を示した。最も発生率が高かったのは40歳未満の男性で、16.83倍(95%CI 9.11-31.11)のリスク増加であり、2回目のワクチン接種後28日以内に発生した。また、ファイザーのいずれかの用量、およびモデナの2回目と3回目の用量を受けたすべての参加者、ファイザーの1回目または3回目とモデナの2回目の用量を受けた女性、およびファイザーのいずれかの用量を受けた男性においても、発生率が有意に増加した。
7.3.4 まとめ
心筋炎は、心筋(心筋壁)の損傷を示す重篤な疾患である
最もリスクが高いのは若い男性であるが、女性も心筋炎に罹患する可能性がある。若年者の突然死のほぼ20%は心筋炎が原因である。生存率は1年後で80%、5年後で50%である[305]。
前述の分析から、mRNAワクチン接種者に心筋炎が有意に存在することが確認され、思春期および若年成人男性で最も多かった。VAERSにおける他のすべてのワクチンと比較して、mRNA COVID-19ワクチンは心筋炎/心膜炎のオッズ増加と関連していた。心筋炎の発生率は、ワクチン100万接種あたり10例未満から100例以上の範囲であった。ワクチン未接種またはベースラインの発症率と比較すると、年齢、性別、ワクチンの種類にもよるが、ワクチン接種者では心筋炎発症率は約2倍から30倍近く高かった。通常、初回接種よりも2回目以降の接種率が高かった。一方、2020年3月から2021年1月にかけてイスラエルで行われた成人約20万人を対象とした大規模なレトロスペクティブ・コホート研究では、COVID-19感染(PCR検査陽性で定義)は心筋炎(調整ハザード比(aHR)1.08、95%CI 0.45-2.56)にも心膜炎(aHR 0.53、95%CI 0.25-1.13)にも関連していなかった[306]。心筋炎に加えて、mRNAワクチンの接種者は、インフルエンザワクチンの接種者と比較して、心臓の有害事象である高血圧クリーゼと上室性頻拍のオッズが増加した。
7.4 血栓性事象
mRNA COVID-19ワクチン接種後の身体および脳の血管系における血液凝固障害は、観察研究および自己対照研究において定量化および評価されている。脳血管イベントはCOVID-19ワクチンのVAERS報告の0.1%未満であったが、COVID-19ワクチンでは、インフルエンザワクチンの60倍以上の脳血管イベントが1用量あたり報告されている[280, 281]。2020年1月から2021年8月にかけてシンガポールのすべての公立急性期病院を対象としたTuらによる観察コホート研究では、mRNA SARS-CoV-2ワクチン(ファイザー・バイオンテックBNT162b2またはモデナmRNA-1273)接種後6週間以内に脳静脈血栓症(CVT)で入院した患者が9人見つかった[307]。これは100,000人年当たり2.59人(95%CI 1.19-4.92)の粗発生率に相当した。
Hippisley-Coxらの自己対照ケースシリーズ研究では、英国の登録で2020年12月から2021年4月の間にCOVID-19ワクチンを接種した約3,000万人のプールにおける入院と死亡を分析した[308]。研究者らは、ワクチン接種後0~28日の参加者を、ワクチン接種28日前と接種後28日のウィンドウを除いたベースライン期間と比較した。ファイザー社製ワクチンを1回接種したことは、以下のことと関連していた。
動脈血栓塞栓症のリスクが1.06倍(15~21日では95%CI 1.01~1.10)、脳静脈洞血栓症のリスクが3.58倍(15~21日では95%CI 1.39~9.27)、虚血性脳卒中のリスクが1.12倍(15~21日では95%CI 1.04~1.20)増加した。
Berildらのレトロスペクティブ自己対照コホート研究では、2020年1月から2021年5月までのノルウェー、フィンランド、デンマークの病院登録を用いて、COVID-19ワクチン接種後28日以内の血小板減少性イベントおよび血栓塞栓性イベントの発生率をワクチン接種前のベースライン期間と比較した[309]。その結果、モデナのワクチン接種後に冠動脈疾患の発生率が1.13倍(95%CI 1.02-1.25)に増加し、ファイザーとモデナのワクチン接種後にそれぞれ凝固障害の発生率が1.12倍(95%CI 1.07-1.19)と1.26倍(95%CI 1.07-1.47)に増加することが判明した[309]。また、ファイザー(1.09倍;95%CI 1.05-1.13)およびモデナ(1.21倍;95%CI 1.09-1.35)のワクチン接種後に脳血管障害の発生率が増加することも観察された。
7.4.1 まとめ
65歳以上の患者において、ファイザーBNT162b2ワクチン接種と肺塞栓症、播種性血管内凝固、免疫性血小板減少症の血栓性疾患との関連を示したWongらのサーベイランス試験結果に加え、mRNA COVID-19ワクチンは脳静脈血栓症、動脈血栓塞栓症、虚血性脳卒中、冠動脈疾患、凝固障害、脳血管疾患と関連している。
7.5 神経学的事象
DuttaらによるWHOのVigiBaseサーベイランスデータの不均衡分析によると、COVID-19ワクチンの投与に関連した神経学的有害事象には、加齢、無感覚、灼熱感、めまい、顔面麻痺、頭痛、感覚低下、嗜眠、片頭痛、神経痛、麻痺、感覚鈍麻、睡眠の質の低下、痙攣、一過性脳虚血発作、振戦が含まれていた[310]。
Hosseini et al. の神経学的副作用に関する系統的レビューでは、mRNAワクチンが頭痛、横紋筋炎、多発性硬化症、視神経脊髄炎などの脱髄障害、小繊維神経障害、パーソンテージ・ターナー症候群、ギラン・バレー症候群、ベル麻痺、外転神経麻痺と関連しているという証拠が見つかっている; 急性播種性脳脊髄炎;脳症;嗅覚障害および幻覚;耳鳴りおよび蝸牛症;アカシジア;痙攣;てんかん;せん妄;ならびに脳静脈洞血栓症、脳内出血、虚血性脳卒中および一過性脳虚血発作を含む脳血管障害 [311] 。
7.5.1 出血性脳卒中
Patoneらの自己対照ケースシリーズ研究では、National Immunisation Management Service(NIMS)データベースの英国データを用いて、2020年12月から2021年5月までの1200万人以上のレシピエントを含むファイザーBNT162b2の初回投与後28日間の神経学的合併症による入院を調査した[312]。ワクチン接種後28日間のウィンドウ外(接種前と28日目以降)のベースライン率と比較すると、ワクチンを接種した患者は出血性脳卒中のリスクが1.38倍(15~21日で95%CI 1.12~1.71)増加した。
7.5.2 ベル麻痺
2010年1月から2021年4月までのSatoらのVAERS不釣り合い分析では、ファイザーワクチンとモデナワクチンは、他のすべてのワクチンと比較して、ベル麻痺の発生率がそれぞれ1.84倍(95%CI 1.65-2.06)、1.54倍(95%CI 1.39-1.70)増加した[313]。
Shibliらのレトロスペクティブ・コホート研究では、イスラエル最大の医療提供者のデータベースから、2020年12月から2021年4月までの期間のファイザーBNT162b2 mRNA COVID-19ワクチン接種に関するデータが検索され、250万人以上のワクチン接種者が含まれていた[314]。患者は、1回目のワクチン接種から21日以内、または2回目のワクチン接種から30日以内に診断され、適切なICDコーディングが割り当てられ、さらに診断から2週間以内にプレドニゾン [315] の処方箋が記入されていた場合、ベル麻痺の症例としてカウントされた。この数を、2019年の発生率に基づいて予想される症例と比較した。1回目のワクチン接種はベル麻痺のリスクを1.36倍増加させることと関連していた(95%CI 1.14-1.61)。リスクは女性の高齢者で高く、45~64歳の女性ワクチン接種者は1.71倍(95%CI 1.10-2.54)リスクが高く、接種者10万人当たりの発症率は2.58例、65歳以上の女性ワクチン接種者は2.51倍(95%CI 1.65-3.68)リスクが高く、接種者10万人当たりの発症率は4.46例であった。
Wanらの自己対照解析および症例対照解析では、香港の人口ベースの電子カルテのデータを用いて、2021年3月から7月の間にファイザーBNT162b2ワクチン接種後28日以内の入院患者におけるベル麻痺の診断を評価した[316]。ワクチン接種は、マッチさせた対照と比較してベル麻痺診断のオッズを1.543倍(95%CI、1.123-2.121)増加させることと関連し、2回接種を受けた10万人あたり最大1.112件の過剰事象が認められた。対照群と比較すると、2回目の投与後14日間にベル麻痺を発症する確率は2.325倍(95%信頼区間1.414-3.821)増加した。彼らの自己対照ケースシリーズ解析では、ワクチン接種後28日間のベル麻痺の発生率と、ワクチン接種後の期間外のベースライン・ウィンドウ(ワクチン接種前とワクチン接種後28日以降)のベル麻痺の発生率を比較したところ、2回目の接種でワクチン接種後14日以内のベル麻痺のリスクが2.44倍(95%CI 1.32-4.50)増加することが示された。
Laiらによるレビューとメタアナリシスには、ベル麻痺を定量化した5つの研究が含まれ、ワクチン未接種群と比較して、ファイザーBNT162b2またはModerna mRNA-1273の投与を受けた人はベル麻痺のオッズが1.36倍(95%CI 1.03-1.79)増加することが示された[317]。
7.5.3 感音性難聴
Yanirらによる、2020年12月から2021年5月までのイスラエルの大規模医療機関を対象とした集団ベースのレトロスペクティブ・コホート研究では、突発性感音難聴のリスクが、2018年と2019年の集団の経験と比較して、ファイザーワクチン初回接種後に1.35倍(95%CI 1.09-1.65)、2回目接種後に1.23倍(95%CI 0.98-1.53)増加することが明らかになった[318]。患者は、1回目または2回目のワクチン投与を受けてから21日以内に診断され、適切なICDコーディングが割り当てられており、さらに診断から30日以内にプレドニゾン[43]の処方箋が記入されていた場合、感音性難聴の症例としてカウントされた。リスクの増加は、16~44歳の女性(1.92倍;95%CI 0.98-3.43)および65歳以上の女性(1.68倍;95%CI 1.15-2.37)、16~44歳の男性(2.45倍;95%CI 1.36-4.07)では2回目の接種後に最も大きかった。突発性感音難聴の患者は、永続的な難聴と耳鳴りを経験する可能性がある。
7.5.4 まとめ サーベイランスデータから、mRNA COVID-19ワクチンは多くの重篤な免疫介在性神経学的状 態を引き起こす可能性があることが示唆されている
短期分析では、出血性脳卒中(リスク1.38倍増)、ベル麻痺(リスク1.36~2.51倍増)、感音性難聴(リスク1.35倍増)がワクチン接種と関連していることが確認されている。
7.6 免疫学的事象
レトロスペクティブなコホート解析により、mRNAワクチンが帯状疱疹感染を活性化し、帯状疱疹を引き起こす可能性が明らかになった。
Hertelらは、2019年11月から2021年11月までの世界的なTriNetXデータベースから100万組以上のマッチした症例対照ペアを解析した結果、mRNA脂質ナノ粒子(LNP)またはアデノウイルスベクターベースのCOVID-19ワクチンを少なくとも1回接種した人では、COVID-19ワクチンを1回も接種しなかった人と比較して、接種60日後に帯状疱疹と診断される頻度が1.802倍(95%CI 1.680-1.932)高いことを明らかにした[319]。ファイザーとモデルナのmRNAワクチン接種者は、この研究におけるCOVID-19ワクチン接種者全体の98.5%を占めていた。
Wanらの2021年2月から7月までの香港保健省の記録を用いた自己対照症例シリーズおよび症例対照研究では、100万人以上のファイザーBNT162b2ワクチン接種者が含まれていた [320] 。ファイザー社製ワクチンを接種した患者は、ワクチン接種にまつわる指定された期間以外の任意の期間をベースライン期間とした場合と比較して、1回目接種後0~13日および14~27日に病院で帯状疱疹と診断される可能性がそれぞれ5.23倍(95%CI 1.61~17.03)および5.82倍(95%CI 1.62~20.91)、2回目接種後0~13日に帯状疱疹と診断される可能性がそれぞれ5.14倍(95%CI 1.29~20.47)高かった。
7.6.1 まとめ COVID-19ワクチン接種者は、未接種群またはベースライン期間と比較して、帯状疱疹の診断頻度が1.80~5.82倍高かった
7.7 生殖に関する事象
7.7.1 臨床試験における妊娠データの欠如
緊急時使用許可につながったmRNA COVID-19ワクチンの第Ⅲ相臨床試験では、妊娠中及び授乳中の女性は除外されていた[321, 322]。2021年2月、ファイザー・バイオンテックは、妊婦を対象としたBNT162b2ワクチンの安全性と有効性を評価する第Ⅱ/Ⅲ相臨床試験を開始したが、最終的に登録されたのはわずか349名であった[323]。現在までのところ、この試験のデータは公表されていない。ファイザーの代表者は、2021年半ばから後半にかけて米国や他の政府がmRNA COVID-19ワクチンを妊婦に正式に推奨した後、この試験への登録が減少したと説明した[324]。同代表は電子メールにこう書いている[324]:
登録者数が減少したため、主要な免疫原性目標を評価するにはサンプルサイズが不足し、世界的な推奨により、このプラセボ対照試験の継続はもはや正当化できなくなった。この提案はFDAおよびEMA(欧州医薬品庁)と共有され、同意された。
FDAで承認されたファイザー社のComirnatyワクチンの添付文書には次のように記載されている[325]:
妊婦に投与されたCOMIRNATYに関する入手可能なデータは、妊娠中のワクチンに関連するリスクを知らせるには不十分である。
FDAが承認したModerna Spikevaxワクチンの添付文書にも同等の開示がある [326]:
妊婦に投与されたスパイクバックスに関する入手可能なデータは、妊娠中のワクチン関連リスクを知らせるには不十分である。
それにもかかわらず、CDCはCOVID-19ワクチン接種を推奨している [327]。
妊娠している人、授乳中の人、現在妊娠を試みている人、将来妊娠する可能性のある人に対してである。
しかし、市販後の調査によると、妊娠、胎児の転帰、女性・男性両方の生殖能に重大な悪影響があることが示されている。
7.7.2 受動的サーベイランスの分析
2020年12月から2022年12月の間にCOVID-19ワクチンについて提出されたVAERS報告のうち、13,000件以上(0.50%)が月経不順の報告であった[280, 281]。これは、COVID-19ワクチンで報告されたワクチン用量あたりの月経不順の数が、インフルエンザワクチンの1,000倍に相当する。英国で提出されたモデナとファイザー・バイオンテックのCOVID-19ワクチンに関するイエローカード報告224,960件のうち、23%(51,695件)に月経異常が記載されていた[281, 328]。
Thorp et al. の1998年1月から2022年6月までのVAERSデータの分析 [329]によると、インフルエンザワクチンと比較して、COVID-19ワクチンは、月経異常、流産、胎児染色体異常、胎児奇形、胎児嚢胞性水腫の妊娠・月経有害事象の有意な増加と関連している、 胎児心疾患、胎児心停止、胎児不整脈、胎児血管不全、胎児発育異常、胎児監視異常、胎盤血栓症、胎児死亡/死産、羊水減少、子癇前症、早産、早産膜破裂、早産児死亡である。これらの事象の比例報告比は、単位時間別、投与量別、接種者別という3つの正規化方法すべてにおいて、CDCが懸念シグナルとしている閾値である2.0を超えていた。
2023年4月7日時点のVAERSデータの未発表の分析によると、2020年12月に最初のCOVID-19ワクチンが導入されて以来、VAERSの32年の歴史の中で、COVID-19ワクチンの自然流産が他のすべてのワクチンの3.28倍(3,576件対1,089件)、不妊症が13.38倍(19,040件対1,423件)報告されている[330]。
MascoloらによるEudraVigilanceデータ解析では、2021年中に妊婦から提出されたCOVID-19注射に関連する3,000件を超える症例安全性報告が検討された[281, 331]。非RNAのCOVID-19ワクチンを接種した妊婦の報告と比較して、mRNAワクチンを接種した妊婦の報告では、胎児死亡率が約12倍(0.81%対0.07%)、死産率が高い(0.22%対0.17%)、妊娠中の出血率が約9倍(0. 62%対0.07%)、胎児障害(2.5%対0.71%)および先天異常(0.11%対0.03%)の3倍以上、未熟児(0.64%対0.17%)の4倍近く、新生児死亡(0.06%対0.03%)の2倍である。
7.7.3 月経調査の分析
2021年4月から6月までにCOVID-19ワクチンを接種した39,000人以上の女性を対象としたLeeらの調査によると、月経周期が規則的な人の42%が通常より出血量が多かった[332]。通常月経がない回答者では、長時間作用型可逆的避妊薬を服用している人の71%、閉経後の女性の66%が、破綻性出血を報告した。
Parottoらは、自己報告による脱落性子宮脱落(子宮内膜全体の異常脱落)が、過去100年間に報告されたパンデミック前の40例に比べ、2021年5月から12月にかけての調査に回答した6,000人以上の女性の4.83%にあたる292例に達し、有意に増加していることを報告した[333]。
7.7.4 ワクチン接種対非接種のコホート解析
DeSilvaらは、New England Journal of Medicine誌の編集者への手紙の中で、CDCが資金提供したレトロスペクティブ・マッチコホート研究について述べている[334]。彼らは、2020年12月から2021年7月にかけて、8つのVaccine Safety Datalinkサイトで16歳から49歳の妊婦を対象とした。これらの女性のうち、32,794人(72.5%)がmRNAワクチンを2回接種していた。いずれかのCOVID-19ワクチンを接種した妊婦は、マッチさせたワクチン未接種の妊婦と比較して、発熱を経験する可能性が2.85倍(95%信頼区間1.76-4.61)、倦怠感または疲労を経験する可能性が2.24倍(95%信頼区間1.71-2.93)、局所反応を持続する可能性が1.89倍(95%信頼区間1.33-2.68)、リンパ節腫脹を経験する可能性が2.16倍(95%信頼区間1.42-3.28)であった。重篤な急性有害事象に差はみられず、観察期間を接種後42日で終了したため、母児への長期的影響を評価することはできなかった。
Sadaranganiらの調査ベースの観察コホート研究では、カナダ7州の15~49歳の妊婦および非妊婦90,000人以上を対象とし、mRNAワクチンを2回接種した妊婦は3,000人以上であった[335]。ワクチン接種を受けた妊婦は、Moderna mRNA-1273の2回目の投与を受けてから7日以内に重大な健康事象が発生する確率が、ワクチン未接種の妊婦対照と比較して4.4倍(95%CI 2.4-8.3)増加したが、Modernaの1回目の投与後やファイザーBNT162b2のいずれの投与後にも発生しなかった。妊娠女性におけるmRNA-1273の2回目投与後の最も一般的な重大な健康事象は、体調不良または倦怠感または筋肉痛、頭痛または片頭痛、および気道感染であった。年齢層、SARS-CoV-2感染の既往、妊娠期間について調整した多変量解析では、mRNAワクチンの2回目投与後7日以内に重大な健康イベントが発生する確率は、対照群と比較して2.4倍(95%CI 1.3-4.5)増加した。
イスラエルの大規模3次医療センターで2020年12月から2021年7月までに出産した女性5,618人を対象としたDickらによるレトロスペクティブ・コホート研究では、第2期にファイザーBNT162b2ワクチンまたはModerna mRNA-1273ワクチンのいずれかを接種した人は、未接種だった人に比べて早産になる可能性が1.3倍高かった(8.1%対6.2%、p<0.001)。この関連は潜在的交絡因子で調整した後も持続し、オッズは1.49倍(95%CI 1.11-2.01)大きかった[336]。
Dickらのその後の研究[337]では、2021年7月から10月の間にファイザーのBNT162b2ワクチンまたはModernaのmRNA-1273 COVID-19ワクチンのいずれかを完全接種し、ブースト(すなわち3種混合ワクチン)した妊婦は、ワクチン未接種の妊婦に比べて分娩後出血を経験する可能性が2.96倍高かった(9.5%対3.21%;p<0.001)。さらに、開業医はトリプルワクチン接種妊婦を妊娠糖尿病と診断する頻度がワクチン未接種妊婦の1.47倍であった(12.2%対8.3%;p 0.02)。
7.7.5 男性不妊分析
37人の精子提供者を対象としたGatらの小規模研究において、研究者らは、ファイザーのBNT162b2ワクチン接種後75日から125日までの期間において、精子濃度が15.4%減少(95%CI 25.5% to 3.9%, p 0.01)し、生存精子の総数が22.1%減少(95%CI 35% to 6.6%, p 0.007)したことを発見した[338]。145日後に測定した場合、精子濃度および総運動精子数はともに減少したままであり、ベースライン値と比較してそれぞれ15.9%(95% CI 30.3%~1.7%)および19.4%(95% CI 35.4%~0.6%)減少した。しかし、これらの結果は、測定のばらつきが大きいこととサンプル数が少ないことから、統計学的に有意ではなかった。この結果は、精液パラメーターの回復が明らかであるという著者らの主張を支持するものではなかった。
7.7.6 まとめ
これらの未検査製品の展開後のサーベイランス、調査、およびレトロスペクティブ・コホート解析のコレクションは、月経不順、有害な妊娠転帰、胎児異常、および男性の生殖能力障害に関する懸念すべき傾向を示している。これらの報告は、専門家の査読を経た文献ではまだ測定も記録もされていない、短期的・長期的な生殖への影響の表面をかすめたにすぎない。
7.8 結論
金銭的利害の対立がなく、ワクチン接種群と未接種群との健康上の転帰を直接比較した大規模な疫学研究は乏しいが、入手可能な証拠から、mRNA COVID-19ワクチン接種後の病気、障害、死亡に関する懸念すべき絵がまとまり始めている。これらは主に短期的な影響に過ぎず、ワクチン接種後数日から6週間以内に観察される。これらの有毒な生物学的薬剤の害が、慢性的な心臓、血栓、神経、免疫、生殖、その他の臓器の機能障害として現れるには、数ヵ月、数年、数十年かかるかもしれない。すでに何十もの査読済み論文がmRNA COVID-19ワクチンの重大な害を証明しているにもかかわらず、CDCはこれらの注射は安全であると主張し続けている[339]。2022年12月現在、CDCはCOVID-19ワクチンを「生後6カ月以上のすべての人に、5歳以上のすべての人に、資格があればブースター接種を」推奨している(同書)。政府の保健機関がそれを認めるかどうかにかかわらず、疫学的研究は、これらのmRNA注射が男性、女性、子供の健康に及ぼす破壊的な影響を解明するのに役立ち続けるだろう。
8. エイズとHIV 医学の倒錯と転覆の青写真
デイビッド・ラスニック博士
もし、予想通りの悲惨な結果をもたらす判断を急ぐことがあるとすれば、それはHIV/AIDS仮説とその余波である。科学的証明が発表される前に記者会見で発表され、アメリカの研究者による。「フランス産」ウイルスの盗用に関する初期の法的論争によって複雑化し混乱し、HIVによるAIDSの因果関係を明確に証明する世界的な科学的努力の継続不能、10年以上と何十億ドルもの資金を費やしても予防や治療に進歩が見られず、AZTのような薬剤の有効性について論争が高まる中、HIV/AIDS仮説は単なる仮説のまま: HIV/AIDS仮説は、HIVとAIDSの間に不規則な相関関係はあるが、因果関係は証明されていない。私が「不規則な」と言ったのは、エイズを発症していない多くのHIV陽性症例と、HIVを発症していない多くのエイズ症例があるためであり、また、エイズの定義(HIVを発症していない=エイズを発症していない)が循環しているため、そもそも相関関係が意味をなさないからである(HIVを発症していないエイズ患者は、CDCによって公式にエイズ患者としてリストアップされていない)。
カリフォルニア大学バークレー校のディック・ストローマン教授による、ピーター・デュースバーグ教授著『Infectious AIDS: Have We Been Misled?』
1980年代から1990年代にかけてのエイズ騒動は、COVID-19を語る上で重要である。というのも、今日の世界を支配している世界的な政府機関・製薬会社のインフラが、この時期に整備されたからである。エイズは私にとって、腐敗した独断的な科学との最初の接触だった。1980年代、私はエイズに関する自由で開かれた科学的探究が、拡大的で創造的な思考が不可欠であったはずの重要な時期に、突然打ち切られるのを目の当たりにした。私は、エイズの伝染性の推定に疑問を呈したことで、友人や同僚を失った。
レーガン大統領の最初の任期は、エイズの最初の4年間と重なった。1984年4月23日、民主党がエイズを選挙争点にするのを阻止するために記者会見が開かれるまで、レーガン政権はエイズについて沈黙を守っていた。保健福祉省(HHS)のマーガレット・ヘクラー長官は、国立がん研究所のロバート・ギャロ博士が、後にHIVと呼ばれるレトロウイルスを発見し、それがエイズの原因である可能性が高いと発表した。(レーガン政権は2年以内にワクチンを開発すると約束した。6つの政権が誕生したが、私たちはまだ待っている!
ギャロによるエイズの原因ウイルスの発見は、世界中の関心を持つ科学者にとって完全な驚きであった。この記者会見に先立ち、科学誌や医学雑誌にはこの発見について一言も掲載されていなかったし、科学者会議でも議論されていなかった。国立アレルギー・感染症研究所(NIAID)の新所長に任命されたアンソニー・ファウチは、エイズ騒動を利用して「プレスリリースによる科学」を完成させた。ファウチによる科学的精査と議論の簒奪は、瞬く間に詐欺的エイズ・シナリオの確立につながり、それは今日に至るまでドグマであり続けている:
– エイズは感染する
– エイズは性行為によって感染する
– エイズはHIVによって引き起こされる
– エイズの起源はアフリカである
– エイズは致死的である
しかし、これらの主張は一つも真実ではない。[340, 341] !
科学的理論は常に変更される可能性がある-いつでも「より良いもの」がその代わりになるかもしれない。その「より良い何か」を探し続け、それが現れたときにそれを認識するのが科学者の仕事である。より優れた理論、より優れた現実理解を提唱する個人やグループは、通常、他の科学者による誠実な挑戦を歓迎する。真に優れた理論に疑問を投げかけることは、その理論をより良いものにするだけであり、その過程で競合する理論の欠陥が明らかになる。少なくとも、科学の進歩はこのように機能するはずなのだが、残念ながら、制度化された科学はこの理想をほとんど破壊してしまった。
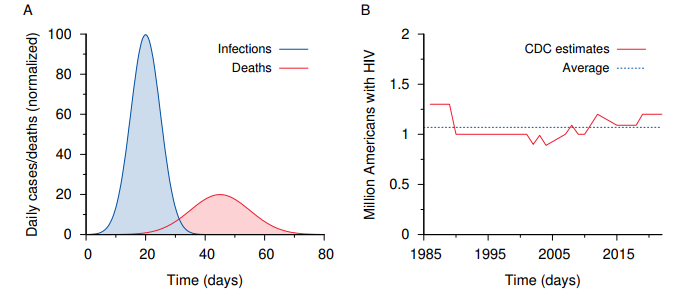
図81 急性伝染病に関するファーの法則と、米国人口におけるHIV感染の長期的傾向
A:免疫のない集団の中で新種の細菌が広がると感染者が増加するが、まだ感染していない感受性のある人の数が減少すると、その数はすぐに減少する。死亡も同様の時間経過をたどるが、数は少なく、病気の自然経過に依存する遅れがある。B:CDCの推定による米国人口におけるHIV感染の時間経過[342]。
アイゼンハワー大統領が1961年に警告した政府、大企業、学会の結合が、今や世界を支配している。この超国家的ネットワークは、疑問や訂正、撤回ができないドグマの押し付けによって少数派の意見や声を封じ込め、現状を守っている。私は、科学的、特に医学的ドグマに異議を唱える者を罰し、迫害し、苦しめ、黙らせる組織的専制主義を目の当たりにしてきた。情報の統制とその組織的な流布は、あまりに広く浸透しているため、人々は何が本当に起こっているのか、何が真実で何が真実でないのかを知ることができない。
8.1 エイズは新奇な伝染病のようには振る舞わない
エイズは伝染病のようにはふるまわない。[340, 341]。伝染病は概して、性別や人種を区別しない。しかしエイズはそうである。さらに、新奇な伝染病は集団全体に急速に広がり、ピークに達した後、数週間から数カ月にわたって釣鐘型の曲線を描きながら急速に減少する(図81A参照)。これはファーの伝染病の法則 [340, p.266]として知られている。
HIVに感染すると、臨床的なAIDSを引き起こすのに数年、あるいは10年以上かかると言われている。[340, p. 156, p. 297]。CDCは、米国では毎年約50,000人が新たにHIVに感染していると発表している。[343, 344]。しかし、1986年から2022年までの37年間!-「HIVとともに生きる」アメリカ人はおよそ100万人一定している(図81B参照)。これは、毎年同数のHIV陽性アメリカ人が死亡している場合にのみ起こりうることである。
8.2 AIDSと薬物乱用
AIDSの定義として当初考えられていた2つの臨床症状は、免疫抑制とカポジ肉腫であった。1984年の少なくとも2年前から、CDCは、ゲイ男性におけるこれら2つの疾患の発生が、ゲイのライフスタイル、特に娯楽用薬物、特にポッパーの多用と強く関連していることを認識していた[345, 346]。ポッパーズは、浴場での媚薬として、また肛門性交を容易にするための筋弛緩剤として、「速攻性」の男性同性愛者が吸入していた。ポッパーは化学的にはアルキル亜硝酸塩として知られているが、化学的に非常に反応性が高く、強力な発癌物質である。有機化学者である私自身は、化学用ヒュームフードの外ではボトルを開けることはないだろう。
ゲイのエイズ活動家、作家、ジャーナリストのジョン・ラウリッツェンが2022年3月5日に死去した。
2022年3月5日に死去した。1980年代初頭、彼はゲイ・コミュニティでレクリエーショナル・ドラッグの危険性について警告を流し始めた。1985年2月14日、ローリツェンは『Philadelphia Gay News』にエイズに関する最初の記事を掲載した: 「CDCの表はエイズと薬物の関係を隠している。彼は、CDCがポッパーとカポジ肉腫との関連を隠していることを示した。1993年、ローリツェンは、1985年までのエイズに関する主な著作をまとめた著書『エイズ戦争:医療産複合体によるプロパガンダ、利益供与、大量虐殺』[347]を出版した。
AIDSにかかったゲイ男性に関する公表された研究によれば、彼らの多くには性的指向以外に共通点があった。彼らは薬物乱用者であり、必ずしも静脈内麻薬とは限らないが、それにもかかわらず、クアールード(バルビツール酸様鎮静剤)、コカイン、亜硝酸塩吸入剤(ポッパー)、塩化エチル、アンフェタミン、チュイナル、バルビツール酸塩、アッパー系、ダウナー系など、さまざまな不健康な化学物質を常用かつ大量に使用していた。ローリツェンは、ゲイ・コミュニティにこれらの薬物の危険性を警告するために最善を尽くしたが、すぐにわかったように、彼のメッセージに対する敵意が広がっていたため、ゲイ向けの新聞にしか発表できず、それもその中のごく一部でしか発表できなかった。
8.3 ピーター・デュースバーグのHIV/AIDS仮説に対する科学的批判
1987年、ローリツェンはHIV/AIDS仮説に懐疑的であることを科学的に支持された。カリフォルニア大学バークレー校のウイルス学者で米国科学アカデミーの会員であるピーター・デュースバーグ教授が、権威ある雑誌『Cancer Research』の編集者ピーター・マギーに依頼されて発表した論文で、HIVはAIDSを引き起こすのに十分ではないと結論づけたのである。ローリッツェンは1987年7月6日付の『ニューヨーク・ネイティブ』紙でデュースバーグにインタビューした。デュースバーグは、HIVのようなウイルスは通常細胞を殺さないし、仮にHIVが細胞を殺したとしても、感染する細胞は非常に少ないので、その死が人の健康に深刻な影響を与えることはないと説明した。
ローリツェンの著書『エイズ戦争』に対する1994年の書評で、マイク・チャペルは次のように述べている[348]:
デュースバーグのような高位の科学者の結論、すなわちHIVはAIDSの原因にはなりえないという結論(そして、他の科学者たちによるこのテーマのバリエーションも増えている)は、今頃はヘッドラインを賑わしているはずだと期待されるかもしれない。しかし、少数の例外(特にロンドンの『サンデー・タイムズ』紙)を除いては、そうはなっていない。とはいえ、HIVとエイズの関連性が明らかになったことで、ローリツェンは最終的に「エイズは存在しない」という驚くべき結論に達することができた。
エイズの最初の10年間、アメリカでは10人の感染者のうち9人が男性であり、主に男性の同性愛者と異性間の静脈麻薬使用者であった。1993年にCDCが子宮頸がんをエイズを定義する病気のリストに加えた後も、アメリカ人女性は頑なにエイズを拒否した。例えば、CDCがエイズを定義する病気の統計を報告した最後の年である1997年には、子宮頸がんは全エイズ患者のわずか1%しか占めていなかった[349]。
エイズは明らかに感染しない。信じられないような話かもしれないが、エイズ、あるいはHIVが性行為によって感染するかどうかを決定するための科学的研究は、これまで一度も計画されたことも実施されたこともない。証拠がないため、AIDSとHIVの性的感染は公然の「真実」となっている。
8.4 HIVは性感染しない
HIVが属するウイルスファミリーであるレトロウイルスに関する文献は、100年以上前にさかのぼる[340, 341]。地球上のすべての人や動物は、そのゲノムに50から100、あるいは1000の休眠レトロウイルスを保有している[350]。ヒトゲノムの最大8%がレトロウイルスで構成されていると推定されている。[351]。3,000種類以上のレトロウイルスがカタログ化されているが、現在までにヒトに病気を引き起こすことが証明されたものは一つもない。
少なくとも70年前から、科学者たちはレトロウイルスが感染した細胞を殺すことはなく、性感染もしないことを知っていた[340]。レトロウイルスは性行為で感染しないため、ネズミの異なる系統のレトロウイルスを混ぜても、異なる系統の性行為のパートナーに感染することはない。これはヒト、類人猿、サル、ネコにも当てはまる。
実験動物で使用されたHIVの実験バージョンは、ウイルスのないセックス・パートナーに性感染することが示されたことはない。HIVの異性間感染の効率を測定しようとした世界最高の対照ヒト研究は、ナンシー・パディアンとその同僚によって行われた[352]。この10年間の研究の最も顕著な結果は、HIV陽性のパートナーとの長年にわたる無防備な性交渉から、HIV陰性のセックスパートナーが誰一人としてHIV陽性にならなかったことである。繰り返すが、10年間の研究期間中、HIV陰性のセックス・パートナーで陽性になった人は一人もいなかった。したがって、観察された感染効率はゼロであった!
しかし、HIVの性行為感染ゼロという報告を避けるために、パディアンと同僚は、彼らの研究に参加したHIV陽性のセックスパートナーは、研究に参加する前に性行為によって陽性になったに違いないと仮定した。この仮定を用いると、HIV陰性の女性が自分がHIV陽性になるまでには、HIV陽性の男性と1,000回性交渉を持つ必要があると推定される。さらに驚くべきことに、彼らはHIV陰性の異性愛男性がHIV陽性になるまでに8,000回の性交渉が必要であると推定した。ほぼ同じ図が他の研究者からも報告されている[350, 353, 354]。
これらの図から考えると、「100万人のアメリカ人がHIVとともに生きている」というCDCの推定は、HIVの性的感染を想定する上で非常に大きな問題を提起している。エイズ騒動が起きていた頃、アメリカには約2億8000万人の男女がいたのだから、HIV陰性の女性がHIV陽性になるには、平均して14万回、男性ならその8倍もの不規則な性交渉が必要になる。このような途方もない数の性交渉は、売春婦でさえ手の届かないものである。このような背景から、CDCが娼婦との性交渉をエイズのリスクカテゴリーに挙げていないのも、ある程度納得がいく。ルート・バーンスタイン[355]によれば、「売春婦と性的関係を持ったことがあり、(薬物乱用などの)他の危険因子が認められず、その後HIVに対する抗体を獲得したアメリカ人やヨーロッパ人の異性愛者の数は、片手の指で数えられるほどである」薬物乱用をしていないアメリカの売春婦は、他の女性に比べてエイズに感染するリスクは高くない[356]。ドイツ、チューリッヒ、ウィーン、ロンドン、パリ、パルデノーネ(イタリア)、アテネの売春婦も同様である[357-361]。
8.5 HIVがAIDSの原因であるという証拠を求めるKary Mullisの探求
1988年、ポリメラーゼ連鎖反応(PCR)の発明で1993年のノーベル化学賞を受賞したカリー・ミュリスは、自分が書いたばかりの文章を裏付ける文献を必要としていた: 「HIVがエイズの原因である可能性が高い。彼は、HIVが確かに「AIDSの原因である可能性が高い」ことを証明した人物を引用したかったのである。その人物は、ノーベル賞の候補になるに違いないと思われたが、名前がなかったのである。1994年、マリスはHIVの発見者であるリュック・モンタニエに、誰を引き合いに出すべきか尋ねる機会を得た。しかし、モンタニエでさえ知らなかった。2000年、モンタニエ自身、HIVがAIDSを引き起こすというAIDSドグマの中心的特徴を否定するようになった[362]。
マリスは、アンソニー・ファウチのエイズに対する誤った扱いや、ウイルスの検出や感染症の診断にPCR検査を用いることを提唱する人々を率直に批判するようになった。ロンドンの『サンデー・タイムズ』紙のインタビューで、マリスはこう述べている[363]:
HIVがエイズの原因である可能性が高いことを示す文献を教えてくれるウイルス学者は一人もいない。これほど重要な問題であれば、科学的な文書がどこかにあるはずで、アクセス可能な人々によって書かれた研究論文がそれを実証しているはずである。しかし、それがない。ウイルス学者にその情報を求めても、答えは返ってこない。
1モンタニエが2008年にノーベル賞を受賞したのは、HIVを発見したからであり、HIVがAIDSの原因であることを証明したからではない。
マリスはPCR検査によって世界的なCOVID-19詐欺が開始される直前の2019年8月7日に死亡した。
2020年4月、モンタニエは、スパイクプロテインをコードする遺伝子にHIVの遺伝子配列が挿入されたため、SARS-CoV-2が実験室で作られたと結論づけた[364]。モンタニエは、COVID-19に対する「ワクチン接種」の世界的な推進を批判したわずか8カ月後の2022年2月8日に死去した[365]。
8.6 反体制派の磔刑
デュースバーグのHIVの原因究明に対する攻撃は、科学文献の中でまったく反論の余地のないものであった。それは、科学者たちの間で、デュースバーグの主張が少なくとも説得力があり、反論の余地のないものである可能性が高いことを暗黙のうちに認めていたからである。ピーター・デュースバーグは、最も信憑性が高く、根気強く、効果的なAIDSドグマ批判者として、アンソニー・ファウチの殺害予定者リストのトップにいた。米国保健社会福祉省(HHS)は、デュースバーグの考えを世間に知られないよう「封じ込める」ことを決定した。デュースバーグのCancer Research論文が発表されてから2カ月後の1987年4月28日、HHS長官室のチャック・クラインは”Media Alert “を発信した[366]:
NCI[国立癌研究所]の助成科学者であるカリフォルニア/バークレーのピーター・デュースバーグ博士が、ガロ博士とモンタニエ博士が同定したHTLV-III/HIVウイルスはエイズの原因ではなく、エイズはウイルスでない可能性もある「まだ同定されていない病原体」によって引き起こされると結論する論文を科学雑誌に発表した。
不可解なことに、この論文は3月1日付の『キャンサー・リサーチ』誌に掲載され、ロバート・ギャロ博士らのクレジットが明記されていないが、4月27日(月)にニューヨークのゲイ出版社から公表されるまで、同局内でもニュース・メディアでも誰もこの論文に気づいていなかったようだ。
デュースバーグ博士はNCIの助成金を受けて17年間レトロウイルスと癌遺伝子の研究をしており、高く評価されている。彼はNCIから「優秀研究者賞」を授与されている。この論文は通常の出版前手続きを経ており、NIHで査読されるはずであった。
そうでなければ、2カ月近く前に出版され、大きな反響を呼ぶはずであった。
劇作家であり、ゲイの活動家であり、NIHの批評家でもあるラリー・クレイマーが現在、この論文をメディアに取り上げているが、まだ話題にはなっていない。例えば、彼はトム・ブローコーにこの件について話したことがある。『ニューズデイ』紙からCDCに電話があったのは1件だけで、プレスオフィスには今のところ1件もない。
これは明らかに多くの論争を巻き起こす可能性がある(もしこれがウイルスでないなら、血液供給が安全だとどうしてわかるのか?もしこれがウイルスでないなら、血液供給が安全だとどうしてわかるのか?あなた方はどうしてそんなに愚かなのか、どうしてまたあなた方を信じなければならないのか)、私たちは対応する準備をしなければならない。私はすでにNIHの広報に、この件について調査を開始するよう依頼している。
チャック・クライン cc:
長官
次官参謀長
保健担当次官補外相
ホワイトハウス広報次官補
第二次世界大戦以来、しかし特にここ数十年の間に、米国では事実上すべての主要な科学分野において、議論の抑制と異論者の迫害が定着してきた。いわゆる生物医学の分野では特にその傾向が強い。
国立衛生研究所(NIH)、国立癌研究所(NCI)、疾病管理センター(CDC)は30年以上もの間、デュースバーグ教授を黙らせ、処罰するためにあらゆる手段を用いてきた。HIVに疑問を呈する以前、デュースバーグ教授はNIHから癌研究者として継続的に資金援助を受けていた。
しかし、1987年に『Cancer Research』誌にAIDSのドグマに疑問を投げかける招待論文を発表した後[367]、あっと言う間にデュースバーグは政府からの助成金をすべて失った。1990年代初頭以来、彼に新しい大学院生はいない。いくつかの一流科学雑誌は彼の研究の掲載を中止している。終身在職権があるため、デュースバーグは解雇できない。このため、カリフォルニア大学バークレー校は、デュースバーグが自発的に去ることを願いながら、彼を疎外し、辱め、罰を与え続けてきた。
8.7 アフリカのエイズ
ほとんどの人は、CDCとそれに追随する世界保健機関(WHO)が、まったく異なる2つのエイズ流行を定義していることを知らない。アメリカ人、ヨーロッパ人、その他の裕福な国々には一つの定義があり、アフリカ人、アジア人、ラテンアメリカ人などには全く異なる定義がある。おわかりだろう。この奇妙な状況の理由は、エイズは住んでいる場所によって全く異なるからである。実際、レーガン政権はWHOに対し、「第三世界」におけるエイズの定義を作るよう求めたほどである。1985年、中央アフリカ共和国の首都バンギで開かれた会議で、アフリカにおけるエイズは、発熱、下痢、しつこい咳、体重減少を含む症状の福袋と定義された[368]。このリストに、1990年代半ばには結核が加わった。これらの長年認識されてきた貧困と栄養失調の病気は、今日に至るまでアフリカにおけるエイズの診断の基礎となっている。驚くべきことに、HIVは定義に含まれていなかった!バンギの定義を使えば、アフリカのエイズは何百年も前から存在していたと言える。
ジョージ・オーウェルの代表作『1984年』では、『ニューズウィーク』誌の表紙がこう問いかけている: 「ブラックアフリカは救えるか?レーガン政権が、エイズはアフリカで始まり、ウイルスが原因だと世界に発信したわずか数ヵ月後のことだった。その2年後、同じ雑誌に「ペスト時代のアフリカ」という記事が掲載された。著者はこう伝えている: 「ウガンダ南西部のラカイ地域ほどこの病気が蔓延しているところはなく、30%の人々が血清陽性(HIV)であると推定されている(断定はしていない)[369]」
1995年、世界保健機関(WHO)は火に油を注いだ: 「1991年半ばまでに、推定150万人のウガンダ人、すなわち一般人口の約9%、性的に活発な人口の20%がHIVに感染していた」[370]。その後数年にわたって同様の報告が繰り返し発表され、人口の30%もの人々が早死にする運命にあり、家族や社会全体に悲惨な結果をもたらすと予言された。この予言は、世界的な流行の発祥の地であるはずの国の崩壊が、事実上避けられないことを告げていた。
今日、ウガンダのエイズに関する記事を目にすることはほとんどないが、それはこうした予言がすべて誤りであることが証明されたからである。ウガンダ統計局[371]は2002年の国勢調査で、ウガンダの人口は1991年から2002年の間に年平均3.3%の割合で増加したと報告している。人口増加率の高さは、主に過去40年間続いている出生率の高さ(女性1人当たり約7人)によるものである。乳児死亡率は、1991年の国勢調査では1,000人当たり422人であったが 2002年には1,000人当たり83人と減少傾向にある。
ウガンダの人口増加率は、1980年から1991年にかけて2.5%であったが、その後の10年間でさらに増加した。ウガンダの人口増加率は現在、世界で最も高い水準にある。にもかかわらず、一般メディアは、サハラ以南のアフリカ全体が30年以上にわたるエイズの結果、大規模な荒廃と人口減少に見舞われたと報じ続けた。このような主張にもかかわらず、統計からは、中世のヨーロッパの疫病に匹敵する規模のアフリカのエイズによる大惨事の証拠を見つけることは極めて困難である。
2001年までに、アフリカでは累計1,093,522人のエイズ患者が発生したと報告されている[372]。しかし、この間(1980年から2000年の間)、サハラ以南のアフリカの人口は3億7800万人から6億5200万人に増加しており、これは年率3.6%に相当する!もちろん、このような背景から、エイズによって通常より多い100万人の命が失われる可能性を統計的に検証するのは難しい:
- 1.この損失は、1999年のアメリカの全人口に相当する2億7400万人の圧倒的な同時増加によって矮小化される;
- 2.バンギの基準によれば、アフリカのAIDSを定義する病気は、従来のアフリカの罹患率と死亡率と区別がつかない[370]。
2019年5月現在、サハラ以南のアフリカの人口は10億8000万人に増加している。1980年と比較すると7億人の増加であり、これは米国の人口の2倍に相当する!アフリカでエイズの流行が始まったとされる時期から、サハラ以南のアフリカの人口は爆発的に2.8倍に増加した。
サハラ以南アフリカの爆発的な人口増加と、アフリカのエイズとアメリカやヨーロッパのエイズとの間の多くの疫学的、臨床的な違いは、アフリカのエイズ流行の存在に疑問を投げかけている。実際、入手可能なデータはすべて、貧困に関連した感染症がアフリカで恒常的に流行し、それが「AIDS」という新しい名前を与えられただけである。
8.8 AIDSの真実に迫ろうとするタボ・ムベキの不運な試み
このような歴史を認識し、自国の「科学者は本を読まない」という不穏な事実に直面した南アフリカのタボ・ムベキ大統領は、1999年にこう問いかけざるを得なくなった。なぜアフリカのエイズは、北米や西欧のエイズとは大きく異なるのか?これらの疑問やその他の疑問に対する答えを得るために、彼は2000年に大統領エイズ諮問委員会を設置した。
エイズを完全に理解するために、国際的な専門家パネルを南アフリカに招き、このテーマに関する問題を審議する場を提供することが決定された。これらの審議の結果は、エイズに対処するための最も適切な行動指針を政府に伝え、助言するために使用される。この決定は 2000年4月に南アフリカ政府の閣議で承認された。基礎科学者、医師、歴史家、経済学者から公衆衛生の専門家や政策立案者まで、AIDSとHIVの分野における著名な専門家を世界中に探し求めた。さらに、エイズ患者だけでなく、一般市民もパネルに招かれることが決定された。
アパルトヘイトの歴史と折り合いをつけてきた南アフリカの最近の経験は、ムベキに反対意見を取り入れる必要性を教えていた。ムベキのエイズ諮問委員会の3分の1は、エイズのドグマに疑問を持つ世界中の科学者や医師で構成された。諮問委員会の2回の会議の結果、広範な報告書が作成された[373]。
しかし、この諮問委員会に反体制派の科学者が参加したことは、エイズ正統派の一部の代表や米国政府には受け入れられなかった。「国境なき医師団」の代表は、「1発の銃弾、1人の反体制派」と書かれた看板を掲げて、南アフリカのダーバン市を行進し、エイズ諮問委員会の科学者たちが、ムベキが質問したのと同じエイズに関する質問への回答を求めていることに抗議した(図82)。また、反体制派を投獄せよ、あるいは米国憲法を改正して彼らの発言を禁止せよと主張する者もいた。

図82 2000年7月14日から20日にかけて南アフリカのダーバンを行進し、エイズがHIVによるものであるか否かに疑問を呈する科学者たちに抗議するHIV陽性者たち
『Mail & Guardian』16巻28号8ページ。
こうした抗議と反体制派を黙らせる努力が進行している間、ムベキのAIDS諮問委員会のオブザーバーは次のように指摘した[373, p. 45]。
パネルの審議は常に、南アフリカにおけるエイズ問題の大きさ、あるいはHIVの有病率に関する正確で信頼できるデータや統計がないことに悩まされていた。そのようなデータや統計を何度も要求したが、南アフリカのパネリストも保健省の役人も、そのようなデータを提供することはできなかった。
主流のAIDS研究者たちは、南アフリカがアフリカで最も優れた統計を持っていることに同意したが、同じ専門家たちは、1994年から2001年まで、南アフリカは年間約2%の人口増加率を記録していることを指摘しなかった。この間、全死因死亡率は上昇したが、政府統計によれば、HIVに起因する死亡は全死因死亡のごく一部に過ぎなかった。
2000年5月、南アフリカの首都プレトリアでオープンフォーラムが開催された。その目的は、アフリカにおけるAIDSの中心的な問題について議論し、政府の具体的な質問に答えることで、政府がどのようなAIDS政策をとるべきかを決定するのに役立つ、入手可能な最良の証拠を提示することであった。政府は、国際的に認知されたエイズの権威を招聘し、彼らはパネルの3分の2を占めたが、残りの3分の1は国際的な批評家の”Who’s Who “であった。
ムベキ大統領のエイズ諮問委員会を妨害するために、エイズ関係者は初日からあらゆる手を尽くした。エイズはHIVに感染して発症するという考え方は、アメリカ政府の保健福祉省が発祥であるため、クリントン政権はムベキ大統領のエイズ・ドグマを否定し、エイズの原因に関する公開討論を阻止しなければならなかった。しかし、ムベキの招待を単に拒否することは、米国とそれに追随する他の政府にとって、政治的にあまりにも受け入れがたいことだった。結局のところ、当時の世界の指導者たちは、アパルトヘイトの抑圧から抜け出したばかりの南アフリカの新しい民主主義を支援することに全力を注いでいたのである。南アフリカ政府に恥をかかせないよう、米国はしぶしぶエイズ当局の代表団を派遣した。アンソニー・ファウチの欠席が目立った。
和解不可能なものを和解させようとしたムベキの努力は失敗に終わった。
主流派のパネリストたちは、誠実に議論に参加しないことで合意していたか、事前に指示されていたことは最初から明らかだった。招待されたパネリストたちが席に着いてすぐの最初の会議で、あからさまな挑発が起こった。アフリカ系アメリカ人の「医師」3人が、まるでFBI捜査官のような身なりで、ダークなスーツを着て、険しい表情をしていた。彼らが全員黒人であることは誰も気づかなかった。招待されたパネリストとは対照的に、新顔を識別するためのネームプレートはなかった。アフリカの代表団の何人かは、突然のよそ者の登場に憤慨していた。会議が始まる前から、その雰囲気はおかしくなろうとしていた。
クリントン大統領が無名のパネリストを加えるようムベキに頼んだという噂が瞬く間に広まった。ムロンゴ教授は、パネルと司会者にその噂が本当かどうか尋ねたが、答えは返ってこなかった。やがて、ムベキの事務所から女性が現れ、クリントンがこの人たちの参加を要請したのは事実だと言った。クリントンの目や耳として威嚇的な存在感を示していた以外には、この見知らぬ人たちが会議に貢献した記憶はまったくない。
いざ会議が始まると、主流派のパネリストたちは参加することを全面的に拒否し、会議を頓挫させるためにあらゆる手を尽くした。ピーター・デュースバーグが最初のプレゼンテーションを行おうとしたとき、誰かが大声で異議を唱えた。中立とは言い難い司会者(カナダの法学教授スティーブン・オーウェン)は、データを発表するなという主流派の要求に応じ、科学的な意見交換という建前さえ崩してしまった。このことは、パネル議事録の公式報告書 [373, p. 108]にも記されている:
パネルの審議の性質と形式は、根本的な性質の科学的問題をめぐる多くの相違を解決するために必要な、綿密な科学的議論を可能にするものではなかった。
ヨハネスブルグで開催されたパネルの第2回会合は、第1回会合よりも明らかに専門的な印象を与えた。南アフリカ政府高官は、第1回会合での主流派の妨害、特に第2回会合の議題を出すためのインターネットでの議論をボイコットしたことへの怒りと不満を表明した。政府は、主流派が独自のインターネット討論会を立ち上げ、ムベキ委員会の他のメンバーに参加しないよう促していたことを知った。主流派は自分たちのエイズドグマを武器に、密かに国際的な電子メールキャンペーンを展開し、ムベキのエイズ諮問委員会の信用を失墜させ、無力化することを目的としたダーバン宣言に至った。
ダーバン宣言は、6月の第2回パネル会議の直前に発表された。その数日後、この宣言は『ネイチャー』誌に掲載された[375]。この18パラグラフの文章の目的は、エイズのドグマに対する批判をきっぱりと止めることだった。AIDSパネルの正統派メンバーの多くが署名した。激怒した南アフリカ政府は、データ提示の禁止を解除し、正統派のパネリストたちを辱め、今度は真の科学的議論をさせようとした。しかし、遅きに失した。
南アフリカ放送協会(SABC)は、政府からエイズパネルの生中継の許可を得ていた。しかし、もしそれが許されるのであれば、主流派メンバーは参加を拒否した。そこで政府は譲歩し、SABCは除外された。とはいえ、パネルの全過程は政府によってビデオ録画された。パネルには、そのビデオと記録はいずれ世界に公開されるだろうと言われていた。もちろん、これは実現していない。南アフリカ国民と世界は、これらのビデオを見る権利がある。主流派の妨害と行動のビデオ記録を公開することは、少なくともニクソンのウォーターゲイト・テープと同じくらい爆発的で、米国を困惑させ、損害を与えるだろう。
エイズドグマの擁護者たちは、歴史的に効果的であった言葉の暴力に必ず頼る。とりわけ反体制派は、平地主義者、否定論者、殺人者、精神病質者、非倫理的、アフリカの血が指から滴る不道徳者であると非難される。もしそのどれかが真実であれば、ムベキ大統領のエイズ諮問委員会は、正統派にとって、エイズが実際には伝染性であり、性行為によって感染し、HIVというウイルスによって引き起こされるという説得力のある証拠を南アフリカ政府や世界中の人々に示す絶好の機会となるはずだった。ムベキが特に要求したように、有毒な抗HIV薬が実際には害よりも効き目があるという証拠を南アフリカ政府に示すこともできたはずだ。それがどのように悪いことなのか、理解するのは難しい。
8.9 エイズの正統性に異議を唱えるいくつかの証拠
主流派の立場からすれば、南アフリカでの会議は、エイズは伝染性ではなく、性行為感染でもなく、HIVが原因でもないという反体制派の立場を正統派が公に抹殺する絶好の舞台となるはずだった。その代わりに、彼らはダーバン宣言を作成した。同席した反体制派を除いては、エイズ・パネルで反体制派に確かな科学的証拠を突きつけて論破することを怠った正統派を諫める者はどこにもいなかった。以下は、パネルの主流派が公の場で検証したがらなかった証拠の例である。
もしHIVが本当に性感染症であるなら、その有病率は他の性感染症の有病率と似ているはずである。しかし、図83は、南アフリカの州の妊婦の性感染梅毒とHIVの有病率の間に負の相関があることを示している[369, 376, 377]。同様の結果がウガンダとタイでも報告されている。また、梅毒とHIV有病率の間には経時的な反相関がある。[376]。ここでもウガンダとタイで同様の結果が報告されている。
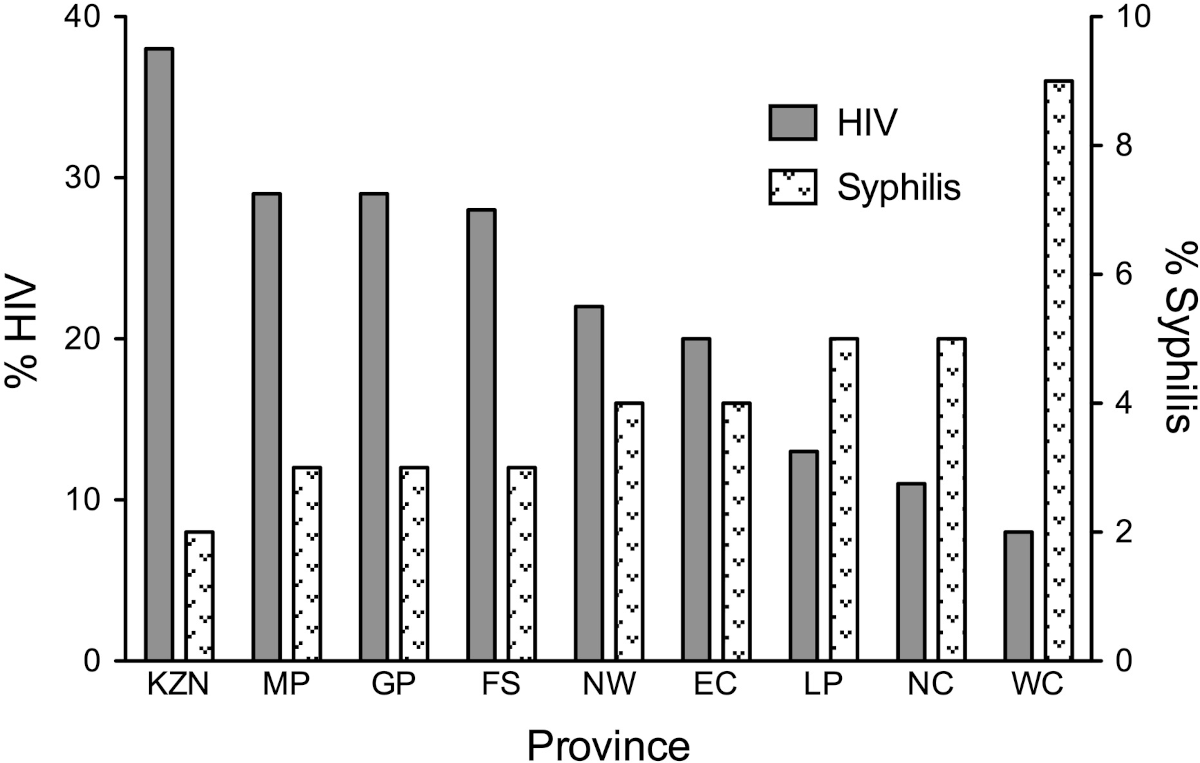
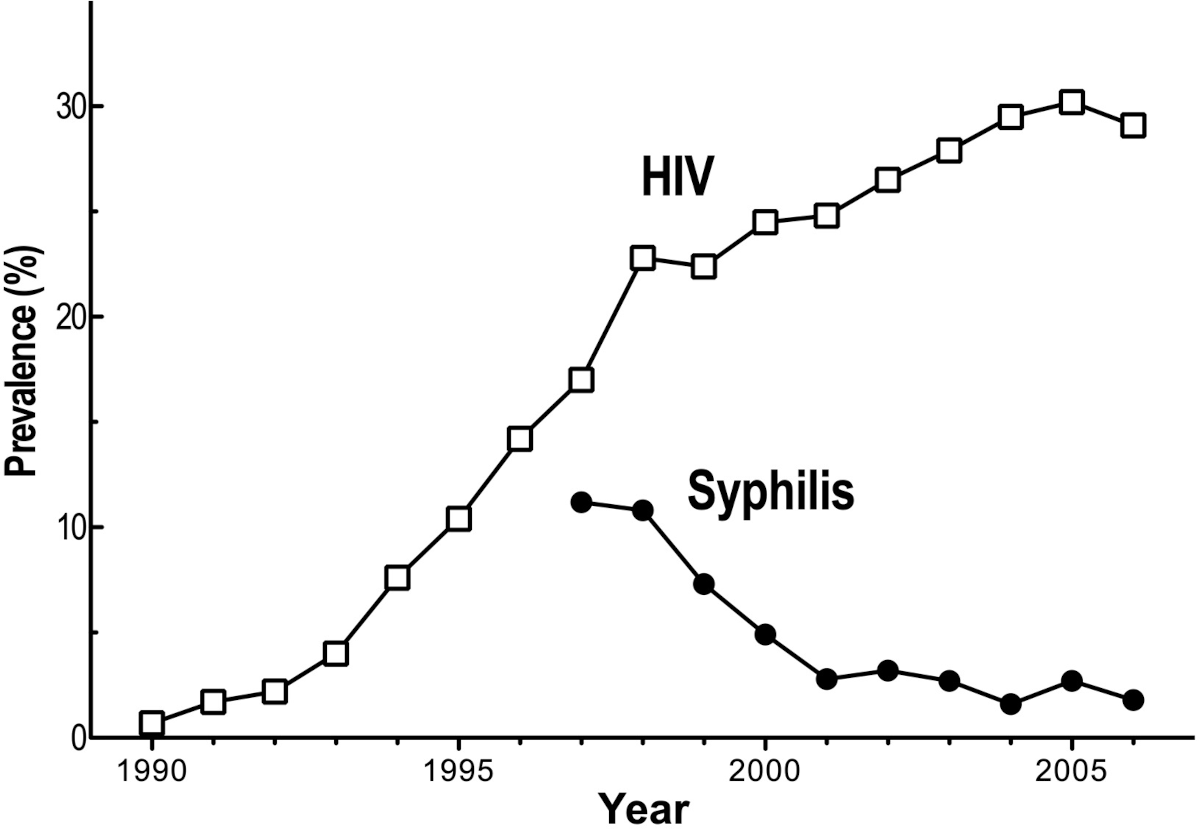
図83 南アフリカにおけるHIVと梅毒の有病率の負の相関[376]
A:2000年の妊産婦クリニック受診者におけるHIVと梅毒の有病率(州別)。州: クワズール・ナタール州(KZN)、ムプマランガ州(MP)、ハウテン州(GP)、フリーステート州(FS)、ノースウエスト州(NW)、東ケープ州(EC)、リンポポ州(LP)、北ケープ州(NC)、西ケープ州(WC)。B: 南アフリカの妊産婦クリニック受診者におけるHIVと梅毒の全国的流行傾向 4. 1997年以前の梅毒のデータは入手できなかった。
このような歴史があり、エイズが伝染性であり、性感染症であり、アフリカの人口減少をもたらすという科学的証拠がまったくないにもかかわらず、CDC、ファウチのNIAID、WHOなどは、HIVがエイズを引き起こすと主張し続けている[374]。
9. まとめと結論
本書の主な目的は、以下の疑問を解決することである:
COVID-19の経験から、将来のmRNAワクチンの安全性について何がわかるだろうか?
エビデンスを調査してわかったことを踏まえて、この問いに答えてみよう。
9.1 mRNAワクチン毒性の重要なメカニズム
私たちは、COVID-19に対するmRNAワクチンで観察された毒性を説明しうる、少なくとも3つの潜在的な病態メカニズムに遭遇した:
- 1. 脂質ナノ粒子の化学的毒性、
- 2.ワクチンによって発現が誘導されるスパイクタンパク質の直接的毒性、および
- 3.スパイクタンパク質に対する免疫反応の破壊的影響である。
これらのうち、我々は3番目のものが最も重要であると考えている:
- 1. 第3章で示した理論的考察から導かれる。
- 2. 第4章で述べられているように、スパイクタンパク質の発現巣の近くで観察される、強い炎症と免疫細胞、特にリンパ球による浸潤という病理組織学的所見を説明できる。
このメカニズムに有利な第三の考慮点は、ワクチン注射を繰り返すと有害事象の発生率と重症度が増加することであり、これは第7章で述べられている。対照的に、カチオン性脂質の化学的毒性は特定の免疫系に依存しないため、各注射後に同程度の強度になると予想される。
さらに、アストラゼネカとジョンソン・エンド・ジョンソンが製造しているアデノウイルスベースのワクチンは、カチオン性脂質を含まないにもかかわらず、有害事象のプロファイルがmRNAワクチンとかなり類似している。スパイクタンパク質の直接的毒性は特異的抗体によって抑制されるはずであり、従って、繰り返し注射することによって、その強度は増加するよりもむしろ減少するはずである。
従って、全体的にはmRNAワクチンによってコードされた抗原を発現する細胞に対する免疫介在性攻撃が主要な病因メカニズムであると結論づけられる。しかし、これは他の2つの危害メカニズムが否定されるべきだという意味ではない。スパイクタンパク質の直接作用は、特にウイルスに対する既存の免疫のない患者において、初回注射後の早期有害事象の一因となる可能性は十分にある。カチオン性脂質の毒性も、以下の理由から否定することはできない:
- 1. 機能不全に陥ったCOVID-19ワクチンの承認プロセスにおいて、これらの物質に関する安全性研究はほとんど実施されなかったが、実施された初歩的な研究では毒性が明確に示唆された(セクション6.1参照);
- 2.カチオン性脂質による活性酸素種(ROS)の誘導(セクション5.3.3参照)はDNA損傷を引き起こす。この損傷は、脂質そのものが除去された後でも残るため、毒性は累積することになる;
- 3. 陽イオン性脂質はすべてのmRNAワクチンの必要成分であるため(セクション5.1.4参 照)、その毒性は、単一のmRNAワクチンの全投与量にわたってではなく、すべての mRNAワクチンの全投与量にわたって蓄積する。
9.2 害の免疫学的メカニズムは完全に一般的である
第2章と第3章で、免疫反応を引き起こすのに必要なのは、何らかの非特異的な炎症刺激と組み合わされた外来抗原の存在だけであることを見てきた。将来のmRNAワクチンはすべて、標的とする微生物に関連した独自の特異的抗原を産生するように我々の細胞を誘導する。したがって、そのようなワクチンは、COVID-19に対するワクチンと同じような規模の免疫学的損傷を引き起こすと予想しなければならない。
9.3 適正製造規範に戻れば、mRNAワクチンの毒性はなくなるのか?
COVID-19のmRNAワクチンに関して、かなり驚くべき観察がある。よく文書化された汚染にはプラスミドDNAや金属粒子が含まれる(セクション5.4.1)。さらに、ロットごとに報告された有害事象の数に非常に大きなばらつきがあること(セクション5.4.2)は、製造基準が非常に一貫していないことを明確に示している。もしこれらの汚染物質が除去され、一貫した基準が守られれば、mRNAワクチンの毒性の脅威はなくなるのだろうか?
考慮すべき点が2つある。ひとつは、観察された主要な毒性メカニズムは、ワクチンが意図したとおりに機能した結果であるということである:ワクチンは我々の体細胞に抗原の発現を誘導し、抗原に対する免疫応答はそれらの細胞を殺す。従って、製品の品質がより安定したものになれば、犠牲者の数は減少するどころか、むしろ増加すると予想せざるを得ない。
第二に、DNA汚染についてである。セクション6.3で指摘したように、ワクチンに含まれるプラスミドDNAがもたらすリスクは2つある。第一に、ゲノムを傷つけ、がんや白血病を引き起こす可能性があること、第二に、抗原の発現が長期化し、抗原に対する免疫反応の持続期間と重症度が増すことである。したがって、ワクチンからDNAを効果的に除去できれば、ワクチンの毒性は軽減されるはずである。しかし、ワクチン接種後数日間は、抗原の発現は主にmRNAそのものに依存している可能性が高い。例えば心筋炎、脳卒中、心臓発作などである(第7章参照)。従って、DNAの混入を避けることでmRNAワクチンの毒性をなくす、あるいは従来のワクチ ンで “許容範囲内 “とされるレベルまで減らすことができるとは考えにくい。
9.4 mRNAワクチンが本質的に危険であるならば、なぜ私たちに接種が促され、強要さえされるのか?
現時点では、藪をつつく必要はない。当局の行動を “正直な間違い “と解釈することはもはや不可能である。遺伝子ベースのCOVID-19ワクチンの背後には、不吉な意図があることを明白に示すことが、あまりにも多く起こっている。必要性のない急ぎの承認、明白な脅迫と強制、正直な科学に対する組織的検閲、多数の死亡または重傷を負ったワクチン被害者に関する真実の抑圧は、すべて意図と目的について疑いを持つことを許すには、あまりにも長い間続いてきた。われわれの政府や国内外の行政機関は、われわれ全員に対して宣言されていない戦争を仕掛けているのである。第8章でデイヴィッド・ラズニックが指摘しているように、この戦争は何十年も続いており、今後も続き、エスカレートしていくことを予想しなければならない。
9.5 私たちに何ができるのか?
何よりもまず、私たちは自分たちが政府から狙われていることを受け入れなければならない。科学や医学の既成の場であろうとなかろうと、自分自身で調査し、誠実な健康アドバイスをどこにでも求めるのである。本書が、その一歩を踏み出す一助となれば幸いである。
あとがき
キャサリン・オースティン・フィッツ、ソラリ・レポート社長
それゆえ、あなたとあなたの子孫の両方が生きるために、いのちを選びなさい。
申命記30:19
COVID倫理のための医師団によるmRNAワクチンの毒性を読んで学んだことについて、考慮すべきことがいくつかある。
mRNA技術は人を殺し、人を傷つけるという確信、そしてCOVID-19の予防接種を作り、世に送り出した人々はそれを知っていたという確信、これは何物にも代えがたい知性である。この知識を持つことは、あなた自身とあなたの愛する人々を守る力を与えてくれる。あなたがそうすることは、これらの危険性を理解し伝えるために働いてきた医師、科学者、研究者のネットワークにとって最も重要なことである。
この3年間、mRNA技術の致死性を暴露する手助けをしてきた医師や科学者の多くは、調査を始めたときには、何が見つかるかほとんど、あるいはまったく予想していなかった。彼らは著名な地位についていたり、退職していたりした。彼らは、科学界、医学界、科学と医学を支える学術機関、そして政府とその規制機関といった体制に信頼を寄せていた。また、彼らは多忙な生活を送っており、腐敗が進むことの危険性を理解しながらも、欧米諸国を含む全世界でこのような手段で大規模な残虐行為が実行される可能性があるとは認識していなかった。しかし、事実を知ったとき、彼らは向き合うべきことに向き合い、耐え抜いた。
彼らの中には、地位や肩書きを失った者もいる。収入や福利厚生を失った。数え切れないほどの時間、無報酬で働いてきた。メディアの誹謗中傷や偽情報の標的にされた。根拠のない調査や訴訟、訴追の対象となった者もいる。医師免許を失った者もいる。家や家族、友人を失った人もいる。毒を盛られたり、暗殺されたりした人もいると思う。そして、彼らの警告に耳を貸そうとしない友人や家族が病気になり、命を落としたとき、誰もが深い悲しみと挫折を味わった。
彼らの犠牲の積み重ねは、あなたへの無償の贈り物であり、あなたが自分自身と愛する人たちを守ることを選択し、他の人たちにも同じことをするよう促すためのものなのだ。私たち一人ひとりが、このかけがえのない贈り物を他の男女に伝えることで、健康と生命を手に入れるチャンスが増える。
科学と医学への貢献の結果、あなたやあなたの愛する人たちが生きることができ、あなたの子供たちが健康で豊饒に育ち、将来同じような世代を生み出すことができる。
あなたが学んだことは、かけがえのない知性かもしれないが、便利なものではない。mRNA技術が人を傷つけ殺すという事実は、重大な意味を持つ。誰がこの技術を応用しているのかを考えると、mRNA技術だけでなく、私たちの日常生活や財政の数多くの側面に関わる、はるかに広範な問題についてである。
信頼できる機関のリストから外れるのは、軍や健康を規制する機関を含む政府である。製薬業界もリストから外されている。リストから外されているのは、mRNAワクチンを推進するために、そしてそれ以前にも、有害でしばしば致死的なCOVID-19治療を実施するために、多額の報酬を得ていた多くの医師や病院である。リスト外のメディアは、世界中の人々の心を戦争に巻き込み、恐怖で満たし、人々とその子供たちをmRNAの “キルボックス “に誘導した。
また、mRNAの技術が人を傷つけ、殺すものだと知っても驚かなかった勇気ある人々もたくさんいた。本書の序文を書いたメアリー・ホランドもその一人である。メアリーは『Turtles All the Way Down』の共同編集者であり、ワクチン産業を支えるために使われた嘘の連鎖についての手強い論評である(原著は2019年にヘブライ語で出版された)。メアリーとロバート・F・ケネディ・ジュニア、そして『Children’s Health Defense』の仲間たちは、危険な医薬品の猛攻、食品システムの堕落、EMF放射線の増加、その他の環境毒や毒性から子どもたちを守るために長年活動してきた。もう一人の勇気ある人物は、本書の中で、mRNAワクチンを製造し、資金を提供し、供給する規制インフラの多くの側面を設計し、資金を提供するために使用されたHIV/AIDSの嘘に関する章を執筆したデビッド・ラスニック博士である。
参考記事

私もまた、mRNA技術の意図的な破壊的効果に驚かないグループの一人だった。アメリカ政府から何兆ドルもの資金が消え始めた後、私は2000年からアメリカ人に、私たちの老後と社会的セーフティネットは単純な数式に依存していると警告し始めた。何兆ドルも盗まれるのを許し続ければ、他の方法で帳尻を合わせることになる。その方法とは、経済的・健康的給付の縮小や膨張、定年退職年齢の引き延ばし、平均余命の意図的引き下げ、あるいはそれらの組み合わせなどである。実際、この20年間、さまざまな政策が平均余命を確実に低下させてきた。現在、アメリカの子供たちの少なくとも54%が1つ以上の慢性疾患を抱えている。2007年から2018年まで投資アドバイザーを務めていたとき、私は子供がワクチンによる傷害に苦しむ顧客を持ち、そのような傷害が個人的にも経済的にも壊滅的な結果をもたらすことを目の当たりにした。
最後に、明晰な目を持つ科学者のグループには、経済学者のマーク・スキッドモア博士もいた。2017年以来、スキッドモア博士は米国政府から消えた何兆もの資金を記録する手助けをしてきた。加えて、2022年と2023年に発表されたCOVID-19とCOVID-19ワクチンの影響に関する彼の調査は、COVID-19ワクチンと関連する義務付けや強制的な措置によってもたらされる異常なレベルの病気、障害、死亡を記録するのに役立っている。
mRNA技術から自分自身と家族を守るための今後の課題に直面するとき、私たちを失望させただけでなく、私たちの人権と財産権の根本的な変更を含むクーデターを企てる体制から、自分自身と愛する人たちを守る方法についても、多くの疑問に直面するだろう。
ワシントンに住む私の牧師は、いつもこう言っていた。mRNA Vaccine Toxicityを閉じるにあたり、私たちは、あなたがmRNA技術のリスクとその広範な意味を直視し、できる限り多くの人々を守るためにその知識を活用することを祈る。もしあなたが現在、この殺戮機械に携わったり、資金を提供したりしているのであれば、死と貧困をもたらすものから、生命を与え富を築くものへと、あなたの時間と支援をシフトしてくださるよう祈る。
生を選択し、あなたの愛する人々が同じようにするのを助けよう。私たちの未来はそれにかかっている。
