コンテンツ
www.mdpi.com/2077-0383/12/11/3625
- 1 米国公衆衛生局(Commissioned Corps, Inactive Reserve, Blacksburg, VA 24060, USA
- 2 クワズールー・ナタール大学健康科学部、ダーバン4041、南アフリカ共和国
- 3 マルケ工科大学医学部哲学・科学・政策センター(イタリア・アンコーナ)
- 4 EbMCsquared CIC, Bath BA2 4BL, UK(英国)
- 5 クイーンズランド大学医学部慢性疾患センター、ブリスベン、4072、オーストラリア
受理された:2023年4月4日/改訂:2023年5月10日/受理された:2023年5月19日 /発行:2023年5月23日 (この記事は「臨床研究法」に属している)。
要旨
プロトコルの不遵守率が高いなどの例外的な状況下では、per-protocol(PP)解析はintention-to-treat(ITT)解析よりも医療介入の実世界での有益性を示すことができる。
この例として、最初に検討されたランダム化臨床試験(RCT)では、ITT解析に基づき、大腸内視鏡検査がわずかながら有益であり、実際に検査を受けたのは介入群の42%に過ぎないことが判明した。しかし、研究著者自身は、そのスクリーニングの医学的有効性は、その42%のPPグループにおける大腸がん死亡の50%減少であると結論付けている。
2番目のRCTでは、COVID-19治療薬とプラセボとの比較で、PP解析では死亡率が10倍減少したが、ITT解析ではわずかな効果しかなかった。
第3のRCTは、第2のRCTと同じプラットフォーム試験のアームとして実施され、別のCOVID-19治療薬を試験したが、ITT解析では有意な利益はないと報告された。この試験のプロトコル遵守の報告における矛盾と不正は、死亡と入院のPPアウトカムを考慮する必要があったが、この試験の共著者はそれを開示することを拒否し、代わりに問い合わせた科学者に、この試験のデータを保有していないデータリポジトリを指示した。
これら 3 つのRCT は、PPの結果が、ITTの結果と大きく異なる可能性のある条件と、このような報告や指摘の不一致が生じた場合のデータの透明性の必要性を示すものである。
GPT-4による解説
Intention-to-Treat (ITT) 解析は、ランダム化された臨床試験の統計解析アプローチの一つであり、すべての参加者が最初に割り当てられた治療群(例えば、試験薬群またはプラセボ群)に基づいて解析される。これは参加者が試験を途中で辞めた場合、またはプロトコルから逸脱した場合でも適用される。
Intention-to-Treat解析の主な目的は、治療の「実世界」の効果を模倣することである。現実の医療環境では、すべての患者が完全に治療プロトコルを順守するわけではなく、またある治療を始めた後で他の治療に切り替えることもある。また、ITT解析は、治療の割り当てがランダムであることによるバイアスの可能性を最小限に抑えることができる。
ただし、ITT解析は治療効果を過小評価する可能性があるという欠点もある。試験を途中で辞めた人々やプロトコルから逸脱した人々が解析に含まれるため、治療の真の生物学的効果が水平に引き下げられる可能性がある。これを補完するために、「Per Protocol」PP解析がしばしば用いられる。これはプロトコルを順守した参加者だけを対象に解析を行うアプローチで、一方で選択バイアスの可能性が高まる。
1.はじめに
薬剤の有効性を評価するランダム化臨床試験(RCT)では、プロトコルの遵守状況にかかわらず、治療群とプラセボ群の全対象者の結果を考慮するintention-to-treat(ITT)解析が一般的に最も信頼できると考えられている[1, 2]。しかし、例えばプロトコルの遵守率が低い場合など、特定の状況下では、ITT解析は大きな負のバイアスを持ち[1,3,4]、新規治療薬の有効性を過小評価する可能性がある[5]。このような場合、per-protocol(PP)アウトカムも考慮する必要があり、治療効果のより信頼できる尺度を提供する可能性がある。本調査の最初の2つのRCTでは、PP解析とITT解析で有意に異なる結論が得られ、それぞれの共著者は、PP解析がその介入の医学的有効性を評価している可能性が高いと判断した。3 番目のRCT では、プラセボ群のプロトコル遵守の報告に矛盾や不正があり、また。2 番目のRCT よりもプロトコル不遵守率が高かったため、PP 結果の開示が必要であったが、繰り返し要求したにもかかわらず、開示されなかった。この3 つの例を用いて、信頼できる結論を得るためにPP 結果を考慮しなければならない条件と、PP 解析が、ITT 解析よりも現実の結果を予測する可能性が高い条件を示したい。
2.信頼できる結論を得るためにPPの結果が必要であった。3 つのRCT
2.1.大腸内視鏡検査は効果的であったが、実際に実施された場合のみであった
私たちが注目した最初のRCTであるBretthauerら2022年[6]は、欧州4カ国の被験者を対象に、大腸がん(CRC)発症および死亡に対する大腸カメラスクリーニングの予防効果を10年間にわたり調査した。このスクリーニングを受けるように誘われた被験者からなる介入群と、このスクリーニングを受けなかった対照群の比較結果をITT解析した結果、CRC発生率と死亡の相対リスク(RR)はそれぞれ0.82と0.90と報告された。この研究に関連して発表された論説[7] は、大腸内視鏡検診の恩恵が比較的小さいと報告されたことを「驚きと失望」と評し、この結論はニュース記事[8,9] でも繰り返された。
しかし、このITT解析の重大な欠陥は、介入群である大腸内視鏡検査を受けるよう勧められた被験者のうち、実際に検査を受けたのは42%に過ぎなかったということである。Bretthauerらは、実際にスクリーニングを受けた人たちのベネフィットを推定するための調整PP解析において、CRC死亡は半減し(RR = 0.50)、CRC発生率についてはRR = 0.69となったと報告した。遵守率が低い場合にITT結果から結論を出すことの問題は、HernanとRobinsによる影響力のある解析で指摘されている[3]。彼らは、S状結腸鏡検査によるスクリーニングの先行研究であるHolmeら2014[10]を検討し、ITT解析からスクリーニングによる全死因死亡率の有意な低下はないと結論付けた。しかし、HernanとRobinsは、介入群の3分の2しか実際に処置を受けなかったため、この結論はスクリーニングの効果を大幅に過小評価していると指摘した(付録C、項目1参照)。
しかし、Holme et al.の主な成果は、スクリーニングによりCRC発症率と死亡率の両方が有意に減少したことであり、ITT試験の全死因死亡率については、ほんの少ししか触れていない。一方、Bretthauer らは、大腸内視鏡検診の有益性が小さいとする。ITT 結果を選択的に強調し、その結果のみを要旨に記載している。この要旨では、全死亡のITT 結果も報告されているが、ITT 介入群対対照群では減少せず、ITT 解析による。CRC 死亡の同様の小さな減少と一致しており、信頼区間の重なりの範囲内であった。全死亡のPPアウトカムは提供されず、対照的にCRC発症と死亡の大幅な減少を示した本試験の他のPPアウトカムは、本書のかなり前に初めて言及された。
ITT解析はプロトコルの遵守が低い場合、大きな負のバイアスを受けるが、PP解析もいわゆる「健常者遵守」バイアスを含む歪みの対象となる[11]。しかし、Bretthauer ら自身は、CRC 発生率が、31%減少し、CRC 死亡率が、50%減少したという彼らの研究のPP 結果について、大腸内視鏡スクリーニング法の「利益をおそらく過小評価している」と結論付けている。また、CRC死亡の減少については、「調整されたプロトコルごとの解析で観察された50%の減少を考慮すると、楽観的な考え方が正当化されるかもしれない」と付け加えている。しかし、彼らの研究は、実際の集団検診プログラムを模倣したものであり、彼らの全体的な目的は、「集団検診における大腸内視鏡検査の有益性を定量化すること」であると説明している。したがって、Bretthauer らは、CRCによる死亡が、50%減少するという。PP 結果が、大腸内視鏡スクリーニングの医学的有効性を特徴づける可能性が高いと結論付けたが、彼らの発表要旨と付随する論説は、この研究のITT 結果を強調した。
Bretthauerらは、本試験のITT結果を強調することを正当化しているが、これは馬より先に馬車を置くことである。大腸内視鏡検査プログラムへのコンプライアンスは、管理スタッフの効果的なパフォーマンスなど医療以外の要因に依存することは別として、スクリーニングによってCRC死亡が半減することを被験者に伝えることによって、おそらく大幅に向上するだろう。逆に、Bretthauerらの演題とそれに付随する論説、およびその後のニュース記事から、この検診が最小限の利益しかもたらさないという誤った印象を受けると、コンプライアンスは低下するだろう。
2.2.PP解析とITT解析で異なる薬効の示唆が得られた
2021年4月から2022年3月にかけて、TOGETHERプラットフォーム試験でブラジルでCOVID-19治療用に試験された再利用薬の詰め合わせの結果が4つの論文で報告された[12,13,14,15]。FDAとNIHはともに、TOGETHER試験の全群で報告された主要アウトカムである救急外来受診+入院は不十分であると結論付けた[16,17]。FDAは、死亡と入院がTOGETHER試験の最も重要なアウトカムであると指摘し[16]、次に検討する2つのRCTではこれらを中心に検討することになる。
2番目のRCTは、TOGETHER試験のfluvoxamine(FLV)群(以後、TOGETHER-FLVと呼ぶ)である[13]。ITT解析では、FLV治療による死亡の統計的に有意な減少が報告されている:ITT治療群741人(2.3%)の死亡17件に対し、ITTプラセボ群756人(3.3%)の死亡25件、相対リスク(RR)0.69、p= 0.24である。しかし、PPアウトカムは、治療による死亡が1/548(0.2%)であったのに対し、プラセボによる死亡は12/618(1.9%)で、死亡の91%(10倍)減少した(RR = 0.09,p= 0.022 )。治療群およびプラセボ群におけるプロトコルの遵守率が最適でなかったため(それぞれ74%および82%)、PP解析とITT解析でこのような乖離した結果が得られた。
ITT 解析で示された緩やかな治療効果とPP 解析で示された大きな治療効果のどちらがリアルワールドと関連性があるかの判断は、プロトコル不遵守の理由など、臨床試験データの複雑な特徴に依存するので、ここでは検討しない。しかし、TOGETHER-FLVの共著者自身は、PP 解析が実世界と関連性があると結論づけ、治療プロトコルを遵守する患者にとって FLV は COVID-19に対して「かなりの臨床的利益」をもたらす可能性があると指摘している[13]。TOGETHER-FLVの上級共著者であるEdward Millsは、2021年8月6日のNIH主催のプレゼンテーションで、この研究の成果は、FLVが「非常に大きな治療効果をもたらす可能性がある」ことだと述べた[18]が、これはITT結果ではなく、この研究のPP結果によって裏付けられた結論だった(付録C、アイテム2)。さらに、TOGETHER-FLVの共著者である。Eric Lenzeと2 つのFLV 試験[19,20] で共同研究し、自身もその後のTOGETHER 試験[15] で共著した。David Boulwareという研究者が、PP 成果データが最も有意義であると考えた。Boulwareは、TOGETHER-FLVの発表後、FLVのCOVID-19治療に対する緊急使用許可をFDAに申請した[21]。この申請において、彼は「死亡率に対する治療効果を示唆するPP解析に大きく依存した」とFDAはその申請を却下したことを説明するメモの中で述べている[16]。
2.3.第3のRCTで必要とされるPPアウトカムの非開示について
注目の3つ目のRCTは、COVID-19の治療にイベルメクチン(IVM)を試験したTOGETHER試験RCT[15]で、以後TOGETHER-IVMとし、効果なしと結論付けている。IVMは大環状ラクトンで、その発見と2つの壊滅的な世界的熱帯病の封じ込めに成功したことが評価され、2015年のノーベル医学賞を受賞している[22]。TOGETHER-IVMのPPアウトカムへの関心は、当初、本試験のプラセボ群のITTからPPへの減少が異常に大きく、一貫性のない報告であったことから高まった:表2([15])では58%、表3([15])では19%であり、この相違はプラセボ群に関する記述が矛盾していることから生じた(付録C、項目3、下記)。ITTからPPへのプラセボ群の減少率58%と19%という異なる値は、それぞれ本試験の治療群のITTからPPへの減少率8%よりもはるかに大きく、なぜIVM錠ではなく不活性錠を服用した被験者のコンプライアンス違反率がこれほどまでに大きくなるのかという疑問がある。また、プラセボ群におけるITT-PP間減少率の19%という低い数値も、PP対ITT解析で治療効果が大きかったTOGETHER-FLVのプラセボ群における18%よりも大きいことは注目すべき点である。
前述のように、FDAとNIHにとって、TOGETHER試験の主要アウトカムは不十分であり、死亡と入院が重要なアウトカムであった[16,17]。また、上述のように、ITT解析は、プロトコルの遵守が低い場合、大きな負のバイアスを持ち、新規治療の有効性を過小評価することがある[1、3、4]。そこで複数の科学者が、TOGETHER-IVMの共著者に対し、未報告であった治療対プラセボの死亡率および入院率のPPアウトカムを要求した。これら4つの数値は、2022年4月11日の電子メール[23]、世界中の66人の科学者と医師が署名した2022年5月10日の手紙[24]、その後2022年5月10日から7月19日まで送られた4つの電子メールで要求した(付録C、アイテム4)。
TOGETHER-IVMの共著者は、TOGETHER-FLV[13]と他の2つのTOGETHER試験論文[12,14] で死亡または入院に関するこれらのPPアウトカムが報告されていたにもかかわらず、これらの4つのPPアウトカム番号の開示要求を6回すべて拒否した。2022年5月10日にTOGETHER-IVMの共著者に送られた、これらのPPアウトカムを要求する手紙に対する電子メールの返信で、皮肉にも、FLVでPP死亡アウトカムの重要性を強調した試験共著者のBoulwareが、IVMではその開示を拒否していた。その代わりにBoulwareは、TOGETHER-IVMのデータ共有声明(DSS)がデータソースとして挙げていたICODAデータリポジトリ[25]を要求者に案内し、「出版後直ちに」利用可能にするよう指示した[26]。
しかし、ICODAの電子メールアドレス(返信なし、自動返信)、電話番号(「現在、電話を受ける設定になっていない」[27])を通じて、その試験データを入手しようと2カ月間試みたが失敗し、ついにICODAはTOGETHER試験データを保有していないことが判明した。6月7日、ICODAのマネージャーは問い合わせた科学者の一人に電子メールを送り、次のように述べた:「ICODAはデータを保有していないので、著者にはデータ共有契約を更新してそれを反映させるよう要請した」[28]。1カ月後の2022年7月7日、研究のDSSリンクは別のリポジトリであるvivli.orgを指定するように変更され、7月14日にTOGETHER試験(NCT04727424)のレコードがそこに表示された。しかし、そのVivliのTOGETHER試験の記録には、この試験の治療薬としてIVMではなく3つの薬剤が記載されていた[26]。このVivliの記録は、本解析の共著者3名(CA、DES、EJF)が7月19日にTOGETHER-IVMの共著者にその省略についてメールした後([24]、付録C、項目5)、7月21日にIVMを含むように変更された([26])。しかし、Vivliのデータは、仮に申請と審査を経て入手できたとしても、PPの死亡率と入院率を決定することはできず、ITT群とPPプラセボ群の構成を明らかにする必要があり、研究共著者から要求されたが開示されていない(下記5項参照)。
3.検討された3 つのRCTにおける。PPの結果の無視または保留による公衆衛生上の影響の可能性
私たちが注目した最初のRCTであるBretthauer et al.2022の大腸内視鏡試験に関するフォローアップ専門家コメントは、PP解析から得られた、CRC死亡の減少における大腸内視鏡スクリーニングの著しい有効性は、ITT解析で評価した42%と低い参加率のスクリーニングプログラムの影響よりも公衆衛生に関連性があると指摘した[29]。この2022年の研究とそれに付随する論説[7] で報告された、ITT 解析に基づく主な結論は、したがって、大腸内視鏡スクリーニングの利用を減らし、公衆衛生に負の影響を与えることになりかねない。
2番目のRCTであるTOGETHER-FLVでは、PP解析により、FLV治療とプラセボの比較で死亡が91%減少した(p= 0.022)。この研究論文とFDAに提出されたCOVID-19治療におけるFLVの緊急使用承認申請では、このPP所見が現実の世界と関連していることが強調された。FDAはこの申請を却下したが、この研究論文は、COVID-19治療への本薬の使用に関する情報に基づいた決定を支持するデータを適切に報告し、評価したものである。
3つ目のRCTであるTOGETHER-IVMについては、TOGETHER-FLVのPPアウトカム番号と同様に、非公開のPPアウトカム番号は薬効を示す可能性がある。もしそうなら、その結果は、IVMの発見で2015年のノーベル共同受賞者が共著した2021年の包括的レビューで検討されたRCTのほとんどと一致し、IVMはCOVID-19の治療と予防の両方に有効であると結論付けられたことになる[30]。COVID-19の治療と予防に対するIVMの有効性を肯定的に報告したいくつかのRCTも、2021年のレビューで引用された[22]。驚くべきことに、2022年8月の論説では、IVMはCOVID-19に対して効果がないと断言されたが[31]、2022年6月に発表されたCOVID-19のIVM治療に関するRCTのメタアナリシス[32] では、IVM治療群とプラセボ群のプールで死亡が2倍減少したと実際に報告され、その支持として盛んに引用されている。具体的には、そのメタアナリシスの結果の項で示された最初の知見は、3,472人の患者を含む10のRCTにおける死亡率のプールされた(自然)対数オッズ比(OR)が「-0.67(95%CI -1.20~-0.13) with low heterogeneity」(I2=29%)で、これはOR 0.51(付録C、項目6参照)に相当することだった。
上記のRCTのうちCOVID-19のIVM治療に関する肯定的な所見とは対照的に、この種のRCTで否定的な所見を持つものが、TOGETHER-IVM、Boulwareが共著した他の3つのRCT[33,34,35]、いくつかの大きなプロトコル違反があった2021年に発表された4番目のRCT[36]を含む、顕著に引用されているものがある[37]。その2021年のRCTでは、38人の患者に対してIVMが誤ってプラセボ投与に置き換えられ、3分の1の患者に対してプラセボとして砂糖水を使用したことにより盲検化が破られた(液体IVMは苦い)。IVMの高用量投与に特徴的な有害事象(一過性で重大ではないもの)は、IVM群とプラセボ群でほぼ同じ割合で発生したが、試験期間中にIVMの店頭販売(OTC)が試験地域で急増した[37]。実際、ラテンアメリカにおけるCOVID-19のIVM使用は2020年に非常に広範囲に及んでおり、そこで臨床試験を行うことは困難であることが判明した[38]。
COVID-19のIVM治療では、前述のようにRCTの結果がまちまちであるため、治療効果に関する結論を出すには一般的にRCTの結果が必要となるが、ペニシリンのような特定の薬剤は、明確なRCT結果よりも前に、治療効果の明確な証拠と対応する試験管内試験活性に基づいて展開に成功したものである。例えば、タガメットやザンタックなどのH2受容体拮抗薬(後者は発がん性物質の含有により2020年に回収[39,40])が緩和効果をもたらすが治癒効果はほとんどない消化性潰瘍の治療に、抗生物質とビスマスを用いて成功した[41,42](Peptic Ulcers)。この併用療法の有効性が最初に示された後[43,44]、1990年にオーストラリアでThomas Borodyが行った非対照臨床試験では、テトラサイクリン、メトロニダゾール、コロイド状ビスマスを4週間にわたって投与した消化性潰瘍に対して96%の治癒効果が報告された[45]。この3剤併用療法の有効性を示す明確なRCTエビデンスは1992年まで蓄積されなかったが[42]、オーストラリアでは1980年代後半から消化性潰瘍のこうした併用療法が広く用いられるようになり、1990年から関連死亡率が急激に低下し、1990年から2015年までに推定18,665人の死亡が防止された[46]。しかし、この3剤併用療法は、TagametとZantacの特許が切れた後の1990年代後半まで、世界の他の地域では広く使用されていなかった[47]。この治療法は現在、消化性潰瘍の世界的な標準治療となっており、その原因菌の発見に関連して 2005年にノーベル医学賞が授与される栄誉に輝いている。
2022年、オーストラリアの研究者Thomas Borodyは3つの臨床研究のうちの1つに協力し、それぞれIVMによる治療後24時間以内に重度のCOVID-19患者の末梢酸素飽和度(SpO2)が急激に上昇することを発見した[48,49,50]。このSpO2の急速な正常化を説明する生化学的メカニズムは、SARS-CoV-2のスパイクプロテイン(SP)への糖鎖結合のIVMによる競合的阻害であると考えられている[51]。これらの糖鎖結合は、例えばウイルスによって誘発される血球凝集によって示されるように、宿主細胞の付着とベータコロナウイルスの罹患に不可欠である。5種類のヒトベータコロナウイルスのうちHKU1およびOC43という2つの非致死株は、同様にこれらの糖鎖結合を阻害する酵素を発現する[52]。最近の研究では、ヒト赤血球と混合したSARS-CoV-2 SPが血球凝集を起こし、IVMがその血球凝集を阻害し、形成後に逆転させることが実証された[53]。この試験管内試験が生体内試験で再現・拡張されれば、生化学的根拠が明確であることから、RCTの結果がまちまちな中、IVM投与に関する3つのSpO2トラッキング試験が、COVID-19に対するIVMの有効性を示す意義ある実証となり得る。そのような場合、TOGETHER-IVMは、PPの結果が公表されるまでは、このエビデンス群に信頼できる貢献をしないことを理解することが重要であろう。
4.検討された3つのRCTにおける科学的誠実性に関する疑問点
COIの開示によると、Bretthauerらの2022年大腸内視鏡検査研究[6]と付随論説[7]の共著者は、まとめて高度CRC検出装置のメーカー9社と、主にコンサルティングや講演料などの金銭関係を有していた[54].ルーチンの大腸内視鏡検査の利点が過小に報告されることにより、そのような機器の売上が増加する可能性があるため、これらのCOIについて若干の懸念がある。
COVID-19の治療薬としてFLVとIVMを試験した、私たちが注目した2番目と3番目のRCTに関して興味深いのは、科学の商品化と規制への脆弱性を利用し、特許医薬品を優先して後発医薬品に偏った歴史である[55,56].消化性潰瘍の3剤併用療法の世界展開が、前述のように、その症状に対する最も売れた2つの緩和薬の特許が切れた後まで10年近く遅れたことは、その顕著な例だ。IVMに対するこのような偏見の可能性は、当時COVID-19治療薬モルヌピラビルを開発していたメルク社の2021年2月4日のプレスリリースで、IVMの「安全性データの不足が懸念される」と主張されたことでも指摘されている[57]。しかし、IVMはメルク社独自の医薬品であり、ノーベル賞委員会は2015年の医学賞でこの医薬品の発見を称えるにあたり、IVMの安全性に関する記録を特に指摘した[58]。IVMは1987年以来、世界中で37億人のヒトへの投与で安全に使用されており[22]、標準よりはるかに多い投与量でも安全であることが証明されている[59,60]。このメルク社のプレスリリースをきっかけに、IVMの中毒に関する主要な報道がなされたが、後に否定された[57]。2020年末までに25カ国でCOVID-19治療に使用され[30]、この疾患のすべてのジェネリック治療薬の中で、IVMは特許取得済みのCOVID-19治療薬に対して最大の競争力を持つことになった。
TOGETHER-IVMの共著者によるある種の行動やコミュニケーションは、臨床試験の報告に対する信頼を維持するために役立つ倫理的規範であるデータの透明性へのコミットメントと適合しないように見える。この試験のDSSや、2022年5月10日の死亡と入院のPPアウトカムを要求する書簡に対する電子メールの回答で、存在しないICODAデータベースへの誤った誘導を行ったことは、確かに懸念を抱かせる。過去 10年間で臨床試験の結果が捏造された顕著な事例は、研究者が求められたときに研究の基礎データを提供しなかったために発覚したものである[61,62]。例えば、2020年、Lancet[63]とNew England Journal of Medicine (NEJM)[64]に掲載された研究の共著者であるSapan Desaiは、Lancet研究の異常について質問されたが、レビューのために基礎データを提供することを拒否した。これらの研究とDesaiが共著した別の研究は、その後数週間以内に撤回された[65, 66, 67, 68]。
さらに、2022年4月11日に電子メールで最初に要求された、死亡と入院のPPアウトカム数を開示しなかった後、TOGETHER試験4報すべての共著者であるEdward Millsは、代わりに質問者に「世界はフラットではない」ことを同僚に伝えるよう提案した(付録C、項目7)。2022年11月22日にロイターから、スキャンダルで有名な暗号通貨会社FTXによるTOGETHER試験への1800万米ドルの資金提供の約束について尋ねられたミルズ氏は、「(FTXから)2022年5月以前に資金は受け取っていない」とメールで答えたが、実際にはFTXは2022年3月3日までにTOGETHER試験の資金提供者として後者のウェブサイトに記載されていた(Appendix C, item8)。TOGETHER-IVMに関する完全な透明性を阻むもう一つの障害は、この試験が掲載されたNEJM誌が、それについて提出された多くの手紙のいずれをも掲載しなかったことである(付録C、項目9)。
ICODAのマネージャーが2022年6月7日に報告したように、TOGETHER-IVMの共著者に対し、DSSにICODAを記載しないよう求めた後、これらの共著者は6月5日と7月11日の2回、ICODAがTOGETHER試験のデータを保有していないことを電子メールで思い出された(付録C、項目10)ことから、速やかに是正措置をとるはずだったと思われる。ほぼ同じTOGETHER試験の共著者が重なったグループは、4つの出版物すべてのDSSを速やかに変更することができたはずだ。しかし、2023年5月22日現在、2021年10月27日に出版されたTOGETHER-FLVのオンライン版と2021年12月13日の別のTOGETHER試験の出版物[14]は、依然としてデータソースをICODA[26]と記載している。実際、TOGETHER-FLVは2022年8月9日にDSSを更新し、試験データはICODAにあると宣言しているが、「他の試験関連文書はVivliにある」と付け加えている。しかし、前述の通り、ICODAはTOGETHER試験の試験データを保有しておらず、2023年5月22日の時点で、VivliはTOGETHER試験の試験文書タブに「ファイルなし」と表示している[26]。
5.考察
今回注目した。3 つのRCTのITT 対 PP 結果について結論を出すにあたり、1975年に冠動脈疾患治療薬の主要なRCT で「健常者遵守」効果が明らかになって以来、非等価試験には ITT 解析が望ましい手法であることを再確認することが重要である[11,69,70]。PP 解析はいくつかのバイアス源にさらされる可能性があるが[1,11,71]、ITT 解析には他にも歪みが生じる可能性があり[72]、プロトコルの遵守が不十分な場合に特に懸念される[1,3,4,5] ことになる。これらの解析方法のうち、どの方法がRCTで試験された介入の実世界での有効性を反映する可能性が高いかの判断は、臨床試験デザインの詳細と治療群とプラセボ群の両方における非遵守者の程度と特徴に依存する。しかし、私たちが注目した最初の2つのRCTでは、上で引用したように、研究者自身が、PP解析はそれぞれ試験された介入と薬剤の有効性を最も反映しやすいと主張している。これらの判断は確証のないものだが、おそらく、臨床試験デザインの根本的な複雑さと、非遵守者の特徴に関する知識を反映しており、それぞれの研究者チームによる、未発表の非識別化患者データのレビューが必要となる可能性があるのだろう。
さらに、今回注目した3番目のRCTのプラセボ群では、プロトコルの遵守がかなり進んでいたことから、Porta et al., 2007が述べた要件は健全である:「プロトコルの逸脱がある場合、CTの結論はITTまたはPPアプローチのどちらか一方のみの報告に頼ることはできない」[4]。TOGETHER-IVMの著者は、報告されたITT結果の実世界での関連性について、十分に説得力のある議論を提供することができるかもしれない。しかし、死亡や入院、治療対マッチングプラセボの4つの要求されたPPアウトカムの報告を保留し、基礎データの要求に対して、研究者を存在しないデータベースに誘導することは、研究者や科学界がそのような主張を正当化したり疑問を呈することを許さないものである。
今回取り上げた最初の2つのRCT、2022年大腸内視鏡試験とTOGETHER-FLVは、プロトコル遵守が不十分な場合に、ITT解析とPP解析が医療介入の有効性をいかに大きく異なる形で示すことができるかを示す例だ。最初の例では、大腸内視鏡スクリーニングを実際に受けた介入群の42%の参加者のCRC 死亡が、50%減少したという。PP 結果が、この処置を受けるかどうかを検討している人や公衆衛生に関連する統計値である。このPPの結果は、大腸内視鏡スクリーニングの医学的有効性を規定するものである可能性が高いが、研究報告書と付随する論説では、わずかな利益しかないというITTの結果が強調されている、と共同執筆者自身が述べている。
2番目のRCTであるTOGETHER-FLVでは、PP解析により、FLV治療とプラセボの比較で死亡数が10倍減少した(RR = 0.09,p= 0.022 )が、ITT解析では死亡数の31%減少(RR = 0.69,p= 0.24 )と、より限定的だった。TOGETHER-FLVのチームと密接な関係にある研究者は「PP解析に大きく依存している」とし、TOGETHER-FLVの上級著者は、FLVが「非常に大きな治療効果をもたらす可能性がある」と述べ、この結論はITT解析ではなくPP解析によって支持されていると結論付けている。このように、本研究は、プロトコルの不遵守の程度が最適でないにもかかわらず、治療効果に関するITT解析とPP解析が大きく異なる可能性があること(治療とプラセボでそれぞれ74%と82%のプロトコルの遵守)、そしてそのような場合にPP解析が現実の臨床効果を最もよく反映できることを実証している。
TOGETHER-IVM では、プラセボ群におけるプロトコルの不適合が、TOGETHER-FLV よりも大きく、一貫性のない報告によって混乱したため、薬効について信頼できる結論を出すためには PPの結果が必要であった。付録Bに詳述するように、TOGETHER-IVMの研究論文と他の研究文書では、ITTプラセボ群について3つの矛盾する記述があった。TOGETHER-IVM研究論文は、通常のper-protocolの意味を無視して、ITTプラセボ群には混合プラセボ(3日間と14日間のみ、または1,3、10,14日間)が含まれていたが、PPプラセボ群では混合プラセボを排除し、3日間のみ含まれていると、異なるカ所で述べている。ITTからPPプラセボ群へのこの異常な選択の根拠は示されておらず、他のTOGETHER試験の出版物でもPPプラセボ群から混合日プラセボを除外したことに言及していない。
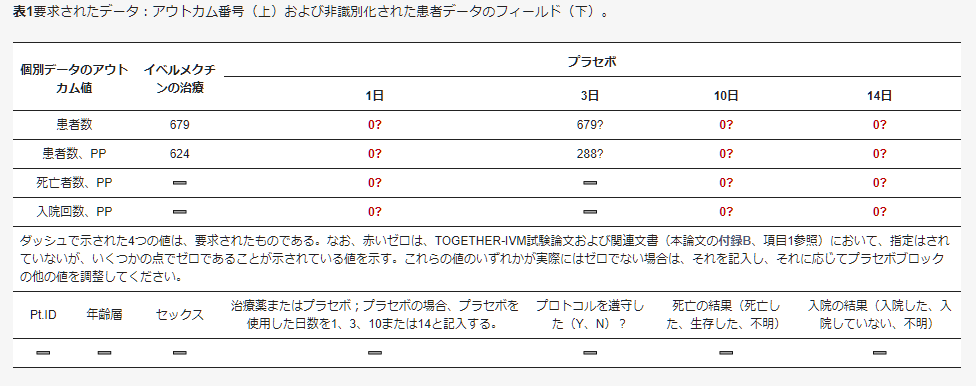
さらに、混合日プラセボの使用は、RCTの基本原則である、薬剤群と盲検化されマッチングされたプラセボ群を持つという原則に違反する。NIHはTOGETHER-FLVについて述べているが、これはTOGETHER試験の全群に当てはまることで、適応プラットフォーム試験デザインの「重要な限界」は、「プラセボ群のすべての患者が、投与経路、投与回数、治療期間でフルボキサミンと一致するプラセボを受けたわけではない」[17]というものである。TOGETHER-IVMの1日プラセボ患者は、研究文書でプラセボ群に含まれると繰り返し報告されているように、1回の模擬注射を受けた患者を含み、明らかに盲検化されていない(Appendix B)。したがって、TOGETHER-IVMプラセボ群、3日間プラセボ群、表1の3日間IVM治療群と一致するPP数を開示する必要がある。NIHが指摘したTOGETHER試験のadaptive platform trial designの限界[17]を克服し、この矛盾の迷路を突き抜け、有用な結論を導き出すためには、これらのPP数が必要である。
表1要求されたデータ:アウトカム番号(上)および非識別化された患者データのフィールド(下)。
さらに、TOGETHER試験において、IVMとプラセボ錠の表示や味の違い、あるいは他の盲検化違反に基づき、プラセボ患者がIVMを使用した可能性があり、本試験の結果が損なわれた可能性がある。TOGETHER試験の実施地であるブラジルでは、IVM試験期間中、OTC IVMの販売が実際に盛んに行われていた[73]。ITTからPPへのプラセボ群の減少の一部が、プラセボ患者が密かにOTC IVMを服用し、プロトコルの遵守が緩くなったことに起因するとすれば、ITT解析は、IVMが本当に有効であるならば、IVMが有効であるとすることにバイアスをかけた可能性がある。
もし、TOGETHER-IVMのCOVID-19に対するIVMの有効性に関する否定的な結論を、IVM治療対プラセボの死亡と入院の4つのPPアウトカム数字が裏付けていたならば、研究の共著者は急いでそれを開示したと思われる。この試験の上級著者である。Edward Mills は、この試験の発表の8 ヶ月前に、2021年 8月 6日のビデオプレゼンテーションで、IVMの有効性に関する否定的な結論を報告しており、その中で、一部のIVM 推進者とTOGETHER 試験チームの間の敵対関係を説明していた[74](31と49)。ITTアウトカムと一致するPPアウトカムは、彼のケースを補強しただろう。共同研究者は、6回の電子メールによる要求に対して、死亡と入院、IVM治療と一致する3日間のプラセボの4つの重要なPPアウトカム番号を開示せず、代わりに存在しないICODAデータベースへ誤誘導したため、データの透明性に対する共同研究者の取り組みやCOVID-19に対するIVM有効性に関するこの試験の報告された否定的結論に信頼を与えることはできない。2022年7月19日に要求されたように、表1に要約されたこれらのPPアウトカム番号とサポートデータの開示があれば、IVMを用いたCOVID-19治療に関するエビデンスの中で、この研究を信頼できるものとして考慮することができるだろう[24]。
6.結論
ITTとPPの結果が大幅に異なることが分かっている、または指摘されている。RCTの3 例を検討した。最初の例では、PP解析の結果、大腸内視鏡検査によるCRC死亡が50%減少し、共同研究者自身によるスクリーニングの医学的有効性の定義がなされた。一方、ITT解析では、介入群の42%しかこの検査を受けず、最小限の利益しか得られないことが示された。2つ目のケースでは、TOGETHER-FLV試験の共著者は、PP解析で算出された死亡率の10倍減少が、ITT解析で得られた死亡率の統計的に有意ではない減少よりも、FLVによる現実の利益を予測するものであるとした。1例目と2例目では、すべてのPP結果が報告され、ITT結果とは大きく異なっており、それぞれのRCTの研究者自身が、PP結果が医療効果を最もよく表していると判断した。
しかし、3つ目の例であるTOGETHER-IVMでは、研究者は、重要な意味を持つPPアウトカム、すなわちIVM治療とプラセボの比較における死亡率および入院率の報告を、再三の要求にもかかわらず拒否したのである。その代わりに、研究者らは科学界に、この研究のデータを保有していないデータリポジトリに誤った案内をした。この試験のPP 結果は、最初に検討した。2 つのRCTと同様に、ITC 結果と大きく異なる可能性があり、実際の薬効を最も代表するものである可能性がある。特に、本試験のプラセボ群におけるプロトコル遵守の報告に矛盾や不正があり、ITT 結果に疑問があることから、重要な関心事であるこれら 4 つのPP 結果の数値を開示する必要がある。本試験の結果に関する信頼できる結論は、そうでなければ信頼できるものではない。
ファンディング
この研究は、外部からの資金提供を受けていない。