Contents
特異的炎症収束性メディエータ(SPM)・オキシリピン・エイコサノイド
Specialized pro-resolving lipid mediator
概要
恒常性を担う抗炎症脂質代謝産物
SPM(Specialized pro-resolving lipid mediator)とは、EPA,DHAなどの多価不飽和脂肪酸から代謝される抗炎症性をもつ内因性の脂質代謝産物の総称。
SPMは体内に炎症が起こった際に、炎症性シグナルを制限するなど自然な反応を抑制することで宿主の過剰な損傷を防ぎ恒常性の復帰を促進する。
これまで体内に炎症が起こった際、その後炎症を引き起こす起因が取り除かれた後の炎症の収束は自然と受動的に起こるものと考えられていたが、SPMによって積極的にブレーキがかけられる能動的な仕組みがあることがわかってきた。
SPM低下による疾患の進行
そのためSPMレベルは炎症のシグナルに応じて、適切なタイミングで増加させて均衡させる必要があるが、重症の患者ではしばしばSPMレベルが減少していることから炎症状態が収束しないことがある。
これはSPMレベルの低下が、病気の進行や悪化の一因となる可能性があることを示す。
www.ncbi.nlm.nih.gov/pubmed/18437155/
低濃度での受容体作用
SPMの機能活性は非常に低濃度(100nMレベル)で発揮することから、SPMの炎症収束作用は脂質の代謝作用そのものではなく、受容体との結合を介したシグナル伝達によるものであると考えられている。
PPARγの活性化を促進するには比較的高濃度が必要となるが、SPMは基質であるEPA、DHAと比較すると1000分の1の濃度で炎症収束作用をもつ。
www.jstage.jst.go.jp/article/jsci/39/3/39_155/_pdf
脳のSPM
脳組織のSPM
SPMには大きく、リポキシン、レゾルビン、プロテクチン/ニューロプロテクチン、マレシンと4種類ある。ヒトの脳組織ではレゾルビンD1、プロテクチン1、マレシン1が生成される。
アルツハイマー病患者の低いSPM
最近の研究の証拠から、アルツハイマー病では引き起こされた炎症を収束させるSPMの作用が失われていることが示されている。
2型糖尿病アルツハイマー病患者のオキシリピンプロファイル
www.ncbi.nlm.nih.gov/pmc/articles/PMC6780570/
海馬
アルツハイマー病患者海馬ではコントロールグループと比較して、レゾルビンD5、マレシン1、プロテクチン1レベルが低かったが、レゾルビンD1、レゾルビンD2については、明らかな違いは観察されなかった。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4824659/
脳脊髄液
脳脊髄液中のリポキシンA4とレゾルビンD1レベルはMMSEスコアと相関していた。
www.ncbi.nlm.nih.gov/pubmed/24530025/
嗅内皮質
アルツハイマー病患者嗅内皮質のマレシン1、プロテクチンD1、レゾルビンD5は、同年齢のコントロールと比較して低かった。炎内因性の炎症収束メディエーター(SPM)の活性化がアルツハイマー病で有益な効果を示した。
www.ncbi.nlm.nih.gov/pubmed/26650044/
肝臓でのSPM代謝(LXR)の低下
食事からのSPMの前駆体であるオメガ3脂肪酸摂取による肝臓での変換(肝臓X受容体/LXR)はアルツハイマー病患者で減少することが報告されている。
www.ncbi.nlm.nih.gov/pubmed/22766509/
そのことから、死後アルツハイマー病脳の海馬や嗅内皮質を含むさまざまな領域でSPMのレベルが低いことが発見されている。
www.ncbi.nlm.nih.gov/pubmed/24530025/
ApoE4と低いSPMの関連
ApoE4メスマウスでは10%低い皮質DHAと皮質SPMの数の減少を示す。
これまでの証拠からは、以下と関連してアルツハイマー病の発症を防ぐメカニズムが損なわれていることが示唆されている。
- 低いオメガ3脂肪酸レベル
- SPMの生合成に関与する酵素の遺伝的多型
- SPM受容体の機能不全
www.ncbi.nlm.nih.gov/pubmed/28087575
www.ncbi.nlm.nih.gov/pmc/articles/PMC5681480/
APOE3遺伝子型と比較してAPOE4では、以下のSPMが有意に減少している。
- プロテクチン(10S、17SdiHDHA)
- レゾルビン(17R-RvD1)
- EPA由来の18-HEPE
以下のSPMでは加齢と遺伝子型の有意な相互作用が観察された。
- DHA由来の17S-HDHA
- 14SHDHA
www.ncbi.nlm.nih.gov/pubmed/31251078
ApoE4遺伝子型とSPMのレベルとの間に相関関係はなかった。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4824659/
進行後のSPM変換低下
アルツハイマー病患者へのオメガ3脂肪酸投与は、MCI患者にのみ有益な効果が示されている。アルツハイマー病の後期では脂肪酸のSPMへの変換が減少することから、進行後ではSPMの保護効果が得られていない可能性がある。SPM治療は進行したアルツハイマー病患者でより効果的である可能性がある。
www.ncbi.nlm.nih.gov/pubmed/20434961/
SPMs
用語
オキシリピン:脂肪酸から生成される生理活性脂質
エイコサノイド:アラキドン酸、多価不飽和脂肪酸から生成される生理活性脂質
SPM:アラキドン酸、多価不飽和脂肪酸から生成される抗炎症性の生理活性脂質
SPMの役割
抗炎症作用
SPMには、炎症抑制作用のあるグルココルチコイド、インターロイキン10(抗炎症性サイトカイン)、インターロイキン1受容体拮抗薬(炎症性サイトカインの作用の阻害剤)などを含む。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4787218/
細胞保護
SPMは炎症の収束だけではなく4タイプのSPMすべてが、細胞の増殖、成長、生存、運動性、代謝機能の重要な役割に関わるPI3K/AKTシグナル伝達経路の発現に影響を与え、細胞保護的な役割を果たすことが報告されている。
PI3K / AKTは、その下流の因子であるmTORおよびNrf2を活性化できる。
抗菌作用
多価不飽和脂肪酸およびSPMであるLXA4、レゾルビン、プロテクチン、マレシンは抗生物質のような作用があり、食作用を調節する。多価不飽和脂肪酸はすべての細胞膜に存在し、特にホスホリパーゼA2の活性化によるLPSの曝露時に多くの刺激に応答して放出される。
その結果内因性の不飽和脂肪酸が天然の抗生物質として機能する可能性があることを示唆する。
www.ncbi.nlm.nih.gov/pmc/articles/PMC5124295/
神経保護効果
リポキシンA4、マレシン1、レゾルビンD1、ニューロプロテクチン、は神経保護作用を示す。マレシン1とレゾルビンD1はミクログリアのアミロイドβ42貧食作用を活性化させ炎症を低下させる。
www.ncbi.nlm.nih.gov/pubmed/26650044
SPMsの活性・増加
アスピリン
リポキシン、レゾルビン、プロテクチン
www.ncbi.nlm.nih.gov/pubmed/24899309https://www.ncbi.nlm.nih.gov/pubmed/21867913
スタチン
www.ncbi.nlm.nih.gov/pubmed/26236990
www.ncbi.nlm.nih.gov/pubmed/18537520
オメガ3脂肪酸
慢性的な頭痛のある患者への、食事によるオメガ3脂肪酸摂取は、血漿レゾルビン、17-HDHA、18-HEPEの増加を示し、同時に頭痛の痛みが軽減された。
www.ncbi.nlm.nih.gov/pubmed/23886520
アルコール(赤ワイン)
ランダム化比較試験 正常血圧男性の赤ワイン(375ml/日)の飲用は、アルコール抜きの赤ワイン、または水を飲んだグループと比較してSPM(18-HEPE、レゾルビンD1、17R-RvD1)の増加が示された。
www.ncbi.nlm.nih.gov/pubmed/28767146
アセチルコリンによる増強
抗炎症分子であるアセチルコリンがLXA4産生を増強することが示唆されている。
その他、神経体液性因子の経路とLXA4、レゾルビン、プロテクチンなどのSPMの間にはリンクがあるようである。
www.ncbi.nlm.nih.gov/pubmed/23296426/
アナバサム
プレドニゾロンと同等の強力な抗炎症効果
LXA4、LXB4、RvD1、RvD3の増加
www.ncbi.nlm.nih.gov/pubmed/29238967
免疫栄養療法
術前の免疫栄養は炎症反応を減少させ、主要な肝胆道切除を受けた患者の術後合併症の悪化から保護した。レゾルビンE1は、免疫栄養にEPAが補充されている場合、急性炎症の解消に重要な役割を果たす可能性がある。
www.ncbi.nlm.nih.gov/pubmed/26965712
SPMsの抑制・低下
NSAID
イブプロフェン治療は、レジスタンストレーニング後に増加するCOX-1およびCOX-2由来プロスタノイドの増加を阻害したがリポキシン、レゾルビン、プロテクチンなど多くのSPM応答の低下も引き起こした。
www.ncbi.nlm.nih.gov/pubmed/24089379
リポキシン
複数のリポキシゲナーゼ(LO)の働きでアラキドン酸から合成される。
リポキシンA4(LXA4)
リポキシンA4(LXA4)は炎症の収束に関与する代表的分子。
リポキシン A4 は複数の細胞を介して合成されることを特徴とする。
リポキシンA4は5-LO、12-LOまたは15-LOによりアラキドン酸から合成される。
リポキシン A4 の受容体は N-ホルミルペプチド受容体2(FPR2/ ALX)であるが、ロイコトリエン受容体や芳香族炭化水素受容体などにも結合する。
アスピリンによって誘発されたリポキシンA4は、マウスのミクログリア活性化を刺激し、NF-κB活性化と炎症性サイトカインおよびケモカインのレベルを低下させ、抗炎症性サイトカインIL-10および形質転換成長因子-βのレベルを上昇させた。
www.ncbi.nlm.nih.gov/pmc/articles/PMC3644736/
BBB機能の改善・MMP-9阻害
リポキシンA4アナログは、局所脳虚血再灌流障害のラットモデルで血液脳関門機能障害を改善し、MMP-9発現を低下させる。
link.springer.com/article/10.1007%2Fs12031-011-9620-5
酸化ストレスからの保護
リポキシンA4は脊髄損傷うさぎモデルの神経機能を大幅に改善し、細胞アポトーシスとMDAレベルを低下させ、SOD活性を増加させる。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4612882/
カンナビノイド受容体CB1へのアロステリック効果
リポキシンA4は、アナンダミド親和性を高めるカンナビノイド受容体CB1の内因性アロステリック調節因子として機能する。
加えてリポキシンA4、アルツハイマー病マウスモデルにおけるアミロイドβ誘発性の空間記憶障害に対してCB1受容体に依存的な保護効果を示した。
www.ncbi.nlm.nih.gov/pubmed/23150578
ライム病
酵素5-リポキシゲナーゼ(5-LO)は、アラキドン酸からロイコトリエンへの変換を触媒する。ロイコトリエンは、炎症や喘息や関節炎などの炎症性疾患の重要な調節因子。ライム関節炎の誘導には5-LO活性が必要ではないことが実証された。
リポキシンとレゾルビンの欠乏は関節炎を解決する宿主の能力を損ない、その結果、慢性疾患を引き起こし、引き金となる感染因子が除去された後に慢性全身性炎症反応を制御できなくなる。
www.ncbi.nlm.nih.gov/pubmed/21270404
15-epi-リポキシンA4
アスピリンによるシクロオキシゲナーゼ2(COX-2)のアセチル化と5-LO
の働きにより、15-epi-リポキシンA4 が合成されN-ホルミルペプチド受容体2(FPR2/ ALX)との結合により炎症の収束作用を示す。
ロバスタチン
ロバスタチンは、脂質低下作用に加えて、アラキドン酸から15-epi-Lipoxin A4の生成を引き起こし、急性粘膜炎症を減少させた。
www.ncbi.nlm.nih.gov/pubmed/20130564
ピオグリタゾン
ピオグリタゾンは、アスピリン誘発性エイコサノイド15-epi-Lipoxin A4(15–epi–LXA4)の血漿レベルを上昇させることを示した。
linkinghub.elsevier.com/retrieve/pii/S0021915012002687
アスピリン
www.ncbi.nlm.nih.gov/pubmed/9112289
レゾルビン Eシリーズ
レゾルビン(Resolvin)
EPAに由来 4つの主要なメディエーター(RvE1-RvE3、18-HEPE)
レゾルビンE1
レゾルビンE1は、好中球遊走の阻害、活性酸素抑制、炎症性サイトカインの抑制、トキソプラズマ感染における樹状細胞の遊走と活性化の抑制などの作用をもつ。
www.ncbi.nlm.nih.gov/pubmed/18480426
www.ncbi.nlm.nih.gov/pubmed/21711247
www.ncbi.nlm.nih.gov/pubmed/22927428
末梢侵害受容ニューロンに対するサブスタンスPの作用を阻害する。
www.ncbi.nlm.nih.gov/pubmed/27738388
レゾルビンE2
低酸素状態では、レゾルビンE2の生合成が促進される。
レゾルビンE3
好中球走化性の阻害、強力な抗炎症効果。好酸球によって合成される。
www.ncbi.nlm.nih.gov/pubmed/22275352
18-HEPE (ヒープ)
5-LOXは18-HEPEをRvE2に変換する。
18-HEPEの心臓保護作用
www.ncbi.nlm.nih.gov/pubmed/25049337
アセトアミノフェン、インドメタシンによる18-HEPE生成
COX-2阻害剤は18HEPEの生成を阻害する。
出生前のオメガ3脂肪酸補給は、ヒト母体および臍帯血の18-HEPEおよび17-HDHA濃度を増加させ、炎症を軽減、早期早産を減らす。
www.ncbi.nlm.nih.gov/pubmed/29031403
レゾルビン Dシリーズ
DHAに由来 6つのメディエーター(RvD1〜RvD6)
レゾルビンD1(RvD1)
アルツハイマー病の脳及び脳脊髄液ではレゾルビンD1とリポキシンA4が減少している。
www.ncbi.nlm.nih.gov/pubmed/24530025
アミロイドβ食作用の増加
ビタミンD3(1,25D3)およびレゾルビンD1(RvD1)の両方が、マクロファージによるアミロイドβの食作用を改善し、アミロイドβ誘導アポトーシスを抑制した。
www.ncbi.nlm.nih.gov/pubmed/23186989
www.ncbi.nlm.nih.gov/pubmed/26650044
認知機能低下の抑制
17R-レゾルビンD1による急性治療は、マウスモデルで神経炎症やシナプス機能障害から脳を保護することにより、認知機能低下を防いだ。
www.ncbi.nlm.nih.gov/pubmed/23709617
PI3K / AKT発現
RvD1は、PI3K / AKT発現を増加させることにより、心筋梗塞のサイズを縮小した。
www.ncbi.nlm.nih.gov/pubmed/25806690/
レゾルビンD2(RvD2)
レゾルビンD2は、白血球の強力な調節因子であり、細菌の殺傷、クリアランスを増強し、強力な臓器の保護作用を示す。
www.ncbi.nlm.nih.gov/pubmed/19865173
抗うつ効果
レゾルビンD1とD2はマウスのうつ病行動を持続的に改善させる。
www.ncbi.nlm.nih.gov/pubmed/28610917
レゾルビンD1およびD2はmTORC1シグナル伝達経路を介してうつ病様行動を逆転させる。
www.ncbi.nlm.nih.gov/pubmed/28419244
レゾルビンD3(RvD3)
レゾルビンD3は、炎症性分泌として強力な分解作用と抗炎症作用を示し、急性炎症反応の後期の収束に関与する。
www.ncbi.nlm.nih.gov/pubmed/23438748
レゾルビンD5(RvD5)
RvD1とRvD5の両方がGPR32依存的に大腸菌の食作用を刺激し抗生物質の投与量を軽減することができた。
www.ncbi.nlm.nih.gov/pmc/articles/PMC3340015/
レゾルビン Tシリーズ
n-3DPAに由来 (RvT)
www.ncbi.nlm.nih.gov/pmc/articles/PMC4560998/
アトルバスタチン・プラバスタチン
アトルバスタチンとプラバスタチンは、n-3DPAをレゾルビンTシリーズに変換する。
レゾルビンTシリーズは器官を保護し食作用と細菌の殺傷を強化し、インフラマソームの成分を調節する。
www.ncbi.nlm.nih.gov/pubmed/26236990
www.fasebj.org/doi/full/10.1096/fj.201700268
RvTとリポキシンはインフラマソームの活性化を低下させる。
www.ncbi.nlm.nih.gov/pubmed/28245134
プロテクチン/ニューロプロテクチン
(PD1〜PDX)
ニューロプロテクチンD1(NPD-1)
抗炎症・神経保護作用
DHA由来の強力な抗炎症作用と神経保護作用をもつメディエーター
中枢神経系が障害を受けた時の恒常性を維持し、神経変性遺伝子の発現や酸化ストレスなどを防御する役割をもつ。
加齢によって低下
PD1レベルは遺伝子型の影響は受けなかったが、海馬の年齢とともに有意に低下し、アルツハイマー病患者の海馬CA1領域のPD1レベルの低下と一致した。
www.ncbi.nlm.nih.gov/pubmed/16151530
アルツハイマー病患者の低いNPD-1
PD1は炎症の初期段階に関与し、アルツハイマー病の初期段階で減少する。
www.ncbi.nlm.nih.gov/pubmed/23022417
アルツハイマー病患者の海馬のNPD1レベルは、同年齢のコントロール郡と比べ20分の1であった。ニューロンの脱落(11~41%)だけではこのNPD1レベルの20倍の減少は説明できない。
link.springer.com/article/10.1007%2Fs10571-005-4010-6
アミロイドβ分泌の減少
アルツハイマー病患者の脳ではNPDの減少が示されており、DHAの補充はNPDへの代謝を介してアストロサイトのアミロイドβ42およびアミロイドβ40の分泌を減少させる。
NPD1は、炎症誘発性の遺伝子を弱め、Bcl-2をアップレギュレートする。
NPDはPPARγを活性化することで、APPプロセシングを非アミロイド形成経路にシフトさせる。
NPD1はβアミロイド前駆体タンパク質(βAPP)プロセシングに影響をおよぼすことでアミロイドβ42の放出を減少させる。可溶性アミロイド前駆体タンパク質αはDHAからのNPD1生合成を刺激する。
www.ncbi.nlm.nih.gov/pubmed/16151530/
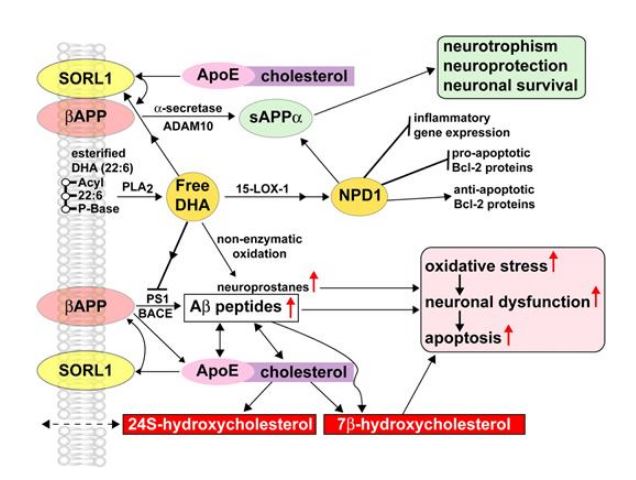
academic.oup.com/jn/article/138/12/2510/4670186
PI3K / AKTシグナル経路の活性
NPD1はPI3K / AKTシグナル経路を活性化することにより網膜色素上皮細胞の生存を誘導した。
www.ncbi.nlm.nih.gov/pubmed/21136150/
NPD1のPPARγ活性化作用
NPD1は、BACE1をダウンレギュレートすることでアミロイドβ42ペプチドの神経脱落を抑制、α-セクレターゼADAM10を活性化、sAPPαをアップレギュレート、βAPPホロ酵素のアミロイド生成を非アミロイド形成性経路のプロセシングへシフトさせる。このダウンレギュレーションはPPARγ依存性であることを示唆する。
www.ncbi.nlm.nih.gov/pubmed/21246057/

www.ncbi.nlm.nih.gov/pmc/articles/PMC3406932/
パーキンソン病
ドーパミン性ニューロンのアポトーシスからの保護効果 in vitro
www.nature.com/articles/cdd2014233
抗ウイルス作用
プロテクチンD1(PD1)は、インフルエンザウイルスの複製を著しく阻害。マウスの重症のインフルエンザを改善した。
www.ncbi.nlm.nih.gov/pubmed/23477864
NPD1アゴニスト・活性経路
アスピリン
アスピリンとDHAの投与によってトリガーされたニューロプロテクチンD1の合成は、脳卒中後の脳虚血傷害を軽減する。in vivo
www.sciencedirect.com/science/article/pii/S0014488612001598
www.sciencedirect.com/science/article/pii/S1388198114001619
BDNF・NGFによる活性
BDNF、NGF、NT3および他のニューロトロフィンはNPD1合成アゴニスト
www.ncbi.nlm.nih.gov/pubmed/17670936
sAPPα
sAPPαは、NPD1生合成酵素PホスホリパーゼA2および/またはNPD1生合成に不可欠な15-LOX様酵素を活性化する可能性がある。
www.jbc.org/content/284/26/17877
www.jbc.org/content/278/44/43807
PPARγ
DHA由来のニューロプロテクチンD1は、アルツハイマー病モデルにおいてセクレターゼおよびPPARγを介したメカニズムを介してニューロンの生存を誘導する。
www.ncbi.nlm.nih.gov/pubmed/21246057
マレシン(Maresin)
(MaR1〜MaR2)
マレシン1(MaR1)とマレシン2(MaR2)は、リポキシゲナーゼである12-LOXによってDHAから代謝される。
マレシン1(MaR1)
マレシン1は、強力な抗炎症作用、鎮静作用、鎮痛作用、創傷治癒作用を示す。
MaR1は炎症収束の後期に生成され、組織再生を促進し、運動機能障害から保護し鎮痛作用を示す。
MaR1の作用の主要な細胞標的は、血管平滑筋(VSM)細胞と血管内皮細胞。
これらの細胞では、MaR1はTNFαによって誘導される内皮への単球の接着を弱める。
マレシン1は、VSMと内皮細胞の両方による活性酸素種の産生も阻害する。
www.ncbi.nlm.nih.gov/pubmed/27893465
アルツハイマー病患者の低いマレシン1
アルツハイマー病患者の嗅内皮質のマレシン1レベルは、同年齢のコントロール郡と比べて低いことが示されている。
細胞モデルの研究では、すべてのタイプのSPMがニューロンの生存を改善でき、マレシン1(MaR1)がミクログリア食作用を介したアミロイドβ42の低下により効果的であることが観察された。
www.ncbi.nlm.nih.gov/pubmed/26650044/
ミクログリアの改変によるアミロイドβ低下
マレシン1は大腸炎マウスモデルのマクロファージ表現型をM1からM2にシフトさせることで保護的作用を示す。
www.ncbi.nlm.nih.gov/pubmed/24038091/
PI3K / AKT経路の活性化
MaR1はPI3K / AKT経路を活性化してNedd4-2タンパク質をダウンレギュレートし、Na、K-アデノシントリホスファターゼ(ATPase)活性を改善し、肺胞液クリアランスを刺激した。
www.ncbi.nlm.nih.gov/pubmed/28218740/
記憶機能障害・炎症の改善
マレシン1はアミロイドβ42によって誘導される炎症誘発性サイトカインTNF-α、IL-6、およびMCP-1産生を減少させ、Aβ42の影響とは関係なく抗炎症性サイトカインIL-2、IL-10分泌を増加させ、アルツハイマー病マウスモデルの炎症と記憶機能障害の改善を示した。
www.ncbi.nlm.nih.gov/pmc/articles/PMC6803487/
神経保護作用
マレシン1は、脊髄損傷後の炎症の解消、神経保護、および機能的な神経学的回復を促進する。
www.ncbi.nlm.nih.gov/pubmed/29109234
マレシン2(MaR2)
マレシン2は好中球の浸潤を減少させ、マクロファージの食作用を増強させ、死細胞と死にかけている細胞の食作用を促進することが示されている。
www.ncbi.nlm.nih.gov/pubmed/25036362
SPM様活性 PUFA代謝産物
EFOX(Electrophilic oxo-derivatives)
EPA、DPA由来の求電子性脂肪酸オキソ誘導体(EFOX)
DHAから酵素、非酵素経路を介して生成される。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4538325/
PPARγリガンド
17-oxoDHAおよび13-oxoDHAはマクロファージの活性化によるCOX-2触媒メカニズムによって生成される。これらのオキソ誘導体は、PPARγアゴニストとして作用し、マクロファージの炎症性サイトカインおよび一酸化窒素の産生を阻害する。
www.ncbi.nlm.nih.gov/pubmed/20436486
17-oxoDHAは、PPARα、γ二重共有アゴニスト。
pubs.acs.org/doi/10.1021/acschembio.6b00338
ヒドロキシ脂肪酸分岐脂肪酸エステル(FAHFA)
FAHFAファミリーは3つのメンバーが同定されている。
9-DHAHLA、13-DHAHLA、14-DHAHDHA。
13-DHAHLAが強力な抗炎症性および分解性を発揮する一方で、リポ多糖によるマクロファージの活性化を抑え、食作用を増強することが実証されている
www.ncbi.nlm.nih.gov/pubmed/27313314
プロスタグランジン
プロスタグランジンは強力な局所作用性血管拡張薬であり、血小板の凝集を抑制する。
血管拡張作用と関連してプロスタグランジンは炎症にも関与する。
en.wikipedia.org/wiki/Prostaglandin
イソプロスタン
痛覚、知覚を増強する炎症性メディエーターとして強力な生物学的活性を有している。
en.wikipedia.org/wiki/Isoprostane
www.ncbi.nlm.nih.gov/pubmed/10869392
ニューロプロスタン/Neuroprostanes
Neuroprostanes(NP)
ニューロプロスタン(neuroprostane)は、DHAのフリーラジカル非酵素的過酸化として生成されるプロスタグランジン様化合物。
痛覚を増強するヒトマクロファージ反応を阻害する抗炎症メディエーターとして強力な生物学的活性がある。
en.wikipedia.org/wiki/Neuroprostanes
エロバノイド(ELV)
(ELV-N32およびELV-N34)
エロバノイド/elovanoids(ELV)は、独自の構造をもつ新しいクラスの内因性プロ恒常性脂質メディエーター。
www.ncbi.nlm.nih.gov/pubmed/30244005
uncompensated oxidative stress (UOS)、酸素グルコース欠乏(OGD)、NMDA受容体の興奮毒性、MCAo誘発虚血性脳卒中などの細胞障害に対抗するために、オメガ3超長鎖多価不飽和脂肪酸(VLC-PUFA、n-3)から急速に作られる最初の生物活性化学メッセンジャー。
www.nature.com/articles/s41598-017-05433-7
エロバノイドの減少は、実験的証拠から脳卒中モデル、脳卒中、てんかん、パーキンソン病、外傷性脳損傷などの神経変性疾患に関与することが示唆されている。
エロンガーゼ酵素 ELOVL4
エロバノイドはELOVL4によって触媒されDHAから合成される。
sciencemission.com/site/index.php?page=news&type=view&id=biochemistry%2Fnew-class-of-lipid

