Peter A McCullough 1, Paul E Alexander 2, Robin Armstrong 3, Cristian Arvinte 4, Alan F Bain 5, Richard P Bartlett 6, Robert L Berkowitz 7, Andrew C Berry 8, Thomas J Borody 9, Joseph H Brewer 10, Adam M Brufsky 11, Teryn Clarke 12, Roland Derwand 13, Alieta Eck 14, John Eck 14, Richard A Eisner 15, George C Fareed 16, Angelina Farella 17, Silvia N S Fonseca 18, Charles E Geyer Jr 19, Russell S Gonnering 20, Karladine E Graves 21, Kenneth B V Gross 22, Sabine Hazan 23, Kristin S Held 24, H Thomas Hight 25, Stella Immanuel 26, Michael M Jacobs 27, Joseph A Ladapo 28, Lionel H Lee 29, John Littell 30, Ivette Lozano 31, Harpal S Mangat 32, Ben Marble 33, John E McKinnon 34, Lee D Merritt 35, Jane M Orient 36, Ramin Oskoui 37, Donald C Pompan 38, Brian C Procter 39, Chad Prodromos 40, Juliana Cepelowicz Rajter 41, Jean-Jacques Rajter 41, C Venkata S Ram 42, Salete S Rios 43, Harvey A Risch 44, Michael J A Robb 45, Molly Rutherford 46, Martin Scholz 47, Marilyn M Singleton 48, James A Tumlin 49, Brian M Tyson 50, Richard G Urso 51, Kelly Victory 52, Elizabeth Lee Vliet 53, Craig M Wax 54, Alexandre G Wolkoff 55, Vicki Wooll 56, Vladimir Zelenko 57
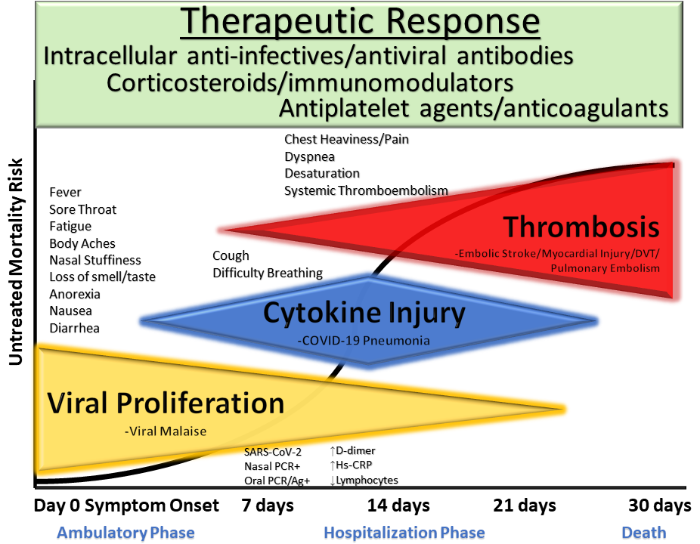
SARS-CoV-2ウイルスの世界的な蔓延は、COVID-19疾患、入院、死亡の急増をもたらしている。生命を脅かすCOVID-19病の複雑で多面的な病態生理は、ウイルス媒介性臓器障害、サイトカインストーム、および血栓症を含むため、壊滅的な疾患のすべての構成要素に対処するための早期介入が必要である。
SARS-CoV-2 SARS-CoV-2; COVID-19; 入院; 死亡率; 外来治療; 抗感染症; 抗炎症薬; 抗ウイルス薬; 副腎皮質ステロイド薬; 抗血小板薬; 抗凝固薬; 続発性多剤併用療法
SARS-CoV-2(COVID-19)のパンデミックは世界各地で進行しており、それぞれの国や地域で頻度、入院、死亡の点で異なる疫学的パターンが開発されている。効果的なパンデミック対応には4つの柱がある。(図1)
さらに、可能な場合には、急性疾患の蔓延と発生率を低下させるために、予防接種を追加の柱と考えることもできる。多くの国では、表1に示すように、ジェネリック医薬品やサプリメントのキットを配布し、早期の在宅治療という第2の柱を含めて、4つの柱すべてを運用している。米国、カナダ、英国、西欧諸国、オーストラリア、南米諸国では、パンデミック対応のために以下の3つの主要分野に重点を置いていた。
現在のところ、COVID-19の経口外来治療に関する包括的な無作為化試験の報告はなく、短期的には期待できない。これまでに報告されたほとんどの経口治療試験は、小規模で、パワー不足、非盲検、偏ったエンドポイントの医師による評価に依存しているか、場合によっては、科学的な正当性や安全性の懸念がないまま、早期に中止されている。
COVID-19は感染性が高いため、多くの米国の外来診療所ではCOVID-19の患者をケアしておらず、入院前の期間に患者に外来治療を行う試みはほとんど、あるいは全く行われていないことが研究から示唆されている(Price-Haywood et al 2020)。切実に必要とされていた試験が早期に閉鎖された最も顕著な例として、米国国立衛生研究所(National Institutes of Health)の研究で、外来COVID-19患者におけるヒドロキシクロロキン( ヒドロキシクロロキン)とアジスロマイシンの30日後の試験で、予算2000人の患者のうち20人しか登録されていない(National Institutes of Health, 2020a, b)。
それ以降、外来試験に関する実質的な連邦政府の取り組みは行われていないため、公衆衛生政策に影響を与えるような将来の結果は期待できない(World Health Organisation, 2020)。
本稿執筆時点では、COVID-19の外来患者における初期のウイルス複製、サイトカインストーム、血栓症の管理を目的としたSMDTレジメンの臨床試験は計画されていない(図3)。したがって、症状の強さや重症度を軽減し、入院や死亡のリスクを軽減するという目標を達成するために、COVID-19における革新的な早期SMDTが緊急に必要とされている。この外来でのもう一押しは、医療システムの負担軽減に劇的な影響を与える可能性がある。
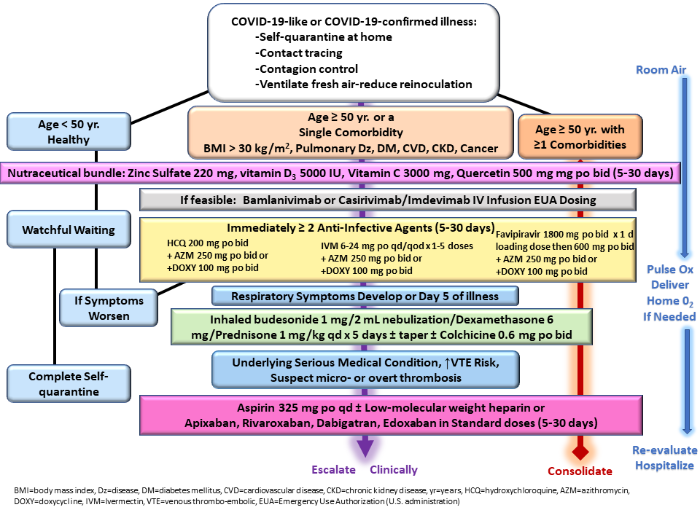
Yr=年、BMI=体格指数、Dz=疾患、DM=糖尿病、心血管疾患=心血管疾患、慢性腎臓病、 ヒドロキシクロロキン=ヒドロキシクロロキン、IVM=イベルメクチン、Mgt=管理、Ox=オキシメトリー、参考文献より許可を得て転載
早期治療の臨床試験からのエビデンスがない場合、または早期治療へのコミットメントがない場合、病態生理学、治療された自然史、および臨床的判断に関する他の科学的情報を合わせて、COVID-19の現代的な外来管理の指針としなければならない(McCullough et al 2020b)。経験的に導き出された早期介入レジメンで一貫して管理されている患者集団における転帰を報告する観察研究は、現在のところ、現在の標準的な非介入に対するこれらの広く利用可能で安価で安全な代替手段の安全性および有効性について許容できるレベルのエビデンスを提供している(Khan et al 2020)。病態生理学および観察データに基づいて、共有の意思決定を用いた各医師および患者は、COVID-19管理のためのコースを設定した:症状の強度および持続時間を減少させ、入院および死亡のリスクを減少させることを目的とした自己検疫または経験的治療での見守り待機(Gopalakrishnan et al 2020)。幸いなことに、50歳未満のCOVID-19を有するほとんどの健康な人は自己限定的な疾患を有しており、重篤な症状がない場合には特定の治療は勧められない。しかしながら、下気道症状の発現は、酸素化状態の評価を正当化し、低酸素血症または肺浸潤の文書化による介入を促す可能性のある胸部画像検査を考慮する必要があることを助言すべきである。
しかし、50歳以上の人、または1つ以上の併存疾患を持つ人は、入院と死亡のリスクが1%以上増加し、年齢が上がるにつれて、またより多くの疾患(肥満、糖尿病、心臓病、肺疾患、腎疾患、悪性腫瘍)を持つ人は、入院と死亡のリスクが40%まで大幅に増加するため、経口治療の利点とリスクを考慮した最善の医学的判断に基づいて、早期の外来治療が必要である。SARS-CoV-2は、多くのウイルス感染症と同様に、経過の早い段階で複数の薬剤に適応する可能性があるが、投与が遅れて入院中に投与されると、同じ治療に対する反応性が低くなる(Vaduganathan et al 2020)。COVID-19に対する革新的なSMDTレジメンは、入院患者から学んだ原則と、治療を受けた外来患者のデータを利用している。
初日にCOVID-19の徴候や症状が認められる外来患者(図2)では、多くの場合、鼻腔内リアルタイム逆転写や経口抗原検査がまだ実施されていないため、以下の3つの治療原則が適用される(Centers for Disease Control and Prevention, 2020):
本症の基本的特徴(発熱、ウイルス性倦怠感、鼻づまり、味覚・嗅覚の低下、乾性咳嗽など)を有し、検査で偽陰性が保留または疑われる患者に対しては、COVID-19が確認された患者と同様の治療を行う。
自己隔離の主要な目標は伝染の制御である(Nussbaumer-Streit et al 2020)。集会環境でのマスキングと社会的距離に大きな重点が置かれてきたが、多くの情報源は、ウイルス感染の主な場所が家庭内(呼吸器、接触、経口糞便)で起こることを示唆している(Xu et al 2020;Jefferson et al 2020)。家庭内の感染していないすべての接触者にマスクを着用し、手指消毒剤を頻繁に使用し、手洗いをすることは、家族の一人以上が病気になった場合には必須である。カウンタートップ、ドアの取っ手、電話機、その他の機器などの表面を殺菌することが推奨されている。可能であれば、他の親しい関係者は家の外に出て、SARS-CoV-2 のない避難所を探すことができる。
複数の研究から得られた知見は、SARS-CoV-2の拡散抑制に関する政策は部分的にしか有効ではなく、ウイルス移行の最も頻繁な部位である家庭への拡大は妥当であることを示している(Hsiang et al 2020; Xiao et al 2020)。COVID-19の在宅治療の大きな利点の1つは、個人または家族単位での隔離および完全な接触追跡を維持できることである。治療が、薬の配達とともに家庭で提供される場合、緊急ケアセンター、診療所、病院への旅行を減らすか、または排除することができる。これにより、運転手、他の患者、スタッフ、および医療従事者への拡散が制限される。逆に、プライマリケアの医師および医療システム側の治療的虚無主義は、見捨てられたと感じる急性COVID-19患者の間に不安とパニックを引き起こし、隔離を解除して緊急ケアセンター、緊急治療室および病院に助けを求める可能性を高める。
Zelenkoら(Derwand et al 2020)によって最初に提案されたように、COVID-19の予防および抗感染症薬との併用による治療のための微量栄養素およびサプリメントの使用について、かなりの関心および研究がなされている。一般に、これらの薬剤は治癒的ではないが、治療反応を増強するための治療レジメンを補助する。補充の目的は、COVID-19の死亡率に関連する欠乏を有する者に補充し、ウイルスの複製および組織損傷を減少させるのを助けることである。
ウイルスの複製の速度、量、および期間を迅速に減少させることは、症状のある病気の初日に開始することを目的とした抗ウイルス療法の目標である。迅速な治療の説得力のある根拠は、呼吸器上皮、血管内皮、および臓器に対するウイルスの直接的な傷害の程度を最小限にすることである(Izzedine et al 2020)。SARS-CoV-2の複製に依存する不適応な宿主応答は、炎症性細胞の活性化、サイトカイン、血管内皮傷害、および血栓症を含む併用抗感染薬の早期開始によって減衰され得る(Singhania et al 2020)。
SARS-CoV-2感染は、50歳以上の患者および1つ以上の合併症を有する患者における重篤な疾患および死亡率の増加と関連しているため、臨床家は、臨床的に適切と考えられる場合には、少なくとも2つの市販の抗感染薬を、医学的に必要な「適応外」処方で使用すべきである(ShojaeiおよびSalari 2020)。
逆に、致命的な可能性のある疾患の早期に経口治療を保留する決定は、ハイリスク成人におけるCOVID-19の自然な未治療歴が、入院、院内合併症、および死亡のリスクを含むことを十分に理解した上で、患者との共有の意思決定プロセスで行われるべきである。医師と患者は、入院を回避する唯一の方法は、許容できる安全性で成功する可能性のあるSMDTを経験的に使用することであることを理解すべきである。
最近拡大されたバマニビマブの静脈内投与の使用許可は、限られた数の患者さんが利用できるもう一つの選択肢であるが、この治療法の広範な基準を満たすすべての患者さんを治療するには供給量が不足するため、経口投与の代替品の利用は依然として不可欠である。
ヒドロキシクロロキン( ヒドロキシクロロキン)は、抗マラリア薬/抗炎症薬であり、ヒト細胞内でのウイルスのエンドソーム転送を障害する。 ヒドロキシクロロキンはまた、亜鉛を細胞内に運搬し、ウイルス複製の中核酵素であるSARS-CoV-2 RNA依存性RNAポリメラーゼをブロックする亜鉛イオノフォアでもある(te Velthuis et al 2010)。継続的に更新された ヒドロキシクロロキン試験の合成は、以下を支持している(COVID-19治療 2020):
ヒドロキシクロロキンは、1955年に米国食品医薬品局によって承認され、それ以来、世界中で何億人もの人々に使用されており、多くの国で市販されており、よく特徴づけられた安全性プロファイルを有している(Fram et al 2020;SchrezenmeierおよびDörner 2020)。無症候性QT延長は、 ヒドロキシクロロキンでの発生頻度は低い(1%未満)が、よく認識されている(Prodromos et al 2020)。
グルコース-6-リン酸脱水素酵素欠損症の患者では、 ヒドロキシクロロキンを使用すべきではない(Aguilar 2020)。急性重症COVID-19疾患の設定では、 ヒドロキシクロロキンの非存在下で症候性不整脈が発現し、サイトカインストームおよび重篤な疾患に起因することがある(Elsaid et al 2020)。データ安全性およびモニタリング委員会は、これまでに発表された ヒドロキシクロロキン臨床試験において安全性の懸念を宣言していない。
QT延長症候群の個人歴または家族歴を有するまれな患者、追加のQT延長薬、禁忌薬(ドフェチリド、ソタロールなど)を服用している患者は、注意して治療し、外来でQTcをモニターする計画を立てるべきである。典型的な ヒドロキシクロロキンレジメンは、症状の継続に応じて200mgを5~30日かけて2回に分けて投与する。
イベルメクチン(IVM)は、最近ではSARS-CoV-2(Heidary and Gharebaghi, 2020)を含む様々なウイルスに対して抗ウイルス活性を有することが示されている幅広いスペクトルの抗寄生虫剤である。この薬剤は忍容性が高く、高い治療指数を有し、37億回以上の治療実績がある安全性プロファイルを有し、COVID-19患者の初期臨床試験において、単独またはドキシサイクリンまたはアジスロマイシンのいずれかとの併用で使用されている(Rahman et al 2020)。無作為化試験およびプロスペクティブ試験が多数あり、いずれも本報告時点で臨床転帰において有効性が示されている(Khan et al 2020;Nunez et al 2020;Alam et al 2020;Gorial et al 2020;Chowdhury et al 2020)。
したがって、 ヒドロキシクロロキンが使用できず、ファビピラビルが利用できない患者においては、IVM(200~600 mcg/kg [6~36 mg]単回経口投与を毎日または隔日で2~3回投与)が、COVID-19の経過の初期にウイルス複製を減少させることを意図したSMDTのベースとなり得ることは合理的である。
ファビピラビルは、RNA依存性RNAポリメラーゼの経口選択的阻害剤であり、複数の国でCOVID-19の外来使用が承認されている(Coomes and Haghbayan, 2020)。ファビピラビルは安全であり、ほとんどの研究でウイルスの鼻腔内脱落を7日未満に短縮する(Pilkington et al 2020;Ivashchenko et al 2020)。
救急外来、救急センター、診療所などの抗体輸液を行う施設での迅速検査でSARS-CoV-2と診断された場合は、抗体輸液と同時にCOVID-19を開始するのが妥当である。逆に、検疫を維持したまま在宅輸液で安全に手配できる場合には、医師が本療法を処方して、長期の経口治療の効果を増強することもある。このとき、患者に隔離を解除してもらい、外来輸液を受けるためにドライバーや医療従事者への感染拡大のリスクを冒すことは魅力的ではない。
入院を促し、多臓器不全に至る可能性のあるCOVID-19の症状は、サイトカインストームに起因する。急性疾患のCOVID-19患者の特徴的なプロフィールは、相対的な好中球減少を伴う白血球症を含む。COVID-19患者のうち、血清IL-6およびIL-10レベルは、重症患者では上昇している(Han et al 2020)。COVID-19では、最初の呼吸器所見のいくつかは、咳および呼吸困難である。これらの特徴は、炎症およびサイトカイン活性化に起因する。経口コルチコステロイドの早期使用は、他の炎症性肺疾患と同様に、これらの特徴を有するCOVID-19患者に対する合理的な介入である(Kolilekas et al 2020;Singh et al 2020)。
ブデソニド1mg/2mLをネブライザーまたは200mcg/吸入器を介して4時間ごとに吸入することも可能であるが、COVID-19での有効性については発表されていない。RECOVERY試験では、COVID-19を有する入院患者6425人を2:1の割合でオープンラベルのデキサメタゾン6mg po/IV qdを10日間まで無作為に投与し、デキサメタゾンが死亡率を減少させたことを明らかにした(HR = 0.65,95% CI 0.51-0.82,P < 0.001)(Horby et al 2020)。同調して、重症のCOVID-19患者1703人を対象としたメタアナリシスでは、死亡の相対リスクが36%減少したことが明らかになった(Sterne et al 2020)。
ステロイドによるウイルス複製の延長に関する安全性の懸念は立証されていない(Masiá et al 2020)。これらの知見を臨床的に拡張したものとして、中等度以上の肺症状を有するCOVID-19患者に、5日目以降に在宅でステロイドを投与することがある(Szente Fonseca et al 2020)。デキサメタゾン6mg po qdまたはプレドニゾン1mg/kgを1日1回5日間経口投与することができ、その後のテーパリングの有無にかかわらず。
コルヒチンは、痛風や心膜炎に使用される非ステロイド性抗ミトチン薬であり、微小管の末端に結合して炎症細胞の細胞内集合を阻害することで、炎症細胞のメタフェースを阻害する。
COVID-19の入院患者105人を対象としたGRECCO-19無作為化オープンラベル試験( ヒドロキシクロロキンで98%、AZMで93%が治療された)では、コルヒチンがDダイマーレベルの低下と臨床転帰の改善に関連していることが明らかになった(Deftereos et al 2020)。臨床主要エンドポイント(世界保健機関(WHO)序数尺度の2ポイント変化)は、対照群で14.0%(50人中7人)コルヒチン群で1.8%(55人中1人)に発生した(オッズ比,0.11;95%CI,0.01~0.96;P=0.02)(世界保健機関 2020)。
短期的な安全性プロファイルは十分に理解されているため、サイトカインストームおよび筋膜炎の影響を軽減する試みとして、本剤をコルチコステロイドとともに検討することは妥当である。0.6mg po bid x 3日後に0.6mg po qdを30日間投与する方法が考えられる。
複数の研究で、病理学的マクロおよびミクロ血栓症の増加率が記載されている(Bösmüller et al 2020;McFadyen et al 2020)。COVID-19患者は、肺血栓症の可能性を示唆する脱飽和に関連した胸の重さを記載している(Bhandari et al 2020)。複数の報告では、急性疾患のCOVID-19患者におけるDダイマーレベルの上昇が記述されており、それは深部静脈血栓症および肺塞栓症のリスクの増加と一貫して関連している(Chan et al 2020;Artifoni et al 2020;Mestre-Gómez et al 2020)。剖検研究では、致死的COVID-19症例の半数以上に深部静脈血栓が認められた肺微小血栓症およびあからさまな塞栓症が記載されている(Ackermann et al 2020;Burlacu et al 2020)。これらの観察は、特異的な内皮損傷および血栓症が、入院および支持療法の重要な理由である酸素脱飽和に役割を果たしているという仮説を支持する(Zhang et al 2020b)。
COVID-19入院患者2773例を対象としたレトロスペクティブ研究では,28%が入院後2日以内に抗凝固療法を受けており,より重症な症例で使用されているにもかかわらず,抗凝固療法の投与は死亡率の低下と関連していた,HR = 0.86/日,95%CI:0.82~0.89;P<0.001.院内抗凝固薬の現代的な使用は、~30%の症例にとどまっている(Vahidy et al 2020) . 低分子ヘパリンまたは新規抗凝固薬の先制使用は、COVID-19死亡率の50%以上の減少と関連している(Billett et al 2020)。抗凝固薬はまた、血栓性合併症、D-ダイマー値の上昇、および併存疾患スコアの高いCOVID-19入院患者の死亡を減少させる(Tang et al 2020)。最後に、多くの急性期外来患者もまた、COVID-19に適用可能な心筋梗塞/静脈血栓塞栓予防の一般的な適応またはリスクを有している(Moores et al 2020;Ruocco et al 2020)。
アスピリンと新規経口抗凝固薬の外来ランダム化試験が進行中である。しかしながら、壊滅的な脳卒中および全身性血栓塞栓症の報告および予防的および治療的使用の両方で死亡率が大幅に減少していることを考えると、COVID-19のハイリスク患者すべてにアスピリン325mg po qdを投与し、心臓、肺、腎臓、または悪性疾患の既往歴のある患者には全身性抗凝固薬を投与することが賢明である(Yamakawa et al 2020)。
遠隔医療は、COVID-19の初期評価と管理のための扱いやすい手段であり、患者が自宅で自己隔離されたままでいることを可能にする。患者の臨床的印象は、音声とビデオのフィードで得ることができる。主な補足情報には、バイタルサインと体温の自己または家族の測定が含まれている。安全な外来管理の重要な要素は、必要に応じて人工呼吸のための入院へとエスカレーションしながら、毎日の遠隔医療による直接監督の下で、室内空気または処方された在宅酸素(酸素濃縮器)で動脈酸素飽和度を維持することである。セルフプローニングは、医学的に洗練された患者で、在宅でのモニタリングが良好であれば可能である(Westafer et al 2020)。
このレビューで議論された介入は、介護施設内のCOVID-19治療ユニットおよび他の非病院設定の高齢者にも拡張され得る。内服薬に加えて、これらのセンターでは、転院のリスクを減らすことを目標に、輸液および非経口薬(すなわち、バムラニビマブ、カシリビマブ/イムデビマブ)酸素、および補助人工呼吸を提供することができる。
SARS-CoV-2の大パンデミックは、100年に一度のパンデミックであり、コミュニティ設定の外来患者での大規模な無作為化試験の実施をサポートするためのインフラストラクチャの迅速な確立によって対処されなかった。インフルエンザのようなウイルス複製の初期段階は、ハイリスク患者のより重篤な後遺症のリスクを軽減する可能性のある治療の機会を提供している。
現在、広く入手可能で安価なジェネリック医薬品を評価する無作為化臨床試験が政府の支援を受けておらず、また、指導的な外来治療ガイドラインがない(米国、カナダ、英国、西欧諸国、オーストラリア、南米諸国の一部)ことを考えると、臨床家は臨床的判断に従って行動し、十分な情報を得た患者と共有した意思決定をしなければならない。
脚注:これらの国でCOVID-19の早期治療に使用されている薬剤を把握するために、ブラジル、ペルー、スペイン、台湾、米国などの政府機関のウェブサイトを検索した。また、中国、フランス、インド、韓国、アフリカ諸国のpubmended誌に掲載されている研究者も探した。追加情報は、アルゼンチン、バングラデシュ、コロンビア、メキシコ、アフリカ諸国などのインターネットの信頼できる情報源からも得た。
AAPS. (2020) A Guide to Home-Based COVID Treatment. American Association of Pharmaceutical Scientists. Available at: https://aapsonline.org/covidpatientguide/.
[Cited within: 1]
Ackermann, M., Verleden, S. E., Kuehnel, M., Haverich, A., Welte, T., Laenger, F., Vanstapel, A., Werlein, C., Stark, H., Tzankov, A., Li, W. W., Li, V. W., Mentzer, S. J. and Jonigk, D. (2020) Pulmonary Vascular Endothelialitis, Thrombosis, and Angiogenesis in Covid-19. New England Journal of Medicine 383, 120-128.
[Cited within: 1]
Agencia Española de Medicamentos y Productos Sanitarios. Información acerca del uso de hidroxicloroquina para el tratamiento de COVID-19. Available at https://www.aemps.gob.es/informa/notasinformativas/laaemps/2020-laaemps/informacion-acerca-del-uso-de-hidroxicloroquina-para-el-tratamiento-de-covid-19/ (Acessed: 11 November, 2020).
[Cited within: 1]
Aguilar, J. (2020) Hemolytic Anemia in a Glucose-6-Phosphate Dehydrogenase-Deficient Patient Receiving Hydroxychloroquine for COVID-19: A Case Report. The Permanente Journal 24, 20.158.
[Cited within: 1]
Ailani, R. K., Agastya, G., Ailani, R. K., Mukunda, B. N. and Shekar, R. (1999) Doxycycline is a cost-effective therapy for hospitalized patients with community-acquired pneumonia. Archives of internal medicine159, 266-270.
[Cited within: 1]
Alam, M. T., Murshed, R., Bhiuyan, E., Saber, S., Alam, R. F. & Choudhury Robin, R. (2020). A Case Series of 100 COVID-19 Positive Patients Treated with Combination of Ivermectin and Doxycycline. Journal of Bangladesh College of Physicians and Surgeons, 38.
[Cited within: 1]
Argenziano, M. G., Bruce, S. L., Slater, C. L., Tiao, J. R., Baldwin, M. R., Barr, R. G., Chang, B. P., Chau, K. H., Choi, J. J., Gavin, N., Goyal, P., Mills, A. M., Patel, A. A., Romney, M. S., Safford, M. M., Schluger, N. W., Sengupta, S., Sobieszczyk, M. E., Zucker, J. E., Asadourian, P. A., Bell, F. M., Boyd, R., Cohen, M. F., Colquhoun, M. I., Colville, L. A., de Jonge, J. H., Dershowitz, L. B., Dey, S. A., Eiseman, K. A., Girvin, Z. P., Goni, D. T., Harb, A. A., Herzik, N., Householder, S., Karaaslan, L. E., Lee, H., Lieberman, E., Ling, A., Lu, R., Shou, A. Y., Sisti, A. C., Snow, Z. E., Sperring, C. P., Xiong, Y., Zhou, H. W., Natarajan, K., Hripcsak, G. and Chen, R. (2020) Characterization and clinical course of 1000 patients with coronavirus disease 2019 in New York: retrospective case series. British Medical Journal 369, m1996.
[Cited within: 1]
Arshad, S., Kilgore, P., Chaudhry, Z. S., Jacobsen, G., Wang, D. D., Huitsing, K., Brar, I., Alangaden, G. J., Ramesh, M. S., McKinnon, J. E., O’Neill, W. and Zervos, M. (2020) Treatment with hydroxychloroquine, azithromycin, and combination in patients hospitalized with COVID-19. International Journal of Infectious Diseases97, 396-403.
[Cited within: 1]
Artifoni, M., Danic, G., Gautier, G., Gicquel, P., Boutoille, D., Raffi, F., Néel, A. and Lecomte, R. (2020) Systematic assessment of venous thromboembolism in COVID-19 patients receiving thromboprophylaxis: incidence and role of D-dimer as predictive factors. Journal of Thrombosis and Thrombolysis50, 211-216.
[Cited within: 1]
Bastaminejad, S. and Bakhtiyari, S. (2020) Quercetin and its relative therapeutic potential against COVID-19: A retrospective review and prospective overview. Current Molecular Medicine 20. Epub ahead of print.
[Cited within: 1]
Beigmohammadi, M. T., Bitarafan, S., Hoseindokht, A., Abdollahi, A., Amoozadeh, L., Mahmoodi Ali Abadi, M. and Foroumandi, M. (2020) Impact of vitamins A, B, C, D, and E supplementation on improvement and mortality rate in ICU patients with coronavirus-19: a structured summary of a study protocol for a randomized controlled trial. Trials21, 614.
[Cited within: 1]
Belayneh, A. (2020) Off-Label Use of Chloroquine and Hydroxychloroquine for COVID-19 Treatment in Africa Against WHO Recommendation. Research and Reports in Tropical Medicine 11, 61-72.
[Cited within: 3]
Bhandari, S., Rankawat, G., Bagarhatta, M., Singh, A., Singh, A., Gupta, V., Sharma, S. and Sharma, R. (2020) Clinico-Radiological Evaluation and Correlation of CT Chest Images with Progress of Disease in COVID-19 Patients. The Journal of the Association of Physicians of India68, 34-42.
[Cited within: 1]
Bhimraj, A., Morgan, R. L., Shumaker, A. H., Lavergne, V., Baden, L., Cheng, V. C. C., Edwards, K. M., Gandhi, R., Gallagher, J., Muller, W. J., O’Horo, J. C., Shoham, S., M. Murad, H., Mustafa, R. A., Sultan, S. and Falck-Ytter, Y. (2020) Infectious diseases society of America guidelines on the treatment and management of patients with COVID-19. Available at: https://www.idsociety.org/practice-guideline/covid-19-guideline-treatment-and-management/.
[Cited within: 1]
Billett, H. H., Reyes-Gil, M., Szymanski, J., Ikemura, K., Stahl, L. R., Lo, Y., Rahman, S., Gonzalez-Lugo, J. D., Kushnir, M., Barouqa, M., Golestaneh, L. and Bellin, E. (2020) Anticoagulation in COVID-19: Effect of Enoxaparin, Heparin, and Apixaban on Mortality. Thromb Haemost. Epub ahead of print.
[Cited within: 1]
Brian, W. (2020) Covid-19: Algeria and Morocco continue using chloroquine despite concerns. al-bab.com. Available at: https://al-bab.com/blog/2020/05/covid-19-algeria-and-morocco-continue-using-chloroquine-despite-concerns (Accessed: 11 November, 2020).
[Cited within: 1]
Bösmüller, H., Traxler, S., Bitzer, M., Häberle, H., Raiser, W., Nann, D., Frauenfeld, L., Vogelsberg, A., Klingel, K. and Fend, F. (2020) The evolution of pulmonary pathology in fatal COVID-19 disease: an autopsy study with clinical correlation. Virchows Archiv477, 349-357.
[Cited within: 2]
Burlacu, A., Genovesi, S., Popa, I. V. and Crisan-Dabija, R. (2020) Unpuzzling COVID-19 Prothrombotic State: Are Preexisting Thrombophilic Risk Profiles Responsible for Heterogenous Thrombotic Events? Clinical and Applied Thrombosis/Hemostasis26, 1076029620952884.
[Cited within: 1]
Carr, A. C. and Rowe, S. (2020) The Emerging Role of Vitamin C in the Prevention and Treatment of COVID-19. Nutrients12.
[Cited within: 1]
Chan, K. H., Slim, J. and Shaaban, H. S. (2020) Pulmonary Embolism and Increased Levels of D-Dimer in Patients with Coronavirus Disease. Emerging Infectious Diseases26, 2522-2533.
[Cited within: 1]
Chen, L. D. (2020) Effects of ambient temperature and humidity on droplet lifetime – A perspective of exhalation sneeze droplets with COVID-19 virus transmission. International Journal of Hygiene and Environmental Health229, 113568.
[Cited within: 2]
Chen, P., Nirula, A., Heller, B., Gottlieb, R. L., Boscia, J., Morris, J., Huhn, G., Cardona, J., Mocherla, B., Stosor, V., Shawa, I., Adams, A. C., Van Naarden, J., Custer, K. L., Shen, L., Durante, M., Oakley, G., Schade, A. E., Sabo, J., Patel, D. R., Klekotka, P. and Skovronsky, D. M. (2020) SARS-CoV-2 Neutralizing Antibody LY-CoV555 in Outpatients with Covid-19. The New England Journal of Medicine NEJMoa2029849. Epub ahead of print.
Chow, J. H., Khanna, A. K., Kethireddy, S., Yamane, D., Levine, A., Jackson, A. M., McCurdy, M. T., Tabatabai, A., Kumar, G., Park, P., Benjenk, I., Menaker, J., Ahmed, N., Glidewell, E., Presutto, E., Cain, S., Haridasa, N., Field, W., Fowler, J. G., Trinh, D., Johnson, K. N., Kaur, A., Lee, A., Sebastian, K., Ulrich, A., Peña, S., Carpenter, R., Sudhakar, S., Uppal, P., Fedeles, B. T., Sachs, A., Dahbour, L., Teeter, W., Tanaka, K., Galvagno, S. M., Herr, D. L., Scalea, T. M. and Mazzeffi, M. A. (2020) Aspirin Use is Associated with Decreased Mechanical Ventilation, ICU Admission, and In-Hospital Mortality in Hospitalized Patients with COVID-19. Anesthesia & Analgesia. Online ahead of print.
[Cited within: 1]
Chowdhury, A., Shahbaz, M., Karim, M.R., Islam, J., Guo, D. and He, S. (2020). A Randomized Trial of Ivermectin-Doxycycline and Hydroxychloroquine-Azithromycin therapy on COVID19 patients. Research Square, published online. doi: 10.21203/rs.3.rs-38896/v1.
[Cited within: 1]
Cione, E., La Torre, C., Cannataro, R., Caroleo, M. C., Plastina, P. and Gallelli, L. (2019) Quercetin, Epigallocatechin Gallate, Curcumin, and Resveratrol: From Dietary Sources to Human MicroRNA Modulation. Molecules25.
[Cited within: 1]
Emiliano Rodríguez Mega. Colombia Latin America’s embrace of an unproven COVID treatment is hindering drug trials. October 2020. Available from: https://www.nature.com/articles/d41586-020-02958-2 (Acessed: 11 Novemeber, 2020).
Colunga Biancatelli, R. M. L., Berrill, M., Catravas, J. D. and Marik, P. E. (2020) Quercetin and Vitamin C: An Experimental, Synergistic Therapy for the Prevention and Treatment of SARS-CoV-2 Related Disease (COVID-19). Frontiers in Immunology11, 1451.
[Cited within: 2]
Coronavirus a Tarde. Ministério da saúde avalia distribuir kit Covid de graça Sptember 2020. Available at: (Cited: 11 November, 2020).
[Cited within: 1]
Coomes, E. A. and Haghbayan, H. (2020) Favipiravir, an antiviral for COVID-19? Journal of Antimicrobial Chemotherapy75, 2013-2014.
[Cited within: 1]
COVID-19 Treatment Guidelines. 2020. Available at: https://www.covid19treatmentguidelines.nih.gov/ (Accessed: 25 November, 2020).
[Cited within: 1]
Dabbagh-Bazarbachi, H., Clergeaud, G., Quesada, I. M., Ortiz, M., O’Sullivan, C. K. and Fernández-Larrea, J. B. (2014) Zinc ionophore activity of quercetin and epigallocatechin-gallate: from Hepa 1-6 cells to a liposome model. Journal of Agricultural and Food Chemistry62, 8085-8093.
[Cited within: 1]
Deftereos, S. G., Giannopoulos, G., Vrachatis, D. A., Siasos, G. D., Giotaki, S. G., Gargalianos, P., Metallidis, S., Sianos, G., Baltagiannis, S., Panagopoulos, P., Dolianitis, K., Randou, E., Syrigos, K., Kotanidou, A., Koulouris, N. G., Milionis, H., Sipsas, N., Gogos, C., Tsoukalas, G., Olympios, C. D., Tsagalou, E., Migdalis, I., Gerakari, S., Angelidis, C., Alexopoulos, D., Davlouros, P., Hahalis, G., Kanonidis, I., Katritsis, D., Kolettis, T., Manolis, A. S., Michalis, L., Naka, K. K., Pyrgakis, V. N., Toutouzas, K. P., Triposkiadis, F., Tsioufis, K., Vavouranakis, E., Martinèz-Dolz, L., Reimers, B., Stefanini, G. G., Cleman, M., Goudevenos, J., Tsiodras, S., Tousoulis, D., Iliodromitis, E., Mehran, R., Dangas, G. and Stefanadis, C. (2020) Effect of Colchicine vs Standard Care on Cardiac and Inflammatory Biomarkers and Clinical Outcomes in Patients Hospitalized With Coronavirus Disease 2019: The GRECCO-19 Randomized Clinical Trial. JAMA Network Open3, e2013136.
[Cited within: 1]
Derosa, G., Maffioli, P., D’Angelo, A. and Di Pierro, F. (2020) A role for quercetin in coronavirus disease 2019 (COVID-19). Phytotherapy Research 10.1002/ptr.6887. Online ahead of print.
[Cited within: 1]
Derwand, R. and Scholz, M. (2020) Does zinc supplementation enhance the clinical efficacy of chloroquine/hydroxychloroquine to win today’s battle against COVID-19? Medical Hypotheses142, 109815.
[Cited within: 1]
Derwand, R., Scholz, M. and Zelenko, V. (2020) COVID-19 outpatients: early risk-stratified treatment with zinc plus low-dose hydroxychloroquine and azithromycin: a retrospective case series study. International Journal of Antimicrobial Agents56, 106214.
[Cited within: 1]
Diario oficial del bicentenario. Modifican el Documento Técnico: Prevención, Diagnóstico y Tratamiento de personas afectadas por COVID-19 en el Perú . Available from https://busquedas.elperuano.pe/normaslegales/modifican-el-documento-tecnico-prevencion-diagnostico-y-tr-resolucion-ministerial-n-270-2020-minsa-1866159-4/ (Acessed November 11, 2020).
[Cited within: 1]
Elsaid, O., McCullough, P. A., Tecson, K. M., Williams, R. S. and Yoon, A. (2020) Ventricular Fibrillation Storm in Coronavirus 2019. American Journal of Cardiology135, 177-180.
[Cited within: 1]
Entrenas Castillo, M., Entrenas Costa, L. M., Vaquero Barrios, J. M., Alcalá Díaz, J. F., López Miranda, J., Bouillon, R. and Quesada Gomez, J. M. (2020) “Effect of calcifediol treatment and best available therapy versus best available therapy on intensive care unit admission and mortality among patients hospitalized for COVID-19: A pilot randomized clinical study”. The Journal of Steroid Biochemistry and Molecular Biology203, 105751.
[Cited within: 1]
Fan, L., Jiang, S., Yang, X., Wang, Z. and Yang, C. (2020) COVID-19 Drug Treatment in China. Current Pharmacology Reports, 1-9.
[Cited within: 1]
Felix, T. (2020) Nigeria goes on with hydroxychloroquine clinical trials. Anadolu Agency. Available at: https://www.aa.com.tr/en/africa/nigeria-goes-on-withhydroxychloroquine-clinical-trials/1854814 (Accessed: 19 August, 2020).
[Cited within: 1]
Fram, G., Wang, D. D., Malette, K., Villablanca, P., Kang, G., So, K., Basir, M. B., Khan, A., McKinnon, J. E., Zervos, M. and O’Neill, W. W. (2020) Cardiac Complications Attributed to Hydroxychloroquine: A systematic review of the Literature Pre-COVID-19. Current Cardiology Reviews.
[Cited within: 1]
Gendrot, M., Andreani, J., Jardot, P., Hutter, S., Delandre, O., Boxberger, M., Mosnier, J., Le Bideau, M., Duflot, I., Fonta, I., Rolland, C., Bogreau, H., La Scola, B. and Pradines, B. (2020) In Vitro Antiviral Activity of Doxycycline against SARS-CoV-2. Molecules25.
[Cited within: 1]
Centers for Disease Control and Prevention. Available at: https://www.cdc.gov/coronavirus/2019-ncov/covid-data/ccovidview/05152020/covid-like-illness.html (Accessed: 03 July, 2020).
[Cited within: 1]
Gérard, A., Romani, S., Fresse, A., Viard, D., Parassol, N., Granvuillemin, A., Chouchana, L., Rocher, F. and Drici, M. D. (2020) “Off-label” use of hydroxychloroquine, azithromycin, lopinavir-ritonavir and chloroquine in COVID-19: A survey of cardiac adverse drug reactions by the French Network of Pharmacovigilance Centers. Thérapie75, 371-379.
[Cited within: 1]
Glatthaar-Saalmüller, B., Mair, K. H. and Saalmüller, A. (2017) Antiviral activity of aspirin against RNA viruses of the respiratory tract-an in vitro study. Influenza and Other Respiratory Viruses11, 85-92.
[Cited within: 1]
Gopalakrishnan, A., Mossaid, A., Lo, K. B., Vasudevan, V., McCullough, P. A. and Rangaswami, J. (2020) Fulminant Acute Kidney Injury in a Young Patient with Novel Coronavirus 2019. CardioRenal Medicine10, 217-222.
[Cited within: 1]
Gorial, F., Mashhadani, S., Sayaly, H.M., Dakhil, B.D., AlMashhadani, M., Aljabory, A.M., Avvas, H.M., Ghanim, M. and Rasheed, J. (2020) Effectiveness of Ivermectin as add-on Therapy in COVID-19 Management (Pilot Trial). MedRxiv, printed online.
[Cited within: 1]
Gupta, A., Kalantar-Zadeh, K. and Reddy, S. T. (2020a) Ramatroban as a Novel Immunotherapy for COVID-19. Journal of Molecular and Genetic Medicine14.
[Cited within: 1]
Gupta, S., Coca, S. G., Chan, L., Melamed, M. L., Brenner, S. K., Hayek, S. S., Sutherland, A., Puri, S., Srivastava, A., Leonberg-Yoo, A., Shehata, A. M., Flythe, J. E., Rashidi, A., Schenck, E. J., Goyal, N., Hedayati, S. S., Dy, R., Bansal, A., Athavale, A., Nguyen, H. B., Vijayan, A., Charytan, D. M., Schulze, C. E., Joo, M. J., Friedman, A. N., Zhang, J., Sosa, M. A., Judd, E., Velez, J. C. Q., Mallappallil, M., Redfern, R. E., Bansal, A. D., Neyra, J. A., Liu, K. D., Renaghan, A. D., Christov, M., Molnar, M. Z., Sharma, S., Kamal, O., Boateng, J. O., Short, S. A. P., Admon, A. J., Sise, M. E., Wang, W., Parikh, C. R. and Leaf, D. E. (2020a) AKI Treated with Renal Replacement Therapy in Critically Ill Patients with COVID-19. Journal of the American Society of Nephrology.
[Cited within: 1]
Gupta, S., Hayek, S. S., Wang, W., Chan, L., Mathews, K. S., Melamed, M. L., Brenner, S. K., Leonberg-Yoo, A., Schenck, E. J., Radbel, J., Reiser, J., Bansal, A., Srivastava, A., Zhou, Y., Sutherland, A., Green, A., Shehata, A. M., Goyal, N., Vijayan, A., Velez, J. C. Q., Shaefi, S., Parikh, C. R., Arunthamakun, J., Athavale, A. M., Friedman, A. N., Short, S. A. P., Kibbelaar, Z. A., Abu Omar, S., Admon, A. J., Donnelly, J. P., Gershengorn, H. B., Hernán, M. A., Semler, M. W. and Leaf, D. E. (2020b) Factors Associated With Death in Critically Ill Patients With Coronavirus Disease 2019 in the US. JAMA Internal Medicine180, 1-12.
[Cited within: 1]
Han, H., Ma, Q., Li, C., Liu, R., Zhao, L., Wang, W., Zhang, P., Liu, X., Gao, G., Liu, F., Jiang, Y., Cheng, X., Zhu, C. and Xia, Y. (2020) Profiling serum cytokines in COVID-19 patients reveals IL-6 and IL-10 are disease severity predictors. Emerging Microbes & Infections9, 1123-1130.
[Cited within: 1]
Heidary, F. and Gharebaghi, R. (2020) Ivermectin: a systematic review from antiviral effects to COVID-19 complementary regimen. The Journal of Antibiotics 73, 593-602.
[Cited within: 1]
Hong, K. S., Jang, J. G., Hur, J., Lee, J. H., Kim, H. N., Lee, W. and Ahn, J. H. (2020) Early Hydroxychloroquine Administration for Rapid Severe Acute Respiratory Syndrome Coronavirus 2 Eradication. Journal of Infection and Chemotherapy52, 396-402.
[Cited within: 1]
Horby, P., Lim, W. S., Emberson, J. R., Mafham, M., Bell, J. L., Linsell, L., Staplin, N., Brightling, C., Ustianowski, A., Elmahi, E., Prudon, B., Green, C., Felton, T., Chadwick, D., Rege, K., Fegan, C., Chappell, L. C., Faust, S. N., Jaki, T., Jeffery, K., Montgomery, A., Rowan, K., Juszczak, E., Baillie, J. K., Haynes, R. and Landray, M. J. (2020) Dexamethasone in Hospitalized Patients with Covid-19 – Preliminary Report. New England Journal of Medicine.
[Cited within: 1]
Hsiang, S., Allen, D., Annan-Phan, S., Bell, K., Bolliger, I., Chong, T., Druckenmiller, H., Huang, L. Y., Hultgren, A., Krasovich, E., Lau, P., Lee, J., Rolf, E., Tseng, J. and Wu, T. (2020) The effect of large-scale anti-contagion policies on the COVID-19 pandemic. Nature584, 262-267.
[Cited within: 1]
Huang, H. D., Jneid, H., Aziz, M., Ravi, V., Sharma, P. S., Larsen, T., Chatterjee, N., Saour, B., Aziz, Z., Nayak, H., Trohman, R. G. and Krishnan, K. (2020) Safety and Effectiveness of Hydroxychloroquine and Azithromycin Combination Therapy for Treatment of Hospitalized Patients with COVID-19: A Propensity-Matched Study. Cardiology and Therapy9, 523-534.
[Cited within: 1]
Huaxia. Senegal Roundup: Senegal to continue to treat COVID-19 patients with anti-malaria drugs: expert. XINHUANET. Available at: .
[Cited within: 1]
Isaac K. Ghana, Kenya approve the use of Chloroquine to treat COVID-19 patients. Taylor and Francis group. 2020. Available at: https://africafeeds.com/2020/04/01/ghana-kenya-approve-use-of-chloroquine-to-treat-covid-19-patients/ (Accessed: 10 November, 2020).
[Cited within: 1]
Ivashchenko, A. A., Dmitriev, K. A., Vostokova, N. V., Azarova, V. N., Blinow, A. A., Egorova, A. N., Gordeev, I. G., Ilin, A. P., Karapetian, R. N., Kravchenko, D. V., Lomakin, N. V., Merkulova, E. A., Papazova, N. A., Pavlikova, E. P., Savchuk, N. P., Simakina, E. N., Sitdekov, T. A., Smolyarchuk, E. A., Tikhomolova, E. G., Yakubova, E. V. and Ivachtchenko, A. V. (2020) AVIFAVIR for Treatment of Patients with Moderate COVID-19: Interim Results of a Phase II/III Multicenter Randomized Clinical Trial. Clinical Infectious Diseases.
[Cited within: 1]
Izzedine, H., Jhaveri, K. D. and Perazella, M. A. (2020) COVID-19 therapeutic options for patients with kidney disease. Kidney International97, 1297-1298.
[Cited within: 1]
Jefferson, T., Spencer, E. A., Brassey, J. and Heneghan, C. (2020) SARS-CoV-2 and the Role of Orofecal Transmission: Evidence Brief. In: Analysis of the Transmission Dynamics of COVID-19: An Open Evidence Review. The Centre for Evidence-Based Medicine. Available at: https://www.cebm.net/covid-19/sars-cov-2-orofecal-transmission/.
[Cited within: 1]
Katharine C. EXCLUSIVE: SA to roll out chloroquine to tackle coronavirus. South African Broadcasting Corporation. 2020. Available from https://www.businesslive.co.za/fm/features/2020-03-27-sa-to-roll-out-chloroquine-to-tackle-coronavirus/ (Accessed: 19 August, 2020).
[Cited within: 1]
Khan, M. S. I., Khan, M. S. I., Debnath, C. R., Nath, P. N., Mahtab, M. A., Nabeka, H., Matsuda, S. and Akbar, S. M. F. (2020) Ivermectin Treatment May Improve the Prognosis of Patients With COVID-19. Archivos de Bronconeumología56, 828-830.
[Cited within: 2]
Kolilekas, L., Loverdos, K., Giannakaki, S., Vlassi, L., Levounets, A., Zervas, E. and Gaga, M. (2020) Can steroids reverse the severe COVID-19 induced “cytokine storm”? Journal of Medical Virology92, 2866-2869.
[Cited within: 1]
Lagier, J. C., Million, M., Gautret, P., Colson, P., Cortaredona, S., Giraud-Gatineau, A., Honoré, S., Gaubert, J. Y., Fournier, P. E., Tissot-Dupont, H., Chabrière, E., Stein, A., Deharo, J. C., Fenollar, F., Rolain, J. M., Obadia, Y., Jacquier, A., La Scola, B., Brouqui, P., Drancourt, M., Parola, P. and Raoult, D. (2020) Outcomes of 3,737 COVID-19 patients treated with hydroxychloroquine/azithromycin and other regimens in Marseille, France: A retrospective analysis. Travel Medicine and Infectious Disease36, 101791.
[Cited within: 1]
Li, J., Zhang, C., Wu, Z., Wang, G. and Zhao, H. (2020) The Mechanism and Clinical Outcome of patients with Corona Virus Disease 2019 Whose Nucleic Acid Test has changed from negative to positive, and the therapeutic efficacy of Favipiravir: A structured summary of a study protocol for a randomised controlled trial. Trials21, 488.
[Cited within: 1]
Liu, F., Zhu, Y., Zhang, J., Li, Y. and Peng, Z. (2020) Intravenous high-dose vitamin C for the treatment of severe COVID-19: study protocol for a multicentre randomised controlled trial. BMJ Open10, e039519.
[Cited within: 1]
Malek, A. E., Granwehr, B. P. and Kontoyiannis, D. P. (2020) Doxycycline as a potential partner of COVID-19 therapies. IDCases21, e00864.
[Cited within: 1]
Masiá, M., Fernández-González, M., García, J. A., Padilla, S. and Gutiérrez, F. (2020) Lack of detrimental effect of corticosteroids on antibody responses to SARS-CoV-2 and viral clearance in patients hospitalized with COVID-19. Journal of Infection.
[Cited within: 1]
McCullough, P. A., Eidt, J., Rangaswami, J., Lerma, E., Tumlin, J., Wheelan, K., Katz, N., Lepor, N. E., Vijay, K., Soman, S., Singh, B., McCullough, S. P., McCullough, H. B., Palazzuoli, A., Ruocco, G. M. and Ronco, C. (2020a) Urgent need for individual mobile phone and institutional reporting of at home, hospitalized, and intensive care unit cases of SARS-CoV-2 (COVID-19) infection. Reviews in Cardiovascular Medicine 21, 1-7.
[Cited within: 1]
McCullough, P. A., Kelly, R. J., Ruocco, G., Lerma, E., Tumlin, J., Wheelan, K. R., Katz, N., Lepor, N. E., Vijay, K., Carter, H., Singh, B., McCullough, S. P., Bhambi, B. K., Palazzuoli, A., De Ferrari, G. M., Milligan, G. P., Safder, T., Tecson, K. M., Wang, D. D., McKinnon, J. E., O’Neill, W. W., Zervos, M. and Risch, H. A. (2020b) Pathophysiological Basis and Rationale for Early Outpatient Treatment of SARS-CoV-2 (COVID-19) Infection. The American Journal of Medicine134, 16-22.
[Cited within: 2]
McFadyen, J. D., Stevens, H. and Peter, K. (2020) The Emerging Threat of (Micro)Thrombosis in COVID-19 and Its Therapeutic Implications. Circulation Research127, 571-587.
[Cited within: 7]
Mega, E. R. (2020) Latin America’s embrace of an unproven COVID treatment is hindering drug trials. Nature586, 481-482.
[Cited within: 2]
Melikov, A. K., Ai, Z. T. and Markov, D. G. (2020) Intermittent occupancy combined with ventilation: An efficient strategy for the reduction of airborne transmission indoors. Science of the Total Environment 744, 140908.
[Cited within: 1]
Meltzer, D. O., Best, T. J., Zhang, H., Vokes, T., Arora, V. and Solway, J. (2020) Association of Vitamin D Status and Other Clinical Characteristics With COVID-19 Test Results. JAMA Network Open3, e2019722.
[Cited within: 1]
Mestre-Gómez, B., Lorente-Ramos, R. M., Rogado, J., Franco-Moreno, A., Obispo, B., Salazar-Chiriboga, D., Saez-Vaquero, T., Torres-Macho, J., Abad-Motos, A., Cortina-Camarero, C., Such-Diaz, A., Ruiz-Velasco, E., Churruca-Sarasqueta, J. and Muñoz-Rivas, N. (2020) Incidence of pulmonary embolism in non-critically ill COVID-19 patients. Predicting factors for a challenging diagnosis. Journal of Thrombosis and Thrombolysis , 1-7.
[Cited within: 1]
Mikami, T., Miyashita, H., Yamada, T., Harrington, M., Steinberg, D., Dunn, A. and Siau, E. (2020) Risk Factors for Mortality in Patients with COVID-19 in New York City. Journal of General Internal Medicine, 1-10.
[Cited within: 1]
Million, M., Lagier, J. C., Gautret, P., Colson, P., Fournier, P. E., Amrane, S., Hocquart, M., Mailhe, M., Esteves-Vieira, V., Doudier, B., Aubry, C., Correard, F., Giraud-Gatineau, A., Roussel, Y., Berenger, C., Cassir, N., Seng, P., Zandotti, C., Dhiver, C., Ravaux, I., Tomei, C., Eldin, C., Tissot-Dupont, H., Honoré, S., Stein, A., Jacquier, A., Deharo, J. C., Chabrière, E., Levasseur, A., Fenollar, F., Rolain, J. M., Obadia, Y., Brouqui, P., Drancourt, M., La Scola, B., Parola, P. and Raoult, D. (2020) Early treatment of COVID-19 patients with hydroxychloroquine and azithromycin: A retrospective analysis of 1061 cases in Marseille, France. Travel Medicine and Infectious Disease35, 101738.
[Cited within: 1]
Ministério da Saúde. Acesse o Plano Nacional de Operacionalização da Vacina contra a Covid-19. Available at: https://www.gov.br/saude/pt-br (Cited: 11 November, 2020).
[Cited within: 1]
Mohhamad, D. (2020) Mohhamad D Egypt uses chloroquine in treating COVID-19 patients: minister. Egypt Today staff. Available at:https://www.egypttoday.com/Article/1/83104/Egypt-uses-chloroquine-in-treating-COVID-19-patients-Minister (Accessed: 11 November, 2020).
[Cited within: 1]
Moores, L. K., Tritschler, T., Brosnahan, S., Carrier, M., Collen, J. F., Doerschug, K., Holley, A. B., Jimenez, D., Le Gal, G., Rali, P. and Wells, P. (2020) Prevention, Diagnosis, and Treatment of VTE in Patients With Coronavirus Disease 2019: CHEST Guideline and Expert Panel Report. Chest158, 1143-1163.
[Cited within: 1]
Mussa, K. (2020) Morocco continues the use of Chloroquine despite controversy. The North Africa Post. Available at: https://northafricapost.com/41247-morocco-continues-use-of-chloroquine-despite-controversy.html (Accessed: 11 November, 2020).
[Cited within: 1]
National Institutes of Health. (2020a) NIH begins clinical trial of hydroxychloroquine and azithromycin to treat COVID-19. National Institutes of Health, Available at: https://www.nih.gov/news-events/news-releases/nih-begins-clinical-trial-hydroxychloroquine-azithromycin-treat-covid-19 (Accessed: 03 July, 2020).
[Cited within: 1]
National Institutes of Health. (2020b) BULLETIN-NIH Clinical trial evaluating hydroxychloroquine and azithromycin for COVID-19 closes early. National Institutes of Health, Available at: https://www.niaid.nih.gov/news-events/bulletin-nih-clinical-trial-evaluating-hydroxychloroquine-and-azithromycin-covid-19 (Accessed: 03 July, 2020).
[Cited within: 1]
Nunez, A. C., Gutierrez, T., Cervantes, J. M. L. and Juarez, M. (2020). Therapeutic Efficacy of Ivermectin as an Adjuvant in the Treatment of Patients with COVID-19. International Journal of Innovative Science and Research Technology, 5(7), 211-215.
[Cited within: 1]
Nussbaumer-Streit, B., Mayr, V., Dobrescu, A. I., Chapman, A., Persad, E., Klerings, I., Wagner, G., Siebert, U., Christof, C., Zachariah, C. and Gartlehner, G. (2020) Quarantine alone or in combination with other public health measures to control COVID-19: a rapid review. Cochrane Database of Systematic Reviews4, Cd013574.
[Cited within: 1]
Pacheco, G. (2020) Estos son los medicamentos que se prueban para combatir el covid-19. Available at: https://www.milenio.com/ciencia-y-salud/medicamentos-para-coronavirus-a-prueba-contra-el-covid-19 (Acessed: 11 November, 2020).
[Cited within: 1]
Palazzuoli, A., Ruberto, F., De Ferrari, G. M., Forleo, G., Secco, G. G., Ruocco, G. M., D’Ascenzo, F., Mojoli, F., Monticone, S., Paggi, A., Vicenzi, M., Corcione, S., Palazzo, A. G., Landolina, M., Taravelli, E., Tavazzi, G., Blasi, F., Mancone, M., Birtolo, L. I., Alessandri, F., Infusino, F., Pugliese, F., Fedele, F., De Rosa, F. G., Emmett, M., Schussler, J. M., McCullough, P. A. and Tecson, K. M. (2020) Inpatient Mortality According to Level of Respiratory Support Received for Severe Acute Respiratory Syndrome Coronavirus 2 (Coronavirus Disease 2019) Infection: A Prospective Multicenter Study. Critical Care Explorations 2, e0220.
[Cited within: 1]
Pani, A., Lauriola, M., Romandini, A. and Scaglione, F. (2020) Macrolides and viral infections: focus on azithromycin in COVID-19 pathology. International Journal of Antimicrobial Agents56, 106053.
[Cited within: 1]
Pereira, M., Dantas Damascena, A., Galvão Azevedo, L. M., de Almeida Oliveira, T. and da Mota Santana, J. (2020) Vitamin D deficiency aggravates COVID-19: systematic review and meta-analysis. Critical Reviews in Food Science and Nutrition, 1-9.
[Cited within: 1]
Pilkington, V., Pepperrell, T. and Hill, A. (2020) A review of the safety of favipiravir – a potential treatment in the COVID-19 pandemic? Journal of Virus Eradication6, 45-51.
[Cited within: 1]
Pormohammad, A., Monych, N. K. and Turner, R. J. (2020) Zinc and SARS‑CoV‑2: A molecular modeling study of Zn interactions with RNA‑dependent RNA‑polymerase and 3C‑like proteinase enzymes. International Journal of Molecular Medicine.
[Cited within: 1]
Price-Haywood, E. G., Burton, J., Fort, D. and Seoane, L. (2020) Hospitalization and Mortality among Black Patients and White Patients with Covid-19. The New England Journal of Medicine 382, 2534-2543.
[Cited within: 1]
Prodromos, C. and Rumschlag, T. (2020) Hydroxychloroquine is effective, and consistently so when provided early, for COVID-19: a systematic review. New Microbes and New Infections38, 100776.
[Cited within: 1]
Prodromos, C. C., Rumschlag, T. and Perchyk, T. (2020) Hydroxychloroquine is protective to the heart, not harmful: a systematic review. New Microbes and New Infections37, 100747.
[Cited within: 1]
Rahman, M. A., Iqbal, S., Islam, M. A., Niaz, M. K., Hussain, T. and Siddiquee, T. (2020) Comparison of viral clearance between ivermectin with doxycycline and hydroxychloroquine with azithromycin in COVID-19 patients. Journal of Bangladesh College of Physicians and Surgeons 38, 5-9.
[Cited within: 1]
Rahman, M. T. and Idid, S. Z. (2020) Can Zn Be a Critical Element in COVID-19 Treatment? Biological Trace Element Research, 1-9.
[Cited within: 1]
Rajter, J. C., Sherman, M. S., Fatteh, N., Vogel, F., Sacks, J. and Rajter, J. J. (2020) Use of Ivermectin Is Associated With Lower Mortality in Hospitalized Patients With Coronavirus Disease 2019: The ICON Study. Chest.
[Cited within: 1]
Regeneron Pharmaceuticals, Inc. Fact sheet for health care providers emergency use authorization (eua) of casirivimab and imdevimab. In: Regeneron Pharmaceuticals, Inc. Available at: https://www.fda.gov/media/143892/download.
[Cited within: 1]
Rhodes, A., Evans, L. E., Alhazzani, W., Levy, M. M., Antonelli, M., Ferrer, R., Kumar, A., Sevransky, J. E., Sprung, C. L., Nunnally, M. E., Rochwerg, B., Rubenfeld, G. D., Angus, D. C., Annane, D., Beale, R. J., Bellinghan, G. J., Bernard, G. R., Chiche, J. D., Coopersmith, C., De Backer, D. P., French, C. J., Fujishima, S., Gerlach, H., Hidalgo, J. L., Hollenberg, S. M., Jones, A. E., Karnad, D. R., Kleinpell, R. M., Koh, Y., Lisboa, T. C., Machado, F. R., Marini, J. J., Marshall, J. C., Mazuski, J. E., McIntyre, L. A., McLean, A. S., Mehta, S., Moreno, R. P., Myburgh, J., Navalesi, P., Nishida, O., Osborn, T. M., Perner, A., Plunkett, C. M., Ranieri, M., Schorr, C. A., Seckel, M. A., Seymour, C. W., Shieh, L., Shukri, K. A., Simpson, S. Q., Singer, M., Thompson, B. T., Townsend, S. R., Van der Poll, T., Vincent, J. L., Wiersinga, W. J., Zimmerman, J. L. and Dellinger, R. P. (2017) Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock: 2016. Intensive Care Medicine43, 304-377.
[Cited within: 1]
Risch, H. A. (2020) Early Outpatient Treatment of Symptomatic, High-Risk COVID-19 Patients That Should Be Ramped Up Immediately as Key to the Pandemic Crisis. American Journal of Epidemiology 189, 1218-1226.
[Cited within: 1]
Rosenberg, E. S., Dufort, E. M., Udo, T., Wilberschied, L. A., Kumar, J., Tesoriero, J., Weinberg, P., Kirkwood, J., Muse, A., DeHovitz, J., Blog, D. S., Hutton, B., Holtgrave, D. R. and Zucker, H. A. (2020) Association of Treatment With Hydroxychloroquine or Azithromycin With In-Hospital Mortality in Patients With COVID-19 in New York State. Journal of the American Medical Association323, 2493-2502.
[Cited within: 1]
Ruocco, G., McCullough, P. A., Tecson, K. M., Mancone, M., De Ferrari, G. M., D’Ascenzo, F., De Rosa, F. G., Paggi, A., Forleo, G., Secco, G. G., Pistis, G., Monticone, S., Vicenzi, M., Rota, I., Blasi, F., Pugliese, F., Fedele, F. and Palazzuoli, A. (2020) Mortality Risk Assessment Using CHA(2)DS(2)-VASc Scores in Patients Hospitalized With Coronavirus Disease 2019 Infection. The American Journal of Cardiology 137, 111-117.
[Cited within: 1]
Santos-Sánchez, N. F. and Salas-Coronado, R. (2020) Origin, structural characteristics, prevention measures, diagnosis and potential drugs to prevent and COVID-19. Medwave20, e8037.
Schrezenmeier, E. and Dörner, T. (2020) Mechanisms of action of hydroxychloroquine and chloroquine: implications for rheumatology. Nature Reviews Rheumatology16, 155-166.
[Cited within: 1]
Schmith, V. D., Zhou, J. J. and Lohmer, L. R. L. (2020) The approved dose of ivermectin alone is not the ideal dose for the treatment of COVID-19. Clinical Pharmacology & Therapeutics108, 762-765.
[Cited within: 1]
Sharma, P., Reddy, P. K. and Kumar, B. (2020) Trace Element Zinc, a Nature’s Gift to Fight Unprecedented Global Pandemic COVID-19. Biol Trace Elem Res, 1-9.
[Cited within: 1]
Sheng, W. H. (2020) Interim Guidelines for Clinical Management of SARS-CoV-2 Infection (5th edition). Available at: https://fightcovid.edu.tw/cdc-guidelines/clinical-management (Acessede: 11 November, 2020).
[Cited within: 1]
Shojaei, A. and Salari, P. (2020) COVID-19 and off label use of drugs: an ethical viewpoint. Daru28, 789-793.
[Cited within: 1]
Singh, A. K., Majumdar, S., Singh, R. and Misra, A. (2020) Role of corticosteroid in the management of COVID-19: A systemic review and a Clinician’s perspective. Diabetes and Metabolic Syndrome14, 971-978.
[Cited within: 1]
Singhania, N., Bansal, S., Nimmatoori, D. P., Ejaz, A. A., McCullough, P. A. and Singhania, G. (2020) Current Overview on Hypercoagulability in COVID-19. American Journal of Cardiovascular Drugs 20, 393-403.
[Cited within: 1]
Sodhi, M. and Etminan, M. (2020) Therapeutic Potential for Tetracyclines in the Treatment of COVID-19. Pharmacotherapy40, 487-488.
[Cited within: 1]
Sterne, J. A. C., Murthy, S., Diaz, J. V., Slutsky, A. S., Villar, J., Angus, D. C., Annane, D., Azevedo, L. C. P., Berwanger, O., Cavalcanti, A. B., Dequin, P. F., Du, B., Emberson, J., Fisher, D., Giraudeau, B., Gordon, A. C., Granholm, A., Green, C., Haynes, R., Heming, N., Higgins, J. P. T., Horby, P., Jüni, P., Landray, M. J., Le Gouge, A., Leclerc, M., Lim, W. S., Machado, F. R., McArthur, C., Meziani, F., Møller, M. H., Perner, A., Petersen, M. W., Savovic, J., Tomazini, B., Veiga, V. C., Webb, S. and Marshall, J. C. (2020) Association Between Administration of Systemic Corticosteroids and Mortality Among Critically Ill Patients With COVID-19: A Meta-analysis. Journal of the American Medical Association 324, 1330-1341.
[Cited within: 1]
Szente Fonseca, S. N., de Queiroz Sousa, A., Wolkoff, A. G., Moreira, M. S., Pinto, B. C., Valente Takeda, C. F., Rebouças, E., Vasconcellos Abdon, A. P., Nascimento, A. L. A. and Risch, H. A. (2020) Risk of hospitalization for Covid-19 outpatients treated with various drug regimens in Brazil: Comparative analysis. Travel Medicine and Infectious Disease38, 101906.
[Cited within: 1]
Tang, N., Bai, H., Chen, X., Gong, J., Li, D. and Sun, Z. (2020) Anticoagulant treatment is associated with decreased mortality in severe coronavirus disease 2019 patients with coagulopathy. Journal of Thrombosis and Haemostasis18, 1094-1099.
[Cited within: 1]
te Velthuis, A. J., van den Worm, S. H., Sims, A. C., Baric, R. S., Snijder, E. J. and van Hemert, M. J. (2010) Zn(2+) inhibits coronavirus and arterivirus RNA polymerase activity in vitro and zinc ionophores block the replication of these viruses in cell culture. PLoS Pathogens6, e1001176.
[Cited within: 1]
The Independent. (2020) Museveni P Uganda records good results in treating COVID with hydroxychloroquine, chloroquine. Available at https://www.independent.co.ug/uganda-records-good-results-treating-COVID-with-hydroxychloroquine-chloroquine/ (Accessed: 19 August, 2020).
[Cited within: 1]
Trial Site News. Ivermectin usage accelerates while the need for data is real: how about an ivermectin registry? Trial Site News. Available at: https://www.trialsitenews.com/ivermectin-usage-accelerates-while-the-need-for-data-is-real-how-about-an-ivermectin-registry/ (Cited: 11 November, 2020).
[Cited within: 2]
Turshudzhyan, A. (2020) Anticoagulation Options for Coronavirus Disease 2019 (COVID-19)-Induced Coagulopathy. Cureus12, e8150.
[Cited within: 1]
Vaduganathan, M., van Meijgaard, J., Mehra, M. R., Joseph, J., O’Donnell, C. J. and Warraich, H. J. (2020) Prescription Fill Patterns for Commonly Used Drugs During the COVID-19 Pandemic in the United States. Journal of the American Medical Association323, 2524-2526.
[Cited within: 1]
Vahidy, F. S., Drews, A. L., Masud, F. N., Schwartz, R. L., Askary, B. B., Boom, M. L. and Phillips, R. A. (2020) Characteristics and Outcomes of COVID-19 Patients During Initial Peak and Resurgence in the Houston Metropolitan Area. Journal of the American Medical Association324, 998-1000.
[Cited within: 1]
Vora, A., Arora, V. K., Behera, D. and Tripathy, S. K. (2020) White paper on Ivermectin as a potential therapy for COVID-19. Indian J Tuberc67, 448-451.
[Cited within: 1]
Westafer, L. M., Elia, T., Medarametla, V. and Lagu, T. (2020) A Transdisciplinary COVID-19 Early Respiratory Intervention Protocol: An Implementation Story. Journal of Hospital Medicine 15, 372-374.
[Cited within: 1]
World Health Organisation (WHO). (2020) COVID-19 Studies from the World Health Organization Database. Available at: https://clinicaltrials.gov/ct2/who_table.
[Cited within: 2]
World Health Organization. (2020) R&D blueprint and COVID-19. Available at: https://www.who.int/blueprint/priority-diseases/key-action/novel-coronavirus/en/ (Accessed: 25 March, 2020).
Xiao, J., Shiu, E. Y. C., Gao, H., Wong, J. Y., Fong, M. W., Ryu, S. and Cowling, B. J. (2020) Nonpharmaceutical Measures for Pandemic Influenza in Nonhealthcare Settings-Personal Protective and Environmental Measures. Emerging Infectious Diseases26, 967-975.
[Cited within: 1]
Xu, X. K., Liu, X. F., Wu, Y., Ali, S. T., Du, Z., Bosetti, P., Lau, E. H. Y., Cowling, B. J. and Wang, L. (2020) Reconstruction of Transmission Pairs for novel Coronavirus Disease 2019 (COVID-19) in mainland China: Estimation of Super-spreading Events, Serial Interval, and Hazard of Infection. Clinical Infectious Diseases.
[Cited within: 1]
Yamakawa, M., Kuno, T., Mikami, T., Takagi, H. and Gronseth, G. (2020) Clinical Characteristics of Stroke with COVID-19: A Systematic Review and Meta-Analysis. Journal of Stroke & Cerebrovascular Diseases29, 105288.
[Cited within: 1]
Yang, B. Y., Barnard, L. M., Emert, J. M., Drucker, C., Schwarcz, L., Counts, C. R., Murphy, D. L., Guan, S., Kume, K., Rodriquez, K., Jacinto, T., May, S., Sayre, M. R., Seattle Fire Department, Seattle, Washington and Rea, T. (2020) Clinical characteristics of patients with coronavirus disease 2019 (COVID-19) receiving emergency medical services in King County, Washington. Jama Network Open 3, e2014549.
[Cited within: 1]
Zhang, J., McCullough, P. A. and Tecson, K. M. (2020a) Vitamin D deficiency in association with endothelial dysfunction: Implications for patients with COVID-19. Reviews in Cardiovascular Medicine 21, 339-344.
[Cited within: 1]
Zhang, J., Tecson, K. M. and McCullough, P. A. (2020b) Endothelial dysfunction contributes to COVID-19-associated vascular inflammation and coagulopathy. Reviews in Cardiovascular Medicine21, 315-319.
[Cited within: 1]