コンテンツ
- An updated and comprehensive review of the antiviral potential of essential oils and their chemical constituents with special focus on their mechanism of action against various influenza and coronaviruses
https://www.sciencedirect.com/science/article/pii/S0882401020309864
ハイライト
- 多数の発表された研究では、エッセンシャルオイルの抗ウイルス効果が顕著に報告されている。
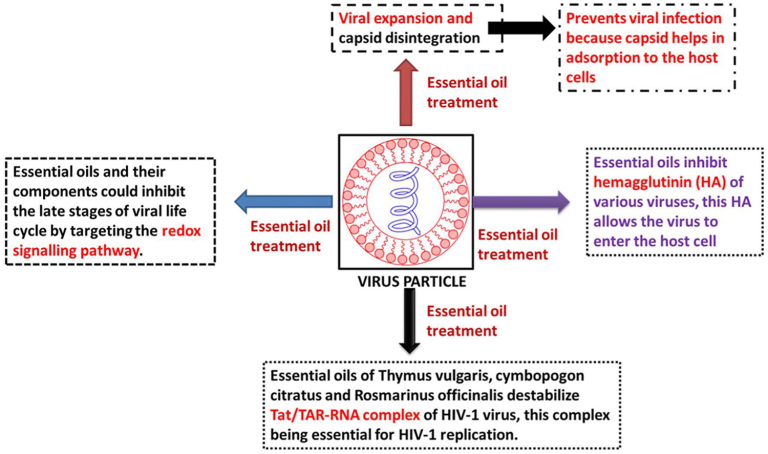
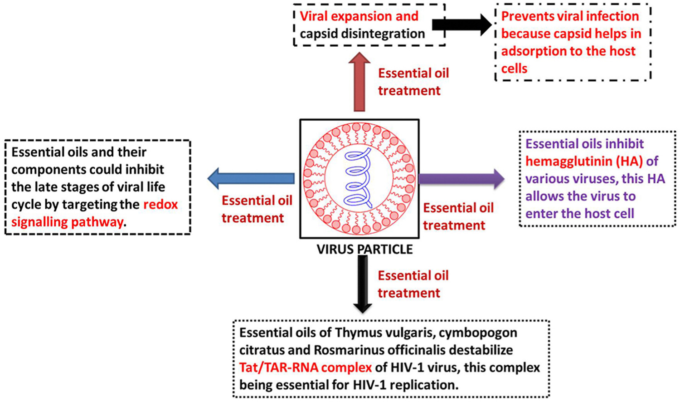
- エッセンシャルオイルは、カプシドの崩壊とウイルスの膨張を引き起こし効果をなくす。
- ある種のウイルスのヘマグルチニン(膜タンパク質)を阻害することが精油によって報告されている。
- エッセンシャルオイルは、ウイルスの複製に不可欠なHIV-1ウイルスのTat/TAR-RNA複合体を不安定にする。
- エッセンシャルオイルは親油性であるため、ウイルスの膜に容易に浸透し、膜の破壊につながる。
概要
エッセンシャルオイルとその化学成分は、細菌、真菌、ウイルス性病原体の範囲に対する抗菌効果が十分に文書化されていると報告されている。定義により、エッセンシャルオイルは、植物の二次代謝の一部として、植物の様々な部分で自然に合成されている揮発性有機化合物の複雑な混合物である。エッセンシャルオイルの化学組成は、エッセンシャルオイルは、病原体の広い範囲に対して有効でなければならないことを推測してフェノリン、テルペノイド、アルデヒド、ケトン、エーテル、エポキシドおよび他の多くの化合物の範囲の存在によって支配されている。このレビュー記事では、主にインフルエンザやコロナウイルスに対するエッセンシャルオイルとその化学成分の抗ウイルス性に焦点を当てている。精油は、インフルエンザや他の呼吸器ウイルス感染症を含むいくつかの病原性ウイルスに対してスクリーニングされている。シナモン、ベルガモット、レモングラス、タイム、ラベンダーの精油は、A型インフルエンザウイルスに対して強力な抗ウイルス効果を発揮することが報告されている。シトラス・レシュニ葉の精油は、H5N1ウイルスに対して有効であることが報告されている。また、11.1μg/mLの濃度のLippia種の精油は、ベロ細胞において黄熱病ウイルスの100%阻害を誘導することが示されている。精油およびオレオレジンは、試験管内試験および生体内試験実験を通して、コロナウイルス感染性気管支炎ウイルスに対する抗ウイルス効果を誘導することが示されている。ある研究では、Vero E6細胞に対するSARS-CoV誘導性細胞病原性効果を測定する細胞ベースのアッセイを用いて、221種類のフィトケミカル化合物とエッセンシャルオイルが重症急性呼吸器症候群関連コロナウイルス(SARS-CoV)に対して有効であることが報告されている。精油の抗ウイルス効果の主なメカニズムは、カプシドの崩壊とウイルスの膨張を引き起こし、ウイルスがカプシドを介して吸着して宿主細胞に感染するのを防ぐことが明らかになっている。また、エッセンシャルオイルは、特定のウイルスのヘマグルチニン(様々なウイルスの重要な膜タンパク質)を阻害し、この膜タンパク質がウイルスの宿主細胞への侵入を可能にする。多くの精油とその成分は、酸化還元シグナル伝達経路を標的とすることで、ウイルスのライフサイクルの後期を阻害する可能性がある。Thymus vulgaris、cymbopogon citratus、Rosmarinus officinalisのエッセンシャルオイルは、HIV-1ウイルスのTat/TAR-RNA複合体を不安定化することがわかっており、この複合体はHIV-1の複製に不可欠である。脂溶性であるため、エッセンシャルオイルはウイルス膜に容易に浸透し、膜の崩壊につながる。今回の包括的なレビューでは,植物由来の化学物質を様々なウイルスに対する阻害剤として発見することが容易になると考えられる.
キーワード
精油抗ウイルステルペン重症急性呼吸器症候群インフルエンザ
1. 序論
植物や植物から抽出された天然物を化粧品や宗教、薬用として消費することは、人類の文明の台頭にまで遡る存在である[1]。植物とその由来の天然物は、医薬品開発、デザイン、研究の分野でリードとして役立つ膨大な化学組成を示している[2]。薬用植物は生体栄養素やフィトケミカルを高濃度に含有しており,顕著な生理活性を示している。フィトケミカルは、冠状動脈性心疾患、糖尿病、癌などの慢性疾患を含む膨大な数の人間の病気に対して作用する可能性を秘めていることが確認されている[3]。これらのフィトケミカルの役割は植物の中で高度に研究されており、これらの化学物質が自己防衛のために生成されることが確立されている。また、フィトケミカルは植物にダメージや病気からの保護カバーを与え、植物の風味や香り、色にも貢献している[4]。芳香植物の薬効は、一般的にエッセンシャルオイルの存在によって保証されている。これらの精油は、植物の二次代謝物の膨大な数で構成されている。エッセンシャルオイルの使用は、主に高い香りの存在のため、香水、化粧品、食品香料にリンクされている。これに加えて、継続的な研究は、いくつかの人間の病気の管理、保護、治癒のために精油とその構成化学種の計り知れない可能性を実証している[5,6]。過去30~40年の間に、アロマテラピーや植物医学の分野で精油の用途が強く注目されるようになった。そのため、エッセンシャルオイルの基礎研究、特に抗酸化作用、抗菌作用、抗腫瘍作用については、研究者の間で広く研究が進められていた。エッセンシャルオイルは、一般的に数十から数百種類の分子を持つ多様な化学混合物で構成されており、その多くはベンゼン誘導体とテルペンの混合物である。これらのテルペンとベンゼン誘導体は、エッセンシャルオイル[7,8]の豊富な生理活性に貢献している。エッセンシャルオイルとテルペンは、植物由来であり、両方とも芳香族であることの負担の類似性として、一見すると似ているように見える。多くの人々は、彼らは両方が似たような目的を果たすと信じてた。エッセンシャルオイルとテルペンの間の類似性は、それらが同じか異なるかの混乱を生み出しているが、これらの2つは異なる[9]。
芳香植物や薬用植物の需要は、消費者の増加と、その薬用、料理用、その他の人為的用途への関心の高まりにより、継続的に増加している。世界中の消費者は、食品、栄養、健康問題に関する情報をより多く得るようになっており、また、芳香植物、薬用植物、植物代謝物を使用することによる健康上の利点を認識するようになってきている[10]。エッセンシャルオイルは、植物によって生成される二次代謝物の一つである。エッセンシャルオイルの使用は、クマ豊富な化学組成物に加えて、主に香水や化粧品のドメインに限定されたままになっている。エッセンシャルオイルは、その生物学的特性と豊富な化学に理解を深める価値がある。より多くの注意は、人間の健康、環境、農業[11]でのアプリケーションのためのエッセンシャルオイルの個々の成分または異なる抽出物を探索するために必要とされている。エッセンシャルオイルは、同一の副次的効果を誘導することなく、化学工業の合成化合物への操作的な代替品または補完品として探索することができる。
2. エッセンシャルオイル、化学組成と異なるヘルスケア製品の用途
2.1. 定義
実用的な定義の豊富な用語揮発性またはエッセンシャルオイルのために存在する。エッセンシャルオイルは、根、果物、木材、ハーブ、樹皮、小枝、葉、種子、芽、根茎、皮、花、花と明確な植物種に属する植物全体を含む様々な植物材料によって生成される高濃度の油性および疎水性の揮発性液体である[[12], [13], [14]. 強い臭気は、精油の顕著な特徴の一つである。さらに、それらは、類似の気候、エダフ条件と共通の収穫時期の下で成長している単一の植物種から抽出された場合、ほぼ同様の化学組成と生物学的活性を表示する[15]。これらのオイルに含まれる植物エッセンスの存在は、それらを “エッセンシャルオイル “という名前を獲得する。ほとんどのエッセンシャルオイルは植物由来であるが、それらのいくつかはあまりにも微生物や動物によって生成されている[16]。菌類、海藻類、肝臓藻類、コケ類もエッセンシャルオイルを生成することが認識されている[17]。彼らは、弱極性および非極性の有機、水(例外を除く)溶剤よりも密度が低く、まれに着色されていないと生ぬるい有機物に可溶である[18]。エッセンシャルオイルは、新鮮なときの外観のほとんどは無色であるが、いくつかは緑色(ベルガモット、シトラスベルガミア)オレンジ色(スイートオレンジ、シトラスシネンシス)青色(カモミール、Matricaria chamomomilla)と淡黄色(イエローマンダリン)になることがある[19]。これらの油は、熱光や空気にさらされることにより、経年変化に伴う酸化を受けやすく、精油の色が濃くなる原因となる[20]。したがって、このような酸化を避けるために、エッセンシャルオイルは、冷暗所で、最も適切に琥珀色のガラス容器で保管する必要がある。植物のテルペンとエッセンシャルオイルは、エッセンシャルオイルがテルペンと他の天然クラスの化合物の両方を収容するように、化学成分のベースで区別されている。
2.2. エッセンシャルオイルの分布と用途
植物の器官、化学型、調製方法、植物の収穫の段階、年齢、土壌の種類や質感、気候などのような異なる植物材料に含まれるエッセンシャルオイルの品質と量を決定するためにいくつかの要因が責任を負います。約2000植物から約3000のエッセンシャルオイル[20,22]から、異なる分野で1つと他の方法で使用される多数の植物由来のエッセンシャルオイルがある。多くの場合、すべての植物がエッセンシャルオイルを生成する傾向があるが、微量で健康的な量のエッセンシャルオイルを生成する植物はほとんどない。商業的に重要な精油を生産する植物は、精油植物として知られている[23]。精油は一般的に約17,500種が知られている高等植物に存在するが、それらはジンギョソウ科、イネ科、キク科、キク科、ラミア科、リュウゼツラン科、コンポジタ科、ラクサ科、コケモモ科、アカネ科、バラ科、キョウチクトウ科、ミリスリ科、ミレスタ科などのいくつかの特定の植物科に健康的な量で存在している。[[24], [25], [26], [27]]. ほとんどの場合、これらの精油の生理活性は不明のままである。精油は、薬理活性の顕著な可能性と天然の防腐剤として作用する傾向があるため、現在、研究やいくつかの産業において高い重要性の対象となっている[28]。精油の生態学的な役割は広範囲に研究され、確立されている。よく知られているのは、退治や捕食者からの保護のための植物と動物の相互作用、発芽阻害剤やアレロパシー剤のような植物の相互作用と受粉を支援する昆虫の魅力[29]である。微生物の分解は顧客の健康を脅かす可能性があるため、産業界は常に化粧品の抗菌性の安全性に注目している。エッセンシャルオイルは強力な抗菌性を持っているため、微生物保護のための化粧品の天然成分として機能することができる。エッセンシャルオイルとエッセンシャルオイルを冠した薬剤は、殺虫剤としての農業、飲料、食品、スパイスや防腐剤のための風味としての食品技術、香水としての香水、ヒーラーとしての薬局、アロマテラピー[30]で顕著な重要性を持っている。精油の重要性と生命力は、植物のケモタキソノミーの分野でも高く評価されている[31,32]。
2.3. 精油の組成
一般的にEOは、低分子量の非極性および半極性の親油性成分の非常に複雑な混合物(60-300)であり、2つまたは3つが主要なものであると考えられている:テルペノイド、側鎖を含まない直鎖化合物、芳香族およびフェノール成分、および硫黄誘導体[33,34]。エッセンシャルオイルの味と香りの違いは、非常に植物の種類、収穫の季節、地理的な場所、乾燥の方法と抽出に関与する技術に依存している[[35], [36], [37]]。精油に含まれる主な揮発性成分は、テルペノイドとポリプロパノイドに分類される[[38], [39], [40]]。ここではテルペノイドのみを考察する。
2.4. テルペン類とテルペノイド
テルペンは、その構造にイソプレン(2-メチルブタ-1,3-ジエン)単位の炭素骨格を持つ植物の二次代謝物である[41]。植物細胞の細胞質に存在するメバロン酸経路はテルペンの生成につながる。テルペノイドは、テルペンの転位や酸化などの生化学的修飾によって生成される。これらの生化学的修飾は、酸、アルコール、ケトン、アルデヒド、エステル、エーテルなどのテルペンの酸素化誘導体のテルペノイドを形成する。テルペノイドは、一次代謝および二次代謝の約40,000種類の化合物で構成されるフィトケミカルの中で最大のクラスである[41]。毎年、このクラスの天然物に新しいメンバーが追加されている。テルペノイドは一般的に、真のテルペン、サポニン、ステロイド、心臓配糖体を含む4つの異なるグループに分類される。化合物のこれらの4つのグループは、主に植物由来のエッセンシャルオイルに、ほぼすべての生活システムに存在している。したがって、これらは、植物由来の天然物の最大かつ構造的に多様なグループと考えられている[42]。ヘミテルペノイド、モノテルペノイドおよびセスキテルペノイドは、精油の唯一の十分な揮発性成分である。広く認められているように、EOの組成物は、主にモノ、セスキ、さらにはジテルペン炭化水素およびそれらのそれぞれの酸素化誘導体によって表される[[43], [44], [45]]。エッセンシャルオイルは、それらを非常に揮発性を作る構造的に低分子量の成分を負担している。エッセンシャルオイルの主な成分はテルペンである[46]。これらのテルペンは、イソプレン単位(5つの炭素基単位)の系統的な集合体によって形成される。これらのユニットの熱と尾部の縮合により、膨大な数のテルペンが生成される。テルペンの構造的および化学的多様性は、これらのイソプレン単位の繰り返し、環化、再配列の結果である。エッセンシャルオイルの主な成分は、C10骨格を持つモノテルペン、C15骨格を持つセスキテルペン、C20骨格を持つジテルペン、C30骨格を持つトリテルペンが含まれている。高位のテルペンおよびその酸素化誘導体は、精油中に非常に低濃度で存在する[47]。
2.5. ヘミテルペン類
ヘミテルペンは、エッセンシャルオイルのテルペン含有量のマイナーな構成要素である。これらは一般にエステル基、アルデヒド基、アルコール基を有する2-メチルブタン骨格である[48]。精油に含まれるヘミテルペンの数は非常に少ない(約100以下)[49]。最近では、Prinsepia utilisの葉に塩素化ヘミテルペンが認められている(図1)[50]。
図1. 精油に含まれるヘミテルペンの構成成分の一部

2.6. モノテルペン類
2つのイソプレンユニットのヘッドからテールへの結合は、規則的なモノテルペン(C10)を生じさせる。モノテルペンは、いくつかの精油に含まれる高濃度(90%以上)で存在する低分子量分子である。したがって、これらの分子は、植物による特定の香りの形成に貢献している[51,52]。モノテルペン類は、その構造部位に二重結合を持ち、ほぼすべての植物精油に含まれている。これらのモノテルペンは一般的に、植物と植物との相互作用や、果実散布、種子散布、受粉、アレロパシー剤のような植物と動物との相互作用に関与している。モノテルペンのための30以上の基本的な骨格があり、それ故に3つのサブグループに細分化することができる:非環式、単環式と二環式。図2に真性テルペンと酸素化テルペンの異なるモノテルペンを示した。
図2. 精油のモノテルペン成分とモノテルペノイド成分の一部。

2.7. セスキテルペン類
セスキテルペンは、エッセンシャルオイルに含まれる主要な構成テルペンのもう一つの主要なクラスであり、モノテルペンよりも揮発性が低い。これらは、3つのイソプレンユニットの組み合わせによって形成され、構造の多様性においてより汎用性の高いものとなっている。セスキテルペンは、直鎖状、単環状、二環状、三環状など、これらの3つのイソプレン単位の組み合わせによって生成された様々な形態で存在している。これらは植物や精油に含まれるテルペノイドの中で最も多様なグループである(図3)。
図3 精油に含まれるセスキテルペンとセスキテルペノイドの構成成分 精油に含まれるセスキテルペンとセスキテルペノイドの構成成分の一部。

2.8. ジテルペン類
ジテルペン類は、化学的にも構造的にもより複雑な物質で、主に植物の樹脂と関連しており、精油抽出時に副産物として発見されることはほとんどない。これらのジテルペンは、C20骨格の存在により高分子量であり、モノおよびセスキテルペンに比べて揮発性が低く、また含有量も少ない。分子量が大きいため、これらのジテルペン類は蒸留工程を経て精油中に単離することが困難である。精油中にジテルペンが存在する場合、通常は極微量である。しかし、伝統的な蒸留プロセスは、エッセンシャルオイルからこれらのジテルペンを同定し、分離するのに役立つ[53]。
一般的に、分子量が300umaを超える分子は、抽出設定が不適切であったり、不純物が混入していることの象徴とみなされる。一般的に精油に含まれるジテルペンとしては、カンフォレン、カフェストール、カフエオール、カンブレン、タキシデメなどが挙げられる(図4)。
図4. 精油のジテルペン成分とジテルペノイド成分の一部。

2.9. 精油の生物活性
精油の薬理学的応用は、代替医療の可能性を探るという観点から広く評価されてきた。過去数十年以来、エッセンシャルオイルは、生物学的システムの配列におけるそれらの可能性のある役割のために広く検索されている[54]。精油は、幅広い生理活性を持つという驚くべき能力を持っている。
2.10. 抗酸化活性
エッセンシャルオイルの抗酸化活性は、それらの最も集中的に調査された特性の一つである。多くの生物学的物質の酸化は、細胞の損傷を引き起こし、いくつかの名前を挙げると、代謝性疾患を引き起こす可能性がある。アルツハイマー病、パーキンソン病、炎症、関節炎、糖尿病、癌[[55], [56], [57], [58], [59]]。精油には、酸化的ダメージを抑制するための研究が可能な抗酸化物質が豊富に含まれていることはよく知られている[60]。抗酸化物質の種は、基質の酸化を遅らせたり、それを抑制する傾向があるものである[61]。精油に含まれる揮発性成分は、酸化ストレスからの保護カバーを作り出すだけでなく、細胞内の酸化還元電位を標的にして、細胞内の生体分子の損傷を誘導することで、プロオキシダントとしても作用する。プロオキシダントとして、エッセンシャルオイルはDNAや細胞内タンパク質にダメージを与える可能性がある。精油の抗酸化力以外にも、精油の抗酸化研究では、プロオキシダント活性も考慮しなければならない。
精油のフェノール含有量は、その抗酸化力が高く評価されている。また、最近の研究では、精油の揮発性成分が、単独または混合物としても精油の抗酸化性に寄与することが報告されている。Melissa officinalis L.(レモンバーム)から抽出された精油は、BHTよりも高い抗酸化力を持つことが報告されている。この精油のGC-MS分析では、主成分はゲラニール、ネラール、シトロネラールで、収率はそれぞれ23.4%、16.5%、13.7%であることが示されている[62]。
2.11. 抗がん作用
がんは、毎年1,810万人の患者が診断されており、世界的な健康の脅威となっている。この疾患は致死性が高く 2018年の1年間だけでも960万人の命の死亡率を占めていた。これらの死亡者のうち、死亡者の70%は低所得国および中間所得国に属していた[63]。現在利用可能ながん治療のための化学療法薬には、タキソール、カンプトテシン、ビンクリスチン、ビンブラスチンがある[64]。精油の抗がん活性を報告している研究はいくつかある。概算では、精油の抗がん活性については500件の研究論文が発表されている[[65], [66], [67], [68]]。しかし、アロマテラピーががんを予防または治療する可能性があると報告した明確な研究はない。より多くの研究では、ペトリ皿を使用して試験管内試験で異なる癌細胞株に対するエッセンシャルオイルの抗癌活性が報告されている。また、エッセンシャルオイルには強い抗炎症作用があることが報告されており、酸化の起点となる活性酸素と炎症との間には直接的な関係があることから、エッセンシャルオイルにも抗がん作用があるのではないかと考えられている。過去10年ほど前から、精油の抗がん作用に対する研究者の関心が高まっており、20以上のファミリーに属する100種類以上の精油を20種類の異なるタイプのがんに対して調査することにつながっている[69]。Bourgou と共同研究者らは、Nigella sativa L. (ブラッククミン)の種子由来の精油が、IC50 値がそれぞれ 43.0 と 46.0 μg/mL で、A-549 と DLD-1 癌細胞株の増殖を抑制することを示している[70]。Wangらは、Rosamarinus officinalis L.の精油と、1,8-セネオール、α-ピネン、β-ピネンを含む成分の毒性学的可能性を報告している。SK-OV-3,HO-8910およびBel-7402を含む3つの異なるヒト癌細胞株を用いて調査を行ったところ、精油のIC50値はそれぞれ0.025%).076%および0.13%(v/v)であった[71]。
2.12. 抗菌活性
精油は抗菌剤としての強力な可能性を持っており、この性質はいくつかの研究で確立され、報告されている。エッセンシャルオイルの抗菌作用は、植物化学的な成分だけでなく、異なる成分間の相互作用によって相乗効果や拮抗効果がもたらされる。精油の抗菌作用を決定する要因には、化学的含有量、濃度、主要な活性成分間の相互作用、微生物の脆弱性などがある[72,73]。それらの不活性成分は、反応速度、吸収、活性成分の生物学的効果に影響を与える可能性がある。したがって、精油のマイナー成分とメジャー成分の両方の存在は、相乗効果または拮抗効果を提起することによって活性の修飾につながる可能性がある[74,75]。タイム、オレガノ、シナモンに由来する精油は、Pseudomonas fluorescens、Listeria monocytogenes、Bacillus thermosphacta、Escherichia coliに対して強い抗菌活性を示すことが報告されている[76]。いくつかの精油の抗菌活性の高い順に、以下のように報告されている。セージ(Salvia officinalis)<マスタード(Sinapis alba)<ローズマリー(Salvia rosmarinus)<ミント(Mentha)<タイム(Thymus vulgaris)<シナモン(Cinnamomum cassia)<コリアンダー(Coriandrum sativum)<クローブ(Syzygium aromaticum)<オレガノ(Origanum vulgare)[77]。抗生物質に対する感染性細菌の耐性は、世界的に見て、人の健康に関する最も深刻な問題である。大腸菌、緑膿菌、Acinetobacter baumannii、Clostridium difficile、Enterococcus faecium、Staphylococcus aureus、Enterobacter species、Klebsiella [78]などの巨大な臨床負担をもたらす細菌が含まれている。グラム陽性菌の細胞膜の外側にペプチドグリカン層が存在するため、エッセンシャルオイルは、それらに対して最大の活性を示している。グラム陰性菌は内膜の外側にリン脂質の二層膜を持ち、内膜とリポ多糖類でつながっている[79]。異なる病原微生物を用いて、細菌や真菌に対する精油の生理活性を報告した研究がいくつかある[80], [81], [82], [83]。先行研究の中には、大腸菌や緑膿菌のグラム陰性菌株が、ピパーギネンスの果実やカルデンセの根から抽出したエッセンシャルオイルによって強く標的とされることを報告しているものもある[84,85]。Thanisseryらが実施した試験管内試験研究では、カンピロバクターとSalmonella entericaの阻害が、クローブ、ローズマリー、および混合タイムオレンジオイルの精油によって示された[86]。タイム油は他の2つの精油と比較して、サルモネラ菌に対する最大の阻害効果を示し、阻害ゾーン(ZI)は18.5 mmであった。オレガノ、タイム、ローズマリー、クローブ、ピメント、シナモンの精油は、緑膿菌、黄色ブドウ球菌、サルモネラチフスに対する抗菌活性が認められている[87]。クローブ油は、これらの試験した精油の中で最も活性が高かった。これらの精油の抗菌活性は、p-cymene、オイゲノール、桂皮アルデヒド、チモール、カルバクロールを含む豊富な化学成分によるものであった。薬用・芳香植物由来の精油にはオイゲノール、カルバクロール、チモールが豊富に含まれており、これらはすべて、ビブリオ・バルニフィカス、リステリア・モノサイトゲネス、サルモネラ・チフィムリウム、大腸菌などの食中毒性病原体を阻害する可能性を示している[88]。Sutiliらによる試験管内試験分析では、Hesperozygis ringens、Ocimum gratissimum、Ocimum americanum由来の精油がAeromonas hydrophilaに対して強い阻害効果を示した[89]。大腸菌(Escherichia coli)および黄色ブドウ球菌(Staphylococcus aureus)は、免疫不全の患者において重篤で生命を脅かす感染症を引き起こす2つの日和見病原体である。ユーカリグロブルス由来の精油は、グラム陽性菌(大腸菌)やグラム陰性菌(黄色ブドウ球菌)に対して強い増殖抑制効果を示すことが報告されている[90]。さらに、オレガノやタイムの精油は、Aspergillus nigerやA. flaousを含むカビの増殖を抑制することが報告されている[91]。クローブ精油は灰色かび病(Botrytis cinerea)に対して顕著な抑制効果が報告されている[92]。
2.13. 抗炎症作用
精油には強い抗炎症作用があることが報告されている。そのほとんどが最初に認識され、酸化性疾患や炎症性疾患の治療に関与していた。最もポピュラーなハーブであるCymbopogon citratusは、抗炎症・鎮痛剤として使用されていた。この精油がCOX-2の発現を抑制することが作用機序の基礎となっていることが明らかになった。シトラールはこの精油の主成分であり、COX-2の抑制やPPARα、γの活性化に有効な成分と考えられている[93]。
2.14. その他の活性
精油の昆虫忌避活性については、いくつかの研究論文が発表されている。Lavandula angustifolia(Miller)Hyptis suaveolens L.およびHyptis spicigera L.の精油は、Sitophilus zeamais成虫に対して強い忌避活性を示すことが報告されている[94]。抗リーシュマン活性は、プロマスティゴートおよび細胞内アマスティゴートに対して評価し、細胞毒性はJ774. G8を異なる濃度のE. bracteolateでインキュベートした。プロマスティゴートの形態は、7.945μg/mL(24時間)のE. bracteolate EO IC50値を示した[95]。さらに、精油は有意な抗制血活性を有することが示されている。Barbosaらによる研究では、Thymus caespititius、Thymbra capitata、Satureja montana、Origanum vulgareおよびChamaespartium tridentatumに由来する精油の、Bursaphelenchus xylophilus(松葉線虫)に対する殺虫活性が報告されている[96]。Cymbopogon citratus(レモングラス)およびTithonia diversifolia(メキシコ産ヒマワリ)の葉に由来するエッセンシャルオイルをCaenorhabditis elegans、Panagrellus redivivus、Meloidogyne incognitaおよびBursaphelenchus xylophilusに対する殺線虫活性を調べた。これらの線虫のうち、M. incognitaに対しては両精油ともに高い活性を示し、IC50値は1.068 μg/mLと0.747 μg/mLであった[97]。
いくつかの研究では、エッセンシャルオイルが人獣共通感染性のアニサキスの増殖を阻害することが示されている。同様の研究では、Origanum compactum由来の精油は、Micromesistius poutassouから分離されたAnisakis simplex L3幼虫に100%の死亡率を誘導することが報告されている[98]。別の研究では、オリガナムシリアクム精油が消化管寄生虫Anisakis simplexと蚊の媒介者Culex quinquefasciatusに対して保護効果を示すことが報告されている [99]。Gómez-Rincónらは、Melaleuca alternifolia(ティーツリー)のエッセンシャルオイルがAnisakis simplexのL3幼虫の成長を抑制することを示している[100]。
2.15. 精油とその化学成分の抗ウイルス活性
文献調査から、単純ヘルペスウイルス1型および2型(HSV-1およびHSV-2)ポリオウイルス、インフルエンザウイルスアデノ3型、デングウイルス2型、コックスサッキーウイルスB-1およびジュニンウイルスのようないくつかのDNAおよびRNAウイルスに対して、精油が強力な抗ウイルス作用を有することが十分に文書化されている[101]。生物活性植物ベースの純粋な天然物は、遺伝的に高い化学的多様性の存在に起因する豊富な抗ウイルス剤の新規な供給源である。ウイルス性疾患は、世界的に人間の健康にとって大きな関心事である。これまでのところ、いくつかのウイルスに対して有効な薬剤が発見されているだけで、強力な抗ウイルス作用を発揮する薬剤や分子が必要とされている。オレガノとクローブの精油は、アデノウイルス3型、コクサッキーウイルスB-1,ポリオウイルス[102,103]を含む多くの非開 発DNAおよびRNAウイルスに対して顕著な抗ウイルス性が報告されている。Melaleuca alternifoliaの精油は、タバコモザイクウイルス(TMV)に対して顕著な抗ウイルス活性を示し、また、投与後10日以内にニコチアナ・グルチノサの病変形成を抑制する結果をもたらしたことが明らかにされている[104]。試験管内試験試験では、茶、ユーカリ、タイムの精油およびそれらのモノテルペン含有量がHSV-1に対して実質的に活性であることが示されている。これらの精油は、ほぼ96%のHSV-1の阻害を産生し、モノテルペンはウイルスに対して約80%の阻害を示した[105]。植物由来の精油とその化学成分の抗ヘルペス能は以前に報告されている[106]。タイム油、マヌカ油、オーストラリア産ユーカリ油、ティーツリー油の精油はすでに抗ヘルペス活性が報告されている[107], [108], [109]。フェニルプロパン、セスキテルペン、トリテルペンなどの精油のいくつかの成分は、ライノウイルスやヘルペスウイルスに対する強力な抗ウイルス活性が承認されている[[110], [111], [112], [113]]。モノテルペンがウイルスの増殖を抑制する能力を報告している研究は非常に少なく,抗ウイルス効果について体系的に分析されていない。イソボルネオールはHSVに対する強力な抗ウイルス剤として報告されているが、テルペンの抗ウイルス活性、ウイルスの増殖サイクルを抑制する役割、作用機序については研究が不足している[114]。多くの試験管内試験研究では、実験条件下でエッセンシャルオイルがHSV-1の増殖能力を抑制することが報告されている[115]。ヒトにおけるHSV-1による原発性ウイルス感染症には、粘膜皮膚ヘルペス感染症、新生児ヘルペス、帯状疱疹性角膜炎、帯状疱疹性脳炎などがある。Glechon spathulata、Artemisia arborescensおよびGlechon marifoiaの精油は、HSV-1に対して強力な抗ウイルス活性を示すことが示されている[116]。メリッサオフィシナリスの精油にはシトロネラールとシトラールという2つの主要な成分が含まれており、HSV-2の複製を阻害する可能性があると考えられている。Eupatorium patensとArtemisia douglasianaの精油はデングウイルスに対して活性があることが確認されている[118]。さらに、Lippia junellianaとLippia turbinateの精油は、ジュニンウイルスに対して強い抗ウイルス活性を示した。ポゴステモンカブリンの精油成分は、H2N2インフルエンザAウイルスに対して活性が認められている[119]。Fortune llamargaritaの葉や果実から抽出した精油からは、抗アビアンインフルエンザウイルスH5N1活性が報告されている[120]。トラキスパーマム精油は、日本脳炎ウイルス(JEV)に対して顕著な抗ウイルス性を示すことが報告されている。Zeedanらによる研究では、Achillea fragrantissima精油の抗ORFウイルス(アパラポックスウイルス)活性が示されている[121]。最近、Pour ghan bariらによる試験管内試験研究が行われ、H9N2鳥インフルエンザウイルスに対するレモンバーム(M. officinalis)精油とノセルタミビルの抗ウイルス活性を評価し、ウイルスに対する相乗効果を分析した[122]。彼らは、様々な濃度のレモンバーム精油がH9N2ウイルスの複製過程を遅らせることを報告している。しかし、これらの複製阻害効果は、セルタミビルとの併用投与により増強された。Ocimum campechianum、Hyptismutabilis、Lepechinia vulcanicola、Minthostachys mollis、Lepechinia salviifoliaなどのコロンビアのMAPに由来する精油は、ヘルペスウイルスの1型および2型に対して優れた効果を示すことが示されている[123]。これらの精油は、初期の段階でウイルス感染を抑制することが報告されていた。したがって、植物由来の精油は、ヒトの様々なウイルス性疾患に対する抗ウイルス剤として開発される傾向が強く、合成抗ウイルス剤に代わる代替品となり得る。Cermelliらは、Myrtaceaen種、特にEucalyptus globulus Labillの揮発性油を、多くの呼吸器系ウイルスや細菌に対して調査した。彼らは、E. globulus揮発油の動物ウイルス株、感染症ウイルス株、Stenotrophomonas maltophilia 10株、腸内細菌肺炎10株、H. parainfluenzae 30株、Haemophilus influenzae 40株、S. aureus 20株、S. agalactiae 40株、Streptococcus pyogenes 120株に対する活性を実証した。さらに、パンデミック性耳下腺炎ウイルスに対しては穏やかな毒性が報告されている[124,125]。
精油およびその抽出成分の抗ウイルス活性をそれぞれ表1,表2に示した。
表1. 植物由来のいくつかの精油の抗ウイルス活性[126]
| S.no. | エッセンシャルオイルのソース | 標的ウイルス | メカニズムタイプ | SI | IC 50 |
|---|---|---|---|---|---|
| 1 | ゼンマイ (チュニジアのシダ) | コクサッキーウイルスB4 | ND | 789.8 | 2.2μg/ mL |
| 2 | Dysphania ambrosioides | コクサッキーウイルスB4 | ND | 74.3 | 21.7μg/ mL |
| 3 | Cymbopogon nardus | HIV-1 | ND | ND | 1.2 mg / mL |
| 4 | Thymus vulgaris vulgaris、 Cymbopogon citratus、 Rosmarinus officinalis | HIV-1 | ND | 1.13–3.6 | 0.05〜0.83μg / mL |
| 5 | Fortunellamargarita フルーツ | 鳥インフルエンザウイルスA(H5N1) | ND | ND | 6.8μg/ mL |
| 6 | 柑橘類のreshni 熟した果実の皮 | 鳥インフルエンザウイルスA(H5N1) | ND | 8.7 | 2.5μg/ mL |
| 7 | ペラルゴニウムグラベオレンス | IFV-A(H1N1) | 細胞間 | > 21 | <3.1μL/ mL |
| 8 | ユーカリグロブルス | IFV-A(H1N1) | 細胞間 | > 0.5 | <50μL/ mL |
| 9 | ラベンダーオフィシナリス | IFV-A(H1N1) | 細胞間 | > 8 | <3.1μL/ mL |
| 10 | 尋常性タイム | IFV-A(H1N1) | 細胞間 | > 4 | <3.1μL/ mL |
| 11 | Cymbopogon flexuosus | IFV-A(H1N1) | ND | > 4 | <3.1μL/ mL |
| 12 | 柑橘類のベルガモット | IFV-A(H1N1) | 細胞間 | > 5 | <3.1μL/ mL |
| 13 | Cinnamomum zeylanicum | IFV-A(H1N1) | 細胞間 | > 4 | <3.1μL/ mL |
| 14 | パチョリ | IFV-A(H1N1) | ND | 1.15 | 0.088 mg / mL |
| 15 | メキシコオレガノ(Lippia graveolens) | アシクロビル耐性HSV-1 | 細胞間 | 13.1 | 55.9μg/ mL |
| 16 | サルビアデソレアナ | アシクロビル耐性HSV-2 | 細胞間および細胞内のA | 55.2 | 28.6μg/ mL |
| 17 | Thymus capitatus | HSV-2 | 細胞間 | 6.0 | 18.6μg/ mL |
| 18 | Thymus capitatus | HSV-1 | 細胞間 | 6.9 | 17.6μg/ mL |
| 19 | Rosmarinus officinalis | HSV-1 | ND | 46.1 | 0.006% |
| 20 | Satureja hotensis | HSV-1 | ND | 32.2 | 0.008% |
| 21 | Artemisia kermanensis | HSV-1 | ND | 66.4 | 0.004% |
| 22 | ユーカリカエシア | HSV-1 | ND | 38.8 | 0.007% |
| 23 | Zataria multiflora | HSV-1 | ND | 55.4 | 0.003% |
| 24 | メキシコオレガノ(Lippia graveolens) | HSV-1 | 細胞間 | 7.4 | 99.6μg/ mL |
| 25 | Pulicaria vulgaris | HSV-1 | 細胞間 | 1 | 0.001% |
| 26 | Lallemantia royleana | HSV-1 | 細胞間 | 6.4 | 0.011% |
| 27 | スターアニス | HSV-1 | 細胞間 | 160 | 1μg/ mL |
| 28 | Mentha suaveolens | HSV-1 | 細胞内 | 67 | 5.1μg/ mL |
| 29 | オーストラリアのティーツリー | HSV-1 | 細胞内 | 43 | 13.2μg/ mL |
| 30 | ノハラガラシ | HSV-1 | 細胞間 | 1.5 | 0.035% |
注:SI=選択性指数、ND=定義されていない、HIV=ヒト免疫不全ウイルス、HSV=ヒトヘルペスウイルス、細胞内=ウイルスのライフサイクルの細胞間イベントへの影響、細胞間=吸着前後のウイルス表面への影響、”a”=ウイルスのライフサイクルの後期を示す。
表2. いくつかの個々の精油化合物の抗ウイルス活性[126]。
| S.no. | 化合物 | 標的ウイルス | メカニズムタイプ | SI | IC 50 |
|---|---|---|---|---|---|
| 1 | 樟脳 | BVDV | 細胞間 | 13.9 | 318.51μg/ mL |
| 2 | 1、8-シネオール | BVDV | 細胞間 | 9.1 | 331.17μg/ mL |
| 3 | ジェルマクローネ | IFV-A(H1N1) | 細胞間および細胞内b | > 41 | 6.03μM |
| 4 | β-サンタロール | IFV-A(H3N2) | 細胞内A | 10〜100μg / mL | |
| 5 | オイゲノール | IFV-A(H1N1) | ND | ND | <3.1μL/ mL |
| 6 | カルバクロール | IFV-A(H1N1) | ND | <0.15 | 2.6μg/ mL |
| 7 | カルバクロール | アシクロビル耐性HSV-1 | 細胞内 | 8.7 | 28.6μg/ mL |
| 8 | リモネン | HSV-1 | 細胞間 | 10.2 | 5.9μg/ mL |
| 9 | β-ピネン | HSV-1 | 細胞間 | 24.3 | 3.5μg/ mL |
| 10 | カルバクロール | HSV-1 | 細胞間 | 43 | 7μM |
| 11 | チモール | HSV-1 | 細胞間 | 43 | 7μM |
| 12 | カルバクロール | HSV-1 | 細胞内 | 5.1 | 48.6μg/ mL |
| 13 | p-シメン | HSV-1 | 細胞間 | ND | > 0.1% |
| 14 | カルバクロール | HSV-1 | 細胞間 | 1.4 | 0.037% |
| 15 | チモール | HSV-1 | 細胞間 | 7 | 0.002% |
| 16 | オイゲノール | HSV-1 | 細胞間 | 2.4 | 35μg/ mL |
| 17 | トランスアネトール | HSV-1 | 細胞間 | 5 | 20μg/ mL |
| 18 | β-ユーデスモール | HSV-1 | 細胞間 | 5.8 | 6μg/ mL |
| 19 | ファルネソール | HSV-1 | 細胞間 | 11.4 | 3.5μg/ mL |
| 20 | β-カリオフィレン | HSV-1 | 細胞間 | 140 | 0.25μg/ mL |
注:SI=選択性指数、ND=定義されていない、BVDV=ウシウイルス下痢ウイルス、HIV=ヒト免疫不全ウイルス、HSV=ヒトヘルペスウイルス、細胞内=ウイルスのライフサイクルの細胞間イベントへの影響、細胞間=ウイルス表面の吸着前または吸着後の影響、”a”=ウイルスのライフサイクルの後期、”b”=ウイルスのライフサイクルの初期段階。
3. コロナウイルスに対する抗ウイルス活性
3.1. コロナウイルスとは?
コロナウイルスは、コロナウイルス科の別の亜科(coronavirinae)に分類されている。コロナウイルス科コロナウイルス属のメンバーは、ニドウイルス目の単系統のクラスターで、魚類(バフィニウイルス)鳥類(コロナウイルス)哺乳類(トロウイルス、カロナウイルス)の3つのクラスの脊椎動物のエンベロープされた陽性鎖RNAウイルスである。変異ゲノム領域を対象とした根無し系統樹と根付き系統樹の研究では、4つの異なるCoVクラスターが明らかになった。3つのクラスターは、すでに発見されている非公式なグループ1,2,3に対応しており、現在ではそれぞれアルファ、ベータ、ガンマのCoVとして正式に分類されている。4番目のクラスターは、農家の3つのクラスターとは異なり、鳥類で発見された。すべての基準では、この4番目のクラスターは、暫定的に「デルタ-CoV’s」と呼ばれる別の属(非公式で、まだ承認されていない)の下にリストされている。さらに、β-CoVの場合には、さらに4つの分岐した系統を区別することができ、それぞれ前者の2A〜Dに対応するA〜Dとされている(図5)。
図5. コロナウイルスの分類

コロナウイルス科を横断すると、ビロンは球形で大きさが120~160nm、桿状、170~200×75~88nm(バフィニウイルス)またはその両方で、特徴的な三日月状に曲がった桿状をしている(トロウイルス)。これらの粒子は、典型的には大きな花びら状またはクラブ状の表面突起(スパイク)で覆われており、電子顕微鏡下では太陽コロナ(図6)のイメージを作り出している。CoVの核酸カプシドはらせん状の核酸カプシドを持ち、洗浄剤を塗布するとウイルスから放出される。コロナウイルスのヌクレオカプシドは緩く巻かれているように見え、トロウイルス科では管状であることが特徴的である。コロナウイルス科は、遺伝子の複雑さとゲノムの大きさの点で、これまでに発見された大型RNAウイルスの中では、オカウイルス(ロニウイルス科に属し、オカウイルスは無脊椎動物の大型ニドウイルスである)に匹敵するものを除いて、最も大きなサイズのウイルスである。
図6 コロナウイルスの一般的な構造 コロナウイルスの一般的な構造

3.2. 精油の抗コロナウイルス活性
精油は、ヒトの様々な病気の原因となるウイルスに対する抗ウイルス性を示すことが示されている。異なるアロマハーブや薬用植物から抽出したオレオレジンと精油の混合物の抗ウイルス作用は、コロナウイルス感染性気管支炎ウイルス(IBV)に対して生体内試験と試験管内試験の両方で評価された[127]。鳥類のIBV治療に使用されたこの混合物は、2つの異なる宿主系、胚乳卵およびVero E6細胞においてウイルス力価の低下をもたらした。この混合物のIBVに対する有効性は、ニワトリにおいても調査された。精油とオレオレジンの混合物を1:20希釈で鶏に噴霧したところ、IBVに曝露した2時間前にはIBVに対して顕著な効果を示したことが報告されている。このタイプの治療法は、鳥類の気管内のウイルスRNAの量を減少させるとともに、鳥類の徴候や臨床病変の重症度を減少させるという実質的な効果を示した。この精油とオレオレジンの混合物を投与された鳥類は、4日間の期間、IBVに対する保護効果を示し、また、2週間以上の臨床症状とウイルス感染の伝播を減少させた。この混合物は、ウイルスの侵入および付着に先立って、より有益であることが証明されたため、殺菌作用を産生した。したがって、これらの結果は、この治療混合物が細胞を持たないウイルスに対してより活性であり、それゆえ、他のヒトコロナウイルスを含む他のタイプのウイルスに対しても活性である可能性があることを示している。Wenらが実施した別の研究では、SARS-CoV(重症急性呼吸器症候群コロナウイルス)に対する221種類の植物化学物質と精油成分の効果を評価した[128]。彼らは、SARS-CoVに感染したVero E6細胞に対する細胞病原性効果を調べるために、細胞ベースのアッセイを使用した。すべての実験成分のうち、10種類のテルペノイド、2種類のセスキテルペノイド、2種類のトリテルペノイドが3.3~10μMの用量で最大の阻害効果を示した。研究者らは、Vero E6細胞の増殖(CC50)と複製(EC50)を50%阻害した22化合物の濃度を測定した。これは、精油由来の植物化学物質がSARS-CoVを阻害する可能性があることを示した初めての研究であり、抗SARS-CoV薬の開発に向けた新たなアプローチを提供した。シトラスシネシス(Citrus sinesis)Anthemis hyalina(Anthemis hyalina)およびNigella sativa(Nigella sativa)に由来する精油は、コロナウイルスの複製およびTRP遺伝子の発現レベルに対して有意な活性を示すことが報告されている[129]。コロナウイルス(CoV)の複製およびコロナウイルス伝染全体にわたるTRP遺伝子の発現に対する抽出物の影響を評価するために、HeLa-CEACAM1a(HeLa-epithelial carcinoembryonic antigen-related cell adhesion molecule 1a)細胞にMHV-A59(マウス肝炎ウイルス-A59)を注射したところ、非毒性の活性量であることが判明した。TCID50/ml(注入された組織培養細胞の50%において細胞病原性の影響をもたらすであろう組織培養感染性用量)は、ウイルス負荷を決定するための治療のために見出された。炎症性サイトカインIL-8のレベルは、抽出物暴露の24時間および48時間後に増強されることが見出された。TRPA1, TRPV4, TRPM6, TRPC4, TRPM7, TRPM8は、抽出液処理後に発現量が大きく変化した遺伝子であった。CoVに感染した細胞に抽出物を添加すると、ウイルス負荷は減少した。いずれの抽出物処理も、CoV感染後のTRP遺伝子発現、IL-8分泌、ウイルス負荷に効果を示しており、治療分子の可能性を秘めた最有力候補であると考えられる。
Laurus nobilusの精油は、β-ピネン、α-ピネン、1,8-シネオール、b-オシメンを主成分とする。この精油は、SARS-CoV-1に対して強い抗ウイルス活性を有しており、選択性指数は4.6,IC50値は120mg/mlであることが報告されている[130]。Juniperus oxycedrus精油は、以前にも抗ウイルス活性が報告されている。この精油には、2.2%のδ-カジネン、2.3%のエピビシクロ-キペラントレン、6.7%のリモネン、α-ペランドレンを主成分とする合計48の化合物が含まれていることが確認されている。これらの化合物はいずれもSARS-CoV-1コロナウイルスに対して顕著な阻害活性を示した[130]。Theileria orientalisの精油は、その化学組成が豊富である。この精油からは43種類の化合物が同定されており、全体の86.6%を占めている。主な成分は、α-セドロール9.55%、δ-3-カレン9.48%、α-ピネン35.72%であった。これらの活性フィトケミカルはいずれもSARS-CoV-1コロナウイルスに対して阻害活性を示すことが報告されている[130]。
4. 精油の抗SARS-CoV-2(COVID-19)活性とその化学成分
4.1. 悲惨なCOVID-19パンデミック
2019年のコロナウイルス感染症は、致死的な健康脅威として浮上し、急速なペースで増加を続けている。この病気は、重症急性呼吸器症候群コロナウイルス2(SARS-CoV-2ウイルス)によって引き起こされる。コロナウイルス病2019の兆候や症状は、曝露後2~14日後に現れることがある。暴露後、症状が出るまでの期間を潜伏期間といいます。一般的な徴候や症状としては、発熱、咳、肺炎、倦怠感、呼吸困難、多臓器不全などが考えられる。このコロナウイルス感染症は、後にCOVID-19と命名されたが、中国の武漢市で発生し、そこから世界中に広がった。世界的にお祭りの月とされる12月に発生したため、世界各地で急速にパンデミックした。2020年9月26日までに、世界的にCOVID-19の32,344,734人以上の症例と984,902人の死亡が報告された[131]。COVID-19パンデミックによって最悪の被害を受けた国の一部には、アメリカ合衆国、インド、ブラジル、ロシア連邦、コロンビア、ペルー、メキシコ、スペイン、アルゼンチン、南アフリカ、フランス、チリ、イラン(イスラム共和国)イギリス、バングラデシュ、イラク、サウジアラビア、トルコなどがある。SARS-CoV-2感染症とその炎症症状に対して承認されている薬剤はわずかである。この病気に対するワクチンは開発されておらず、世界的には20種類以上のワクチンが開発されている。COVID-19の症例数と死亡者数を持つ最初の10カ国を表3に示する。
表3. COVID-19による世界で最も被害の大きかった国の症例数と死亡者数[131]。
| S.No | 国 | 症例数 | 死亡者数 |
|---|---|---|---|
| 1 | アメリカ合衆国 | 6,910,082 | 201,634 |
| 2 | インド | 5,903,932 | 93,379 |
| 3 | ブラジル | 4,657,702 | 139,808 |
| 4 | ロシア連邦 | 1,136,048 | 20,056 |
| 5 | コロンビア | 790,823 | 24,924 |
| 6 | ペルー | 788,930 | 31,938 |
| 7 | メキシコ | 715,457 | 75,439 |
| 8 | スペイン | 704,209 | 31,118 |
| 9 | アルゼンチン | 678,266 | 14,766 |
| 10 | 南アフリカ | 667,049 | 16,283 |
4.2. SARS-CoV-2に対する精油の抗ウイルス活性とその作用機序
精油は、抗ウイルス作用、免疫調節作用、抗炎症作用、気管支拡張作用を有することが知られている。精油とその化学成分は、その親油性の性質から、SARS-CoV-2感染症の治療薬として提案されている。これらの油は、膜の破壊につながるウイルス膜に入る可能性を持っている。エッセンシャルオイルとその構成成分のフィトケミカルは、ウイルスの複製を妨害し、また、粘液溶解と気管支拡張を介して宿主の呼吸器系に利益をもたらす。エッセンシャルオイルの抗COVID-19活性に関するこれまでのデータは、ほとんどが試験管内試験研究とコンピュータ支援ドッキング技術に基づいている。
古くから、ニンニクオイルはインフルエンザや風邪、その他の感染症などの治療に使用されていた。ガーリックオイルのGC-MS分析では、18種類の化合物が確認されている。主な化合物は、6.5%のジアリルテトラスルフィド、6.7%のアリルメチルトリスルフィド、8.2%のアリル(E)-1-プロペニルジスルフィド、22.8%のアリルトリスルフィド、28.4%のアリルジスルフィドであった。18成分のうち、17成分について、ウイルスメインプロテアーゼMpro/6LU7およびSARS-CoV-2のACE-2タンパク質に対する作用を調べた。ACE-2はウイルスの宿主細胞への侵入を助ける酵素であり、Mproはウイルスの複製を助ける。調査した17の化合物は、MproおよびACE-2との顕著な相互作用を示し、それゆえ、COVID-19の治療にニンニクオイルの強力な効力があることが明らかになった[132]。ウイルスが宿主細胞内で産生する酸化ストレスは、ウイルスによって引き起こされる疾患のライフサイクルおよび病態形成において主要な役割を果たしている。酸化ストレスにより、宿主細胞では、核内因子エリスロイド1p45関連因子2(Nrf2)を含む抗酸化経路が活性化される[133]。Nrf2転写因子は、抗ウイルス作用に関連するいくつかの遺伝子の発現レベルを調節することがよく知られている[134]。化合物PB125®はNrf2を刺激する可能性が高く、HepG2ヒト肝臓由来細胞においてTMPRSS2 mRNAとACE-2レベルのダウンレギュレーションをもたらしたことが報告されている。ACE-2とTMPRSS2 mRNAはともに、SARS-CoV-2の宿主細胞への浸透に関与している。さらに、PB125®は、重度のCOVID-19症例の経過において、サイトカインストームと認識されたヒト初代肺動脈内皮細胞のサイトカイン関連遺伝子約36個の発現を変化させることが報告されている。Nrf2の活性化は、SARS-CoV-2患者のサイトカインストームを抑制する可能性が示唆された[134]。HoらとPatelらによる研究では、ニンニク油の活性成分の一つであるジアリルサルファイドが、肺MRC-5細胞においてNrf2を活性化する可能性があることが示された。活性化後のNrf2の核への転座は、p38/ERKシグナリングの引き金となり、酸化ストレスの抑制を通じて肺損傷を抑制した[135,136]。
Kulkarniらによるin silico研究では、COVID-19ウイルスのスパイク蛋白質のS1(受容体結合ドメインとしても知られている)サブユニットに対する、異なるファミリーに属する異なる植物由来のエッセンシャルオイルの可能性を調査した[137]。スパイクタンパク質のS1サブユニットは、ACE-2受容体を介してウイルスと宿主細胞との相互作用に関与している。使用した精油のうち、ピュレゴネ、チモール、L-4-テルピネオール、シンナミルアセテート、ゲラニオール、カルバクロール、シンナマルデヒド、アネトールは、シリコでS1サブユニットを阻害する可能性を示した[137]。同様のドッキング研究がElfikyによって行われ、RdRps(SARS-CoV RNA依存性RNAポリメラーゼ)およびCOVID-19に対するチモキノンおよびシンナムアルデヒドの有効性が実証された。どちらの化合物もRdRpsに対する低い結合親和性を有することが判明した[138]。Elifikyは、シンナムアルデヒドがSARS-CoV-2のウイルス付着を標的とすることができると結論付けたが、この事実を確立するためには、生体内試験および試験管内試験でのさらなる研究が必要である。黄(Huang)らは、キセノグラフト化されたマウスモデルにおいて、リポ多糖を介して誘導される急性肺損傷に対するシンナムアルデヒドの保護効果を評価した[139]。シンナムアルデヒドは、肺水腫および湿潤乾燥比を減少させることで、マウスの肺に有益な効果をもたらした。さらに、シンナムアルデヒドは気管支肺胞液中のマクロファージ、好中球、総細胞数を抑制した。さらに、シナマルアルデヒドは、IL-1β、IL-13,IL-6,TNF-αを含む炎症に関与するサイトカインの産生を減少させた[139]。このin silicoデータは、シナマルアルデヒドがCOVID-19に対して重要な役割を果たす可能性が示唆され、より多くの生体内試験とin vitostudiesを提供する必要がある。
ユーカリグロブルスに由来する精油は、咽頭炎、副鼻腔炎、気管支炎などのいくつかの呼吸器疾患を治療するために使用されている。ユーカリ油の有効成分の一つである1,8-シネオールは、異なる薬剤による平滑筋の収縮を抑制し、筋弛緩作用があることが報告されている[140,141]。また、シネオールの吸入により鎮痛効果や抗炎症効果が得られることが報告されており、COPDや喘息患者への使用が期待されている[142]。ユーカリ精油は、単純ヘルペスウイルスHSV-1,HSV-2,おたふくかぜウイルスに対して強い抗ウイルス活性を示すことが報告されている[143]。ユーカリ精油とその成分の抗ウイルス活性を裏付ける強力な証拠があることから、研究者たちは試験管内試験アッセイやドッキングによりSARS-CoV-2に対する活性を調査することになった。ユーカリ精油の活性成分の一つであるジェンノンは、SharmaらによってウイルスプロテイナーゼMpro/3CLproに対する活性が調査されている。その結果、ジェンソン分子はPRO184,TRY126,LEU29,TRP207,PRO52,ALA7との疎水性相互作用、HIS163,ARG38,ASP34,LYS3とのイオン性相互作用、T16,D10,L30,V18,M4との水素結合相互作用を介してMproと反応し、複合体を生成することが明らかになった[144]。Sharmaらは、ユーカリ油の他の活性成分の一つであるユーカリトール(1,8-シネオール)について分子ドッキング解析を行い、それがMproと結合してウイルスの複製を阻害することを示した。ユーカリプトールとMproの複合体は強いイオン相互作用、水素結合相互作用、疎水性相互作用を形成することが報告されている[145]。しかし、これらの結果の妥当性は、SARS-CoV-2に対する試験管内試験酵素アッセイによって検証されるべきであることが著者らによって示唆された。Meradらによる研究では、SARS-CoV-2患者のほぼすべてが肺異常を発症していることが示されている。CoVID-19患者の死亡および重症度は、過活動性および異常な炎症反応に起因している。このような炎症反応ストームは、肺や腎臓、リンパ節、脾臓、心臓などの他の影響を受けた臓器でサイトカインのレベルが高くなり、かなりの単核細胞の浸潤と深遠なリンパ球減少症を引き起こす原因となっている。SARS-CoV-2患者のサイトカインプロファイルは、TNF、IL-6,-7などのサイトカインやその他の炎症性サイトカインのレベルが高いことを示していた[146]。ユーカリ油とその活性成分であるユーカリプトールの肺感染症や炎症時のマクロファージや単球のリクルートに対する効果を調べるために、ex vivoおよび試験管内試験でのさまざまな研究が行われていた。これらの研究のデータから、ユーカリ油とその活性成分であるユーカリプトールの両方に顕著な免疫調節作用があることが明らかになった。どちらの治療法もマクロファージや単球からの炎症性サイトカインの排出を減少させたが、それらの貪食性は止められなかった[147]。これらのデータをまとめると、臨床試験および前臨床試験のデータは、ユーカリ油およびその有効成分の顕著な抗COVID-19の可能性を示している。したがって、この点では、直ちにさらなる調査が必要である。
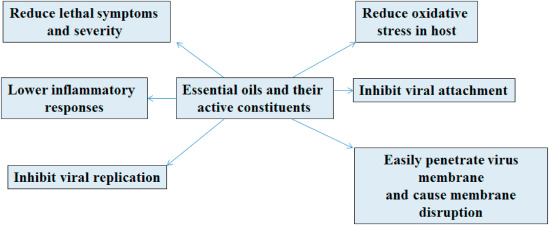
Silvaらは、171種類の精油とその構成化合物を、分子ドッキングにより、スパイク蛋白質、Rdrp、ADP-リボース-1-ホスファターゼ、エンドリボヌクレアーゼ、ヒトアンジオテンシン変換酵素、ウイルスプロテアーゼMproを含むSARS-CoV-2の様々な蛋白質に対してスクリーニングした[148]。171種の化合物の中でMproに高い結合効果を示したのは、(E)-ネロリドール、(E,E)-ファルネソール、および(E,E)-α-ファルネセンを含む少数の化合物のみであった。その結果、これらの精油成分を混合または単独で投与することで、ウイルスの複製を抑制できることが明らかになった。SARS-CoVのウイルス感染に関与する主要なタンパク質には、エンドリボヌクレアーゼと非構造タンパク質15(Nsp15)が含まれている[149]。化合物(E)-ネロリドール、(E,E)-ファルネソール、(E,E)-α-ファルネセン、および(E)-β-ファルネセンは、Nsp15に対する顕著な結合親和性を示している。RNAウイルスのウイルス複製はRdRpによって触媒され、ウイルス複製の主要かつ重要なステップである。そのため、RNA ウイルスに対する抗ウイルス療法の主要なターゲットとなっている[150]。(E,E)-farnesolはRDRpに対する最高のドッキングスコアが報告されている。SARS-CoV-2ウイルスにはスパイク蛋白質が存在し、宿主細胞膜上に存在するACE-2と相互作用することで宿主細胞への侵入を助けている[151]。したがって、ACE-2はCOVID-19に対する管理療法の主要なターゲットの一つと考えられている。α-ブルネセン、エレマンチン、(Z)-スピロエーテル、β-セスキペランドレン、(E)-ネロリドール、(E,E)-ファルネソール、(E,E)-β-ファルネセン、(E,E)-α-ファルネセンなどの精油成分は、ACE-2に対してより高い親和性を示すことが報告されている。また、ギ酸ゲラニル、(E,E)-ファルネソール、(E)-β-ファルネセン、(E,E)-α-ファルネセン、エレマンチン、および(E)-酢酸シンナミルという化合物は、SARS-CoV-2のスパイク蛋白質に対してより高い有効性を示した。図7は、SARS-CoV-2感染症における精油およびその化学成分の可能性を示すものである。
図7. SARS-CoV-2に対する精油とその成分のさまざまな作用機序を表したもの。
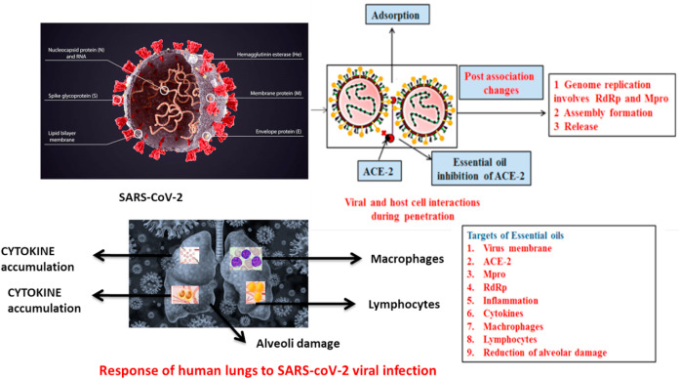
SARS-CoV-2 のいくつかのタンパク質に対するカルバクロール、メントール、オイゲノール(精油の主要成分)の効果を分析するために、Silva と共同研究者らによって分子ドッキング研究が行われた。これらの化合物は、ACE-2,RdRp、Mpro、スパイク蛋白質に対して高い親和性を示すことが報告されている。同様に、Kumarらは、SARS-CoV-2の主要なプロテアーゼタンパク質とカルバクロールの結合能を評価したin silico研究を行った[152]。その結果、カルバクロールはMproを阻害することでウイルスの複製を顕著に抑制することが示された。メントールはラットモデルにおいて、胃腸保護作用、抗炎症作用、免疫調節作用などの豊富な薬理作用が報告されている。メントールを投与したラットでは、インターロイキン-1,腫瘍壊死因子α(TNF-α)インターロイキン-23などの炎症性サイトカインの発現やレベルが大幅に低下することが明らかになっている[153,154]。オイゲノールは、HSV-1およびHSV-2に対してそれぞれ抗ウイルス活性を有することが示されている[155]。オイゲノール治療は、白血球の有意なリクルートとサイトカイン(TNF-αおよびIL-6)の抑制を介して肺の炎症性嵐を抑制することが報告されている[156]。Gamesらは、エラスターゼ誘発性肺気腫マウスモデルにおけるカルバクロールを含む3つの分子の影響を評価する生体内試験試験を行った[157]。その結果、カルバクロールは気管支肺胞液中のマクロファージのリクルート、肺胞の拡大、IL-1β、IL-6,IL-8,IL-17 の発現を抑制することが示された。また、カルバクロール投与マウスでは、疾患対照群と比較して炎症反応は低かった。以上、生体内試験およびin silico試験の結果から、カルバクロール、メントールおよびオイゲノールがCOVID-19に対して潜在的な役割を果たしていることが示唆された。SARS-CoV-2に対するこれらの結果をさらに確立するためには、より多くの試験管内試験試験および生体内試験試験が必要である。ゼラニウム油およびレモン油は、上皮細胞において有意なACE2阻害効果を示した[158]。図8にSARS-CoV-2感染症に対する精油とその有効成分の標的となりうるものを示した。
図8 SARS-CoV-2に対する精油と化学成分のターゲットとして考えられる生化学的経路 SARS-CoV-2に対する精油およびその化学成分の標的として考えられる生化学的経路。肺におけるSARS-CoV-2感染後の事象とその有害症状を抑制するための精油の役割。
4.3. 今後の展望
コロナウイルスに対する天然物、特に精油やその化学成分をベースとした抗ウイルス治療薬は、費用対効果が高く、副作用も少ないため、今後も開発を進めていく必要がある。SARS-CoV-1およびSARS-CoV-2を含むいくつかのウイルスに対する潜在的なワクチンは開発されていない。したがって、これらの感染性ウイルスを克服することは、問題があり、困難であるように思われる。しかし、植物由来の精油とその化学成分には顕著な抗ウイルス作用があることが報告されており、ドッキング研究の結果、コロナウイルスに対しても有効であることが証明されている。コロナウイルスに対する抗ウイルス薬の主な欠点は、特定のウイルス遺伝子やタンパク質を標的とすることであり、HIV、HSV、SARS-CoV-2で観察されるようなゲノム突然変異が急速に起こることである[159,160]。精油の抗ウイルス特性に関する研究は初期段階にある。したがって、活性物質の同定、基礎となるメカニズムの記述だけでなく、有効性と明らかな生体内試験でのアプリケーションの分析は、エッセンシャルオイルから強力な抗ウイルス化学療法のプローブをバックアップするために提案されている。エッセンシャルオイルとその化学成分は、コロナウイルス[161]を含む異なるウイルスのいくつかの潜在的な二分子経路を標的とすることが報告されている。したがって、他の天然成分や処方された薬との併用療法によってCOVID-19に対抗する可能性を探るために、より多くの研究が行われるべきである。精油には薬理学的に重要な化学成分が豊富に含まれている。これらの分子は、SARS-CoV-2に対する抗ウイルス作用について研究されるべきである。精油は、ウイルスのいくつかの潜在的な経路を標的とする大きな可能性を持っており、COVID-19に対しても同様の作用を発揮すると考えられている。エッセンシャルオイルの吸入は、β-オシメン、1,8-シネオール、β-ピネン、α-ピネン、カルノシン酸、ロスマリン酸などの活性揮発性成分が豊富に含まれているため、COVID-19患者の補助療法になる可能性がある。揮発性分子は高い蒸気圧を示し、摂取後に肺に排出されやすい性質を持っている。また、精油の揮発性成分の摂取・排出が容易であることは、薬理学的な観点からドラッグデリバリーに利用できる可能性がある。このように、COVID-19のための仮説分子は、その薬理作用とともに、肺による摂取と呼気の間の適切なバランスを維持しなければならない。この点では、精油は、経口的にもエアゾール化された形態でも投与することができるので、COVID-19に対する使用において有利である。アロマハーブや薬用植物由来の精油などの自然療法は、今後も重要な役割を果たし、抗コロナウイルス薬の開発と発展に貢献していくことを期待している。
5. おわりに
結論として、精油の抗ウイルス効果に関する文献調査から、精油とその化学成分がCOVID-19に対する薬剤開発やデザインのリードとなる可能性があることが示された。精油は、ウイルスのライフサイクルの発症に重要な経路を標的とする可能性が高い。精油は、ウイルス膜に容易に浸透し、それによって膜破壊を引き起こすことができる。エッセンシャルオイルは、ウイルスの付着(ACE-2の阻害)と複製(Mproの阻害)を阻害する顕著な可能性を持っている。また、精油はSARS-CoV-2感染時に発生するサイトカインストームを抑制する傾向が強く、肺胞の炎症を抑制する。さらに、これらの精油は、損傷部位へのマクロファージのリクルートを抑制する。これらの作用により、COVID-19の患者さんにも効果があると考えられ、また、感染症による重篤な症状を抑えることができると考えられる。