コンテンツ
The angiotensin-converting enzyme 2 (ACE2) receptor in the prevention and treatment of COVID-19 are distinctly different paradigms
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7360378/
要旨
COVID-19感染時の高血圧管理のためのアンジオテンシン変換酵素(ACE)阻害薬やアンジオテンシンII 1型受容体拮抗薬(ARB)の使用については、現在議論がなされている。
具体的には、ACE阻害薬またはARBは、理論的にはACE2受容体の発現を増加させ、それゆえにウイルス負荷を増加させることを介して感染に寄与する可能性が示唆されている。
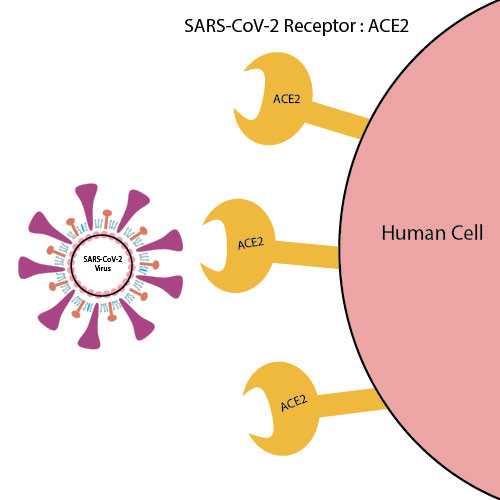
ACE2受容体は、SAR-CoV2ウイルススパイクと結合し、COVID-19感染を引き起こす役割を担っている。ACE阻害薬やARBの議論をやや曖昧にしているのは、ACE2受容体の発現は、SIRT1の発現を活性化または増加させる化合物によって増加させることができるということである。
したがって、一般的な食事介入、ビタミンおよび栄養素は、直接的または間接的にACE2受容体の細胞発現に影響を与える可能性がある。ビタミンC、メトホルミン、レスベラトロール、ビタミンB3およびビタミンDを含む、ACE2受容体の発現を増加させることができる多くの一般的な化合物が存在する。
細胞性ACE2受容体のダウンレギュレーションまたはブロックは、おそらくプロ炎症性であり、COVID-19における末梢臓器病理および死亡率に寄与する可能性があることを認めることが重要である。
結論として、ACE2受容体の観点から、COVID-19の予防と治療は明らかに異なる。本レターは、このような現在の議論を反映しており、高血圧患者や正常血圧の患者に対して、アンジオテンシン変換酵素阻害薬やARBがCOVID-19感染時に有益である可能性が高いことを示唆している。
キーワード
ACE2受容体、COVID-19、SIRT1、ACE阻害薬、ARB、ビタミンC、メトホルミン、レスベラトロール、コロナウイルス、SAR-CoV2
本文
アンジオテンシン変換酵素2(ACE2)受容体は、SAR-CoV2ウイルススパイク複合体の受容体結合ドメインとして作用する[1]。これにより、ウイルスの付着、融合、細胞内への侵入、COVID-19への感染が可能となる[1]。ACE2受容体の発現を増加させる可能性のある化合物は、メディアの関心を集めている[2]。特に、ACE2受容体の発現を増加させることで、SAR-CoV2のウイルス負荷、罹患率、死亡率を増加させ、感染性を高める可能性があるという観点から、ACE2受容体の発現を増加させる化合物が注目されている[2-4]。ACE2受容体の観点から見ると、COVID-19の予防と治療は明確に異なる。
細胞性ACE2受容体を標的としたCOVID-19の予防は理論的には興味深いが、実際には有用な戦略ではなく、死亡率を増加させる可能性がある[2, 3]。一方で、SAR-CoV2スパイクと結合してウイルスを不活性化する可溶性ACE2受容体を送達することに関心が寄せられている。これは、細胞性ACE2受容体システムをそのまま残すので、実用的な解決策となるだろう(すべてのウイルスが囮の可溶性ACE2受容体に結合している場合)[5]。可溶性ACE2受容体は、(細胞培養において)最大5000倍のバイアル負荷を減少させることができ、ウイルス負荷を早期に減少させるために、または急性および重度の呼吸器病変時に肺を温存するための治療オプションとして使用することができる[6]。
いくつかの研究グループは、COVID-19感染症のすべての患者に対してACE阻害薬が論理的に選択される可能性があることを示唆している[7]。これは、高血圧症の既往があるかどうかとは無関係である。すべての患者にACE阻害薬を投与する根拠は、ACE2受容体の発現を増強し、細胞性炎症をさらに低下させる可能性があるということである [2, 7]。
ACE阻害薬またはアンジオテンシンII型1受容体拮抗薬(ARB)がACE2受容体のmRNAおよび発現をアップレギュレートする可能性があるという限られた証拠がある[2]。
重要なことに、COVID-19感染は、ACE2調節領域の感染関連転写因子に付着することで、ACE2受容体を効果的にダウンレギュレーションする[2]。ANG IIもまた、ACE2受容体の発現を低下させる。心臓、肺、肝臓、および腎臓の損傷は、COVID-19における罹患率および死亡率の原因である[8]。これらの臓器系は、他の身体系よりもACE2受容体の発現が高い。ACE2はAng IIをAngに変換するので[1-7]、ACE2受容体のダウンレギュレーションは、アンジオテンシンII(ANG II)[2]の逆らわない増加を介して、重要な臓器系を高炎症の影響を受けやすくする。COVID-19およびSARSにおける呼吸困難は、ACE2受容体発現の低下と関連している可能性が高い [2, 7-9]。糖尿病、高血圧、メタボリックシンドローム、高齢者(臓器ACE2発現が低下している)は、より高い致死率になりやすい[10]。
また、COVID-19の血圧管理をめぐって、メディアでも大きな議論がなされている[2]。アンジオテンシン系を標的とする血圧治療薬は、ジャーナルの編集記事で長く議論されてきた。専門学会は現在、ACE阻害薬とARBをCOVID-19の予防策としても治療の選択肢としても中止すべきではないとする見解を発表している[2]。高血圧患者において、モノクラスとしてのACE阻害薬やARBを休薬すれば、アンジオテンシンII形成が優位になるだろう[2, 4]。高血圧症では、ACE阻害薬はACE2とANG II形成のバランスを回復させる役割を果たしている。ACE阻害薬は、COVID-19におけるANG II形成の減少を介してACE2受容体のダウンレギュレーションを減少させる可能性がある[2, 7, 9]。
興味深いことに、ACE2発現に影響を与え得るのは、ACE阻害剤および治療用量でのARBだけではない。カリウム摂取量の増加[11]、断続的な絶食[12]、ニコチン[13]、ビタミンD[14]など、ACE2の発現を増加させる可能性のある他のメディエーターが存在する。
ACE2の発現は、SIRT1の発現を活性化または増加させる化合物によって増加する可能性があることを考慮することが重要である[15、16]。SIRT1 は ACE2 遺伝子のプロモーター領域に隣接して発現しているため、SIRT1 の発現が増加したり、機能的に活性化されたりすると、ACE2 の発現が増加する [16]。
SIRT1 の発現または活性化と(直接的または間接的に)正の相互作用を示す一般的なメディエーターには、カロリー制限 [17]、レスベラトロール [18、19]、ビタミン C [20、21]、アスピリン [20]、メトホルミン [22]、ビタミン B3 [23] がある。これは、COVID-19 [10]の重症急性呼吸窮迫症候群に対する高用量ビタミンCの救済治療の可能性の理由についての機序的説明を提供する可能性がある。
COVID-19呼吸器感染症に関するポイント
- 細胞性ACE2受容体のダウンレギュレーションまたは阻害は、プロ炎症性であり、末梢臓器病理に寄与する可能性がある。
- ACE2受容体の機能的発現を刺激するか、またはACE IIを阻害する治療薬は、有用な治療アプローチとなり得る。
- ACE阻害薬またはARBは、高血圧患者および正常血圧患者の両方において安全である可能性がある
- ACE2発現に関して、ACE阻害薬やARBを中止すべきか、継続すべきかの論説は、鈍いように思われる。特に、他の治療薬、食事介入、ビタミンおよび栄養素が直接または間接的にACE2受容体の細胞内発現に影響を及ぼす可能性がある場合はなおさらである。
- ビタミンC、メトホルミン、レスベラトロール、ビタミンB3およびビタミンDを含むACE2受容体の発現を増加させることができる多くの一般的な化合物がある。