コンテンツ

掲載:2018年07月06日 記事履歴
要旨
ステビオール配糖体甘味料は、ステビアrebaudiana Bertoni植物、それは何百年もの間、その甘いプロパティのために使用されている南米に自生しているキク科(Compositae)のメンバーから抽出し、精製されている。肥満、糖尿病、および他の関連する合併症の継続的な増加率で、これらの問題を抑制するための手段として砂糖の摂取量の削減を求める世界的な公共政策と連動して、ステビアなどの低カロリーおよび無カロリー甘味料(LNCSs、また、高ポテンシャル甘味料として知られている)は、消費者や食品メーカーの間で関心を集めている。
この魅力は、ステビアは、植物ベースであることに関連しているゼロカロリーと砂糖よりも甘い50〜350倍である甘い味で、それは砂糖とカロリーを削減した食品や飲料製品で使用するための優れた選択肢を作る。ステビアの安全性は、世界中のいくつかの食品規制当局および安全当局によって肯定されているにもかかわらず、LNCS全般の安全性に関する継続的な懸念を含め、ステビアの安全性および利点に関する十分な教育が行われていないため、医療専門家および消費者は、ステビアを推奨または使用することを躊躇している。
したがって、本レビューおよび2017年のASNの年次大会で本レビューに先立って開催されたステビアシンポジウムの目的は、ステビアに関する科学の現状、その安全性と潜在的な健康上の利点、および今後の研究と応用について包括的に検討することであった。
対象となったトピックは、代謝、安全性と許容可能な摂取量、食事への暴露、血糖値やインスリン濃度への影響、エネルギー摂取量と体重管理、血圧、虫歯、自然性と加工、味と感覚特性、規制状況、消費者の洞察、市場動向などであった。ステビアに関するデータは、エネルギー摂取量や体重管理、腸内マイクロバイオームに関するデータと同様に限られているため、シンポジウムではLNCSに関するより広範な文献がレビューされたため、本レビューにも含まれている。
ステビア、ステビオール配糖体、ADI、EDI、糖尿病、肥満、味覚、代謝、安全性
序論
ステビアrebaudianaベルトーニは、パラグアイ、ブラジル、アルゼンチンに自生するキク科(Compositae)の小さな多年草である。この植物の葉は、薬やマテ、緑のハーブティー(1-3)などの飲み物を甘くするために何世紀にもわたって先住民によって使用されている。植物は、最初にパラグアイのインディアン(1,3)からその特性を学んだ1887年に植物学者モイセスサンティアゴベルトーニによって世界の残りの部分の注意を持って来た。ステビアの独特の甘味の原因となるステビオール配糖体として知られる植物の天然成分の化学的特徴は、1931年に2人のフランス人化学者ブリデルとラビエルがステビアの葉から一次ステビオール配糖体であるステビオシドを単離したときまで特定されなかった(1)。日本は、1970年代にS. rebaudianaの粗精製されていない抽出物を大規模に商業化して使用した最初の国である(2)。その後、その利用はアジアやラテンアメリカの数カ国に広がっていった(4)。1990年代には、ステビア抽出物は健康食品店で栄養補助食品として米国で入手できるようになったが、初期の製剤は甘草の風味があり、甘味や苦味のある後味があることが知られていたため、その普及には限界があった(2, 5)。粗抽出物に含まれる精油、タンニン、フラボノイドの存在が、味の悪さの一端を担っていたため、抽出物を精製し、ステビオール配糖体を化学的に特徴づける努力がなされた(5)。
ステビオシドの単離後、ステビアの葉からリバウディオシド(Reb)A, B, C, D, E, およびダルコシドAなどの他のステビオール配糖体が同定され、単離された(6)。一般的に、ステビアの葉に最も豊富に含まれるステビオール配糖体は、ステビオシド(4-13% wt:wt)レバウディオシドA(2-4%)およびレバウディオシドC(1-2% wt:wt)である(7, 8)。今日までに、40以上のステビオール配糖体が同定されている(例えば、Reb F、G、H、I、J、K、L、M、N、O、およびQ;ステビオシドA、D、およびEなど)(9-12)。植物由来のステビオール配糖体のほとんどは、ステビオールとして知られる13-ヒドロキシ-エン-カウル-16-エン-19-オイ酸をバックボーンとする4環状ジテルペンである(1,12)。様々な配糖体は、アグリコンステビオールのR1(OH)とR2(H)の位置に取り付けられた単糖の数とタイプが異なるだけである。グルコース、フルクトース、ラムノース、キシロース、およびデオキシグルコースは、ステビオール背骨に付着している糖の例である(12)。2つの一次ステビオール配糖体、ステビオシドおよびReb Aは、R1で1つのグルコース部位によってのみ異なる;ステビオシドは2つのグルコース分子を有するのに対し、Reb Aは3つのグルコース分子を有する。
ステビアは現在、アルゼンチン、ブラジル、コロンビア、パラグアイ、中国、日本、マレーシア、韓国、ベトナム、イスラエル、オーストラリア、ケニア、米国で商業的に栽培されている。高純度のステビオール配糖体は、世界中のすべての主要な規制当局によって甘味料として承認されており、150カ国以上で食品や飲料への使用が承認または採用されている。Reb Aは、市場で発売された最初の商業的なステビオール配糖体でした(13)。
ステビオール配糖体の代謝
ステビオール配糖体の吸収、代謝、排泄については、欧州食品安全局(EFSA)(14)最近ではMagnusonら(15)など、複数の科学的権威や専門家によって広範囲に検討されている。ステビオール配糖体は上部消化管で未消化である。それらは、グリコシド結合を切断して糖鎖を除去し、全身的に吸収され、肝臓でグルクロン酸化され、ヒトでは尿を介して、ラットでは糞便を介して排泄されるステビオール骨格を残して、大腸内の微生物と接触したときにのみ、加水分解または分解される(15)。
試験管内試験研究では、ヒトの唾液、唾液α-アミラーゼ、ペプシン、パンクレアチン、膵臓α-アミラーゼ、およびマウス、ラット、ハムスターの空腸ブラシ境界酵素は、ステビオシドに存在するグリコシド結合を加水分解することができないことが示されている(16)。しかし、ヒト、げっ歯類、ハムスターの腸内微生物は、ステビオシドをステビオールに分解することができる(16)。ステビオシドとReb Aをヒトの糞便微生物とインキュベートすると、両者はそれぞれ10時間と24時間でステビオールに完全に加水分解されることが示された(4, 17)。放出された糖分は吸収されず、エネルギー源として腸内微生物によって迅速に利用される可能性が高いため、ゼロカロリーの甘味料となる(2)。腸管バリアの試験管内試験モデルでは、単分子膜を介したステビオシドとReb Aの輸送が非常に低いのに対し、ステビオールの吸収性輸送は高いことが示されており、ステビオールは腸内微生物によって代謝されず、腸から吸収されることが示唆されている(18)。バクテロイデス種は、そのβ-グルコシダーゼ活性を介して腸内でのステビオール配糖体の加水分解に主に関与している(17)。
試験管内試験での調査からの証拠は、血漿中のグリコシドの検出可能な存在を示さなかったヒトの代謝研究と一致しており、腸からの取り込みがなく、尿や糞中のステビオシドまたはReb Aはほとんどまたは全くないことを示唆している(19-22)。これらの研究はまた、ステビオールは速やかに吸収され、肝臓に運ばれ、そこでグルクロン酸と共役してステビオールグルクロニドを形成し、ヒトでは尿中に排泄されることを示している(19-22)。図1は、ヒトにおけるステビオール配糖体の吸収、代謝、排泄経路をまとめたものである。
図1
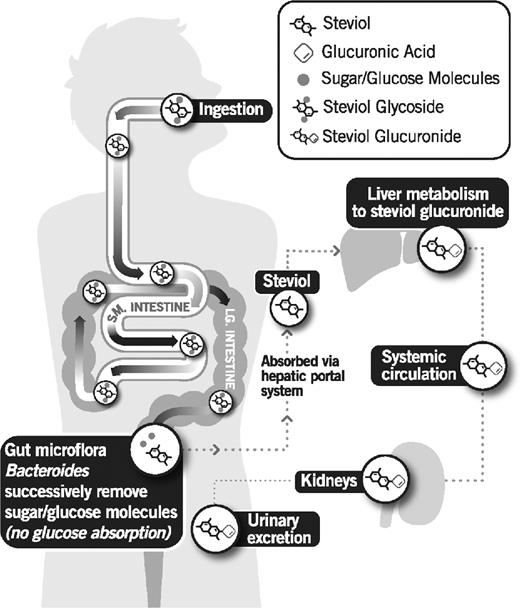
Wheelerら(21)は、健康な成人におけるステビオシドとReb Aの薬物動態および代謝を72時間にわたって比較した。血漿中濃度のピークはステビオシドとReb Aでそれぞれ8時間と12時間に発生し、半減期(t1/2)は両者とも14~16時間であった。Reb Aを摂取した場合、ステビオシド摂取後(62%)と比較して、ステビオールグルクロニド濃度(59%)が有意に低下した。ステビオールのグルクロニド濃度の違いは,Reb Aと比較して構造が単純であり,ステビオシドの細菌分解が速いことに起因していると考えられた。薬物動態解析の結果、ステビオシドとReb Aはヒトにおいて同様の代謝・排泄過程を経ることが示された。
ステビオールの配糖体代謝に関する先行研究のほとんどは、Reb Aまたはステビオシド(別名:一次配糖体または主要配糖体)を対象としていた。しかし、いくつかのステビオール配糖体の微生物代謝の類似性は、プールされた健康な男性と女性のアジア人と白人被験者のヒト糞便ホモジネートの試験管内試験研究で確認された(12,23)。異なる糖部位(グルコース、ラムノース、キシロース、フルクトース、およびデオキシグルコース)と異なる連結型[αβ(1-2)β-1,β(1-2)β(1-3)およびβ(1-6)]を含むReb A、B、C、D、E、F、およびM;ダルコシドA(別名:マイナーグリコシド);およびステビオールビオシド(中間代謝物)は、すべて24~48時間以内にステビオールに分解された。被験者の男女間や民族間での違いは認められなかった。これらのデータは、異なるステビオール配糖体がReb Aと同様の加水分解速度を有していることを示唆しており、したがって、Reb Aと同様のステビオール吸収速度、代謝および薬物動態を有することが期待される。これらのデータは、メジャーとマイナーの両方のステビオール配糖体が共通の代謝運命を共有しているように見えることを示している。
ステビオール配糖体の安全性と1日の許容摂取量
数多くの毒性学的、生物学的、臨床研究から得られたステビオール配糖体の安全性は、いくつかの出版物でレビューされている(2, 7, 14, 25, 26)。このレビューの「規制状況」のセクションで説明したように、すべての主要な世界的な科学・規制機関は、高純度のステビオール配糖体を一般の人々が消費しても安全であると判断している。規制当局の承認の大部分は、高純度(95%以上)のステビオール配糖体に関係している。ステビアの未精製の粗抽出物は、動物の繁殖力に悪影響を及ぼすことが報告されている(27, 28)が、食品や飲料への使用が承認されているよく特徴づけられた高純度のステビオール配糖体では観察されていない。したがって、粗抽出物を用いて実施された研究は、知識のある科学専門家や規制当局によって、高純度ステビオール配糖体の安全性評価には関係がないと判断されている。
高純度ステビオール配糖体の急性・長期毒性、生殖・発達毒性、発がん性に対する潜在的な影響は、主にげっ歯類を用いて研究されているが、他の動物モデルでも研究されている(29-34)。ステビオール配糖体は、主にヒトではステビオールグルクロニドとして尿中に排泄されるが、ラットでは遊離ステビオールとステビオールグルクロニドは主に胆汁を介して糞便中に排泄され、尿中には3%未満が現れる(2, 35)。この種間の違いは、ラットの胆道排泄の分子量閾値がヒトよりも低いことに起因している(2)。ステビオール配糖体の排泄経路はヒトとラットで異なるが、2 種間では代謝や薬物動態が類似しているため、これは毒性学的には重要ではない(2)。つまり、両種ともステビオール配糖体を摂取した後、体内の大部分の組織や細胞は同程度の濃度の同一代謝物に同程度の時間さらされているため、最終的な排泄経路が異なっていても、毒性学的影響の発現の可能性は同じであると考えられる。したがって、ラットは、ステビオール配糖体の消費の安全性を評価するための適切な試験動物であり、ラットの研究から生成された毒性学的データは、ヒトに適用される(2)。
許容一日摂取量(ADI)とは、ある個人が生涯にわたって、健康上のリスクを評価することなく毎日摂取できる物質の量のことである。これは、毒性試験の結果に基づいて規制機関によって設定されている。NOAEL(No Observed Adverse Effect Level)とは、長期試験において有害な毒性学的影響が認められなかった動物に与えられた最高用量のことで、ADIの基準とされている。NOAELは、ADIが小児などのサブグループを含むすべての潜在的な消費者にとって安全であることを保証するために、種内および種間の違いを考慮して安全係数(通常100)で割られている。ステビオール配糖体の現在の ADI は、ステビオシド(純度 95.6%)をラットの食事の 0%、2.5%、5%の濃度で 2 年間試験し,0,970,2387 mg・kg-1・d-1(36)の摂取量を得た毒性と発がん性の研究に基づいている。この研究では、生理学(体重、食物消費量、最終臓器重量)、行動、眼科、生化学(血液化学、血液学、尿分析、肝酵素)、組織学的変化への影響を評価した。試験したすべての用量において、ステビオシドは癌の発生に影響を及ぼさなかった。ステビオシドを食事の2.5%以下で与えたラットでは、副作用は観察されなかった。最高用量(食事の5%)では、腎臓、体重、生存率に変化が観察された。したがって、本試験のNOAELは飼料の2.5%、970 mg・kg-1・d-1であり、ステビオール当量(SE)に換算すると383 mg・SEs・kg-1・d-1となる。
383 mg SEs に 100 倍の安全率を適用すると、ADI は 0-4 mg SEs ⋅kg-1 ⋅d-1 となる。すべてのステビオール配糖体はステビオールに代謝されるため、ADIはすべてのステビオール配糖体に適用することができるので、ADIはSEで表される。ステビオール配糖体は、構造および分子量が異なり、したがって、ステビオール配糖体1グラムあたりのステビオールの量が相対的に異なることに寄与する。したがって、Reb AのADIは12mg・kg-1・d-1,ステビオシドのADIは10mg・kg-1・d-1となり、ステビオシドのADIは10mg・kg-1・d-1となる。
妊婦や子供が摂取するステビオール配糖体の安全性を確立した重要な研究は、Reb A (純度97%以上)の生殖・発達研究です(31)。ラットに2273 mg・kg-1・d-1以下のReb Aを2世代にわたって給与し、体重、食物摂取量、成長と発育、生存、生殖能力、性成熟をモニターした。最高用量では、どの世代においても生殖・発育に有害な影響は認められなかった。同様の結果は、精製ステビオシドを用いた生殖毒性試験でも報告されている(29, 37)。rebaudiana の粗抽出物を用いたラットを対象とした初期の研究では、対照(28)と比較して、受胎能力の低下(27)または精液小胞重量の低下が観察されたが、高純度ステビオール配糖体抽出物を用いた研究(31,36,37)では、性器、性ホルモンのレベル、交尾行動、受胎可能性、妊娠期間、子孫の生存率、または性的成熟度への負の影響は観察されなかった。授乳中、授乳中、および2世代のための成人への子孫の成長と発達全体の前と妊娠と妊娠の重要な期間中に高純度のステビオール配糖体の高用量への暴露後の悪影響の欠如は、確立されたADI以下で妊婦や子供による消費のためのステビオール配糖体の安全性を示している。
ステビオール配糖体は突然変異原性がないという安全性の専門家による広範なレビューと結論にもかかわらず、2つの出版物は、ステビオール配糖体の遺伝毒性の可能性について十分な試験が行われているかどうかを疑問視している(38, 39)。彼らの懸念に応えて、Urbanら(40)は、発表されたすべての試験管内試験および生体内試験研究の包括的かつ広範なレビューを実施した。懸念の多くは、非常に特異的な細菌株である Salmonella typhimurium TM677 を用いたステビオールの突然変異原性が報告されているいくつかの古い試験管内試験研究に由来していたが、これはヒトには適用できない生育条件を必要とする。Urbanら(40)によるレビューでは、Reb Aとステビオールについては一貫して陰性であり、ステビオシドについては1つの研究を除いてすべて陰性であることが示されている。Nunesら(41)による生体内試験研究は陽性であったが、その方法およびデータ解釈について、複数のレビュアーによって批判されている(20, 40, 42, 43)。そこで、Urbanら(40)は、ステビオール配糖体に関する試験管内試験および生体内試験研究のデータベースは、ステビオール配糖体が遺伝毒性を有するという証拠がなく、堅牢であると結論付けている。
試験管内試験および動物試験に加えて、ヒトの安全性試験も実施されている。Reb Aの1000 mg/d以下の用量を1~4カ月間、ステビオシドの750 mg/dを3カ月間投与しても、健常者、高血圧患者、1型および2型糖尿病患者を対象に、血圧や空腹時血糖値に悪影響を及ぼすことはなかった(44-46)。また、血清化学、血液学、尿分析においても臨床的に有意な変化は認められなかった。安全性試験のほとんどは、Reb Aとステビオシドについて行われてきたが、それは、これらがS. rebaudiana Bertoni植物に最も多く含まれるステビオール配糖体であるからである。しかし、すべての主要なステビオール配糖体およびマイナーなステビオール配糖体は、ヒトの微生物によってステビオールに分解されるため、同じ代謝運命を共有している。ヒトの糞便ホモジネートを用いた一連の試験管内試験試験では、マイナーなステビオール配糖体-Reb B、C、D、E、F、およびM、ダルコシドA、およびステビオールビオシド(12,23)のいくつかについてこれを確認した-そのため、Reb Aとステビオシドに関する研究は、同様にマイナーなステビオール配糖体にも適用できるようになる。
いくつかによって提起された別の懸念は、一部の個人で過敏症を誘発することができる植物(例えば、ラグウィード、ゴールデンロッド、菊、エキナセア、カモミール、レタス、ヒマワリ、およびチコリ)とステビア植物の共通の分類学に起因するステビオールグリコシドのアレルゲン性の可能性である。包括的な文献検索では、精製されたステビオール配糖体のアレルゲン性の可能性を示す証拠は見つからなかった(47)。Urbanら(47)によると、文献で報告されているアレルギー反応のいくつかのケースは、市場に高純度のステビオール配糖体が導入される前に発生した。同様に、高純度ステビオール配糖体を用いたヒトの研究では、膨満感、ガス、下痢、吐き気、またはborborygmus(44-46)などの否定的な胃腸の副作用は報告されていない。
全体的に、高純度ステビオール配糖体の安全性データは徹底的に評価されており、植物ベースの、ゼロカロリー甘味料としての使用は、世界中で承認されている。それは結論的に高純度のステビアの葉のエキスの甘味料(すなわち、ステビオール配糖体)の承認された量を含む食品や飲料は、子供、妊娠中および授乳中の女性、および糖尿病を持つ個人を含むすべての個人のために安全であることが決定された。
食事暴露
消費の安全性を確保するために、食品添加物の推定一日摂取量(EDI)はADIを超えてはならない。そのため、使用が承認される前に、食品消費調査からの情報と一緒に、様々な食品カテゴリーでの食品使用レベルの提案を使用して、潜在的な摂取量を推定している。ステビオール配糖体の EDI は、様々な集団について推定されている(表1
)。ほとんどの場合、ステビオール配糖体のEDIはADIよりも低く、それらが評価されている保守的な性質のため、推定摂取量は一般的に実際の消費者の摂取量または平均的な消費者の摂取量を過大評価していると認識されている。
表1 高純度ステビオール配糖体の1日の推定摂取量1
| 推定摂取量、mg SE・kg −1・d −1 | ||||
|---|---|---|---|---|
| 研究、年(参照) | 人口 | 平均摂取量 | 最大または高摂取量 | 推定方法 |
| JECFA、2006(52) | ヨーロッパ | NR | 3.5 | 相対的な甘さのために200:1の係数を使用して、SGで置き換えられた食品として、または食品として使用されるすべての食用糖。非常に控えめな見積もり |
| 極東 | NR | 1.6 | ||
| 中東 | NR | 3.2 | ||
| アフリカ | NR | 1.3 | ||
| ラテンアメリカ | NR | 3.5 | ||
| 日本 | NR | 3 | ||
| 米国 | NR | 5 | ||
| レンウィック、2008(53)2 | 大人 | 0.4 | 1.1 | 北米、ヨーロッパ、オーストラリアで実施された調査からのLNCS消費量に基づいたRebAの推定食事曝露。LNCSユーザーのみ。高摂取量、90パーセンタイル |
| 糖尿病の成人 | 0.5 | 1.5 | ||
| 子供達 | 0.7 | 1.7 | ||
| 糖尿病の子供たち | 1.1 | 1.5 | ||
| FSANZ、2011(54) | オーストラリア、ニュージーランド、すべて | <2.4 3 | <2.4 3 | 最大レベルで幅広い食品グループの30%の市場シェア。高摂取量、90パーセンタイル |
| オーストラリア:2〜6年 | NA | 4.4 4 | 水ベースのフレーバードリンクのブランドロイヤルティ消費者 | |
| ニュージーランド:5〜14年 | NA | 4 5 | ||
| オーストラリア:2〜6年 | 2.2 6 | 4 5 | フレーバーミルク製品のブランドロイヤルティ消費者。 | |
| カナダ保健省、2012(55) | 全人口 | 0.01 | NR | 方法1:代表的な食品消費データを使用して卓上甘味料の提案レベルを使用しました。高摂取量、90パーセンタイル |
| 卓上用甘味料ユーザー、すべて | 0.2 | 0.3 | ||
| 卓上用甘味料の使用者、3〜11歳の子供 | NR | 1.3 7 | ||
| 子供、1〜3歳 | 0.5〜2.1 | 4.2 8 | 方法2:食品消費データを使用して、すべて/特定の食品カテゴリで提案された最大値を使用しました。高摂取量、95パーセンタイル | |
| 子供、4〜8歳 | NR | 4.1 8 | ||
| 子供、1〜3歳 | NR | 4.9 9 | ||
| EFSA、2014(56) | 幼児、12〜36か月 | 0.6〜2.4 | 2.0〜4.3 10 | ヨーロッパの消費データベース、17カ国からの26の食事調査。各食品カテゴリーに認可された使用のMPL。高摂取量、95パーセンタイル |
| 子供、3〜9歳 | 0.5〜1.8 | 1.3〜3.9 | ||
| 青年、10〜17歳 | 0.2〜0.7 | 0.6〜1.8 | ||
| 成人、18〜64歳 | 0.1〜1.0 | 0.4〜2.2 | ||
| 成人、65歳以上 | 0.1〜0.4 | 0.3〜1.3 | ||
| 米国FDA、2016(57) | 大人 | 0.16〜0.85 | 0.43〜2.24 | レンウィックと同じ方法論(53) |
| 糖尿病の成人 | 0.18〜0.93 | 0.57〜2.97 | ||
| 子供達 | 0.27〜1.41 | 0.63〜3.28 | ||
| 非糖尿病の子供 | 0.43〜2.23 | 0.57〜3.01 | ||
| Dewinter et al。、2016(58)ベルギー | 子供、4〜6歳 | 1.32 | 4.75 11 | 1型糖尿病の子供-ティア2:実際の食品消費量と食品カテゴリーのMPLに基づく最大濃度。高摂取量、95パーセンタイル |
| 子供、7〜12歳 | 0.90 | 2.88 | ||
| 子供、13〜18歳 | 0.63 | 2.54 | ||
| 子供、4〜6歳 | 1.32 | 4.75 11 | 1型糖尿病の子供-ティア3:実際の食品消費量に基づく最大濃度と食品カテゴリーのLNCSの平均濃度。SGの実際のデータが不足しているため、MPLが使用されました。高摂取量、95パーセンタイル | |
| 子供、7〜12歳 | 0.93 | 2.89 | ||
| 子供、13〜18歳 | 0.67 | 2.54 | ||
- ADI, Acceptable Daily Intake; EFSA, European Food Safety Authority; FSANZ, Food Standards Australia New Zealand; JECFA, FAO/WHO Joint Expert Committee on Food Additives; LNCS, Low and no-calie sweetener; MPL, maximum permitted level; NA, not applicable; NR, not reported; Reb, rebaudioside; SE, steviol equivalent; SG, steviol glycosides.
- Reb Aの摂取量から計算。Reb Aからステビオール当量への換算係数は0.33。
- ADIの60%未満から計算した。
- ADIの110%未満から計算した。
- ADIの100%から計算している。
- ADIの55%から計算した。
- 甘味料の消費量が得られなかったため、平均摂取量を2倍にして推定した。
- すべての食品カテゴリー。
- 飲料、ミックス、濃縮物。
- 1カ国(オランダ)を除き、すべての国で摂取量がADIを下回っていた。
- この年齢層では9人のみ。
調査は、高純度ステビオール配糖体の一日の消費量の推定値を決定するために、様々な世界的な管轄区域で利用されてきた。FAO/WHOの食品添加物に関する合同専門家委員会(JECFA)は、ショ糖に対するステビオール配糖体の相対的な甘さに基づいて、ステビオール配糖体が食品に使用されている、または食品として使用されているすべての甘味料に取って代わ ると仮定したモデルを使用して、国際的な食生活暴露の推定値を評価した(52)。委員会は、1.3-5 mgのSEs・kg-1・d-1の最大摂取量を世界的に推定した。しかし、委員会はこれらの推定値は非常に保守的であり、実際の摂取量はこれらの値の 20-30%である可能性が高いと指摘している(52)。Renwick (53)は、北米、オーストラリア、ヨーロッパの既存の低カロリー・無カロリー甘味料(LNCS)消費量調査に基づいた等価摂取量計算を用いて、成人、小児、糖尿病児のReb A摂取量を推定した。一般人の平均摂取量は0.4~0.7mg SEs・kg-1・d-1,大人と子供の平均摂取量は1.1~1.7mg SEs・kg-1・d-1となっている。
2011 年、オーストラリア・ニュージーランド食品基準局(FSANZ)は、ステビオール配糖体の承認拡大のための審査の中で、3 つの食生活暴露評価モデル(市場シェア 30%のシナリオと 2 つの「ブランドロイヤ ル」シナリオ)を検討した(54)。ブランドロイヤル・シナリオの90%の食餌曝露は、2~6歳のオーストラリアの子供のADIの110%、5~14歳のニュージーランドの子供のADIの100%であったが、FSANZは、3つのモデルすべてが過大評価である可能性が高いと結論付けた。カナダ保健省(55)は2012年の暴露評価で2つのアプローチを用いている。方法1は、すべての卓上甘味料を代用し、方法2は、すべての食品カテゴリで最大認可された使用を想定していた。両方のアプローチは、よくADIを下回っていた平均摂取量をもたらした。最大使用レベル(95パーセンタイル)は、わずかに1-3と4-8 Y歳の子供のためのADIを超えたが、カナダ保健省は、健康の観点から、これらの推定値は取るに足らないと考えられている。
2014,欧州委員会からの要請を受けて、EFSAはステビオール配糖体(E 960)の暴露評価を2010年と2011年に実施したものに修正した(56)。EFSAパネルは、1カ国(オランダ)の幼児を除いて、すべての集団において平均曝露量がADIである4mg SEs・kg-1・d-1を下回っていると結論付けたが、この点については考慮しなかった。しかし、パネルはこれを安全性評価の結果を変えるほどの有意性とは考えていなかった。2016 年に米国で行われた再評価では、米国の一般人口におけるステビオール配糖体の推定摂取量は ADI を下回ってた(57)。最も摂取量が多かったのは糖尿病ではない子供で、95パーセンタイルで3.28 mg SEs ⋅kg-1 ⋅d-1の摂取量でした。Dewinterら(58)は、糖質/糖質を減らした食事を管理しようとする努力の中で、砂糖代替品の消費量が多いため、甘味料のADIを超えるリスクが最も高い1型糖尿病の子供の摂取量を推定している。95 パーセンタイルでは、すべての年齢層は、4.75 mg SEs ⋅kg-1 ⋅d-1 で ADI を超えた 4 ~ 6 歳児を除いて、ADI 以下の摂取量を持ってた。今回の解析は保守的な内容であったため、1型糖尿病の子供がADIを超える可能性は低いと結論づけている。これまでのところ、世界の様々な国や地域での推定食生活暴露評価に基づき、ステビオール配糖体を含む食品や飲料の典型的な消費パターンでは、糖尿病の成人や子供を含めて、成人も子供もステビオール配糖体のADIを超える可能性は低いと考えられている。安全性の懸念はないが、今後の研究では、成人、小児、およびステビオール配糖体の高消費者と予想される集団のサブセットにおける実際の食事摂取量を調査し、経時的な傾向を把握することは貴重なことであろう。
ステビオール配糖体の健康への影響と関連バイオマーカー
背景
WHOの新しい糖質ガイドラインは、成人と子供が総エネルギー摂取量の10%未満にまで添加糖質の摂取量を減らすことを推奨し、さらに健康上の利点を得るために5%未満にまで減らすことを推奨している(59)。このガイドラインは、2025年までに糖尿病、肥満、早死に25%の増加に歯止めをかけるというWHOの取り組みの一環である(59)。また、英国の栄養科学諮問委員会は、遊離糖を5%以下に減らすことを推奨している(60)。成人の場合、10%と5%のガイドラインは、それぞれ約50と25gの砂糖/dに相当する。WHOの推計によると、成人の糖分摂取量は、ハンガリーとノルウェーでは総エネルギーの7~8%、スペインとイギリスでは16~17%となっている(59)。子供の場合はさらに高く、デンマーク、スロベニア、スウェーデンでは 12%から、ポルトガルでは 25%近くになる(59)。米国では、糖質添加物の摂取量は減少しているが、依然として高く 2011-2012年には成人と2-18歳の子供と青年がそれぞれ総エネルギー摂取量の14%と17%を消費している(61)。これらの量は、他のいくつかの国と同様に、米国で推奨されている総エネルギーの10%を超えている(62)。
食後血糖値とインスリンの効果
ショ糖やグルコースの摂取が食後の血中グルコースとインスリン濃度の上昇をもたらすことはよく知られている(63)。したがって、高純度のステビオール配糖体が食後の血中グルコースおよびインスリン濃度に影響を与えるかどうかを決定することは興味深いことである。いくつかのヒトの研究では、ステビオール配糖体を用いた低糖質/カロリーの食事と完全糖質/カロリーの食事を比較した単一の食事評価でこの効果を調べているが、他の研究では、食事操作を行わずにサプリメントとしてカプセルに入れたステビオール配糖体の効果を調べている(表2)。3つの無作為化比較試験では、健康な被験者と糖尿病患者を対象に、精製ステビオール配糖体を低糖質/カロリーの食事(64,65)またはサプリメント(66)の形態で使用した場合、食後血糖値の有意な低下が観察された。Antonら(64)は、除脂肪および肥満の被験者において、ショ糖と比較して、ステビアを中朝の食事で摂取した場合、食後血糖値(P < 0.01)およびインスリン濃度(P < 0.05)の有意な低下を観察した。同様に、Jeppesenら(65)は、2型糖尿病の被験者において、食後血糖値のAUCが156%低下した(P < 0.01)など、食後血糖値の有意な低下(P < 0.05)を指摘した。Gregersenら(66)は、試験前に血糖降下薬の服用を中止していた2型糖尿病患者12人の食後効果を、カプセル状のトウモロコシデンプンプラセボ(1000mg)とアイソコロリックミールを併用して投与した場合と比較して、1000mgのステビオール配糖体(91%ステビオシド)の食後効果を調査した。試験群間に糖質、炭水化物、またはカロリーの差がなかったにもかかわらず、ステビオシドは、プラセボと比較して、グルコースのAUC(P < 0.02)に加えて、食後血糖値を18%(P < 0.004)有意に低下させた。ステビオシドをプラセボと比較して摂取した場合、インスリン反応(AUC)が増加し、インスリン原性指数(AUCインスリンとAUCグルコースの比)が40%増加する傾向があった(P < 0.001)。
表2 単食試験における高純度ステビオール配糖体の食後血糖値およびインスリンに対する効果1
| 研究、年(参照) | 被験者、n | 研究デザイン | 治療、mg / d | コントロール、g / d | カロリー差、2 kcal | 血糖値 | 血中インスリン |
|---|---|---|---|---|---|---|---|
| アントン他、2010(64) | 31人の痩せた肥満の成人、正常なBG | RCT、CO | NR、ステビア | 62、ショ糖 | 203 | ↓ | ↓ |
| Jeppesen、2014(65) | 12型2糖尿病3 | RCT、CO | 150、ステビオシド | 55、ショ糖 | 223 | ↓ | NR |
| Gregersen et al。、2004(66) | 12型2糖尿病3 | RCT、CO | 1000、91%ステビオシド | 1、コーンスターチ | 0 | ↓ | ↑(P = 0.08); ↑インスリン産生指数 |
| Jeppesen etal。2006(67) | 55型2糖尿病3 | RCT、PL、3カ月、SMT試験終了 | 500、ステビオシド | 0.5、トウモロコシ澱粉 | 0 | NS | ↓(プラセボ) |
| RCT、PL、3カ月、IVGTT試験終了 | 0 | NS | ↑ | ||||
| Guens et al。、2007(20) | 大人9名、通常のBG | FS、3 d、SMT研究終了 | 750(ステビオシドカプセル) | 水 | 0 | NS | NR |
| マキ他、2009(68) | 大人45名、通常のBG | RCT、CO | 500、750、1000(Reb Aカプセル) | プラセボカプセル | NR | NS | NS |
| 48型2型糖尿病患者 | NR | NS | NS |
- BG、血糖値;CO、クロスオーバー;FS、固定配列;IVGTT、静脈内耐糖能試験;NR、報告なし;PL、パラレル;RCT、無作為化比較試験;Reb、レバウディオシド;SMT、単食試験;↓、有意な減少(P<0.05);↑、有意な増加(P<0.05)。
- ステビオール配糖体投与群と対照群のカロリー差を示し、ステビオール配糖体投与群は糖質/カロリーを低下させた。
- 被験者は血糖降下薬の服用を中止した。
他の3つの研究(20, 67, 68)では、ステビオ配糖体をサプリメントとして摂取した場合、健常者または糖尿病患者の食後血糖値に有意な影響は観察されなかった。しかし、Jeppesenら(67)は、プラセボ群では45%のインスリン反応の低下(P<0.05)を観察し、ステビオール配糖体群ではインスリン濃度が維持されたことから、ステビオール配糖体が2型糖尿病患者のβ細胞機能に好影響を与える可能性が示唆された。静脈内耐糖能試験では、ステビオシド群ではプラセボ群と比較して、ブドウ糖注射後のインスリン反応が21%増加した(P < 0.05)。この研究に含まれていた患者は、すでに糖尿病の後期段階にあったため、β細胞機能が制限されていた可能性があり、これが他のヒトおよび動物の研究と比較した結果の違いを説明している可能性がある。
全体的に、ステビオール配糖体と対照との比較が糖/炭水化物またはカロリーの差を伴う場合、食後血糖値の低下が観察されており、この効果は、Jeppesen(65)およびAntonら(64)の研究で観察されたように、主に糖とカロリーの置換によるものである。一方、治療薬と対照薬の間にカロリー差がなかったGregersenら(66)の研究で観察された食後血糖値の低下は、特定の用量では、ステビオシドが糖尿病患者において潜在的な血糖値低下効果を有する可能性があることを示唆している。これらの結果は、Makiら(68)の研究のように、血糖降下薬の服用を継続している糖尿病患者では明らかではないかもしれない。同様に、Makiら(68)の研究では食後のインスリン濃度に変化は見られなかったが、糖尿病患者が血糖降下薬の服用を中止した研究では、インスリン濃度が上昇する可能性があるという証拠があった(66,67)。ステビオール配糖体が糖尿病患者のインスリン濃度と食後血糖濃度に独立した効果を持つかどうか、それが1つのステビオール配糖体に特異的であるかどうか、また、これらの効果が観察されるメカニズムと用量をより明確に決定するためには、追加の研究が必要である。
空腹時血糖値とインスリン効果
長期的な研究では、食事の炭水化物やカロリー操作を行わない介入の中で、サプリメントの形で高純度のステビオール配糖体を摂取しても、空腹時血糖値、インスリン値、または糖化ヘモグロビン(HbA1c)濃度を有意に低下させないことが示されている(補足表1)。研究は、健康な被験者、1型および2型糖尿病を有する被験者、ならびに高脂血症および高血圧の被験者を対象に、幅広い投与量で実施された(20,45,46,67,69-71)。これらの研究では、糖尿病患者を対象としたプロトコルが異なっており、ある者は血糖降下薬を継続し、ある者は研究開始直前に中止していた。空腹時血糖測定値はいずれもステビオール配糖体治療によって有意な変化はなかったが、注目すべきは、1件の研究では、750mgのステビオシド/dが3-mo期間にわたって空腹時血糖濃度を維持したのに対し、プラセボ群では血糖降下薬を継続した1型糖尿病患者ではベースラインと比較して有意な上昇がみられたことである(46)。Jeppesenら(67)の研究でも同様の結果が観察されており、血糖降下薬を中止した2型糖尿病患者にステビオシド1500mg/日を3カ月間摂取させた。空腹時血糖値(P < 0.007)およびHbA1c(P < 0.01)について、治療群とプラセボ群の間に有意な差が認められた。これらの知見は、ADI以上のレベルのステビオシドが糖尿病の静止状態を維持するのに役立つ可能性を示唆しており、糖尿病患者にとっては、糖尿病の進行を最小限に抑えたり、遅らせたりする上で有益である可能性がある。さらに、OnakpoyaとHeneghan(72)によるこれらの研究のいくつかのメタアナリシスは、空腹時血糖値の小さいが有意な減少を示した(-0.63 mmol/L; P < 0.00001)。しかし、メタアナリシスで観察された0.63 mmol/Lの減少の臨床的関連性は限定的であるかもしれない。
JeppesenとLarsen(73)はまた、15人の男性サイクリストの筋肉のグリコーゲン再合成に対する等心性炭水化物の補充と比較して、運動後の経口炭水化物と一緒に、500 mgのステビオール配糖体を補充することの効果を検討した。グリコーゲン再合成率は35%増加し(P < 0.02)グリコーゲン濃度はプラセボと比較してステビオールグリコシドで有意に高かった(P < 0.009)。ステビオール配糖体がどのようにしてこれらの効果をもたらすのかを理解するためには、さらなる研究が必要である。
血糖値に関連する可能性のあるメカニズム
ステビオール配糖体や他のLNCSが食後血糖値を低下させる間接的な方法の1つは、ショ糖や他の炭水化物の置換を介したものであることは明らかである(74)。しかし、ステビオール配糖体については、いくつかの試験管内試験および動物実験で、主に糖尿病モデルにおけるインスリン分泌、シグナル伝達、および放出;主要遺伝子のアップレギュレーション;および強化されたグルコース吸収が関与する、潜在的な独立したより直接的なメカニズムが示唆されている。Jeppesenら(75)は、ステビオシドとステビオール(1 nmol/L~1 mmol/L)の両方が、グルコースの存在下でインキュベートしたマウス小島からのインスリン分泌を用量依存的に増強することを示した、我々の知る限りで初めての研究であった(P < 0.05)。ステビオシドおよびステビオールのインスリン分泌促進効果は、グルコース濃度に決定的に依存し、≥8.3 mmol glucose/L(P < 0.05)で発現した。ステビオシドおよびステビオールが膵臓β細胞に直接作用するかどうかを決定するために、β細胞株INS-1を使用した。ステビオシドとステビオールの両方がINS-1細胞からのインスリン分泌を増強した(P < 0.05)。
ステビオール配糖体の動物研究は、インスリン分泌および感受性およびグルコネクシスに対する効果を示唆している。Jeppesenら(76)は、2型糖尿病の後藤柿崎と健常者のWistarラットを対象に、ステビオール配糖体0.2g・kg-1・d-1の静脈内耐糖能試験を行った。糖尿病ラットでは、ステビオシドは血糖反応を有意に抑制し(増分 AUC、P < 0.05)インスリン反応を増加させた(増分 AUC、P < 0.05)。Chenら(77)は、ステビオシド0.5mg・kg-1・d-1を胃腸に投与したところ、正常ラットと糖尿病モデルラット2匹の血中グルコース濃度が用量依存的に低下し、インスリン分泌を促進するだけでなく、肝臓のグルコース新生に関与する酵素であるホスホエノールピルビン酸カルボキシキナーゼの濃度を低下させ、肝臓のグルコース新生を遅らせることを報告している。Nordentoftら(78)は、遺伝的に肥満の糖尿病KKAyマウスに20mg・kg-1・d-1・d-1を投与した9週間の介入試験で、ステビオシド誘導体イソステビオールが大腸からのバイオアベイラビリティーが高く、主要なインスリン調節遺伝子やインスリン転写因子の遺伝子発現をアップレギュレートすることで、グルコースとインスリン感受性が改善されることを観察している。Changら(79)は、果糖を多く含む飼料を4週間与えたラットに0.5mgのステビオシドを90分間単回経口投与すると、血漿中グルコース濃度が低下し、グルコース-インスリン指数(グルコース-インスリン指数)が逆転することを観察した。ステビオシドの反復投与は、これらのラットのインスリン抵抗性の発現を遅らせ、ストレプトゾトシン糖尿病ラットの外因性インスリンに対する反応を増加させた。Philippaertら(80)は、ステビオシド0.5mg・kg-1・d-1を耐糖能試験の2時間前に経口投与したところ、正常野生型マウスでは血中グルコース濃度が有意に低下したが、一過性受容体電位陽イオンチャネルサブファミリーMメンバー5(TRPM5)マウスでは低下しなかったことを示している。TRPM5は舌のII型味覚受容体細胞や膵臓のインスリン産生β細胞に存在するCa2+依存性のカチオンチャネルである。TRPM5ノックアウトマウスは、グルコース誘導性インスリン放出障害により耐糖能が低下している。
メタボリックシンドロームの転帰に関するReb Aの研究では、ステビオシドと同様の転帰が示唆されている。Jeppesen(81)はラットに高フルクトース食を16 wkにわたって与え、その後8.4mgのReb A/dと16.8mgのアスパルテームまたは高フルクトースコーンシロップ(HFCS)/dを総カロリー摂取量の13%で8 wkにわたって与えた。耐糖能試験後の増分AUCグルコースは、Reb A群がHFCS群と比較して有意に低かった(P<0.05)。HOMA-IRで測定したインスリン抵抗性(P < 0.005)および肝TG含量(P < 0.05)は、Reb A群およびアスパルテーム群で有意に低下した。また、肝臓における脂肪酸代謝遺伝子Srebf1の発現、肝臓および筋肉におけるFasの発現は、Reb A群でHFCS群と比較して有意に低かった(P < 0.001)。
全体的に、本研究は、ステビオール配糖体を食品、食事、または食事中の糖分やカロリーを減らしたり、代替したりするために使用した場合の血糖管理に対するステビオール配糖体の有益な効果を支持し、有害な影響はないことを示している。健常者および糖尿病患者を対象とした3カ月から1年間の長期安全性試験では、ステビオール配糖体は安全であり、1500mg/d以下の用量で空腹時血糖値、インスリン、およびHbA1cに対して中立的な効果があることが示されている。1つのメタアナリシスでは、空腹時血糖値の中程度の低下が示唆された。いくつかの長期研究で検討された用量は、ADIを十分に上回っていた。いくつかの前臨床研究および臨床研究では、糖尿病患者における食後血糖値の低下、インスリン分泌の増強、インスリン感受性の改善におけるステビオール配糖体の潜在的な独立した効果が示唆されており、これらの効果に関するいくつかの機序論的証拠が示されている。これらの知見を明らかにし、確認するためには、追加の臨床試験が必要である。
エネルギー摂取量と体重管理
食品および飲料中のカロリー甘味料をLNCSで完全に置換することにより、ほとんどまたは全く砂糖およびカロリーを含まない望ましい甘味を提供することができる。食事中の糖分を減少させるためのいくつかの最近の政策提言(59,62,82)を考慮すると、ステビオール配糖体を含むLCNCSは、食事中の糖分およびカロリーの両方を減少させるための簡単で効果的な方法を提供し、それによってまた、エネルギー摂取量および体重の両方を管理するのに有用な方法を提供する。
ステビオール配糖体
これまでに、2つの研究(64,83)が満腹感とエネルギー摂取量に対するステビオール配糖体の効果を評価している(表3)。Antonら(64)は、主観的な満腹感の増加は観察されなかったが、ステビオール配糖体を用いた2回の低エネルギー/スクロースプレロード食を昼食と夕食の20分前に摂取した場合、エネルギー摂取量が1日の間に有意に減少することを発見した。ステビオール配糖体を使用した場合の消費量は、ショ糖処理と比較して31人の被験者で309kcal減少した(P < 0.001)。昼食時と夕食時のエネルギー摂取量に差はなかった;したがって、1日のエネルギー差は、主に2つの前負荷のエネルギー差によるものであった。ステビオール配糖体投与期間中のエネルギー補填量は24%であった。2つ目の研究では、30人の男性を対象に、スクロースコントロールと比較して水で摂取したステビオール配糖体の効果を評価し、満腹感の評価に差は見られなかったが、1日の総エネルギー摂取量が70kcal減少したことを指摘した(83)。ステビオール配糖体期間中のエネルギー補償率は73%であった。この研究では、最初の研究よりも高いエネルギー補償率が得られたのは、異なるプリロードの数と使用、プリロードと自由食の間の時間間隔、およびTeyら(83)による研究では、エネルギー摂取量の違いを評価するための統計的な動力は与えられていなかったが、血糖値処理の30%の違いを検出するための動力は与えられていたという事実など、いくつかの要因に起因している可能性がある。2つの研究の平均エネルギー補償率は約50%で、他のLNCSで観察された平均エネルギー補償率に類似している(84)。
表3 高純度ステビオール配糖体が満腹感と食物摂取量に及ぼす影響1
| 研究、年(参照) | 総被験者数、n | 処理 | 研究デザイン | ポジティブコントロール | 満腹、空腹 | エネルギー摂取量の違い、kcal / d | 毎日のエネルギー補償、% |
|---|---|---|---|---|---|---|---|
| アントン他、2010(64) | 大人31名 | クリームチーズに含まれるステビオール配糖体は、昼食と夕食の20分前に自由に摂取しました。予圧、290 kcal | バランスの取れた予圧、CO | ショ糖プリロード、493 kcal | NS | −309 2 | 24 2 |
| Tey et al。、2017(83) | 30人の男性 | フレーバー水中の0.33gのステビオール配糖体は、自由な昼食の1時間前に消費されました。予圧、0 kcal | RCT、CO | ショ糖プリロード、260 kcal 2 | NS | −70 2 | 73 |
1CO、クロスオーバー;RCT、ランダム化比較試験。
2提供されたデータから算出。
LCNS
ステビオール配糖体の体重への影響に関する臨床試験が行われていないため、シンポジウムでは、ステビオール配糖体でも同様の効果が期待されることから、LNCSの摂取エネルギーと体重への影響について簡単なレビューを行った。研究では、エネルギー摂取量とエネルギー消費量の正確な生理的バランスは存在しないことが示されている。即時のエネルギー必要量の過不足にかかわらず、エネルギーの消費は、次の食事やその後の食事での摂取量の調整によって完全に補われない(85)。したがって、LNCSsの使用によるエネルギー摂取量の減少は、体重を維持または減量しようとする人に役立つはずである。これと矛盾しないように、1970年と2015年の間に人間の参加者における69の急性および長期ランダム化比較試験の最近のメタアナリシスは、食事中の(一部の)砂糖の代わりにLNCSsの消費がエネルギー摂取量と体重を減少させるという明確な証拠を発見した(84)。これらの知見にもかかわらず、クレームは、LNCSsはむしろ食欲と体重管理を助けるのではなく、妨げていることを主張している。
げっ歯類モデルに基づいて、1つの主張は、カロリー含有量から甘味を “デカップリング “することによって、LNCSは、エネルギー摂取量を調節するために動物の学習能力を混乱させることを示唆している(86,87)。これらの研究では、サッカリン甘味ヨーグルトを摂取したラットは、グルコース甘味ヨーグルトを摂取したラットと比較して、食物の摂取量を増加させ、体重増加および体脂肪蓄積の増加をもたらし、カロリー補償量を減少させた(86,87)。これらの研究の根底にある大前提は、甘い味はエネルギー摂取量増加の有効な予測因子であるということである。しかし、甘味は食品のエネルギー含有量を確実に予測するものではないため、これには疑問が残ることがある(88)。さらに、ラットやヒトがエネルギー摂取量をコントロールするために単純な味と栄養素の関係だけに頼っているのかどうかという疑問もある。腸内で検出された栄養素によって引き金となるシグナルが満腹感に影響を与える可能性が高い(85)。最近の研究では、以前の「デカップリング」の知見を再現することはできなかった。Boakesら(89, 90)は2つの実験で、グルコースを断続的に摂取させたラットの方が、サッカリンを断続的に摂取させたラットよりも、体重、脂肪量、またはその両方が増加したことを観察した。これは、Swithersら(86)によって報告された結果とは反対である。結果のこれらの2つのセットの間の不一致は、Swithersら(86)による研究では、サッカリンで甘くしたヨーグルトの低い受容性を示したラットを除外したという事実によって説明されるようである。Boakesら(90)は、サッカリンの受け入れは、チャウを与えた後の体重増加に関連付けられているため、これは、成長の早いラットに向かってサンプルを偏らせることを示した。言い換えれば、Swithersら(86)によって報告された結果は、LNCSs “あなたの体を混乱させる “主張をサポートするために広く引用され、手続き上のアーティファクトである。一方、Boakesら(89)の結果は、グルコース入りヨーグルトのより高いエネルギー含有量を完全に補えていないことによって説明できる。これは、LNCSへの連続暴露の動物研究68件中59件が有意な体重変化または体重減少を示さなかったシステマティックレビューで確認された(84)。
もう一つの主張は、甘味への反復暴露が「甘い歯」を促し、その結果、甘いエネルギーを含む食品や飲み物の摂取量が増加することを示唆している(91, 92)。この主張は最近の2つの研究で検証された。39人の参加者のサンプルでは、食事の前にLNCS飲料を摂取した場合、水を摂取した場合に比べて、アップルジュース、アップル、アップルパイを摂取したいという欲求が有意に減少した(P < 0.05)。2つ目の研究では、甘い飲み物の消費が甘いものと香ばしいものの摂取に及ぼす影響を試験した。3回に分けて、50人の参加者に、水、LNCSソーダ、または通常の甘味ソーダを摂取した後に、香ばしいスナック(ドリトス、フリトー・レイ)と甘いスナック(チョコレートチップクッキー)を提示した(93)。甘いおやつの摂取は、水と比較して、LNCSソーダ(P < 0.05)および通常のソーダ(P < 0.01)を摂取した後に有意に減少した。一方、甘いおやつの摂取は、甘味飲料の摂取では有意な影響を受けなかった。これらの結果は、最近食べた食べ物の好感度や報酬価値が、最近食べなかった食べ物や味と比較して低下する「感覚特異的満腹感」という現象と一致している(94,95)。これは、カロリー飲料をLNCS飲料に置き換えた参加者が、カロリー飲料を水に置き換えた参加者と比較してデザートの摂取量を有意に減少させた6-mo介入研究の知見とも一致している(96)。別の研究では、3ヶ月間甘い食べ物や飲み物の摂取量を減らした参加者は、甘味の強さ(低濃度のショ糖で)の知覚の増加を示したが、甘い試験品の快感の知覚には変化がなかった(97)。最後に、無作為化比較試験では、一般的に、糖分が適度に多い食事と、遊離糖分が低糖質炭水化物の等エネルギー交換によって置き換えられた食事の間では、体重への影響は見られなかった(98)。
LNCSがエネルギー摂取量の減少にうまく寄与するためには、代償的なエネルギー摂取が起こらないことが必要である。この問題に対処するために、システマティックレビューとメタアナリシスでは、短期(1日未満)と持続(1日以上)の無作為化比較試験の両方が検討された(84)。短期解析では、LNCS前負荷がその後のエネルギー摂取量に及ぼす影響を、砂糖、無糖製品、水、無添加、プラセボカプセルと比較して検討した56件の論文から218件の比較を評価した。比較のほとんど(83%)は、砂糖と比較したLNCSであり、砂糖で代用した場合、LNCSは一貫して短期的なエネルギー摂取量を減少させることが観察された。砂糖と比較したLNCSの摂取は、小児では70%、成人では43%のエネルギー補填となり、すべての研究で平均50%の補填となった。また、LNCSの摂取量は、水、無糖製品、無添加のいずれと比較しても差はなかった。持続的エネルギー摂取量の分析には、太りすぎ、肥満、正常体重の参加者を対象とした10日間から1年間の9件の研究からの10件の比較が含まれており、すべての場合において、LNCSの使用はエネルギー摂取量の減少につながった。このレビューの後に完了した別の研究の結果は、それが食事と一緒にLNCS飲料の消費は、習慣的または非習慣的な消費者であった人のいずれかで、総エネルギー摂取量、マクロ栄養素摂取量、または選択された甘い食品を増加させなかったことが指摘されたロジャースら(84)の調査結果と一致していた(99)LNCSがエネルギー含有量と甘味をデカップリングすることによってエネルギー摂取量を増加させるかもしれないという懸念に反して、または甘いものへの嗜好性を高めることによって、またはMattesとPopkin(100)によってレビューされた他の潜在的なメカニズムによって、。
LNCSの摂取量と体重の関係は、いくつかの観察研究(すなわち、前向きコホート)と無作為化比較試験によって検討されてきた。ランダム化比較試験は最も質の高いエビデンスを提供している。表4は、システマティックレビューおよびメタアナリシス(74,84,101-106)の結果をまとめたものである。プロスペクティブコホート研究の7件のシステマティックレビューの結果は混合しており、大部分は明確な傾向を示さなかった。あるメタアナリシスではBMIのわずかな減少(kg/m2; -0.002)が観察された(84)が、別のメタアナリシスではBMIのわずかな増加(kg/m2; 0.03)が観察され、体重または脂肪量との有意な関連は認められなかった(102)。観察研究では、すべての潜在的な交絡因子をコントロールすることは不可能であるため、残留交絡の可能性や逆因果関係の可能性が残る(106)。ランダム化比較試験の6件のシステマティックレビューと2件のメタアナリシスのうち、ほとんどがLNCSの使用に伴う体重またはBMIの減少を示した。いずれのメタアナリシスも、LNCSの使用はBMI、体重、またはその両方を減少させると報告している(84, 102)。MillerとPerez(102)は、LNCSの使用は体重(-0.80kg)BMI(kg/m2;-0.24)ウエスト周囲長(-0.83cm)および脂肪量(-1.10kg)の減少と有意に関連していることを発見した。同様に、Rogersら(84)は、LNCSを砂糖(-1.35 kg)または水(-1.24 kg)で代用した場合、体重の有意な減少を報告した。
表4 BW1に対するLNCSの効果に関するシステマティックレビューおよびメタアナリシスの結果
| 人間の研究 | ||||||
|---|---|---|---|---|---|---|
| 重要なBWまたはBMIの変化 | 重要なメタアナリシスの結果 | |||||
| 研究、年(参照) | 動物実験 | OB | RCT | PCS | RCT | BWの変更に関する全体的な結論 |
| Brown et al。、2010 2(101) | NR | ↑ | ↔ | NR | NR | ↔ |
| ガードナー他、2012 3(74) | NR | ↔ | ↓ | NR | NR | ↓ |
| ミラーとペレス、2014(102) | NR | ↑/↔ | ↓ | BW:NS; BMI:0.03 FM:NS | BW:–0.80 kg; BMI:–0.24; FM:–1.10 kg; WC:–0.83 cm | ↓ |
| ペレイラ、2014(103) | NR | ↔(LNCS bevs) | ↔(LNCS bevs) | NR | NR | ↔(LNCS bevs) |
| Bruyéreetal。、2015(104) | NR | ↔ | ↓ | NR | NR | ↔ |
| Fernstrom、2015(105) | NR | ↔ | ↓ | NR | NR | ↓ |
| Peters and Beck、2016(106) | NR | ↑/↔ | ↓ | NR | NR | ↓ |
| Rogers et al。、2016(84) | ↓または↔ | ↓ | ↓ | BMI:–0.002 | BW:–1.35 kg(LNCS対砂糖); BW:–1.24 kg(LNCS対水) | ↓ |
1システマティックレビューおよびメタアナリシスでは、包括的な文献検索から関連するすべての研究を特定している。BMIはkg/m2単位。 bevs、飲料、BW、体重、FM、脂肪量、LNCS、低カロリー・無カロリー甘味料、NR、報告されていない、OB、観察研究(横断的研究およびプロスペクティブコホート研究を含む)PCS、プロスペクティブコホート研究、RCT、無作為化比較試験、WC、ウエスト囲い、↑、全体的な証拠は体重増加を示す、↓、全体的な証拠は体重減少を示す、↔、明確な傾向がない、または効果がない。
2青少年におけるLCNSのシステマティックレビュー。
3米国心臓協会および米国糖尿病協会の科学的声明。
まとめると、これまでの研究では、ステビオール配糖体を含むLNCSの摂取は、LNCSがエネルギー摂取量を増加させる可能性があるという示唆に反して、一貫してエネルギー摂取量を減少させるのに役立つことが示されている。さらに、研究では、甘味への暴露は味の好みを訓練し、”甘い歯 “を奨励しないことが示されている。実際には、LNCSsで「甘味」への持続的な暴露がエネルギー摂取量の増加につながることを示唆するヒトの臨床研究はない。ステビオール配糖体に関しては、研究デザインの違いにもかかわらず、利用可能な2つの研究(64, 83)では、平均50%のエネルギー補償で、エネルギー減少の有益性が示された。全体的に、現在の証拠は、現在の専門家のコンセンサス論文(107)と一致しており、高エネルギー成分の代わりに使用した場合、LNCSはエネルギーを減らすのに役立つと結論付けている。LNCSが食欲と体重を増加させるという主張は、LNCSの摂取が健康的な体重管理に寄与することが期待できることを示す証拠によって明らかに矛盾している。また、ステビオール配糖体は、他のLNCSsの無作為化比較試験で観察された同様の体重減少効果をもたらす可能性が高いと仮定しても安全である。
血圧
8つの臨床試験群からなる6つの無作為化臨床試験では、4週間から2年間の血圧に対するステビオール配糖体の効果が調査されている。4つの臨床試験群では、1型および2型糖尿病患者においてステビオール配糖体の血圧への有意な影響は認められなかったが、4つの実施例すべてにおいて、被験者は高血圧の場合には血圧の薬の服用を継続していた(45,46,67)。血圧薬を服用していない軽度から中等度の高血圧の被験者を2件の研究で調査したが、いずれも750~1500mgのステビオシド/dで中等度の血圧低下効果を示した(70,71)。ステビオール配糖体介入は、その安全性と独立した血圧への効果を検討する目的で、食事操作を行わずにサプリメントの形で提供された。
ステビオール配糖体を急性単食と長期の両方の設定で評価した7つのランダム化比較試験のメタアナリシスでは、収縮期血圧に有意差はないが、拡張期血圧の有意な低下(-2.24 mm Hg; P = 0.03)が示された(72)。しかしながら、有意な不均一性が観察されたが、これは、ステビオール配糖体の組成の違い、利用された用量、被験者による血圧および抗糖尿病薬の継続使用、および正常血圧の被験者を含めたことによるものと思われる。これらの研究のほとんどは、これらのコンテキスト内でステビオール配糖体の安全性を調査するように設計されており、いくつかの研究では、負の影響がないADIの3-4倍の用量を使用して、ステビオール配糖体の安全性をさらに支持している。
腸内細菌叢
ヒトの腸内微生物叢は、大きくて複雑な微生物の集団である。合計で1000種以上の微生物が同定されており、そのうち160種が一人の人間の腸内に存在している(108)。90%以上の種は、FirmicutesとBacteroidetesの2つの主要な系統に分類され、他の一般的な系統には、Actinobacteria、Proteobacteria、Verrucomicrobia、Fusobacteriaが含まれている(109)。また、微生物叢が肥満や2型糖尿病にも関与している可能性があるという証拠もある(110)。しかし、これらの病態に関与する微生物を特定することは、より困難であることが証明されている。
系統とその構成属と種の相対的な割合だけでなく、腸内微生物代謝は、個人間で著しく異なることができ、産後すぐの時期の初期の植民地化、宿主の遺伝学、および薬物や環境化学物質への曝露など、様々な要因によって影響を受けることができる(111)。しかしながら、確立された証拠は、食生活、習慣的な食生活の変化、長期的および短期的な食生活の変化の両方が、腸内細菌叢の全体的な構成およびその機能性に影響を与える最も重要な因子であるように見えることを示している。
食品中でのそれらの広範な使用のため、LNCSと腸内微生物叢との相互作用は、実験動物およびヒトを対象とした多数の研究の対象となっているが、LNCSはその摂取量が非常に少ないため、臨床的に意味のある影響を及ぼす可能性は低い。それにもかかわらず、サッカリン、アスパルテーム、およびスクラロースに関するいくつかの研究では、微生物相の組成または代謝に対する効果が示されているが、通常のヒトの消費量を超える非常に高用量の場合、またはデザインに問題があるか、適切なコントロールが欠如している研究でのみ示されている(112-116)。LNCSは、Magnusonら(15)によってレビューされているように、消費後に非常に異なる代謝運命を有する化合物の構造的に多様なグループである。大部分(例えば、アセスルファムK、サッカリン、アスパルテーム、およびスクラロース)は、腸内細菌によって代謝されない。唯一の2つの例外は、ステビオール配糖体およびシクラメートである。後者は微生物によってシクロヘキシルアミンに変換され、その後吸収されて尿中に排泄される(117)。
ステビオール配糖体の腸内微生物叢への影響に関する研究は少ない。Gardanaら(17)は、ヒトの糞便懸濁液をステビオシドまたはReb Aで24時間インキュベートした。ステビオシドでは全嫌気性菌、バクテロイデス、および乳酸菌の数が減少し、Reb Aでは全好気性菌、ビフィズス菌、および腸球菌の数が減少した。同様に、Kunováら(118)は、別の試験管内試験研究において、ステビオール配糖体の存在下では、グルコースコントロールと比較して、乳酸菌およびビフィズス菌株の増殖が不良であったことを指摘した。また、BALB/c マウスに Reb A を 5.5 mg または 139 mg ⋅kg-1 ⋅d-1 (1.8 mg SEs ⋅kg-1 ⋅d-1)で 4 wk 間経口投与した試験では、ステビオール配糖体の存在下では乳酸菌やビフィズス菌の生育が悪く、ステビオール配糖体の存在下では乳酸菌やビフィズス菌の生育が悪かったとの報告がある。 8 mg SEs ⋅kg-1 ⋅d-1 または 46 mg SEs ⋅kg-1 ⋅d-1)を水と比較して 4 wk で経口投与した試験では、糞中の主要群の生菌数や総バクテリアの多様性指数に変化は見られなかった(120)。唯一の違いは高用量での乳酸菌の多様性の増加で、ADIは4mg SEs・kg-1・d-1の10倍以上であった。このように、現在のエビデンスは、ステビオール配糖体が腸内細菌叢に与える影響が少ないことを示している。
ステビオール配糖体の腸内細菌叢への影響はないが、ステビオール配糖体は腸内細菌によって代謝されるというデータがある。腸内細菌叢は、ヒトには存在しない酵素を提供することで、食物成分の分解に重要な役割を果たしている(121)。グリコシラーゼは微生物叢のメンバーの間で共通しているが、Gardanaら(17)は、ステビオールグリコシドを脱グリコシル化する能力は、Bacteroides属内にのみ存在するように見えることを発見した。テストしたクロストリジア、ビフィズス菌、大腸菌、乳酸菌、腸球菌の培養は、ステビオールグリコシドまたはReb Aを代謝することができなかった。ステビオールグリコシドの加水分解におけるヒトの変動は、バクテロイデスが大腸で発見された最も豊富な細菌群の1つであるため、最小限であると予想される(122)。
むし歯
砂糖の摂取と虫歯の発生率との関連性は十分に確立されている。ステビアを用いた2つの短期臨床試験が行われた。Brambillaら(123)は、成人20人を対象に、すすぎ後5,10,15,30分後に同一濃度のステビオシドまたはReb Aを投与した場合と比較して、1回のすすぎ後のプラークpHが有意に低下したことを示した(P<0.01)。Zanelaら(124)は,0.12%クロルヘキシジン(0.12%)と0.05%フッ化ナトリウム(0.05%)を含む0.5%ステビオシドと0.05%フッ化ナトリウム(0.05%)を含む0.5%ステビオシドを含む毎日の口内洗浄液では、200人の子供のプラークの蓄積が減少しなかったことを報告している。S.ミュータンス菌の数は両群間で差はなかったが、すべての群でベースライン時にS.ミュータンス菌のレベルが低かった子供が20%いたため、この結果は混同されている可能性がある。さらに、クロルヘキシジンではなく、ステビオシドとスクロースの比較がより適切な比較であったかもしれない。ストレプトコッカス・ソブリンに感染したラットの仔を対象とした研究では、5週間の投与後、ステビオシドとReb Aは非化膿性であることが観察されたが、ショ糖とは対照的に、深い亀裂と表面齲蝕、およびS. 典型的な薬理学的介入と比較したステビアの効果については、さらに2件の試験管内試験研究が報告されている。ある研究では、S. mutansの増殖抑制効果は水溶液およびアルコール溶液中のステビア抽出物よりもクロルヘキシジンの方が高かった(126)。全体的に、データは、ステビオール配糖体はカリエスを起こさず、栄養性甘味料(例えば、ショ糖、HFCSなど)と比較して、う蝕を予防する上で有益な効果を有する可能性があることを示唆している。しかし、カリオジェニックな栄養性甘味料の代わりにステビアの使用との追加の長期的な人間の研究は保証されている。
ステビオール配糖体の自然性および処理
高純度のステビアは、サトウキビから得られるショ糖と同様の方法でステビアの葉から抽出・精製される。ステビオール配糖体の抽出と精製に関与する特定の変数は、ステビアの生産者によって異なる場合があるが、すべての場合において、プロセスは、収穫、乾燥、粉砕されたS. rebaudiana Bertoni植物の葉から始まる(128, 129)。彼らはその後、お茶の注入(130)に似て、暖かい水に浸されている。ステビオール配糖体は、その単糖部位のために水に可溶であり、収量≦100%の大規模な商業的プロセスで抽出することができる。この水抽出物が暗褐色であるのは、葉に含まれる他の成分、例えばタンパク質、繊維、色素、ポリフェノール、ミネラル、塩類なども抽出されるためである。精製ステップで非糖質成分を除去し、残りのステビオール配糖体を噴霧乾燥して、80~95%のステビオール配糖体を含むオフホワイトの中間体にする(131)。この最終製品は、水またはエタノール混合物を使用した結晶化によってさらに精製され、純度≧95%の白色の最終製品になる。これらの精製ステップは、ステビオール配糖体を濃縮することを可能にする葉の不要な成分を除去するために使用される物理的なプロセスである(13)。抽出と精製のプロセスは、ステビオール配糖体の化学的同一性に影響を与えず、それらが葉の中にそのまま配置されているとき、それらがそのまま残っていることを可能にする。一部の人は、この結論を疑問視しており、したがって、高純度ステビア葉抽出物の自然性または自然の真正性を求めている。この疑問に対処するために、最近の研究では、ステビア植物の葉から高純度の最終製品になるまでの抽出と精製の過程で、ステビオール配糖体分子が変化しているか、あるいはそのパターンが変化しているかどうかを調べた(131)。
乾燥葉(SL)最初の水抽出物(ESL)および最終製品である純度95%以上(SLE95)のステビア葉抽出物を含む、大規模な商業的抽出精製プロセスの3つの別々のバッチを調べた(131)。JECFAの2010年仕様書(129)に記載されている9つのステビオール配糖体(Reb A、B、C、D、およびF; rubusoside; steviolbioside; dulcoside A; stevioside)のすべてが検出され、HPLCおよびMS検出を使用してよく分離された。3つの処理工程からのサンプルは、Reb Dを除いて、米国薬局方の参照標準物質と同じパターンと保持時間で同等のクロマトグラムを示したが、Reb Dはかなり早く溶出し、最終製品でしか検出できなかった。MS検出器が適用され、テストの最初のラウンドで適用されたものと同等のHPLC条件で、Reb Dを含む9つのステビオール配糖体のすべての同一性は、葉、最初の水抽出物、および高純度の最終製品(131)で明確に確認された。
また、各バッチの甘味料の相対的な分布を算出した。Reb A、C、およびF;ダルコシドA;およびステビオシドの相対量は、SLE95,ESL、およびSLのサンプル間で同程度であったことが判明した。SLE95のサンプルでは、ESLとSLのサンプルと比較して、ルブソシド、Reb B、ステビオシドにやや枯渇傾向が見られた。しかし、最も顕著な点は、葉から検出された9種類のステビオール配糖体が、水の注入液(ESLサンプル)と高純度の最終製品粉末(SLE95サンプル)で同様のパターンで検出されたことである。これらの結果は、本研究で試験したステビオール配糖体は、高純度のステビオール配糖体甘味料を製造するために使用される従来の大規模な商業的抽出・精製プロセスで化学的に修飾されたり、分解されたりしていないことを確認しており、ステビオール配糖体の天然の真正しさを裏付けるものである。
ステビオールグリコシド製造のための代替技術
グリコシル化、生物変換(バイオコンバージョンとしても知られている)および遺伝子組み換え酵母からの「ステビオール配糖体」の生産における革新は、コストを削減し、いくつかのステビオール配糖体で発見されている余韻の苦い後味やオフフレーバーを最小限に抑えることによって味を改善することに焦点を当てていた。
グリコシル化は、ステビア植物から抽出されたステビオール配糖体分子に≧1の糖部位(通常はグルコース単位)が添加されたときに味が改善されるという前提に基づいている(132,133)。プロセスは、伝統的な抽出および精製方法を用いて製造される精製ステビア葉エキスから始まる。抽出物は、次に、酵素シクロデキストリングリコシルトランスフェラーゼで処理され、これは、糖源、例えばコーンスターチからのグルコースのステビオールグリコシドへの移行を可能にし、したがって、その化学構造を改変する。グリコシル化の最終生成物は、ステビア植物には見られないいくつかの新しいグリコシル化されたステビオールグリコシドと、変更されていないステビオールグリコシドの数が少ないステビアの構造的に変更された形態である。
近年、Reb A、D、Mなどのステビオール配糖体の生合成をコードする遺伝子が発見されたことにより、Saccharomyces cerevisiae(134,135)やYarrowia lipolytica(136)などの遺伝子組換え酵母株でReb A、D、Mの生産が行われている。これらの酵母株は、ステビア植物のステビオール配糖体代謝経路を発現するように遺伝子操作されており、糖源としてトウモロコシデキストロースまたはグルコースを用いた発酵槽中で、酵素、中間体、およびReb A、D、Mなどのステビオール配糖体を生産することができる。遺伝子組換え酵母から製造されたステビオール配糖体は、ステビア植物に由来せず、その過程でステビア植物のいかなる部分も使用しない。
バイオトランスフォーメーションまたはバイオコンバージョンとして知られる別の最近開発された技術は、ステビオシドまたはReb Aのような伝統的に抽出されたステビオールグリコシドから始まり、それは 2017年の米国GRAS通知(137)に記載されているように、複数の遺伝子組換え酵母-例えば、Pichia pastoris株AおよびBを使用して形質転換される。これらの遺伝子組換え酵母は、グルコース源、例えばトウモロコシデキストロースからのグルコース単位を選択的に抽出されたステビオールグリコシド、例えばステビオシドに移行させるステビオールグリコシドの生合成経路の特定の酵素を含むように設計され、それをReb Eに変換し、次いでReb Mまたは他の所望のステビオールグリコシドに変換する。生物変換の最終生成物は、植物中に見出されるステビオールグリコシドと同一である。それは、植物からの抽出物が形質転換されることから始まる。
ステビアの葉からのステビオール配糖体の伝統的な抽出および精製は、遺伝子組み換えではなく、製品の自然な真正性に影響を与えない高純度のステビオール配糖体を生産するための良い方法として残っている。最近の独自の伝統的な遺伝子組み換え生物(非遺伝子組み換え)の育種方法は、PureCircle Ltd.のStarleafとして知られる品種のような新しいステビア品種を生み出しており、この品種は、望ましいステビオール配糖体であるReb MおよびDを歴史的に知られているステビア植物品種の20倍以上のレベルで含有するように開発された(138)。これらの育種方法は、食品や飲料の糖分含有量の大幅な削減を可能にする、植物由来のよりおいしいステビオール配糖体甘味料を利用できるようにしている。
味と感覚的側面
甘味の強さと風味のプロファイルは、異なるステビオール配糖体の間で大きく異なる(補足表2)。一般に、ステビオール配糖体を含むLNCSの甘味の強さは、ショ糖基準濃度に依存する。例えば、Reb Aとステビオール配糖体の相対的な甘味力は、2.5〜10%水溶液中のスクロースの甘味力の180〜350倍である。ステビア研究の進歩により、Reb MやDのようなマイナーなステビオール配糖体のいくつかは、Reb Aやステビオシドのようなステビオール配糖体と比較して、より高い甘味の強さを持ち、より砂糖のような味であり、後味が最小限であることがわかってきた[(139-142); PureCircle, 2017 unpublished data]。これまでステビオール配糖体の組み合わせに焦点が当てられてきたため、ショ糖と比較したマイナーステビオール配糖体すべての相対的な甘さは完全にはわかっていない。しかし、独自の組み合わせに関する研究から、マイナーステビオール配糖体が甘味と風味の修飾の両方に寄与していることが知られており、他のものと比較して、特定の食品や飲料マトリックスでの組み合わせがどのように機能するかに影響を与えることができる(PureCircle, 2017年未発表データ)。
砂糖は食感、粘度、口当たりを提供し、後味に余韻がないため、食品や飲料製品で砂糖を置き換えることは簡単ではないが、これはすべてのLNCSが完全に模倣できるわけではない。例えば、製パンにおいて、砂糖は、甘味を提供するだけでなく、クリスプ性、細胞構造、褐変、軟化、および棚の安定性にも寄与し、これらはすべて、口当たり、甘味、風味の知覚、および水分活性の制御に影響を与える。したがって、焼成食品中で糖分を減少させる場合、マルトデキストリン、糖アルコールまたは繊維、およびハイドロコロイドまたはタンパク質などの増量剤をステビアとともに使用して、糖分の特性を模倣し、完全糖バージョンが提供する水分および食感を提供する。最近の研究では、ステビアを用いた20%〜50%還元糖マフィンについては、食感、甘味、および風味の最適なレベルを提供するために、ココア繊維およびイヌリンが使用された(143,144)。ステビアは一般に熱安定性があり、塩、スパイス、褐色の芳香剤のような焼き菓子の風味を高めることさえある(PureCircle、未発表データ)。
市販の高純度ステビア葉抽出物は、単一のステビオール配糖体(例えば、Reb A)またはステビオール配糖体の様々な組み合わせのいずれかを含んでいてもよい。他の甘味料とは異なり、ステビアの甘味は、ステビアが単一化合物の甘味料よりも複雑に動作するようになる>40ステビオール配糖体から自然に派生している。さらに、ステビアを含むLNCSの課題のいくつかは、苦味や金属的な味、遅発性の味、甘味が後を引く味などの「オフ」の味を持つことができることである(145)。Reb DやReb Mは比較的すっきりとした甘味があるのに対し、ステビオサイドやReb Aは甘味はあるものの、使用量に応じて程度の差こそあれ、苦味やメタリックな味、あるいは甘草のような味を付与することもある(5)。甘味増強力の範囲からさておき、ステビオール配糖体のそれぞれは、異なる溶解度を有し、また、レモン、フルーティー、フローラル、ブラウン、スパイシーなノートなどの風味を変更または強化することができるユニークな感覚的および機能的属性を示している。
ほとんどの消費者は、味に妥協することを望まず、ショ糖の味を好む。したがって、高ポテンシャルLNCSを使用する際の目標は、ショ糖の味と機能性を可能な限り忠実に再現することである。味覚は製品のマトリックスに影響され、ステビアの場合、特定の食品や飲料のマトリックスのために最適に設計された独自の高純度ステビオール配糖体の組み合わせを使用することで、甘味を大幅に改善することができる。これらの革新は、Reb AやReb Mのような単一のステビオール配糖体を単独で使用するよりもはるかに優れた味の利点を指摘している(146)ので、カロリーや苦味のあるオフノートを追加することなく、より砂糖のような味を付与しながら、最大の糖質削減を達成するのに役立つ。図2は、酸性化された水の中で2つの高純度ステビア葉エキス製品、すなわちReb A(97%)とPureCircle Ltd.から販売されているステビオール配糖体の組み合わせ(PSB-1198)を含む独自の成分とショ糖コントロールを比較した30人のパネラーを対象とした官能研究の結果を示している。酸性水を使用したのは、ステビアを使用した厳選された市場の飲料の特徴を代表するものであるためである。パネリストの報告によると、Reb AはPSB-1198と比較して味の余韻が少なく、甘みが少ないことから、このステビオール配糖体の組み合わせの優位性が示されている。結果は、PSB-1198の味覚プロファイルがショ糖の味覚プロファイルに近かったことを示している(146)。
図2 時間経過に伴う甘味の時間的プロファイル強度
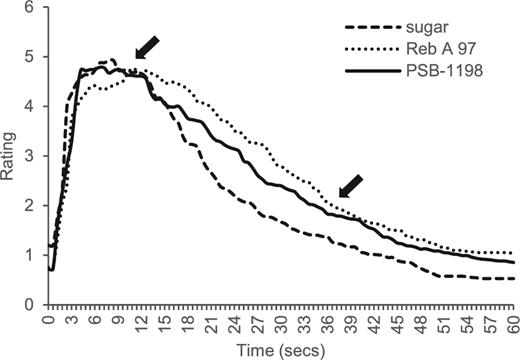
矢印は、ステビオール配糖体の添加が先行した甘味を提供し、PSB-1198の味をより砂糖のような味にするReb A97単独と比較して、ステビオール配糖体の組み合わせで余韻を減らす場所を示している。レブ レバウディオシド
時間経過に伴う甘味の時間的プロファイル強度。矢印は、ステビオール配糖体の添加が先行した甘味を提供し、PSB-1198の味をより砂糖のような味にするReb A97単独と比較して、ステビオール配糖体の組み合わせで余韻を減らす場所を示している。レブ、レバウディオシド
味覚科学の分野での研究は、ステビアの全体的な口当たりを向上させるためのさらなる手がかりを提供することができる。人間は、甘味、うま味、苦味、塩味、酸味の5つの基本的な味覚を知覚する。これらのうち、甘味と苦味はステビアに最も関連している(147)。味覚は、食品や飲料の中で複数の味覚刺激が一緒に提示されたときに、1つの刺激と比較して変化することがあり、二元的な味覚相互作用として知られている(148)。ステビオール配糖体に見られる甘味と苦味が相互作用し、ステビオール配糖体の全体的な苦味閾値が影響を受ける可能性がある(149)。甘味および苦味は、異なる味覚受容体細胞によって検出される(147,150)。Bachmanovら(147)によると、ヒトの味覚知覚、特に苦味は、遺伝的変異のために個人間で大きく異なることがある。10人の訓練を受けたパネラーを対象とした感覚研究では、ステビオール配糖体が舌によってどのように知覚されるかを試験管内試験の細胞ベースの受容体アッセイと組み合わせて決定した(149)。結果は、2つの受容体、TAS2R4とTAS2R14がステビオール配糖体の苦味を媒介することを示した。研究者らはまた、ステビオール配糖体の甘味と苦味を調節するように見える3つの重要な構造的特徴があることに注目した-すなわち、グリコン鎖の長さ、ピラノース置換、およびC16二重結合。より多くのグルコース分子が結合しているステビオール配糖体は甘く、苦味が少ないことがわかった。
甘味受容体細胞の研究は、ステビオール配糖体の味を最適化するためにも活用できるかもしれない。味覚受容体細胞のうち、味覚物質が結合する領域はドッキング部位と呼ばれている(151)。8つのステビオール配糖体のドッキング研究から得られた結果は、テストしたすべてのステビオール配糖体のドッキング位置に有意な変動を示した。ドッキングスコアは、ステビオール配糖体の甘味の効力を予測した。研究者らは、C13およびC19グルコース分子と活性なドッキング部位の特定のセットとの相互作用が、それらの特徴的な味の原因であることを指摘した(152)。これらの結果は、ステビオールの構造を改変し、甘味受容体細胞内の特定のポイントに向けて結合させることが、ステビオール配糖体の味の質と甘味指数を向上させるための有用な手段である可能性を示唆している。
規制状況
ステビオール配糖体の安全性と使用については、世界中の複数の科学団体や規制機関で検討されている。高純度ステビア葉抽出物は、米国、欧州連合、中東、オーストラリア、ニュージーランド、カナダ、中国、日本、韓国、マレーシア、インド、メキシコ、ブラジル、チリ、パラグアイ、アルゼンチン、エジプト、ガーナ、南アフリカ、ケニア、その他アジア、ヨーロッパ、中南米、アフリカの多くの国を含む150以上の国と地域で、食品や飲料への使用が承認または採用されている。
米国では1990年代からステビアからの抽出物が栄養補助食品として使用されており(18)、食品や飲料への高純度ステビオール配糖体の使用は、公表されている毒性試験からのエビデンスと、使用の安全性を評価する資格のある専門家による製品固有のデータのレビューに基づいてGRASと決定されている(153)。高純度のReb Aは 2008年に米国FDAからの「no objection」レターでGRASステータス(GRN 252)を取得した(130)。今日までに、米国FDAのGRAS通知インベントリによると、FDAは、ステビオール配糖体のGRAS通知について40件以上の「異議なし」レターを発行している。最低95%の純度で9つのステビオール配糖体(Reb A, B, C, D, F; rubusoside; steviolbioside; dulcoside A; stevioside)からなる高純度ステビア仕様が 2010年にコーデックス委員会によって確立された(129)。2011年には、コーデックスは、様々な食品および飲料カテゴリーにわたる食品使用基準の確立に伴い、ステビオール配糖体を食品添加物として採用した。フランス食品安全局は 2009年に欧州で初めてReb Aの安全性を評価し、その使用を承認した。EFSAによる好ましい科学的意見(14)により 2011年には、JECFAとReb Eが承認した9種類のステビオール配糖体を含む10種類のステビオールが欧州委員会により承認された。香港とスイスの承認は2010年に発生し 2011年から 2012年の間に、カナダ保健省とアジア、ラテンアメリカ、ロシア連邦のいくつかの国が食品や飲料へのステビオール配糖体の使用を承認した。2014年から 2016年の間に、高純度のステビオール配糖体がインド、東南アジアのいくつかの国、中東の湾岸協力会議の国々で承認された。
純粋なReb Aと比較したRebA-80(ステビオール配糖体純度80%)やRebA-50(ステビオール配糖体純度50%)などの低純度製品を用いた研究は、ステビオール配糖体の混合物が純粋なReb Aよりも優れた味を提供する可能性があるという認識につながり、その結果、異なる組み合わせや純度レベルで構成されたいくつかのステビア甘味料製品が開発された。さらに、マイナーなステビオール配糖体の研究は、その味と機能性についての理解の向上につながった。その結果 2013年から 2016年の間に、Reb M、Reb D、またはその両方を含む3件の米国GRAS通知があった(134,154,155)。GRN 473および512は、ステビア植物の葉から抽出されたReb Mのためのものであり(154,155)GRN 626は、遺伝子操作された酵母の株、S. cerevisiae(134)によって生産されたReb MおよびDのためのものである。Reb M は、EFSA、FSANZ、およびカナダ保健省によっても承認されている。2016年の米国FDAからのノーオブジェクションレター付きの最近のGRAS通知(GRN 619)は、ステビアの使用を≥40のステビオール配糖体の安全な使用を含むように拡大している(57)。さらに、JECFAの2017年の安全性レビューと提案は、グルコース、ラムノース、キシロース、フルクトース、デオキシグルコース(156)など、S. rebaudiana Bertoniの葉に存在する任意の配向性の主要糖鎖の任意の数または組み合わせに共役したステビオール骨格を含むすべての天然由来のステビオール配糖体(≥50)の使用を提案することで、以前の仕様に取って代わられている。この新しい提案された仕様は 2018年にコーデックスで採択される予定である。
ステビオール配糖体を生産するように遺伝子組み換えされた2つの既知の遺伝子組み換え酵母Y. lipolytica(136)およびS. cerevisiae(135)のうち、これまでのところ、JECFAは、「Yarrowia lipolyticaで発現した複数の遺伝子ドナーから」生産されたReb Aの使用を、最低95%の純度で承認している(157)。代替技術を使用した追加の成分が承認されているか、またはGRASステータスを有している。2011年から 2016年の間に、グルコシル化ステビオールグリコシドに対する米国FDAからのノー・オブジェクションレターを有するいくつかの米国GRAS通知(例えば、GRN452,656,448,375,337,および607)は、それらの商業化を許可した(132,158-162)。中国、米国、日本、マレーシア、韓国もグルコシル化ステビア成分の使用を認めている。さらに、バイオコンバージョンによって製造された2つのステビオールグリコシド成分(GRN 667と715)は、米国のGRASステータスを持っている(137,163)。
規制当局によるステビオールグリコシドの食品カテゴリーと使用許可レベルは、地域によって異なる。それらは一般的に、風味付きおよび炭酸飲料、発酵乳製品を含む乳製品、食用アイス、卓上甘味料、果物および野菜の調製、ジャムおよびゼリー、ココアおよびチョコレート製品、菓子およびチューインガム、様々なソース、朝食用シリアル、いくつかのベーカリー製品、加工魚製品、特別な食事目的のための食品、アルコール、いくつかの地域の甘味および塩味のスナックベースの製品、デザート、および食品補助食品を含む(164,165)。
ステビアの主な利点は、天然由来の植物性甘味料であることである。「天然」という用語の世界的な定義や合意された主張は存在しない。しかしながら、韓国、マレーシア、インドネシアの食品規制において、ステビア葉抽出物またはS. rebaudiana Bertoni植物からのステビオール配糖体は、天然甘味料として明確に定義されており、JECFAの第69回会合報告書において、ステビア植物の「天然成分」として報告されている(26)。製造された食品の砂糖を減らすことに関する最近の出版物では、WHOは、また、非カロリー甘味料(すなわち、天然および人工)の分類で天然甘味料としてステビアを認識している(166)。それは一般的に米国の天然起源の甘味料として認められており、画像や「自然」のフレーズは、消費者に天然起源の植物ベースのステビア甘味料の使用を伝えるために、世界の多くの部分で使用されている。食品や飲料製品の成分リストのステビオール配糖体のラベリングは、ある国から別の国に異なることがある。例としては、ステビア葉エキス、ステビオール配糖体、Reb A、レビアナ、ステビア、ヨーロッパではステビオール配糖体(E960)などが挙げられる。
消費者の洞察と市場動向
世界中で、カロリーと糖質を減らすことが健康にもたらす潜在的な利点についての消費者の意識が高まっていることから、カロリーや糖質を抑えた食品や飲料に対する消費者の嗜好が変化しており、これらの嗜好に対応する上での砂糖代替品の潜在的な役割が増大している。さらに、味と機能を損なうことのないクリーンラベル、オーガニック、天然のLNCSへの関心が高まっていることから、ステビアの利点に対する認識が高まり、ステビアをベースにした製品への需要が増加している。
ステビアの世界的な成長は、現在の市場動向に基づいて、2021年までに10億ドルを超えると推定されている(167)。世界中で高純度のステビア葉抽出物が承認されたことで、何百もの食品や飲料の発売が生まれている。Mintelの世界製品データベースからアクセスしたデータによると、ステビアを使用した製品の数は過去5年間で大幅に増加している(168)。2011年だけでも14,000以上の製品が世界で発売され(図3)2016年にはステビアを使用した製品の45%が食品で、55%が飲料でした。
図3 世界で発売されたステビア食品・飲料製品の数:2011年~2017年8月
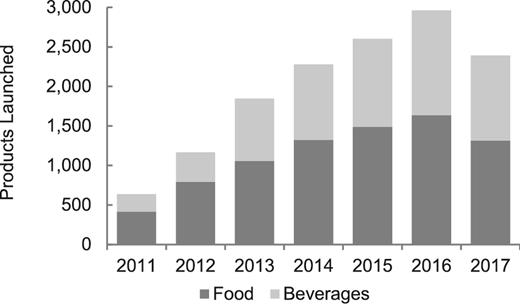
データはミンテルのグローバル新製品データベース(168)より作成。
世界で発売されたステビア食品・飲料製品の数:2011年~2017年8月。データはMintelのGlobal New Products Database(168)から出典。
LNCSに関する消費者と医療従事者の認識と態度に関する査読付き研究は限られている。ステビアを含むLNCSsに関する認知度、信念、感情を調べるために、米国、英国、ドイツ、中国、インド、ブラジル、メキシコの18~64歳の成人約1000人を対象に 2011年から 2017年の間に全国的に代表的な人口サンプルを調査した(169; PureCircle、独自データ)。回答者の50%は男性、50%は女性であった。調査には甘味料関連の質問が約30項目含まれていた。その結果、発売当初の市場では、ステビアの認知度は8%から35%の範囲であったが、メキシコでは77%にまで上昇していることがわかった(図4)。ステビアに対する消費者の認知度が時間の経過とともに上昇していることは、ある国での製品発売の増加に対応しているように思われる。同じ研究では、参加者にステビアに対する印象と、天然由来の植物由来成分としてのステビアに対する信念について、非常に肯定的なものから非常に否定的なものまでの5段階のリッカート尺度に基づいて質問した(図5)。ステビアの全体的な印象についての質問に対する肯定的な回答(非常に肯定的から中程度に肯定的)は、いくつかの国で57%から87%となっている。ステビアは「自然な」製品であると考える人は、国によって48%から86%であった(図5)。ステビアに対する全体的な印象と、ステビアが自然なものであるという信念との間には関係があるように思われ、またその逆もある(169)。
図4 米国(A)英国(B)ドイツ(C)中国(D)メキシコ(E)における世界各国の消費者のステビアに対する意識
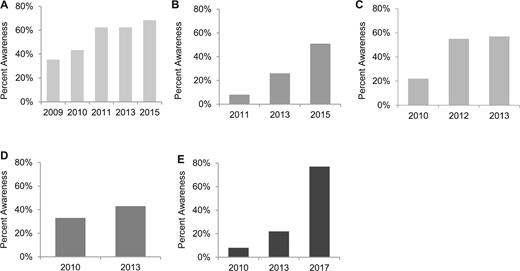
消費者調査のタイムポイント()は、高純度ステビオール配糖体の規制承認のタイミング、市場の関心などの影響を受けるため、国によって異なる。データは参考文献169より。
米国(A)英国(B)ドイツ(C)中国(D)メキシコ(E)における世界各国の消費者のステビアに対する意識。消費者調査のタイムポイント()は、高純度ステビオール配糖体の規制承認のタイミング、市場の関心などの影響を受けるため、国によって異なる。データは参考文献169から。
図 5 肯定的な消費者感情とステビアが天然であると信じる割合
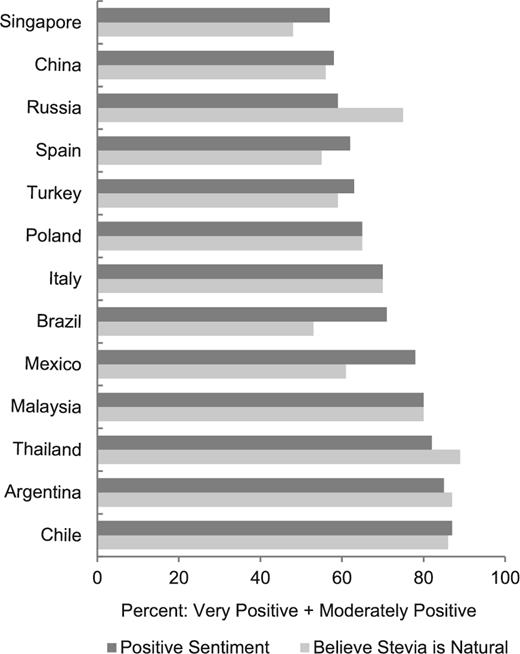
一般的な消費者感情とステビアが天然由来の植物性甘味料であるという信念は、参加者にそれぞれ次の質問をすることによって評価された。次の甘味料のそれぞれのあなたの全体的な印象は何か?次の甘味料のそれぞれについて、全体的な印象はどうですか?それぞれが非常に肯定的なものから非常に否定的なものまでランク付けされた(5ポイントのスケール)。(ステビアは評価された甘味料の一つであり、ステビアのデータのみが示されている)。参考文献169のデータである。
肯定的な消費者感情とステビアが天然であると信じる割合。一般的な消費者感情とステビアが天然由来の植物性甘味料であるという信念は、参加者にそれぞれ次の質問をすることによって評価された。次の甘味料のそれぞれのあなたの全体的な印象は何か?次の甘味料のそれぞれについて、全体的な印象はどうですか?それぞれが非常に肯定的なものから非常に否定的なものまでランク付けされた(5ポイントのスケール)。(ステビアは評価された甘味料の一つであり、ステビアのデータのみが示されている)。参考文献169のデータ。
18歳以上の米国成人3361人のオンライン飲料調査では、参加者の40%未満が、食事中の添加糖を減らすための食事指導にもかかわらず、飲料を選択する際の主要な懸念事項として添加糖を特定したことが報告された(170)。この研究では、飲料に含まれる糖質の種類に関する消費者の誤解や混乱もかなりのレベルで報告されている。英国で行われた別のオンライン研究では、参加者の65%がWHOの糖質摂取ガイドラインを知らないと報告していた(171)。被験者(女性回答者77%)は、食品ラベルに記載されている13種類のカロリー糖(付加糖)またはLNCS(アスパルテームとサッカリン)を特定して分類するように求められたが、成分リストから10以上の糖を正しく分類したのはわずか4%であった。著者らは、高学歴の消費者でさえ、食品ラベルに記載された付加糖を理解するのに苦労していると指摘している。
欧州 5 カ国(フランス、ドイツ、ハンガリー、ポルトガル、英国)の栄養士による LNCSs の認識に関する研究では、栄養士は LNCSs の健康への悪影響について不確かであったり、両義的であったり、恐れを持っていたりすることが示されている(172)。管理栄養士の知識とLNCSsの意見は、様々なアプローチに翻訳されている:一部の管理栄養士は未定であり、一部の管理栄養士はLNCSsを使用すべきではないという意見を持っていた。強力な科学的証拠の欠如にもかかわらず、一部の栄養士は、甘い味が食欲を刺激すると信じていた。栄養士がLNCSsを推奨しない理由として、健康への悪影響やLNCSsの安全性についての不確実性、業界への不信感が挙げられた。この研究の著者は、曖昧さ、不確実性、恐怖心を緩和する鍵として、適切で信頼できる情報源からの権威ある立場と推奨の明確な必要性を確認した。
ユーロモニターの2017年7月の砂糖と甘味料に関する報告書によると 2015年に世界の消費者が購入した総砂糖量は73g/dで、そのうち22%がテーブルシュガー、19%がフルーツ(内在糖)16%が清涼飲料水であった(173)。ビスケット、スナックバー、菓子類などの甘いスナック菓子は、一部の高糖質消費市場では一人当たり20g以上の砂糖を共同で摂取していた。消費者の認識は重要な要因であり、ユーロモニターによると、天然甘味料、特に蜂蜜、ココナッツシュガー、玄米糖などの天然のフルカロリー甘味料へのシフトがあるようである。ユーロモニターによると、将来の開発は、天然甘味料(173)に焦点を当てることが期待されている。
非栄養性甘味料の使用に関する権威ある立場
Academy of Nutrition and Dietetics, the American Heart Association (AHA), and the American Diabetes Association (ADA)などの栄養と健康関連の組織は、現在、ステビアを含むLNCSsの使用を支持する立場、科学的な声明、またはその両方を持っている(74, 174)。栄養と栄養学のアカデミーの2012年のポジションペーパーは、彼らの評価に含まれているステビアのデータを「公正」として等級付けし、LNCSsのための全体的な結論は、”消費者は安全に栄養と非栄養甘味料の範囲を楽しむことができる消費者のための食事の計画の中で消費されたときに、そのようなアメリカ人のための食事のガイドラインと食事の基準摂取量だけでなく、個々の健康目標と個人的な好みなど、現在の連邦政府の栄養勧告によって導かれている “と述べている(174)。その時点で利用可能なステビアに関する証拠のレビューを含む、LNCSsの使用と健康の観点に関するAHAとADAの2012年の共同科学的な声明は、賢明に使用された場合、LNCSsは、それによって減少したエネルギー摂取量と体重減少/体重制御をもたらし、関連する代謝変数に有益な効果を伴う、追加のカロリーを代償として消費することにつながらない限り、添加糖摂取量の削減を促進することができると結論付けた(74)。さらに、アメリカ小児科学会の学校保健評議会は、スナック菓子、甘味飲料、学校用添加糖類に関する見解の中で、学齢期の子供のエネルギー減少のためにLNCSを使用する可能性を認めている(175)。さらに、英国の最近の専門家パネルは、砂糖とのブレンドで、ステビアなどの天然由来の甘味料は、消費者が遊離糖からのエネルギーの5%以上の英国の勧告を満たすのを助けるための方法を提供すると結論付けた(176)。
世界中のすべての主要な規制当局が承認され、食品や飲料で高純度のステビオール配糖体の使用をサポートしているが、栄養と栄養学とAHAとADAのアカデミーによるものと同様のLNCSの使用に関する政策的立場と科学的な声明は、地球の他の多くの部分で欠けている。これらの声明は、一般の人々がしばしば必要とする情報やアドバイスの重要で尊敬されるソースとして機能する実務家や医療専門家のための実用的な方向性を提供するため、これは重要なギャップである。消費者と医療従事者の双方が、信頼できる科学的根拠に基づいた情報に基づいた選択をすることを理解し、支援するためには、より多くの研究と教育が必要である。
まとめと結論
いくつかの世界的および国レベルの権威ある食事ガイドラインでは、世界中で過体重、肥満、糖尿病が増加しているため、添加糖の摂取量を減らすことが推奨されている。これらのガイドラインは、WHO(59)と栄養に関する英国科学諮問委員会(60)によると、追加の健康上の利点のために5%として低く、総カロリー摂取量の10%未満に追加された砂糖の摂取量を維持するための推奨事項が含まれている。高純度のステビア葉エキス甘味料(すなわち、ステビオール配糖体)と食品や飲料のカロリー甘味料の交換は、追加された砂糖の摂取量を減らすのに有用で費用対効果の高いツールである。
天然由来のステビオール配糖体は、S. rebaudiana Bertoni植物の葉の天然の甘い成分であり、抽出と精製の間に変更されずに残っている。ADI以下の高純度ステビオール配糖体の摂取の安全性は十分に確立されている。これらの議事録のセクションで概説されているように追加の研究の機会があるが、今日までの証拠は、ステビオール配糖体は安全で、非心因性であり、非降圧性であり、腸内細菌叢への影響を最小限に抑えていることを示している。ヒトの研究では、否定的な胃腸の副作用は報告されていない。食事中の炭水化物と糖質を置き換えるために使用された場合、健康な人と糖尿病患者を対象とした高純度のステビオール配糖体を用いた研究では、食後血糖値の低下だけでなく、糖質とエネルギー摂取量の減少が支持されている。LNCSやステビア含有食品を摂取した場合に、砂糖や甘いものに対する食欲の増加を示す証拠はない。したがって、ステビア葉抽出甘味料は、糖質およびカロリーの減少、糖尿病、体重管理、および健康的なライフスタイルにおいて有益かつ重要なツールである。最近の技術革新は、製品開発者と消費者の両方が、現在の健康と栄養政策の推奨事項と一致している食事のガイドラインを満たすことを支援するために、フルカロリー/砂糖製品から削減またはゼロカロリー/砂糖添加製品への切り替えを行うのに役立つ、より良い味、天然由来の、高純度のステビアの葉の抽出物をもたらした。
