Post-COVID-19 Symptom Burden: What is Long-COVID and How Should We Manage It?
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7875681/
要旨
COVID-19が患者に及ぼす永続的な影響は最近の研究で検討されており、Long-COVIDの記述につながっている。我々は、パンデミックの第一波からのCOVID-19患者の持続的な症状負担について報告する。
大規模な教育病院から退院したCOVID-19肺炎患者全員を対象に追跡調査を行った。バーチャル外来診療予約時に標準化されたデータ収集技術を用いて、フォローアップ時の症状負担を評価した。
患者の86%がフォローアップ時に少なくとも1つの残存症状を報告した。持続的なX線異常を認めた患者はいなかった。追跡調査時の症状の存在は、COVID-19急性疾患の重症度とは関連していなかった。女性は不安(p = 0.001)疲労(p = 0.004)および筋肉痛(p = 0.022)を含む残存症状を報告する可能性が有意に高かった。長引く症状の存在は COVID-19 患者では一般的である。
我々は、Long-COVIDの現象はSARS-CoV-2の影響に直接起因するものではない可能性を示唆しており、COVID-19の生物心理社会的影響がその病因においてより大きな役割を果たしている可能性があると考えている。
キーワード
Long-COVID、COVID-19,症状負担
序論
最近の研究では、COVID-19の持続的な症状負担と患者への影響が検討されている [1-4]。これらの知見により、ポストコービッド症候群(Long-COVIDとしても知られている)の記述につながっている。現在のところ、誰がLong-COVIDを発症するリスクが最も高いかはわかっていないが、急性疾患の重症度とLong-COVID発症の可能性との間にはほとんど関係がないことが認識されている [7, 8]。
我々は、パンデミックの第1波の間にCOVID-19肺炎で入院した患者コホートの持続的な症状負担について、イングランドの1つのNHS(英国保健医療局)病院から報告している。我々の知見は、これらの患者をサポートするために医療システムがどのようにサービスを組織化すべきかについて重要な意味を持つ可能性がある。
研究方法
COVID-19肺炎の治療後にHull University Teaching Hospitals NHS(英国保健医療局) Trustから退院したすべての患者は、現地で開発された臨床パスウェイに従ってフォローアップを受けた。パスウェイは公表されたモデル[3]に基づいており、地域のサービス構成を反映させるために修正された。患者の入院がCOVID-19とは無関係であった場合、または症状が軽度で胸部X線(CXR)が正常であった場合はフォローアップを行わなかった。我々のコホートに含まれるすべての患者は、RT-PCRでCOVID-19肺炎が確認されていた。我々のデータには、地域のフレイルティチームの下でフォローアップされた患者(ケアホーム居住者およびClinical Frailty Scoreが6以上の患者 [9])は含まれていない。
すべての患者は、専門の看護師および/または理学療法士によるフォローアップCXRおよび標準化された臨床評価を受けた。症状が持続している患者や回復期の胸部X線に異常がある患者は、上級医主導のクリニックで診察を受け、臨床上の必要性に基づいてさらなる検査が行われた。クリニカルパスウェイはオンラインに掲載されている。
各患者について、人口統計学、COVID-19の急性期入院の詳細、治療、追跡調査時の症状負担を含む標準的なデータセットを収集した。呼吸困難(MRC dyspnoea scale)およびQOL(EQ-5D-5Lとして知られる5レベルのEuroQol-5 Dimension)を定量化するために有効な質問票が使用された;その他のすべての症状は、標準化されたフォローアップ評価用の書式を使用して評価され、現在特定の症状を経験しているかどうかを患者に直接尋ねた。入院時およびフォローアップCXRをレビューし、British Society of Thoracic Imaging(BSTI)コーディングを用いて分類して分析した [10]。電子カルテをレビューし、フォローアップ画像や質問票の結果との相関性のために生化学的マーカーの分析を行った。
フォローアップ時の症状を比較する統計解析は、カイ二乗検定およびMann-Whitney U検定を用いて行った。生化学的マーカーを比較する分析は、Wilcoxon符号付き順位検定を用いて実施した。ロジスティック回帰を用いて症状の「クラスター」を同定するために、共起マトリックス [11] を作成した。この中から、高い相関係数を持つ症状のペアを分析し、一般的に同時に報告される症状のグループを同定した。すべての分析は、SPSS統計26を使用して行われた。報告された値は四捨五入誤差の対象となる。
含まれているすべてのデータは、ルーチンのフォローアップの一部として記録され、この研究への包含は、ハル大学教授病院NHS(英国保健医療局)トラスト臨床ガバナンス委員会によって承認された。
結果
COVID-19のコード化された診断を受けて退院した患者は合計387人であった。これらのうち298人がフォローアップの基準(COVID-19肺炎に関連した入院)を満たした。108人は地元のフレイルティチームによってフォローアップされたが、そのデータはこの分析には含まれなかった。さらに56人の患者がフォローアップから外れた。
合計134人の患者(年齢中央値58[範囲25~89]、男性65.7%[n=88])がフォローアップの予約に参加した。患者は退院後、中央値113日(範囲=46-167)でフォローアップを受けた。人口統計学、COVID-19以前の併存疾患、および入院の詳細は表11に示されている。すべての患者にCOVID-19肺炎の放射線学的証拠があり、87%(n = 116)が酸素および/または呼吸器サポートを必要とした。80%(n = 107)は病棟で治療を受け、20%は入院中に集中治療室(ICU)で治療を受けた。
表1 全患者のベースラインの人口統計学、入院データ、臨床フォローアップ情報
| すべての患者(n = 134) | 病棟ベース(n = 107) | ICU(n = 27) | P値 | |
|---|---|---|---|---|
| 年齢(SD) | 59.6(14.0) | 60.9(14.0) | 54.7(13.2) | 0.038 * |
| 男性(%) | 88(65.7) | 69(64.5) | 19(70.4) | 0.565 |
| 滞在期間(範囲) | 7(1–45) | 5(1–45) | 13(5–42) | <0.001 a |
| BMI(範囲) | 28.8(17.3–49.8) | 28.5(17.3–48.6) | 30.7(23.4–49.8) | 0.012 a |
| 民族性(%) | ||||
| 白–すべて | 122(91.0) | 100(93.5) | 22(81.5) | – |
| 黒–すべて | 2(1.5) | 2(1.8) | 0(0) | – |
| アジア–すべて | 8(6.0) | 4(3.8) | 4(14.8) | – |
| 混合/その他 | 2(1.5) | 1(0.9) | 1(3.7) | – |
| 併存疾患(%) | ||||
| 1型糖尿病 | 1(0.7) | 1(0.9) | 0(0) | 0.121 |
| 2型糖尿病 | 30(22.0) | 22(20.6) | 8(29.6) | 0.074 |
| 虚血性心疾患 | 22(16.4) | 19(17.8) | 3(0.11) | 0.102 |
| COPD | 11(8.2) | 9(8.4) | 2(7.4) | 0.135 |
| 喘息 | 19(14.2) | 17(15.9) | 2(7.4) | 0.078 |
| 高血圧 | 55(41.0) | 41(38.3) | 14(51.9) | 0.049 |
| CKD | 6(4.5) | 4(3.7) | 2(7.4) | 0.094 |
| VTEの歴史 | 3(2.2) | 3(2.8) | 0(0) | 0.522 |
| 癌 | 7(5.2) | 6(5.6) | 2(7.4) | 0.113 |
| 家の換気 | 3(2.2) | 5(4.7) | 2(7.4) | 0.113 |
| CVD | 6(4.5) | 4(3.7) | 2(7.4) | 0.544 |
| 喫煙歴 | 59(44.0) | 51(47.7) | 8(29.6) | – |
| アルコールの使用 | 57(42.5) | 46(43.0) | 11(40.7) | – |
| 3つ以上の併存疾患 | 19(14.2) | 15(14.0) | 4(14.8) | 0.916 |
| 最大酸素/呼吸サポート要件(%) | ||||
| 空気 | 18(13.4) | 18(16.8) | 0(0) | – |
| 鼻カニューレ/フェイスマスク | 80(59.4) | 80(74.8) | 0(0) | – |
| CPAP / BIPAP | 8(5.9) | 6(5.6) | 2(7.4) | – |
| ハイフロー鼻カニューレ | 18(13.4) | 3(2.8) | 15(55.5) | – |
| 挿管 | 9(6.7) | 0(0) | 9(33.3) | – |
| ECMO | 1(0.7) | 0(0) | 1(3.7) | – |
| 入院時の炎症マーカーの中央値 | ||||
| 白血球数(×10 9 / L) | 6.55(2.4–90.1) | 6.25(2.4–90.1) | 7.0(3.4–22.2) | 0.040 |
| C反応性タンパク質(mg / L) | 107(0.4–380) | 80(0.4–269) | 136(5–380) | 0.001 |
| 分泌物の炎症マーカーの中央値 | ||||
| 白血球数(×10 9 / L) | 7.5(2.3–43.9) | 6.75(2.3–43.9) | 9.35(3.4–14.4) | <0.001 |
| C反応性タンパク質(mg / L) | 23(0.4–221) | 22.5(0.4–206) | 25.5(6.1–221) | 0.817 |
| フォローアップ炎症マーカーの中央値 | ||||
| 白血球数(×109 / L) | 6.6(2.3–21.0) | 6.6(2.3–21.0) | 8.6(3.6–13.7) | 0.094 |
| C反応性タンパク質(mg / L) | 2.9(0.2–33) | 3.2(0.1–33) | 1.8(0.2–11) | 0.289 |
| BSTICOVID-19アドミッションCXRコード | ||||
| CVCX0(通常) | 4(3.0) | 4(3.7) | 0(0) | – |
| CVCX1(クラシックCOVID-19) | 92(68.7) | 70(65.4) | 22(81.5) | – |
| CVCX2(不定COVID-19) | 23(17.2) | 19(17.8) | 4(14.8) | – |
| CVCX3(非COVID-19;異常) | 8(6.0) | 8(7.5) | 0(0) | – |
| BSTICOVID-19フォローアップCXRコード | ||||
| PCVCX0(通常の解決された変更) | 103(76.9) | 88(82.3) | 15(55.6) | – |
| PCVCX1(50%以上の解像度) | 11(8.2) | 7(6.5) | 3(11.1) | – |
| PCVCX2(≤50%の解像度) | 0(0) | 0(0) | 0(0) | – |
| PCVCX3(永続的または悪化する変更) | 0(0) | 0(0) | 0(0) | – |
| PCVCX4(COVID関連以外の変更) | 12(9.0) | 8(7.5) | 4(14.8) | – |
*不対のt検定
aMann-Whitney U試験
フォローアップ時の症状負担
最も多く報告された症状は息切れで、60%の人がCOVID-19投与前の状態と比較して息切れの増加を経験していた。その他の一般的な症状としては、筋肉痛(51.5%の患者が報告)不安(47.8%)極度の疲労(39.6%)気分の低下(37.3%)睡眠障害(35.1%)などが報告された。女性は男性に比べて、不安(p=0.001)気分の低下(p=0.031)筋痛(p=0.022)疲労(p=0.004)睡眠障害(p=0.009)記憶障害(p=0.001)を報告する可能性が有意に高かった。高BMIは、筋痛(p = 0.012)および疲労(p = 0.046)と関連していた。
介護度、最大酸素量、または受けた呼吸器サポートに基づく持続的な症状負担には有意差はなかった。
持続的な症状を報告する患者の割合は、追跡期間が長くなるにつれて減少したが、この傾向は有意ではなかった。症状データを表22と図1に示す。
表2 フォローアップ時の症状負担を、ケアレベル、性、およびフォローアップまでの時間で層別化して表示する
| すべての患者(n = 134) | 病棟ベース(n = 107) | ICU(n = 27) | 男性(n = 88) | 女性(n = 46) | フォローアップ47〜75日(n = 7) | フォローアップ76〜100日(n = 26) | フォローアップ101〜125日(n = 78) | フォローアップ126〜167日(n = 23) | |
|---|---|---|---|---|---|---|---|---|---|
| フォローアップ時の症状(%) | |||||||||
| 息切れ | 80(59.7) | 60(56.1) | 19(70.4) | 51(58.0) | 29(63.0) | 5(71.4) | 19(73.1) | 43(55.1) | 13(56.5) |
| 筋肉痛 | 69(51.5) | 53(49.5) | 16(59.3) | 39(44.3) | 30(65.2) | 6(85.7) | 18(69.2) | 33(42.3) | 12(52.2) |
| 不安 | 64(47.8) | 52(48.6) | 12(44.4) | 33(37.5) | 31(67.4) | 4(57.1) | 16(61.5) | 34(43.6) | 10(43.5) |
| 極度の倦怠感 | 53(39.6) | 44(41.1) | 9(33.3) | 27(30.7) | 26(56.5) | 5(71.4) | 13(50.0) | 26(33.3) | 9(39.1) |
| 機嫌が悪い | 53(39.6) | 43(40.2) | 10(37.0) | 29(33.0) | 24(52.2) | 4(57.1) | 11(42.3) | 30(38.5) | 8(34.8) |
| 記憶障害 | 50(37.3) | 43(40.2) | 7(25.9) | 24(27.3) | 26(56.5) | 3(42.9) | 12(46.2) | 24(30.8) | 11(47.8) |
| 睡眠障害 | 47(35.1) | 37(34.6) | 10(37.0) | 24(27.3) | 23(50.0) | 4(57.1) | 11(42.3) | 27(34.6) | 5(21.7) |
| 咳 | 47(35.1) | 42(39.3) | 5(18.5) | 27(30.7) | 20(43.5) | 2(28.6) | 11(42.3) | 29(37.2) | 5(21.7) |
| 注意欠陥 | 34(25.4) | 29(27.1) | 5(18.5) | 18(20.5) | 16(34.8) | 3(42.9) | 9(34.6) | 16(20.5) | 6(26.1) |
| 胸膜性胸痛 | 24(17.9) | 23(21.5) | 1(3.7) | 14(15.9) | 10(21.7) | 1(14.3) | 3(11.5) | 17(21.8) | 3(13.0) |
| 喉の痛み | 17(12.7) | 12(11.2) | 5(18.5) | 10(11.4) | 7(15.2) | 2(28.6) | 4(15.4) | 8(10.2) | 3(13.0) |
| 熱 | 14(10.4) | 14(13.1) | 0(0) | 6(6.8) | 8(17.4) | 1(14.3) | 1(3.8) | 11(14.1) | 1(4.3) |
| 無嗅覚症 | 13(9.7) | 13(12.1) | 0(0) | 8(9.1) | 5(10.9) | 0(0) | 3(11.5) | 8(10.2) | 2(8.7) |
| 認識機能障害 | 13(9.7) | 11(10.3) | 2(7.4) | 5(5.7) | 8(17.4) | 1(14.3) | 5(19.2) | 4(5.1) | 3(13.0) |
| 味覚不足 | 12(9.0) | 11(10.3) | 1(3.7) | 8(9.1) | 4(8.7) | 0(0) | 4(15.4) | 6(7.7) | 2(8.7) |
| 発疹 | 11(8.2) | 11(10.3) | 0(0) | 5(5.7) | 6(13.0) | 0(0) | 1(3.8) | 9(11.5) | 1(4.3) |
| 症状クラスターA * | 41(30.6) | 34(31.8) | 7(25.9) | 19(21.6) | 22(47.8) | 4(57.1) | 13(50.0) | 18(23.1) | 6(26.1) |
| 症状クラスタBのA | 21(15.7) | 18(16.8) | 3(11.1) | 13(14.8) | 8(17.4) | 2(28.6) | 4(15.4) | 10(12.8) | 5(21.7) |
| 症状クラスタC B | 19(14.2) | 17(15.9) | 2(7.4) | 12(13.6) | 7(15.2) | 2(28.6) | 3(11.5) | 11(14.1) | 3(13.0) |
| EQ-5D-5Lインデックス値 | 0.657(0.30) | 0.650(0.30) | 0.668(0.29) | 0.676(0.31) | 0.610(0.28) | 0.486(0.26) | 0.629(0.35) | 0.660(0.29) | 0.708(0.28) |
| MRC息切れスケールスコアの中央値(範囲) | |||||||||
| 前 | 1(1–5) | 1(1–5) | 1(1–4) | 1(1–5) | 1(1–5) | 1(1–5) | 1(1–4) | 1(1–5) | 1(1–4) |
| 後 | 2(1–5) | 2(1–5) | 2(1–5) | 2(1–5) | 3(1–5) | 3(2–5) | 2(1–5) | 2(1–5) | 2(1–5) |
*症状クラスターA=筋肉痛、疲労感
a症状クラスターB=気分の低下、不安、睡眠障害
b症状クラスターC=記憶障害、注意欠陥、認知障害
図1 a 性別の症状を示すクラスター棒グラフ。 b 追跡期間別の症状負担を示すクラスター棒グラフ
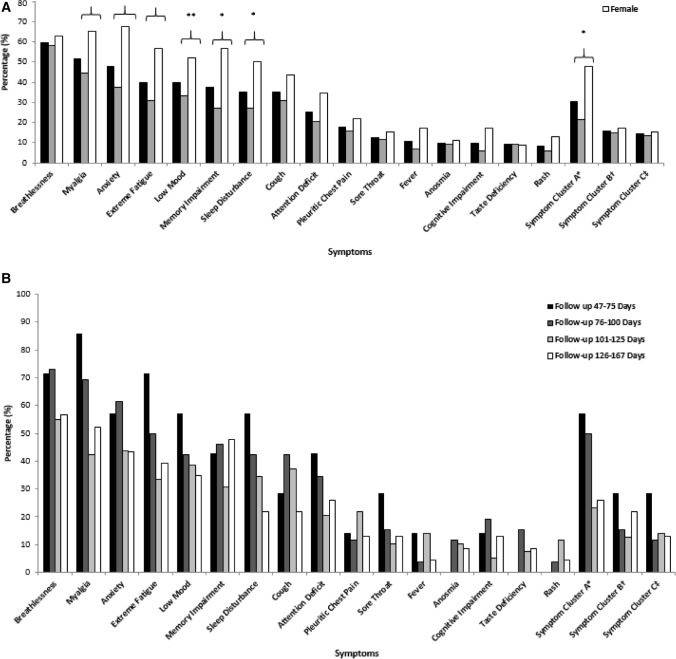
アスタリスクはカイ二乗検定のp値<0.05,二重アスタリスクはカイ二乗検定のp値<0.001を示す。
炎症マーカー
退院時のCRP(CRP)値の中央値は、入院時よりも有意に低かった(107mg/L vs 23mg/L、p<0.001,Wilcoxon signed-rank test)。追跡調査時に検査を受けた76人の患者のうち、CRPおよび白血球数はそれぞれ84%(n = 64)および92%(n = 70)で正常範囲内であった。
放射線所見
130人の患者は、提示時にCOVID-19肺炎のX線像証拠を有しており、残りの4人の患者は入院中にCOVID-19肺炎を発症した。125人の患者がフォローアップCXRを受けたが、そのうち77%(n=103)が正常(PCVCX0)8%(n=10)が50%以上の異常の消失(PCVCX1)を示した。残りはCOVIDに関連しない変化が持続していた。患者のCXRに変化がなかった患者や、変化が悪化した患者はいなかった。フォローアップ時のCXRがPCVCX0とPCVCX1とコードされた患者間では、フォローアップ時の症状負担に差はなかった。
症状の「クラスター」
共起マトリックス[11]を用いて、3つの症状「クラスター」を同定することができた。クラスターAには筋痛と疲労が含まれ、クラスターBには気分の低下、不安、睡眠障害が含まれ、クラスターCには記憶障害、注意欠陥、認知障害が含まれていた。男性と比較して、女性はクラスターAの症状を報告する可能性が有意に高かった(p = < 0.001)。クラスターBとCについては、患者間の有意差は観察されなかった。
これらのクラスターを特定するために使用された共起マトリックスは、図22に示されている。図22.
図2 共起する2つの症状の頻度と相関係数の両方を表示した共起マトリックス アスタリスクは回帰分析で算出した相関係数を示す

議論
我々の結果は以前に発表された報告と一致しており、86%の患者がフォローアップ時に少なくとも1つの症状を報告している。我々の研究は、入院中のCOVID-19の重症度とフォローアップ時の症状負担との間に相関関係がないことを補強するものである。Long-COVIDの初期の記述では、入院を必要とした重度のCOVID-19から回復した患者とは異なる症状の雑多さが描かれている [12]。Long-COVIDでは心理学的/精神神経学的要素が優勢であり、心的外傷後の苦痛に似ているのではないか?湾岸戦争病や9/11後症候群などの類似した心的外傷後症候群では、Long-COVIDで観察されているものと同様のパターンで身体的・心理的症状の発生が記述されている [13, 14]。我々は、新しい、十分に理解されていない、致死的なウイルスの影響と、それが引き起こした関連する社会的混乱を控えめにしてはならないことを示唆している。COVID-19の生物心理社会的影響の重要性を理解し、それらが身体的および精神的健康に影響を及ぼす長期的な症状の発現をどのように促進するかを理解しなければならない。
利用可能な証拠の乏しさから、我々はLong-COVIDが明確な病態生理学を持つ新しい疾患として存在するかどうかを疑問視している。我々は、COVID-19の持続的な効果とは対照的に、他の外傷的出来事の後に観察される、よく認識されている現象の新しい症状であることを示唆している。現在のエビデンスは、咳などの古典的なウイルス後呼吸器症状は、Long-COVID患者では頻度が低いことを示唆している[15]。実際、我々の研究では、咳の有病率が中程度(35%)であることが報告されており、このことが補強されている。これらの理由から、資源配分はリハビリテーションと心理的サポートを優先し、高度な診断や専門的な呼吸器サービスにはあまり重点を置かないべきであると考えている。
COVID症状研究アプリからのデータでは、自己申告による疲労がLong-COVID患者の大規模なグループで最も一般的な愁訴であることが確認された [8]。これらの症状が4ヵ月間持続していた場合、慢性疲労症候群(CFS) の診断基準を満たすことになる。CFSの診断は、患者が労作後の疲労、認知困難、 睡眠障害、慢性疼痛を報告した場合に検討される [16]。これは、我々や他の人がLong-COVIDで観察してきた症状複合体と著しく類似している。また、疫学的にも顕著な類似点がある。CFSの文献では、女性が多いことがよく知られており [17]、肥満もまた、症状の負担が大きいことと関連している [18]。我々の研究では、これらの人口統計学的特徴の両方が、特に CFSで一般的にみられる症状の負担の増加と関連していた。CFSの病因は不明であるが、ウイルスが誘因であると いう仮説が立てられている[19]。英国のCFSサービスは、患者の管理に合わせたアプロー チを提供している。症状管理、心理的治療、就労支援、病状に関する 教育など、多面的なサービスが提供されている[16]。私たちの患者の効果的な管理を確保するためには、これらの原則をLong-COVIDサービス提供に取り入れることが適切かもしれない。
我々の研究では、評価が仮想的であるため、フォローアップ時に末梢酸素飽和度などの生理学的データを記録できないなどの制限がある。障害の既往のない患者では、身体能力の低下が認められることが観察されている [20] 。20] これらのデータを含めることで、生理学的変化、身体能力、および報告された持続的症状との間に相関関係があるかどうかを確認するのに役立ったかもしれない。我々の研究のさらなる限界は、持続性症状の存在の単純な評価であった;患者が症状を経験しているかどうかを確認することしかできず、個々の症状の重症度を記録することができなかった。
結論
我々は、COVID-19後の症状負担の有病率に関する現在のエビデンスと一致するデータを報告する。我々は、症状負担とX線写真または生化学的異常との間に関連性がないことを示した。我々は、Long-COVIDの現象はSARS-CoV-2の影響に直接起因するものではなく、むしろ神経精神医学的侮辱がその病因においてより大きな役割を果たしている可能性があることを示唆している。我々の観察は、これらの患者のケアのためのサービスデザインと優先順位の決定を知らせるのに役立つ。
