Positive impact of oral hydroxychloroquine and povidone-iodine throat spray for COVID-19 prophylaxis: An open-label randomized trial
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8056783/
オンラインで公開2021年4月20日

https://www.cnbctv18.com/healthcare/throat-spray-oral-drug-for-malaria-arthritis-effective-in-reducing-spread-of-covid-19-spore-study-9055601.htm
要旨
背景
我々は、既存の認可された薬物療法が新型コロナウイルス(COVID-19)の感染拡大を抑制できるかどうかを検討した。
方法
シンガポールの大規模多層寮に隔離された健康な移民労働者を対象に、非盲検並行無作為化対照試験を実施した。40のクラスター(各クラスターは寮の各階と定義)を、ヒドロキシクロロキンの経口投与(400 mgを1回、その後200 mg/日)イベルメクチンの経口投与(12 mgを1回)ポビドンヨードのどスプレー(3回/日、270 μg/日)亜鉛の経口投与(80 mg/日)とビタミンCの経口投与(500 mg/日)の組み合わせ、またはビタミンCの経口投与(500 mg/日)のいずれかの42日間の予防レジメンを受けるように無作為に割り付けた。主要評価項目は,以下のいずれかによって示されるSARS-CoV-2感染の実験的証拠とした。主要評価項目は,以下のいずれかによって示されるSARS-CoV-2感染の実験的証拠であった:(1)42日目にSARS-CoV-2抗体の血清学的検査が陽性であること,または(2)ベースラインから42日目までの間のいずれかの時点でSARS-CoV-2のPCR検査が陽性であること。
結果
ベースライン時にSARS-CoV-2の血清反応が陰性であった無症状の参加者3037名(平均年齢33.0歳、全員男性)を主要解析対象とした。追跡調査はほぼ完了していた(99.6%)。ビタミンCと比較して,ヒドロキシクロロキンの経口投与(21%,2~42%)とポビドンヨードのどスプレー(24%,7~39%)では,有意な絶対的リスク低下(%,98.75%信頼区間)が認められた。亜鉛・ビタミンC配合剤の経口投与(23%、-5~+41%)イベルメクチン(5%、-10~+22%)では、統計的に有意な差は認められなかった。副作用による中断は,亜鉛/ビタミンC配合剤を投与された被験者が最も多く(6.9%),次いでビタミンC(4.7%),ポビドンヨード(2.0%),ヒドロキシクロロキン(0.7%)の順であった。
結論
若くて健康な男性のSARS-CoV-2感染を減少させる上で,ヒドロキシクロロキンの経口投与またはポビドンヨードのどスプレーを用いた化学予防は,ビタミンCの経口投与よりも優れていた。
キーワード
ヒドロキシクロロキン,ポビドンヨード,亜鉛,ビタミンC,イベルメクチン,SARS-CoV-2
はじめに
ワクチンの大量接種が世界的に成功するまでは、非薬理学的介入(NPI)がCOVID-19の感染を軽減するための唯一の証明された手段である(Lee er al 2020,Sun er al 2020,Chen er al 2020,Wiersinga er al 2020)。ほとんどの国では、国境、学校、レストラン、バー、宗教施設の閉鎖など、物理的な移動を制限するための厳しい措置がとられており、標的検疫では、特定された接触者の移動が制限されている(Lee et al 2020,Sun et al 2020,Chen et al 2020)。しかし、最初の検疫措置の後も新たな症例群が出現し、さらには数が急増したため、このアウトブレイクの封じ込めは困難を極めた。COVID-19の予防に有効な薬理学的薬剤は、特に感染が制御されていない状況では、NPIの補助として有用であろう。2種類の抗寄生虫薬(ヒドロキシクロロキン(Yao et al 2020,Liu et al 2020,Rakedzon et al 2021)およびイベルメクチン(Rakedzon et al 2021年、Caly et al 2020))は、試験管内試験でSARS-CoV-2のアンジオテンシン変換酵素2受容体への親和性を低下させることが示されている。ヒドロキシクロロキンはエンドソームのpHを上昇させることでVero細胞のSARS-CoV-2感染を阻害し(Yao et al 2020,Liu et al 2020)イベルメクチンはImpα/β1ヘテロ二量体に結合してSARS-CoV-2の複製を阻害する(Caly et al 2020)。防腐剤のポビドンヨードは、SARS-CoV-2に対して即効性のある殺ウイルス効果があり(Anderson et al 2020,Frank et al 2020)亜鉛は少なくとも6種類のコロナウイルス(SARS-CoVをはじめ、風邪の原因となる他のウイルスを含む)の複製を阻害する(te Velthuis et al 2010,Hunter et al 2020)。コロナウイルスに対する有効性を示す前臨床の証拠がないにもかかわらず、ビタミンCはこのパンデミックの際に広く使用される治療薬となっている(Feyaerts and Luyten, 2020)。
2020年4月以降、シンガポールでは、移民労働者の居住寮でCOVID-19が広く発生したことを受けて、ウイルスの感染を封じ込め、一般住民への波及を抑えるために厳しい隔離措置がとられた(Chen et al 2020,Koh 2020,Tan et al 2020a、Tan et al 2020b、Yi et al 2020)。2021年3月5日現在、シンガポールで報告された59,998件のうち、90%以上が移民労働者に関わっている(Singapore Ministry of Health, 2020)。寮の人口密度が高いことを考えると、感染した労働者を隔離・検疫する取り組みは困難を極めている(Liu er al 2020,Koh 2020)。我々は、閉鎖された高暴露環境で生活する人々のSARS-CoV-2に対する予防として、少なくとも1つの薬理学的薬剤(ヒドロキシクロロキン、イベルメクチン、ポビドンヨード、亜鉛/ビタミンC併用、ビタミンC)が有効であるという仮説を立てた。
方法
試験デザインおよび監督
本研究は、SARS-CoV-2予防のためのヒドロキシクロロキン経口投与、イベルメクチン経口投与、ポビドンヨード喉スプレー、亜鉛・ビタミンC併用経口投与、ビタミンC経口投与の有効性を評価する非盲検並行無作為化臨床試験である。被験者は無作為にクラスター分けされ、各クラスターは複数階建ての寮の居住階で定義された。フロアごとに単一の介入を割り当てることで,被験者募集のワークフローと,フロアレベルでの厳しい移動制限,および参加希望者への投薬指示を一致させ,募集の規模と時間に応じて投薬ミスの可能性を最小限に抑えた。対照的に、個別に無作為化する方法では、5種類の薬を同時に調剤する必要があり、部屋やフロア内での投薬ミスや交換が発生する可能性がある。非盲検試験デザインは、試験対象の予防薬の投与経路(経口投与と喉スプレー)や投薬スケジュール(1回投与、1日1回投与、1日2回投与)が異なることを考慮して、実用的な判断として選択された。
さらに、効果的な予防策を講じることで、同じ寮のフロアに住む住人間でのSARS-CoV-2感染を減らすことができるかもしれない。試験登録時点では,SARS-CoV-2感染を確認するための承認された血清学的検査はなかった。これらが利用可能になった時点で、症状に基づくエンドポイントに代わって、主要な副次的エンドポイントが主要エンドポイントにアップグレードされた()。本試験は,National Healthcare GroupのDomain-Specific Review Board(2020/00561),保健省,複数省庁合同タスクフォースの承認を受け,シンガポールのすべての臨床試験を監督するHealth Sciences AuthorityのClinical Trial Authorization(CTA2000053)に基づいて実施された。
対象者
21歳から60歳までの寮生で、試験プロトコルを遵守し、42日後に再診を受け、モバイルアプリケーションを用いて毎日症状をフィードバックする意思のある者が本試験に参加した。なお、過去1カ月間に呼吸器系の症状(発熱、咳、鼻水、喉の痛み、息切れ)味覚異常、異臭があった場合、COVID-19の診断を受けたことがある場合、その他の除外基準に該当する場合は参加者から除外した()。
設定
募集は、シンガポールのTuas South Dormitoryで行った。寮には5つの建物があり、各建物は9階建てで、各階に同じ数の部屋があるが、調査中はすべての部屋が満室ではなかった。各部屋は、2階建てのベッド、共同のダイニング、洗面所、2つの共有バスルームを備えた異なるセクションに分かれている。収容人数は、大部屋(約72平方メートル)に最大14人、小部屋(約60平方メートル)に最大10人となっている(最大収容人数は、1人あたり5.15~6.00平方メートル)。この寮での集団発生は、シンガポールの移民労働者を対象とした大規模な集団発生の一部であり、これらの労働者がよく利用する大型スーパーマーケットに関連していた(Tan er al)。 連鎖感染していない症例は、異なるブロックやフロアで散発的に検出され、明確なパターンはなく、この寮では指標となる症例が疫学的に特定できなかった。この寮は 2020年4月7日にTuas South Dormitoryで最初の症例が確認された後 2020年4月23日にシンガポールの感染症法に基づく隔離区域として公示された。
試験への参加登録は2020年5月18日に開始され、できるだけ多くの未感染者を参加させるために14日間の募集枠が設定された。モニタリング強化の一環として、寮の居住者は全員が注意深くモニタリングされ、呼吸器症状を発症したとき、または呼吸器症状を発症した人の同居人であるときは、早期隔離を促進するために、SARS-CoV-2 PCRのための鼻咽頭スワブを受けた(Young er al)。 医師と看護師からなる医療チームが毎日現場に常駐し,寮生の医療ニーズに対応するとともに,隔離期間中は鼻咽頭スワブを実施した。最初の登録日には、PCR陽性の症例346人が確認され、敷地外の隔離施設に移された。公報規制の一環として、住民の移動は法律で厳しく制限された。異なる部屋、フロア、ブロックに住む住民同士の交流は禁止されており、ブロック間に設置されたバリアと24時間体制の警備員によってこの対策が強化された。居住者は、付き添いのもとでの医療行為以外は寮から出ることができず、共同の調理施設も閉鎖されていた。食事は個人の好みに合わせて個別に用意され、調理器具は共有しないように指示されていた。各部屋の代表者が1日3回、決められた時間に個別包装された食品を回収する。NPIとしては、マスク着用の義務化や、社会的距離の取り方、手指の衛生、環境の清掃などを促すメッセージを定期的に発信した。部屋の中では、マスクの着用とこまめな手洗いが求められたが、警備員の目が届かない部屋ではこれらの対策は徹底されなかった。これらの対策は、試験期間中も継続された。試験開始の1週間前には、試験の目的、任意参加であること、試験参加者としての約束などを説明した文書やビデオ資料へのインターネットリンクが掲載されたパンフレットを配布するとともに、試験担当者が部屋を訪問し、グループセッションを行うなどして、住民に試験の告知を行った。この資料は、英語と、移民労働者がよく使う現地語(ベンガル語、ビルマ語、中国語、タミル語)で用意された。
募集当日は、訓練を受けた通訳者が、英語と労働者の母国語でインフォームド・コンセントの内容を読み上げて説明した後、個々の参加者から書面によるインフォームド・コンセントを得ました。人口統計(年齢、性別)出身国、病歴などの情報は、直接インタビューで入手し、シンガポールのGovTech Data Science & Artificial Intelligence Capability Centreが開発した暗号化ツール「FormSG」を用いて入力した。体重、身長、血圧、心拍数はすべての参加者で測定した。各部屋は、SARS-CoV-2に曝されるリスクに応じて等級付けされ、曝されていない部屋は、無作為化前のいかなる時点でもCOVID-19確定症例が確認されていなかった。参加者は、フォームSGを用いて毎日症状を報告するよう求められた。各参加者には、研究期間中に電話またはSMSで研究チームに連絡するための携帯電話番号が与えられた。COVID-19治療にヒドロキシクロロキンを使用した際に発生した有害な安全性報告を受けて、シンガポールの規制当局と協議の上、追加の安全対策が追加された(Mehra et al 2020)。ヒドロキシクロロキンの投与を受けるように無作為化された参加者全員に12誘導心電図を実施した。以下の心電図および血圧・心拍数の所見がある参加者は、ヒドロキシクロロキンの予防投与から除外した:補正QT間隔が450msを超える、任意の不整脈(良性のものを含む、例えば、早発心房または心室複合体)左心室肥大、左脚束枝ブロック、収縮期血圧>140mmHg、拡張期血圧>85mmHg、心拍数>100/分。
無作為化時に全参加者から血液を採取し,その42日後に抽出した血清を,Elecsys®抗SARS-CoV-2抗体検査(ドイツ・ロシュ社)を用いてSARS-CoV-2に対する抗体反応を分析した。また、定量的RT-PCR法によるSARS-CoV-2 RNAの検出(Young et al 2020)のために鼻咽頭ぬぐいを行った参加者の結果を医療記録から検索し、SARS-CoV-2の感染状況を確認した。
介入方法
無作為化後、各参加者は割り当てられた介入薬を42日分投与され(ただし、イベルメクチンは単回投与)研究チームによる直接的な監督や観察を受けることなく、指示通りに薬を服用する責任を負った。ヒドロキシクロロキンは硫酸ヒドロキシクロロキンとして上海製薬控股有限公司から 100mgの錠剤を、イベルメクチンはEdenbridge Pharmaceuticals LLCから3mgの錠剤を、ポビドンヨードはポビドンヨード0.45%(Betadine®)としてMundipharma Pte Ltdから、亜鉛は酸化亜鉛40mgとビタミンC250mg(Macu-Vision®)の組み合わせとしてBlackmores Ltdから、ビタミンCは500mgの錠剤として同じくBlackmores Ltdからそれぞれ入手したものを使用した。硫酸ヒドロキシクロロキンの投与方法は、1回400mg(4錠)を投与した後、1日200mg(2錠)を42日間投与した。薬物動態研究では,SARS-CoV-2の複製を阻害するためには,より高用量のイベルメクチン(承認限界の50~100倍)が必要であることが示唆されたが(Calyら,2020),これらの用量でのSARS-CoV-2に対するイベルメクチンの安全性と有効性を裏付けるヒトでのデータはまばらである。このような不確実性を考慮し、イベルメクチンの投与量は承認されている範囲内の200μg/kgにとどめ、体重が60kgを超える参加者には12mgを単回投与した。ポビドンヨードのどスプレーは、1日3回(約270μg/日)42日間自己投与した。亜鉛(40mg)はビタミンC(250mg)と併用して1日2回投与(合計、亜鉛80mg、ビタミンC 500mg/日)ビタミンC(500mg)は1日1回投与した。ヒドロキシクロロキン(400 mg)またはイベルメクチン(12 mg)の初回投与は,研究チームの立会いのもとで行われた。42日目に、参加者に服薬アドヒアランスを0~10のスコアで評価してもらい(0=非アドヒアランス、10=完全アドヒアランス)残りの薬の数を数えて確認した。シンガポールの慈善団体であるTemasek Foundationからはヒドロキシクロロキンとイベルメクチンが、Mundipharma Pte Ltdからはポビドンヨードのどスプレーが、Blackmores Ltdからは本研究で使用した亜鉛/ビタミンCとビタミンC錠剤が寄贈された。これらの団体は、本研究のデザインや分析には一切関与していない。
試験結果
主要評価項目は,以下のいずれかによって実験室で確認されたSARS-CoV-2感染であった。主要評価項目は,以下のいずれかによって実験室で確認されたSARS-CoV-2感染であった:(1)42日目にSARS-CoV-2抗体の血清学的検査が陽性である,または(2)ベースラインから42日目までのいずれかの時点でSARS-CoV-2のPCR検査が陽性である.副次評価項目は、急性呼吸器症状(発熱、咳、息切れ、喉の痛み、鼻水、匂い・味の変化のいずれかの症状があることで定義)症候性感染症、入院を要する肺炎とした。症候性感染とは、実験室でSARS-CoV-2の感染が確認されている状態で、急性呼吸器症状があることを指す。SARS-CoV-2 RNAスワブの陽性率データを用いて、各介入群間のSARS-CoV-2感染の発生率を比較するために、事後的な生存分析を行った。
サンプルサイズの算出
当初のサンプルサイズの算出は,参加者数を優先した個人無作為化に基づいていた。当初、介入群と対照群の間で20%の差を検出するためには、各予防群に550人の被験者を登録する必要があると見積もっていた。検出力は80%、α=0.0125(複数介入比較の場合はBonferroniの方法で調整)である。ベースライン時の血清陽性率を10%、離脱率を10%と仮定し、各群の最小サンプルサイズを660名と予測した。しかし,この計算では,現地の状況から唯一の現実的な選択肢であったクラスター無作為化を考慮していなかった。期待される効果に基づいてアームごとに当初予測されたサンプルサイズ、アームごとに8クラスタ(無作為化可能な階数が固定されていたため)被験者75人のクラスタサイズ、ρ=0.1のクラスタ内相関(実際の研究で観察されたもの)を用いると、リスクの絶対値の差0.3を検出する本研究のレトロスペクティブパワーは約70%となった。ポビドンヨードとヒドロキシクロロキンとビタミンCの条件付きパワーはそれぞれ99%と85%であった()。
無作為化
各部屋をブロックとフロアごとに連番で並べ、統計コンピュータソフトStata V.16に取り込み、試験開始前にフロアを介入群と対照群に無作為に割り付けた。クラスターの割り当てに関する情報は、研究統計担当者が隠しており、準備をしやすいように、募集の前日に介入とフロアの割り当てを研究チームに伝えた。
統計手法
ベースラインでの血清反応陽性者は除外した。実験室で確認されたSARS-CoV-2感染を介入群間で評価し、クラスタリングを考慮してランダム効果を用いたロジスティック回帰法を用いて、導き出されたオッズ比(多重検定を考慮して98.75%の信頼区間を設定)とWald p値を算出した。ビタミンCと比較した絶対リスクおよび相対リスクの差の信頼区間は、クラスタレベルでブートストラップ法により98.75%の信頼区間を算出した。二次解析では,探索的解析でリスクが変化したことから,募集時点で同じ部屋にいた症例への曝露を調整した。SARS-CoV-2 感染の累積発生率は,積極的な追跡調査の終了前に発生した PCR 確認された感染を用いて評価した。PCR検査を受けていない者,またはPCR検査が陰性であっても研究を継続した者は,積極的追跡調査の終了時,すなわち登録から約42日後に血清検査が行われた時点,またはイベントが発生するまでの間に打ち切られた。それ以外の場合は,有効な追跡調査が終了した時点で打ち切られた。ビタミンCと比較した他の4つの介入群から生じる多重検定に対応するため,統計的有意性の判定には,ボンフェローニ補正レベルα=0.0125を用いた。すべての統計解析にはR(R Core Team, 2020)を使用した。
結果
主要コホートの募集
利用可能な45フロアのうち、3フロアは、特定された症例が適切なケアのために敷地外に移される前に、専用の隔離施設として再利用された。残りの42フロア(「クラスター」)は、無作為化に利用可能であった。残りの42フロア(「クラスター」)が無作為化の対象となり,そのうち40フロアが無作為に選択され,試験的介入を受けるフロアとして同率で割り当てられた(図1)。各予防群のサンプル数のバランスをとるために2つのフロアが確保された。住民の臨床試験への参加意欲が当初は不確かであったため、このような不測の事態に備えた措置が必要であった。標本数の目標を達成するために、これらの2つの無作為化されていないフロアの男性を異なる群にリクルートし、イベルメクチンの体重基準とヒドロキシクロロキンの血圧・心拍数基準を満たさない人にはビタミンCを投与することにした。合計998人の男性が参加資格基準を満たさなかったため、除外された(図1)。募集した4257人の男性のうち、非無作為化フロアから募集した男性849人(ビタミンCを投与したが、ヒドロキシクロロキンとイベルメクチンを割り当てられたフロアから募集した人を含む)(、表S1)と、募集時にSARS-CoV-2の血清陽性であることが判明した男性(n=359)のデータは、主要な分析から除外した。クラスターごとのベースライン血清陽性率は、ヒドロキシクロロキン10.0%、イベルメクチン12.4%、ポビドンヨード14.5%、亜鉛・ビタミンC8.1%、ビタミンC6.3%であった。12名の男性が辞退し、3037名の男性が42日間の試験を完了した(継続率99.6%)。
図1 スクリーニングと無作為化
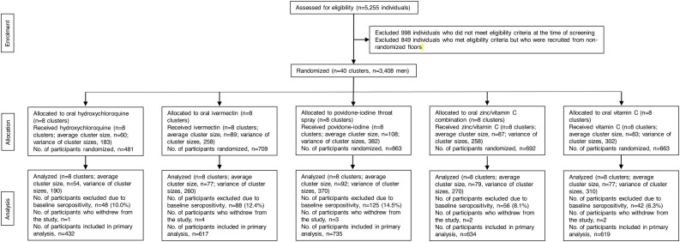
適格性を評価した5255名のうち,998名がスクリーニング時に適格性基準を満たさず,除外された。さらに、適格基準を満たした849人は、無作為化されていないフロアから募集されたため除外された。ヒドロキシクロロキンとイベルメクチンが割り当てられたフロアの参加者で、追加の試験除外項目を満たし、ビタミンCを投与された人は、この849人の一部であった。全体として、40のクラスターが異なる介入を受けるよう等比で無作為化され、3408人の男性が参加した。ヒドロキシクロロキン群では,ベースラインでの血清陽性により 48 名が除外され,1 名が試験から脱落した。イベルメクチン群では、ベースラインの血清陽性により88名が除外され、4名が試験から脱落した。残りの617名の参加者はイベルメクチンの主要解析に含まれた。ポビドンヨード群では,無作為化された863名のうち,ベースラインでの血清陽性により125名が除外され,3名が試験から脱落したため,残りの735名がポビドンヨードの主要解析に含まれた。亜鉛/ビタミンC群では,無作為化された参加者692名のうち,ベースラインでの血清陽性により56名が除外され,2名が試験から離脱したため,残りの634名が亜鉛/ビタミンCの主要解析に含まれた。 ビタミンC群では,無作為化された参加者663名のうち,ベースラインでの血清陽性により42名が除外され,2名が試験から離脱したため,残りの619名がビタミンCの主要解析に含まれた。
主要コホートは、ヒドロキシクロロキン(n=432)イベルメクチン(n=617)ポビドンヨード(n=735)亜鉛とビタミンCの併用(n=634)ビタミンC(n=619)を投与された3037人の男性(平均年齢33.0歳、主にインドとバングラデシュ出身)で構成された(表1)。42名(1.4%)の男性が慢性的な健康状態を報告しており、高血圧が最も多く(1.0%)次いで糖尿病(0.3%)高脂血症(0.1%)であった。2009名(66.2%)の男性は、COVID-19の存在が知られている人との接触がない部屋に住んでいた。ヒドロキシクロロキンを投与された階の男性653名が最初に評価されたが、血圧と心拍数(n=162)および心電図の除外基準(n=10;早発心室、n=8,心房複合体、n=2)を満たした172名が除外された。
表1 試験参加者
| ヒドロキシクロロキン | イベルメクチン | ポビドンヨード | 亜鉛とビタミンC | ビタミンC | |
|---|---|---|---|---|---|
| N = 432 | N = 617 | N = 735 | N = 634 | N = 619 | |
| 参加者の特徴 | |||||
| 年齢(y)、平均(SD) | 30.6(6.4) | 33.6(6.9) | 32.0(6.6) | 33.2(7.8) | 32.9(7.1) |
| 原産国 | |||||
| バングラデシュ | 166(38.4%) | 324(52.5%) | 259(35.2%) | 305(48.1%) | 288(46.5%) |
| インド | 265(61.3%) | 256(41.5%) | 474(64.5%) | 327(51.6%) | 320(51.7%) |
| その他 | 1(0.2%) | 37(6.0%) | 2(0.3%) | 2(0.3%) | 11(1.7%) |
| 余地露光Aません | 293(67.8%) | 378(61.3%) | 482(65.6%) | 457(72.1%) | 399(64.5%) |
| 病歴 | |||||
| 高血圧 | 2(0.5%) | 8(1.3%) | 3(0.4%) | 12(1.9%) | 3(0.5%) |
| 糖尿病 | 1(0.2%) | 2(0.3%) | 3(0.4%) | 2(0.3%) | 2(0.3%) |
| 高脂血症 | 0 | 3(0.5%) | 0 | 1(0.2%) | 0 |
| ベースラインパラメータ | |||||
| 収縮期血圧(mmHg) | 123.8(11.3) | 132.8(15.1) | 130.2(15.0) | 130.1(16.6) | 128.4(16.1) |
| 拡張期血圧(mmHg) | 79.2(6.9) | 86.7(10.0) | 84.8(10.7) | 86.3(11.0) | 84.5(10.7) |
| 脈拍数(1分あたり)b | 86.5(9.3) | 92.6(12.2) | 92.9(13.5) | 89.9(13.7) | 90.9(12.9) |
| ボディマス指数(kg / m 2) | 23.2(3.2) | 25.2(2.7) | 23.8(3.5) | 24.2(3.5) | 24.0(3.2) |
年齢と出身国は雇用証明書で確認、その他の出身国は中国、マレーシア、ミャンマー、フィリピン、タイ。
a無作為化の時点でCOVID-19と診断された人がいなかった部屋に住んでいた被験者の数(%)を示す。
b安静時心拍数を示す。
主要評価項目
実験室で確認されたSARS-CoV-2感染は,男性3037名中1681名(55.4%)に認められた。SARS-CoV-2感染の頻度は,ヒドロキシクロロキン(432名中212名,49%)およびポビドンヨードのどスプレー(735名中338名,46%)の投与を受けた被験者では,ビタミンC(619名中433名,70%)と比較して有意に低かった。α=0.0125(多重比較を考慮)に基づくと、亜鉛/ビタミンC(参加者634人中300人、47%)とイベルメクチン(参加者617人中398人、64%)の間には、ビタミンCと比較して、統計的に有意な差は認められなかった(表2)。ビタミンCと比較して、ヒドロキシクロロキンの経口投与(21%、2-42%)およびポビドンヨードのどスプレー(24%、7-39%)では、有意な絶対リスクの低減(%、98.75%信頼区間)が認められた(表3 )。亜鉛/ビタミンC配合剤(23%,-5~+46%)とイベルメクチン(5%,-10~+22%)では,統計的に有意な絶対的リスク低減効果は認められなかった。ヒドロキシクロロキンとポビドンヨードのどスプレー群のSARS-CoV-2感染症発症率の低下は、潜在的な交絡因子(同一クラスター内での過去の室内暴露、年齢区分、国籍、服薬遵守、ベースラインの血清陽性率)を調整しても、統計的に有意であった(表4 )。若年層とインド国籍の人は統計的に感染率が低かったが(、表S2)年齢と国籍を含めても、各群の感染オッズにはほとんど影響がなかった。
表2 主要および副次評価項目
| ヒドロキシクロロキン
|
イベルメクチン
|
ポビドンヨード
|
亜鉛とビタミンC
|
ビタミンC | |||||
|---|---|---|---|---|---|---|---|---|---|
| N = 432 | P値 | N = 617 | P値 | N = 735 | P値 | N = 634 | P値 | N = 619 | |
| 主な結果 | |||||||||
| 実験室で確認されたSARS-CoV-2感染 | 212(49.1%) | 0.011 * | 398(64.5%) | 0.50 | 338(46.0%) | 0.011 * | 300(47.3%) | 0.033 | 433(70.0%) |
| 血清陽性 | 179 | 0.058 | 308 | 0.56 | 288 | 0.073 | 250 | 0.12 | 348 |
| RNA陽性 | 32 | 0.10 | 90 | 0.97 | 50 | 0.054 | 50 | 0.14 | 85 |
| 二次的な結果 | |||||||||
| 急性呼吸器症状 | 31(7.2%) | 0.14 | 35(5.7%) | 0.012 * | 43(5.9%) | 0.054 | 34(5.4%) | 0.029 | 69(11.1%) |
| 症候性COVID-19 | 29/212(13.7%) | 0.80 | 32/398(8.0%) | 0.0034 * | 42/338(12.4%) | 0.41 | 33/300(11.0%) | 0.17 | 64/433(15.0%) |
| 入院が必要な肺炎 | 0(0%) | – | 0(0%) | – | 0(0%) | – | 0(0%) | – | 0(0%) |
| 死亡者(数 | 0(0%) | – | 0(0%) | – | 0(0%) | – | 0(0%) | – | 0(0%) |
P値は対ビタミンC群の比較。主要アウトカムと急性呼吸器症状については、p値はランダム効果ロジスティック回帰によりクラスタリングを調整したもの。呼吸器症状とは、発熱、咳、息切れ、喉の痛み、鼻水、匂い・味の変化のいずれかの症状を指す。ボンフェローニ補正レベル0.0125で有意なP値は星印で示した。数量は、特に指定のない限り、数(%)である。
表3 異なる介入方法と比較対象(ビタミンC)との間のSARS-CoV-2感染症の発症における絶対的リスク減少および相対的リスク
信頼区間は,各クラスタ(住宅レベル)をサンプリング単位としたブートストラップ区間。ボンフェローニ補正αは0.0125,信頼区間はボンフェローニ補正αに合わせて98.75%で計算。
| アーム | 感染(N) | 合計(N) | SARS-CoV-2陽性(%、98.75%CI) | 絶対的なリスク削減(%、98.75%CI) | 相対リスク(比率、98.75%CI) |
|---|---|---|---|---|---|
| ビタミンC | 433 | 619 | 70(57、81) | 参照 | 参照 |
| ヒドロキシクロロキン | 212 | 432 | 49(31、62) | 21(2、42) | 0.70(0.44、0.97) |
| イベルメクチン | 398 | 617 | 65(51、73) | 5(–10、22) | 0.93(0.71、1.18) |
| ポビドンヨード | 338 | 735 | 46(35、56) | 24(7、39) | 0.66(0.48、0.88) |
| 亜鉛とビタミンC | 300 | 634 | 47(27、72) | 23(–5、46) | 0.67(0.38、1.08) |
表4 交絡因子を調整した場合としない場合の、異なる介入策と比較対象(ビタミンC)との間のSARS-CoV-2感染事故における調整済みオッズ比(aOR)
クラスターレベルのランダム効果と、表に示した変数の固定効果を併用した。モデル1では、混合効果ロジスティック回帰において、各クラスタをランダム効果として組み込んだ。モデル2では,試験開始時の曝露を追加した。Bonferroni補正αは0.0125であり、このレベルで有意な検定には星印が付けられている。信頼区間は、ボンフェローニ補正アルファに合わせて、98.75%で計算されている。モデル3には年齢層、モデル4には国籍、モデル5には服薬コンプライアンス、モデル6には同一クラスタの他の男性におけるベースラインの血清有病率を考慮した。信頼区間は、ランダム効果の空間上で積分するための適応的なGauss-Hermite求積法によって得られ、p値は、尤度面がほぼガウスであるという仮定のもと、漸近的なWald検定から得られる。これらの仮定が異なるため,p値と信頼区間は完全には一致しない。
| モデル1 | モデル2 | モデル3 | モデル4 | モデル5 | モデル6 | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 腕 | aOR(98.75%CI) | p | aOR(98.75%CI) | p | aOR(98.75%CI) | p | aOR(98.75%CI) | p | aOR(98.75%CI) | p | aOR(98.75%CI) | p |
| ビタミンC | 1.00(参考) | – | 1.00(参考) | – | 1.00(参考) | – | 1.00(参考) | – | 1.00(参考) | – | 1.00(参考) | – |
| ヒドロキシクロロキン | 0.37(0.13、1.01) | 0.011 * | 0.37(0.14、0.98) | 0.0085 * | 0.38(0.14、1.00) | 0.0099 * | 0.38(0.14、1.01) | 0.011 * | 0.34(0.12、0.92) | 0.0052 * | 0.39(0.15、0.99) | 0.0094 * |
| イベルメクチン | 0.77(0.27、2.14) | 0.50 | 0.74(0.27、2.00) | 0.44 | 0.73(0.27、1.96) | 0.41 | 0.73(0.27、1.98) | 0.41 | 0.89(0.32、2.48) | 0.78 | 0.83(0.32、2.15) | 0.61 |
| ポビドンヨード | 0.37(0.13、1.02) | 0.011 * | 0.36(0.13、0.97) | 0.0073 * | 0.36(0.13、0.96) | 0.0068 * | 0.37(0.14、1.00) | 0.0097 * | 0.38(0.14、1.03) | 0.012 * | 0.40(0.15、1.03) | 0.012 * |
| 亜鉛とビタミンC | 0.43(0.15、1.20) | 0.033 | 0.42(0.16、1.15) | 0.026 | 0.42(0.15、1.13) | 0.022 | 0.42(0.15、1.15) | 0.025 | 0.42(0.15、1.16) | 0.027 | 0.45(0.17、1.19) | 0.032 |
| 変数 | ||||||||||||
| 以前の部屋の露出 | – | – | 1.42(1.13、1.78) | 0.00012 * | 1.42(1.13、1.78) | 0.00013 * | 1.38(1.10、1.74) | 0.0004 * | 1.39(1.10、1.76) | 0.0005 * | 1.44(1.14、1.80) | <0.0001 * |
| 30歳未満 | – | – | – | – | 1.00(参考) | – | – | – | – | – | – | – |
| 30〜39歳 | – | – | – | – | 1.20(0.97、1.50) | 0.036 | – | – | – | – | – | – |
| 40〜49歳 | – | – | – | – | 1.40(1.03、1.92) | 0.0062 * | – | – | – | – | – | – |
| 50〜59歳 | – | – | – | – | 1.17(0.54、2.58) | 0.62 | – | – | – | – | – | – |
| バングラデシュ | – | – | – | – | – | – | 1.00(参考) | – | – | – | – | – |
| インド人 | – | – | – | – | – | – | 0.78(0.63、0.98) | 0.0056 * | – | – | – | – |
| インド人でもバングラデシュ人でもない | – | – | – | – | – | – | 0.99(0.47、2.19) | 0.97 | – | – | – | – |
| 投薬への高いコンプライアンス | – | – | – | – | – | – | – | – | 0.56(0.43、0.73) | <0.0001 * | – | – |
| 同じクラスター内のベースライン血清陽性率(%) | – | – | – | – | – | – | – | – | – | – | 0.98(0.95、1.01) | 0.05 |
副次評価項目
合計201名(6.6%)の男性が、試験中に急性呼吸器症状を報告した。感染率が低いという証拠はないものの,イベルメクチンを投与された男性は,ビタミンCと比較して症候性感染症が少なかった(表2)。入院を要する肺炎や死亡はなかった。鼻咽頭ぬぐい液から SARS-CoV-2 RNA を検出することで COVID-19 と診断された男性は 309 名であり,SARS-CoV-2 感染と介入群の間で時間軸に基づく事後解析が可能であった。クラスタリングを考慮した結果、感染のタイミングについて両群間で統計的に有意な差があるという証拠は得られなかったが(表S3および図S1)効果量の方向と大きさは主要評価項目と一致していた。主要評価項目をさらに詳しく検討するために、追加の解析を行い、服薬アドヒアランスがSARS-CoV-2感染に与える潜在的な影響を群別に検討した。その結果、服薬アドヒアランスが高い男性は、感染の可能性が有意に低いことがわかった(、表S4,図S2)。
アドヒアランスと安全性
試験参加者のアドヒアランスは中程度に良好で、80%がアドヒアランスを7以上(10段階評価)と評価した。摂取量が直接観察されたイベルメクチン投与群を除き、ポビドンヨード投与群で最も高く(88%)ヒドロキシクロロキン投与群で最も低かった(71%)(表5)。副作用による中断は、亜鉛とビタミンCの併用療法を受けた男性で最も多く(6.9%)次いでビタミンC(4.7%)ポビドンヨード(2.0%)ヒドロキシクロロキン(0.7%)の順であった。ヒドロキシクロロキンの服用率が低かったのは、実際の副作用よりも、潜在的な副作用への懸念(12%)と個人的な判断(3%)が主な理由であった。ポビドンヨード群の男性は、他の治療法(ヒドロキシクロロキン20%、イベルメクチン22%、亜鉛とビタミンCの併用18%、ビタミンC20%、p = 0.003)と比較して、症状が最も少なかった(14%);ポビドンヨード群では、頭痛、食欲不振、便秘を訴える人が少なかった(表4)。ヒドロキシクロロキンの投与を受けた男性では、補正されたQT間隔はベースライン時とフォローアップ時で統計的に有意な差はなかった(平均、それぞれ379ms対378ms、ペアードt-テスト、p = 0.387)。
表5 参加者が報告したアドヒアランスとサイドエフェクト
| ヒドロキシクロロキン | イベルメクチン | ポビドンヨード | 亜鉛とビタミンC | ビタミンC | P値 | |
|---|---|---|---|---|---|---|
| 治験介入への70%を超える遵守が報告された–いいえ。(%)a | 292/409(71.4%) | 572/572(100%) | 623/707(88.1%) | 471/610(77.2%) | 463/579(80.0%) | <0.001 |
| 治験介入への順守が最適ではない理由-いいえ。(%)a | <0.001 | |||||
| 開発された副作用 | 3(0.7%) | – | 15(2.0%) | 44(6.9%) | 29(4.7%) | |
| 副作用の懸念 | 53(12.2%) | – | 11(1.5%) | 15(2.4%) | 20(3.2%) | |
| 介入を減らすか止めるかの個人的な決定 | 14(3.2%) | – | 13(1.8%) | 29(4.6%) | 16(2.6%) | |
| 介入が機能しないと考える | 1(0.2%) | – | 1(0.1%) | 0 | 0 | |
| 友人や家族に服用しないことをお勧めします | 3(0.7%) | – | 1(0.1%) | 3(0.5%) | 0 | |
| COVID-19を開発 | 9(2.1%) | – | 11(1.5%) | 14(2.2%) | 25(4.0%) | |
| 試験的介入を開始した参加者の症状サーベイランス–いいえ/合計いいえ。(%)b | N = 413 | N = 605 | N = 703 | N = 579 | N = 563 | |
| どれか | 82(19.9%) | 132(21.8%) | 98(13.9%) | 106(18.3%) | 115(20.4%) | 0.003 |
| 頭痛 | 39(9.4%) | 62(10.2%) | 42(6.0%) | 41(7.1%) | 53(9.4%) | 0.029 |
| 食欲減少 | 14(3.4%) | 32(5.3%) | 13(1.8%) | 14(2.4%) | 32(5.7%) | <0.001 |
| 便秘 | 13(3.1%) | 25(4.1%) | 17(2.4%) | 17(2.9%) | 34(6.0%) | 0.009 |
| 眠気の増加 | 30(7.3%) | 23(3.8%) | 35(5.0%) | 30(5.2%) | 23(4.1%) | 0.117 |
| 皮膚反応 | 15(3.6%) | 24(4.0%) | 19(2.7%) | 19(3.3%) | 22(3.9%) | 0.717 |
| 体の痛み | 14(3.4%) | 21(3.5%) | 19(2.7%) | 12(2.1%) | 23(4.1%) | 0.330 |
| 胸痛 | 5(1.2%) | 16(2.6%) | 13(1.8%) | 6(1.0%) | 11(2.0%) | 0.258 |
| 吐き気、嘔吐 | 2(0.5%) | 8(1.3%) | 6(0.9%) | 6(1.0%) | 7(1.2%) | 0.698 |
| 関節痛 | 7(1.7%) | 6(1.0%) | 8(1.1%) | 4(0.7%) | 9(1.6%) | 0.534 |
| 胃痛 | 8(1.9%) | 14(2.3%) | 11(1.6%) | 9(1.6%) | 8(1.4%) | 0.767 |
| 気分が変わる | 6(1.5%) | 10(1.7%) | 8(1.1%) | 11(1.9%) | 9(1.6%) | 0.856 |
| 下痢 | 7(1.7%) | 4(0.7%) | 7(1.0%) | 6(1.0%) | 6(1.1%) | 0.634 |
| 胸の圧迫感 | 5(1.2%) | 10(1.7%) | 12(1.7%) | 5(0.9%) | 8(1.4%) | 0.721 |
| 動悸 | 6(1.5%) | 6(1.0%) | 4(0.6%) | 6(1.0%) | 6(1.1%) | 0.691 |
a服薬アドヒアランスは、最終訪問時に客観的なアドヒアランス・スコアを用いて評価され、残りの錠剤を数えることで検証され、介入群間で比較された。COVID-19と診断された後に外部の施設に隔離され、薬のパッケージを再現して錠剤を数えることができなかった参加者は、アドヒアランスの分析から除外された。70%未満のアドヒアランスしか得られなかった参加者を対象に、アドヒアランス不良の理由を調査した。
副作用に関する情報は、FormSGモバイルアプリケーションを用いて、42日間の試験期間中に参加者の日常的な症状を調査することで収集した。最終訪問時に不在で、症状日記で30%未満の回数を報告した参加者は、副作用の分析から除外した。
考察
この非盲検無作為化臨床試験では、閉鎖的かつ高暴露環境で生活する男性を対象に、実験室で確認されたSARS-CoV-2感染の発生率を低下させる上で、ヒドロキシクロロキンの経口投与またはポビドンヨードのどスプレーを短期間使用することが、ビタミンCよりも優れていることがわかった。一方、SARS-CoV-2感染症は、亜鉛とビタミンCの組み合わせを経口投与した男性と、イベルメクチンを単回投与した男性の間で、ビタミンCと比較して統計的に有意な差はなかった。 本研究では、主観的な症状報告に頼らずに血清学的・分子的測定法を取り入れ、参加者を42日間という長期にわたって追跡調査することで、先行研究(Boulware et al 2020,Abella et al 2020,Mitjà et al 2020)の限界に対処した。実験室法で診断を確認することで、主要な結果が報告バイアスの影響を受けないようにし、感染しても無症状またはpauci-symptomaticなままの参加者の特徴を明らかにすることができる(Wiersinga er al 2020,Li er al 2020,Nikolai er al)。 無症候性および有症候性の人からの感染を防ぐことは、どちらも感染を媒介することが知られているため、ウイルスの拡散を食い止めるための中心となる。
今回の結果は、最近の無作為化試験(Boulware et al 2020,Abella et al 2020,Mitjà et al 2020)霊長類研究(Maisonnasse et al 2020)ヒト細胞株を用いた試験管内試験研究(Hoffmann et al 2020)で、SARS-CoV-2予防に対するヒドロキシクロロキンの有効性の欠如が示唆されたデータと対照的である。今回の研究では、1日あたりのヒドロキシクロロキンの投与量が少ない男性でも、42日間というより長い期間にわたってSARS-CoV-2感染の有意な減少が認められた。このような矛盾した結果の一因として,これまでの研究では予防を開始するのが遅く(自己申告による曝露から最大6日後),ヒドロキシクロロキンが予防効果を発揮するのに十分な時間がなかったことで説明できるかどうかは不明である。一方、今回の研究では予防期間が長かったため、より高い累積ヒドロキシクロロキン濃度が得られた。興味深いことに、有害事象の発生が少なかったにもかかわらず、より多くの男性が副作用を懸念し、友人や家族からヒドロキシクロロキンの投与を中止するよう勧められた。これまでの試験(Boulware et al 2020,Abella et al 2020,Mitjà et al 2020)と同様に、急性期治療後に報告されている臨床的に明らかな心臓への影響(Rosenberg et al 2020,Stevenson et al 2020,Goldman et al 2020)や、心電図の補正QT測定値の不顕性変化は観察されなかった。しかし、血圧や心電図に異常のある男性をスクリーニングしたことで、ヒドロキシクロロキン群の健康な男性の選択が偏り、本剤の心臓作用を受けやすい可能性のある男性を誤って除外してしまったかどうかも不明である。一般化には限界があるものの、本研究は、特定の環境下での予防におけるヒドロキシクロロキンの有用性に関する問題が、まだ決定的には解決していないことを示唆している。
この研究は、ポビドンヨードを喉にスプレーして投与するという局所療法が含まれている点が新しい。ポビドンヨードはビタミンCと比較して、SARS-CoV-2の感染を24%低下させた。これらの知見は、ポビドンヨードのSARS-CoV-2に対する強力な殺ウイルス効果を示唆する試験管内試験のデータ(Anderson et al 2020,Frank et al 2020)を支持しており、中咽頭腔内に比較的耐性のある環境を作ることができる可能性がある。その結果、ウイルス量が減少すれば、感染の潜伏期および無症候期にエアロゾル化したウイルス粒子が身近な人に曝露されることが少なくなり、SARS-CoV-2の感染を遮断することができる。他の介入方法と比較して、ポビドンヨードのどスプレーを投与された参加者は、ビタミンC群よりも副作用の報告や投薬中止が少なく、最も高い服薬アドヒアランスを報告したことから、その忍容性と将来的な適用が支持された。一方,亜鉛/ビタミンC併用群とイベルメクチン単回固定用量(承認用量200μg/kg以内)を投与された参加者の間では,SARS-CoV-2感染に差は認められなかった。亜鉛/ビタミンC配合剤投与群のサンプルサイズが大きければ,この結論が変わるかどうか,また,イベルメクチンの投与量を増やして繰り返し投与した場合に結果が異なるかどうかは不明である.
この研究にはいくつかの限界がある。まず、サンプルサイズを算出する際に、本試験のクラスター無作為化デザインを反映していなかった。これは、クラスター化の程度が事前に不明であったため、介入群間の差を検出するために必要なクラスター数と被験者数を過小評価していたと考えられる。ヒドロキシクロロキン群に除外基準が追加されたことで、この群の適格な参加者が少なくなり、投薬群間の無作為化のバランス特性が損なわれる可能性がある。第二に、ビタミンCが適切な比較対象であるかどうか、またプラセボ錠がより良い対照として機能するかどうかについては議論の余地がある。プラセボを投与しないことにしたのは、非盲検試験のデザインを考慮すると、プラセボ群の募集に支障をきたす可能性があることと、アウトブレイクの場でプラセボ錠を投与することの倫理的正当性を考慮してのことである。第3に、本研究では、若年層から中年層の男性を対象とし、合併症(高血圧、高脂血症など)の少ない寮生活者を対象とした。そのため、病気が軽く、肺炎も見られなかったと考えられ、本研究結果の一般化には限界がある。第4に、寮ではNPIを徹底するための積極的な取り組みが行われていたにもかかわらず、社会的距離の取り方、個人の手指衛生、マスク着用の遵守状況は評価されなかった。しかし、本研究は、インフラや物資が統一され、警備員による厳格な取り締まりが行われている単一の寮で実施されたため、有意なばらつきが生じるとは考えられない。第5に、資源、微生物学的および物流上の理由から、全コホートに対して鼻咽頭スワブを実施しなかったため、採用時に無症候性感染症を保有している参加者がいる可能性を排除できなかった。しかし、定量的PCRの感度は、病気の潜伏期、前駆期、回復期のいずれの時期に検査を行うかによって異なり、無症候性の人では30%程度と低くなる可能性があるため、無症候性感染の診断は困難である(Dong er al 2021, Ternovoi er al 2020)。さらに精度を高めるためには、PCR検査を繰り返し行う必要があるかもしれない。
同様に、抗体反応を起こす能力には個人差があり、反応が遅れると偽陰性の結果となる可能性がある。しかし、異なる投薬群間で採血のタイミング(ベースラインと42日目)を標準化することで、このようなばらつきの影響は最小限に抑えられる。第6に、ヒトの臨床試験では、感染性病原体への曝露の不均一性をコントロールすることが難しい。本研究では、曝露の異なる代替指標(異なる階の部屋での曝露とベースラインの血清陽性率)を調整しても、主要な知見に変化はなかった。
今回のパンデミックでは、感染が抑制されない脆弱な環境が明らかになっている。このような環境でNPIを実施することは非常に困難であり、感染拡大を防ぐための新たな手段が急務となっている。このような環境には、クルーズ船、刑務所、難民キャンプ、食肉加工施設などがある。本研究は、閉鎖された環境で生活する隔離された人々のSARS-CoV-2感染を減少させるために、ヒドロキシクロロキンの経口投与またはポビドンヨードのどスプレーによる予防的治療が有効であることを示した初めての研究である。これらの薬物療法は、ワクチンの展開を待つ間、感染率が高い環境で既存のNPIを補完するために使用できる可能性がある。さらに研究を進めれば、高齢者や女性、免疫力低下やその他の重大な併存疾患のある人における効果を、より長期にわたって分析することができるであろう。
