コンテンツ
—
ffects of alternative steeping methods on composition, antioxidant property and colour of green, black and oolong tea infusions
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4648929/
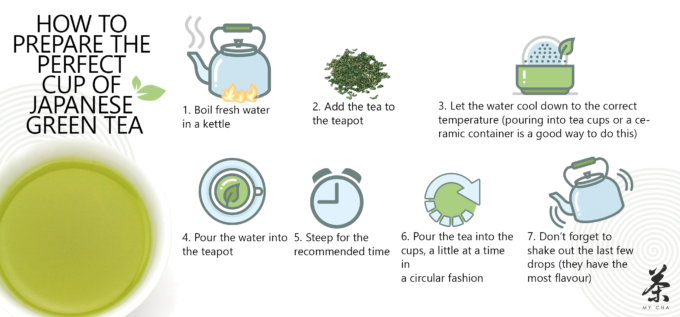
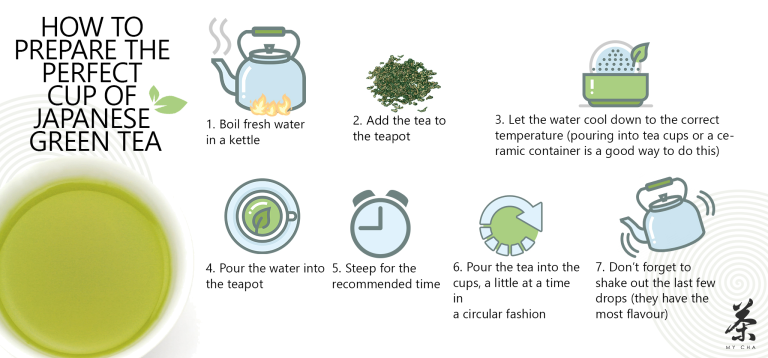
https://mychateaco.com.au/how-to-make-japanese-green-tea/
要旨
冷水抽出はお茶の健康効果を最大化することが報告されているが、長い注入時間を必要とする。本研究では、短時間のホットステップの後に氷を加える方法を採用することを検討した。緑茶、黒茶、ウーロン茶を対象に、この革新的な方法をホットおよびコールド抽出と比較検討した。カテキン、キサンチン、ガロン酸の含有量、抗酸化力、総フェノール、色の分析を行った。ホットインフュージョンでは抽出力は速いが、関連する化合物の分解が見られた。逆に、冷たい注入は遅い速度で健康な分子のより高いレベルを抽出した。この革新的な方法は、抗酸化力の点では低温輸液と同様の特性を短時間で達成した。ガロン酸やエピガロカテキンガレートなどの生理活性化合物については、緑茶と黒茶で、熱湯煎じに比べて約2倍の高い値を記録した。この浸漬法は、工業用飲料の調製法として代替的なアプローチとなる可能性がある。
キーワード
緑茶、紅茶、ウーロン茶、色、FRAP、カフェイン
序論
お茶は水に次いで世界で最も多く飲まれている飲料である。酸化の度合いなどの加工法(いわゆる「発酵」)によって、緑茶(非発酵)ウーロン茶(半発酵)紅茶(完全発酵)の3種類が知られている。欧米諸国では紅茶が最も消費されているが、近年、より高い抗酸化活性と関連する健康効果のために緑茶に大きな注目が集まっている(Steinmann er al 2013; Park er al 2014; Pang er al 2015)。
伝統的なお茶の調製方法は、種類に応じた温度(70〜100℃、Yang er al)。 多くの研究では、茶の種類(Bae er al 2015; Lin er al 2014a, b; Yang and Liu 2013)地理的起源(Dias er al 2014)および季節変動(Laddi er al 2014)に応じて、異なる茶のポリフェノールおよび生理活性化合物の含有量に応じて品質および抗酸化特性が異なることが報告されている(Chen er al 2012; El-Shahawi 2012; Rahim er al 2014; Zhang er al 2013)。生物活性化合物の抽出に対する注入条件の影響は、温度および時間がポリフェノール含有量および抗酸化能力に影響を与える最も重要なパラメータであることを示す研究が行われてきた(Araújo Ramalho et al 2013; Bae et al 2015; Rusak et al 2008)。緑茶から抗酸化物質を最適に抽出するためには、低温を使用することが推奨されている(Banerjee and Chatterjee 2014)。
最近では、冷水(4℃または室温)抽出は、注入のための新しい人気のある方法となっている。それは、より低いカフェイン、より低い苦味およびより高い香りを提供する(Lin er al 2014a, b)。カフェイン、カテキンおよびガテン酸の輸液率は、熱水の場合よりも低く、輸液時間とともに増加した(Liao er al)。 Venditti et al 2010)は、潜在的な健康上の利点を最大化するために温度の影響を研究した。しかし、有望なコールド抽出技術は、長時間の注入を必要とする。これを克服するために、潜在的な修正は、機能性化合物の内容物の変化を引き起こすゆっくりとした冷却プロセスを避けて、熱水での注入ステップに続いて氷の添加を含む(Ananingsih et al 2013)。
機能性化合物と有機物の品質に対する冷水の効果はまだ調査されておらず、お茶の消費が健康に有益な効果を宣伝していることを考慮すると、より多くの注目に値する。本論文では、3種類の茶葉(紅茶、緑茶、ウーロン茶)に対する3つの異なる蒸らし方の効果について説明する。インフューズの調製に用いた方法論は、熱湯、冷水、熱水の後に氷を加えたものである。得られた飲料の特性を比較するために、抗酸化活性、色、カフェイン、テオブロミン、テオフィリン、カテキン、ガロン酸含量を評価した。
材料と方法
化学品
胆汁酸(GA)、アスコルビン酸、テオブロミン、テオフィリン、カフェイン、(-)-エピカテキン(EC)、(-)-エピガロカテキンガレート(EGCG)、2,4,6-トリピリジル-s-トリアジン(TPTZ)。氷酢酸、メタノール(MeOH)アセトニトリル(ACN)フォリンチオカルテウのフェノール試薬および2,2-ジフェニル-1-ピクリルヒドラジル(DPPH)は、シグマ・アルドリッチ・ケミカル社(Sigma-Aldrich Chemical Co.(St. Louis, MO, USA)から購入した。酢酸ナトリウムおよび塩化第二鉄は、Carlo Erba Reagents (Milano, Italy)から入手した。リン酸はJ.T. Baker(イタリア、ミラノ)から供給され、炭酸ナトリウムはSigma-Aldrich(イタリア、ミラノ)から供給された。脱イオン水(’18 MΩ cmの抵抗率)はMilli-Q(Millipore, Bedford, MA, USA)から得た;ボトル入りミネラルウォーター(180℃での乾燥残渣80.5 mg/l)25℃での導電率124 μS/cm、5.9 °F)は市場から購入した。
茶およびインフューズの調製
煎茶針未発酵緑茶、桐頂半発酵烏龍茶、オレンジペコエ花のような完全発酵黒茶を “Ferri dal 1905” (Mantova, Italy)から寄贈されたものを分析した。緑と黒の茶葉のサイズは約1.5mm、ウーロン茶の茶葉は直径3mmのロール状のものを使用した。質量拡散に利用できる総表面積は、ウーロン茶で104.4mm2,緑茶で44.8mm2,黒茶で16.8mm2と推定された。経験豊富なティーテイスターのパネルによって調整された蒸らし方法を表1.1に報告する。熱水による抽出(”ホット”):お茶(12 g)を特定の温度に持ってきた1 Lの水に入れた。冷茶は冷蔵温度(4℃±1)で12時間かけて煎じて調製した。氷茶は80℃の水600mLに30gの茶を入れ、煎じて葉を取り除いた後、400gの氷を加えて調製した。すべてのサンプルを3回に分けて調製し、ろ過(0.45mm)した。
表1 注入準備の概略図
| お茶 | 抽出 | 葉(g / L) | 温度(°C) | 時間(分) | 水(L) | 氷(kg)a |
|---|---|---|---|---|---|---|
| 緑 | ホット | 12 | 75 | 4 | 1 | – |
| コールド | 8 | 4 | 720 | 1 | – | |
| ホット+アイス | 30 | 80 | 5 | 0.6 0.6 | 0.4 | |
| ウーロン茶 | ホット | 12 | 85 | 4 | 1 | – |
| コールド | 7 | 4 | 720 | 1 | – | |
| ホット+アイス | 30 | 80 | 4 | 0.6 0.6 | 0.4 | |
| ブラック | ホット | 12 | 90 | 3 | 1 | – |
| コールド | 7 | 4 | 720 | 1 | – | |
| ホット+アイス | 30 | 80 | 3 | 0.6 0.6 | 0.4 |
注入後に追加
高速液体クロマトグラフィー
分離は、以前の方法(Wang er al 2000)を修正したKinetex C18カラム(100 mm × 2.1 mm ID, 2.6 μ)を備えたAgilent Technologies 1200液体クロマトグラフで行った。移動相 (0.2 ml/min) は、85 % の溶媒 A (0.1 % v/v オルトリン酸を含む水) と 15 % の溶媒 B (MeOH) で構成されていた。溶媒Bは16分後に27%まで直線的に増加した。13分間静置し、1分間で15%Bにグラジエントを戻した。注入量20μl。モニタリング波長:210および280 nm。
直線性、精度、選択性、および回収率に関する研究を、Eurachemガイドライン(www.eurachem.org)に従って実施した。
検出限界(yD)および定量限界(yQ)は、平均ブランク(y̅b)およびブランク信号の標準偏差(sb)に基づいて信号として計算された。
![]()
t = 信頼度と自由度に応じたt-Student分布(片側分布)の定数(ν = n-1; n = 測定数). 10個のブランクがy barbとsbを計算するために実行された。yDとyQの値は、適切な較正関数を用いて、それぞれLODとLOQを推定するために、信号領域から濃度領域に変換された。
直線性は、ガロン酸およびカフェインについては0.05〜100mgL-1,テオブロミンについては0.05〜50mgL-1,テオフィリンについては0.05〜25mgL-1,エピカテキンについては0.5〜25mgL-1,エピガロカテキンガレートについては0.5〜100mgL-1の範囲で確立された。5つの等間隔濃度レベルを選択し、各レベルで3つの複製注射を行った。ホモスケダスティシティ検定を実施し、マンデルのフィッティング検定を適用して検量線の適合性を評価した。切片の有意性を確認するためにt検定を実施した(信頼度95%)。精度は、分析のための2つの濃度レベルで、面積と保持時間の日間および日内再現性の両方をRSD%として計算した。
日間の再現性は、2つの濃度レベルで5回の測定を3回に分けて行い、ピーク面積と保持時間について計算した。日間の再現性は、2つの異なる日に同じ分析を行った場合に計算された。
3つの濃度レベルの全分析物で強化されたサンプルの回収率は、以下のように計算された。
回収率 (%) = (C1 – C2)/C3 × 100
(強化試料で決定されたC1濃度、未強化試料で決定されたC2濃度、強化試料で決定されたC3濃度)。
総フェノール含有量
全フェノール含量(TPC)は、Folin-Ciocalteauの手順(Jayasekera er al)。 簡単に言うと、1 mL のアリコートに、7.5 %炭酸ナトリウム溶液 4 mL と Folin-Coocalteau 試薬 (10 %) 5 mL を加えた。混合物を暗所で室温で 60 分間反応させた。吸光度を750nmで測定した。校正はガロン酸水溶液(25-300μg/mL)で行った。全フェノール値は、ガロン酸当量(GAE)として表された。各サンプルの抽出を二重に行い、各アッセイを三重に実施した(n = 6)。
第二鉄還元性抗酸化力(FRAP)の測定
還元鉄/抗酸化力(FRAP)アッセイは、電子供与性抗酸化剤の作用により無色酸化FeIII形態から青色のFeII-トリピリジルトリアジン化合物が形成されることによる593 nmでの吸光度の変化を測定することにより、Benzie and Strain (1996)に従って実施された。FRAPは、酢酸緩衝液300mM、pH3.6,TPTZ 10mMとFeCl3 6H2O(20mM)を10:1:1:1の比率で混合することによって調製した。茶インフューズの200 mLに、37℃で温めたワーキングFRAPの380μLを加えた。直ちに、そして4分後に再び、593 nmでの吸光度をブランクサンプルに対して測定した。
リカートータルカラーとCIElabパラメータの決定
液体総色(LTC)は、Obanda et al 2004)に従って決定した。3 mLの輸液を45 mlの蒸留水で希釈した。吸光度は蒸留水に対して460nmで読み取った。結果は乾物含有量で補正した:サーモバランス法(BEL Engineering, Monza, Italy)を用いて、黒、緑、ウーロンのそれぞれ93.5,92.6,93.7%の値を得た。
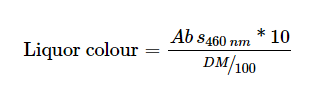
透明な容器に入れたサンプルを、デスクトップフラットベッドスキャナ(Hewlett Packard Scanjet 8200, Palo Alto, CA, USA)を用いて、1cmあたり236ピクセル(解像度600dpi、トゥルーカラー24ビット)でスキャンした。取得中、スキャナは周囲の光や外部からの反射を避けるために黒い箱の中に入れられてた。フラットベッドスキャナの色は、以前にN’Dri et al 2010)によって報告されているように特徴づけられ、補正された。
消費者テスト
18歳から40歳までの若年成人(男性10名、女性14名)24名を対象に、嗜好性ランキング試験(ISO2006)を実施した。サンプルは、総合的な受容性と有機嗅覚的品質に基づいてランク付けされた。データはフリードマンのカイ二乗ノンパラメトリック検定を用いて分析され、サンプルの差別性(p値)の全体像が示された。最小有意順位差(LSRD)を計算して、選好順位の結果として得られた順位和の間のペアワイズサンプル差を識別した。
統計的分析
データの平均値と標準偏差(SD)は、サンプル間の違いを識別するために、一方向分散分析(ANOVA)と最小有意差(LSD)検定を95%の信頼水準(p < 0.05)で実行するためにも使用されるSPSS(バージョン20.0)ソフトウェアを使用して計算された。分析データ間のピアソン相関(0.01レベル、2-tailed)を実行するために同じソフトウェアを使用した。
結果と考察
高速液体クロマトグラフィー(HPLC
キサンチン類(カフェイン、テオフィリン、テオブロミン)カテキン類(エピカテキン、エピガロカテキンガレート)ガリン酸を約14分で分離した(図1)。表22に報告されている定量データは、採用した葉と水の比率の違いにもかかわらず、抽出の有効性を示している。浸漬方法の間には有意な差が認められた。
図1 緑茶インフューズのHPLCクロマトグラム
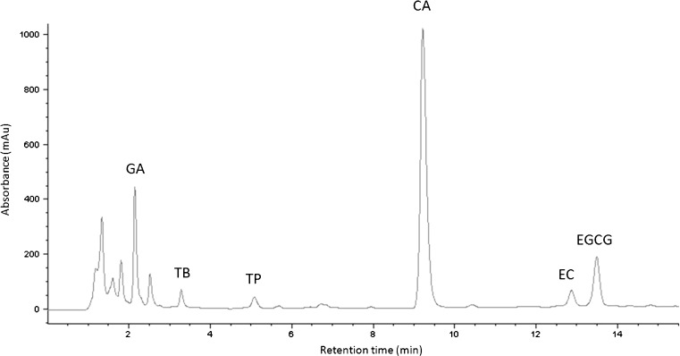
GA ガリン酸、TB テオブロミン、TP テオフィリン、CA カフェイン、EC エピカテキン、EGCG エピガロカテキンガレート
表2 茶サンプルの分析結果(平均値±標準偏差)mg/g葉で表されるデータ
| お茶 | 抽出 | フラップ | TPC | GA | EC | EGCG | TP | TB |
|---|---|---|---|---|---|---|---|---|
| 緑 | ホット | 1463.1±129.7 A | 13.5±0.1 C | 3.46±0.03 C | 1.36±0.06 B | 4.09±0.12 B | 0.20±0.00 A | 0.63±0.01 B |
| コールド | 1653.5±147.1 A | 19.7±0.1 A | 3.93±0.03 B | nd | 4.13±0.10 B | 0.19±0.01 A | 0.65±0.03 B | |
| ホット+アイス | 1432.6±80.8 A | 14.2±0.0 B | 5.13±0.06 A | 1.61±0.05 A | 7.36±0.02 A | 0.19±0.00 A | 1.22±0.03 A | |
| ウーロン茶 | ホット | 325.4±64.9 B | 12.8±0.2 C | 1.05±0.01 C | 0.23±0.05 A | 0.62±0.01 C | 0.06±0.01 B | 0.25±0.01 B |
| コールド | 1278.5±81.1 A | 21.0±0.1 A | 2.94±0.02 A | nd | 2.45±0.01 A | 0.24±0.01 A | 0.43±0.01 A | |
| ホット+アイス | 1183.5±124.3 A | 14.1±0.2 B | 2.12±0.02 B | 0.11±0.02 B | 1.17±0.07 B | 0.06±0.00 B | 0.25±0.00 B | |
| ブラック | ホット | 1111.8±139.2 B | 14.2±0.1 B | 3.62±0.15 B | nd | 0.43±0.01 C | 0.09±0.00 A | 1.29±0.01 B |
| コールド | 1218.8±38.0 B | 20.4±0.1 A | 4.11±0.14 A | nd | 0.60±0.01 B | 0.10±0.01 A | 1.15±0.00 C | |
| ホット+アイス | 1629.0±189.6 A | 14.8±0.2 B | 4.07±0.15 A | 0.03±0.00 | 0.76±0.03 A | 0.11±0.01 A | 1.62±0.06 A |
略語。GA ガロン酸、EGC(-)-エピガロカテキン、EC(-)-エピカテキン、EGCG(-)-エピガロカテキンガレート、TP テオフィリン、TB テオブロミン
a,b,c各列内の同一文字は有意差なし(n = 5; p < 0.05)
EGCG は最も優勢なカテキンであった (El-Shhahawi er al 2012)。キサンチンの中ではカフェインが最も多く、次いでテオブロミン、テオフィリンの順であったが、文献で報告されている範囲であった(Friedman er al)。 ガリン酸は、最近の研究によると、1.05から5.13mg/gの範囲で有意な量が検出された(Bae er al)。
緑茶および紅茶については、ホット+アイスインフュージョンは、量が一定であるTPを除いて、すべての分析物の中で最も高い量を抽出することができた(表(表2).2)。化合物の抽出は、温度と注入時間の両方に明らかに依存している。Yang er al)。 (2007)の報告によると、緑茶からのガテン酸の抽出率は熱水よりも冷水の方が低いことから、温度が最も影響を与えるパラメータと考えられる。
緑茶、紅茶ともに、低温法の方が高温法よりもわずかに高い抽出量が得られたことから、低温でも接触時間を長くすることで、関連する化合物が確実に移行することが示された。また、長時間接触している間に高量の分析物が抽出され、その後、12時間に沿って発生する重合現象のような酸化や副反応によって破壊されるという仮説も立てられる(Samaniego-Sannchez et al 2011; Ananingsih et al 2013)。このような現象は、ホット+氷の注入は、活性化合物の高い量を維持するために迅速に低温に到達しながら、注入後、冷却プロセス中に発生する可能性がある。EGCGの酸化的分解は、保存中に起こることが以前に報告されている(Yang er al 2007)。同様に、Kim et al 2007)は高温でカテキンの減少を観察しており、エピマー化や酸化が起こっている可能性を示唆している。また、コールドインフューズ(Wang and Helliwell 2000)ではECは認められなかった。
ウーロン茶では、冷間抽出後に分析物の最高値が検出された。この明らかに予想外の挙動は、圧延された葉の形状と寸法を考慮すると説明することができる(直径は他のものよりも明らかに高い)。ロール状の葉の形状は、抽出の速度を遅くし、移行プロセスを困難にする。低温ではあるが、水との接触時間が長くなると、葉が展開し、質量拡散のために利用可能な表面が大きくなる(Astill er al 2001)。ホット+アイス法とホット+アイス法の比較では、緑茶と同様に、後者の抽出物では前者に比べてガリン酸とECGCの量が2倍になっているのに対し、ECでは逆の結果が得られた。
紅茶では、ホット+アイス法の方がわずかに高く、ホット抽出法の方が低い値を示すなど、3つの蒸らし方の差が小さくなっていた。熱間抽出は最高温度で行われたため、高温での抽出は化合物の分解につながるというこれまでの知見を裏付ける結果となった(Samaniego-Sannchez et al 2011; Kim et al 2007)。
結論として、異なるお茶のカテキン含有量に関するデータは、Zhang et al 2013)およびKim et al 2007)のデータと一致している。
図2に報告されているカフェイン含有量は、図2(aパネル)に示されている。図22(パネルa)は、緑茶がより高い値を示している(Yang er al)。 カフェイン抽出は温度に直接依存し、水温が上昇するほど質量移動率が高くなる(Perva-Uzunalić er al 2006)。緑茶では、紅茶と同様にホット+氷抽出で最も高い値が記録された。一方、ウーロン茶では、冷法が最も高い値を示した。このように、緑茶と紅茶では、葉の寸法が物質移動の制限因子であり、水温が重要な役割を果たしていることがわかった。また、ウーロン茶では、表面積と体積の比が大きいため、低温でも抽出時間が長くなり、効率的な抽出が可能となった。
図2 パネルa カフェイン含有 mg/g 葉 パネルb カフェイン含有量、mg/カップ-200 mL
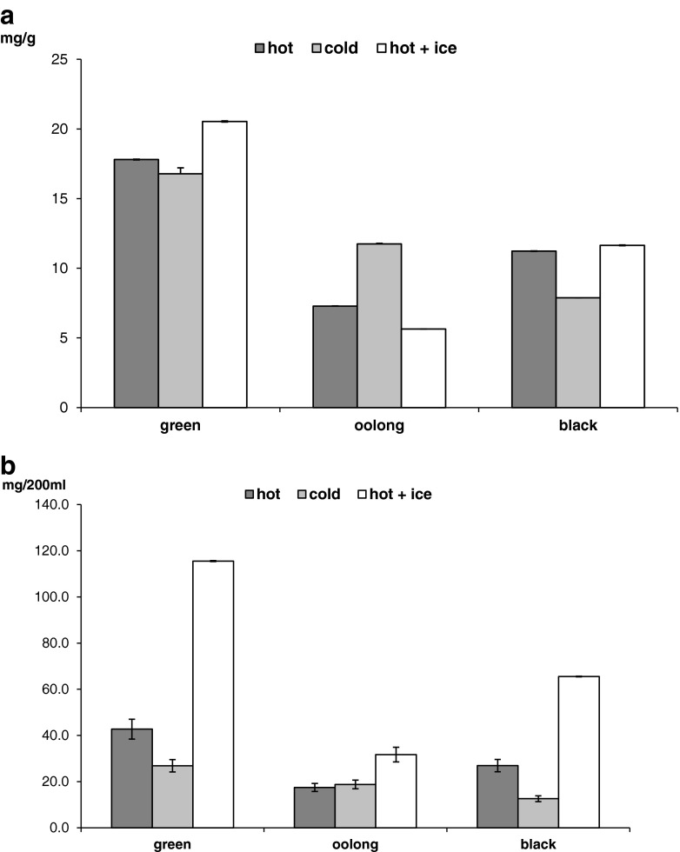
最後に、カフェインは重要な精神活性物質であり、摂取量を管理する必要があることから、茶葉と水の比率が異なる場合の摂取量を評価するために、1杯に含まれるカフェイン量を算出した(図2,2,2,パネルb)。すべての茶葉と水の比率が高いホット+アイス法が最も高いカフェイン量を示した(表1).1)。緑茶と黒茶は表面積が少ないため、ホット+アイス法と他の方法との間に大きな差が見られた。また、葉と水の比率が高いことから、ホット法の方がコールド法よりもカフェイン量が多いことが予想されたが、これは抽出温度が高いことによるものであった。
総フェノール含有量
フォリン-キオカルトー法は、すべての還元性化合物に敏感であるので、抽出物の総還元力の推定値を与えた。フェノリックの量は、一般的に抗酸化物質の主要なソースと考えられている食品の有益な健康効果に接続されている。
データが同様の傾向(表(表2):2)に従うように、異なる輸液の間に大きな違いは観察されなかった:低温輸液は、Damiani et al 2014)に従って、ホット+氷とホット法に続いて、最も高いフェノール含有量を与えた。2つの可能な理由は、この挙動を説明することができる:抽出時間が長いことは、より多くの量の活性化合物の移行を決定し、および/または低温で分解から分子を保護した。
時間と温度の間の支配的な変数を理解するために、我々は他の抽出物のデータを考慮に入れた:時間が支配的な効果を持っているように思われる一方で、高温は、酸化、エピマー化、重合現象を引き起こす分子の破壊につながる。このことから、ホット+アイス法での急冷がこれらの影響を抑え、高温に長時間さらされなかった分子に保護効果を発揮したと推測される。
FRAP値
緑茶については、抽出方法に違いはなく、高い値が記録された(表2).2)。このことは、緑茶には抗酸化化合物が豊富に含まれていることを確認し、この活性に関与する化合物も高温で安定していることを示唆している。
逆に、最も低い値を記録したのはウーロン茶であった。また、冷間抽出やホット+氷抽出の方がホットインフュージョンよりも高い値を示したことから、ウーロン茶のFRAP試験で反応する化合物は高温に非常に敏感であると推測される(Damiani er al)。 また、低温法では抽出時間が長くなるほど交換面が高くなるため、より多くの活性化合物が抽出されたのではないかと推測される。同時に、低温は抗酸化分子を分解から保護していた。
同様の挙動は紅茶についても見られた:ホット+氷の注入が最も高い値を示したが、他の抽出物の間に有意な差は観察されなかった。
お茶の挙動の間の高い変動性は、抗酸化活性を担う化合物のパターンが異なっていること、および/または葉からの活性分子の移動の異なる速度論が発生したことを示唆している。
それにもかかわらず、茶葉の組成物および注入濃度が、栽培品種の種類、栽培環境、摘み取り慣行および製造条件などの多くのパラメータに依存することを念頭に置くことが重要である(Astill et al 2001; Dias et al 2014)。
リカートータルカラー(LTC)と測色パラメータ
また、ホットインフュージョンのサンプルは、コールドのサンプルと比較して総酒色が有意に高く(表(表3),3)ホット+アイスのサンプルと比較して有意に高い値を示した。Kim er al)。 (2007)は、緑茶の場合、加熱温度とともにL*が減少し、a*とb*が増加することを報告しており、カテキンの酸化やクロロフィルの分解により、茶液の緑色が薄くなり、黄色が濃くなることを示唆している。アイスインフューズは、固液比が最も高いにもかかわらず、色の値が最も低い結果となった。
表3 リキュール総色および色判定値(L*, a*, b*)のティーインフュージョンについて
| 緑 | ウーロン茶 | ブラック | |||||||
|---|---|---|---|---|---|---|---|---|---|
| ホット | コールド | ホット+アイス | ホット | コールド | ホット+アイス | ホット | コールド | ホット+アイス | |
| LTC | 10.1±0.0 A | 10.1±0.0 A | 9.5±0.0 A | 9.9±0.0 A | 9.8±0.0 A | 10.0±0.0 A | 11.1±0.0 A | 10.2±0.0 A | 10.4±0.0 A |
| L * | 56.3±0.5 A | 57.5±0.6 A | 56.4±0.5 A | 56.1±0.3 A | 56.9±0.5 A | 57.2±0.8 A | 47.3±0.8 B | 54.4±0.9 A | 46.7±0.8 B |
| a * | −4.4±0.1 a | −4.8±0.1 b | −4.9±0.1 b | −4.7±0.1 a | −4.6±0.1 a | −5.1±0.4 a | 1.1±0.1 B | −3.8±0.0 c | 2.6±0.1 A |
| b * | 7.9±0.2 B | 4.7±0.5 C | 11.3±0.2 A | 10.1±0.2 A | 7.9±0.1 B | 9.5±1.7 A | 35.6±1.2 B | 18.3±0.2 C | 44.7±2.0 A |
略語 LTCリキッドトータルカラー
a,b,c各行内の同一文字は有意差なし(n = 10; p < 0.05)
画像分析による指標については、ウーロン茶ではL*、a*、b*に有意差は認められず、非常に淡い色調であることから、この方法では感度が低く、色の違いを区別することができなかったのではないかと考えられる。一方、緑茶については、a*では、ホットサンプルが他のサンプルに比べて有意に緑が少ないことから、高温でのカテキンの酸化やクロロフィルの分解が確認され、b*では、ホット+アイス<ホット<コールドの順で、b*の値が最も高く、より黄色味が強いことがわかった。
最後に、紅茶の場合、低温抽出のL*値は、ホット+氷とホットの両方の方法と比較して有意に高く、逆に、コールドサンプルは緑色に対応する負のa*値を示したが、ホットとホット+氷の両方は正の値を示し、赤色に対応し、後者の方が有意に高い値を示した。おそらく、低温試料では高温の影響でクロロフィルがフェオフィチンに分解されず、注入後も葉の色が維持されていたのではないかと考えられる。
また、b*値はすべてのサンプルで有意な差が見られ、高温+氷の方が黄色味が強く、低温の方が黄色味が少ないことがわかった。
消費者試験
24名の専門家ではないパネリストによって順位付けテストが行われたため、嗜好性を仮定した場合の有意値は13.6(ISO 2006)に等しくなった。結果は、紅茶では冷たいものと熱いもの+氷、緑茶では冷たいものと熱いもの+氷、熱いものと熱いもの+氷の間でのみ有意な嗜好性が示され、前者のサンプルに嗜好性があることが示された。ウーロン茶については、有意な差は観察されなかった。このように、専門家ではない消費者は、ホット+アイスの方が渋みが強く、アロマティックな香りを持つ化合物の濃度が高いため、ホット+アイスを好まなかったと考えられる。
相関関係
データはピアソンの相関指数を評価して分析した。紅茶については、FRAPデータはカテキンと有意な相関を示したが(R2 > 0.86, p < 0.01)総フェノール含量(TPC)とは相関しなかった。この挙動は、FRAPとFolin試薬が注入液に含まれるいくつかの抗酸化化合物と異なる速度で異なる反応をすることを考慮に入れて説明することができる。
TPCはL*(R2 > 0.96, p < 0.01)と有意に直接相関し、他の指標(a*とb*, R2 < -0.90, p < 0.01)とは逆相関し、ランキングテストの結果(R2 = -0.92, p < 0.01)と相関していた。
ウーロン茶では、カフェインは苦味への寄与の鍵を握る味として同定された以前の報告(Scharbert and Hofmann 2005)によれば、ランキングテストと逆相関していた(R2 = -0.94, p < 0.01)。さらに、ウーロン茶では、TPCとFRAPがそれらと高い相関を示したことから、カテキンとガロン酸が抗酸化力に強く関与していると認識されている(R2 > 0.89, p < 0.01)。TPCの場合、すべてのキサンチンと高い相関が見られた(R2 > 0.92, p < 0.01)。
他のものとは異なり、緑茶では、TPCとFRAPの相関が見られた(R2 = 0.71, p < 0.01)フェノール化合物と抗酸化活性との関連性を確認した(Samaniego-Sánchez er al)。
グリーンとウーロンのサンプルでは、ECとEGCGはb*値と相関していた(R2 > 0.86,p < 0.01)Kim et al 2007)と一致しており、カテキンの酸化が色の変化に関与している可能性を示唆している。注目すべき点は、全酒色(TLC)との相関が記録されていないことで、この分析が異なる方法を比較するのに適していないことを示している。
結論
従来の熱間抽出法と代替法を比較し、化合物の抽出、抗酸化活性、総フェノール含量、色、味の違いを記録した。冷間抽出では、抗酸化活性、総フェノール含量、ガロン酸含量が最も高く、この技術の人気が高まっていることを裏付ける結果となった。革新的な注入法は、高温にさらされることによる生理活性分子の分解を防ぎ、抗酸化特性を高めることを可能にする。また、低温注入法と同様の特性を短時間で得ることができる。
ピアソンの相関関係は、消費者の受容性がカフェイン、カテキン、総フェノール含量、酒の色などのパラメータと有意に相関しており、全体的な味に貢献していることを示していると解釈できる。
本研究は、従来の方法によらない調製法の効果や、葉からの活性化合物の抽出に関する新たな情報を追加するものである。得られた結果は、さまざまな茶葉の調製方法によって、潜在的な健康効果を最大化するための新たな方法の調査に貢献する可能性がある。