Contents
Dementia and co-occurring chronic conditions: a systematic literature review to identify what is known and where are the gaps in the evidence?
www.ncbi.nlm.nih.gov/pmc/articles/PMC5962963/
オンライン版2017 Feb 1
要旨
目的
複数の慢性疾患を抱えながら生活する人々が直面する課題は、認知症やその他の重大な認知機能障害を持つ人々に特有のものである。疾患管理、移動性、死亡率に対する認知機能障害の影響をよりよく理解するために、慢性疾患と認知症の併発に関する既存の文献を見直すことが近年求められている。
方法
本研究では,高齢者,中等度から重度の認知機能障害(認知症と診断されたもの,診断されていないものを含む),および慢性疾患をキーワードとして,PubMedデータベースを2011年までに検索した(2016年に更新)。査読者は、論文の適格性を評価し、掲載された各論文から主要なデータを抽出した。独立した専門家パネルが、エビデンスの強さと質を評価し、今後の研究に必要なギャップを優先した。
結果
433件の論文が確認され、そのうち147件がレビューの基準を満たしていた。その結果、中等度から重度の認知機能障害は、複数の慢性疾患を持つ人の死亡リスクを高め、施設滞在の長期化や機能低下と関連していた。また、重度の認知機能障害と、心血管疾患や高血圧症の治療薬の使用との間には、関連性は認められなかった。今後の研究課題としては、入院、疾患別アウトカム、糖尿病、慢性疼痛、心血管疾患、うつ病、転倒、脳卒中、複数の慢性疾患などが挙げられた。
結論
本レビューでは、重大な認知機能障害や認知症を抱えながら生活することが、複数の慢性疾患を抱える人々の死亡率、施設入所、機能的アウトカムに悪影響を及ぼすことをまとめた。今回の知見から、慢性疾患管理のための介入は、共存する認知機能障害に対処する必要があることが示唆された。
キーワード:認知症、認知機能障害、複数の慢性疾患、系統的文献レビュー、公衆衛生、高齢化
はじめに
現在、世界には4400万人の認知症患者がおり(米国では500万人(Hebert et al 2013))その数は2050年までに3倍以上になると予想されている(Prince et al 2013)。認知症は、あらゆる慢性疾患の中で、高齢者の障害や介護の必要性の最大の原因となっており(Wimo and Prince, 2010)認知症の総金銭コストは、心臓病やがんと同様の経済的負担となっている(Hurd er al)。 認知症は、近年、公衆衛生上の介入対象となる重要な慢性疾患として認識されている(Machlin and Soni, 2009; Goodman et al 2013)。
現在、高齢者の数が増加し、慢性疾患が主要な死因となっていることから、複数の慢性疾患を抱えながら生活する人々が直面する課題が認識されている(Goodman er al)。 最近の米国メディケア受給者のデータによると、認知症患者の4人に1人が脳卒中を併発し(24%)3人に1人が冠動脈疾患を併発していることが示唆されている(National Academy on an Aging Society, 2000)。認知症が進行すると、記憶力、言語力、判断力、推論力が低下するため、症状や副作用を認識して報告すること、投薬を継続すること、治療や経過観察を遵守することが困難になる(McGuire et al 2006,Boustani et al 2007,Arlt et al 2008,Puntakee et al 2012)。また、認知症の高齢者は、機能障害のない高齢者に比べて医療費が高い(Hill et al 2002,Frytak et al 2008,Kuo et al 2008,Zhao et al 2008,Marengoni et al 2009,Suehs et al 2013)。同時に、複数の慢性疾患を持つ人は不均衡な数の医療を消費しており(Thorpe et al 2010; Centers for Medicare and Medicaid Services (CMMS), 2012)複数の慢性疾患を持つ人には、より多くのケアコーディネーションとより高い自己管理スキルが求められている(Redelmeier et al 1998; Committee on Quality of HealthCare in America, 2001)。
認知症と併発する慢性疾患の関係を公衆衛生の観点からよりよく理解することが必要である。「ヘルシー・ブレイン・イニシアティブ」。The Public Health Road Map for State and National Partnerships, 2013-2018 ((Alzheimer’s Association (AA) and Centers for Disease Control and Prevention (CDC), 2013) は、”うつ病、疾病管理、罹患率、死亡率などの様々なアウトカムに対する認知症の影響を理解するために、アルツハイマー病を含む慢性疾患sと認知症の併発に関する文献をレビューすること “を求めている。このシステマティックな文献レビューでは、中等度から重度の認知機能障害(診断された認知症と診断されていない認知症の両方を含む)が共起する慢性疾患に与える影響を検証し、現在わかっていること、研究文献に残っているギャップを記録している。
方法
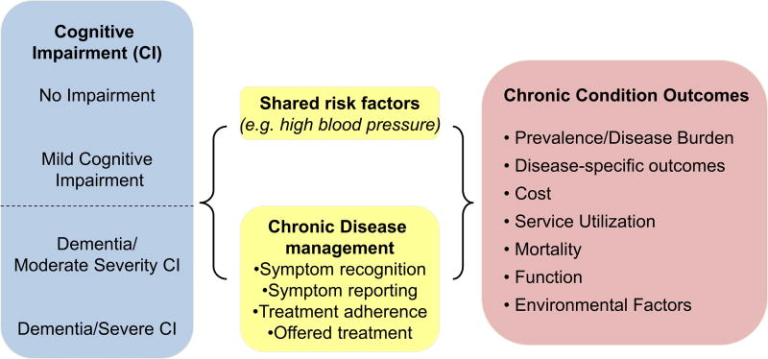
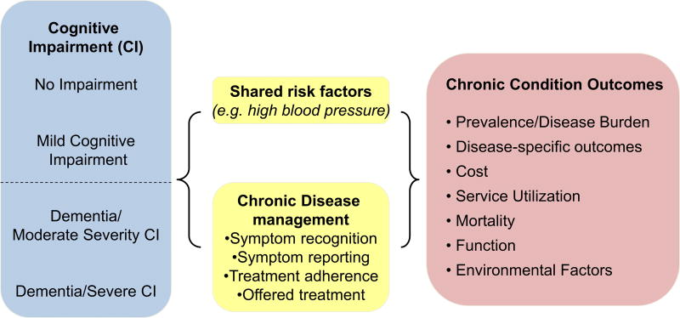
概念的枠組み(図1)は、米国国立衛生研究所(NIH)のCognitive and Emotional Health Projectに基づいて作成された。このプロジェクトでは、中等度から重度の認知機能障害が、共通の危険因子(高血圧など)や疾患管理(症状の認識、報告、治療の継続など)を通じて、どのように慢性疾患を併発するかを明らかにした(NIH, 2001; Hendrie et al 2006)。アウトカムとしては、疾患固有のアウトカム(例:中等度から重度の認知障害があり、脳卒中の既往がある人の脳卒中の再発)医療費(例:外来・入院医療費)サービス利用(例:入院・施設入所)死亡率、機能などが挙げられる。
図1 概念的枠組み。[カラー図はwileyonlinelibrary.comで見ることができる】。
レビュー方法は、Guide to Community Preventive Services “The Guide” (Briss et al 2000; Norris et al 2002)および過去に実施されたシステマティックレビュー(Frederick et al 2007; Snowden et al 2011)を参考にし、PRISMAガイドライン(Moher et al 2009)に沿ったものとした。PubMedを用いて,創刊時(1967)から 2011年までの査読付き文献を検索した。主題の見出しとテキストワードは,高齢者,中等度から重度の認知障害,および慢性疾患の主要な構成要素を反映したものとした(表1)。また,メタアナリシス,レビュー論文,掲載された論文の参考文献を調べ,論文の可能性を検討した。
表1 PubMed検索用語
| 構築する | 検索ワード | |
|---|---|---|
| 高齢者 | 高齢者[mh] | |
| 80歳以上[mh] | ||
| フレイル高齢者[mh] | ||
| 高齢者[ティアブ] | ||
| 高齢者[tiab] | ||
| 先輩[tiab]) | ||
| 認識機能障害 | 認知症[mh] | |
| 「認知障害」[tiab] | ||
| MCI [tiab] | ||
| CIND [tiab] | ||
| 慢性疾患と老年症候群 | 偶発的な転倒[Majr] | うつ病[Majr] |
| 高脂血症[Majr] | 統合失調症[Majr] | |
| 肺疾患、慢性閉塞性肺疾患[Majr] | 多発性硬化症[Majr] | |
| 肺気腫[Majr] | 骨の病気[Majr] | |
| 糖尿病[Majr] | 慢性的な痛み[ティアブ] | |
| 心血管疾患[Majr] | 変形性関節症[Majr] | |
| 心血管疾患[tiab] | フレイル[ティアブ] | |
| 頭蓋内動脈疾患[Majr] | てんかん[Majr] | |
| 頸動脈疾患[Majr] | 脳虚血[Majr] | |
| 高血圧[tiab] | ストローク[Majr] | |
| 心臓病[ティアブ] | 睡眠障害[Majr] | |
| 新生物[Majr] | 口腔衛生[Majr] | |
| パーキンソン症候群[Majr] | 尿失禁[Majr] | |
| 喘息[Majr] | 骨粗鬆症[Majr] | |
| 物質関連障害[Majr] | 併存症[Majr] | |
| ストレス障害、心的外傷後[Majr] | 併存疾患[tiab] | |
| 双極性障害[tiab] | 併存症[tiab] | |
| 躁うつ病[tiab] | 慢性疾患[Majr] | |
| 研究デザイン | 横断研究[メッシュ] OR断面スタッド* [tiab] ORコホート研究[メッシュ] ORコホートスタッド* [tiab] ORケースコントロール研究[メッシュ] ORケースコントロールスタッド* [tiab] OR縦断スタッド* [tiab]または縦方向のスタッド* [tiab]または将来のスタッド* [tiab]または遡及的なスタッド* [tiab] | |
[Mesh]はMedical subject headings,[mh]はMeSH見出しの検索,[majr]は論文の主要なトピックであるMeSH見出しの検索,[tiab]はタイトルまたはアブストラクトである。
a注:英語のみの研究の制限も設定した。
除外・包含基準
研究の除外基準は以下の通り。(i)サンプルサイズが100以上、(ii)参加者が50歳以上、(iii)中等度から重度の認知機能障害を持つ集団と持たない集団の両方のデータ、(iv)認知症または中等度から重度の認知機能障害の有効かつ信頼性の高い測定値、(v)少なくとも1つの他の慢性疾患または老年症候群または共存性の測定値、(vi)共存する慢性疾患に対する認知機能障害の有病率または効果の記述。
認知機能障害を定義するために、論文には有効かつ信頼性の高い認知症の臨床診断(例えば、Diagnostic Statistical Manual criteria, fourth edition (DSM-IV) (American Psychiatric Association, 2000); National Institute of Neurological and Communicative Disorders and Stroke and the Alzheimer’s Disease and Related Disorders Association (NINCDS-ADRDA) criteria for Alzheimer’s disease (Mckhann et al, 1984年)血管性認知症のNINDS-AIREN(National Institute of Neurological Disorders and Stroke and Association Internationale pour la Recherché et l’Enseignement en Neurosciences)基準(Erkinjuntti, 1994年)または記憶と実行機能や言語など少なくとも1つの他の認知領域を捉えた中等度から重度の認知機能障害の有効で信頼性の高い尺度。これらには、多次元的な測定法(例えば、Mini-Mental Status Examination(MMSE))も含まれる。(Folstein et al 1975)や、複数の個別の認知機能測定法のうち、少なくとも1つは記憶に焦点を当てたものである。今回のレビューでは、中等度から重度の認知機能障害に焦点を当て、正式な認知症の診断を受けた人と受けていない人を含めた。正式な診断を受けていない人の割合が高いことから、後者のグループを対象とした。現在、認知症の診断を受けている人は、高所得国では半数以下、低・中所得国では10%以下とされている(Prince et al 2013)。
専門家パネルは、慢性疾患の定義を「1年以上継続し、継続的な医療を必要とし、かつ/または日常生活動作(ADL)を制限する状態」(Warshaw, 2006; US DHHS, 2010)とし、The NIH Cognitive and Emotional Health Project(Hendrie et al 2006)U.S. DHHS multiple chronic conditions (M慢性疾患) Strategic Framework(US DHHS, 2010)およびPubMedの疾患カテゴリーから、一般的な慢性疾患のリスト(表2)を作成した。生活の質や障害に大きな影響を及ぼすことから、老年症候群(フレイルやポリファーマシーなど)も対象とした(Inouye er al 2007)。老年症候群とは、高齢者によく見られるが、個別の疾患カテゴリーには当てはまらない症状である(Ahmed er al 2007,Inouye er al 2007,Chaudhry er al 2010)。このレビューに含めるためには、少なくとも1つの慢性疾患疾患または老年症候群(表2)を持つ人を対象とするか、有効で信頼性の高い共存性の指標(Charlson’s Comorbidity Indexなど)を用いて共存性を証明する必要があった(Charlson et al 1987)。
表2 慢性疾患と老年症候群
| 慢性疾患 | 老年症候群 |
|---|---|
| 喘息 | 転倒、骨折、その他の怪我 |
| 関節炎 | フレイル |
| 骨疾患(例、骨粗鬆症) | 機能障害 |
| 脳疾患(例、パーキンソン病) | 多剤併用/高リスク薬 |
| 癌 | 尿失禁。 |
| 心血管疾患(例、CAD、高血圧、高脂血症) | |
| 脳血管障害(例、脳卒中) | |
| 慢性腎臓病 | |
| 慢性の痛み | |
| 歯の問題 | |
| うつ病およびその他の慢性精神疾患(PTSD、統合失調症、双極性障害) | |
| 糖尿病 | |
| 肺気腫/ COPD | |
| 神経学的状態(てんかんおよび多発性硬化症) | |
| 睡眠障害 | |
| 薬物乱用 | |
| 慢性状態が存在する場合の危険因子(例、肥満、喫煙、歩行) |
論文は、世界中の地域社会に住む人々と施設に入所している人々の両方を対象とした。英語で発表されていない論文、認知機能障害や認知症のICD診断のみを用いている論文、認知機能障害をせん妄、外傷性脳損傷、発達障害、MCIと定義している論文、レビュー、コメンタリー、メタアナリシスのみを報告している論文は除外した。
データ収集
論文が組み入れ基準を満たしているかどうかを評価するために,2段階のスクリーニングプロセスを用いた。まず、タイトルと要旨を確認した。要旨だけでは組み入れられない、あるいは除外された論文は、2回目のスクリーニングで全文を調べた。タイトルと要旨の審査は、80%の合意が得られるまで、研究チームのメンバー(LS、LB、慢性疾患)が共同で行い、その後のタイトルと要旨の審査は別々に行った。論文の審査は各審査員が行った。論文が適格性基準を満たしているかどうかを再確認するために、別の研究チームメンバーが受理された論文のデータを抽出した。査読者は週に一度、タイトル・要旨と論文の審査について話し合った。査読者間で疑問や意見の相違が解消されない場合は、研究責任者(MS)が最終的な判断を下した。
エビデンスの評価
標準化されたフォームを用いて、各論文から、研究デザイン、サンプルサイズ、設定、慢性疾患の併発、アウトカム指標、結果、研究の質を示す指標(交絡因子の調整など)などのデータを系統的に収集した。データは、エビデンス評価のための要約表にまとめられた(付録参照)。エビデンスを分類的に評価するために、論文を慢性疾患とアウトカムの組み合わせにグループ化し、パネリストは各グループ内のエビデンス全体を評価した。
専門家パネルのメンバーは、過去のシステマティックな文献レビューの定性的なアプローチを用いて、各慢性疾患とアウトカムの組み合わせにおける論文のエビデンスの質と強さの両方を評価した(Frederick er al 2007; Snowden er al 2011)。質の指標としては、サンプルサイズと一般化可能性、認知障害と慢性疾患の適切な測定、多変量解析の使用、年齢、性別、教育を具体的にコントロールすることなどが挙げられた。質の評価については、パネルメンバーがそれぞれの条件と結果の組み合わせを「良い」、「まあまあ」、「限定的」と独立して評価した。
エビデンスの強さを示す指標としては、研究の質とデザイン、慢性的な条件と結果の組み合わせにおける研究の数、研究間の一貫性、および統計的所見が挙げられた。エビデンスの強さの評価については、パネルメンバーが、各条件と結果の組み合わせについて、「強い」、「十分」、「不十分」のいずれかに独立して評価した(不十分の評価は、少なくとも公正な質の研究の数が不十分であったか、利用可能な研究の数は十分であったが結論の出ないデータであったかを記録した)。
証拠の質と強さの最終決定は、パネルメンバーの80%の同意(すなわち、7人のパネリストのうち6人の同意)に基づいて行われた。意見が一致しなかった部分についてはパネルで議論し、パネルメンバーは議論の後に投票を変更することができたが、説得力のあるバイアスを減らすために、合意に達することは求められなかった。
エビデンスが “不十分 “と評価されたギャップの特定と優先順位付け
また、パネルは、エビデンスが不十分な領域を特定し、優先順位をつけた。Qソートランキング(Brown, 1996)という項目の順位付けを行う手法を用いてギャップの優先順位付けを行った。パネリストは、エビデンスが不十分な42のアウトカムと慢性疾患/老年症候群のそれぞれについて、今後の研究の優先順位(「5」=最も高い優先順位、「1」=最も低い優先順位)を付けた。Qソート法を用いて、情報提供者に1,2,3,4,5の限られた正規分布の割り当てを行い、順位の正規分布を作成した。
結果
文献調査の結果,4,33件の論文が確認された。PubMed検索では4,005件,レビュー論文やメタアナリシスの参考文献リストから 28件を抽出した(図2)。レベル1の要旨審査で48件,レベル2の要旨審査で99件の論文が組み入れ基準を満たし,147件の論文が組み入れられた。除外された理由は、サンプル数が少ないことや、認知症・認知機能障害のある人とない人の両方が含まれていないことなどである。
図2 文献検索のフローチャート
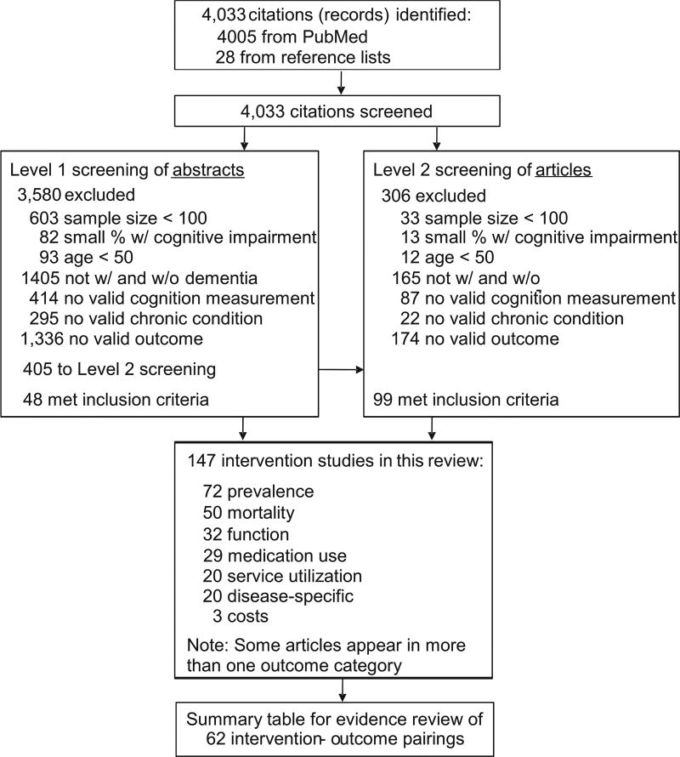
収録された147件の論文は、エビデンスを評価するために、62の慢性疾患とアウトカムの組み合わせ、つまりカテゴリーに分類された。十分なエビデンスがあると評価されたのは9%(N=7)で、そのすべてが少なくとも公正な品質であると評価された(表3)。中等度から重度の認知機能障害が、特定の慢性疾患を併発している人の死亡率、施設での滞在期間、機能、心血管治療薬の使用に及ぼす影響については、十分なエビデンスが得られた。その他の組み合わせについては、研究数が少ない(2件以下)または決定的な証拠がない(研究内または研究間で結果が混在している)ため、十分な証拠がないと判断された(表4)。
表3 十分な証拠がある慢性疾患とアウトカムの組み合わせの証拠評価の概要
心血管疾患は心血管疾患、M慢性疾患は複数の慢性疾患、NHは介護施設。
a147件の研究の中には、複数の慢性疾患と結果の組み合わせで掲載されているものもある。また、地域住民と臨床住民の両方を対象とした論文もある。
b 質の評価は「良い」「普通」「限定的」。効果の評価は、「強い」、「十分」、「不十分」。7人の専門家パネリストが品質と効果を個別に評価し、その後、意見を集約した。
c心血管疾患治療薬には、抗高血圧薬以外のものを含む。
表4
十分な研究が行われていないために十分な証拠が得られていない慢性疾患とアウトカムの組み合わせに関する証拠評価の要約。研究結果が混在している、または結論が出ていないためにエビデンスが不十分なカテゴリーは斜体で記載されている。)
CHFはうっ血性心不全、心血管疾患は心血管疾患、NCは合意なし、M慢性疾患は複数の慢性疾患、NHは介護施設。
a各慢性疾患とアウトカムの組み合わせの論文引用は、共著者に連絡すれば入手できる。147件の研究の中には、2つ以上の慢性疾患と結果の組み合わせで掲載されているものもある。
b少なくとも6人の専門家パネリストが、研究数が少ない(通常2件以下)ために証拠不十分と評価した。エビデンスが混在しているカテゴリーは、イタリック体で表示されている。
*一部の研究は複数の論文に記載されている(例:文献132と133には同じ研究が記載されている)。
死亡率
29件の研究(Kukull et al 1994年、Arfken et al 1995年、Bruce et al 1995年、Gale et al 1996年、Agüero-Torres et al 1999年、Foley et al 1999年、Kammoun et al 2000,Helmer et al 2001,Stump et al 2001,Freels et al 2001)。2001;Freels et al 2002;Ganguli et al 2002;Feil et al 2003;Nguyen et al 2003;Tschanz et al 2004;Cacciatore et al 2005;Fitzpatrick et al 2005;Magaziner et al 2005;Bursi et al 2005年。2006; Guhne et al 2006; Llinàs-Regla et al 2007; Lyketsos et al 2007; Meerman et al 2008; Rothman et al 2008; Zekry et al 2009; Lavretsky et al 2010; Wang et al 2010a; Gombojav et al, 2011; Millán-Calenti et al 2011; Nikolova et al 2011)では、複数の慢性疾患を有し、中等度から重度の認知機能障害や認知症を有する人と有しない人の死亡率を比較した。17件はコミュニティベースのサンプルを使用し、12件はクリニックベースのサンプルを使用した。ほとんどの研究はサンプルサイズが500以上(79%)で、52,644人の被験者を対象としていた。大半の研究が多変量解析を採用しており(90%)そのうち約半数(46%)が年齢、性別、教育を調整していた(残りの研究はこれらの人口統計学的共変量のうち1つまたは2つのみを調整していた)。
死亡率は、死亡率、死亡リスク(ハザード比(HR)など)生存率のいずれかで測定された。死亡率は、中等度から重度の認知機能障害のある人では40.2%から82%、重度の認知機能障害のない人では16.0%から37.7%であった(Stump et al 2001,Nguyen et al 2003,Tschanz et al 2004,Guhne et al 2006,Llinàs-Regla et al 2007,Lavretsky et al 2010,Wang et al 2010a)。6件の研究(Bruce et al 1995年、Stump et al 2001,Fitzpatrick et al 2005,Llinàs-Regla et al 2007,Meerman et al 2008,Lavretskyら。Llinàs-Regla et al 2007)から7.4(4.9-11.4)(Lavretsky et al 2010)までの範囲の死亡率の未調整相対リスク(RR)(95%信頼区間(CI))が報告された。
14件の研究(Helmer et al 2001,Stump et al 2001,Freels et al 2002,Feil et al 2003,Nguyen et al 2003,Tschanz et al 2004,Fitzpatrick et al 2005,Bursi et al 2006,Guhne et al 2006,Llinàs-Regla et al 2007,Meerman et al 2008,Rothman et al 2008,Lavretsky et al 2010,Gombojavら。2011)は、重大な認知機能障害の死亡リスクに対する調整後HR(95%CI)が1.5(1.1~2.1)(Rothman et al 2008)から 2.99(2.53~3.53)(Tschanz et al 2004)までの範囲で報告されており、共変量には人口統計、慢性疾患、その他6つの虚弱基準が含まれていたと考えられる(Rothman et al 2008)。認知症診断に関連した死亡の帰属リスク(PAR%)は、11.8%(Guhne et al 2006,Llinàs-Regla et al 2007)から 16.6%(Tschanz et al 2004)の範囲であった。Tschanz (Tschanz et al 2004) と Feil (Feil et al 2003) は、認知症の死亡率 RR と PAR を他の 慢性疾患 と比較している。また、2つの研究(Feil et al 2003; Tschanz et al 2004)では、認知症または中等度から重度の認知機能障害は、他の慢性疾患に比べて死亡率のRRが大きく(例えば、RRが2〜3倍)、死亡率PAR%も高いことがわかった。
さらに、中等度から重度の認知機能障害者は、平均生存期間が短く、認知機能障害のない人の4.0年から 11.0年に比べ、3.0年から7.1年であった(Agüero-Torres et al 1999年、Fitzpatrick et al 2005,Guhne et al 2006,Lavretsky et al 2010,Wang et al 2010a)。中等度から重度の認知機能障害者は生存率も低く、中等度から重度の認知機能障害者の調整後の5年生存率は16.1%対正常な認知機能障害者の28.5%(Wang et al 2010a)調整前の生存率は22%対39%(Bursi et al 2006)MMSEのスコアが低い(悪い)と生存の可能性が低くなる(Bruce et al 1995)。
いくつかの研究では、有意ではない、あるいは負の関係が報告されている。例えば 2005年にMagaziner et al 2005)は、認知症で複数の慢性疾患を持つ人の死亡率の調整前RRは0.61(0.53-0.71)調整後RRは0.63(0.51-0.77)と報告した。本研究では、老人ホームに入居している人(N=2,153,平均年齢>80歳)を対象とし、そのほぼ半数がDSM基準で認知症と診断されていた。この研究では、認知症ではないグループには、診断が困難な人が含まれてた。
また、専門家パネルは、中等度から重度の認知機能障害がパーキンソン病患者の死亡率を高めることを示す十分な証拠を見つけた(Ebmeier et al 1990年、Marder et al 1991年、MitchellとRockwood 2000,Levy et al 2002,Parashos et al 2002)。2002; Parashos et al 2002; Buter et al 2008; Lo et al 2009; Hobson et al 2010, N = 4,513)および脳卒中(Tatemichi et al 1994; Desmond et al 1998; Desmond et al 2002; Liebetrau et al 2003; Melkas et al 2009; Oksala et al 2009, N = 2,302)。これらは、死亡率を検討するのに十分な証拠が見つかった唯一の特定の共起性慢性疾患であった。その他の論文では、様々な原因(脳卒中、パーキンソン病、その他)による認知症または中等度から重度の認知機能障害を持つ人を対象としていた。
サービス利用
3つの研究(Smith et al 2000; Magaziner et al 2005; Rothman et al 2008, (N = 3,423))では、複数の慢性疾患を持つ人の施設滞在期間が調査された(Inouye et al 2007)。2008,Rothman et al 2008)は、認知機能障害(MMSE<24)のある人とない人の長期介護施設滞在の調整後HRは3.7(95%CI)2.5-5.4であると報告した。2000,Smith et al 2000)は、DSM-III-R基準で診断された認知症患者の介護施設滞在期間の中央値を無調整で946日としたのに対し、認知症でない患者は579日であった。最後に、Magazinerらは、DSM-III-R基準で診断された認知症患者は、そうでない患者に比べて、自宅に退院する可能性が低いことを報告している(調整後RR 0.23 (95% CI 0.17-0.31))。
機能
19の研究(Agüero-Torres et al 1998年、Zhu et al 1998年、Agüero-Torres et al 2002,Covinsky et al 2003,Lyketsos et al 2005,Magaziner et al 2005,Lyketsos et al 2007,Cankurtaran et al 2008,Rothman et al 2008,Zekry et al 2008)。2008,Zekry et al 2008,Huang et al 2009,Sousa et al 2009,Stewart et al 2009,Zekry et al 2009,Feng et al 2010,Wang et al 2010b、Gombojav et al 2011,Millán-Calenti et al 2011,Nikolova et al 2011)。) (N = 37,466)では、重大な認知機能障害と複数の併存疾患の共存が機能に及ぼす影響を検討した。機能とは、通常、基本的な日常生活動作(ADL)または手段的ADL(IADL)と定義される。9件の研究では、認知症と診断されたサンプルを対象とし、7件では施設入所者を対象とした。半数の研究が多変量解析を用いており、そのうち半数は年齢、性別、教育を調整していた。認知症で複数の慢性疾患を持つ人は、著しい認知障害のない人に比べて、IADLおよびADLの障害が有意に多かった。
薬物使用
7つの研究(Freels et al 2002; Lopponen et al 2005; Bursi et al 2006; Rastas et al 2007; Andersson et al 2008; Barzilay et al 2008; Cankurtaran et al 2008)(N = 5,245)では、心血管疾患(心血管疾患)を併発している人の心血管治療薬(高血圧以外)の使用に、認知症がどの程度影響するかが検討された。その結果、認知症(VaD、AD、特記事項なし)とβ遮断薬、ACE阻害薬、アスピリンなどの心血管疾患薬の使用との間に統計的に有意な差を認めたのは、Barzilay et al 2008)のみであった。
また、専門家会議では、中等度から重度の認知機能障害は、高血圧を併発している人の高血圧治療薬の使用に影響を与えないという十分なエビデンスで合意している(Freels er al 2002; Hanon er al 2006; Barzilay et al, 2008; Vinyoles et al 2008; Huang et al 2009; Stewart et al 2009; Gombojav et al 2011)7つの研究のうち5つ(Freels er al)。 (N = 8,236)では、中等度から重度の認知機能障害がある人とない人で、統計的に有意な差がないことが報告されている。
エビデンスのギャップの優先順位付け
専門家パネルは、エビデンスが不十分または皆無の55の組み合わせを特定した(表4)。その中には、18のアウトカム(コストや機能など)と10の慢性疾患または老年症候群(がんや慢性閉塞性肺疾患など)が含まれていた。喘息、関節炎、骨疾患、慢性腎臓病、慢性疼痛、歯科疾患、その他の慢性精神疾患、神経疾患、睡眠障害、物質乱用、他の慢性疾患が存在する場合の危険因子(例:肥満、喫煙)フレイル、機能障害、尿失禁などの14の疾患・症候群に対する著しい認知機能障害の影響についてはエビデンスがなかった。
専門家パネルがこれらのギャップに優先順位をつけた結果、サービス利用-入院と疾患別アウトカム、および糖尿病、慢性疼痛、心血管疾患、うつ病、転倒・骨折、脳卒中、多重慢性疾患(中等度から重度の認知障害があり、他に2つ以上の慢性疾患がある状態)が今後の研究の最優先事項として挙げられた。
レビューの更新
最近 2011年半ばから 2016年6月の間に発表された、より新しい論文を含めるために、文献レビューを更新するよう依頼された。その結果、22件の論文が基準を満たし、2つの新しい慢性疾患と結果の組み合わせに十分なエビデンスがあることがわかった。1つ目は、認知機能障害と心血管疾患の併発が死亡率に及ぼす影響について調べたものである。2つの研究(O’Donnell et al 2012年およびHuijts et al 2013)では、中等度から重度の認知機能障害を有
する人の死亡リスクが50%以上増加することが明らかになった(調整後のHRは1.53(95%CI 1.02-2.30)から 1.68(1.49-1.90))。2つ目の新しいアウトカムは疾患特異的なもので、すなわち、認知症と糖尿病を併せ持つ生活は、糖尿病と認知症を併せ持たない生活者と比較して、重度の低血糖症のリスクを高めるというものであった(Abbatecola et al 2015,Prinz et al 2015)。新たに14件の論文(Chang et al 2012,Chen et al 2014,Huijts et al 2013,Llibre et al 2014,Katsoulis et al 2014,Lee et al 2015,Mignardot et al 2014,Murao et al 2014,O’Donnell et al 2012,Park et al 2016,Sanyal et al 2014,Warchol-Celinska et al 2015,van Aschら、。2013)は、既存の慢性疾患とアウトカムの組み合わせに当てはまり、エビデンスの質や強さに変化はなかった。また、4つの論文(Hawkins et al 2012;Jacobs et al 2012;Hajduk et al 2013;Provencher et al 2015)は、これまでエビデンスがなかった別の分野で発見された。
考察
このレビューでは、中等度から重度の認知機能障害(診断された認知症と診断されていない認知症の両方を含む)が、慢性疾患を併発している場合、死亡率の増加、施設での滞在期間の増加、機能の低下に有意な影響を及ぼすという十分なエビデンスが得られた。さらに、中等度から重度の認知機能障害は、心血管疾患や高血圧症の薬の使用とは関連しないという十分な証拠があった。その他のアウトカムと慢性疾患の組み合わせについては、パネルは十分なエビデンスがない、あるいはエビデンスがないと判断した。
高齢者を対象とした過去の研究では、認知機能低下と心血管疾患などの他の慢性疾患を併発する複数の危険因子が確認されている(NIH, 2001)。重度の認知機能障害を有する高齢者とそうでない高齢者を比較すると、前者の方が病気がちであり、複数の慢性疾患を抱え、機能障害が大きいことが示唆されている(Hill et al 2002,Bynum et al 2004,Frytak et al 2008,Kuo et al 2008,Zhao et al 2008,Marengoni et al 2009)。今回のレビューでは、これらの初期の知見(特に死亡率、施設滞在期間、機能低下のリスク)が部分的に確認され、さらに、重大な認知機能障害自体が、その後の高齢者の他の慢性疾患や症候群の発症に影響を及ぼす可能性があることが確認された。このレビューで見つかった十分なエビデンスのほとんどは、中等度から重度の認知機能障害と複数の慢性疾患に関するものであり、著しい認知機能障害と特定の慢性疾患(例:うつ病)の経過との関係を支持するエビデンスは十分ではなかった。
中等度から重度の認知機能障害(診断された認知症と診断されていない認知症の両方を含む)は、臨床的な悪化と関連している。また、認知機能が著しく低下すると、慢性疾患、老年症候群、機能低下などの初期症状に気づかず、適切な対応ができなくなる可能性が高くなる。診断時の重症度が高いことや、薬物療法の維持や副作用の管理ができないことは、少なくとも部分的には、重大な認知障害を持つ高齢者の医療費が、そうでない人に比べて増加する原因となっている可能性がある(Gutterman et al 1999)。重大な認知機能障害を持つ人のモニタリングを改善する政策と手続きは、タイムリーな診断と治療を促し、十分なサポートがあれば重症度を下げ、健康の改善を促進することができる。さらに、複数の慢性疾患を持つ人の認知能力を評価することは、医療従事者の疾病管理の改善に役立つ可能性がある。薬の管理が困難であることが、薬の入手に影響しないことは心強いかもしれないが、罹患者が自分の状態をコントロールするためには、さらなる支援が必要かもしれない。
既存のエビデンスを検討し、ギャップを明らかにすることは、臨床医、研究者、政策立案者が、国際的、国内的、地域的なレベルで、重大な認知機能障害が慢性疾患に及ぼす影響を理解し、エビデンスに基づいた適切な疾患管理プログラムを設計・提供するための第一歩となる。NIHの「Cognitive and Emotional Health Project」(NIH, 2001; Hendrie et al 2006)やCDCの「Healthy Brain Initiative」(CDC and the AA, 2007; AA and CDC, 2013)などのいくつかの国家機関では、これらの重要な研究ギャップに答えるために既存のデータセットを特定して使用することを強調している。我々の研究チームと諮問委員会は、認知障害と慢性疾患の両方の測定値を含む既存の主要データセットの目録を作成した(Bell er al)。 本レビューで得られた知見は、Healthy People 2020の目標(US DHHS ODPHP, 2010)である、1つ以上の慢性疾患を持つ高齢者のうち、自分の状態を管理する自信があると報告する人の割合を増やし、アルツハイマー病やその他の認知症の人の予防可能な入院(多くは慢性疾患を併発している)の数を減らすことにも役立つ。
このシステマティックレビューの強みは、重大な認知機能障害が慢性疾患に与える影響に焦点を当てていること、Guide to Community Preventive Services(Briss et al 2000,Norris et al 2002)を参考にした正式なプロセスを採用していること、経験豊富な研究チーム(Frederick et al 2007,Snowden et al 2011年)学際的な専門家パネルの意見を参考にして、関連する研究を特定し、質を評価し、エビデンスをまとめていることである。慢性疾患が中等度から重度の認知障害にどのような影響を与えるかを調べた文献は、これまでにはるかに多くある。実際には、身体的な状態が精神的な状態に影響を与え、その逆もあり得るという、両方を考慮すること、すなわち双方向性(Mercer er al)。 脳卒中と認知機能障害のような一致した状態とは、これらの状態のうち一方の管理が他方の慢性疾患の管理に影響を与える可能性が高い状態を指す。
このレビューにはいくつかの制限がある。ほとんどのPRISMA推奨ガイドライン(Moher er al 2009)に準拠しているが、研究内および研究間のバイアスのリスクを評価していない。専門家パネルには、研究デザイン、サンプル、測定法、分析、およびアウトカムの詳細を提供し、エビデンスの強さと質の評価に役立ててもらった。第二に,レビューを実施するための時間とリソースの制限から,1つのデータベース(PubMed)のみをレビューした。このデータベースを選んだのは、認知機能障害と慢性疾患を併発した場合の公衆衛生への影響に着目したためである。さらに、機能障害が認知症の診断基準の一部であることを考慮すると、重要な結果としての機能と老年症候群の両方を含めることの複雑さを認識している。複雑ではあるが、機能(および機能障害)は、慢性疾患の管理に大きな影響を与え、それが死亡率やサービス利用などの他のアウトカムにも影響を与えることから、重要なアウトカムであると考えられた。同様に、パーキンソン病や脳卒中は、認知症の原因として確立されており、死亡率のリスクも高いため、これらの疾患で死亡率が上昇するという結果は予想される。最後に、我々の除外基準、特に他の慢性疾患の原因となりうるMCIを除外したことで、参考になる研究が除外された可能性があるが、専門家パネルは、定義やスクリーニング基準が確立されていないことは、要因として評価するにはあまりにも曖昧であるとした。
本レビューで得られた主な知見としては、認知機能障害が、慢性疾患を併発している人々の死亡率、サービス利用率、機能的アウトカムに大きな影響を与えること、また、中等度から重度の認知機能障害と慢性疾患併発時の薬物使用との関連性を支持する強いエビデンスはなかったことなどが挙げられる。さらに、本レビューでは、二次データ分析を含む今後の研究の指針となるよう、エビデンスのギャップを特定し、優先順位をつけた。本システマティックレビューの結果と文献のギャップの特定は、臨床医、研究者、政策立案者が、認知障害の増加に起因する高齢者の慢性疾患sの負担増に対応する能力を強化するものである。
キーポイント
- 高齢化社会において、重大な認知機能障害と慢性疾患sを共存させることは、公衆衛生上の重要な問題である。
- 認知症やその他の重大な認知機能障害が、複数の認知機能障害を持つ人々の罹患率、死亡率、その他の転帰にどのような影響を与えるかについては、ほとんど知られていない。
- 今回のシステマティックレビューでは、中等度から重度の認知機能障害(認知症を含む)が、複数の慢性疾患を持つ人の死亡リスクを高め、施設滞在の長期化や機能低下と関連するという十分なエビデンスが得られた。また、重度の認知機能障害と、心血管疾患や高血圧症の治療薬の使用との間には、関連性は認められなかった。
- 認知症やその他の重大な認知機能障害が、複数の慢性疾患を有する患者の入院、疾患別転帰、糖尿病、慢性疼痛、心血管疾患、うつ病、転倒、脳卒中にどのような影響を及ぼすかについては、さらなる研究が必要である。