コンテンツ
Concern about the Effectiveness of mRNA Vaccination Technology and Its Long-Term Safety: Potential Interference on miRNA Machinery
pubmed.ncbi.nlm.nih.gov/36674919
オンライン公開2023年1月11日doi:10.3390/ijms24021404
Gianmarco Stati,1,*Paolo Amerio,1Mario Nubile,2Silvia Sancilio,1Francesco Rossi,3andRoberta Di Pietro1,4
要旨
COVID-19感染によるパンデミック発生後、公衆衛生上の危機に対処するため、短期間で複数のワクチンが開発された。そこで、より迅速な承認プロセスでmRNAワクチンの投与を可能にするため、緊急時使用承認(EUA)が適用された。SARS-CoV-2のBa.5(オミクロン)変異型は、現在主流となっているものである。その変異の激しい一本鎖RNAゲノムは、高い感染力とともに、ワクチン接種の効果に対する懸念を生んだ。
ワクチンと宿主細胞との相互作用は、幅広い生物学的プロセスを統括する複雑なネットワークであるmiRNAマシンによって細かく制御されている。miRNAの制御異常は、COVID-19感染時の臨床的合併症の発生、さらに、いくつかのヒトの病態、中でも癌疾患と関連しているとされている。
現在、一部の地域ではmRNAワクチンの4回接種が行われているが、その有効性と長期的な安全性について疑問を持つのは当然のことである。
キーワードはCOVID-19、mRNAワクチン、miRNA、SARS-CoV-2、革新的製剤、がん、mRNA1273、BNT162b2
1.はじめに
2020年にパンデミックが発生して以来、COVID-19感染に対抗し、感染者の死亡率や罹患率を減らすために、新しいワクチンを開発するための大きな取り組みが行われていた[1]。米国の疾病管理予防センター(CDC)が定めたガイドラインでは、通常のワクチン開発プロセスで、すべてのフェーズを完了するには約10年かかるとされている。これは、米国食品医薬品局(FDA)のワクチン規制を統括する部門である生物製剤評価研究センターから報告されている。緊急の公衆衛生危機に立ち向かうため、FDAはワクチン開発を加速させるために、通常の規制の多くを回避する必要性を認識した。それが、これまでにない全く新しいワクチン技術であるmRNAワクチンである。コロナウイルスのパンデミックによる世界的な危機に対抗するための主要な手段は、緊急事態においてこれらの治療法の投与を許可するための処理EUAを申請することだった[2]。世界中で、短期的な副作用の割合は限られていることが示されており[3]、短期および中期における一過性の局所的、全身的な反応のみが評価されている[4]からである。何百万人もの患者がmRNAワクチンの投与を受けるようになった今、このようなワクチンの長期的な安全性について疑問を抱くのは当然のことである。
2.懸念されるSARS-CoV-2変異体の違いとワクチン接種の有効性
現在では、COVID-19に対する感受性と個々の患者の特異的な特性との関連はまだ解明されていない。SARS-CoV-2は非常に変異しやすい一本鎖RNAゲノムを示し、これがSARS-CoV-2のいくつかの亜種が世界中で増殖し、このウイルス性疾患のアウトブレイクの複数の波を引き起こしている理由である。それにもかかわらず、SARS-CoV-2の拡散による変異の獲得は、地域拡散の不均一性を説明することができなかった[5]。
オミクロンは、Ba.1(B.1.1.529.1), Ba.2(B.1.1.529.2), Ba.3(B.1.1.529.3), Ba.4, Ba.5という5系統があり、2021年11月に南アフリカで初めて検出された[6]。SARS-CoV-2のBa.5変種は、現時点では優勢である。最近、Ba.2と同一の受容体結合ドメイン(RBD)配列を含みながら、それぞれL452RとF486Vの置換を加えた新しいオミクロン変種が登場し、Ba.2.12.1およびBa.2.13と名付けられた。いずれもBa.2より高い伝染率を示した[7]。
たった1つのアミノ酸の交換が、免疫系を回避するウイルスの能力に大きな影響を与え、ウイルスに対するワクチン開発の進捗を無効にする可能性がある。実際、SARS-CoV-2は、他のRNAウイルスと同様に、新しい宿主であるヒトに適応する際に遺伝的進化を起こしやすく、新しい変異が生じる可能性があり、その結果、祖先の株と比較して複数の変異体が出現することになる[8].
2021年12月下旬および2022年1月上旬のデータでは、オミクロン Ba.2はBa.1およびデルタのそれぞれ約1.5倍および4.2倍の感染力があることが示されている[9]。オミクロンはBa.1感染によって引き出される体液性免疫を回避するために変異を進化させたため、Ba.1由来のワクチンはオミクロンの新種に対する広域防御を達成できない可能性を示唆している[10]。欧州疾病予防管理センター(ECDC)は、多くのEU/EEA諸国においてBa.4およびBa.5感染の割合の増加を観察し[11]、オミクロン亜系Ba.4およびBa.5を関心亜種から懸念亜種に再分類した[12]。先祖代々の亜種Ba.2と比較して、懸念される亜種Ba.4およびBa.5の流行は、おそらく、事前のワクチン接種や感染によって誘導される免疫保護を回避する能力によるもので、それも時間の経過と共に急速に衰える傾向がある[13]。
最後に出現したBA.2.75 SARS-CoV-2変異体(別名「ケンタウルス」)は、BA.2変異体と比較して9個のS変異を追加し、mRNAワクチン接種者における中和抗体の脱出が強化されている[14]。さらに、BA.2.75変異体は、主にN460K変異によって細胞間融合が強化されている。これは、新たな受容体との接触を可能にし、シンシチア形成が増強されるメカニズムを裏付けている[15]。オミクロンBa.2.75は、世界中で次の主流となる変種になる道を歩んでいると考えられている。最新の変異体の高い伝染性は、世界の一部の地域で4回目の接種にさえ達した現在、ワクチン接種の有効性とその長期的な安全性に対する懸念を生んでいる[16]。
3.免疫応答とmiRNAを含む循環型細胞外小胞
最近の研究では、マイクロRNAを含む循環細胞外小胞が、COVID-19ワクチン接種後の抗体産生や副作用と強く関連していることが示された[17]。それぞれmRNA-1273およびBNT162b2として知られるmRNAワクチンの投与は、細胞内で一連の生体分子反応を引き起こすことが証明されており[18]、一本鎖のウイルスmRNAは、エンドサイトーシスによって細胞内に侵入した後は自由に循環させることができる。MiRNAは、20-24個のヌクレオチドからなるノンコーディングRNA分子で、転写後の遺伝子発現を制御する。
MiRNAは、幅広い生物学的プロセスに作用することから、ワクチン-宿主細胞相互作用の複雑なネットワークを通じて、免疫関連遺伝子ターゲットの制御因子として浮上した。それらは、特定のmRNAターゲットとの強い相補性により、細胞質における遺伝子発現の負の転写後調節因子として作用することができる[19]。MiRNAは遺伝子発現パターンのエピジェネティックなレギュレーターであり、共転写の代替スプライシングイベントを調節する[20]。数多くのmiRNAは、細胞の分化だけでなく、分化した状態の維持にも決定的に関与しているようである[21]。
科学的な証拠によると、miRNAをコードする遺伝子は、生物学的ストレスを含む細胞内シグナル伝達経路や崩壊メカニズムなどの様々な刺激に反応する複雑な転写パターンを持っている[22]。いくつかの証拠は、miRNAが細胞生物学、免疫系の制御、および多くの種類の疾患の発症と進行の本質的なメカニズムに関与していることを示している。
マイクロRNAを含む循環細胞外小胞とともに、COVID-19炎症発症におけるS1スパイクプロテインの極めて重要な役割が記述された。S1スパイクプロテインは、宿主細胞へのウイルスの付着や侵入、サイトカインストームの発症に関与するだけでなく、Long-コビッド症候群の原因となっている可能性がある[23]。さらに、COVID-19感染時の血中フリーS1スパイクの数が多いほど、COVID-19の予後不良と相関があると推定された[24]。幸い、懸念される最新の変異体のスパイクプロテインに蓄積された膨大な数の変異は、特定のToll様受容体(TLR)の認識を阻害し、結果としてNF-κB経路および関連するシグナル伝達経路の活性化を低下させる[25]。
4.mRNAワクチンの既知の副反応について
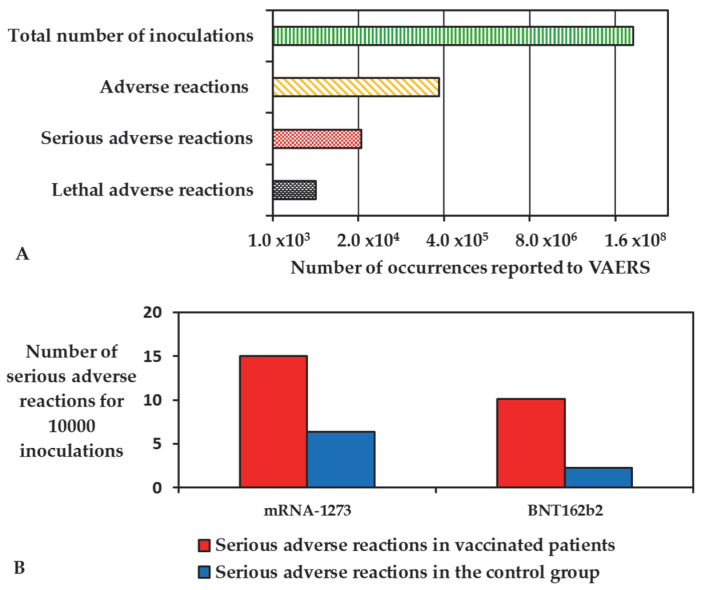
BNT162b2およびmRNA-1273ワクチンの筋肉内投与は、比較的限られた数の副作用を引き起こしながら、COVID-19に対する強固な液性免疫応答を生成することが証明されている。Rosenblumら(2022)は、ワクチンの安全性を監視するために設置された主要な管理機関の1つであるVaccine Adverse Event Reporting System(VAERS)への報告に関する観察研究を報告し、米国で298,792,852回分の投与により340,522件の有害反応が発生したと述べている。これらの報告のうち、22,527件が重篤と判断され、4496件が患者の死亡につながった(図1A)[26]。
図1 (A)ワクチン接種キャンペーン6カ月後の米国における総接種数との比較でVAERSデータベースに報告された副作用、(B)mRNAワクチンの臨床試験中に報告された重篤な副作用とそのプラセボ対照群との比較である。
mRNAワクチン接種を受けた患者の大部分は、注射部位の痛みや疲労、頭痛、筋肉痛などの軽度の副作用を経験する[27]。重篤な副作用は、プラセボ対照群と比較した場合、mRNA-1273では1万人中15例、BNT162b2では1万人中10.1例(それぞれ1万人中6.4例、2.3例、図1B)以上と報告されている[28]。
重篤な副作用は2回目の注射後に多く、心筋梗塞[29]、心筋炎・心膜炎[30]、脳静脈洞血栓症[31,32]、代謝亢進リンパ節腫脹[33]などであった。
心筋炎と心筋梗塞は、イスラエルと米国の多施設統計解析により報告されており[29,30]、16~30歳の男性患者の発生率は1/20,000、全患者間の発生率は、男性患者の予想平均発生率0.12~0.15/10万例、女性患者の0.07~0.08/10万例に対して1/10万となっている。すべての年齢層の男性患者に患者が多く、性別に関係なく12~24歳の範囲に心筋炎の有病率があることが強調されている[34]。
脳静脈洞血栓症はSARS-CoV-2の症状であり、ウイルス不活化ワクチンの副反応であると報告されているが[31,32]、mRNAワクチン投与後にも低い割合で登録されており、世界保健機関のファーマコビジランスデータベース(2021年9月30日までに756例)で報告された重篤な副反応全体の0.07%に当たる[36]。本研究で調査した2つのmRNAワクチンのうち、BNT162b2が620例(0.06%)と大半を引き起こし、136例(0.01%)はmRNA-1273に起因し、女性患者に症例が優位であった[35]。
Cohenら, 2021は、mRNAワクチン接種後の悪性代謝亢進性リンパ節症(MHL)とワクチン関連代謝亢進性リンパ節症(VAHL)の良性を区別するために、PET-CT検査を受けた合計728人の腫瘍患者を検討した[36]。代謝亢進性リンパ節症(HLN)は、前状態にかかわらず、完全接種者の45.6%に報告されており[36]、その強さは様々である。これらの報告のうち、80.1%はワクチン接種の効果によるものであり、接種後5日間で消失した[37]。
その他、ベル麻痺、脳卒中、虫垂炎、自己免疫などの副反応がmRNAワクチン接種と関連していることが報告されているが[38]、mRNAワクチン接種がこれらの疾患の発生を大きく変えるという明確な証拠や研究グループ間のコンセンサスは得られていない。
5.考察
miRNAの生合成機構の崩壊は、いくつかのヒトの病態の原因となっている[39]。miRNAの調節障害は、COVID-19感染時の臨床合併症の発症と関連している[40]。COVID-19ワクチン接種後、多数のmiRNAの発現レベルが変化することが実証されている[41]。したがって、循環するmiRNAの発現レベルの変化は、一度罹患した病気の重症度に影響を与える可能性がある。SARS-CoV-2がコードするmiRNAは、宿主の免疫反応に影響を与える可能性がある[42]。これらの小分子の発現の乱れは、他の長期的な疾患の発症に寄与すると考えるのが妥当であろう。複数の遺伝子発現を調節する宿主のmiRNA範囲の調節異常は、直接的または間接的に癌の発生に影響を与える可能性がある[43]。実際、異なるmiRNAは、癌遺伝子または癌抑制遺伝子として機能することができる[44]。例えば、最近の研究では、COVID-19ワクチン接種後にダウンレギュレーションされるmiRNA-451(miR-451)が、さまざまなヒトの生理的・病理的プロセスに関与していることが明らかにされている[45]。miR-451は、エクソソームを介して腫瘍微小環境に分泌された後、直接的だけでなく間接的にも腫瘍細胞の浸潤や転移に影響を与え、複数の種類のがんの進行に関与していることが示されている。
ワクチン接種のスケジュール[46]に基づけば、1回の接種で膨大な数のウイルスmRNAが組み込まれ、その結果、宿主細胞内に大量に侵入することになる。トロイの木馬」に例えると、miRNAによって制御された遺伝子ネットワークでは、正のフィードバックループとして一連の代謝イベントが引き起こされると考えることができる。また、核内で働くmiRNAの多くは、細胞質で転写物の安定性を同時に制御し、その逆もまた同様であることが知られており、高度に統合されたメカニズムになっている。細胞の代謝経路は大量作用の法則に従うので、多数のウイルスmRNAを標的とする相当数のmiRNAが生成されるはずだ。また、宿主のmiRNA機構がmiRNAの処理に圧倒され、通常の細胞機能や分子経路から逸脱してしまう可能性もある。これは、miRNA経路の危険で長期にわたる制御不能につながるかもしれない。ウイルスメッセンジャーRNAの中には、宿主のmiRNAの転写プロファイルや安定性に変化をもたらすものがあり、その結果、変化したmiRNAクラスターが様々な疾患の発症を促進すると考えるのが妥当であろう。このことは、変化したmiRNAシストロンに癌化特性を持つ宿主miRNAが含まれている場合、特に関連性が高いかもしれない。
6.結論
世界保健機関(WHO)のアドホック協議の一環として、COVID-19 mRNAワクチンの安全性の継続的な評価について、一般的なコンセンサスが形成されつつある。現在、COVID-19ワクチンは安全で効果的である。それらは、臨床試験の何万人もの参加者全体で評価された。mRNAワクチンは、安全性、有効性、製造品質に関する食品医薬品局(FDA)の厳格な科学的基準を満たした。ファイザー・バイオエヌテックとモデルナは、史上最も集中的な安全性監視を継続的に実施する予定である。このモニタリングには、COVID-19ワクチンの安全性を確保するために、確立された安全性モニタリングシステムと新しい安全性モニタリングシステムの両方を使用することが含まれる。よく知られているように、COVID-19ワクチンを接種した後に副作用が出る人もいれば、副作用が出ない人もいるかもしれない。短期的な副作用は、日常生活の能力に影響を与えることがあるが、数日以内に治まる。まれに、COVID-19ワクチン接種後に重篤な健康上の問題が発生した人がいる。ワクチン接種後に起こる健康上の問題は、ワクチン自体に関係ない偶然の出来事、例えば、ワクチン接種後に起こる無関係な発熱などによって引き起こされる可能性のある有害事象とみなされる。VAERSでは、COVID-19ワクチン接種後に、稀ではあるが重篤なタイプの有害事象が、稀な死亡例とともに明らかにされたが、ワクチンが原因であるかどうかは不明である。短期的なポジティブな結果が期待できるにもかかわらず、これらのmRNAワクチンの長期的な安全性をさらに明確にするために、既存の試験でプラセボ投与者の盲検追跡調査を継続することは倫理的に適切である。この種の技術は非常に有望であると思われ、もし期待が確認されれば、他の多くの薬物製剤に採用されるかもしれない。
資金調達
この研究は、外部からの資金提供を受けていない。