Contents
pubmed.ncbi.nlm.nih.gov/22050485/
歯周病研究ジャーナル
R. Hirsch, H. Deng, M. N. Laohachai
アデレード大学歯学部、アデレード、サウスカロライナ州、オーストラリア
2011年8月23日掲載
要旨
アジスロマイシンはマクロライド系抗生物質で、上気道感染症、中耳炎、性感染症、トラコーマなど幅広い感染症の治療に広く用いられている。また、最も一般的な歯周病原体にも有効である。マクロライド系抗菌薬の多用途性は、その抗生物質としての特性だけでなく、免疫調整作用や抗炎症作用にも及んでいる。そのため、アジスロマイシンを含むマクロライドは、重度の喘息や慢性閉塞性肺疾患、最近では嚢胞性線維症など、細菌とは関係のない疾患の治療にも使用されている。
アジスロマイシンは好中球、マクロファージ、特に線維芽細胞に濃縮され、これらの細胞はすべてほとんどの歯周病発症の中心的な役割を担っている。本論文では、アジスロマイシンの多様な特性と、歯周炎の治療と薬物関連歯肉過剰増殖の解消の両方におけるその効果に関する歯周臨床研究について概説する。
進行した歯周病の治療において、アジスロマイシンの1コースの使用を支持するエビデンスが存在する. アジスロマイシンは歯周病の治療と治癒に3つの役割を果たす可能性がある。
すなわち、歯周病原体の抑制,抗炎症活性,歯周組織中のマクロファージや線維芽細胞への低レベルの残存による治癒である。今後の歯周病研究でこれらの特性が確認されれば、歯周病治療における貴重なホストモジュレーターとなる可能性がある。
Dr. Robert Hirsch, MDS, PhD, アデレード大学歯学部, アデレード, SA 5005, オーストラリア
キーワード
アジスロマイシン;歯肉過剰増殖;歯周炎;歯周治療
はじめに
9-デオキソ-9a-アザ-9a-メチル-9a-ホモエリスロマイシン(アジスロマイシン)は、マクロライドのサブクラスであるアザライドの一種であり(1),1980年に初めて合成された(2). アジスロマイシンは、グラム陰性病原体に対する活性がエリスロマイシンなどよりも高いため、幅広い感染症の治療に用いられている(1)。また、アジスロマイシンは免疫調節作用も有しているため、感染症とは異なる疾患の治療にも用いられている。最近では、急性・慢性歯周炎や薬剤性歯肉過剰増殖症など、さまざまな歯周病治療の補助薬として使用されている。
化学構造、用量および副作用
アジスロマイシンは、エリスロマイシンの半合成アナログで、大環状ラクトン環にさらに窒素原子が挿入されている。この15員環マクロライドはアザライドとも呼ばれる(2)。エリスロマイシンと比較して、窒素原子が追加されているため、アジスロマイシンの構造安定性が高く、組織への浸透性に優れ、毒性が低く、半減期が約68時間と長い(3-5)。
アジスロマイシン(500mg)を1日1回3日間、食前1時間前に経口投与するのが最も一般的な投与法である。投与期間が短く、副作用の発現率が低いため、患者のコンプライアンスは良好である(6)。エリスロマイシンに対する過敏症が知られている患者には、アジスロマイシンを処方すべきではない。アジスロマイシンの1コースの使用に関連する副作用は比較的まれで、最も頻度の高いもの(約5%)は吐き気、腹痛、下痢である。アジスロマイシン治療を受けている患者で、血管浮腫やアナフィラキシー(まれに致命的)を含む、まれに重篤なアレルギー反応が報告されている。薬物相互作用としては、制酸剤、ワルファリン(作用が増強される可能性がある;7)、ジゴキシン、エルゴ誘導体などがある。アジスロマイシンの副作用の一覧は、ジスロマック処方ガイド(8) に記載されている。
アジスロマイシンの抗生物質特性
他のマクロライド系抗生物質と同様に、アジスロマイシンは感受性菌の50Sリボソームサブユニットの23SリボソームRNAを標的として細菌のタンパク質合成を可逆的に阻害する(9,10)。終末半減期が長い(12)ため、アジスロマイシンは他の抗生物質よりも少ない投与量と短い治療期間で細菌感染と闘うことができる。上気道感染症、中耳炎、マラリア、性感染症、トラコーマなど、さまざまな細菌感染症に有効である(3,12-19)。
アジスロマイシンは、黄色ブドウ球菌や化膿レンサ球菌などのグラム陽性菌を含む幅広い細菌に対して試験管内試験で静菌作用を示し、エリスロマイシンやクラリスロマイシンなどの初期のマクロライド系抗菌薬と比較して、グラム陰性嫌気性菌に対して特に強い抗菌活性を示す(1,5,20-22)。インフルエンザ菌、モラクセラ・カタルハリス(Moraxella catarrhalis)、百日咳菌(Bordetella pertussis)などの一般的な呼吸器系病原菌は、すべて低用量のアジスロマイシンに感受性があることが示されている;アジスロマイシンはインフルエンザ菌に対してエリスロマイシンの8倍の効力を示した(20) 。エリスロマイシン、クラリスロマイシン、ロキシスロマイシンの高用量に耐性を示す大腸菌、サルモネラ・エンテリティディス、アグレガチバクター・アクチノミセテムコミタンス(侵襲性歯周炎にも関与していると考えられている)などの心内膜炎に関連する腸内病原菌やグラム陰性桿菌は、すべて低用量のアジスロマイシンに感受性を示している(23)。アジスロマイシンはポルフィロモナス・ジンジバリス(Porphyromonas gingivalis)に対して非常に有効:試験した全菌株はアジスロマイシン1.0 lg/mLポンドで阻害された。最小発育阻止濃度(MIC)は、50%の菌株で0.25 lg/mL、90%の菌株で0.5 lg/mLであった(24) 。生体内では、バイオフィルム内の細菌は抗生物質から保護されていると考えられている(25)。しかし、他のマクロライドやテトラサイクリンとは異なり、アジスロマイシンはこのバリアに効率的に浸透することができるため(22,26)、バイオフィルム内の微生物に対してより効果的な抗菌活性を発揮することができる。
アジスロマイシンを歯周治療前に1日1回3日間経口投与すると、スケーリング・ルートプレーニング後の菌血症発生率が20%と、スケーリング・ルートプレーニング単独(90%)およびエッセンシャルオイルを含む消毒薬による歯肉下灌流を併用した場合(70%)と比較して有意に低下した(27) 。試験した細菌種は以下の通りである。
P. gingivalis、Prevotella intermediaおよびTannerella forsythiaであった。健康なボランティアにアジスロマイシン(500mg、その後2日ごとに250mgずつ)を投与したところ、歯肉溝液中のアジスロマイシン濃度は血清中のアジスロマイシン濃度の40倍以上であった。7日後、歯肉溝液中のアジスロマイシン濃度はA. actinomycetemcomitans、P. gingivalisおよびP. intermediaに対するMICを上回っていた(28)。著者らは、これは周辺組織の細胞によるアジスロマイシンの能動的蓄積によるものと考えている。
さらに、アジスロマイシンは緑膿菌のクオラムセンシングを阻害し、病原性因子の産生を減少させ(29,30)、バイオフィルム形成や酸化ストレス耐性を低下させる(31) 。MIC以下の濃度のアジスロマイシンは、試験管内試験で緑膿菌のクオラムセンシングシグナルの産生とバイオフィルム形成を有意に阻害した(32) 。抗生物質の使用が増えるにつれ、マクロライド耐性菌の出現が懸念されている(33) 。ある研究では、マクロライドに対するViridans群口腔咽頭連鎖球菌耐性が成人の71%で認められ、32%に複数のマクロライド耐性菌が認められた(34)。アジスロマイシン(500mgを1日1回、3日間)、クラリスロマイシン(500mgを1日2回、7日間)またはプラセボを1コース服用する前と後の被験者の扁桃腺と後咽頭壁から口腔連鎖球菌を採取した(35)。全対象者の約28%が試験開始時にマクロライド耐性連鎖球菌を保有していた。マクロライド耐性連鎖球菌の割合は、治療後14日目、28日目および42日目にアジスロマイシン群(クラリスロマイシン群と比較)で有意に高かったが、180日後には認められなかった。アジスロマイシンは治療後少なくとも3~4週間は持続するため、耐性菌の播種が増加する恐れがあると考えられた(35) 。アジスロマイシンを含む一連の抗生物質に対する5種類の歯周病原菌の耐性をスペインとオランダで比較した(36)。両国のP. gingivalisの全菌株がアジスロマイシンに感受性であったのに対し、A. actinomycetemcomitansの33%がスペインの分離株ではアジスロマイシンに耐性であったが、オランダのサンプルでは全菌株が感受性であった。
アジスロマイシン、メトロニダゾール、亜抗菌薬ドキシサイクリンの微生物学的効果に関する研究では、耐性分離株の割合と耐性種(主に連鎖球菌種とVeillonella parvula)を保有する部位の割合は、これらの薬剤の投与前と投与12カ月後に同程度であった(25)。歯周病原菌は一般にアジスロマイシンにほとんど耐性を示さなかった.
アジスロマイシンの免疫調節作用
マクロライドの免疫調節作用は、重症喘息、びまん性汎細気管支炎、慢性閉塞性肺疾患、最近では嚢胞性線維症や気管支拡張症など、細菌とは関係のない疾患の治療に応用されている(10,13,37,38)。マクロライドの作用スペクトルは、炎症の抑制、好中球やマクロファージの活性調節、サイトカインの産生から、線維芽細胞の活性や宿主免疫の変化まで多岐にわたる。効果的な抗炎症作用は、主に慢性炎症性気道疾患において研究されてきた。しかし、正確なメカニズムはまだ完全には解明されていない(39,40)。
アジスロマイシンは経口投与で全身に広く分布し、血清中の濃度が低下した後も組織への浸透性がよく、濃度が持続するため、他のマクロライド系薬よりも免疫調節薬として有利である(13)。アジスロマイシンは好中球、マクロファージ、線維芽細胞に速やかに取り込まれ(41-43)、高度に保持される(44)。
アジスロマイシンはその活性を維持したまま、走化性により好中球によって炎症組織に効率的に運ばれる(45)。アジスロマイシン(500mgを1日1回、3日間)を健康なボランティアに服用させたところ、好中球前駆細胞に蓄積された結果であろう、最終服用後28日間好中球に残存した(46)。アジスロマイシンは好中球の顆粒状酵素の放出、酸化バーストおよび酸化的防御機構に急性作用を及ぼした;循環好中球の脱顆粒が延長したことから、亜急性の非感染性炎症反応の治療における抗炎症作用の可能性がある(46)。ヒト好中球におけるアジスロマイシンとエリスロマイシンの濃度勾配は、内部で10倍、外部で10倍、マウスマクロファージでは26倍であった(41)。培養液から細胞外薬物を除去した後、最初の1時間以内に放出された細胞内薬物はアジスロマイシンが19%であったのに対し、エリスロマイシンは85%であった。同様の取り込み差(72時間後にエリスロマイシンの21倍)が、各薬剤10lg/mLで培養したヒト線維芽細胞でも認められた。このことは、線維芽細胞がアジスロマイシンの持続的放出のリザーバーとして、また炎症組織内を移動する好中球へのアジスロマイシンの移動のリザーバーとして働く可能性を示している。
アジスロマイシンの有意な免疫調節作用は、試験管内試験でさまざまな濃度で観察されている。アジスロマイシンは、活発に貪食する肺胞マクロファージの数を増加させ、炎症性サイトカイン[インターロイキン(IL)-1b、IL-6、IL-8、腫瘍壊死因子(TNF)-a]や顆粒球マクロファージコロニー刺激因子などの増殖因子の発現を減少させることがわかった(19,47)。同様の抗炎症作用が嚢胞性線維症の気道上皮細胞でも認められた;試験管内試験でアジスロマイシンはIL-8、炎症性転写因子である核内因子κB(NF-jB)および活性化因子タンパク質1(AP-1)の発現を減少させた(48) 。アジスロマイシンはマクロファージの表現型を変化させ、交互に活性化された表現型へとマクロファージの分極をシフトさせ、その結果、炎症性サイトカインの産生を抑制し、抗炎症性サイトカインの産生を増加させる(49,50)。
In vitroでのTNF-a誘導性NF-jBに対する阻害作用は、強力な抗炎症剤(すなわちコルチコステロイド)であるヒドロコルチゾンやデキサメタゾンの阻害作用よりも有意に低いようであった(51)。ヒト歯肉線維芽細胞をP. gingivalis由来のリポ多糖(LPS)で刺激し、デキサメタゾンを投与した研究がある。
gingivalis 由来のリポ多糖(LPS)で刺激し、アジスロマイシンで処理したヒト歯肉線維芽細胞を調べたところ、IL-8の産生が用量依存的に増加した(52)。一方、アジスロマイシンは、口腔上皮細胞株においてLPS誘導性IL-8産生を減少させ、自然免疫を修正し、ヒト口腔上皮細胞に対して抗炎症作用を発揮することが判明した(53)。これらの著者らは、歯周治療の初期段階でアジスロマイシンを投与することは、IL-8レベルの低下を促進する有用な方法であると結論づけた。歯周病健常人にアジスロマイシン(500mg、その後2日間250mg/日)を投与したところ、最終投与日に歯肉溝液量の著明な減少が認められ、14日後には歯肉溝液量はベースライン値に戻った。
アジスロマイシンの歯周臨床試験
32名の被験者(喫煙状況は報告されていない)を対象に、アジスロマイシン(500 mg)を3日間単回投与した後,血漿,唾液,正常歯肉および病的歯周組織中のアジスロマイシン濃度を最長6.5日間測定した(55) . アジスロマイシンの濃度は最終投与から12時間後にピークを示したが、6.5日後も残存していた. 病的歯周組織におけるアジスロマイシン濃度は、最終投与から4.5日後まで正常歯肉よりも有意に高かった. 歯肉,歯槽骨および唾液中のアジスロマイシンの残存期間は以前にも確認されているが(56) ,その試験期間は6.5日間であった.
アジスロマイシンの歯周微生物学的臨床試験
アジスロマイシンの歯周臨床試験は1996年に初めて報告された(57)。歯周炎患者46例に歯周治療の補助としてアジスロマイシン(500mgを1日1回3日間)またはプラセボを投与した。各患者の同じ歯周ポケットの微生物学的評価が22週まで行われ、色素性嫌気性菌はアジスロマイシンにより3週目と6週目に有意に減少し、スピロヘータは試験期間中抑制された。
アジスロマイシン500mgを1日1回3日間服用した34人の歯周炎患者において、臨床的および微生物学的改善が報告された(5)。この研究では、寒天拡散バイオアッセイ法により歯周ポケット内組織中のアジスロマイシン濃度を測定した。14日目においても、アジスロマイシンは炎症を起こした歯周組織において、P. intermediaおよびA. actinomycetemcomitansに対して有効な濃度で検出可能であった. 6種の歯周病原性細菌数の持続的減少は、14日目まで認められなかった.
スケーリング・ルートプレーニング単独群と、アジスロマイシン、メトロニダゾール、またはドキシサイクリンの亜抗菌薬用量を併用したスケーリング・ルートプレーニング単独群との微生物学的効果を、12カ月にわたる92人の被験者による無作為化対照単盲検試験で比較した(25) 。すべての治療法において、P. gingivalis、T. forsythia、P. intermediaおよびその他の細菌(赤色およびオレンジ色の複合細菌)の平均数が有意に減少した。アジスロマイシンとメトロニダゾールの両群で、治療開始後2週以内に赤色およびオレンジ色の複合細菌数の有意な減少が観察されたが、12カ月後にはアジスロマイシン群のT. forsythiaのみが有意に減少した。この研究は、歯周ポケット内の細菌に対するアジスロマイシン単回コースの長期的効果を示唆するものである。
アジスロマイシンの臨床試験
歯周治療の結果に対するアジスロマイシンの効果に関する臨床試験は比較的少ない。その多くは被験者数が少ないこと、適切な治療コントロールがなされていないこと、いくつかの研究では喫煙のコントロールがなされていないことが明らかにされている。また、アジスロマイシンの使用に伴う歯周治療プロトコルに関しても、研究はさまざまである。このような制約を考慮すると、歯周治療と併用するアジスロマイシンは歯周治療単独と比較して歯周臨床成績および微生物学的成績を改善するというのが一貫した研究結果である. アジスロマイシンの単独療法および非外科的歯周治療の補助療法としての効果を検討する決定的で適切にコントロールされた歯周臨床研究が必要である.
症例報告
アジスロマイシンをスケーリング・ルートプレーニングと併用した歯周膿瘍患者の4症例報告では、重度の限局性歯周欠損に有意な骨増生がX線写真上認められた(58). 3人の患者にアジスロマイシン(500mg、1日1回、3日間)を最長5年間隔で3コース投与し、1人の患者には32カ月間隔で2コース投与した。1人の患者には経過観察がなく、3人の患者には歯周病のメインテナンスのための断続的な受診があったが、歯周外科手術を受けた患者はいなかった。これは、歯槽膿漏に関連した骨破壊症例におけるアジスロマイシンの骨再生能に関する最初の報告であった。著者らはまた、定期的な歯周病メインテナンスを受けている15人の患者にアジスロマイシンを2~3コース投与したところ、臨床的にも患者からの報告でも出血の有意な減少が認められ、長期的に有益な効果が得られたと報告している。メンテナンスのための来院間隔も延長した。著者らは、臨床試験ではアジスロマイシンを1コース以上投与することを検討すべきであると示唆した。
最近、重度の限局性歯周炎および汎発性歯周炎患者において、アジスロマイシンの単回投与により有意な歯周治癒、骨再生、薬物誘発性歯肉過剰増殖の消失を認めた3症例が報告された(59)。これらの患者のうち1人は歯周治療を受けておらず、もう1人は最小限のデブライドメントを受けていた。治癒は6~8カ月にわたって徐々に進行し、炎症の消失、歯肉組織の輪郭の改善、骨の再生が観察された。この報告は、アジスロマイシンの臨床的可能性を垣間見るものであり、その歯周病に対する可能性について臨床的および実験的研究をさらに進める必要性を支持するものである。
アジスロマイシンと歯肉の過剰増殖
アジスロマイシンの長期的な歯周免疫調整作用に関する知見は、シクロスポリンAによって誘導された歯肉の過剰成長を抑制する効果に関する報告から得られている。
(60). シクロスポリンAに関連した実質的な炎症性歯肉過剰増殖の2人の患者は、胸部感染症の治療でアジスロマイシンを処方されていた。歯周介入やシクロスポリンAの減量なしに、歯肉出血は3~4カ月で消失し、歯肉過剰増殖は1例で消失、もう1例で退縮したと報告している。シクロスポリンAを服用している19歳の女性では、アジスロマイシン治療(500mgを1日1回、3日間)後、重度の歯肉過剰増殖が3カ月で部分的に退縮した(61)。シクロスポリンAが誘発した歯肉過剰増殖がメトロニダゾールの投与により消失したという報告が1件ある(62)。
カルシウム拮抗薬による歯肉過形成の消失は、1997年にシクロスポリンAを服用していた被験者で初めて報告され(63)、その後8カ月にわたって観察されたアジスロマイシンの歯周組織に対する長期的な有益な効果のひとつであることが判明した(59)。
表2はシクロスポリンAによる歯肉の過剰増殖に対するアジスロマイシンの効果に関する臨床研究をまとめたものである。これらの研究の多くは適切なコントロールと科学的厳密性に欠けるが、一貫した所見として、アジスロマイシンは歯周治療を行わない場合でも歯肉の炎症と歯肉の過剰増殖を抑制した。
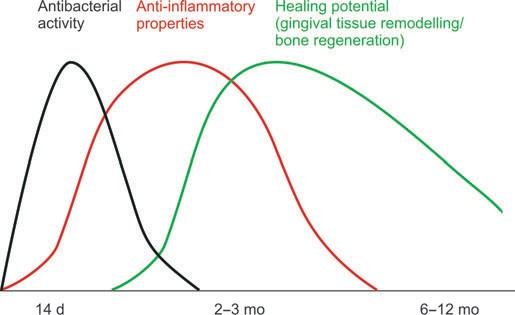
図1. 歯周炎治療におけるアジスロマイシンの1クール投与後の歯周活性の3つの重なり合う段階の時間的モデル
アジスロマイシンの抗炎症作用と好中球、マクロファージ、および血芽細胞における濃度はよく知られているが、これらの作用が1回の投与でどのくらい持続するのか、また免疫調節作用を発揮するために必要な薬剤の細胞内濃度はどのくらいなのかはわかっていない。最後に、アジスロマイシンがシクロスポリンAによる歯肉の過剰成長を長期にわたって退縮させるというエビデンスがあるほか、アジスロマイシンの単回投与後、最長12ヵ月にわたって歯周病が治癒し、骨が再生したという症例報告もある。
アジスロマイシンと歯肉過剰増殖に関する動物および試験管内試験
ラットにシクロスポリンAを6週間投与して歯肉の過剰増殖を誘導し、その後ミネラルオイルにアジスロマイシンを1週間経口投与した(64)。アジスロマイシンを含まないミネラルオイルをコントロールとして用いた。7週目に組織学的分析と歯肉線維芽細胞の培養を行った。シクロスポリンAは歯肉の過剰増殖を引き起こし、線維芽細胞の貪食活性を低下させた。アジスロマイシンは歯肉の過剰増殖量を減少させ、培養中の歯肉線維芽細胞の貪食活性を有意に増加させた。
ある試験管内試験研究では、健康な歯肉組織またはシクロスポリンA誘発性歯肉過剰増殖症患者から採取した歯肉組織から培養したヒト歯肉線維芽細胞に対するアジスロマイシンの効果を検討した(65)。アジスロマイシンは、健常および歯肉過剰増殖の両方の線維芽細胞において、シクロスポリンAによる線維芽細胞の増殖を阻害し、MMP2を活性化した。さらに、アジスロマイシンはシクロスポリンAによるコラーゲンの蓄積を抑制した。アジスロマイシンは、シクロスポリンAが細胞増殖とコラーゲン産生を誘導する能力を阻害し、シクロスポリンAの影響を受けた線維芽細胞においてMMP1ではなくMMP2を活性化することにより、シクロスポリンA誘発性歯肉過剰増殖の症状を改善すると考えられていた。
アジスロマイシンと薬物関連歯肉過剰増殖に関する既存のエビデンスがあるにもかかわらず、アジスロマイシンのこの特性が歯周病理論および臨床においてほとんど知られていないことは不可解である。アジスロマイシン単独で、あるいは歯周治療の補助として、シクロスポリンA、カルシウム拮抗薬、フェニトインに関連した歯肉過形成の管理を強化できるかどうかを決定するためには、確実な臨床研究が必要である。
考察
抗生物質は、慢性および侵襲性歯周炎の治療の補助として使用されてきた長い歴史があるが、その結果はさまざまである(66,67)。多くの抗生物質に対する耐性菌が増加していることから、ヒトと動物の両方における抗生物質の乱用に対する懸念は正当なものである。集団における抗生物質の使用量の増加と耐性菌の発生との間には明らかな関連がある(35)。これらの問題は、歯周治療における抗生物質の使用に関しても取り上げられている(6,36,67)。
最も広く研究されている歯周抗生物質レジメンは、アモキシシリン(375mg)とメトロニダゾール(500mg)を1日3回、7日間併用する方法である(67) 。現在までのところ、臨床的または微生物学的に定義された歯周病の変種において、アモキシシリン/メトロニダゾールに対する他の抗生物質レジメンの優越性を示した比較試験はない(67)。しかし、最近の研究では、クロルヘキシジン局所投与による機械的治療が、6カ月後にはアモキシシリン(500mg)とメトロニダゾール(250mg)を併用した同じ治療と同程度に有効であり、初期の効果は短期間であることがわかった(68,69)。
アジスロマイシン(1.5g)と比較して、Mombelliら(67)が用いたレジメンは、3日間ではなく7日間にわたって有意に大きな抗生物質負荷(18.4g)を患者に与え、耐性菌発生の潜在的リスクを増加させる。抗生物質の短期投与は、耐性菌の発生を抑える可能性がある(70)。副作用はアモキシシリン/メトロニダゾールレジメンで非常に多く(42%;71)、したがってコンプライアンスが損なわれる。アモキシシリンは、その抗生物質としての効果とは異なる免疫調節作用や抗炎症作用については注目されていない。メトロニダゾールはヒト歯根膜細胞による炎症性サイトカインの産生を抑制したが(72)、特異的な免疫調節作用を示す証拠はほとんどない。
第一に、アジスロマイシンは、500mgの錠剤を3錠、単回投与することで、中等度から進行した歯周炎の治療において、3つの役割を果たす可能性がある。グラム陰性菌に対する有効性、バイオフィルムに浸透する能力、長い抗菌性半減期と短期間の投与により、進行した炎症性歯周炎の治療の補助として魅力的な抗生物質の選択肢となる。第二に、アジスロマイシンは好中球やマクロファージに取り込まれることで、歯周炎症部位を標的として集中的に作用し、抗炎症作用を発揮する。「高応答性」マクロファージは、LPSや細菌産物に反応して炎症性サイトカインを大量に産生することにより、歯周炎に罹患しやすいかどうかを決定すると考えられているため、アジスロマイシンの有益な役割は、炎症性サイトカインの産生を抑制することであると考えられる(49)。第三に、アジスロマイシンは歯周組織に長期的な治癒効果をもたらすと考えられる。この性質は、マクロファージの表現型を変化させ(M2に変化させ)、抗炎症性サイトカインの産生を増加させ(49) 、治癒を促進する効果に関連していると考えられる。炎症性歯周炎を治療するために特別に設計された薬剤であれば、このような明確で時間的に重複する活性を持つであろう(図1)。アジスロマイシンの戦略的使用は、抗菌作用と免疫調節作用の両面から、治療効果の乏しい患者の歯周一次治療に有用となる可能性がある(53)。
アジスロマイシンの組織内濃度が抗菌レベルを下回った後も、マクロファージや線維芽細胞(44)などの歯根膜の長寿命細胞や、おそらく歯周幹細胞において生物学的(免疫調節)活性が長期間保持されることで、薬剤の抗炎症作用や治癒作用が発揮される可能性がある。シクロスポリンによって誘発された歯肉の過剰増殖が時間の経過とともに消失することは、この薬剤の長期的な宿主調節・治癒特性を示唆するものである。アジスロマイシンの薬剤性歯肉過剰増殖抑制作用は歯周病関連文献では一般に知られていない。
アジスロマイシンは、低用量ドキシサイクリン(1日2錠を3カ月以上服用する必要があり、副作用を伴う(73))よりも、歯周炎の治療においてより効果的な宿主モジュレーターであることが証明されるかもしれない。潜在的な耐性菌を回避する亜抗菌薬アジスロマイシンの投与レジメンを開発することは可能であろう。興味深いことに、アジスロマイシンに由来する非抗生マクロライドの開発が最近報告されている;これは炎症性腸疾患と関節炎の動物モデルにおいて免疫調節効果を示した(74)。
結論
歯周病治療におけるアジスロマイシンの使用を支持するいくつかのエビデンスが存在する。
アジスロマイシンの歯周病菌に対する強力な活性、患者のコンプライアンスを確保する短期間の治療レジメン、副作用の発現率の低さ、持続的な抗生物質効果、さらに1回の投与でより長く持続する免疫調節効果、これらはすべて好ましい特徴である。
今後の歯周病研究でこれらの特性が確認されれば、抗菌活性と宿主調節作用により、進行性または抵抗性の炎症性歯周炎や重度の歯肉過剰増殖の治療を強化するユニークな薬剤となる可能性がある。
