タウタンパク質の研究
キーワード:タウ、タウタングル、NFT、神経原線維変化、タウ蛋白、pタウ、リン酸化、アミロイドβ、タウ凝集、タウ蓄積、p-tau
概要
アルツハイマー病におけるタウタンパク質の病態生理学的役割は、実はまだよく理解されていない。タウ凝集体の形成と沈着がアルツハイマー病の重大な事象であることが、これまでの大量の関連研究から示唆されている。
タウの過剰リン酸化
タウは健常者の脳においてもある程度リン酸化されるが、アルツハイマー病の初期段階でタウが凝集する前に過剰にリン酸化される。アルツハイマー病の進行期には、タウのほとんどのリン酸化部位がリン酸化され、病理学的タウ凝集体は、生理学的タウよりも3倍高くリン酸化される。
生理学的な応答からの逸脱
アルツハイマー病初期において起こる過剰リン酸化は、非生理学的な作用が生じたというよりも生理学的な応答の過大な結果を反映している可能性がある。
タウの過剰リン酸化は、おそらくタウプロテインキナーゼとタウホスファターゼ活性の間の不均衡から生じる。
神経原線維変化の形成にはタウの過剰リン酸化が大きく影響を与えると考えられている。
タウ凝集の多段階プロセス
生理学的に機能しているタウが病理学的タウの凝集物に変化するには、多段階のプロセスが必要であると考えられている。
微小管からのタウの脱離には、タウのリン酸化、アミロイド毒性、酸化ストレス、など多くのメカニズムによって促進される。
立体配座の変化によるタウ凝集の誘導
高濃度の結合されていないタウは、タウのミスフォールディングおよび立体配座の変化を促進し、それによってタウの凝集、神経原線維変化となる可能性を高めると考えられる。
3リピートタウはPHFとして集合し、4リピートタウはストレートフィラメント(SF)として集合する。
微小管の損傷によるタウの局在化
タウの凝集物の局在化は、微小管安定化能の機能喪失と関連している可能性がもっとも高い。その結果としてシナプス機能障害、および軸索輸送障害が予測される。
しかし、アルツハイマー病のニューロン微小管密度と全長はPHF形成とは無関係に減少している。このことは、PHF形成よりも過剰リン酸化タウの相互作用するプールが、微小管の不安定化に関連していることを意味するかもしれない。
可溶性タウオリゴマー凝集体仮説
タウが有害であるもう一つの可能性は、有毒なのは巨大分子のタウ凝集体ではなく、可溶性の原繊維タウオリゴマーの凝集体が有害なタウ種であるという説明である。
タウの可逆的なリン酸化は、グルコース欠乏、飢餓、低体温、麻酔、慢性ストレスによって観察されている。
用語
タウオパチー
tauと疾患を意味する「-pathy」の造語で、神経原線維変化を示す神経変性疾患の病理の総称
PSP、CBDのタウオパチーはグリア封入体を含む
タウオパチーを引き起こすタウ変異のほとんどが、微小管結合領域、c末端領域に集中している。
MAP(微小管関連タンパク質)
微小管に結合して、微小管を構成するチューブリンの重合を促進し微小管を安定化させる役割を果たすタンパク質。
脳神経細胞の主要な構造的MAPはタウタンパク質とMAP2。MAP2はニューロン細胞体と樹状突起に局在し、MAP4は非常に広範囲に存在する。
MAP2
MAP2はタウとは対照的に繊維形成能に大きな違いがあり、病因への影響はさほどないと考えられている。しかしMAP2の枯渇はレビー小体型アルツハイマー病と関連していることが示唆されている。
https://www.ncbi.nlm.nih.gov/pubmed/20024519
MAP2とαシヌクレインはパーキンソン病において共局在している。
in vitroでMAP2アイソフォームに結合し、チューブリン集合を刺激する能力を増大させる3β-メトキシ-プレグネノロンは、ラットにおいて抗うつ効果を有する。
https://www.pnas.org/content/109/5/1713.short
MAP2c
https://www.mdpi.com/2218-273X/9/3/105/htm
タウタンパク質
タウタンパク質とは細胞骨格の一種である微小管(Microtuble)を安定化させるタンパク質。神経細胞、軸索に豊富に存在し、アストロサイトやオリゴデンドロサイトでもごくわずかに発現している。
https://www.researchgate.net/figure/Normal-function-of-tau-protein-Tau-protein-stabilizes-microtubules-through-four-tubulin_fig2_225294145
タウタンパク質は、MAPT(microtubule-associated protein tau) 遺伝子によって選択的スプライシングによって切り出され産生される。
MAPTのH1ハプロタイプの遺伝はPSP、CBD、パーキンソン病、筋萎縮性側索硬化症(ALS)の危険因子として寄与する。(ピック病は関係しない)
タウの役割
軸索の安定性・微小管の構造・微小管間隔の決定
タウの主な役割は、軸索の安定性を調節すること。微小管の重合を促進したり安定化したりする。
タウは、微小管を機械的に安定化させかつ硬化させて、軸索微小管が軸索の長く伸びた構造を支持することを可能にする。
その他タウタンパク質は、微小管において細胞内輸送に関わるキネシンをカーゴから引き離す(強固に結合している)ことで、軸索輸送への影響を及ぼす。
https://www.ncbi.nlm.nih.gov/pubmed/18511549/
微小管との相互作用を通して、動的に微小管形態形成および分化、神経突起の極性、軸索伸長および伸長、神経可塑性、キネシンおよびダイネジナクチンモータータンパク質により媒介される軸索輸送の調節にも関与する。
タウによる鉄の恒常性
アミロイド前駆体タンパク質(APP)のフェロキシダーゼ活性は、フェロポーチンと結合して鉄を排出する。しかし、その活性はアルツハイマー病においては阻害されるため神経細胞において鉄の蓄積を引き起こす。
タウノックアウトマウスでは、細胞からの鉄排出が有意に遅延する。
可溶性タウの濃度は、アルツハイマー病、タウオパチーの脳領域では低下しており、このことはAPPを介した鉄輸送を損い、鉄蓄積による認知症を伴うパーキンソニズムを誘発する。
タウの増加は鉄の蓄積による細胞毒性を防ぐための代償応答であるかもしれない。
https://www.ncbi.nlm.nih.gov/pubmed/25031639/
染色体安定性の制御
タウノックアウトマウスでは染色体の分離にエラーが生じDNA損傷が起こる。
MAPT変異を有する患者とタウ変異を発現するマウスの両方においてリンパ球と線維芽細胞において染色体異常が観察された。
オリゴデンドロサイトの突起伸長
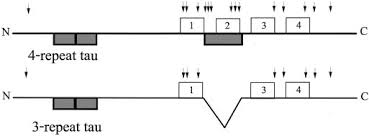
タウのアイソフォーム
エキソン2、エキソン3、エキソン10の選択的スプライシングにより切り出されたタウには、6種類のアイソフォームが存在し結合ドメインの数によって区別される。
タウタンパク質の構造は、N末端ドメイン、プロリンリッチ領域、リピートドメイン、およびC末端ドメインに分けられる。
C端側の微小管結合領域が3つ繰り返されているものを3リピートタウ、4つ繰り返されているものを4リピートタウと呼ぶ。
アルツハイマー病は、3,4リピートタウが1:1でPHFとして蓄積する
https://www.ncbi.nlm.nih.gov/pubmed/1530909/
3リピートタウ
ピック病 3リピートタウが多い
4リピートタウ
PSP、CBD、MAPT 4リピートタウが多い
PSPとCBDの4Rタウは、生化学的に区別が可能
https://www.ncbi.nlm.nih.gov/pubmed/14705114/
タウアイソフォームは種で異なる。成体マウスでは4リピートタウがほぼ独占し、(3Rから4Rタウへ切り替わる)成体ニワトリでは3、4、5リピートタウが発現している。
タウタンパク質のアイソフォーム発現を変化させる突然変異が、過剰なタウタンパク質のリン酸化につながる。
リン酸化タウ
もっとも長いタウのリン酸化部位は85箇所存在し、脳に存在するタウ分子は通常2~3箇所がリン酸化されている。アルツハイマー病で見られる過剰リン酸化タウは約8箇所がリン酸化されている。(しかし胎児のタウは7箇所がリン酸化されているが凝集せず、PHFと異なり微小管と結合する能力もある)
過剰にリン酸化されたタウは微小管を重合する能力をもたない。
凝集し神経原線維変化を形成し毒性をもたらすと考えられているが、リン酸化による凝集が疾患の誘導となるかは証明されていない。
タウのリン酸化の役割
リン酸化タウは微小管と相互作用する能力をオフに調節することで、微小管の構築を促進ではなく阻害する。
https://www.ncbi.nlm.nih.gov/pubmed/26635213?dopt=Abstract
リン酸化タウは酸化還元活性重金属を隔離して、酸化ストレスから保護する作用があることが分かっている。
https://www.sciencedaily.com/releases/2016/11/161117151205.htm
シナプス可塑性
タウのリン酸化は海馬のシナプス伝達の長期抑制(シナプス可塑性)の誘導に必要である。
https://www.ncbi.nlm.nih.gov/pubmed/25810511/
シナプスブレーキ
タウのリン酸化はシナプスブレーキとして機能する可能性がある。それによりNMDA受容体のダウンレギュレーションが迅速に可能になる。
代謝低下を必要とするコントロールされた条件下でのタウの過剰リン酸化は、保護作用を目的とした生理学的な応答である可能性がある。
https://www.physiology.org/doi/full/10.1152/ajpregu.00117.2013
http://dx.doi.org/10.1074/jbc.M112.401240
ツキノワグマの冬眠時のタウリン酸化
https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0014530
タウをリン酸化させる酵素
- GSK3(GSK3β)
- 分裂促進因子活性化タンパク質キナーゼ(MAP)
- サイクリン依存性キナーゼ5(CDK5)
- cdc2
タウの脱リン酸化酵素
- プロテインホスファターゼ1
- PP2A(アルツハイマー病患者で低下している)
- PP2B
CYF1P2(細胞質FMR1相互作用タンパク質2)
アルツハイマー病においてダウンレギュレーションされている、タンパク質でありタウの過剰リン酸化をもたらすαCaMKIIキナーゼを抑制する。
Pin1
parvulin familyに分類されるPPIase(プロリルイソメラーゼ)
Pin1の喪失は異常なタウの蓄積、およびβアミロイドの過剰産生につながる。
Pin1は細胞周期を調節し細胞分裂に必要な酵素。
Pin1の過剰発現はガンを促進することができる。ガンとアルツハイマー病の逆相関関係を説明しうる因子。
http://www.eurekaselect.com/95489/article
Pin1機能の低下は、細胞内にアミロイドβタンパク質前駆体を局在化させ、プロセシングに影響を与えることで、アミロイド形成に寄与する。
https://www.ncbi.nlm.nih.gov/pubmed/22430533

http://www.discoverymedicine.com/Jane-A-Driver/2014/02/07/regulation-of-protein-conformation-by-pin1-offers-novel-disease-mechanisms-and-therapeutic-approaches-in-alzheimers-disease/
正常な海馬ではPin1は、CA2、CA3、CA4で高く、CA1や海馬鉤では低く発現している。
アルツハイマー病初期での神経原線維変化はCA1や海馬鉤で見られることから、Pin1が神経原線維変化の生成を阻害している可能性がある。
Pin1は、アルツハイマー病初期ではリン酸化タウタンパク質の生成を防ぐが、ある程度まで凝集した変性タウタンパク質には結合してしまうでのはないか。
Pin1によるPP2A活性
タンパク質の脱リン酸化は、PP2Aによって起こるが、Pin1はリン酸化タウタンパク質のシストランス回転を促進することで、PP2Aの活性を促進する。
http://lifesciencedb.jp/dbsearch/Literature/get_pne_cgpdf.php?year=2005&number=5011&file=9FKebKaBF1Bu3yN6a/GQGw==
https://www.intechopen.com/books/understanding-alzheimer-s-disease/pin1-protects-against-alzheimer-s-disease-one-goal-multiple-mechanisms
Pin1遺伝子およびタンパク質発現ならびにSIRT1発現は、アミロイドβ25-35細胞において減少する。BDNFはアミロイドβによって増加しており神経毒性障害に対する代償的反応を反映している。
https://www.sciencedirect.com/science/article/abs/pii/S0940299316300069?via%3Dihub
Pin1 mRNAはApoE3よりもApoE4マウスの海馬においてより高いが、嗅内皮質、頭頂皮質では低い発現が検出される。低いPin1は神経原線維変性およびアミロイドの形成を増加っせる可能性がある。
https://www.ncbi.nlm.nih.gov/pubmed/24161275
リン酸化によるタウLLPS
修飾タウ
糖化化タウ
タウは微小管結合ドメイン内で糖化されることが示されている。
タウは糖化にタウと微小管の相互作用を阻害し、それによってタウ過剰リン酸化を促進することが示唆されている。
https://www.ncbi.nlm.nih.gov/pubmed/8063802/
https://www.ncbi.nlm.nih.gov/pubmed/28521765
糖化はタウの凝集を間接的に促進するか、または凝集したタウ種を安定化させることが示唆されている。
https://www.ncbi.nlm.nih.gov/pubmed/7561862/
糖化-PHF-タウは糖化されていないタウと比較して凝集傾向が高いため、PHFをより複雑な構造の凝集体へ形成を導き安定化させると思われる。
https://www.ncbi.nlm.nih.gov/pubmed/10366687/
糖化は装飾されるタウアイソフォームによって凝集に異なる影響をおよぼす。3R0Nにはタウオパチーに影響をおよぼさず、4Rタウオパチーにおいては最も重要な役割を果たす。ルレングスタウアイソフォームは糖化されると広範囲の凝集を示す。
糖化部位の減少、4R:3R比率の調節はタウオパチーに対する潜在的な治療的意義を有する。
https://www.ncbi.nlm.nih.gov/pubmed/26655600/
ADマウスモデルにおけるタウは、海馬および皮質においてRAGEと共局在している。
https://www.ncbi.nlm.nih.gov/pubmed/24503708/
RAGEがAGE誘発性のタウの過剰リン酸化ならびにシナプス機能障害およびラットの空間記憶障害と関連している。
https://www.ncbi.nlm.nih.gov/pubmed/21450369/
ピック病および他の神経変性疾患の場合においてもタウ陽性の封入体は、AGEが存在した。
https://www.ncbi.nlm.nih.gov/pubmed/9777946/
グリコシル化タウはタウはプリオン様伝播特性を増強する可能性がある。
https://www.ncbi.nlm.nih.gov/pubmed/29982964
ユビキチン化タウ
ユビキチンは、アルツハイマー病患者脳の老人斑に含む成分として同定されている。正常な対照と比べてより多くのユビキチンを含むようであった。
https://www.ncbi.nlm.nih.gov/pubmed/3029875/
ユビキチン化は凝集体の形成を増強することが示唆されている。
https://www.ncbi.nlm.nih.gov/pubmed/14962978/
モノユビキチン化、ポリユビキチン化の両方が、神経変性疾患において生じる不溶性たんぱく質封入体の形成に寄与する。
https://www.ncbi.nlm.nih.gov/pubmed/16807328/
https://www.ncbi.nlm.nih.gov/pubmed/17981811/
プロテアソームへのPHFタウの結合の阻害は、アルツハイマー病脳で観察されるプロテアソーム障害の原因である。
https://www.ncbi.nlm.nih.gov/pubmed/12641733/
アルツハイマー病脳のPHF中に存在する大部分のユビキチンは、モノユビキチン化形態として生じるが、一部のユビキチンしかポリユビキチン鎖を形成しない。(プロテアソームに認識されて分解されない)
マウスモデルへのリチウムの長期投与は、ユビキチン化を増強することによりタウ病変を減少させる。
https://www.ncbi.nlm.nih.gov/pubmed/16228182/
タウはユビキチン化を介してプロテアソームによって分解されうるが、タウは本来変性していないタンパク質であるため、正常なタウ分解はその先行するユビキチン化を全く必要としないかもしれない。
ニトロ化タウ/Nitration of tau protein
チロシン残基の芳香環にニトロ基が共有結合的に付加されること。
神経原線維変化にニトロ化されたタウが存在することが明らかになっている。
ニトロ化によってタウの微小管との結合能が失われると考えられている。
https://www.ncbi.nlm.nih.gov/pubmed/12937143
アセチル化タウ
タウ分子内には20を超えるアセチル化部位がある。可溶性タウのアセチル化は、安定性、タンパク質同士の相互作用、凝集に重大な影響をおよぼす。
https://www.ncbi.nlm.nih.gov/pubmed/24708343/
タウのアセチル化はアルツハイマー病において増加する。リジン174でのタウアセチル化は、アルツハイマー病の初期において生じる。
https://www.ncbi.nlm.nih.gov/pubmed/26390242/
タウはリジンアセチル化により広範囲に修飾されることにより、タウ機能障害を引き起こしタウの凝集を引き起こすことが実証されている。治療候補としてのHDAC6阻害剤
https://www.ncbi.nlm.nih.gov/pubmed/25031639/
タウアセチル化阻害剤による治療は、タウモデルマウスの記憶障害が回復し、海馬萎縮が予防された。
https://www.ncbi.nlm.nih.gov/pubmed/26390242/
https://www.ncbi.nlm.nih.gov/pubmed/27104579/
非ステロイド(NSAID)は、アセチルトランスフェラーゼp300誘導のタウアセチル化を抑制し、前頭側頭での行動障害および神経変性を海鮮することがFTDマウスモデルで示されている。
https://www.ncbi.nlm.nih.gov/pubmed/26390242/
PSP患者へのサルサレート(NSAID)経口投与
https://clinicaltrials.gov/ct2/show/NCT02422485
GSK3阻害剤投与による進行性核上性麻痺患者の脳萎縮の進行を軽減
https://www.ncbi.nlm.nih.gov/pubmed/24488721/
メチル化タウ
メチル化は、タンパク質基質への1つ以上のメチル基の酵素的付加を指す。典型的には、メチル基はS-アデノシルメチオニンに由来し、それは標的タンパク質のリジンまたはアルギニン側鎖の末端アミノ基に付加される。
メチル化タウは、特に後期アルツハイマー病の脳においてNFTと高度に共局在する。
https://www.ncbi.nlm.nih.gov/pubmed/22033876/
タウのメチル化は、たんぱく質の異常凝集に対して保護的役割を果たしている可能性がある。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5554484/#s3title
タウSUMO化
スモールプロテインが翻訳後に標的たんぱく質に結合する修飾をSUMO化と呼ぶ。
SUMOアイソフォーム SUMO1、SUMO2、SUMO3が細胞内で発現している。
タウの過剰リン酸化はおそらくSUMO化に先行するが、タウのSUMO化とリン酸化は相互に増強しあう。
SUMO化はタウのユビキチン化を調節する。K340での過剰リン酸化タウのSUMO化は、ユビキチン化、プロテアソームによる分解を阻害する。
SUMO化は、タウの溶解性を低下させることによりタウ凝集を増強し、タウクリアランスの低下に寄与しえる。
https://www.ncbi.nlm.nih.gov/pubmed/25378699/
SUMO化がタウオパチーのオートファジー – リソソーム経路に関与している可能性があることを示しているが、これはまだ解明されていない。
https://www.ncbi.nlm.nih.gov/pubmed/23229893
SUMO1は、シナプス機能、脊椎密度、記憶に影響を与える。
https://www.ncbi.nlm.nih.gov/pubmed/26022678/
Bin1-タウ
大規模ゲノムワイド関連解析(GWAS) BIN1 アルツハイマー病(AD)のリスクを高変異型
Bin1は、エンドソーム-アミロイド前駆体タンパク質(APP)のプロセシングを増加させることによって、アルツハイマー病の進行を速めることができる。
https://www.nature.com/articles/mp20131
BIN1-タウ複合体の毒性作用
https://actaneurocomms.biomedcentral.com/articles/10.1186/s40478-015-0237-8
サルコシル不溶性タウ / sarkosyl-insoluble-tau
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4713716/
64kDaタウ
https://www.ncbi.nlm.nih.gov/pubmed/22941973/
トリプシン耐性タウ / trypsin resistant tau
https://www.researchgate.net/figure/Trypsin-resistant-tau-bands-in-tauopathies-the-N-terminal-sequences-of-the-tau-species_fig3_301715410
アルツハイマー病では7、10、15 kDaのトリプシン耐性フラグメントが観察された。
タウは直径10〜20 nmのPHFに組み立てられるが、ピック病では約12 kDaのフラグメントが検出された。
CBDおよびMAPTで10〜25 kDaのトリプシン耐性フラグメントがいくつか検出され、10〜25 nmの直径を持つ独特のリボン状の繊維状構造が観察された。
PSPでは細いねじれ状の繊維状構造が観察され、〜33 kDのCTFsと10〜16 kDのトリプシン耐性バンドが見られた。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4713716/
タウの凝集
神経原線維変化(NFT)
タウタンパクが、細胞質中で線維化し沈着したものを指す
神経原線維変化には3つのタイプがある。
タウタンパク質のアセチル化がアルツハイマー病のタウ凝集の原因である可能性が示唆されている。
マウスモデルの研究では、タウ凝集の構造の違いが、脳の特定の領域によって脆弱だったりそうでなかったりする可能性がある。(同じタウ病理でありながら、異なる進行過程を見せる神経変性疾患の説明につながる)
https://www.sciencedaily.com/releases/2016/10/161028205358.htm
また、NFT自体が毒性をもつという直接的な証拠はなく、NFTはタウオリゴマーなどの可溶性タウの高い毒性を防ぐために凝集したということを示唆する研究もいくつかある。
タウオリゴマー
タウの異常リン酸化が初期にタウオリゴマーを形成し神経原線維変化へと発展していく。
タウオリゴマーのプリオン様拡散が示唆されている。
タウフィラメント(PHF)
対のらせん構造であるペアードヘリカルフィラメント(PHF)とストレートフィラメント(SF)が存在する。
Hsp70はタウオリゴマーとは結合するが、タウフィラメントとは結合しない。
脊髄中のリン酸化タウ、アルツハイマー病の前臨床段階で見出されている。
https://www.ncbi.nlm.nih.gov/pubmed/23246918
嗅上皮のPHFタウはアルツハイマー病患者の大多数において観察されており、脳病理と相関する。
https://www.ncbi.nlm.nih.gov/pubmed/20437581
ゴーストタングル
細胞内にあった神経原線維変化が神経細胞の膜構造がなくなったことで細胞外に出現したものをゴーストタングルと呼ぶ。
タウタンパク質に過剰リン酸化が起こる。 → 他のPHFと絡み合る → 軸索からニューロンの体細胞樹洞区画へタウタンパク質が移動 → 微小管の崩壊、輸送システム、不溶性の凝集体が形成される。→ ニューロン細胞の死 → 残りのNFTは死滅した細胞外で「ゴーストタングル」として存在する。
ゴーストタングルはアルツハイマー病発症前段階でも起こりうる。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4939203/
可溶性タウ
不溶性の凝集タウの有害性は広く研究されてきたが、最近では可溶性タウ(単量体と二量体がほとんど)も神経細胞に有毒であるという証拠も増えてきている。
正常なタウからNFT(神経原線維変化)へと変化する過程で、タンパク質が過剰にリン酸化され、誤った場所に局在化し、立体構造が変化してしまったオリゴマー性のタウはNFTではなく、広い意味での「可溶性タウ」と定義されている。
可溶性タウとNFTは、異なる方法異なる時間スケールで細胞に対して有毒である。
タウタングルの存在が、ニューロンの可溶性タウに閾値があることを示しており、細胞の補償機構が働いてくれない可能性がある。
つまりタウ凝集阻害剤が、可溶性タウを増加させることで有害となる可能性がある。
タウの削減には、従来と異なる戦略が必要かもしれない。
タウによる液-液相分離
完全長タンパク質は、液-液相分離(LLPS)を起こすことが示されており、タウの凝集を開始させることが報告されている。
https://www.ncbi.nlm.nih.gov/pubmed/28683104
https://www.ncbi.nlm.nih.gov/pubmed/29472250
リジンに富むタウの微小管結合リピートは、液-液相分離を受ける。
https://www.ncbi.nlm.nih.gov/pubmed/28819146/
液-液相分離
タウ病理の進行
古典的なタウによるアルツハイマー発症機序仮説
古典的な理解は、正常なタウタンパク質は微小管に結合して、微小管の形成や安定化を助ける役割をもっている。しかし、タウタンパク質が過剰にリン酸化されると微小管は不安定になり、崩壊し始める。崩壊したタウタンパク質はからみついて神経原線維変化を呼ばれる塊となる、といったものだろう。
大雑把に書くと
正常なタウタンパク質(MAP) → タウの過剰なリン酸化 → タウオリゴマー → ヘリカルフィラメント(PHF) → 神経原線維変化(NFT)
という流れでアルツハイマー病の発症因子として変化していくのだが、タウオリゴマー、タウ凝集体であるNFTの構造にもいくつかのタイプがあって、どういったタイプがあり、どのタイプが最も有毒であるかなど、まだ多くの点が議論の段階にある。
タウ病理の初期部位
過去のブラークステージにおけるタウ病理の推移は、大脳皮質の原繊維に限定されており皮質下神経核は考慮されていなかったが、最近では皮質下神経核のもつれ前段階a~cとして拡張されている。
https://www.ncbi.nlm.nih.gov/pubmed/26283673
皮質全体のコリン作動性神経支配、皮質のノルアドレナリン作動性神経支配する青斑核、縫線状片などの皮質マントル帯への広範な投射を伴う皮質下神経核にタウ病理が広がることはよく知られている。
セロトニン作動性神経核は、皮質病変のブラークステージ0またはIに対応する初期病理に関与している
タウのもつれは、MCI患者の嗅内皮質に生じる前にすでに基底核において見出されている
https://www.ncbi.nlm.nih.gov/pubmed/19381658
タウ病理は非視床下皮質核、脳幹核に加えて、視床下部、視床、嗅覚、皮質下の辺縁系、運動系、感覚系に見いだされている。
https://www.ncbi.nlm.nih.gov/pubmed/19381658
タウ病理は、最初に内嗅皮質隣接細胞に進み、続いて歯状回、海馬のCA領域、および帯状皮質などのシナプス回路の下流のニューロンに伝播する。タウタンパク質はこれらの領域に広がり凝集する。加齢とともに、シナプス変性が内嗅覚の標的領域で起こり、嗅内皮質ニューロンが失われる。
https://www.ncbi.nlm.nih.gov/pubmed/22365544
タウ病理の早い始まり
発症10年前から増加するタウ
臨床症状が現れる少なくとも10年前には、脊髄液中のタウレベルが上昇していることが報告している。
https://www.ncbi.nlm.nih.gov/pubmed/22784036
https://www.ncbi.nlm.nih.gov/pubmed/22213792
皮質神経核から開始するNFT
4歳下ら29歳まで42人の脳を調べたところ、42人中38人で脳神経細胞に異常にリン酸化されたタウたんぱく質が示された。しかしアミロイドβたんぱく質の沈着は42人中41人で示さなかった。一般的にアルツハイマー病で観察される大脳皮質の神経原線維変化は大脳皮質からではなく皮質神経核から非常に早い時期に始まっていることが示唆される。
https://www.ncbi.nlm.nih.gov/pubmed/21170538
しかし、これらのタウのもつれが不可逆的に原線維凝集体に進行し、アルツハイマー病やその他のタウオパチーの初期ステージとなるのかどうかの問題は依然として論争の問題である。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3673457/
初期のタウ病理は一般的に信じられているよりはるかに早く起こり、そしてその後は非常にゆっくりと進行すると考えられる。
https://link.springer.com/article/10.1007/s004010050645
タウとアミロイドの相互作用
タウとアミロイドの相互作用がタウの神経変性にどのように関与しているかの正確なメカニズムはいまだによく理解されていない。
これは、アルツハイマー病の上流にタウがくるのか、アミロイドがくるのかという問題とも重なる。
アミロイドとタウは両方に病理学的な中心的役割を示す有利な議論がある。
https://www.ncbi.nlm.nih.gov/pubmed/20083042
https://www.ncbi.nlm.nih.gov/pubmed/26007212
https://www.ncbi.nlm.nih.gov/pubmed/23332364
https://link.springer.com/article/10.1007/s00401-010-0794-7
いくつかの証拠が、タウとアミロイドの両方向における相互作用を示唆している。
アミロイドがタウ病理を促進することが可能であり、タウもまたアミロイド病理を促進することができる。
https://www.ncbi.nlm.nih.gov/pubmed/25442111
https://www.ncbi.nlm.nih.gov/pubmed/21193853
アミロイドβオリゴマーは、体細胞、樹状突起へタウの再分布を誘導することができる。
https://www.ncbi.nlm.nih.gov/pubmed/22156588
アミロイドβとタウの相互作用による推定発症機序
アミロイドβ増加 → タウ蛋白の異常リン酸化 → 微小管から単量体タウ蛋白が遊離 → 軸索から神経細胞の細胞体樹状突起部分に移動 → チロシンキナーゼfynと相互作用→ fynが高濃度に → NMDA受容体GluN28をリン酸化安定化 → グルタミン酸シグナルが増幅 → 細胞内へのCa2+流入増加 → アミロイドβ毒性が増加 → 以下繰り返し
NADA受容体の仲介
アミロイドβオリゴマーは、NMDARを過剰活性を仲介してタウのリン酸化、シナプス機能不全の一因となる可能性がある。
https://www.nature.com/articles/cddis2013129
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2772133/
NMDAR活性の阻害は野生型タウ、アミロイドβ誘導によるタウの両方の毒性を無効にするが、GSK-3βの阻害は野生型タウからの毒性に対しての保護効果のみ示し、アミロイドβ誘導性によるタウの毒性を防がない。
https://www.ncbi.nlm.nih.gov/pubmed/19923278
https://www.ncbi.nlm.nih.gov/pubmed/22592800
https://www.ncbi.nlm.nih.gov/pubmed/23618906
アミロイドβへの曝露後のニューロンの過剰興奮は、タウが存在しない場合には低下する。タウはアミロイド誘発性の神経毒性に必要であると考えられる。
https://www.ncbi.nlm.nih.gov/pubmed/11959919
内因性のタウの減少はマウスのアミロイドβレベルに影響を与えず、行動障害を改善する。
https://www.ncbi.nlm.nih.gov/pubmed/17478722
https://www.ncbi.nlm.nih.gov/pubmed/20655099
アミロイドβ、Fynの相乗効果による認知機能障害は、タウレベルに依存する。
https://www.ncbi.nlm.nih.gov/pubmed/21228179
タウが海馬のシナプス可塑性を損なうにはアミロイドβが必要。アミロイドβとタウの相互作用を防ぐことが認知障害治療に有望な戦略でありえる。
https://www.ncbi.nlm.nih.gov/pubmed/21289177
ピログルタミル化アミロイドβの毒性が、タウ発現によって大きく増幅される。
https://www.nature.com/articles/nature11060
タウを除去するとアミロイドプラーク負荷が低下することから、タウもアミロイドを調節するフィードバックメカニズムを示唆する。
https://www.ncbi.nlm.nih.gov/pubmed/23026200
タウのプリオン様伝播
現在のタウ病理学におけるタウの伝播の研究では、タウはプリオン様式によって脳内に広がり進行するモデルが示唆されている。
https://www.ncbi.nlm.nih.gov/pubmed/6801762
https://www.ncbi.nlm.nih.gov/pubmed/19789378
異常型タウの発現は、マウスのタウ凝集は引き起こすが認知障害は起こさない。
https://www.ncbi.nlm.nih.gov/pubmed/23029293
タンパク質が、エンドサイトーシスを介してニューロンによって輸送されるためには、オリゴマー化またはフィブリル化のある特定の状態になければならないことが示唆される。
これらのデータは、蓄積タンパク質は最初に誤って折り畳まれ、ミスフォールディングがプリオンの形式によって正常なタンパク質を汚染することを示唆する。
https://www.ncbi.nlm.nih.gov/pubmed/24035591
Cis P-タウ
生理的に存在するタウは、タウオパチーに見れられる病理的凝集を引き起こすことはできない。可溶性タウの変異体であるCis P-タウが毒性をもつ可溶性タウ変異体であると考えられるようになってきた。
https://www.ncbi.nlm.nih.gov/pubmed/27654282/
Thr231部位のタウリン酸化は、リン酸化タウの立体配座異性化を可能にする。Cis-リン酸化タウは、神経毒性を有しプリオン様式によってニューロンからニューロンへと拡散する。
トランス p-タウとは異なり、Cis立体配座は微小管の構築を促進することができず、脱リン酸化と分解に対してより耐性があり、そしてより凝集しやすい。
https://www.ncbi.nlm.nih.gov/pubmed/23154634/
CisからTransへ変換するPin1
ペプチジル – プロリルシス – トランスイソメラーゼであるPin1は、主にThr231残基でリン酸化タウに結合し、その部位でCisからTrans p-タウへの変換を触媒する。
Pin1のダウンレギュレーションにより、タウのCis立体配座が蓄積する可能性がある。
Pin1遺伝子多型では、遅発型アルツハイマー病発症リスク増加と関連している。
https://www.ncbi.nlm.nih.gov/pubmed/16384626/
対照的に、Pin1阻害の減少をもたらすPin1 SNP(rs 2287839)は、ADの発症遅延と関連している。
https://www.ncbi.nlm.nih.gov/pubmed/20580132/
https://www.ncbi.nlm.nih.gov/pubmed/22464332/
p53は小胞体ストレス下でPin1発現を負に調節する
https://www.ncbi.nlm.nih.gov/pubmed/25451271
EGCGはPin1酵素に直接結合して活性を阻害する。
https://www.ncbi.nlm.nih.gov/pubmed/21893494
Pin1によるPP2A活性
https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0021521
外傷性脳損傷 TBI
Cis P-タウは、外傷性脳損傷、慢性外傷性脳損傷において急激に増加する。Cis P-タウ抗体はCis P-タウを遮断しタウオパチーの発症を防ぐ。
https://www.ncbi.nlm.nih.gov/pubmed/26176913/
エキソソーム・ニューロン結合を介したタウ伝播
αシヌクレイン、タウはエキソソームを介して細胞外へ分泌されえる。タウおよびαシヌクレインは、ニューロンの結合部位を介して輸送することが可能であり、in vitro研究で、変異体タウ、野生型タウ、繊維状αシヌクレイン、野生型TDPが逆行および順行軸索を介して輸送することができる。
https://www.ncbi.nlm.nih.gov/pubmed/25588378
https://science.sciencemag.org/content/349/6248/1255555.long
in vitro研究では、単量体タウではなく原線維タウ凝集体が細胞によって取り込まれ、続いて細胞内タウのフィブリル化の増殖を誘導することができることが示された。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2966103/
https://www.ncbi.nlm.nih.gov/pubmed/19282288
変異型タウは神経変性および過剰リン酸化タウからなる豊富なフィラメントを含むタウオパチーの特徴を示す。対照的に、野生型ヒトタウの単一アイソフォーム発現では、マウスにタウフィラメントの生成を起こさず神経変性も示さない。
https://www.ncbi.nlm.nih.gov/pubmed/19503072
嗅内皮質にヒト型変異タウを発現するマウスでは、凝集したタウは、シナプス伝達を経由してその他の脳部位に広がっていくことが示唆される
https://www.ncbi.nlm.nih.gov/pubmed/25534024
タウ病理の伝播は、空間的な近接性ではなく連結性、シナプス結合性に依存して広がっていく。
https://www.ncbi.nlm.nih.gov/pubmed/24531916
http://www.jneurosci.org/content/33/3/1024
神経活動によるタウ放出の増加
神経活動は細胞外へのタウ放出を増加させる。ニューロン活性によるタウの放出は数時間以内にタウを放出させるが、タウクリアランスは数日かかるため、タウの代謝サイクルが遅いことによってタウが凝集しタウ病態を引き起こす。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3949564/
グルタミン酸神経伝達のようなシナプス興奮は、例えばタウの細胞外空間への分泌を誘導することが示されている
https://www.ncbi.nlm.nih.gov/pubmed/24534188
タウは正常な細胞からも低レベルで、従来の経路とは異なる経路で放出されており温度依存性である。
https://www.ncbi.nlm.nih.gov/pubmed/22668776
内因性のタウの生理的な分泌は、神経活動によって刺激される。可溶性タウのシナプス前放出から生じている可能性が示されている。
https://www.ncbi.nlm.nih.gov/pubmed/23412472
タウのミスフォールディング
細胞外の凝集したタウはミスフォールディング状態のまま細胞内に伝播する。ミスフォールディングタウが脳内で伝播するには、ニューロンの近接性、接合性、リン酸化タウ、タウの組み合わせによって反映されるであろう。
https://www.ncbi.nlm.nih.gov/pubmed/19282288
神経活動はタウの放出と拡散を増進する。下流の神経細胞性においてミスフォールディングたんぱく質およびシード形成をもたらしタウ病理を増強する。
深部脳刺激(DBS)、または経頭蓋磁気刺激(TMS)などの刺激療法は、否定的な影響をもたらす可能性がある。
https://www.ncbi.nlm.nih.gov/pubmed/27322420
タウのミスフォールドされた配座異性体のタウが播種されると、大量の可溶性タウが著しく動員される。
https://www.ncbi.nlm.nih.gov/pubmed/21372138
ミクログリア媒介のタウ伝播
タウ病理のエキソソーム経路はミクログリアを含むことがある。
タウ病理を媒介するこのエキソソーム経路はミクログリアを含むことがある。
https://www.ncbi.nlm.nih.gov/pubmed/25833819
ミクログリアの枯渇は、タウの増殖を抑制し歯状回の興奮性を低下させる。ミクログリアはエキソソーム分泌を介してタウを拡散させるが、エキソソーム合成を阻害すると、in vitro、in vivoでタウ増殖を有意に減少させることができる。
タウのシナプスを介した脳内の伝播に加えて、シナプス結合のないニューロン間において、エキソソームを介したミクログリア媒介によるタウ伝播が、タウ病理を促進する機序として存在しえる。
https://www.ncbi.nlm.nih.gov/pubmed/26436904
https://www.ncbi.nlm.nih.gov/pubmed/25833819
https://www.ncbi.nlm.nih.gov/pubmed/19289607
アストロサイト・オリゴデンドロサイト
病理学的タウの細胞間伝播は、ニューロンに加えて、アストロサイト、オリゴデンドロサイトも含む。
https://www.ncbi.nlm.nih.gov/pubmed/23690619
タウ免疫療法
タウ凝集体のシードはマウスの腹腔内注射によっってタウシードが中枢神経系に到達することがある。タウ免疫療法(tau immunotherapy) の可能性
https://www.ncbi.nlm.nih.gov/pubmed/24050961
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5979300/#sec6-ijms-19-01160title
タウ凝集体立体配座によるタウオパチーの進行パターン
マウスではタウ凝集体の異なる「立体配座株」が存在する。
https://www.ncbi.nlm.nih.gov/pubmed/24857020
立体配座の異なりは、異なる神経病理と表現型を生じさせることは実証されている。
https://www.ncbi.nlm.nih.gov/pubmed/21421910/
タウの凝集体の立体配座は、天然に存在するものと合成されたものでは播種の効力に違いが生じる。
https://www.ncbi.nlm.nih.gov/pubmed/25406315
https://www.ncbi.nlm.nih.gov/pubmed/21372138
この立体配座の違いがプリオン様式によって脳内を伝播することにより、タウオパチー疾患が、病理の進行する領域、パターンに違いを生じさせるのかもしれない。
https://science.sciencemag.org/content/349/6248/1255555.long
ニューロンネットワークの再ルーティングを阻害
アルツハイマーにおける認知喪失の背後にある原因は、生存ニューロンの内部に蓄積する可溶性タウタンパクであることが示唆されている。神経保護剤の単独使用は可溶性タウが減少した場合にのみ記憶が救済され得る。
ニューロンにタウが蓄積し始めると、機能不全で生き残り脳における電気信号伝達、および記憶形成の障害につながる可能性がある。
タウが内部に蓄積されたままニューロンを保存する神経保護戦略(例レスベラトロールなど)は疾患を加速させる可能性があり、疾患を改善するには複数の薬物を用いた戦略が必要である。(+可溶性タウを標的にするべき、メチレンブルーなど)
A 正常な脳の神経シグナル
B タウの蓄積により正常なシグナル伝達ができない。
しかし、ニューロンが完全には死んでいないので、再接続、再ルーティングもできない状態
C ニューロンが死んだことで、ネットワークの再ルーティングができている状態、可塑性のある状態
https://www.ncbi.nlm.nih.gov/pubmed/21559875
高度なヒト脳機能の脆弱性
https://www.ncbi.nlm.nih.gov/pubmed/22002422
ヒトの脳は一生を通じて常に情報を書き込み、書き換えており、非常に高い可塑性が要求される。この高い可塑的能力はシナプス結合の調節に必要な分子、成長栄養因子、膜代謝回転、、シナプス代謝回転が求められる。アルツハイマー病の発症はこの高い脳の高次機能を維持することが難しくなり、自己組織化メカニズムが機能しなくなった状態であるかもしれない。
https://www.ncbi.nlm.nih.gov/pubmed/11182240
アルツハイマー病によって影響を受ける脳領域は、海馬、新皮質関連領域、コリン作動性基底前脳神経細胞などの、ヒト化の脳の進化に伴う高次の脳機能構造と関与している。
ニューロンが成熟後に特に脆弱性ををもつのは、「不安定な分化状態」(G0停止期)である。この細胞周期と分化制御による構造的な脳の自己組織化は、ヒトに特有のものでありその脆弱性が神経変性と関連するかもしれない。
https://www.ncbi.nlm.nih.gov/pubmed/11124422
神経変性疾患とタウ
タウと関連する疾患
- アルツハイマー病
- 筋萎縮性側索硬化症/パーキンソニズム – 認知症複合体
- 嗜銀顆粒性認知症
- 慢性外傷性脳症
- 皮質基底核変性症
- 石灰化を伴うびまん性神経原線維変化
- ダウン症候群
- 家族性イギリス痴呆
- 家族性デンマーク認知症
- 家族性前頭側頭型認知症とパーキンソニズム
- Gerstmann-Sträussler-Scheinker disease
- Guadeloupe パーキンソニズム
- ハンチントン病
- 髄膜血管腫症
- 筋緊張性ジストロフィー
- 脳内鉄蓄積を伴う神経変性
- ニーマンピック病、C型
- 神経原線維変化を伴う非グアマ人運動ニューロン疾患
- ピック病
- 脳炎後パーキンソニズム
- 進行性核上性麻痺
- SLC9A6に関連する精神遅滞
- 亜急性硬化性全脳炎
- 神経原線維変化型老年認知症
- 球状グリア封入体を伴う白質タウオパチー
タウ関連遺伝子変異
タウをコードするMAPT遺伝子は50を超える突然変異が同定されている。
https://www.frontiersin.org/articles/10.3389/fnagi.2015.00192/full
散発性タウオパチー
毒素アノナシン
散発性タウオパチー
カリブ海に浮かぶ西インド諸島のなかのリーワード諸島の一角をなすグアドループ島(フランスの海外県)(Guadeloupe)
ここでは、サソプ果実などに含まれる天然毒素アノナシン(annonacin) が消費されることと関連して高い非定形パーキンソン病患者の発症率を示す。
http://www.jneurosci.org/content/27/29/7827
https://www.ncbi.nlm.nih.gov/pubmed/17303592
https://en.wikipedia.org/wiki/Annonacin
アノナシンは、ミトコンドリア複合体I阻害作用をもつ。
複合体Iの阻害作用は、ROS産生の増加とATP産生の減少をもたらす。
https://www.ncbi.nlm.nih.gov/pubmed/12911637
ATPの枯渇がタウの細胞蓄積をもたらすかもしれない。
https://www.ncbi.nlm.nih.gov/pubmed/10987850
ヘロイン
ヘロイン乱用歴のある患者の脳では、過剰リン酸化タウの広範囲な沈着が実証されている。しかしアミロイドβの沈着は検出されなかった。またヘロイン中毒はαシヌクレイン、TDP-43タンパク質を誘発することも確認できなかった。パーキンソン病はαシヌクレインとも関連しており、ヘロイン中毒によるパーキンソン症候群はまれである。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4609594/
タウクリアランス・分解経路
タウクリアランスのメカニズムはほぼアミロイドβと同様であると考えられている。
アミロイドβとタウは、ユビキチン-プロテアソームシステム(UPS)、オートファジー-リソソームシステム(ALS)、プロテアーゼ(トロンビン、HTRA1、カルパイン、カスパーゼ)、ミクログリアによって分解されることが研究によって示されている。
タウのBBB経路は存在しない
タウクリアランスはアミロイドβクリアランスよりも理解が進んでいないが、アミロイドβクリアランスほど複雑ではない。
BBB経由のタウの特異的なトランスポーターは同定されていない。おそらくタウはBBBを通してはクリアランスされない。その他のクリアランス経路はアミロイドβと同じく、くも膜絨毛、血液脳脊髄液関門(BCSFB)を介して血流に、またはリンパ管クリアランスによって頸部リンパ節に排出することができる。
脳損傷を受けるとBBBの透過性は一時的に高まり、タウのクリアランスが促進される。
https://www.ncbi.nlm.nih.gov/pubmed/11532253/
シンク効果によるバルクフロー
タウは主に、脳間質液によるバルクフロー、脳脊髄液への吸収クリアランスによって脳から除去されると考えられている。
アミロイドβ同様、タウも抹消シンク機構によってタウが脳から除去できることが示されており、シンク機構を利用したアルツハイマー病治療戦略がありえる。
https://www.ncbi.nlm.nih.gov/pubmed/24647946/
細胞内タウのオートファジー・UPS経路
タウタンパクはプロテアソーム系、オートファジー系の両者によってそのほとんどが分解される。
細胞内のタウは、主として、オートファジー -リソソーム経路を介したリソソームによる分解とユビキチン–プロテアソーム経路を介したプロテアソーム分解によって排出される。
どちらもタウの処理に負われて処理できなくなると、クリアランスの機構が不全になるだけでなくクリアランス機構そのものが壊れる可能性がある。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3759803/
https://www.ncbi.nlm.nih.gov/pubmed/24531154/
https://www.ncbi.nlm.nih.gov/pubmed/22817709
これらの経路はアルツハイマー病で障害を起こしており、可溶性細胞内タウが蓄積することが示されている。
https://www.ncbi.nlm.nih.gov/pubmed/24027553
UPSの機能不全は過剰リン酸化タウオリゴマーの沈着をもたらす。
https://www.ncbi.nlm.nih.gov/pubmed/22867711
オートファジーとUPSの相互作用
オートファジー系とプロテアソーム系との間に、有意で広範な相互作用がある。
ラットのプロテアソームを阻害することで、オートファジーの代償的アップレギュレーションにより細胞中のオートファゴソームが増加し、総タウタンパクが減少した!
家族性アルツハイマー(PS1)はリソソーム酸性化、オートファゴソーム作用の障害に両方に関連している。オートファージ障害はおそらくp62(両方の系のシャペロン)の蓄積を介してプロテアソームを阻害する。
オートファジー
・マクロオートファジー
(オートファゴソームで取り囲みバルク分解)
・ミクロオートファジー
(オートファゴソームを介さない)
・シャペロン介在性オートファジー
(HSPを使った標的型分解)
・マイトファジー
(障害のあるミトコンドリアスカベンジャーとして選択的に作用、アルツハイマー病ではマイトファジーに障害がある。)
アルツハイマー病においてオートファジー障害があることを示唆する証拠が存在する。
BAG3によるUPSとオーロファジーの調節
プロテアソームを阻害 → コシャペロンBAG3とJNK活性 → タウクリアランスが増加
BAG3がタウタンパク質レベルに重要な役割を担っている。
ミスフォールドタンパク質が分解経路によって効率的に除去されない場合、ミスフォールドタンパク質は蓄積し、UPSおよびオートファジーをブロックしえる。
BAG3およびBAG1は、HSP70結合クライアントに対して競合し、標的化する。
https://www.ncbi.nlm.nih.gov/pubmed/25212465
オートファジーの阻害とフラグメントF1
オートファジー-リソソーム系は、タウ凝集体およびタウ凝集の先駆体の両方を除去する役割を有する。オートファジーの阻害は、サイトゾルプロテアーゼによってN末端付近を切断されたフラグメントF1を生じさせる。
フラグメントF1はリソソームには完全に入らず、リソソーム膜と会合したままとなり表面でタウオリゴマーを形成する。このタウオリゴマーがリソソーム機能を妨げる可能性がある。
https://www.ncbi.nlm.nih.gov/pubmed/19654187
カルパイン分解
細胞内タウは、細胞内カルシウム濃度の上昇にカルパインが応答して分解する。
プロテインキナーゼAによるタウの過剰リン酸化は、カルパインによる分解への耐性を増加させる。
https://www.ncbi.nlm.nih.gov/pubmed/1730702/
カルパインが仲介するタウの開裂は、タウ断片化をもたらす可能性がある。
この断片化されたタウフラグメントは、タウ凝集を部分的に阻害する可能性が示唆されるが、タウ凝集はまたカルパインによる開裂を妨げ、毒性タウフラグメントの蓄積を招くフィードバック回路が生じるかもしれない。
https://www.ncbi.nlm.nih.gov/pubmed/21442128
ミクログリアの食作用
ミクログリアの食作用は、細胞外タウのクリアランスに中心的な役割を果たす。
https://www.ncbi.nlm.nih.gov/pubmed/26638867
細胞外可溶性タウのリンパ管経路
細胞外の可溶性タウは、くも膜絨毛およびBCSFBを介して脳から血液中へと輸送される可能性があり、細胞外タウはリンパ管クリアランスによって除去されることができる。
脳のアクアポリンAQP4を喪失すると、このリンパ管クリアランス機構は損なわれる可能性がある。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4252540/
可溶性細胞外タウは、プリオン様のようなタウ病変をもたらす。可用性細胞外タウは、ムスカリン性タイプ1に結合することで細胞内のカルシウム濃度を上昇させ、さらに細胞内タウを放出させるかもしれない。
グリンパティック系経路
細胞外タウがエンドサイトーシスによって除去されない場合、グリンパティック系を介して除去される可能性がある。
https://www.ncbi.nlm.nih.gov/pubmed/25471560
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4694579/
外傷性脳損傷後のマウスグリンパティック系によるクリアランスはマウスで60%低下した。AQP4ノックアウトマウスではさらに大きく損なわれた。グリンパティック経路の機能障害は外傷性脳損傷のタウ病態を促進する。
https://www.ncbi.nlm.nih.gov/pubmed/25471560/
タウの抹消クリアランス
顎下腺、S状結腸、肝臓、頭皮、腹部皮膚などのヒト末梢組織にタウ種が存在することが示唆され、タウも末梢で除去される可能性があることが示された。
https://www.ncbi.nlm.nih.gov/pubmed/27716678/
タウタンパク質を分解する化合物
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3759803/
しかし、これらの酵素はタウタンパク質のクリアランスへは直接的に結びつかず、装飾タウ種を再び生成することで、タウ病理の進行、タウのクリアランスの増強どちらか、または両方に寄与しうる。

