Contents
Front Mol Neurosci.2018; 11: 220.
オンライン公開 2018 Jun 28. doi:10.3389/fnmol.2018.00220
The Orexin/Receptor System: Molecular Mechanism and Therapeutic Potential for Neurological Diseases
要旨
オレキシン(Hypocretins)は、主に外側視床下部(LH)のオレキシン含有ニューロンから分泌される2つの神経ペプチドで、ハイポクレチンとも呼ばれる。オレキシンは、オレキシン受容体1型(OX1R)と2型(OX2R)という2つのGタンパク質共役型受容体(GPCR)に結合して活性化することにより、その作用を制御している。
オレキシン/受容体経路は、摂食行動、睡眠覚醒リズム、報酬と中毒、エネルギーバランスなど、多くの生理的プロセスにおいて重要な調節機能を担っている。さらに、ナルコレプシー、うつ病、虚血性脳卒中、薬物中毒、アルツハイマー病などの神経疾患の病態にオレキシン/受容体経路が関与していることが、いくつかの報告で明らかにされている。
本総説では、神経疾患におけるオレキシン/受容体システムの発現パターン、生理機能、潜在的な分子メカニズムについてまとめ、神経疾患の基礎研究および臨床治療の観点からこれらの経路を考察するための全体的な枠組みを提供する。
キーワード オレキシン、受容体、神経保護、パスウェイ、神経疾患、分子機構、、Suvorexant 、スボレキサント (ベルソムラ)
はじめに
オレキシンはハイポクレチンとも呼ばれ、主に外側視床下部(LH)のオレキシン含有ニューロンに由来する一対の神経ペプチドである。オレキシン-A (OA; hypocretin-1)とオレキシン-B (OB; hypocretin-2) は近縁の低分子ペプチドで、中枢および末梢神経系に広く分布している。(de Lecea et al.,1998; Sakurai et al.,1998).オレキシンは脳室内投与により食物摂取を刺激し、当初は摂食行動の制御因子として報告された(Yamanaka et al.,1999)。その後の実験により、睡眠覚醒周期の調節(de Lecea and Sutcliffe,2005; Chow and Cao,2016)、エネルギー恒常性(Tsuneki et al.,2012)、神経内分泌機能(Inutsuka and Yamanaka,2013)、糖代謝(Tsuneki et al.,2016)、ストレス適応反応(Xiao et al,2013)、報酬追求や薬物中毒(Aston-Jones et al.,2010)などのこれらのペプチドの多くの重要な生理機能が判明した。
オレキシンは、その同族であるGタンパク質共役型受容体(GPCR)、オレキシン受容体1型(OX1R、Hcrtr-1とも命名)および2型(OX2R、Hcrtr-2)と結合し、異なる下流のシグナル経路を活性化し、それによって様々な生理機能を発揮する(桜井ら、1998)。オレキシンおよびオレキシン受容体は、多くの疾患(Perez et al.,2015; Imperatore et al.,2017)、特に神経疾患(Feng et al.,2014; Liguori et al.,2014)において異所性発現しており、オレキシン/受容体経路がこれらの疾患の病態や発症に重要な役割を果たすことが示唆されている。本総説では、オレキシンとその受容体の発現量と生理機能に焦点を当てる。さらに、ナルコレプシー、薬物中毒、うつ病、虚血性脳卒中、アルツハイマー病(AD)などの神経疾患におけるオレキシン/受容体経路の貢献の可能性について議論する。これらの議論を総合すると、オレキシン/受容体システムに関する現在の知見と、この情報を神経疾患の臨床治療に応用する展望がまとめられる。
オレキシンの構造
1998年、2つの実験グループがほぼ同時に、ラット脳のLHとその隣接領域において、一対の新しい神経ペプチドを発見した。一方のグループ(de Lecea et al.,1998)はDNAサブトラクティブハイブリダイゼーションを用い、もう一方は高速液体クロマトグラフィー(HPLC)を用いた(de Lecea et al.,1998; Sakurai et al.一方、Sakurai et al.(1998)は、ギリシャ語の「食欲」にちなんでOAとOBと命名した。
オレキシン遺伝子の構造は、2つのエクソンと1つのイントロンからなり、すべての脊椎動物で保存されている。ヒトのオレキシンをコードするゲノムDNA配列は1432塩基対(bp)である。第1エキソンには5’非翻訳領域(UTR)とシグナルペプチドの最初の7アミノ酸(aa)が含まれ、第2エキソンにはオープンリーディングフレーム(ORF)の残りと3’UTRが含まれている。ヒトオレキシンのmRNA配列は616塩基からなり、131aaの残基を含む前駆体ペプチド(prepro-orexin)をコードしている。prepro-orexinの最初の33 aaはシグナルペプチドを構成し、それに続くOAとOBのそれぞれ33 aaと28 aaは46% (13/28)のアミノ酸同一性を有している。(Sakurai et al.,1998; Alvarez and Sutcliffe,2002).オレキシン前駆体およびオレキシンの分子構造を(図(Figure11)に示す。
図1 オレキシン前駆体およびオレキシンの分子構造
(A)2つのエクソンと1つのイントロンを含むヒトプレプロオレクシンゲノムDNA。(B)5’非翻訳領域(UTR)、シグナルペプチド、オレキシンA(OA)またはオレキシンB(OB)をコードするオープンリーディングフレーム(ORF)、および3’UTRを含むヒトオレキシンのmRNA(mRNA)。(C)OA(33aa)およびOB(28aa)のアミノ酸配列。緑色のラベルは、OAとOBの両方で同一であるアミノ酸を示す。
OAとOBの分子量はそれぞれ3562 Dopamine (DA)と2937 Daである。OAには4つのCys残基があり、2つの鎖内ジスルフィド結合を形成している(図(Figure1C).1C)。ヒト、マウス、ラット、ウシのOA配列は同一であり、その高い保存性から、OAが重要な生理機能を持つことが予測される(Wong et al., 2011)。マウスとラットのOB配列も同一だが、ヒトのOBは2つの位置でネズミのペプチドと異なっている(図(Figure2).2)。ヒトのペプチドの2位のセリン残基は、ウシとイヌではプロリンに置き換わっている。また、ラット、マウス、ブタでは18位のセリンはアスパラギンに置き換わっている。
図2 異なる生物種におけるOAとOBのアミノ酸配列
(A)OAのアミノ酸配列は、ヒト、ラット、マウス、ウシ、ブタにおいて同一である。(B)OBのアミノ酸配列は、ヒト、ラット、マウス、ウシ、イヌで高度に保存されている。色の違いは、種間で異なるOBのアミノ酸を示す。
オレキシン受容体(Orexin Receptors)
OAとOBは、OX1RとOX2Rという2つのGPCRに結合して活性化することで、様々な作用を発揮する。ヒトのOX1RとOX2RのmRNAの長さはそれぞれ1564bpと1843bpで、425aと444aaのタンパク質に翻訳される。OX1RとOX2Rは64%のアミノ酸を共有している。ラットOX1RとOX2RのmRNAは、それぞれ2469bpと3114bpの長さで、413aaと460aaのタンパク質をコードしている。ヒトとラットのOX1RとOX2Rは94%と95%の同一性を持っており、オレキシン受容体は哺乳類間で高度に保存されていることが示された。
オレキシン受容体に関する最初の報告では、OAとOBは異なる親和性で受容体サブタイプに結合することが明らかにされた(Voisin et al., 2003)。OAがOX1Rに優先的に結合し、OBの5-100倍の親和性を持つのに対し、OAとOBは共に選択性の低いOX2Rに対して同様の親和性を持つ(Sakurai et al.,1998; Ammoun et al.,2003)。
オレキシンを含むニューロンは様々な脳領域に広く投射しているが、2つの受容体は異なる分布をしている(Marcus et al., 2001)。両タンパク質は少なくとも中枢神経系のいくつかの領域で共発現しており(Trivedi et al.,1998; Hervieu et al.,2001; Cluderay et al.,2002)、例えば腹側被蓋野(VTA)、小脳側被蓋核(PPT)、後背位被蓋核(LDT)などがある。OX1Rは神経節(LC)に優先的に発現し、OX2Rは主に結節乳頭核(TMN)に分布している。オレキシンのOXRに対する選択性と受容体の明確な分布が、オレキシン/受容体経路による生理学的作用の違いに関与していると考えられる。
オレキシン/レセプターシグナル伝達経路
2種類のオレキシンと2種類の受容体が存在することは、細胞内シグナル伝達経路に多様性をもたらすと考えられている。オレキシン/受容体シグナル伝達経路は、組換え細胞株やネイティブシステムで説明されている。ほとんどのGPCRを介した経路と同様に、オレキシンはまずOXRに結合し、次に少なくとも3つのサブタイプのGタンパク質(Gq/11、Gi/o、Gs)または他のタンパク質(例えばβ-アレスチン)を活性化する。これらのエフェクターはその後、ホスホリパーゼ、イオンチャネル、プロテインキナーゼを制御し、最終的に様々な下流のシグナル伝達経路の活性化を誘発する(Dalrymple et al., 2011;Kukkonen and Leonard、2014;Leonard and Kukkonen、2014)。
カルシウムは、GPCRを介したシグナル伝達の非常に重要なセカンドメッセンジャーである。これまでの研究で、オレキシンを投与すると、OX1RとOX2Rを過剰発現した細胞において、細胞内Ca2+濃度([Ca2+]i)が著しく上昇し、この効果は主に古典的ホスホリパーゼC(PLC)カスケードの活性化によって引き起こされる(PLC-IP3/DANG;Lundら、2000; Ammounら、2006a; Johanssonら、2008)ことが示されている。その後の研究で、OAがOX1Rに作用し、それが過渡受容体電位チャネル3(TRPC3)を活性化し、それによってCa2+応答が引き起こされることが示された(Peltonen et al., 2009)。これらの結果から、オレキシン受容体は、カルシウムレベルの変化が主にGPCRを介して媒介されるという当初の考えとは対照的に、非選択的カチオンチャネル(NSCC)を介して[Ca2+]i上昇の新しいメカニズムを活性化することが明らかになった。
その他のオレキシン/レセプターシグナル伝達経路も報告されており、ホスホリパーゼD(PLD)/ホスファチジン酸(PA;Johansson et al., 2008)、ホスホリパーゼA(PLA)/アラキドン酸(AA;Turunen et al., 2012)、およびマイトジェン-アクティベーションプロテインキナーゼ(MAPK)カスケードを含む(Ramanjaneya et al.)ヒトOX1Rを安定的に発現するCHO細胞では、ヒトOX1RはnPKCを介してPLD1を強力に活性化するが、RhoファミリーGタンパク質は活性化しない(Jäntti et al., 2012)。OX1Rを発現するHEK293細胞やNeuro-2a細胞では、OAによるOX1Rの刺激が2-アラキドノイルグリセロール(2-AG)とAAの両方を解放する(Turunen et al., 2012)。オレキシンはまた、細胞株と組織の両方において、p38-MAPKシグナル経路を活性化し、用量および時間依存的にリン酸化ERK1/2のレベルを増加させる(Milastaら、2005;Ammounら、2006b)。オレキシンによって誘導されるERK1/2の活性化には、PKA経路ではなく、Gq/PLC/PKCシグナルが関与している(Wenzel et al., 2009)。また、Ramanjaneyaらは、OAやOBに応答してERK1/2とp38が急速にリン酸化され、主にGqと、より少ない程度ではあるがGiによって媒介されることを示した(Ramanjaneya et al.,2009).また、OAは、OX1RによるAKTシグナル経路の刺激を介して、ラットインスリノーマ細胞の増殖に影響を与える(Chen et al., 2013)。これらの結果は、オレキシン/受容体システムが古典的なシグナル伝達経路以外の経路を介して強力な細胞内シグナルを活性化できることを示している(図(Figure33)。
図3 オレキシン/受容体系が介在するシグナル伝達経路の模式的概要
オレキシンがオレキシン受容体1型(OX1R)またはOX2Rに結合すると、GqまたはGiサブタイプが刺激され、その後、ホスホリパーゼC(PLC)、ホスホリパーゼA(PLA)、ホスホリパーゼD(PLD)またはアデニルサイクラーゼ(AC)の活性化を誘導し、最終的には細胞質Ca2+の上昇と下流のカスケード反応が起こる。さらに、OAがOX1Rに結合し、非選択的カチオンチャネル(NSCC)を活性化することでCa2+を上昇させる。
ニューロン様細胞では、オレキシン/受容体経路は上記の経路と同様であり、PLCの活性化と[Ca2+]iの上昇がシグナルの中心的役割を果たす(Holmqvist et al., 2002)。様々なタイプのニューロンにおいて、オレキシンはOXRに結合し、その後、PKC依存または非依存経路を通じて細胞内カルシウムシグナルを活性化する(Ozcan et al., 2010)。例えば、ドーパミン作動性ニューロンでは、L型およびN型Ca2+チャネルの活性化によって[Ca2+]iを上昇させ、この効果はホスファチジルコリン特異的PLCおよびPKCによって媒介される(Uramura et al., 2001)。OAとOX1Rの組み合わせは、前頭前野のニューロンにおいて、細胞内のPLC-PKCシグナル経路によって活性化されたL型Ca2+チャネルを介した細胞外Ca2+流入に依存して、[Ca2+]iの増加を誘導する(Xia et al.,2009)。OX1R-PLC-PKCを介して、OAが電位依存性L型カルシウムチャネルをアップレギュレートし、その後、NPYニューロンにおける視床下部AMPKシグナル伝達経路を活性化する(Wu et al., 2013)。また、オレキシンはOX2Rを介してシナプス後[Ca2+]iを増加させ、[Ca2+]iの増加はAC-PKAを介した電位依存性R-およびT型Ca2+チャネルの活性化によって誘導される(Nakamura et al., 2010)。オレキシンは、低酸素ストレスを受けたラット皮質神経細胞においてAktキナーゼ活性化を刺激し、オレキシンの生存促進作用は濃度および時間依存的に発現した(Sokoowska et al., 2014)。また、分化した神経芽腫細胞では、OA結合型OX1Rがジアシルグリセロール活性化チャネルを介してCa2+の流入を増加させ、活性化したPKCによって抑制される(Nasman et al.,2006)。
オレキシン/受容体とアデニルシクラーゼ(AC)/cAMPの結合は、いくつかの研究で報告されている。例えば、培養ラット皮質ニューロンでは、OAやOB刺激によりOX2RがGiタンパク質に結合し、cAMP形成が抑制される(Urbanska et al., 2012)。しかし、OAもOX1Rを活性化し、培養ラットアストロサイトのcAMP合成を刺激する(Woldan-Tambor et al., 2011)。さらに、オレキシン/受容体シグナルは、mTORC1経路を急速に活性化し、この経路はリソソームv-ATPase経路によって引き起こされ、その結果、一過性の細胞質カルシウムに依存する(Wang Z. et al.,2014)。
一般に、OA/OX1R経路はオレキシン/OX2R経路よりもはるかに詳細に検討されてきたが、最近の研究で後者が解明され始めている。一般に、オレキシンによるOX2R活性化に対する反応は、OX1Rに対する反応と同様である。しかし、一部の活性化は弱く、特定のカスケードに対する2つの受容体のカップリングが異なっていることを示している。最後に、オレキシン/受容体システムの細胞内作用の根底にある分子メカニズムを解明し、この経路に関連する疾患を治療するための新しい臨床アプローチを開発するためには、より詳細なネットワーク解析が不可欠である。
オレキシン受容体の二量体化について
従来、GPCRは単量体として存在し、機能すると考えられてきた。しかし、多くの研究により、GPCRはホモおよびヘテロ二量体を形成することもでき、これらの二量体は対応するモノマーによって誘導されるシグナル伝達経路に異なる影響を及ぼすことが示されている(Bulenger et al., 2005;Cottet et al., 2010)。OX1RとCB1受容体は、試験管内試験ではヘテロダイマー/オリゴマーとして存在する(Ellis et al., 2006)。さらに、OX1RとOX2Rは、互いにホモおよびヘテロマー複合体を容易に形成する。CB1受容体はホモダイマーを形成し、また両オレキシン受容体とはヘテロダイマーを形成する(Jäntti et al., 2014)。私たちの研究室では、同じ脳領域で共発現している2つのGPCRが二量体を形成するかどうか、そしてもしそうなら、その二量体化が神経疾患の病態に関与しているかどうかを研究した。マウスオレキシン受容体mOX2αRとmOX2βRを共導入したHEK293細胞において、生物発光共鳴エネルギー移動(BRET)および共免疫沈降(Co-IP;Wang C. et al.,2014)を用いてmOX2αRとmOX2βRの2量体化を観察した。mOX2αRとmOX2βRの二量体化は、mOX2αRまたはmOX2βRを単独でトランスフェクトした細胞で起こるよりも、OAまたはOBによる刺激後にp-ERK1/2の増加および細胞内Ca2+上昇を引き起こすことがわかった。さらに、蛍光共鳴エネルギー移動法(FRET)を用いて、OX1Rとκオピオイド受容体(KOR)の両方がヘテロ二量化できることを明らかにした。ヘテロ二量体はGαタンパク質と結合し、cAMPレベルやcAMP応答エレメント(CRE;図4;Chen et al.,2015)のアップレギュレーションなど、PKAシグナル伝達経路の活性化につながる。また、OX1RとCCK1Rのヘテロダイマーは、OAまたはCCK単独による刺激と比較して、Gαq、Gαi2、Gα12、およびGα13の活性化を抑制することが確認された。これらの実験では、Duolink IIin situPLA検出キットを用いて、HT-29細胞に内因性OX1RおよびCCR1Rを発現させた。さらに、OX1R/CCK1RヘテロダイマーはHT-29細胞の移動に影響を与え、OX1R/CCK1Rヘテロダイマー化がヒト大腸がん細胞において抗移動的役割を果たすことが示唆された(Bai et al.,2017)。これらの結果はすべて、異なるGPCRのヘテロ二量体が、構成する単量体の機能とは異なる特定の機能を発揮し、生理的プロセスに様々な影響を及ぼすことを示している。
図4 OX1R-κオピオイド受容体(KOR)ヘテロダイマーが介在するシグナル伝達経路の変化の模式図。
OX1Rは主にGqサブタイプを活性化し、その後、下流のカスケード反応を誘導する。KORはGiサブタイプに結合し、cAMPとp-CREBの活性を阻害する。OX1RとKORの二量体化は、主要なシグナル伝達経路を変更するが、Gαsサブタイプを活性化し、cAMPとp-CREBの活性を増加させる。
オレキシン/レセプターシグナルと神経系疾患
オレキシン含有ニューロンは LHとその近傍にのみ分布しているが、その神経線維は複数の脳領域に広く投射している。(Chen et al.,1999; Nambu et al.,1999)。さらに、オレキシン受容体は、この広範な投射に対応して拡散的な分布を示す(Marcus et al., 2001)。オレキシン神経の広範な投射と受容体の特徴的な発現は、オレキシン/受容体システムが多面的な機能の制御に関与する構造的基盤を提供すると考えられる。現在の研究では、オレキシン/受容体系が神経系の活動制御に関与しているという考えが支持されている。特に、OA は単純な拡散によって血液脳関門を速やかに通過することができる(Kastin and Akerstrom,1999)。さらに、プレプロオレキシン遺伝子は染色体17q21に位置しており、神経疾患の候補遺伝子となっている(Wilhelmsen,1997)。実際、オレキシン/レセプター系がいくつかの神経疾患で異所性に発現していることを示す証拠が蓄積されており、これらの疾患の発症や病態に重要な役割を担っていることが示唆されている。
オレキシン/レセプターシグナルとナルコレプシー
ナルコレプシーは、カタプレキシー、睡眠麻痺、過眠、催眠幻覚、覚醒から急速眼球運動(REM)睡眠への異常移行を特徴とする慢性睡眠障害である(Mignot、1998)。ナルコレプシーは、視床下部の障害やヒスタミン系の異常と密接な関係があると広く信じられている(John et al., 2004)。上記のいずれにおいても、オレキシン/受容体系が重要な役割を担っていることから、ナルコレプシーの病態に関与していることが強く示唆されている。
複数の研究により、オレキシン/受容体システムの欠損がヒトのナルコレプシーと関連していることが報告されている。これと一致して、このシステムの破壊は動物モデルでナルコレプシー症状を引き起こす。Linら(1999)は、イヌのナルコレプシーモデルで初めて変異型OX2R遺伝子をクローニングし、OX2Rの破壊がイヌのナルコレプシーを引き起こすことを示し、ナルコレプシー患者の治療ターゲットとなることを示唆した。同時に、prepro-orexin遺伝子のノックアウトマウスは、ヒトやイヌのナルコレプシーに酷似したナルコレプシー様表現型を示し、ナルコレプシーがオレキシン系に関連していることを示唆した(Chemelli et al.,1999)。1999年の初め、西野らはナルコレプシー患者9人のうち7人で脳脊髄液(CSF)中のOA濃度が異常に低いことを発見し、これらの患者ではオレキシンの伝達が欠損していることを示唆した(西野ら、2000)。その後の研究で、同じグループは、ナルコレプシー-カタプレキシー連続38例中32例でCSF OA値が劇的に低下したことを報告した(Nishino et al., 2001b)。これらの結果から、彼らは、ヒトのナルコレプシーのほとんどの症例でオレキシンが欠乏していると結論づけ、診断への応用の可能性を示唆した。さらに、ナルコレプシー患者のLH では、オレキシンニューロンの数が、85%-95%減少している。(Thannickal et al.,2000)。ナルコレプシー患者の視床下部、大脳皮質、皮質ではオレキシンmRNAと神経ペプチドは全く存在せず、オレキシン遺伝子の分泌シグナル配列は早発ナルコレプシーの重症例では欠損している(Peyron et al., 2000)。これらの観察から、ナルコレプシーがオレキシン系の欠損と関連していることがさらに証明された。
OX1Rは睡眠覚醒行動に穏やかな影響を与えるが、OX2R-およびOX1R/OX2R-ノックアウトマウスのみがナルコレプシー症状を示し、ダブルノックアウトではより重度の表現型となる(Beuckmann et al.,2004; Scammell and Winrow,2011)。さらに、OX2Rおよびデュアルオレキシン受容体拮抗薬は覚醒を抑制するが、OX1R拮抗薬は抑制しない(Kalogiannis et al.,2011)。これらの結果から、ナルコレプシーの作用は、主にOX2RまたはOX1RとOX2Rの組み合わせによって媒介され、OX1R単独では媒介されないことが示された。
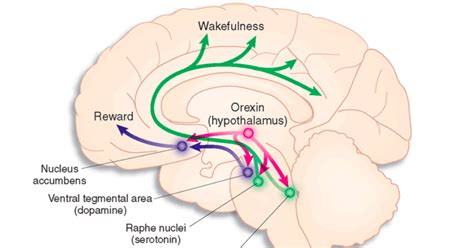
オレキシン含有ニューロンは、求心性神経を介して標的ニューロンを支配するだけでなく、その標的ニューロン、特にモノアミン作動性(すなわちノルアドレナリン作動性;桜井、2007)、セロトニン作動性(Brownら、2001)、ヒスタミン作動性(Erikssonら、2001)、ドーパミン作動性(Korotkovaら、2003)およびコリン作動性ニューロン(Burletら、2002)からの突起を受け入れる。オレキシンニューロンとモノアミンニューロンは、背側ラペ核(DR)とLCにおいて負のフィードバック経路を形成している(Brown et al., 2002;Muraki et al., 2004)。したがって、オレキシンニューロンの活動は、モノアミン作動性ニューロンの活動を増加させる可能性がある。逆に、モノアミン作動性ニューロンはオレキシン作動性ニューロンの抑制作用を低下させ、このダイナミックなメカニズムによって覚醒を安定化させることができる。さらに、オレキシンを含むニューロンの2つの排出経路は、DRセロトニン作動性ニューロンとLCノルアドレナリン作動性ニューロンによって媒介されていると考えられる。OXRを欠損したマウスのDRとLCでOXRの発現を回復させるとカタプレックス様エピソードが抑制され、抑制の程度はOXR発現が回復したDRのセロトニン作動性ニューロンの数と相関し、覚醒の維持はLCで回復したノルアドレナリン作動性ニューロンの数と相関している(Hasegawa et al.,2014).さらに、OX1RとOX2Rの両方を発現するDRのセロトニン作動性ニューロンにおけるOA/受容体シグナルは、カタプレックス様エピソードの予防に極めて重要な役割を果たす(Hasegawa et al., 2014)。実際、ナルコレプシーのドーベルマンのいくつかの脳構造やナルコレプシーのヒトの死後脳ではDAレベルが高く(Nishino and Mignot,1997; Nishino et al.,2001a)、ヒポクレチン欠損ナルコレプシーの睡眠異常にDAの変化が関与しているという仮説と一致した。また、ヒトのナルコレプシーモデルとしてオレキシンノックアウトマウスを用いると、DAがD2様受容体を介したカタプレキシーとD1様受容体を介した睡眠発作を抑制することが示され、ナルコレプシー症状にドーパミン作動性メカニズムが寄与していることが確認された(Burgess et al., 2010)。
これらの結果から、オレキシン/受容体システムは、おそらく複雑な回路を制御することによって覚醒を促進し、睡眠を抑制していることがわかる。ナルコレプシーでは、オレキシンを含むニューロンが徐々に死滅し、オレキシンの量が減少していく。最終的には、このような神経伝達系のバランスが崩れ、ナルコレプシーの症状を引き起こすと考えられる(図(Figure55)。

図5 オレキシンとナルコレプシーの関係の可能性
オレキシンニューロンとモノアミン作動性ニューロンは、負のフィードバック経路でつながっている。オレキシンニューロンが損傷すると、オレキシンレベルが低下し、これらの神経伝達系のバランスが崩れ、ナルコレプシーにつながる可能性が高いと考えられている。
オレキシン/レセプターシグナルと不眠症
不眠症は、世の中に慢性的に蔓延している睡眠障害である。不眠症は、入眠および/または睡眠維持が困難で、日中の眠気、疲労、イライラ、記憶障害などの日中機能の障害につながりやすいことが特徴である(Roth and Roehrs,2003; Ishak et al.,2012)。現在、臨床における不眠症の治療は、認知行動療法に薬物療法を組み合わせたものである(Holbrook et al.,2001; Equihua et al., 2013)。しかし、薬物療法には日中の眠気、耐性、依存性、離脱症状などの潜在的な悪影響があるため(Dundar et al.,2004; Lieberman,2007)、悪影響が少ない新しい不眠症治療が検討されている。
オレキシン/OXR系は、覚醒を促進・維持する役割を持ち、睡眠・覚醒サイクルの制御に強く関与している(Piper et al., 2000)。自由に動き回る猫を対象とした実験では、日中のOA濃度は徐波睡眠時よりも活動的な覚醒時に高かった。さらに、OAレベルはレム睡眠時にSWS時よりも有意に高かった(Kiyashchenko et al., 2002)。リスザルを用いた実験では、CSF中のOAレベルは、起床時には低く、1日のうちで活動レベルが高くなるにつれて徐々に上昇し、夜間の睡眠時には低下した(Zeitzer et al., 2003)。これらの結果は、オレキシンレベルが時間帯と有意な相関を持つことを示唆した。逆に、オレキシン/OXR系を過剰発現させると、睡眠覚醒のサイクルが乱れることになる。ゼブラフィッシュを用いた実験では、オレキシン作動性ニューロンを過剰発現させると、不眠症に似た表現が示された(Prober et al., 2006)。また、不眠症の患者では、正常な睡眠者よりもOAレベルが有意に高いことがわかった。さらに、OAレベルは不眠症の経過や重症度と正の関係を持つことが検出された(Tang et al., 2017)。
オレキシン/OXR系は覚醒を促進するため、オレキシン受容体を遮断するアンタゴニストは睡眠を促進し、覚醒を抑制することになる。このことは、不眠症の治療法として重要かつ効果的な選択肢を提供するに違いない。いくつかのオレキシン受容体拮抗薬は、ラット、イヌ、ヒトの不眠症の治療のために設計され研究されている(Brisbare-Roch et al.
SORAの一つであるSB-334867は、OX1Rに選択的に拮抗するように設計された最初の薬剤である(Smart et al., 2001)。ラットにおけるレム睡眠の抑制を打ち消す可能性があるが、覚醒度の低下や睡眠時間の増加は期待できない(Smith et al., 2003)。EMPA、TCS-OX2-29、JNJ-10397049などのOX2Rアンタゴニストは、OX1Rアンタゴニストよりも覚醒度を低下させる効果があるとされている。
現在、広く議論されているDORAは、SB-649868、almorexant、suvorexantである。前臨床試験において、SB-649868の投与は、ラットのOAによって誘発されるグルーミング活動を減弱させた。さらに、SB-649868(3-30mg/kg)は、ノンレム睡眠およびレム睡眠の潜時を有意に減少させ、持続時間を増加させた(Di Fabio et al., 2011)。さらに、第I相ポリソムノグラフィーのデータから、SB-649868は持続睡眠までの時間を有意に短縮し、総睡眠時間を明らかに改善することが示された(Bettica et al., 2012)。Almorexantは、用量依存的にレム睡眠とノンレム睡眠を増加させ、マウスとラットのOAによって誘発される運動量を減少させることが証明されている(Mang et al., 2012)。Suvorexantは、ラット、イヌ、アカゲザルにおいて、覚醒を有意に減少させ、レム睡眠とノンレム睡眠を用量依存的に増加させた(Whitman et al., 2009; Winrow et al., 2011)。また、suvorexantのクロスオーバー試験では、不眠症患者の睡眠効率を有意に改善することが示された(Herring et al.,2012)。suvorexantの第II相および第III相試験における有効性と忍容性から、2014年のFDAはsuvorexantを不眠症治療のためのファーストインクラスDORAとして承認した(Winrow and Renger,2014)。
実際、不眠症の治療は、不眠症が多因子性病因であるため、通常、複雑で臨床的に困難である。オレキシン受容体拮抗薬が効果的な代替薬として設計され、利用できるようになれば、不眠症の治療において重要な進展となる。しかし、睡眠の質と量に対する拮抗薬の有効性は十分に理解されていない。
オレキシン/レセプターのシグナル伝達と抑うつ状態
うつ病は、世界中でその発症率が増加している精神疾患である。うつ病の特徴として、気分の低下、悲惨さ、無気力、自尊心の低下、無感動、意欲の低下、食欲不振、睡眠障害、思考と行動の遅れ(Mathers and Loncar,2006; Ionescu and Papakostas,2017)、結果的にこの病気は人間の身体と精神の健康を著しく危険にさらす。オレキシン含有ニューロンは、感情活動の重要な調節因子であるドーパミン作動性腹側被蓋核や黒質に神経線維を投射しており、オレキシン/受容体系がうつ病の病態生理に関与していることが示唆される。
オレキシン/レセプター系の調節障害は、うつ病患者やその動物モデルで報告されている。2003年、Ronald M. Salomonは、うつ病患者の髄液中のOA濃度を測定し(Salomon et al.,2003)、患者におけるOA濃度がコントロールよりも高いことを示した。また、抗うつ剤Sertralineを5週間投与するとOA濃度が低下する傾向があり、うつ病とOAとの相関が確認された。Fengら(2008)は、うつ病モデルラットにおいて、若年層ではオレキシンレベルが有意に低下していたが、成熟したラットでは有意にオレキシンレベルが高く、アミネルグニューロンの欠陥による抑制が原因であると考えられると報告した。うつ病のラットモデルにおいて、オレキシンニューロンの数とサイズの減少は、うつ病症状と関連している(Allard et al.,2004)。これと一致して、OA mRNAは、うつ病患者の末梢血細胞において、入院後1日目、14日目、28日目に検出される(Rotter et al., 2011)。これらの結果は、OA mRNAレベルがうつ病の重症度と負の相関があることを示している。さらに、Itoら(2008)は、抗うつ作用の行動学的スクリーニングとして知られている強制水泳試験に対するOAをi.c.v.投与した場合の効果をマウスで検討した。その結果、歯状回における細胞増殖の促進により、少なくとも部分的に抗うつ様作用を示すことが示唆された(Ito et al., 2008)。
しかし、様々なうつ病の動物モデルで行われた実験では、以下に述べるような矛盾した結果が得られている。LHのオレキシン含有ニューロンの存在量は、年齢をマッチさせたコントロールと比較して、高いストレスと長時間の外的ストレスを受けたうつ病マウスで約20%増加する(Jalewa et al., 2014)。また、オレキシン含有ニューロンは、ネズミのうつ病モデルでも活性化され、その増加は抗うつ薬であるfluoxetineによって逆転する(Nollet et al., 2011)。うつ病マウスにおけるオレキシンの発現は、脳領域によって異なる(Arendt et al., 2013)。海馬では、オレキシンの低発現が抑うつ行動と負の相関を示すのに対し、扁桃体では、オレキシンおよびOX1RmRNAの高発現が抑うつ行動と正の相関を示す。これらの結果は、オレキシン/受容体経路が脳領域によって異なる役割を担っていることをさらに裏付けるものである。
OX2Rは抗うつ作用があり、OX1Rは親うつ作用がある。季節性情動障害(SAD)モデルラットにOX1Rの選択的アンタゴニストであるSB334867を投与すると、甘味溶液嗜好性の低下と強制水泳試験における不動性の増加を特徴とする抑うつ行動を示す(Deats et al.,2014).一方、SB334867を投与したOX1Rノックアウトマウスと正常マウスの両方が、行動的絶望感の同様の減少を示すのに対し、OX2Rノックアウトマウスは行動的絶望感の増加を示している。著者らは、オレキシン/受容体システムが、OX1RとOX2Rのどちらが活性化されるかによって、抗うつ作用またはプロうつ作用を誘導すると推察した(Scott et al.)OX1Rの発現は、うつ病モデルマウスとコントロールマウスの間でほとんど差がない。一方、うつ病マウスでは、視床下部、腹側視床、海馬でOX2Rのレベルが低下している(Nollet et al.,2011)。
私たちの研究室では、ラットの初代海馬ニューロンでOX1RとKORが共発現していることを確認している。注目すべきは、マウスうつ病モデルの海馬と視床下部において、OX1RとKORの両方がコントロールマウスよりも低いレベルで発現していることである(図(Figure6).6)。しかし、KORの発現量のわずかな減少に比べ、うつ病モデルではOX1Rの発現量のはるかに大きな減少が確認された。これらの結果は、OX1RとKORの調節異常がうつ病の発症を促進するという見解(Chen et al.,2015)と一致し、うつ病が脳組織におけるOX1RとKORのバランスを崩す可能性を示唆した。また、ダイノルフィンは視床下部においてオレキシンと高度に共局在している。うつ病の動物モデルでは、ダイノルフィン量が上昇する一方で、オレキシン量が減少し、快楽を欠く症状が現れる。ダイノルフィンとオレキシンは、脳内報酬系の制御において相互に拮抗する役割を果たし、うつ病の生理的・病理的プロセスの調節に共同で関与している(Miczek et al., 2011)。

図6 オレキシンとうつ病の関係の可能性
低濃度のオレキシンは5-HTニューロンを直接興奮させる作用があり、高濃度のオレキシンは5-HTニューロンを間接的に抑制する。
その結果、オレキシンはK+リーク電流やNa+依存性NSCCを活性化することにより、セロトニン(5-HT)ニューロンを直接興奮させることがわかった(Brown et al., 2001)。また、意外なことに、高濃度では、オレキシンはGABA作動性介在ニューロンの興奮によって間接的に5-HTニューロンを抑制する(Liu et al., 2002)。今回の研究から、うつ病の発症過程において、両者の間に一定の関係があるのではないかと推測される。
これらのことから、うつ病の病態を制御する上で、オレキシン/受容体システムが重要な役割を担っていることが明らかになった。これらの知見は、オレキシン/受容体システムの機能についての理解を深めるだけでなく、うつ病の分子メカニズムに新たな知見を与えるものである。
オレキシン/レセプターシグナルと虚血性脳卒中
虚血性脳卒中は、世界中で高い死亡率と障害率を示す神経系疾患であり、虚血と無酸素状態により脳組織のアポトーシスと壊死が生じる(Kang et al., 2003)。虚血性脳卒中の病態生理は、興奮性アミノ酸毒性、エネルギー生成障害、酸化ストレス傷害、炎症反応などが関与し、かなり複雑である(Abas et al., 2010)。
オレキシン、特にOAが脳虚血障害や虚血再灌流障害(IRI)において神経保護作用を示すことが多くの研究により明らかにされている。脳梗塞患者では、脳脊髄液の濃度が持続的に低下する(Nishino and Kanbayashi,2005).また、くも膜下出血では、発症後10日間,髄液のOA濃度が低下する。SAH患者における症候性血管攣縮に起因する遅発性虚血性神経細胞欠損(DIND)の合併症に関しては、DINDを発症しない患者の方がCSF OA値は高い(Doi et al.,2005)。これらの結果と一致して、OAを含む神経細胞の数は、虚血側で非虚血側より明らかに多い(Kitamura et al., 2010)。さらに、OAを投与すると、脳梗塞面積が有意に減少する。
OX1Rが脳虚血傷害と関連していることを示唆する研究がいくつかあった。ラットおよびマウスの脳虚血モデルにおいて、OX1Rは神経細胞のみならず、アストロサイトやオリゴデンドロサイトにも高度に誘導され、OAとOX1Rが虚血障害に重要な役割を果たすことが示唆された(Nakamachi et al.,2005).また、脳虚血モデル動物では、脳でOX1Rの発現が増加し、脳脊髄液中のOA濃度の低下と関連することが示されている。特に、Irvingら(2002)は、中大脳動脈永久閉塞(MCAO)後のラット虚血皮質において、OX1RのmRNAおよびタンパク質レベルが上昇し、OX2Rは上昇しないことを報告した。その結果,CSFのOA値は虚血24時間後に一過性に上昇し、虚血2日目,4日目には徐々に低下し、7日目にはベースラインに戻っていた。これらの変化は、虚血後1日目と2日目のCA1におけるOX1Rの発現量の上昇と相関していた。これらの変化は、一過性の虚血に伴う神経細胞障害において、オレキシンとOX1Rの動態が機能的に関与している可能性を示唆している(Dohi et al.,2006)。
OAを脳室内注射すると、虚血後3日目のマウスのMCAOによる神経損傷が抑制された(Harada et al.)また、別の報告では、脳梗塞を発症した被験者において、OAが神経障害を有意に改善し、梗塞領域の面積を減少させた。OAによる神経保護作用のメカニズムは、アポトーシス細胞数の減少やHIF-1αの活性化が関係していると考えられる。さらに、HIF-1α阻害剤を投与すると、脳梗塞に関連したHIF-1αの増加が抑制され、OAによる神経保護効果が逆転する(Yuan et al.,2011)。
ラット大脳皮質において、オレキシンは濃度依存的に神経細胞の生存率を著しく上昇させる。このオレキシンの生存促進能は、カスパーゼ3活性の低下と関連している(Sokoowska et al., 2012)。Haradaら(2013)は、OAが脳由来向神経性因子(BDNF)の発現を促進することにより、脳虚血性神経細胞障害を予防することを明らかにした。オレキシン/アタキシン-3トランスジェニックマウスを用いたMCAOモデルにおいて、OA投与はmRNAレベルでTNF-αとIL-6の発現を明らかに変化させ、このプロセスに慢性炎症反応が関与していることを示唆した(Xiong et al.,2013)。
これらのことから、オレキシン/受容体システムは、抗アポトーシス反応と炎症反応を制御することにより、脳虚血や脳梗塞から神経細胞を保護することがわかった。オレキシン/レセプターによる神経保護作用のシグナル伝達経路をより深く理解することで、脳虚血や脳梗塞に対する新たな治療法の設計が可能になると考えられる。
オレキシン/受容体シグナルと依存症
薬物依存症は、他の活動を犠牲にして薬物を求める強迫的な行動によって区別される慢性的かつ再発性の障害である。1954年、OldsとMilnerは、報酬系においてLHが重要な脳領域であることを明らかにした(Olds and Milner,1954)。Velley ら(1983)は、LHの固有ニューロンが自己刺激に関与しているかという長年の疑問に答えた。オレキシン/受容体系、特にOX1Rを介するものが、薬物、特にアルコール、ニコチン、コカインの依存症に強く関係していることが報告された(Smith et al.,2009; Dehkordi et al.,2017; Moorman et al.)OX2Rは一般的に覚醒や睡眠調節と密接な関係があるとされているが(Willie et al.,2003)、オレキシン/OX2Rシグナルは、いくつかの報告で薬物探索行動の重要なメディエーターであることも報告されている(Smith et al.,2009; Cason et al.,2010; Shoblock et al.,2011)。
オレキシン/レセプターシグナルとエタノールシーキング
蓄積された報告により、いくつかのアルコール摂取モデルにおいて、オレキシンおよびその受容体が異常に発現していることが明らかになった。例えば、高用量のエタノールはLHのオレキシン濃度を上昇させる(Morganstern et al., 2010)。視床下部のオレキシン含有ニューロンは、動物がエタノールの利用可能性にさらされると、著しく多くなる(Dayas et al., 2008)。OAを室傍核(PVN)およびLHに投与すると、エタノール飲用ラットのエタノール摂取が誘導される(Schneider et al., 2007)。これらの観察結果に従い、OX1RアンタゴニストSB334867の腹腔内投与は、高エタノール嗜好性ラットのエタノール摂取と嗜好性を低下させる(Moorman and Aston-Jones,2009)。さらに、様々な濃度のSB334867(10,15,20mg/kg)は、10%エタノールのオペラント自己投与を減少させる(Richards et al., 2008)。別の実験では、SB334867がエタノールに対する反応点とブレークポイントも有意に減少させることが証明された(Jupp et al., 2011)。
さらに、自発的なエタノール飲用と胃内投与エタノールの両方がaPVTのOBの遺伝子発現を増加させることから、エタノール摂取の調節にOBが重要な役割を果たすことが示唆された(Barson et al.,2015)。さらに、OX2RアンタゴニストTCSOX229をaPVTに注入すると、エタノール摂取が有意に減少する可能性がある。さらに、別の選択的OX2RアンタゴニストであるJNJ-10397049の末梢注射は、マウスにおけるエタノール自己投与、エタノール条件付場所選好(CPP)の獲得・発現・復職に関する行動、およびエタノール誘発多動性を減少させる(Shoblock et al.)同様に、TCSOX229を側坐核(NAc)に注射すると、エタノールの自己投与が減少する。しかし、TCSOX229は、手がかりによって誘発されるエタノール探索の再上昇を変化させない。OX1Rとは異なり、OX2Rはおそらく、キュー条件付きエタノール探索よりもエタノール自己投与においてより顕著な役割を果たしている(Brown et al.,2013)。
Andersonら(2014)は、OX1R拮抗薬SB334867、OX2R拮抗薬LSN2424100、およびOX1/2R混合拮抗薬アルモアキサン(ACT-078573)を用いて、エタノール自己投与に対するOX1RおよびOX2Rの影響を評価した。異なるオペラント実験の結果、OX1RとOX2Rは、消費行動に対して非特異的な効果を持つものの、エタノール自己投与を減少させることが示された(Anderson et al., 2014)。Almorexantは、VTAに直接注入するとエタノール自己投与を減少させる(Srinivasanら、2012;図77)。

図7 エタノールシーキングにおけるオレキシン/レセプターの役割を示す模式図。OAまたはOBをPVN、LH、aPVTに投与すると、エタノールシーキングが誘導される。これらの知見に基づき、OX1RまたはOX2Rアンタゴニストを腹腔内投与すると、エタノール摂取およびエタノール自己投与が減少する。略号PVN、室傍核、LH、外側視床下部、aPVT、前部傍室視床、NAc、側坐核、VTA、腹側被蓋野。
オレキシン/レセプターシグナルとニコチンシーキング
オレキシン/レセプターシステムは、ニコチン投与による生理的・行動的反応の調整に関連している。OX1Rは、ニコチン強化のラットモデルにおいて活性化される。さらに、OX1RアンタゴニストとOX2Rアンタゴニストは、ともに用量依存的にニコチン自己投与を減少させる(LeSage et al., 2010)。脳室内OAにより、ニコチン探索により誘発される行動が復活するが、SB334867はニコチン動機付け反応を効果的にブロックする(Plaza-Zabala et al., 2010)。Hollanderら(2008)は、島皮質へのSB334867の低用量投与により、ラットのニコチン摂取量が効果的に減少し、薬物を得るための動機付けも減少することを示した。重要なことは、SB334867は食物に対する反応を変化させることなく、ニコチン摂取量を選択的に減少させることである。さらに、SB334867はニコチン自己投与を減少させる(Hollander et al., 2008)。C57BL/6Jニコチン依存性マウスにおいて、SB334867で前処理したマウスおよびプレプロヒポクレチンノックアウトマウスではニコチン離脱症候群が減少するが、OX2RアンタゴニストTCSOX229で前処理したマウスでは症候群は全く認められなかった(Plaza-Zabala et al., 2012)。
ニコチンはオレキシン分泌ニューロンのFos発現細胞の割合を増加させ、この効果はニコチン拮抗薬によって減少する(Pasumarthi et al., 2006)。OX1RアンタゴニストSB334867の前処理は、OX2RアンタゴニストTCSOX229ではなく、ニコチン探索の復職を減少させた。さらに、PKCシグナルはニコチン探索行動の再発を調節する(Plaza-Zabala et al., 2013)。別の高選択的OX1RアンタゴニストであるGSK1059865は、エタノール依存性マウスにおいて自発的なエタノール摂取を有意に減少させるが、非依存性マウスでは減少しない(Lopez et al.,2016)。
これらのデータを総合すると、ニコチンによって増強されたOA/OX1R伝達は、ニコチンの刺激特性を制御する上で重要な役割を果たすことが示された。したがって、受容体拮抗薬は、ヒト喫煙者におけるニコチン中毒の維持に必要な重要な神経生物学的基質である可能性がある。
オレキシン/レセプターとコカインシーキング
オレキシン/レセプター系はコカイン摂取を刺激することが示された。OAは、用量依存的にコカイン探索の再上昇をもたらし、明らかに自己刺激閾値を増加させることから、脳報酬回路の活性をネガティブに調節することが示された(Boutrel et al., 2005)。腹腔内SB334867は、コカインによって誘発される条件付き復職を用量依存的に逆転させ(Martin-Fardon and Weiss,2014)、OX1Rノックアウトマウスは野生型マウスよりもコカインの自己投与量がはるかに少ない(Hollander et al,2012)。SB334867をOAと共投与してもコカインシーキングをブロックできないが、別のOX2RアンタゴニストであるTCSOX229はOAによって誘導されるコカインシーキングを完全に防止し、OAをpPVTに注入するプライミング効果がOX2Rによって媒介されていることを示している(Matzeu et al.,2016)。SB334867の前処理は、薬物に関連する文脈によって誘発される条件付きコカイン探索を有意に減衰させる(Smith et al.,2010)。同様に、SB334867は、中脳辺縁系DAシステムを調節することにより、おそらくコカイン自己投与を減少させる(Espana et al., 2010)。
SB334867を中心扁桃体(CeA)にマイクロインジェクションすると、モデルラットのコカイン摂取量が用量依存的に減少する。さらに、SB334867は内側CeA内のGABA作動性神経伝達をブロックし、GABA作動性神経伝達がオレキシンを介したコカイン摂取の制御に関与することを示している(Schmeichel et al.,2017)。両側VTAへのSB334867のマイクロインジェクション、またはAMPA受容体拮抗薬CNQXはコカイン探索の復食を減弱させるが、AMPA受容体の陽性モジュレーターであるPEPAはSB334867による減弱を完全に復食させる。このことは、コカイン探索行動の復職がVTAにおけるOX1RとAMPA受容体の相互作用に依存していることを示唆している(Mahler et al., 2013)。Borglandら(2006)は、OAがPLC/PKC依存性シグナル経路の活性化を介してVTA DAニューロンのNMDAR EPSCを増強することを報告した。OX1Rアンタゴニストは、コカインに対する感作をブロックし、コカインによって誘発される興奮性電流の増強を封じる。このように、VTAにおけるオレキシン/OX1Rシグナルは、コカインに対する行動感作に重要である(Borgland et al.,2006)。オレキシンプレプロペプチドのノックアウトマウスでは、コカインに対するCPPが発現せず、DAの放出と取り込みが減少している。さらに、ノックアウトマウスにおけるDAシグナルの低下は、コカイン投与後も持続することから、オレキシンを介した強化の制御がDA神経伝達と関連している可能性が示唆された(Shaw et al., 2017)。SB334867は、コカインを自己投与する動機を低下させ、コカインによるDAシグナル伝達の増強を減衰させる。オレキシンのノックアウトがコカインに対するDA反応を減少させるという観察結果と合わせて、これらの知見は、オレキシン/OX1Rが、おそらく中脳辺縁系DAシステムを介してコカイン強化を調節することを示唆している(Espana et al., 2010)。
OX1Rの遮断、あるいはOX1RとOX2Rの同時遮断は、コカインのDAシグナルへの影響とコカイン摂取の動機付けを減少させる。一方、OX2Rの単独遮断では、DAシグナル伝達や自己投与に大きな影響を及ぼさない。これらの知見は、DAシグナル伝達とコカイン自己投与の調節において、OX1RがOX2Rよりも重要な役割を果たすという、2つの受容体の差異のある関与を示唆している(Prince et al.,2015)。しかし、コカイン刺激を繰り返すと、NAcにおいてOX2Rタンパク質の発現が増加し、この領域のOX1R、OA、OBには影響がないことがある。NAと比較して、前頭皮質、海馬、VTA、背側線条体では、OX2Rはコカインによって変化しない。驚くべきことに、OX2Rのアップレギュレーションは、コカイン中止後60日まで持続する(Zhang et al.,2007)。
これらの結果から、コカイン自己投与にはオレキシン/OX1Rが必要であり、オレキシン/OX2Rはあまり重要ではないことが示唆された。今後、コカイン探索の制御におけるオレキシン/受容体システムの役割に関する研究が進めば、拮抗薬を用いたコカイン探索に対する介入法の開発が容易になると考えられる。
オレキシン/レセプターシグナルとアルツハイマー病
ADは、進行性の認知機能障害と行動障害を特徴とする中枢神経系の変性疾患である。ADの病態は、細胞外のβアミロイドの沈着により神経細胞が変性し、タウ蛋白の高リン酸化により神経原線維のもつれが形成され、神経細胞とシナプスの正常な機能が損なわれることに要約される。ADはオレキシンを含む神経細胞の消失やオレキシン神経伝達のある程度の障害と関連していることを報告する文献もあり、オレキシン/レセプターシステムがAD発症に重要な役割を果たしていることが示唆されている。ある研究では、AD患者においてOAニューロンの数は40%減少し、CSF中のOA濃度は14%低下していた(Fronczek et al.)逆に、AD患者ではCSFのオレキシン濃度が上昇することが報告されている(Liguori et al., 2016、2017)。さらに、ADにおけるCSF OAのアップレギュレーションは、アミロイドβ42レベルと相関している(Gabelle et al., 2017)。これらの矛盾した結論は、オレキシン/OXR系とADの関係が複雑であることを示している。ADにおけるオレキシン/OXR系について、より広範で深い研究が必要である。
アミロイド前駆体タンパク質(APP)/プレセニリン1(PS1)トランスジェニックマウスにおいて、オレキシン遺伝子をノックアウトすると、Aβ病理の程度が著しく減少する。逆に、APP/PS1におけるオレキシン作動性ニューロンのレスキューはAβ病理量を増加させることから、オレキシンが脳内のAβ病理を調節していることがわかる(Roh et al., 2014)。Urrestarazu and Iriarte(2016)は、AD患者はオレキシンの分泌に何らかの障害があり、それが睡眠障害をもたらし、その後アミロイドβレベルが上昇し、最終的にADの病態に寄与していると推測している。
OA/B処理は、Aβフィブリル周囲のアクチンフィラメントの形成に影響を与え、PI3K、Akt、p38-MAPKなどの貪食制御分子をダウンレギュレートし、オレキシンが貪食およびオートファジックフラックスの抑制を通じてAβ分解を損なうことが実証されている(An et al.,2017)。さらに、ADではAβプラーク形成やタウの過リン酸化により、OXRやGPR103の発現が低下していることが分かっている。さらに、試験管内試験のADモデルでは、OXRsとGPR103が機能的なヘテロダイマーを形成し、ERK1/2シグナル経路を活性化することで神経保護作用を発揮する。
オレキシンの過剰発現がAβの蓄積とタウを介した神経変性を引き起こすことを考慮すると、オレキシン受容体拮抗薬はADに対する予防・治療戦略の可能性を示している。しかし、ADの病態生理におけるオレキシン/OXRシステムの役割とメカニズムを明らかにするためには、さらなる研究が必要である。
結論と展望
オレキシン含有ニューロンの広範な投射、他のタイプのニューロンとの複雑な回路、オレキシン受容体の拡散分布を介して、オレキシン/受容体システムは、複数の中枢神経系機能の調節に関与している。
オレキシン含有ニューロンが損傷したり失われたりすると、オレキシン含有ニューロンと関連するニューロンとの間にアンバランスが生じる。これらの神経伝達系がいったん壊れたり、混乱したりすると、神経疾患の症状が現れる。
現在、オレキシン/受容体系に関連する神経疾患に対する有効な戦略は、オレキシン含有ニューロンの活動を選択的に促進すること、あるいは代わりに、受容体拮抗薬を用いてオレキシン受容体の機能を遮断することである。特に、オレキシン受容体を標的とした薬理学的介入は、神経疾患に対する有効な対策であることが示されている。
しかし、神経疾患におけるオレキシン/受容体システムの生理的役割を決定的にするためには、薬理学的および分子生物学的な詳細な研究が必要である。オレキシン受容体に関する理解が深まり、近い将来、この知見が神経疾患の臨床治療に応用されることは間違いないだろう。
利益相反に関する声明
本研究は、潜在的な利益相反と解釈されうる商業的または金銭的関係がない状態で実施されたことを宣言するものである。
フットノーツ
資金提供本研究は、中国国家自然科学基金(81501018 to CW and 816712276 to BC)、山東省自然科学基金(ZR2013CQ31 to CW)、Jining Medical University Supporting Fund for Teachers’ research(JY2017KJ036 to QQ and JY2017KJ034 to YP)からの助成により快く支援された。