コンテンツ
Repurposed agents in the Alzheimer’s disease drug development pipeline
オンラインで公開2020年8月17日
要旨
背景
アルツハイマー病の蔓延に対処するための治療法が必要とされている。2003年以降、臨床試験では、食品医薬品局(FDA)の承認を得るためのアルツハイマー病治療薬が開発されておらず、医薬品開発プロセスは時間とコストのかかるものとなっている。医薬品の再利用は、他の適応症で承認された薬剤のアルツハイマー病関連効果を調べることで、このプロセスを加速させる機会を提供している。これらの薬剤は、安全性プロファイル、薬物動態特性、剤形、用量、製造プロセスが既知である。
試験方法
2020年2月27日時点でClinicalTrials.govに登録されている現行のアルツハイマー病パイプラインの第I相、第II相、第III相に代表される再利用型アルツハイマー病治療薬を評価した。
結果
我々は、58のFDA承認薬を含む53の臨床試験を同定した。試験に参加した薬剤の78%は、疾患修飾作用を有すると考えられる作用機序を有していた。開発中の再利用薬のうち、20%が血液腫瘍学的製剤、18%が心血管系の適応症に由来する薬剤、14%が精神医学的用途の薬剤、12%が糖尿病治療に使用される薬剤、10%が神経学的製剤、残りの26%がその他の条件に該当する薬剤である。これらのプログラムで利用された知的財産戦略には、同じ薬剤を使用しながら、用量、投与経路、または製剤を変更することが含まれている。リパーポージング試験のほとんどは、学術医療センターの支援を受けており、バイオ製薬業界からの資金提供は受けていない。我々の結果を欧州の試験登録と比較したところ、ClinicalTrials.govから得られた結果と同様の結果が得られた。
結論
薬物の再利用は、アルツハイマー病治療薬開発の一般的なアプローチであり、現在のアルツハイマー病治療薬パイプラインにおける試験の39%を占めている。多くの疾患領域からの治療薬は、アルツハイマー病治療に有用な薬剤を提供している。リパーパスされた薬剤のほとんどはジェネリック医薬品であり、その経済的価値を高めるために様々な知的財産戦略が採用されている。
キーワード アルツハイマー病、臨床試験、リパーポージング、用量、剤形、疾患修飾
背景
アルツハイマー病は、世界的な高齢化の進展により有病率が上昇している進行性の神経変性疾患である[1]。2050年までに85人に1人がアルツハイマー病と診断されて生活すると推定されている[2]。この無力化し、最終的には致命的な疾患と闘うための効果的な治療法を特定することが急務となっている。アルツハイマー病のための新しい治療法を見つける試みは、学術センターやバイオ製薬会社によって行われていた:新しい化学物質の同定、ヒトへの使用のための最適化、臨床試験でのその効果の調査。しかし 2003年以降、食品医薬品局(FDA)によってアルツハイマー病治療薬が承認されていないことは、この目的の複雑さを示している[3]。
アルツハイマー病の新しい治療法を生み出す努力は、主に症状を改善し、病気の進行を遅らせ、発症を遅らせ、あるいは最終的に病気を予防する可能性のある新しい化合物を特定することに焦点を当てている。新しい治療法を進めるための別のアプローチは、オンターゲットまたはオフターゲットのメカニズムを通じてアルツハイマー病の生物学に影響を与える可能性のある、アルツハイマー病に関連していない適応症で承認された薬剤の開発である。この再利用戦略は他の疾患で成功しており、多くのFDA承認薬が試験管内試験、動物実験、疫学的研究、観察研究を通して明らかなアルツハイマー病関連効果を示しているため、アルツハイマー病治療に有望であると考えられている[4-9]。
アルツハイマー病 治療薬開発プロセスにおける再利用をよりよく理解するために、FDA 承認薬を含む進行中のすべての アルツハイマー病 臨床試験の分析を行った。我々は、米国内で実施されたすべての臨床試験の登録が義務付けられている包括的な米国政府のデータベースであるClinicalTrials.govに報告された試験データを分析した。我々は、再利用薬を含む現在進行中のすべての臨床試験を調査し、アルツハイマー病のパイプラインにあるすべての薬剤と比較した [10-14]。また、欧州連合臨床試験登録簿(EUCTR)に報告されている、再利用されたアルツハイマー病治療薬の進行中の試験活動も比較した。私たちの目的は、アルツハイマー病治療薬パイプラインにおけるリパーポージングの取り組みが、米国(米国)および国際的なパイプラインにおける全体的な薬剤開発活動とどのように比較されるかを検証し、薬剤開発戦略としてのリパーポージングについての洞察を提供することであった。
試験方法
本研究は、ClinicalTrials.govに報告された臨床試験の活動に基づいている。米国の法律では、米国内で実施されるすべての臨床試験は、最初の参加者の登録から 21日以内に登録しなければならない[15, 16]。ClinicalTrials.govは、米国内で実施された臨床試験の研究のための包括的で有効なデータソースである。米国外で実施された第1相臨床試験は登録されていないことが多く、我々の調査結果は世界的な第1相臨床試験を実施している薬剤を過小評価している可能性がある。
我々は、関心のあるデータを含む、以前に構築された試験データベース[10-14]を使用し、現在フェーズI、II、IIIで再利用された薬剤を試験しているすべての試験について報告した。ここで報告する結果は 2020年2月27日時点でClinicalTrials.govに登録されている試験に基づいている。ClinicalTrials.govのラベルを使用し、募集中の試験、活動中だが募集していない試験、招待制で登録中の試験、まだ募集していない試験を対象とした。幹細胞治療の臨床試験は対象としていない。
我々は、再利用された薬剤に焦点を当てており、FDAの承認を受けた適応症を持つ薬剤を重視している。Drugs@FDA(fda.gov/drugsatfda)は、1939年以降に承認された医薬品を収録した米国政府のデータベースで、毎日更新されている [17]。各薬剤の承認された用途は、Drugs@FDAが提供する最新のラベルによって決定した。薬物によっては、FDAが承認した適応症が1つ以上あるものもあり、その旨を記載している。
薬剤は、その承認された適応症によって決定された各薬剤が処方されている治療領域に基づいて、さらに分類された。この分類をもとに、すべてのアルツハイマー病試験を横断して研究されている薬剤の治療領域由来を調べた。中には複数の試験が進行中の薬剤もあるので、これらを「ユニーク」な薬剤と定義した。また、2つ以上の試験で見られる特定の化合物の多様性(用量、投与経路など)にも注目した。
いくつかの試験では、別々の治療群(例:テルミサルタン vs ペリンドプリル)または併用(例:ロサルタン、アムロジピン、アトルバスタチンの単剤投与)で複数の再利用薬を検討している。本研究では、前者を別個の治療薬として扱い、後者は単剤治療としての固定併用の効果を検討することを目的としているため、その臨床試験に関しては単剤とした。
アルツハイマー病における薬物の作用機序(MOA)は、ClinicalTrials.govに掲載されている情報、または特定の薬物に関する文献の包括的なレビューから決定した。我々は、作用機序を疾患修飾療法(DMT)と対症療法に分類した。後者はさらに、認知改善薬と神経精神症状や行動症状に対処する薬に分けた。我々は、介入の目的が基礎となる疾患の生物学的変化を修正し、疾患の発症を遅らせたり、進行を遅らせたりすることを目的としている場合には、薬剤をDMTと同定した。DMTは、アミロイド関連の標的、タウ関連のメカニズムを標的とするものと、「その他」のメカニズム(すなわち、神経保護、抗炎症、代謝作用)を有するものに分けられた。症候性薬剤とDMTの区別は任意であり、いくつかの薬剤は両方の特性を有することがある。本研究の目的のために、我々は主要なMOAと思われるものを選択した。
我々は 2016年以降に開始された過去のアルツハイマー病パイプラインレビューからの過去のデータと、現在のリポージング試験のデータをレトロスペクティブに比較した [10-14]。我々は、上記で詳述したように臨床試験の包含を確認するために同一の方法論を用いた。
本研究では、EUCTRに報告されている試験情報を用いて、米国と欧州のアルツハイマー病パイプライン間の並行した活動を分析している。この公開登録は、欧州連合(EU)または欧州経済領域(EEA)で実施された試験のプロトコルと結果を含む欧州連合医薬品規制当局臨床試験(EudraCT)データベースからのデータへのアクセスを可能にしている。EUCTRを用いて 2020年2月27日時点で進行中の第I相、第II相、第III相アルツハイマー病試験を検索した。EU/EEAに限定した臨床試験と、米国で並行して実施されているオーバーラップ試験を区別している。
試験結果
概要
ClinicalTrials.govに報告されている53の臨床試験には、合計58剤の再利用薬がある。第III相臨床試験12試験で15剤、第II相臨床試験32試験で33剤、第I相臨床試験9試験で10剤が確認されたが、これらの試験のうち、6剤が第II/III相臨床試験、2剤が第I/II相臨床試験でした。いくつかの試験では複数の薬剤が使用されており、複数の試験にまたがって試験が行われている薬剤もある。
FDAが承認しているすべての再利用薬のパイプラインの適応を分析すると、20%が血液腫瘍薬、18%が循環器薬、14%が精神科薬、12%が糖尿病治療薬、10%がその他の神経疾患治療薬、残りの26%がその他の治療領域に由来する薬であることが示された。第III相試験で再利用された精神科治療薬は、アルツハイマー病の神経精神症状の治療のために評価されている全薬剤の50%を占めている。試験中の循環器系薬剤の半数が第Ⅲ相試験に入っている。パイプラインの血液腫瘍薬、抗糖尿病薬、神経学的薬の大部分は第II相試験中である(それぞれ70%、67%、67%)。フェーズIIでは、フェーズIとフェーズIIIを合わせた数よりも多くのリパーゼントが実施されている。図1は、FDA承認の適応症別に、それぞれの臨床フェーズ内での全リパーゼ薬の分類を示したものである。
図1 FDA承認済みの適応症別の再利用薬の分類(ClinicalTrials.gov 2020年2月27日現在)
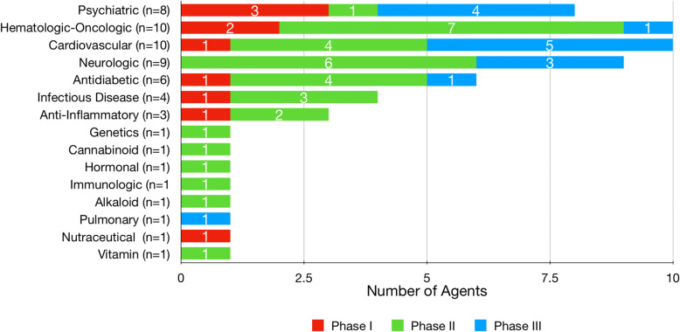
全剤のアルツハイマー病関連MOAを見てみると、78%がDMTとして開発されており、16%が神経・行動の変化に対応する対症療法剤、7%が認知機能強化剤であることがわかる(表1)。エシタロプラムは、第I相試験で認知機能改善剤として、第III相試験で神経精神科領域の薬剤として、それぞれ個別に開発が進められている。DMT試験の中では、血液腫瘍、心血管、抗糖尿病を主な適応症とするものが26%、18%、16%となっている。対照的に、対症療法薬は、ほとんどが精神疾患を対象とした治療薬に由来している(50%)。図2は、再利用された薬剤のアルツハイマー病関連MOAを示している。
表1 アルツハイマー病に関連した作用機序の再利用薬のパイプライン(ClinicalTrials.gov 2020年2月27日現在
| 承認された治療領域 | 疾患修飾療法 | 向知性薬 | 行動症状 | 行動+認知症状 | エージェントの総数(%) |
|---|---|---|---|---|---|
| 血液腫瘍学 | 10 | – | – | – | 10(20.0) |
| 心臓血管 | 7 | 1 | 1 | – | 9(18.0) |
| 精神的 | 1 | 1 | 4 | 1 | 7(14.0) |
| 抗糖尿病薬 | 6 | – | – | – | 6(12.0) |
| 神経学 | 3 | – | 2 | – | 5(10.0) |
| 感染症 | 3 | – | – | – | 3(6.0) |
| 抗炎症薬 | 2 | – | – | – | 2(4.0) |
| 遺伝学 | 1 | – | – | – | 1(2.0) |
| カンナビノイド | – | – | 1 | – | 1(2.0) |
| ホルモン | 1 | – | – | – | 1(2.0) |
| 免疫学 | 1 | – | – | – | 1(2.0) |
| アルカロイド | – | 1 | – | – | 1(2.0) |
| 肺 | 1 | – | – | – | 1(2.0) |
| 栄養補助食品 | 1 | – | – | – | 1(2.0) |
| ビタミン | 1 | – | – | – | 1(2.0) |
| 合計 | 38 | 3 | 8 | 1 | 50(100.0) |
図2 作用機序別に現在研究中の再利用薬の割合(ClinicalTrials.gov 2020年2月27日現在
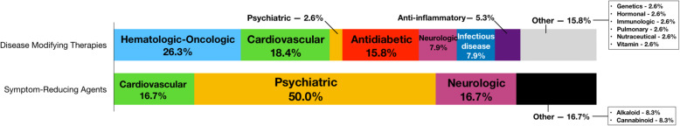
ユニークな再利用エージェント
アルツハイマー病の全パイプライン試験の中で研究中の50種類のユニークな再利用薬(全58種類のパイプラインの中から少なくとも一度は代表される薬と定義される)がある。20%が血液腫瘍薬、18%が心血管薬、14%が精神科薬、12%が抗糖尿病薬、10%が神経科薬であり、残りの26%の治療薬は他のカテゴリーで使用されていた。図3は、現在のアルツハイマー病パイプラインに代表されるすべてのユニークな再利用された薬剤の分類をグラフィカルにまとめたものである。
図3 現在検討中のリパーゼント剤の治療領域の分類(2020年2月27日現在のClinicalTrials.gov)

すべての試験の中で最も代表的な薬剤はレベチラセタムである(第II相試験4件、第III相試験1件)。テルミサルタン、モンテルカスト、エスシタロプラム、バラシクロビルは、それぞれ複数の第II相および第III相試験を実施している。また、レベチラセタムの適正な低用量製剤(AGB101,投与量1/15)については、第Ⅱ相試験および第Ⅲ相試験で検討中である。
第Ⅲ相試験
第III相試験では、12の試験で15の再利用薬がある(表2);これはアルツハイマー病パイプラインの全第III相試験の3分の1に相当する[14]。これらには8つのDMT剤、1つの認知増強剤、および6つの行動症状を扱う薬剤が含まれている。DMT剤の中では、1剤がアミロイド関連の標的を有し、5剤が抗炎症性MOAを有し、4剤が代謝性と考えられ、2剤が神経保護剤であった。
表2 現在、アルツハイマー病開発パイプラインの第III相で再利用されている薬剤(2020年2月27日現在)
| エージェント名 | 段階 | エージェントメカニズムクラス | 研究中の治療目的 | ドラッグクラス | FDA承認の適応症 | 治療分野 | ClinicalTrials.gov ID(EudraCT ID) |
|---|---|---|---|---|---|---|---|
| ALZT-OP1a、ALZT-OP1b(イブプロフェンの有無にかかわらずクロモリン) | III | 抗アミロイド、抗炎症 | ニューロンの損傷を減らします。肥満細胞はアミロイド病理学(DMT)でも役割を果たす可能性があります | マスト細胞安定剤 | 気管支ぜんそく; 肥満細胞症 | 肺 | NCT02547818(2015-002147-34) |
| アムロジピン | II / III | 抗炎症、代謝 | 認知機能(DMT)を維持するための血管リスクの低減 | カルシウムチャネル遮断薬 | 高血圧; 冠動脈疾患 | 心臓血管 | NCT02913664 |
| アトルバスタチン | II / III | 抗炎症、代謝 | 認知機能(DMT)を維持するための血管リスクの低減 | スタチン | 心筋梗塞、血行再建術、狭心症の補助療法 | 心臓血管 | NCT02913664 |
| AXS-05(DM +ブプロピオン) | II / III | 神経伝達物質ベース | 神経精神症状を改善する(興奮) | ノルエピネフリン-ドーパミン再取り込み阻害薬 | 大鬱病性障害; 季節性情動障害; 禁煙 | 精神的 | NCT03226522 |
| エスシタロプラム | III | 神経伝達物質ベース | 神経精神症状を改善する(興奮) | 選択的セロトニン再取り込み阻害薬 | 大鬱病性障害; 全般性不安障害 | 精神的 | NCT03108846 |
| グアンファシン | III | 神経伝達物質ベース | ノルアドレナリン作動性欠損の調節(認知増強剤) | アルファ受容体アゴニスト | 注意欠陥多動性障害 | 心臓血管 | NCT03116126 |
| イコサペントエチル | II / III | 神経保護 | ニューロンを疾患病理学(DMT)から保護する | 精製されたw-3脂肪酸(エイコサペンタエン酸) | 高トリグリセリド血症 | 心臓血管 | NCT02719327 |
| レベチラセタム(AGB101) | III | 神経保護 | アミロイド誘発性神経活動亢進(DMT)を減少させる | 抗けいれん薬 | 部分てんかん発作の補助療法; 若年ミオクロニンてんかん; 一次全身性強直間代発作 | 神経学 | NCT03486938 |
| ロサルタン | II / III | 抗炎症、代謝 | 認知機能(DMT)を維持するための血管リスクの低減 | アンジオテンシンII受容体遮断薬 | 高血圧; 糖尿病性ニューロパチー; 脳卒中のリスク低減 | 心臓血管 | NCT02913664 |
| マシチニブ | III | 抗炎症薬 | マスト細胞の活動、炎症過程の調節(DMT) | 選択的チロシンキナーゼ阻害剤 | 肥満細胞腫(獣医) | 血液腫瘍学 | NCT01872598(2010-021218-50) |
| メトホルミン | II / III | 代謝 | インスリン感受性を改善し、認知(DMT)を改善する可能性があります | インスリン感作物質(ビグアニド) | 2型糖尿病 | 抗糖尿病薬 | NCT04098666 |
| メチルフェニデート | III | 神経伝達物質ベース | 神経精神症状(無関心)を改善する | 刺激 | 注意欠陥多動性障害 | 精神的 | NCT02346201 |
| ミルタザピン | III | 神経伝達物質ベース | 神経精神症状を改善する(興奮) | 四環系抗うつ薬 | 大鬱病性障害 | 精神的 | NCT03031184 |
| ゾルピデム | III | 神経伝達物質ベース | 神経精神症状(睡眠障害)を改善する | 鎮静剤-催眠薬 | 不眠症 | 神経学 | NCT03075241 |
| ゾピクロン | III | 神経伝達物質ベース | 神経精神症状(睡眠障害)を改善する | 鎮静剤-催眠薬 | 不眠症 | 神経学 | NCT03075241 |
略語 DMT 疾患修飾療法、DM デキストロメトルファン
再利用された薬剤の治療領域は、循環器系5剤、精神系4剤、神経系3剤、血液腫瘍系1剤、糖尿病系1剤、肺系1剤であった。これらの薬剤のうち、鎮静剤、催眠剤が最も多かった。
第III相では、認知機能正常者(前臨床試験)を対象とした予防試験が2件、前駆性アルツハイマー病/軽度認知障害(MCI)患者を対象とした試験が3件、軽度~中等度アルツハイマー病患者を対象とした試験が5件、軽度~中等度/重度アルツハイマー病患者を対象とした試験が2件行われた。
第II相試験
アルツハイマー病パイプラインの第II相試験では、33の再利用薬が関与する32の試験が行われている(表3);これは第II相試験の全アルツハイマー病試験の44%である[14]。再利用された薬剤のうち、DMTが27種類、認知機能改善剤が1種類、行動症状改善剤が3種類であった。DMTsのうち、3つはアミロイド標的に関与しており、1つはタウ関連標的を対象としており、1つはアミロイド標的とタウ関連標的の両方に関連するメカニズムを有しており、22は他のMOA(例えば、神経保護、代謝、または抗炎症)を有している。症状を示す薬剤のうち、4つの薬剤はすべて神経伝達物質に基づくものである。
表3 アルツハイマー型認知症開発パイプラインのフェーズⅡで現在再利用されている薬剤(2020年2月27日現在
| エージェント名 | 段階 | エージェントメカニズムクラス | 研究中の治療目的 | ドラッグクラス | FDA承認の適応症 | 治療分野 | ClinicalTrials.gov ID(EudraCT ID) |
|---|---|---|---|---|---|---|---|
| ベンフォチアミン | II | 代謝 | 複数の細胞プロセスを改善します。ブドウ糖利用(DMT)の低下を最小限に抑える | 合成チアミン | 糖尿病性腎症; 2型糖尿病 | 抗糖尿病薬 | NCT02292238 |
| カンデサルタン | II | 抗アミロイド、神経保護、代謝 | 血管機能を改善し、アミロイド(DMT)を減らします | アンジオテンシンII受容体遮断薬 | 高血圧; 心不全 | 心臓血管 | NCT02646982 |
| シロスタゾール | II | 神経保護 | アミロイドの蓄積を減らし、タウのリン酸化を減らします。脳循環(DMT)を改善する | 抗血小板薬 | 間欠性跛行 | 血液腫瘍学 | NCT02491268 |
| ダパグリフロジン | I / II | 代謝 | インスリン感受性(DMT)を改善する | ナトリウム-グルコース共輸送体2阻害剤 | 2型糖尿病の補助療法 | 抗糖尿病薬 | NCT03801642 |
| ダラツムマブ | II | 抗炎症薬 | 広範囲の免疫調節効果; ミクログリア(DMT)を調節する | CD38を標的とするヒト抗体 | 多発性骨髄腫 | 血液腫瘍学 | NCT04070378 |
| ダサチニブ+ケルセチン(コンボ) | I / II | 抗炎症薬 | 老化細胞とタウ凝集(DMT)を減らすための老化細胞除去療法アプローチ | チロシンキナーゼ阻害剤+抗酸化剤/抗炎症剤(フラボノイド) | 慢性期のフィラデルフィア染色体陽性慢性骨髄性白血病 | 血液腫瘍学 | NCT04063124 |
| デフェリプロン | II | 抗アミロイド、神経保護 | ニューロンに損傷を与える活性酸素種を減らします。アミロイドおよびBACE病理学(DMT)への影響 | 鉄キレート剤 | 鉄過剰症(サラセミア症候群) | 血液腫瘍学 | NCT03234686 |
| ドロナビノール | II | 神経伝達物質ベース | 神経精神症状を改善する(興奮) | カンナビノイド | 食欲不振(エイズに関連); 吐き気/嘔吐(化学療法に関連) | カンナビノイド | NCT02792257 |
| インスリングルリジン | II | 代謝 | 細胞のシグナル伝達と成長を促進します。神経代謝(DMT)を促進する | インスリン | 糖尿病 | 抗糖尿病薬 | NCT02503501 |
| レノリドマイド | II | 抗炎症薬 | 炎症性サイトカイン(TNF-α、IL-6、IL-8)を減らします。炎症性およびAD関連のバイオマーカーを減らします。認知力の向上(DMT) | 抗腫瘍性 | 多発性骨髄腫 | 血液腫瘍学 | NCT04032626 |
| レベチラセタム | II | 神経保護 | アミロイド誘発性神経活動亢進(DMT)を減らす | 抗けいれん薬 | 部分てんかん発作の補助療法; 若年ミオクロニンてんかん; 一次全身性強直間代発作 | 神経学 |
(2016–003109-32) |
| レベチラセタム | II | 神経保護 | アミロイド誘発性神経活動亢進(DMT)を減らす | 抗けいれん薬 | 部分てんかん発作の補助療法; 若年ミオクロニンてんかん; 一次全身性強直間代発作 | 神経学 | NCT02002819 |
| レベチラセタム | II | 神経保護 | アミロイド誘発性神経活動亢進(DMT)を減らす | 抗けいれん薬 | 部分てんかん発作の補助療法; 若年ミオクロニンてんかん; 一次全身性強直間代発作 | 神経学 | NCT03875638 |
| レベチラセタム(AGB101) | II | 神経保護 | アミロイド誘発性神経活動亢進(DMT)を減らす | 抗けいれん薬 | 部分てんかん発作の補助療法; 若年ミオクロニンてんかん; 一次全身性強直間代発作 | 神経学 | NCT03461861 |
| リラグルチド | II | 代謝 | 細胞シグナル伝達を強化します。CNSグルコース代謝(DMT)を改善する | グルカゴン様ペプチド-1アゴニスト | 2型糖尿病の補助療法; 主要な心血管イベントのリスク低減 | 抗糖尿病薬 | NCT01843075(2013-000962-13) |
| リチウム | II | 神経伝達物質ベース | 神経精神症状を改善する(精神病を伴うまたは伴わない興奮/攻撃性) | 抗躁病 | 双極性障害 | 精神的 | NCT02129348 |
| リュープロリドデポ | II | 代謝 | 脳(DMT)に対する上昇したGnRHおよびゴナドトロピンの悪影響を軽減します | ゴナドトロピン放出ホルモンアゴニスト | 子宮内膜症; 子宮平滑筋腫 | ホルモン | NCT03649724 |
| モンテルカスト(バッカルフィルム) | II | 抗炎症薬 | 炎症経路(神経損傷、血液脳関門の完全性、アミロイドβ蓄積)を減らします。認知およびADバイオマーカー(DMT)への影響 | ロイコトリエン受容体拮抗薬 | 喘息; 運動誘発性気管支収縮; アレルギー性鼻炎 | 抗炎症薬 | NCT03402503 |
| モンテルカスト(錠剤) | II | 抗炎症薬 | 神経損傷、血液脳関門の完全性、アミロイドβ蓄積(DMT)を媒介する炎症経路を減らす | ロイコトリエン受容体拮抗薬 | 喘息; 運動誘発性気管支収縮; アレルギー性鼻炎 | 抗炎症薬 | NCT03991988 |
| ニコチンアミド | II | 抗タウ、神経保護 | タウによって誘発される微小管の解重合を減らします。タウのリン酸化を減らす(DMT) | ビタミンB3 | ペラグラ | ビタミン | NCT03061474 |
| ニコチン(経皮パッチ) | II | 神経伝達物質ベース | アセチルコリンシグナル伝達を強化する(認知エンハンサー) | アルカロイド | 禁煙離脱症状 | アルカロイド | NCT02720445 |
| ニロチニブ | II | 抗アミロイド、抗タウ | オートファジーエンハンサー; アミロイドおよびタウタンパク質(DMT)のクリアランスを促進します | チロシンキナーゼ阻害剤 | 慢性期のフィラデルフィア染色体陽性慢性骨髄性白血病 | 血液腫瘍学 | NCT02947893 |
| ペリンドプリル | II | 神経保護、抗炎症 | 血管機能(DMT)を改善します | アンジオテンシン変換酵素阻害剤 | 本態性高血圧症; 安定した冠状動脈疾患 | 心臓血管 | NCT02085265 |
| プラゾシン | II | 神経伝達物質ベース | 神経精神症状を改善する(興奮) | アルファ受容体拮抗薬 | 高血圧 | 心臓血管 | NCT03710642 |
| リファキシミン | II | 抗炎症薬 | 血中アンモニアを低下させることにより、認知と機能を改善します。有害な腸内細菌(DMT)によって分泌される下部循環炎症誘発性サイトカイン | 非全身性抗生物質 | 旅行者下痢; 明白な肝性脳症; 過敏性腸症候群(下痢サブタイプ) | 感染症 | NCT03856359 |
| リルゾール | II | 神経保護 | グルタメートを介した興奮毒性(DMT)を減らす | ベンゾチアゾール | 筋萎縮性側索硬化症 | 神経学 | NCT01703117 |
| Sagramostim | II | 抗アミロイド、神経保護 | 自然免疫系を刺激してアミロイド病変を取り除きます。ニューロンの接続性(DMT)を増やす | ヒト顆粒球-マクロファージコロニー刺激因子 | 骨髄刺激 | 血液腫瘍学 | NCT01409915 |
| フェニル酪酸ナトリウム | II | 神経保護 | 神経細胞死をブロックし、神経炎症(DMT)を調節します | 抗高アンモニア血症 | 慢性尿素回路障害の補助 | 遺伝学 | NCT03533257 |
| タクロリムス | II | 神経保護 | アミロイドβ樹状突起棘の喪失を防ぎます。脳の脳神経活動を正常化する(DMT) | カルシニューリン阻害剤 | 臓器移植の拒絶反応を防ぐ | 免疫学 | NCT04263519 |
| テルミサルタン | II | 神経保護、抗炎症 | 血管機能(DMT)を改善します | アンジオテンシンII受容体遮断薬 | 高血圧; 糖尿病性ニューロパチー; 脳卒中のリスク低減 | 心臓血管 | NCT02085265 |
| チエチルペラジン | II | 抗アミロイド | 輸送タンパク質ABCC1を活性化し、脳から血液への輸送アミロイドβペプチドを増強します(DMT) | フェノチアジン | 吐き気/嘔吐 | 神経学 | NCT03417986(2014-000870-20) |
| バラシクロビル | II | 神経保護、抗炎症 | 感染(DMT)に応答したアミロイドの過剰産生を防ぐことにより、アミロイドβ凝集を減少させます | 抗ウイルス剤(ヌクレオシド類似体) | 口唇ヘルペス; 性器ヘルペス | 感染症 | NCT03282916 |
| バラシクロビル | II | 神経保護、抗炎症 | 感染(DMT)に応答したアミロイドの過剰産生を防ぐことにより、アミロイドβ凝集を減少させます | 抗ウイルス剤(ヌクレオシド類似体) | 口唇ヘルペス; 性器ヘルペス | 感染症 | NCT02997982 |
略称 DMT 疾患修飾療法
第II相再利用薬の治療領域は、血液腫瘍薬(7)神経系薬剤(6)循環器系薬剤(4)糖尿病治療薬(4)その他のクラス(カンナビノイド、アルカロイドなど)で構成されている(合計12)。抗けいれん薬は第II相試験で最も代表的な薬物クラスであった。
予防試験が1件、進行性/MCIまたは進行性/軽度アルツハイマー病患者を対象とした試験が19件、軽度中等度アルツハイマー病患者を対象とした試験が11件、軽度中等度/重度アルツハイマー病患者を対象とした試験が1件である。DMT試験のうち、認知機能正常者を対象とした予防試験が1件、進行性・軽度アルツハイマー病患者を対象とした試験が17件、軽度・中等度アルツハイマー病患者を対象とした試験が8件である。
第Ⅰ相試験
9つの第I相臨床試験のうち、リパーゼント薬は10種類(表4)あり、パイプライン中の第I相臨床試験の33%である[14]。このうち、DMTが8剤、認知増強剤が2剤である。神経精神症状を対象とした薬剤は、第Ⅰ相試験のパイプラインには含まれていない。フェーズIのDMTのうち、1剤はアミロイド関連の標的を対象としているが、7剤は他のMOA(例:神経保護、代謝、抗炎症)を有している。現在のパイプラインの第I相試験では、タウ関連のリパーゼント剤の研究は行われていない。
表4 アルツハイマー型認知症の開発パイプラインにおいて、現在、第I相試験中の再販薬(2020年2月27日現在)
| エージェント名 | 段階 | エージェントメカニズムクラス | 研究中の治療目的 | ドラッグクラス | FDA承認の適応症 | 治療分野 | ClinicalTrials.gov ID |
|---|---|---|---|---|---|---|---|
| アロプレグナノロン(ブレキサノロン) | 私 | 神経保護、代謝 | 強化された神経新生は海馬の萎縮を遅らせます。シナプス接続(DMT)を改善する | GABA-A受容体モジュレーター; 神経活性ステロイド(抗うつ薬) | 産後うつ病 | 精神的 | NCT03748303 |
| BDPP(生理活性食餌ポリフェノール調製) | 私 | 神経保護 | アミロイドとタウの凝集を防ぎます(DMT) | ポリフェノール | ダイエットサプリ | 栄養補助食品 | NCT02502253 |
| ダビガトラン | 私 | 神経保護 | 神経血管損傷(DMT)を減らす | 抗凝固剤 | 脳卒中のリスクを軽減します。心房細動、深部静脈血栓症、肺塞栓症に関連する塞栓症 | 血液腫瘍学 | NCT03752294 |
| エファビレンツ | 私 | 抗アミロイド | コレステロール除去を高め、アミロイド減少(DMT)を高める | 非ヌクレオシド逆転写酵素阻害剤 | HIV / AIDS | 感染症 | NCT03706885 |
| エスシタロプラム | 私 | 神経伝達物質ベース | 神経伝達を増加させる(認知エンハンサー) | 選択的セロトニン再取り込み阻害薬 | 大鬱病性障害; 全般性不安障害 | 精神的 | NCT03274817 |
| エンパグリフロジン | 私 | 代謝 | 脳内のケトンレベルを上げます。ニューロンの健康を改善し、認知障害(DMT)の発症と進行を遅らせる | ナトリウム-グルコース共輸送体2阻害剤 | 2型糖尿病の補助療法 | 抗糖尿病薬 | NCT03852901 |
| サルサレート | 私 | 抗炎症薬 | 神経損傷(DMT)を減らす | 非ステロイド性抗炎症薬 | 関節リウマチ; 変形性関節症 | 抗炎症薬 | NCT03277573 |
| テルミサルタン | 私 | 神経保護、抗炎症 | 血管機能とアミロイド病理(DMT)への影響を改善する | アンジオテンシンII受容体遮断薬 | 高血圧; 糖尿病性ニューロパチー; 脳卒中のリスク低減 | 心臓血管 | NCT02471833 |
| ベンラファキシン | 私 | 神経伝達物質ベース | 神経伝達を増加させる(認知エンハンサー) | セロトニン-ノルエピネフリン再取り込み阻害薬 | 大鬱病性障害; 全般性不安障害; 季節性情動障害; パニック障害 | 精神的 | NCT03274817 |
| ボリノスタット | 私 | 神経保護 | タウ凝集およびアミロイド沈着(DMT)を含む複数の細胞プロセス | ヒストンデアセチラーゼ阻害剤(抗がん剤) | 皮膚T細胞リンパ腫 | 血液腫瘍学 | NCT03056495 |
略語 DMT、疾患修飾療法
第I相試験では、リパーゼント剤は精神科領域の薬剤3剤、血液腫瘍領域の薬剤2剤、循環器領域の薬剤1剤、糖尿病領域の薬剤1剤、その他の薬剤クラスの薬剤3剤(抗炎症剤、感染症領域の薬剤など)が含まれている。
治験スポンサー
再利用された薬剤の全試験において、9%がバイオ製薬企業、79%が学術医療センター(国立衛生研究所、産業界、コンソーシ アムや慈善財団などの他団体からの資金提供を受けている)11%がその他のスポンサーである。表 5 に開発フェーズごとのスポンサーを示す。
表5 薬剤開発のフェーズ別再利用薬の治験依頼者(2020年2月27日現在
| スポンサー | フェーズI | フェーズII | フェーズIII | 合計(%) |
|---|---|---|---|---|
| 学術医療センター | 6 | 14 | 4 | 24(45.3) |
| バイオ医薬品 | 0 | 2 | 3 | 5(9.4) |
| NIH(アメリカ国立衛生研究所)(#文字数制限がない場合、初出時にかっこ書きを追加 | 1 | 0 | 0 | 1(1.9) |
| NIHおよび学術医療センター | 0 | 4 | 2 | 6(11.3) |
| NIHとコンソーシアム | 0 | 1 | 0 | 1(1.9) |
| NIHと業界 | 0 | 0 | 1 | 1(1.9) |
| 学術医療センターと産業 | 0 | 2 | 0 | 2(3.8) |
| 学術医療センターと財団 | 1 | 4 | 0 | 5(9.4) |
| 学術医療センター、産業、およびNIH | 0 | 0 | 1 | 1(1.9) |
| 他の組み合わせ | 1 | 4 | 0 | 5(9.4) |
| その他の連邦情報源 | 0 | 1 | 1 | 2(3.8) |
| 合計 | 9 | 32 | 12 | 53(100.0) |
略語 NIH 国立衛生研究所
2016年から 2020年までのパイプラインで再利用されているエージェント
表6は、過去の年次アルツハイマー病パイプライン報告書[10-14]におけるリパーポージング試験の数をまとめたものである。2016年以降、リパーポージング薬が関与する試験の数は89%増加している。試験数は年々増加しており、最も増加率が高いのは2019年から 2020年の間(23%の増加)である。2016年から 2020年の間に、DMTの再使用試験は180%増加したが、症状の軽減に焦点を当てた再使用試験は67%減少した。
表6 2016年~2020年の間に再利用する薬剤の治験
| 2016年 | 2017年 | 2018年 | 2019年 | 2020 | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| DMT | 症候性のエージェント | DMT | 症候性のエージェント | DMT | 症候性のエージェント | DMT | 症候性のエージェント | DMT | 症候性のエージェント | |
| フェーズI | 1 | 3 | 1 | 2 | 3 | 2 | 7 | 1 | 8 | 1 |
| フェーズII | 10 | 7 | 11 | 9 | 15 | 10 | 19 | 7 | 28 | 4 |
| フェーズIII | 4 | 3 | 4 | 4 | 2 | 5 | 3 | 6 | 6 | 6 |
| 合計 | 15 | 13 | 16 | 15 | 20 | 17 | 29 | 14 | 42 | 11 |
略語 DMT 疾患修飾療法
リパーゼ薬の第I相試験は2016年から 125%増、第II相試験は88%増、第III相試験は71%増となっている。現在のパイプラインでは、リパーゼント剤のDMT試験がリパーゼント剤全体の79%を占めている(2016年の54%から増加、図4)。
図4 アルツハイマー病治療薬開発パイプラインにおける経時的な試験の再利用(2016年~2020年)
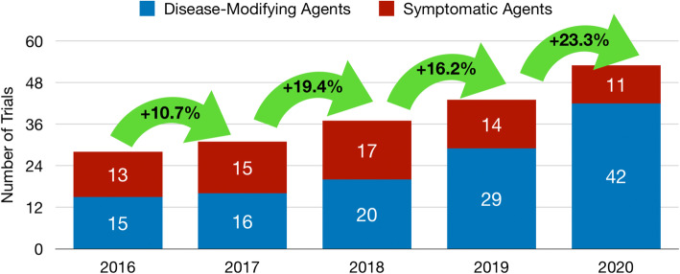
欧州のアルツハイマー病パイプラインで再利用されている薬剤
EUCTRに登録されている進行中の138のアルツハイマー病試験のうち、14のFDA承認薬を含む14の試験を確認した(表7)。そのうち11試験は、米国とEU/EEAデータベースに二重登録されていた。5つの試験が第III相試験で、9つの試験が第II相試験であった。ClinicalTrials.govに掲載されている情報と比較すると、6つの試験は終了または終了していた。エポエチンアルファ、レボドパ-カルビドパ、カンナビジオールの3つの試験がEUCTRに独占的に登録されていた。
表7 欧州アルツハイマー病の開発パイプラインで現在開発中の再利用薬(2020年2月27日現在)
| エージェント名 | フェーズ | エージェントメカニズムクラス | 研究中の治療目的 | ドラッグクラス | FDA承認の適応症 | 治療分野 | EudraCT ID(Clinicaltrials.gov ID) |
|---|---|---|---|---|---|---|---|
| ALZT-OP1a、ALZT-OP1b(イブプロフェンの有無にかかわらずクロモリン) | III | 抗アミロイド、抗炎症 | ニューロンの損傷を減らします。肥満細胞はアミロイド病理学(DMT)でも役割を果たす可能性があります | マスト細胞安定剤 | 気管支ぜんそく; 肥満細胞症 | 肺 | 2015-002147-34(NCT02547818) |
| カンナビジオール | II | 神経伝達物質ベース | 神経精神症状を改善する(興奮) | カンナビノイド | 発作(レノックス・ガストー症候群またはドラベ症候群) | 神経学 | 2019-002106-52 |
| ドロナビノール | II | 神経伝達物質ベース | 神経精神症状を改善する(興奮) | 合成デルタ-9-THC | エイズ関連の食欲不振; 化学療法誘発性の悪心および嘔吐に対する制吐剤 | 神経学 |
2011-005289-39 * 2010-024577-39 * |
| エポエチンアルファ | II | 抗炎症、代謝 | 神経損傷(DMT)を減らします。神経精神症状(うつ病)を改善する | 赤血球生成刺激剤 | 貧血(慢性腎臓病、ジドブジン治療、化学療法); 赤血球輸血の減少 | 血液腫瘍学 | 2008-000453-35 |
| レベチラセタム | II | 神経保護 | アミロイド誘発性神経活動亢進(DMT)を減らす | 抗けいれん薬 | 部分てんかん発作の補助療法; 若年ミオクロニンてんかん; 一次全身性強直間代発作 | 神経学 | 2016-003109-32(NCT03489044) |
| レボドパ-カルビドパ | II | 神経伝達物質ベース | ドーパミン神経伝達を強化する(認知エンハンサー) | ドーパミンプロドラッグ | パーキンソン病 | 神経学 | 2009-011093-15 |
| リラグルチド | II | 代謝 | 細胞シグナル伝達を強化します。CNSグルコース代謝(DMT)を改善する | グルカゴン様ペプチド-1アゴニスト | 2型糖尿病の補助療法; 主要な心血管イベントのリスク低減 | 抗糖尿病薬 | 2013-000962-13(NCT01843075) |
| マシチニブ | III | 抗炎症薬 | マスト細胞の活動、炎症過程の調節(DMT) | 選択的チロシンキナーゼ阻害剤 | 肥満細胞腫(獣医) | 血液腫瘍学 | 2010-021218-50(NCT01872598) |
| ロシグリタゾン | III | 代謝 | PPAR-ガンマアゴニスト(向知性薬) | チアゾリジンジオン | 2型糖尿病の補助療法 | 抗糖尿病薬 |
2012-002764-27 ** 2006-001403-11 * 2006-001402-92 * |
| ロチゴチン | II | 神経伝達物質ベース | ドーパミン神経伝達を強化する(認知エンハンサー) | 非エルゴリンドーパミン作動薬 | パーキンソン病; 不穏下肢症候群 | 神経学 |
2015-002965-43 * |
| チエチルペラジン | II | 抗アミロイド | 輸送タンパク質ABCC1を活性化し、脳から血液への輸送アミロイドβペプチドを増強します(DMT) | フェノチアジン | 吐き気/嘔吐 | 神経学 |
2014-000870-20 |
略語
DMT 疾患修飾療法、THC テトラヒドロカンナビノール
*CiinicalTrials.govで報告された「完了」の状態にある試験
**ClinicalTrials.govで報告された「Terminated」ステータスの試験
再利用された薬剤の中には、DMTが6剤、認知機能強化剤が5剤、精神神経症状に対応する薬剤が3剤含まれていた。治療領域は、神経内科領域が4剤、血液腫瘍領域が2剤、肺適応症が1剤、糖尿病治療薬が1剤であった。
考察
薬物の再利用は、アルツハイマー病治療薬候補の開発期間を大幅に短縮するユニークな機会を提供する。これらの薬剤は、通常、開発の非臨床および第1相段階で必要とされる薬物動態学的特性と毒性について広範囲に評価されている。すべての薬剤の半分以上は、これら、2つの理由で開発に失敗しており、再利用はこれらの課題を回避している[18]。FDA承認薬はすでにヒト試験を受けており、安全性、有効性、および有害事象のプロファイルが知られている。以前の試験の結果は、非臨床試験段階や初期の臨床試験段階を回避するのに十分であろう。新薬の開発にかかる総費用は57億ドルにもなり、非臨床試験には16.6億ドル、第Ⅰ相試験には11.9億ドルが必要である[19]。総開発コストは、新規化学物質の開発コストと比較して50%削減される可能性がある。
FDAで承認された薬剤は、本来の適応症に合わせて最適化されている。異なる用量が必要とされるかもしれず、また、その薬剤が最初に開発された他の集団と比較して、アルツハイマー病の集団では異なる有害事象プロファイルが発生する可能性がある。開発プロセスのいくつかのステップは、これらの不測の事態を考慮して繰り返されるかもしれない。再利用された薬剤は多くの場合、ジェネリックであり、知的財産権に制限があるため、開発を促進することができる投資を集めることができない[20]。
現在のアルツハイマー病治療薬のパイプラインに含まれている再利用薬を調べたところ、DMT試験は主に血液腫瘍(チロシンキナーゼ阻害薬)心血管(アンジオテンシンII受容体拮抗薬、アンジオテンシン変換酵素阻害薬)神経学的適応(抗痙攣薬)糖尿病に由来する薬剤に基づいていることが明らかになった。これらの薬剤が標的とする主要な病理学的変化とアルツハイマー病の基礎となる生物学との関連性を支持する証拠が増えている[21-24]。認知症に関連した症状とチロシンキナーゼ経路の異常活性化、心血管疾患、インスリン感受性の低下との関連は、これらの薬剤が再利用薬のパイプラインに存在することによって反映されている。アルツハイマー病におけるこれらのプロセスについての知識が増えていることから、リパーポージングはアルツハイマー病治療薬に対する精密医療のアプローチを構成する可能性がある[25]。精神医学的化合物の大部分は対症療法薬のクラスを構成しており、その大部分(一部の非抗精神病薬を含む)はアルツハイマー病に関連した動揺を緩和することを目的としている。このことは、患者や介護者にとってアルツハイマー病の苦痛を与える側面の治療法を特定することが、この分野での優先事項であることを示しているのかもしれない。これらの試験は、患者の同定と転帰の決定を助ける動揺の新しい診断基準の開発によって促進された [26]。
特定の再利用候補は、アルツハイマー病の標的に直接関与することなく治療上の利益を提供する可能性がある。脳血流の低下はアルツハイマー病の病態と相関している[27]。パイロット研究では、抗血小板薬であるシロスタゾール(NCT02491268)は、脳血流の局所的な増強を含む多動的効果により認知機能の低下を遅らせる可能性が示唆されている[28-30]。アルツハイマー病における神経炎症の役割を標的とする薬剤もある:血液脳関門の機能に影響を与える炎症は、モンテルカストの2つの試験(NCT03402503,NCT03991988,[31,32])で関心の高い成分である。リファキシミン(NCT03856359)の試験では、プロ炎症性サイトカインとアンモニアレベルの低下による認知機能の改善が報告されている[32]。
リパーポージング薬の試験は 2020年のアルツハイマー病パイプライン全体の39%を占める(2016年は24%)。フェーズIIでは、リパーポージング試験と全体のパイプラインの両方で最も多くの試験が行われている(それぞれ60%と55%)。これは、リパーポージング薬が直接フェーズIIまたはフェーズI/IIに参入したことによるものと思われる。DMT試験は2020年のアルツハイマー病パイプラインの約79%を占めているのに対し、リパーポーザント薬のサブセットを見ると75%となっている。アミロイドは第II相および第III相DMT試験全体で最も一般的な特異的標的であるが、再構成されたDMTの大部分はタウを標的としている。
すべてのアルツハイマー病試験の46%は、少なくとも一部がバイオ製薬業界からの資金提供を受けている。対照的に、再利用薬の試験の大部分(79%)は、学術医療センターからの部分的または完全な資金提供を受けており、バイオ製薬業界からの資金提供はわずか9%に過ぎない。これは、営利企業がこの開発経路で実行することを阻む、再利用された薬剤の知的財産保護を得るという課題を反映している。この観察は、アルツハイマー病医薬品開発のエコシステムにおける学術医療センターと連邦政府および博愛主義的な資金提供の重要性を強調している。
さまざまな戦略は、再利用された薬剤の知的財産ポジションを確保しようとするために評価されている。薬剤の本来の適応症とは異なる用量を使用することは一つのアプローチであり、各適応症に必要とされる薬物曝露量に依存する。この戦略はHOPE4MCI試験(NCT03486938)に例示されており、この試験では、抗痙攣目的で使用されるレベチラセタムの10分の1の用量を使用している。もう一つのアプローチは、新規な剤形の使用である。インスリングルリシン(NCT02503501)は、インスリンの速効型である;長時間作用型(NCT01595646)は、アルツハイマー病での試験のために開発された[33]。Montelukastは、経口錠剤と頬膜パッチを用いた2つの別々の試験(NCT03991988,NCT03402503)で認知機能向上剤として研究されている。このことは、有効性を高め、知的財産権を確保するための手段として、リパーポスド製剤の新しいデリバリーメカニズムを開発する機会があることを示している。
リパーポージングの顕著な増加は、アルツハイマー病治療薬開発における戦略としてのリパーポージングの利点を明らかにすることを目的とした最近の取り組みを反映していると考えられる[7, 34]。連邦政府、アドボカシー、慈善団体からの資金提供は、リパーパスされた薬剤の試験を不均衡に支援しており、これがリパーポージングの増加を促進した可能性がある。再利用は、表現型または高含量スクリーニング、in silico技術、バイオインフォマティクスまたは計算戦略、医学的遺伝学に基づくアプローチを含む、アルツハイマー病に有効な医薬品を同定するために使用されている方法論の進歩によって加速された可能性がある [9, 35-39]。電子カルテは、他の適応症で承認された治療法によるアルツハイマー病または他の神経変性疾患に対する有益な効果の証拠を提供する可能性があり、再利用薬剤を発見するためのもう一つの手段である[39, 40]。しかし、これらの薬剤への長期曝露の効果は、ほとんどの現在のアルツハイマー病試験の18~24ヵ月間では再現されないかもしれない。
2016年から 2020年の間に、再利用薬剤の20の試験は「終了」状態に達したが、4つの試験は様々な理由で「中止」された。メトホルミンのパイロット第II相試験(NCT01965756)の事後分析では、本剤は安全で忍容性が高く、執行機能の改善が認められた[41]。別の研究では、アルツハイマー病の軽度認知障害(MCI)段階でニューガム10%IVIG(免疫グロブリン静注;NCT01300728)の短期経過を投与したところ、脳の萎縮が減少し、認知機能の低下が改善されたが、有益な効果は2年後には持続しなかった[42]。第I相試験(NCT01780519)では、ロラゼパムがアルツハイマー病の遺伝的リスクを有する患者において、症状前の認知機能障害を明らかにする可能性があることが示された[43]。NIL血管性認知症試験(NCT02017340)の一次アウトカム解析では、プラセボ群と比較した場合、ニルバジピンは安全で忍容性が高いことが判明したものの、ニルバジピンによる治療効果を示すことはできなかった[44]。GrifolsによるAMBAR試験(NCT01561053)は、免疫グロブリンの有無にかかわらず、治療的アルブミン補充を介した潜在的なアルツハイマー病治療への新しいアプローチを提供している[45]。アウトカム解析では、治療を受けた中等度アルツハイマー病の進行が統計学的に有意に61%減少したことが明らかになった。試験の「失敗」はいずれも安全性または忍容性に関連した問題に起因するものではなく、これは再利用された薬剤がすでに受けている広範な研究を示しているのかもしれない。
エシタロプラムは動揺と認知機能の改善を対象とした試験で同時に研究されている(NCT03108846, NCT03274817)。ALZT-OP1(NCT02482324)は、マスト細胞安定剤(クロモリン)と非ステロイド性抗炎症剤イブプロフェンの2剤併用療法である。ロサルタン、アムロジピン、アトルバスタチンの組み合わせは、アルツハイマー病の血管の次元に対処するために再利用された薬剤を含む組み合わせ試験(NCT02913664)である。
我々はEUCTRで再利用を評価し、ClinicalTrials.govの解析と比較した。米国政府のデータベースを検索するために使用したのと同じ基準を使用して、現在進行中のEU/EEAのアルツハイマー病試験の約10%がリパーポージング試験であることがわかった(米国のアルツハイマー病パイプラインでは39%であるのに対し、リパーポージング試験は約10%)。米国のパイプラインと同様に、試験の大部分(64%)は第II相試験であり、DMT薬(43%)が関与している。EU/EEA試験で確認された薬剤の大部分は、ClinicalTrials.govで確認された薬剤の中に含まれてたが、EUCTRで確認された薬剤は3つの試験のみでした。
両方の試験登録を比較する際には、いくつかの大きな相違が見られた。EUCTRで実施された14試験のうち6試験(43%)がClinicalTrials.govで「完了」または「終了」となってた(表7)。EUCTRでの二重登録試験の不正確な報告は一般的な問題である[46]が、EudraCTデータベースへの試験結果の手動入力をスポンサーに依存していることを一部反映している可能性がある。RCTプロトコルと結果の最適な完成度が低いと、試験活動の過大評価につながる可能性がある [47-50]。
リパーポージングは、ライフサイクル管理の一環として、独自の薬剤の適応拡大を開発することとは区別されるべきである。例えば、ピマバンセリンはパーキンソン病の精神病における幻覚や妄想の治療薬として承認されており、現在、いくつかの認知症症候群に対する認知症関連精神病の適応拡大が開発されている[51, 52]。同様に、スボレキサント(ベルソムラ)は不眠症で承認されており、アルツハイマー病の不眠症に対する試験が成功しており、この化合物の表示はこの情報を含むように調整されている。ブレキシプラゾールは統合失調症の治療および大うつ病性障害の併用療法として承認されており、アルツハイマー病のパイプラインでは激越の治療法として評価されている[53]。これらのプログラムは適応の拡張であり、リパーポージングではない。
リパーポージングは、スポンサーの開発プログラムに含まれる未承認薬が、疾患関連、化合物関連、または商業的な状況から、ある病態では別の病態よりもさらなる開発に成功する可能性が高いことが示唆されているために、ある適応症から別の適応症に変更されるリポジショニングとは区別される[54, 55]。
限界
現在の分析には限界がある。すべての第I相試験の活動がclinicaltrials.govデータベースに記録されているわけではないため、我々のデータはこの段階の実際の試験数を過小評価している可能性がある。DMTと対症療法薬に指定された薬剤の推定値は、薬剤の原則的なMOAとして認識されるものによっては、曖昧なものになる可能性がある。投稿、ピアレビュー、出版を可能にした時点でデータベースへの新規データの入力を停止しており(最終データ収集は2020年2月27日に停止)本書に反映されていない新規試験や現在の試験への変更があるかもしれない。
結論
要約すると、リパーポージングはアルツハイマー病治療薬開発の有望な手段であり、現在のアルツハイマー病治療薬パイプラインのかなりの部分を構成しており、パイプラインの絶対数と割合として増加している。リパーポージングは、医薬品開発コストを最大50%削減し、パイプラインにおける進行のタイムラインを加速させる可能性がある。リパーポージングは、他の多くの適応症の開発プログラムを利用している。リパーポージングは、現在のアルツハイマー病医薬品開発のエコシステムにおいて重要な役割を果たしている。