コンテンツ
アルツハイマー病と鉄の関係
関連記事
概要
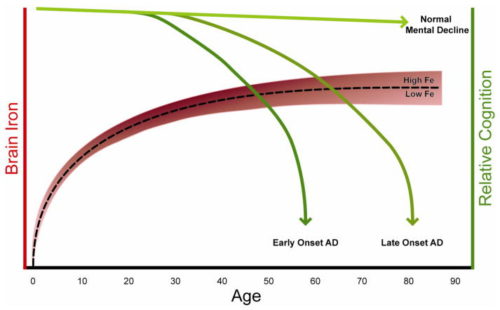
加齢と共に上昇する脳鉄
脳内の鉄は、健康な人であっても年齢とともに上昇する。(下記図参照)
鉄代謝の調節不全が、アルツハイマー病初期に起きているという証拠は積み重なってきている。
また鉄ホメオスタシスバランスの崩れと、アミロイド班形成はお互いに因果的な作用をもつ。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4672943/
脳内の鉄量と年齢の関係
アミロイドと鉄の相互作用
三価鉄はアルツハイマー病初期の段階では、βアミロイドと相互作用し、モノマー、二量体、四量体形成の間で変動する。
鉄とアミロイドの相互作用が二価鉄を増加させ、ROSの発生につながる。
アミロイドプラークが成熟すると、脳機能に必要な三価鉄を枯渇させ、二価鉄を増殖させる働きをする。

https://www.sciencedirect.com/science/article/pii/S2213231717307267
脊髄液中の鉄レベルとアルツハイマー病の強い相関
ApoE4と強く関連
脊髄液中のフェリチン濃度がAPOE4遺伝子陽性の認知低下と強く関連している。すでに確立されているバイオマーカー、タウやアミロイドβよりもフェリチンとの関連がはるかに大きい。
http://www.medscape.com/viewarticle/874539
3年間発症を遅らせる
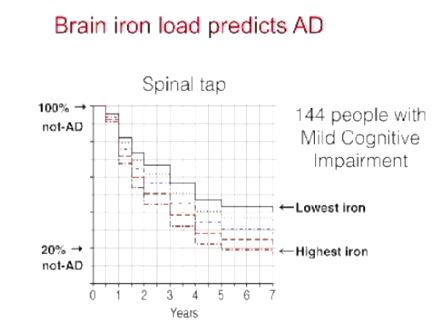
脊髄液中のフェリチンを低下させることは、MCIからアルツハイマー病への移行を最大で3年遅らせることができる可能性がある。
https://www.nature.com/articles/ncomms7760
鉄とアルツハイマー病 動画
鉄はアルツハイマー病に寄与するのか
アミロイドだけでは認知症は発症しない
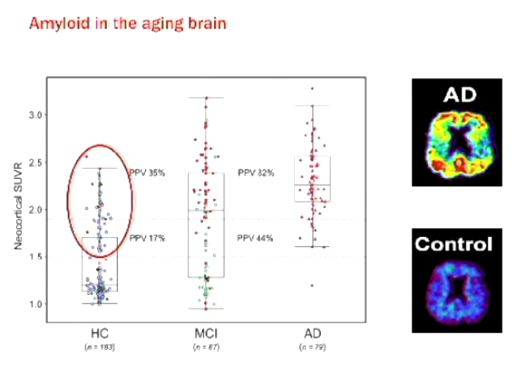
ショッキングなことに65歳を超えた健常者の30%はアルツハイマー病ではなくとも、アルツハイマー病患者と同じレベル(PETスキャン)でアミロイドが蓄積している!
これはアミロイドが単独で認知機能の低下をもたらしているわけではないことを示唆する。
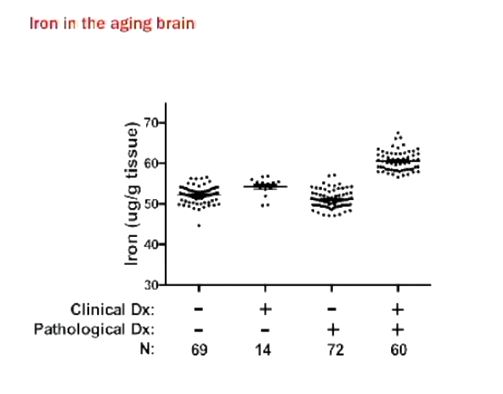
左から
アルツハイマー病の
・臨床診断は正常、病理も正常
・臨床診断はAD陽性、病理は正常
・臨床診断は正常、病理には問題あり
・臨床診断はAD陽性、病理にも問題がある人(組織に含む鉄の量が多い)
脳内鉄によって加速する海馬萎縮
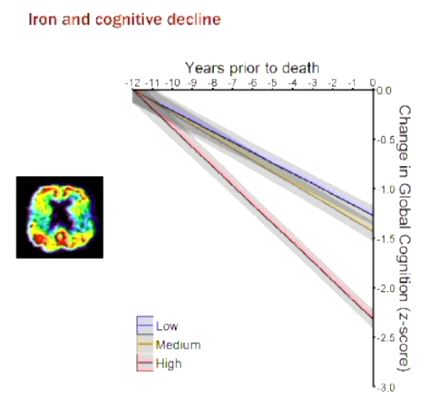
青色ライン 脳内鉄が少ないアルツハイマー病患者
黄色ライン 脳内鉄を中程度に保持するアルツハイマー病患者
赤色ライン 脳組織に鉄を多く含むアルツハイマー病患者
脊髄液の鉄によって加速する認知機能低下
アルツハイマー病 鉄の神経化学、治療標的
一般的な鉄の役割
酸素輸送
ミトコンドリア呼吸
細胞増殖と分化
金属酵素の活性部位
神経系に関する鉄の役割
ミエリン合成に必須
神経伝達物質の合成および代謝
一般的な過剰鉄の問題
フェントン反応によるヒドロキシラジカルの生成
→ DNA損傷、タンパク質損傷、過酸化脂質、その他のROS生成
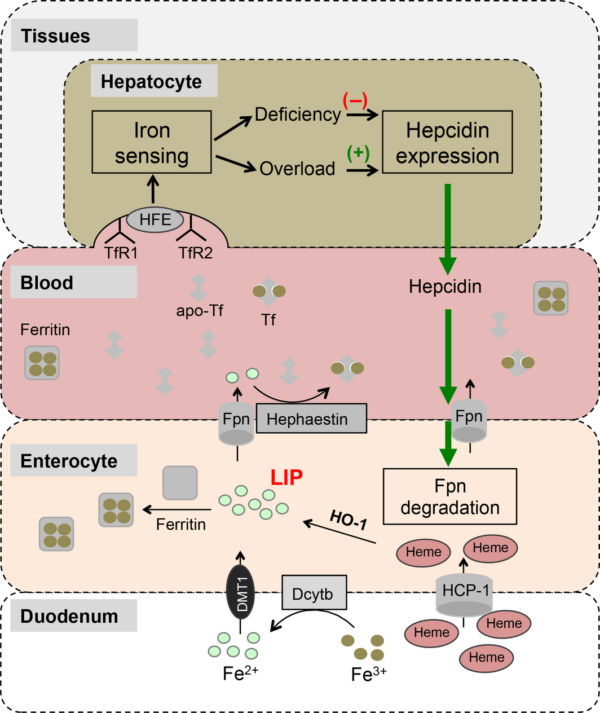
鉄レベル増加・低下する脳部位
正常な老化であっても、脳における進行性の鉄蓄積は生じる。
鉄の蓄積は、老人斑、神経原線維に限定されない。
以下の脳領域内で鉄蓄積が年齢とともに増加する。
- 黒質
- 被殻
- 淡蒼球
- 尾状核
- 皮質
https://www.ncbi.nlm.nih.gov/pubmed/15210960/
https://www.ncbi.nlm.nih.gov/pubmed/13611557/
最も鉄濃度が高くなる脳部位 大脳基底核の以下の部位
- 淡蒼球
- 黒質
- 小脳
鉄の濃度が低い部位
- 皮質灰白質
- 白質
- 中脳
- 小脳
- 橋(脳)
- 髄質
https://www.ncbi.nlm.nih.gov/pubmed/24075790/
- 被殻
- 脊柱視床路
- 赤核
- 海馬
- 側頭皮質
アルツハイマー病患者は、被殻、脊柱視床、赤核、海馬および側頭皮質において鉄濃度が上昇している。
https://www.ncbi.nlm.nih.gov/pubmed/23942230
- 前頭皮質
死後、アルツハイマー病患者は健常高齢者に比べ前頭皮質に鉄が多く蓄積
https://www.ncbi.nlm.nih.gov/pubmed/26721301
鉄排出能力の低下
アルツハイマー病患者の末梢血単核細胞において、
アコニターゼ1、セルロプラスミン、APPが減少
細胞からの鉄排出が抑制されている。
鉄排出能力の低下
アルツハイマー病患者では、タウの過剰リン酸化と、それによる神経原線維変化凝集が可溶性タウプールを減少させることによって、ニューロンの鉄排出能力が低下する。
GPI結合セルロプラスミン
GPI結合セルロプラスミンがないと、鉄の輸送に必要なフェロオキシダーゼ活性が欠損し、細胞膜のフェルロポルチンがすぐに分解されることで、細胞外への鉄排出が阻害され、細胞内に鉄が蓄積される。
また、局所的な鉄の蓄積によって鉄を奪うことにより、他の脳部位における鉄の枯渇をもたらすことも神経変性にむすびつく
鉄による神経変性メカニズム
酸化還元金属によるアミロイドβの毒性増強
酸化還元金属が存在しない状態では、アミロイドβの毒性はない。アミロイドβの凝集には金属が必要。
鉄はアミロイドβペプチドだけでなくタウにも結合し、リン酸化に影響を与える。
脳鉄レベルの増加によるアミロイドβ産生
脳の鉄濃度は、翻訳レベルでAPP発現を調節するため、ニューロン中の鉄濃度の増加は、アミロイド形成プロセシングにより、潜在的にアミロイドβ産生を増加させる。
(鉄は、APPのαセレクターゼ切断に対して調節作用をもつ。)
ヘムオキシゲナーゼ-1(HO-1)の過剰発現
神経原線維変化のタウ蓄積は、細胞質基質のヘムオキシゲナーゼ1(HO-1)増加と関連している。
HO-1は第一鉄(二価鉄化合物)の放出に寄与し、酸化ストレスにつながる可能性がある。
https://www.ncbi.nlm.nih.gov/pubmed/19457088/
https://www.ncbi.nlm.nih.gov/pubmed/21613741/
https://www.ncbi.nlm.nih.gov/pubmed/7778849/
https://www.ncbi.nlm.nih.gov/pubmed/16399210/
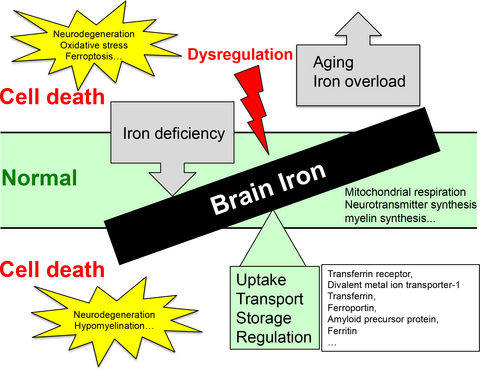
鉄不均衡
アルツハイマー病患者の全脳における鉄の単独増加が、必ずしも脳内の酸化ストレスの誘発するというわけではない。
むしろ鉄恒常性の不均衡が問題。
鉄過剰と鉄不足
鉄過剰環境において、アミロイド班、神経原線維変化周辺に酸化ストレスおよび、細胞死をもたらし、他の脳領域は反対に鉄を奪われることによって、神経機能を損なう可能性がある。
高齢の健常者では、ニューロンの不安定鉄プール(LIP)の増加に応じて、鉄を取り込んだり、貯蔵、排出に関わる鉄応答タンパク質(IRP1、IRP2)が応答する。
鉄の選択的な除去の必要性
重要なことは、恒常性としての鉄欠乏を引き起こすことなく、特定の脳領域から鉄を除去すること。
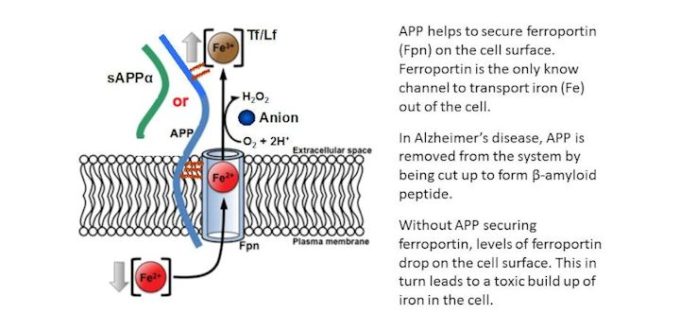
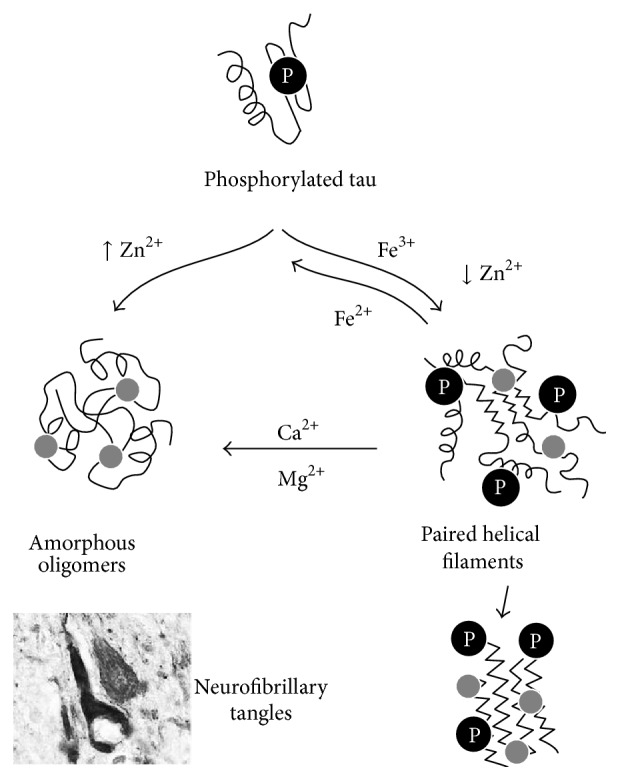
http://www.fbs-wp.leeds.ac.uk/blogs/dementia/resource-map/iron-regulation-in-alzheimers-disease/
https://www.ncbi.nlm.nih.gov/pubmed/26881049
アルツハイマー病患者の病変部である海馬に大量の鉄が含まれている。
死後の脳への鉄の蓄積、前頭側頭葉変性症のみ有意に過剰蓄積
https://www.ncbi.nlm.nih.gov/pubmed/24698410
トランスフェリン機能不全
アルツハイマー病患者の鉄過剰は、血中にある鉄輸送を担うトランスフェリンの機能不全が関与している可能性。
https://www.ncbi.nlm.nih.gov/pubmed/22635102
進行指標としてのフェリチンレベルバイオマーカー
脳脊髄液中のフェリチン濃度とMCIからADへ移行は強く関連、認知能力とは逆相関
https://www.ncbi.nlm.nih.gov/pubmed/25988319
検査指標
血清鉄
血清鉄の矛盾する結果
アルツハイマー病患者の血漿鉄量は減少し特発性貧血と関連する。
アルツハイマー病症例ではトランスフェリン濃度には有意差を示さず、トランスフェリン結合鉄総量の減少のみ示した。
https://www.ncbi.nlm.nih.gov/pubmed/25588002/
アルツハイマー病患者の低い血清鉄
メタアナリシス AD患者の血清鉄は健常者よりも有意に低い。
https://www.ncbi.nlm.nih.gov/pubmed/24916541
病期によって異なる血中鉄濃度
銅、鉄、およびセレンの血中濃度とアルツハイマー病との関係
アルツハイマー病患者では血清中の高レベルの銅と鉄の上昇が示されるが、病気によって異なる。
臨床認知症評価(CDR)CDR-1では金属レベルに有意な差は示されなかったが、CDR-2およびCDR-3では銅および鉄のレベルの上昇が観察された。
CDR−3の患者では、健常者と比較して、セレンのレベルは低かった。
https://www.ncbi.nlm.nih.gov/pubmed/28500578
アルツハイマー病患者のフェリチン・血清鉄レベル
AD初期の高い血清フェリチン
MCI患者では高い血清フェリチンが観察され、アルツハイマー病患者の初期の段階では高い血清鉄レベルが観察される。
相反する結果
アルツハイマー病患者と健常者の血清鉄、フェリチン濃度に有意差はない。
グレード2のアルツハイマー病患者の平均血清鉄濃度は有意に低い。
炎症と関連する可能性もある
アルツハイマー病患者の高い血清フェリチンは炎症が関連しているかもしれない。
https://www.ncbi.nlm.nih.gov/pubmed/25991443
https://www.ncbi.nlm.nih.gov/pubmed/20099321
AD後期での血清鉄の上昇
MCI、初期アルツハイマー病で観察されるフェリチン濃度の増加とは対照的に、アルツハイマー病の後期では血清鉄の上昇が特徴的である。
フェリチン濃度の上昇はアルツハイマー病の炎症性シグナルと関連している可能性があり、血清鉄濃度の上昇、それぞれ2つの事象は、独立して起こりうることを示唆している。
血液脳関門の破壊
アルツハイマー病患者では、血清フェリチンレベルは、血液脳関門の破壊により脳から露出することによって影響を受けている可能性がある。
https://www.ncbi.nlm.nih.gov/pubmed/19924258
アルツハイマー病患者のヘプシジン障害
アルツハイマー病患者の3倍高いヘプシジン
アルツハイマー病患者のヘプシジンレベルは対照群よりも3倍高い。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5362180/
フェリチンについては有意に異なったが、血清アミロイドβ40、42レベルは低下する傾向にあった。
ヘプシジン調節制御の破綻
アルツハイマー病患者の鉄レベルとヘプシジンレベルの相関関係が喪失しており、ヘプシジンの調節作用が破綻している可能性を示唆する。
これはフェリチンのサブユニットであるH鎖とL鎖の不均衡による可能性がある。
https://www.ncbi.nlm.nih.gov/pubmed/7616228
ヘプシジンとグルコースレベルの相関
血清ヘプシジンと血漿グルコースレベルにも相関があることも見出される。
高い血清ヘプシジンは、アルツハイマー病患者の低血糖症との関連を説明するかもしれない。
https://www.ncbi.nlm.nih.gov/pubmed/17429063
https://www.ncbi.nlm.nih.gov/pubmed/14871914
https://www.ncbi.nlm.nih.gov/pubmed/19815242
https://www.ncbi.nlm.nih.gov/pubmed/18434354
マクロファージは、赤血球からの鉄の再利用、およびフェリチンに鉄を貯蔵するなど鉄ホメオスタシスにおいて重要な役割を果たす。
毛髪ミネラル
AD患者の毛髪は対照群と比べ、有意にセレニウムと亜鉛が低く、銅とマンガンが高かった。鉄とマグネシウムの違いに有意差はなかった。MMSE、性差による違いも有意差はなかった。
https://www.ncbi.nlm.nih.gov/pubmed/26738344
アルツハイマー病患者の毛髪に含まれる微量元素
対照群と比べ亜鉛が有意に低く、マンガン、銅濃度が高かった。鉄とマグネシウムに有意差はなかった。
血清成分の銅、セレン、亜鉛、マグネシウム、マンガン、鉄濃度は認知機能や性別による差はなかった。
https://www.ncbi.nlm.nih.gov/pubmed/26738344
脳鉄蓄積疾患を伴う神経変性疾患(NBIA)
アセロプラスミン血症(CP)
脳内の鉄は主にアストロサイトに沈着、フリーラジカルの産生を促し、脂質過酸化の亢進,ミトコンドリアの障害を引き起こして細胞傷害をきたす。
神経細胞にも鉄沈着はみられるが、ノックアウトマウスの実験から、神経細胞はアストロサイトから鉄が動員されないために、二次性の鉄欠乏による細胞障害が起きている。
脳内の鉄沈着は広範に生じるが,特に基底核,小脳歯状核,視床の鉄濃度が高く,それを反映して不随意運動,小脳性失調,認知機能障害などの神経症状を引き起こす。
脳以外にも全身の組織に鉄の蓄積が生じるため,臓器の重量に対する蓄積量が相対的に多い,甲状腺,心臓,膵臓では障害が起こりやすい。
βプロペラタンパク質関連神経変性(BPAN)
幼少期に運動と認知機能のゆっくりとした発達を示す。青年期、成人期には進行性のジストニア-パーキンソニズム、認知症を発症する。
https://www.ncbi.nlm.nih.gov/pubmed/23176820
COASYタンパク質関連神経変性(CoPAN)
少数の被験者では、早発型の痙縮性失調症を示し、その後下顎ジストニア、構音障害、軸索ニューロパシー、パーキンソニズム、認知障害および強迫行動を発症した。
脂肪酸ヒドロキシラーゼ関連神経変性(FAHN)
典型的には小児の時期に発症し、歩行障害の一因となる皮質脊髄路の関与によってゆっくりと進行する。
FA2H 脂質二重膜の維持,あるいは細胞活動を制御するシグナルとなるセラミドの生合成に関与する Fatty acid hydroxylase の遺伝子
クフォルレーキブ症候群(ATP13A2)
遺伝性のパーキンソニズムとジストニアを中心とした神経症状をきたし、脳内の鉄沈着が認められる疾患 Kufor-Rakeb disease(PARK9)の原因遺伝子
ATP13A2 蛋白質は、ライソゾーム内のpHの維持を行い、脂質代謝において脂質のリサ
イクルに関与している。
ライソゾームは細胞内の血中の小器官、特にミトコンドリアへの鉄供給の役割をもっており、ライソゾームに障害があるとミトコンドリアの鉄代謝に影響を及ぼすと考えら
れている。
糖脂質を分解するライソゾーム酵素、グルコセレブロシダーゼ(GBA)の欠乏による Gaucher 病では、パーキンソニズムを合併しやすく鉄の沈着もみられている。
ミトコンドリア膜タンパク質関連神経変性(MPAN)
MPANの特徴は、ジストニアよりも顕著な痙縮、視神経萎縮症、早期の上部運動ニューロンニューロン所見を伴う運動ニューロンニューロパシー、その後の下部運動ニューロン機能不全の徴候、および成人期までの生存を伴うゆっくりと進行する経過。
その他のNBIAとは異なり、MPAN患者の大多数は進行性の認知機能低下を発症する。
他の所見は、対麻痺または四肢麻痺および神経精神医学的変化。
発症は、一般に、幼児期から成人期前半にかけてゆっくりと進行し、成人期まで生存する。
神経フェリチノパチー(FTL)
フェリチンのL 鎖の遺伝子異常による常染色体優性遺伝疾患
基底核の鉄沈着によりジストニアなどの不随意運動、運動障害、認知機能障害をきたす す。
鉄蓄積はグリア細胞,主にアストロサイトに認められる。
PLA2G6関連神経変性(PLAN)
遺伝性のパーキンソニズムとジストニアを中心とした神経症状をきたし,脳内の鉄沈着が認められる疾患 Early onset PARK14-linked dystoniaparkinsonism(PARK14)の原因遺伝子。
PLA2G6たんぱく質はミトコンドリア内膜のリン脂質代謝に関与し、脂質二重膜の維持を行っていると考えられている。
パントテン酸キナーゼ関連神経変性(PKAN)
PKANを有する小児は3歳前後で歩行異常を発症し、の後進行性ジストニア、構音障害、硬直性、痙縮、反射亢進、および伸筋指徴候を発症する。
https://www.ncbi.nlm.nih.gov/pubmed/12510040
ウッドハウスサカティ症候群(DCAF17)
神経学的所見には、進行性錐体外路系障害、全身性ジストニアおよび限局性ジストニア、構音障害、認知機能低下が含まれる。
内分泌異常には、性腺機能低下症、脱毛症、および真性糖尿病が含まれる。
https://www.ncbi.nlm.nih.gov/books/NBK121988/
https://kenkyuukai.m3.com/journal/FilePreview_Journal.asp?path=sys%5Cjournal%5C20130823104919-74A096DD4AC0AFD0CC13A890BF67F6C4024D9603893B225CC2ABA164FDF7BE90.pdf&sid=738&id=877&sub_id=17433&cid=471
https://www.e-jmd.org/journal/view.php?number=123
脳鉄 蓄積症の原因遺伝子
NBIA関連遺伝子
- PANK2(最も多い)
- PLA2G6
- C19orf12
- FA2H
- ATP13A2
- WDR45
- COASY
- FTL
- CP
- DCAF17
C19orf12
C19orf12遺伝子の突然変異は、ミトコンドリア膜タンパク質関連神経変性(MPAN)を引き起こすことが知られている。
脳鉄蓄積(NBIA)4型障害を伴う神経変性
尿中有機酸、血清アミノ酸、タンデム質量分析、血清銅、血清CP、24時間尿中銅濃度、全血球数、血清鉄、フェリチン濃度、神経伝導検査、眼科評価のすべてが正常であったが、脳の磁気共鳴画像法(MRI)は、大脳基底核への鉄の沈着を示していた(両側淡蒼球でT2低強度)
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5187394/
https://snpedia.com/index.php?title=Special%3ASearch&search=C19orf12&fulltext=1
パーキンソン病
パーキンソン病における鉄関連遺伝子のプール解析 トランスフェリンとの関連https://www.ncbi.nlm.nih.gov/pubmed/24121126
パーキンソン病の鉄恒常性の変化 セルロプラスミン遺伝子、トランスフェリン遺伝子、
https://www.ncbi.nlm.nih.gov/pubmed/26000822
鉄代謝と恒常性に関わる遺伝子
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3643980/
血清鉄増加によるパーキンソン病リスクの減少
疫学研究では血清鉄の増加はパーキンソン病リスクを減らす。
保護効果の仕組みは不明だが、鉄はチロシンヒドロキシラーゼの重要な補因子であり、ドーパミン合成に必要なため、鉄欠乏はニューロンの酵素、受容体の機能低下、ドーパミン作動性の機能低下に寄与する可能性がある。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3672214/
レビー小体型認知症
レビー小体型認知症、死後の脳組織には健常者より銅が少なく鉄が多かった。
https://www.ncbi.nlm.nih.gov/pubmed/25024342