COVID-19 Genetic and Environmental Risk Factors: A Look at the Evidence
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7577231/
要旨
COVID-19パンデミックは、間違いなく21世紀最大の健康危機である。この病気はコロナウイルス科のウイルスによって引き起こされ、重症急性呼吸器症候群(SARS)の原因ウイルスと密接に関連している。2019年12月以降、このウイルスは最初に記録された症例の場所(中国・武漢市)を超えて広がり続けている。現在までに、世界で500万人以上の症例が診断され、30万人以上が死亡している。COVID-19の患者さんは呼吸器症状に苦しみ、一部の患者さんでは急速に急性呼吸窮迫症候群(ARDS)に移行する可能性がある。
現在、多くの薬剤やワクチンが臨床試験中であるが、現在承認されている治療法やワクチンはない。したがって、高感受性群の症状悪化につながる危険因子を正しく特定することが重要である。
リスクの高いグループには、55歳以上の人、特に心血管疾患などの基礎疾患を持つ人が含まれる。アフリカ系アメリカ人のような特定の民族はリスクが高いことがわかっており、男性は症例の数だけでなく重症度も高いようである。これらのグループは、その分子構造がウイルスの感染や増殖をより許容しやすいため、リスクが高いという仮説が立てられている。異なる職業、特にヘルスケア関連の職業やマスク着用文化を持たない集団は、環境曝露によりリスクが高くなる。
この論文では、本疾患に対してより感受性の高い異なる集団に関するエビデンスを検討し、COVID-19の感染と予後に関連する仮説を検討する。また、COVID-19感染の分子景観に関連しうる危険因子や、環境や職業的条件に関連した危険因子についても議論する。
キーワード
COVID-19,SARS-CoV-2,感染、リスク因子、分子的素因、環境・職業曝露
序論
コロナウイルスは、ウイルスの外側に王冠のようなトゲが存在することから、コロナと名付けられている(Ouassou et al 2020)。コロナウイルス(CoV)は、確定的なポジティブセンス一本鎖RNAゲノムを有するエンベロープされた非分割ウイルスである(Arabi et al 2020;Chen J.このウイルスのファミリーは、常にヒトおよび他の哺乳類に広く分布する非致死性病原体のファミリーと考えられてきた。通常、それらは、一般的な風邪の症例の15%を引き起こす原因となっていた(Yi et al 2020)。過去20年間で、重症急性呼吸器症候群(SARS)を引き起こす重症急性呼吸器症候群関連コロナウイルス(SARS-CoV)が、死亡率10%で中国に出現した(ファウチ et al 2020)。別のCoVである中東呼吸器症候群関連コロナウイルス(MERS-CoV)は、サウジアラビアで2012年に死亡率37%でパンデミックした(Huang er al)。
これまでに既に同定されたコロナウイルスは氷山の一角に過ぎないかもしれず、今後さらに新規で重篤な人獣共通感染症イベントが明らかになる可能性がある(Wang C. et al 2020a)。このレビューでは、COVID-19の伝播の様々な傾向、SARS-CoV-2ウイルスの遺伝的景観を要約し、その病原性と伝播性に影響を与える要因に関する現在の証拠の詳細な分析を行う。
SARS-COV-2年表
2020年1月25日頃、新型ウイルスによる肺炎患者が相次いで発生し、中国政府は留守番警告を発令した(Yi er al)。 入院した肺炎感染者5人の気管支肺胞洗浄液と咽頭スワブからウイルスゲノムの塩基配列を取得したところ、全員から新規のβ-CoV株が検出され、国際ウイルス分類委員会(IVCC)により「SARS-CoV-2」と命名された(Yi er al)。 このパンデミックは中国の武漢で始まり、瞬く間に中国全土、そして世界100カ国以上に広がった(Wang et al 2020a)。SARS-CoV-2の軌跡におけるいくつかのマイルストーンを図1に示す(Peng et al 2020; Yi et al 2020)。世界保健機関(WHO)が2020年5月15日に報告した世界的な現状を図2に示す(Livingston er al)。
図1 COVID-19発生時に発生した主な出来事の年表
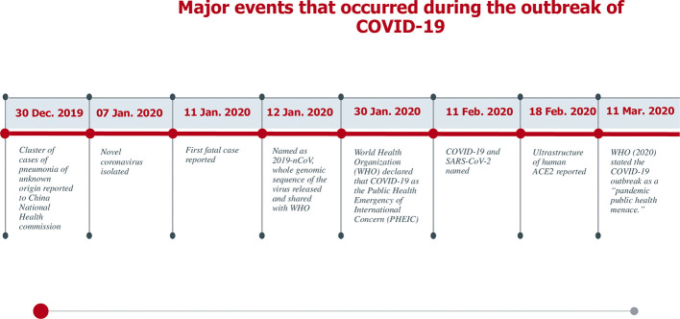
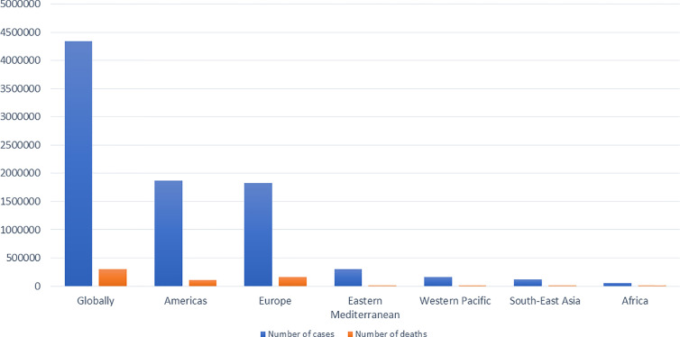
図2 2020年5月15日にWHOが報告した現在の状況
COVID-19 臨床像・診断・治療プロトコル
発熱、倦怠感、下痢、および乾いた咳を含む、前駆期の2019-nCoV感染に起因する症状は、最も一般的な症状であるが、非特異的である(Huang et al 2020)。上気道症状は他のヒトコロナウイルス感染症とは異なり、異常な所見であった(Repici et al 2020)。COVID-19の最初の41人の患者の臨床所見を報告した研究では、リンパ球減少症を含む6つの一般的な臨床検査所見が観察され、胸部CTスキャンにおける末梢両側のグランドガラスの不透明性または圧密性である最も特徴的な放射線学的所見が観察された(ファウチ et al 2020)。これらの臨床所見は、人口の間で循環している他の継続的な風邪やインフルエンザとは対照的に、感染例の早期発見に大いに役立った。華南海産物卸売市場への暴露履歴は、しばらくの間は重要な手がかりとなっていたが、より多くの二次および三次症例が発生するにつれてその価値を失った(Huang et al 2020)。現在では、この病気が伝染性の急性呼吸器疾患であり、キャリアー宿主との直接接触、その感染した飛沫、または他の呼吸器分泌物のいずれかによって感染することが知られている(Patel et al 2020)。
COVID-19の重大性に寄与する理由の1つは、潜伏期間が通常1日から14日であるため、潜伏期間中に急速に拡散する能力である(Guo et al 2020)。米国疾病対策センターは、COVID-19患者の間で示された一般的な症状は、発熱、咳、および呼吸困難であると述べている。軽度の場合、症状は軽度の発熱、喉の痛み、頭痛、倦怠感、乾いた咳などであった。その後、中等症になると呼吸困難が出現して症状が悪化する。重症になると、患者は発熱、毎分30回以上の呼吸数に達するタキプネア、呼吸困難などの症状を呈するようになる。より不幸な状態では、重症患者は急性呼吸窮迫症候群または敗血症性ショックのいずれかに苦しんでおり、死亡のリスクを高めることになる(Cascella et al 2020)。定量的リアルタイムポリメラーゼ連鎖反応はSARS-CoV-2感染症の診断のための基準となる方法であり、抗体検出のための血清学的アッセイも使用されることがあるが、それらは感染時期によって感度が異なる(Mathuria and Yadav, 2020)。放射線検査は状況を評価するための補助的なツールではあるが、決して診断的なものではない。これは、X線撮影の感度が限られており、多くの患者がCTスキャンで有意な所見を示さないという事実に起因している。しかし、いくつかの症例で共有されている特徴的なX線画像特徴は、胸部CT上でのグラウンドグラス不透明性と両側性のパッチ状のシャドウイングである(Cascella et al 2020;Guo et al 2020;Hassan et al 2020;Wang et al 2020a)。
昨年1月、WHOは、以前のヒトコロナウイルスパンデミックで踏襲されたプロトコルに基づいたガイドラインを発表し、より重症な症例において体外膜酸素療法を提供する必要性とともに、早期のモニタリングおよび支持的パラダイムについて議論した(Cascella et al 2020)。いくつかの研究では、レムデシビル、リバビリンまたはアビドールなどの抗ウイルス薬の投与が示唆されている。レムデシビルの使用はRNAウイルスの感染を抑制することが明らかになったが、3種類以上の薬剤を同時に摂取することは好ましくないことを付け加えておくことが重要である(Wang et al 2020a)。2020年5月1日、米国食品医薬品局(FDA)は、入院中の成人及び小児における重症COVID-19(確認済み又は疑われる)に対する本剤の緊急使用を認めるため、レムディビルの緊急使用許可(EUA)を発出した(O委員 2020a)。
クロロキンはマラリアの治療薬であり、試験管内試験でSARS-CoV及びMERS-CoVに対して有効な抗ウイルス作用を有することが報告されていた。そのため、COVID-19症例では、病状の悪化を抑制し、ウイルス抑制作用があることが示唆されたため、使用されていた(Ahn et al 2020)。しかし、最近撤回された96000人以上のCOVID-19患者を対象とした研究では、混乱が生じた。Mehraらは、COVID-19の治療に使用した場合、クロロキンおよびヒドロクロロキンの投与による利益は見られなかったと結論付けている。それどころか、それらの使用は、心室性不整脈の発生率を増加させることさえあった(Mehra et al 2020)。最後に、臓器支持は、併存疾患に罹患している患者の臓器損傷および崩壊のリスクを防ぐために不可欠である(Hassan et al 2020)。COVID-19の様々な症状のため、すべての症例が人工呼吸または挿管を必要とするわけではない。酸素療法介入を必要とする重篤な合併症は、急性低酸素血症呼吸不全または急性呼吸窮迫症候群(ARDS)である。いくつかの研究では、疾患の初期段階では患者を臥位にした状態で人工呼吸を行うことが推奨されている。この方法は、重症ARDS症例での死亡率を低下させると考えられる(Guérin et al 2013)。換気モードが他のモードよりも効率的であるという十分な証拠はないが、高周波振動換気の利用はエアロゾルの発生につながる可能性があるため好ましくない。挿管はCOVID-19の治癒を保証するものではない。例えば、昨年3月に武漢では挿管された患者22人中19人が死亡した。Shoemakerらによる以前の研究では、48時間以内の酸素負債の蓄積を防ぐことと、患者の生存の可能性が高くなることとの間に密接な関係が説明されていたので、この死亡は判断の遅れによるものである可能性が示唆された(Shoemaker et al 1992; Meng et al 2020)。
コロナウイルスは、ニドウイルス科の中で最大の属と考えられている(Fehr and Perlman, 2015)。長年にわたって、世界的に検出されたヒトコロナウイルスの7つの株があった。229EおよびNL63はアルファ型の例であり、HKU1,OC43,SARS、MERS、および新規なCOVID-19はベータ型を表す(Ibrahim er al)。 これらの同定された株はいくつかの共通の特徴を共有している:それらは27から32kbの長さであり、ポジティブセンスであり、伝染性であり、エンベロープされたRNAウイルスである。これらの基準と相まって、それらが構造的タンパク質および非構造的タンパク質を含むことが認識された。これらの構造タンパク質の中には、アンジオテンシン変換酵素2(ACE2)受容体と結合してウイルスの宿主細胞への侵入を促進するために不可欠なスパイクタンパク質(S)が含まれている。Sタンパク質は、ウイルスの悪性度を決定する重要な因子の一つである。また、Sタンパク質の他にも、ウイルスのゲノムを詰め込んだカプシドを形成するヌクレオカプシド(N)タンパク質、ウイルスのエンベロープを形成する膜(M)とエンベロープ(E)タンパク質があることが明らかになった。最後に、ウイルスの中には、エンベロープに関連したヘマグルチニンエステラーゼ(HE)タンパク質が含まれている可能性があることも明らかになった。一方、非構造タンパク質(NSP)には、NSP3,NSP5,NSP12が含まれている(Li, 2016)。株のタンパク質配列に関する慎重な研究の結果、現在、新興のSARS-CoV-2についての理解が深まっている(Li, 2016; Ibrahim et al 2020)。データは、SARSおよび他のヒトコロナウイルスが自然界に根強く存在し、動物をリザーバーとして利用し、循環し、その株を進化させ、何年にもわたって小規模な規模で病気の大発生を引き起こしていたことを示唆している(Graham and Baric, 2010)。
ワクチンは便利な治療法であるにもかかわらず、過去数十年の間に発見されたコロナウイルスの治療や予防のために開発されたワクチンはなかった。そこで、新世代と考えられているmRNAワクチンのようないくつかのアプローチが慎重に研究されていた。一般的に、mRNAワクチンは免疫反応が高いため、従来のワクチンよりも好ましいとされている。現在、COVID-19のSタンパク質をコードするmRNAワクチンの開発に臨床試験が集中している。もう一つのアプローチは、サブユニットワクチンである。サブユニットワクチンは、ウイルス成分を導入することなく宿主の免疫応答を高めるため、非常に安全性が高い。そのため、「分子クランプ」は、抗原の同定を強化し、広範囲のエンベロープされたウイルスに対する免疫を高めるポリペプチドを開発するための試験である。他のモダリティとしては、T細胞の活性化を高めるDNAワクチンや、ウイルス特異的な抗体を導入する方法である抗体依存性増強(ADE)に注目が集まっていた。試験管内試験では、MERS-CoVおよびSARS-CoVでADE試験が成功した(Ahn et al 2020)。しかし、当面はウイルスの隔離、対症療法、栄養価の高い食事、酸素療法が第一の治療ラインとなる。
COVID-19の分子景観
ゲノムの特性評価
前述したように 2019年までにヒト感染症を引き起こすことができるコロナウイルスは6株検出されており(Cui et al 2019年)そのうち、感染力が強くなく、軽度の呼吸器感染症のみを引き起こすことができるヒトコロナウイルスは4株であり、これらにはHCoV-OC43,HCoV-229E、HCoV-NL63,およびHCoVHKU1が含まれる(Cui et al 2019)。一方、他の2つのコロナウイルスは、SARS-CoV-1(Zhong et al 2003)およびMERS-CoV(Zaki et al 2012)である。2003年には、SARS-CoV-1は8,000人以上の患者を生み出し、26カ国で800人近くの関連死をもたらした。さらに 2012年には、MERS CoVは、サウジアラビアでの約860人の関連死を含む約2500件の症例をもたらした(Cui er al)。
中国がCOVID-19のアウトブレイクを宣言した直後、彼らは9人の入院患者からサンプルを分離し、そのうちの8人が武漢のウェットマーケットを訪れたばかりの患者からサンプルを分離することで、そのゲノム配列の解析を開始した。第二世代シークエンシングを行うために患者から気管支肺胞洗浄液を採取し、完全長ゲノム解析のためにサンガーシークエンシング法を用いてウイルスセグメントを採取した(Lu et al 2020)。その結果、収集されたサンプルでは、分離された完全ゲノム全体の配列同一性は99.98%以上であり、ウイルスがヒトに新たに出現したことを示していた。2つの部分単離されたゲノム(WH02およびWH19002)も同様に配列決定されており、その結果、それらは完全ゲノムとほぼ100%の類似性を示した(Lu et al 2020)。Luらは、新しいSARS-CoV-2は、バット-SL-CoVZC45およびバット由来の別のSARS様β-コロナウイルスであるバット-SL-CoVZXC21と密接に関連していると結論付けた。科学的文献に沿って、これらの研究結果は、SARS-CoV-2がコウモリ由来であり、分子レベルで96%同一であることを支持している(Lu et al 2020)。所見はまた、SARS-CoV-2株は、SARS-CoV-1株(約79%)およびMERS-CoV株(約50%)と比べて分子レベルでの同一性が低いことを明らかにした。ほとんどのコードされたタンパク質は、SARS-CoV-2株とコウモリ由来のコロナウイルスとの間で有意な同一性を示したが、スパイクタンパク質は約80%、タンパク質13は73.2%の同一性しか示さなかった(Lu et al 2020)。
SARS-CoV-2およびβコロナウイルス属の関連ウイルスの系統解析は、SARS-CoV-2がサルベコウイルス亜属に属する新規なβコロナウイルスであることを支持する。さらに,SARS-CoV-2はSARS-CoV-1とは系統的に異なっていた。最近の研究では、異なる宿主由来のCoV間で進化的な組み換えや選択パターンが存在する可能性が示されており、種を超えた感染がSARS-CoV-2の出現につながった可能性がある(Li X. et al 2020)。SARS-CoV-2の起源とそのゲノムの特徴は、異なる宿主種における選択パターンの解明とともに、コウモリとパンゴリンを攻撃するウイルス間の先祖代々の再結合から進化した可能性がある(Li X. er al)。
COVID-19感染の分子機構
コロナウイルスは、病原性の際に宿主細胞膜とウイルス膜の融合を媒介する際に、コロナウイルス表面のエンベロープ上のスパイクタンパク質であるS糖タンパク質を利用して宿主細胞に付着する(Li, 2016)。S糖タンパク質は、S1とS2の2つの領域から構成されており、S1は受容体結合のための領域、S2は膜融合のための領域である。S1領域は、N末端ドメインと3つのC末端ドメイン、CTD1,CTD2,およびCTD3を含む(Gui er al)。 SARS-CoV-1のRBDは、S1領域のCTD1に配置されている。したがって、SARS-CoV-1がヒト宿主細胞に付着するためには、まず、RBDとアンジオテンシン変換酵素IIの相互作用が活性化される必要がある(図3)(Song et al 2018)。SARS-CoV-2は、2つのウイルス間の高い相同性により、SARS-CoV-1と同様のメカニズムを利用してヒト細胞に感染することが期待されている(Wan er al)。
図3 SARS-CoV-2の受容体結合機構の模式図
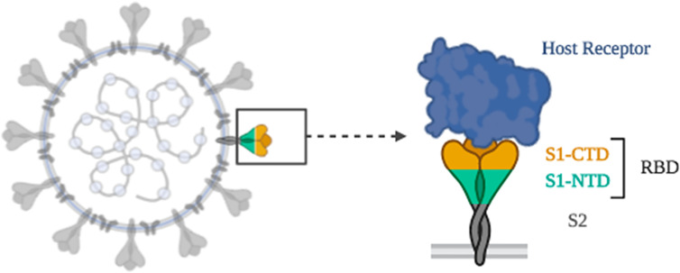
研究により、予測されたSARS-CoV-2のRBDとアンジオテンシン変換酵素IIの複合体は、SARS-CoV-1のRBD-ACE2複合体構造に近接していることが示された。さらに、SARS-CoV-2のRBDは、SARS-CoV-1と同じ位置のACE2受容体に結合している(He et al 2020)。SARS-CoV-1とSARS-CoV-2の両方でRBD-ACE2複合体が形成される方法についての洞察を得るために、MDシミュレーションを用いた。SARS-CoV-2は、SARS-CoV-1(-36.75 kcal/mol)よりも低い結合自由エネルギー(-50.43 kcal/mol)を有しており、SARS-CoV-2はSARS-CoV-1よりも高い親和性でACE2を結合していることを意味している。これらの結果から、SARS-CoV-2は前身のSARS-CoV-1よりも病原性が高いことが明らかになった。
研究者は、ACE2とSARS-CoV-2のSタンパク質との相互作用を研究し、理解することで、この相互作用がCOVID-19の必須条件であると考えられていることから、治療法の可能性を考え出すことに興味を持っている。レニン-アンジオテンシン-アルドステロン系(RAAS)は、ヒトの生理学における重要なプロセスを組み立てる血管作動性ペプチドの特徴的なカスケードである(Vaduganathan er al)。 SARS様CoVは、RAASの活性化に対抗するACE2を介してRAASと相互作用する。したがって、研究者は、進行中のCOVID-19パンデミックをもたらす可能性のあるACE2の発現に対するRAAS阻害剤の効果を観察しようとしてきた。実験動物モデルでは、ARBがACE2に及ぼす影響に関して一貫性のない結果が示されている;ある研究ではARBによるACE2のmRNA発現の増加が示されたが、他の研究ではARBがACE2発現に影響を及ぼさないことが示された(Vaduganathan et al 2020)。ヒトを対象として実施されたいくつかの研究に関して、ある研究では、冠動脈疾患患者におけるACE阻害剤の静脈内投与がアンジオテンシン-(1-7)の産生に影響を及ぼさないことが示されたが、これは、ACE阻害剤がACE2誘導アンジオテンシンII代謝に直接的な影響を及ぼすかどうかに疑問を投げかける所見である(Campbell et al 2004)。
心血管疾患の患者を対象とした別の横断的研究では、ACE阻害薬またはARBを服用した患者の血漿ACE2の活性は、未治療の患者と比較して高くないことが示された(Vaduganathan et al 2020)。これらの観察は、ACE阻害剤とARBがアンジオテンシンIIに及ぼす異なる効果を調べることによって説明されるかもしれない;それらの活性部位は異なっており、ACE阻害剤はACE2発現に直接影響を及ぼさない(Rice et al 2004)。
さらに、ACE阻害薬を含む以前の治療は、ある研究でACE2の腸内mRNAの上昇と相関していた;しかしながら、この所見はARBでは示されなかった;肺のACE2発現に対するRAAS阻害薬の効果に関しては、利用可能なデータはない(Vuille-dit-Bille et al 2015)。したがって、これらの結果がヒトに翻訳されるかどうかを決定するための正確なデータは得られておらず、COVID-19患者におけるRAAS阻害剤の役割を調査するためにさらなる研究が必要である;また、他の受容体がSARS-CoV-2のヒト宿主細胞への侵入に関与している可能性がある。
スパイク変異とより伝染性の高いSARS-CoV-2の出現
研究者たちは最近、Sタンパク質を標的とする可能性のある突然変異を追跡することで、SARS-CoV-2のより持続性の高いバージョンを生み出すことに関心を寄せている。Korberらは、Global Initiative for sharing All Influenza Data(GISAID)を用いて、SARS-CoV-2のSタンパク質の変化と進行を追跡するための解析パイプラインを実施し、ウイルス表現型または抗原性のいずれかの変化とともに「陽性選択」を示す可能性のある遺伝子変化の数の変化をより広いコミュニティに警告することを目的としている(Korber et al 2020)。突然変異スパイクD614Gは、3月上旬に検出された緊急の懸念の最初の部位であった;それは、183個のサンプリングされた配列において7回観察された;最初のD614G染色体のうち4個は、ヨーロッパで検出され、1個はメキシコで検出され、1個はブラジルで検出され、1個は武漢で検出された(図4A)。D614G変異は、別の2つの変異、1つのサイレント変異(nsp3遺伝子におけるC-to-T変異)およびRNA依存性RNAポリメラーゼ(RdRp)アミノ酸修飾をもたらすC-to-T変異に続いた(Korber et al 2020)。つの突然変異の組み合わせは、「Gクラッド」と呼ばれ;そしてヨーロッパで最初に出現した。月中旬に、第2の報告では、Gクラードが広がり始め、世界中のサンプルの29%に存在していたことが明らかになった;しかし、まだ主にヨーロッパで発見された(Korber et al 2020)。4月上旬、別のサンプルでは、G614の頻度がスパイラルしていることが示された;さらに、G614バージョンが出現し、数週間でヨーロッパと中国で支配的なバージョンになった(図4B)。アフリカや南米でのD614の伝播に関するデータは、まだサンプル数が少ない。したがって、D614G突然変異は、中国で最初に発見された系統からの単一の祖先に由来している可能性がある。さらに、D614Gの突然変異については、3つの異なるパターンが観察されている。
図4
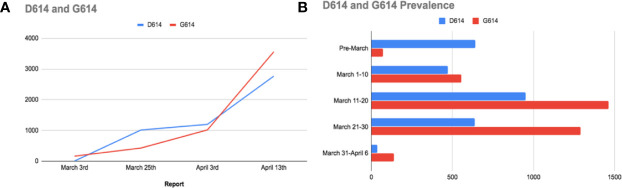
A)世界的なD614とG614の普及状況の比較。B)中国における元祖D614変異の有病率と、G614変異の出現(主にヨーロッパ)を表した棒グラフ。
- 同系統に属していると思われる変異(イギリスやオーストラリアではP1263L。 アイスランドではA831Vも)。
- 様々な地域に存在し、世界的に散在している変異(L5F
- 同じ地理的領域に属する突然変異;しかし、それらは異なる系統で発生する(S943P、ベルギーでのみ存在)。
これらの最近の発見は、SARS-CoV-2ゲノムが突然変異を受けていることを示しており、KorberらはSタンパク質にも13の変異を検出しており、D614Gはそのうちの1つに過ぎないことを示している。彼らはさらに、D614Gが感染の増加と関連している理由を説明する可能性のある2つの理由を特定した;第1の理由は、D614のユニークな構造とSタンパク質プロモーター上の配置である;したがって、それは近くのプロモーターと容易に通信することができる(Korber et al 2020)。驚くべきことに、SARS-CoV-2のスパイクタンパク質における突然変異は、コンフォメーションの変化を課し、ウイルス抗原性を変化させ、そして伝達性に影響を与え、これは、いくつかの国でのより高い死亡率を説明することができる(Eaaswarkhanth et al 2020)。D614の変異が伝達に影響を及ぼす可能性がある第二の方法は、D614がSARS-CoVのネイティブSタンパク質中の免疫優勢抗原性決定因子に打ち込まれていることである;このエピトープは、ネイティブSARS-CoVから回復した患者で発見された抗体によって認識される。さらに、Wangらは、この抗原は霊長類ではワクチンによって攻撃されると述べている。したがって、このエピトープは、感染者の「保護的なD614指向の抗体反応」に対する抵抗性を獲得した可能性があり、その結果、D614からG614への出現は、感染者を再感染させやすい状態にしている可能性がある。この遺伝子進化は、抗体応答およびConvalescent Plasma Transfusion(CPT)にD614Gが課した変化を理解する上で極めて重要である(Korber et al 2020)。
危険因子としての遺伝的/分子的素因および基礎条件
性別の違い
COVID-19の分布と有病率について議論する様々な研究が発表されている。COVID-19の伝播に関するより興味深い観察の一つは、ウイルスが男性に多く発現しているように思われるという事実である。あるアジアの研究では、ACE2受容体は女性よりも男性の方がはるかに多く発現していることがわかった(Zhao er al)。 中国で行われた別の研究では、140人の患者の集団における本疾患の性別分布は同じであったが、重症患者のサブグループではほとんどが男性であったことが示されている(Zhang J.-J. er al)。 中国からの別の報告では、552の病院のデータを網羅しており、患者の半数以上が男性であることが示されている(Guan er al)。 最後に、1000人以上の中国の症例データを調査した別の研究では、男性は重症度が上がると女性よりも2倍以上高い死亡率になることが示された(Jin er al)。
これらの観察結果を見ると、データは男性にCOVID-19の素因があることを示しているように思われる。この素因の理由を支持するいくつかの仮説があり、最初の仮説は、喫煙が女性よりも男性に多く見られるため、喫煙が関与している可能性があるというものである(Shah et al 2019)。注目すべきは、単一の研究では、ACE2は通常、すべての異なる民族、性別、および年齢層の間で同じレベルで発現していることが示された(Smith er al)。 しかし、この研究では、喫煙者はACE2の発現レベルがはるかに高いようであった。現在の文献では、喫煙がCOVID-19への感染の有意な素因因子として支持されていないため、この証拠は性の素因を完全に説明するのに十分ではない。中国で実施された2つの研究(Zhang J.-J. et al 2020;Guan et al 2020)は、それぞれ、研究集団の中の喫煙者の数が非常に少なく、これは中国の人口自体の中の喫煙者の数と不釣り合いであった。現在のところ、喫煙とCOVID-19の素因との間の強い関連を支持する具体的な証拠はない。
(Fagone et al 2020)が行った研究では、ネットワーク解析などの計算機的手法を用いて、一度ウイルスに感染すると細胞内で実際に何が起こるのかを解明した。著者らはまた、病気との戦いに役立つ可能性のある新しい治療薬や再利用されたものを予測した。特に注目されたのは、感染した細胞のウイルス感染によって誘導される転写シグネチャを男女で比較することであった。健常者の肺組織のトランスクリプトームプロファイルを、ウイルス感染した組織のトランスクリプトームプロファイルと比較検討した。注目すべきは、40~60歳の女性のトランスクリプトームプロファイルは、SARS-CoV-2感染組織のトランスクリプトームプロファイルと非常に類似していたことである。この類似性は、男性よりも女性のトランスクリプトームプロファイルで顕著であった。著者らは、このプロファイルが、その年齢の女性における急性反応のより高い閾値につながると予測した。しかし、この仮説が正しいと結論づけるには時期尚早である。この関係を分析するためには、疫学的データのレビューと試験管内試験試験の両方がさらに必要である。
更年期障害に関連する女性特有のホルモンが、トランスクリプトームプロファイルのこの違いの理由である可能性がある。本研究では、COVID-19誘導遺伝子のうち2つの遺伝子(好中球化学戦術因子CXCL1および優勢な樹状細胞化学戦術因子CCL20)がアンドロゲン受容体による制御を受けることが明らかになった。他の2つの遺伝子は、エストロゲン受容体(ER)によって制御されていることが明らかになった。アンドロゲン受容体は、特にマクロファージおよび好中球のリクルートにおける免疫系の調節に関与している;COVID-19感染に大きく関連している2つのタイプの細胞(Zhang w. et al 2020)。CXCL1およびCXCL2は、COVID-19ウイルスへの曝露によって重く関与し、変調されているようである。この変調は、性別間で異なる可能性があり、感染の転帰に影響を与える可能性がある。さらに、エストロゲン受容体は免疫、特に抗ウイルス反応に大きく関与しており、ERモジュレーターが治療薬として提案されている点でも、エストロゲン受容体モジュレーターは免疫に大きく関与している。選択的エストロゲン受容体モジュレーター(SERMs)(トレミフェンやエクイリンなど)は、ウイルス侵入後の段階で干渉し、ウイルス膜とエンドソーム膜の融合の引き金に影響を与えることから、特に示唆されている(Kovats, 2015)。
COVID-19感染、重症度、および死亡率における観察された性差の決定論的なものであると疑われるもう一つの要因は、TMPRSS2の発現の違いが疑われることである(Hoffmann et al 2020)。SARS-CoV-2は、細胞内に入るために、ACE2受容体とTMPRSS2に付着し、タンパク質のプライミングを行う。TMPRSS2は、腎臓、前立腺、小胞、および管腔で深く発現している(Vaarala et al 2001)。理論的には、男性と女性の間でのTMPRSS2の発現の違いは、男性のCOVID-19関連死亡リスクの増加につながる素因因子として機能する可能性がある。しかしながら、これまでのところ、これらの主張を裏付ける証拠はほとんど提示されていない。ウイルスの精液感染の可能性を分析した研究では、その可能性は非常に低いことがわかった。それにもかかわらず、この研究に参加した患者の19%が陰嚢の不快感を症状の一つとして報告しており、精巣組織への損傷の可能性を示唆している(Pan et al 2020)。
民族性
COVID-19の病因に大きな影響を及ぼす凝固の役割を示唆する仮説は、異なる人種および民族間の違いを見るためにさらに検討された(Fogarty et al 2020;Zhou F. et al 2020)。血栓性リスクは人種および民族間で異なるため、研究は、アフリカ系アメリカ人は白人集団よりも高いリスクにあり(Huang et al 2019)中国人集団は白人集団よりも約3〜4倍低い静脈血栓塞栓症リスクを有することを示している(Liao et al 2014)。アイルランドで行われた白人患者の凝固を調べた研究では、観察されたデータは、凝固障害とCOVID-19疾患の重症度との間に有意な関係を示した(Fogarty et al 2020)。凝固活性は、肺線溶の増加に加えて、Dダイマーのレベルの増加を伴って明らかであった。したがって、血栓症のリスクが高い人種とCOVID-19の病態と凝固障害との関係は、それらの人種がCOVID-19による死亡率に影響を受けやすい可能性を示していると考えられる(Fogarty et al 2020)。
シカゴでは 2020年6月11日の時点で、報告されたCOVID-19陽性例のうち29.8%がアフリカ系アメリカ人であり、死亡例の44.7%が同様にアフリカ系アメリカ人であった(Shah et al 2020)。アフリカ系アメリカ人はCOVID-19関連の死亡率および罹患率が高い(Krishnan et al 2020)。これは、アフリカ系アメリカ人が低所得で医療施設へのアクセスが悪い人口密度の高い地域に住んでいることが原因である可能性がある(Shah et al 2020)。さらに、ACE2とTMPRSS2の遺伝子発現の増加がCOVID-19の症状の重症度の増加に関連していることを調べた研究では、アフリカ系アメリカ人はACE2とTRPSS2の遺伝子発現が増加し、COVID-19感染症のリスクが高くなることが示されている(Peters et al 2020)。
さらに、CDCによると、入院患者の33%が黒人であるのに対し、8%はヒスパニック系である(CDC, 2020a)。死亡率が最も高いのは黒人で92.3人/10万人、ヒスパニック系で74.3人/10万人となっている。少数民族は人口密度が高く、医療へのアクセスが困難な地域に住んでいる傾向があることなど、いくつかの要因が考えられる。彼らの多くは、有給の病気休暇がなく、医療保険にも加入していない本質的なサービス業に従事している。
小児におけるCOVID-19の感染率の低下
世界的に見ても、報告されている小児のCOVID-19症例数は大人の症例数よりも大幅に少ない(El-Shabrawi and Hassanin, 2020; Hossny and El-Owaidy, 2020)。2020年1月20日は、中国の深センでSARS-CoV-2感染症の最初の小児確定症例が報告された日であり、1月31日までに20例の小児症例が報告されるまでにエスカレートした。その後、世界各地で複数の小児症例が発表された。しかし、COVID-19の小児の臨床的・疫学的パターンは、依然として非常に不明確である(Tezer and Bedir Demirdağ, 2020)。
中国で実施された366人の入院小児を対象とした呼吸器感染症のレトロスペクティブ研究によると、COVID-19への感染はパンデミックの初期に起こり、重篤な呼吸器感染症を引き起こしていた(Liu er al)。 小児症例のほとんどは、成人患者の疫学的なつながりを持つ家族クラスター症例であった(Rasmussen et al 2020)。小児のCOVID-19症例の多くは成人に比べて咳や発熱の報告が少なく軽度であるにもかかわらず、中国のデータから得られた同様の知見に基づいて、この年齢層では重篤なCOVID-19疾患がまだ起こり、入院につながる可能性がある(CDC COVID-19対応チーム 2020)。中国のCOVID-19陽性確定症例に関する最大規模の調査結果では、2歳から 19歳の小児が確定症例44,672例の2%を占め、診断時の年齢が10歳未満の症例が0.9%を占めていることが示されている(Ludvigsson, 2020)。同様に、3月に発表されたイタリアのデータでは、イタリアの陽性症例22,512例のうち、子どものCOVID-19症例は1.2%にすぎないと報告されている(Ludvigsson, 2020)。さらに、それに対応して韓国のCDCは、3月20日までに確認されたCOVID-19症例のうち6.3%が19歳以下の小児であったのに対し、米国では2020年3月までに報告された4,226例のうち5%が小児であったと発表している(Ludvigsson, 2020; Brodin, 2020)。初期の証拠に基づいて、COVID-19に対するヒトの感受性は、逆説的に、喘息やアレルゲン過敏症などの個人のアレルギー疾患のレベルが上がるにつれて低下する(Abrams and Szefler, 2020)。さらに、利用可能な証拠は、年齢とCOVID-19重症度との間に逆の関係を提案しており、乳児のCOVID-19死亡率に対する脆弱性が高いことを示唆している(Hagmann, 2020)。いくつかの研究では、大多数の小児は1〜2週間の回復期間を有する中等度のCOVID-19疾患症状を呈するようであるが、心血管疾患、慢性肺疾患(喘息を含む)免疫抑制などの基礎疾患を有する小児は、COVID-19でより重篤な症状を呈するリスクが高いことが示唆されている(Tezer and Bedir Demirdağ, 2020)。
小児におけるCOVID-19の病態に関する利用可能なデータは限られているにもかかわらず、様々な大規模な疫学研究は、小児における疾患発現の重症度が成人よりも低いことを示唆している(Brodin, 2020)。現在の国際的な証拠は、小児は成人に比べて軽度のCOVID-19症状を有する可能性が高いことを示している。咳および発熱は、成人よりも消化器症状を報告する可能性が高いと思われる小児の最も一般的な症状であり続けている。軽度の疾患または臨床症状の欠如が、ほとんどの国が成人に比べて小児の症例の検出数が相対的に少ない理由に寄与している可能性がある(El-Shabrawi and Hassanin, 2020; Hossny and El-Owaidy, 2020)。
軽度の小児のCOVID-19感染の背後にある理論的根拠は依然としてつかみどころがなく、図5に要約されているように複数の仮説が存在する。主に、大人と子供の免疫系は、その機能的応答性および構成に関して互いに異なる。さらに、10代、未就学児、乳児の免疫系にも違いがある。例えば、新生児は劇的な変化を受け、広範囲の外部環境曝露にさらされる(Brodin, 2020)。さらに、最初の数ヶ月間の乳児は、年長児には存在しないいくつかの母体抗体を持っている。小児と成人との間のCOVID-19ウイルスに対する応答の質的な違いは、小児におけるCOVID-19疾患発現の重症度が低いことの一つの可能性のある説明を提供するかもしれない(Brodin, 2020)。小児における肺および気道の粘膜における複数の同時多発ウイルスの身近な存在は、ウイルス間の直接的な競合および相互作用によってSARS-CoV-2の増殖を減少させる可能性があり、COVID-19の重症度とウイルスコピー数との間の可能性のある関連を示唆する現在のパンデミックデータと一致する可能性のある説明も提供する(Brodin, 2020)。さらに、SARS-CoV-2ウイルスの軽症児感染の別の信憑性のある理論は、SARS-CoV-2ウイルスの結合および感染のために必須であるACE2受容体の発現変動である。ACE2受容体は免疫細胞ではなく、腸や気道、肺で発現している。成人に多く見られる高血圧の治療では、ARBsやACE阻害剤を用いてACE2の発現を誘導し、そのレベルの上昇が成人におけるSARS-CoV-2感染の影響を悪化させる可能性を説明している(Brodin, 2020)。
図5 小児におけるCOVID-19感染の軽症化のために考えられる仮説
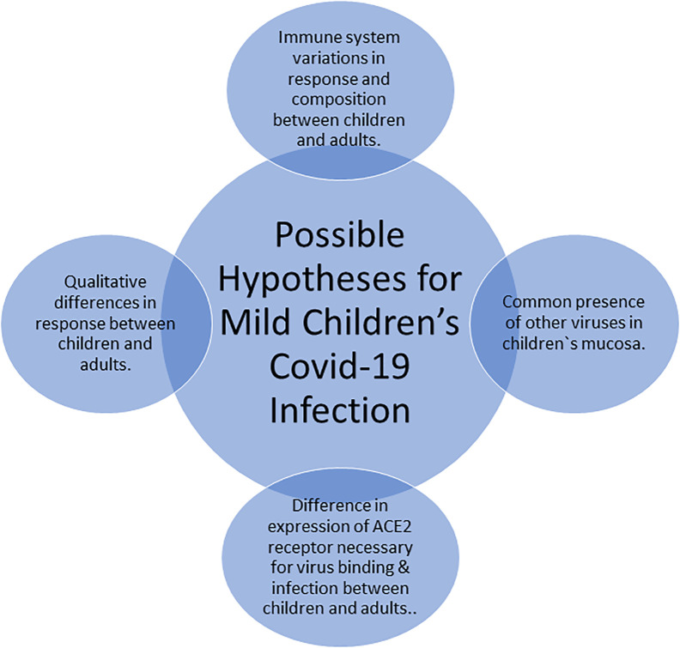
ウイルス学、解剖学、免疫学の分野には、小児におけるCOVID-19感染の軽度な症状を説明しうる複数のもっともらしいメカニズムが存在する。COVID-19パンデミックでは、小児は成人よりも感染リスクが低いようである(Liu et al 2020)。小児のCOVID-19検査の国際的な過少提示のため、小児と成人との間の異なる症状プロファイル、およびエビデンスが検査例に大きく依存している年齢特異的な発症パターンについての仮定を立てることは困難である。その結果、集団ベースの検査戦略における十分な数の子どもの数と有意なサンプルサイズが、子どもの間の真のCOVID-19感染を探索するために必要とされる(Hossny and El-Owaidy, 2020)。感染制御対策の強化、健康管理の実施、コミュニティ内での意識向上は、世界的なパンデミックの軽減に役立つために決して強調しすぎることはできない(Rasmussen er al)。 COVID-19については、非常に短い期間で多くのことが学ばれていたが、COVID-19ウイルスの子どもへの影響とともに、子どものウイルス感染拡大への影響については、まだ多くのことが学ばれている(Hagmann, 2020)。
心血管疾患とCOVID-19
異なるコロナウイルスの種類と心血管疾患との間には、確立された関連がある(Xiong et al 2020)。COVID-19もまた、この関連を踏襲している。米国CDCの報告によると、併存する健康状態を持つ人は、この基礎疾患を持たない人よりも重度のCOVID-19からのリスクに直面しているようである。1 つ以上の危険因子または基礎疾患を有する患者の割合は、緊急治療室への入院を必要とする患者(78%)と、重篤な治療室への入院を必要としない患者(71%)では、入院していない患者(27%)よりも高くなってた。慢性肺疾患・心血管疾患(心血管疾患)と糖尿病が最も多く記録されていた(CDCMMWR 2020)。
これらの報告は、多くの研究によって裏付けられていた。症例シリーズ研究では、ワシントン州の病院の救急ユニットに入院した全21例のうち、併存疾患を有する18例が同定された(Arentz et al 2020)。慢性腎疾患(47.6%)とうっ血性心不全(42.9%)が最も一般的に報告された併存疾患であった。中国で行われた138例の入院症例を対象とした大規模な症例シリーズ研究(Zhou F. et al 2020)では、症例のうち(14.5%)が心血管疾患を有し、(31.2%)が高血圧であった。中国で入院した191例(Zhou F. et al 2020)を対象にレトロスペクティブコホート研究が行われ、そのうち48%が基礎疾患を有していた。最も多い併存疾患は高血圧(30%)と冠動脈性心疾患(8%)であった。
発生した心機能障害には多くの説明がある。心血管疾患関連リスクの一つの説は、COVID-19患者に関連する検査所見によって説明されている。COVID-19が確認された入院患者の臨床像が研究された(Huang er al)。 臨床検査所見では、急性心不全を示す患者41人中5人(12%)でトロポニン-Iレベルが上昇していた。この中には、救急ユニットに入院した患者13人中4人(31%)入院していない患者28人中1人(25%)が含まれている。炎症反応を示すほとんどの患者で発生しているプロカルシトニンおよびプロ炎症性サイトカインのレベルの増加があるが、COVID-19がTヘルパー2サイトカインを増加させることも示されている(Huang et al 2020)。それにもかかわらず、COVID-19の肺組織に対する重篤な影響、およびその結果として生じる低酸素血症、灌流および血管異常(Lang et al 2020)は、心機能に大きな影響を与える。
もう一つの説は、COVID-19の管理に使用される薬剤が心機能に影響を与える可能性があるというものである。使用される抗ウイルス薬として示唆されているのは、ロピナビル/リトナビルである。英国ナショナルフォーミュラリー2020によると、この組み合わせは、心血管疾患を有する患者において注意して使用され、いくつかの薬物-薬物相互作用が他の心血管治療薬との間で生じる(Driggin et al 2020;Osborne et al 2020)。レムデシビルは、緊急使用承認薬である別の薬剤である(Commissioner O of the, 2020b)。最近の無作為化臨床試験では、レムデシビルを投与された患者は、心肺状態の悪化を含む副作用のために、レムデシビルの服用を早々に中止した(Wang et al 2020b)。COVID-19管理のためのもう一つの未調査薬であるクロロキン(Cortegiani et al 2020)は、重篤な不整脈を引き起こすことが知られている(Moore 2020)。表1は、現在使用されているか、または臨床研究中であるが、特定の心血管系の副作用を引き起こす薬剤のいくつかを示す。
表1 COVID-19の治療薬として考えられる薬と心血管系への影響
| 投薬 | 状態 | CVの副作用 |
|---|---|---|
| レムデシビル | FDAによる緊急使用許可(Lim et al。、2020)。 | 心肺状態が悪化した(Wang et al。、2020b)。 |
| クロロキン | 2020年5月下旬、安全上の懸念から、この治療群がWHO連帯試験から一時停止しました(COVID-19治療の「連帯」臨床試験)。 Mehraet。al。クロロキンが病院の生存率を低下させると述べたランセット紙を撤回した(Mehra et al。、2020)。 3は上RD研究のこの腕を継続することを決定した死亡率データに基づいて、2020年6月11日(「連帯」COVID-19の治療のための臨床試験) |
重度の不整脈(ムーア、2020年)。 |
| ロピナビル/リトナビル(Shaffer、2020) | 臨床試験(WHO連帯試験)による調査不足(COVID-19治療のための「連帯」臨床試験)。 | 脂質異常症を引き起こし、 CVD患者に注意して使用する(Dorward and Gbinigie、2020) |
| コルチコステロイド(Shaffer、2020) | サポートエージェントとしての臨床試験による調査中(Huanzhong、2020)ですが、これまでのところその有効性の臨床的証拠はありません(ASHP -COVID-19-Evidence-Table.pdf)。 | 浮腫や体液貯留を引き起こし、高血圧や不整脈を引き起こす可能性があります(Yasir et al。、2020)。 |
これらのデータは、現在使用されているか、またはCOVID-19の管理のための潜在的な候補である薬剤の多くが、心血管系の副作用を有することを示している。これらの薬剤のほとんどはまだ臨床試験中であり、それらのうちのいくつかはCOVID-19患者におけるそれらの使用に関する臨床的証拠を欠いている。さらに、これらの薬剤のいくつかの使用は議論の対象となっており、特にオセルタミビルおよびクロロキンである。オセルタミビルは、その使用を支持する証拠はないが、COVID-19患者によって広く消費されている。MehraらはLancetの論文の中で、クロロキンは病院の生存率を低下させると主張し、その後WHOは一時的にCOVID-19患者へのクロロキンの使用を停止した。結局、この論文は撤回され、WHOはこの薬剤の臨床試験を再開した。これらの矛盾した結果は、特にパンデミック時には、様々な不本意な論争を引き起こし、既存の緊張した状況に更なる混乱をもたらした。
COVID-19の管理に使用される薬剤は心血管の状態に影響を与えるとされているだけでなく、心血管疾患患者が使用する薬剤もCOVID-19の感受性に影響を与える可能性がある。例えば、異なるACE阻害剤またはARBを使用すると、ACE2受容体のアップレギュレーションを引き起こす可能性があり(Wang et al 2016;KaiおよびKai 2020)ACE2はCOVID-19の細胞への侵入に使用される機能的な受容体であり、このアップレギュレーションが感染の影響を悪化させると推測されている(Nadar et al 2020;Zhou P.別の研究では、COVID-19はACE2受容体を介して細胞に入るが、それをダウンレギュレーションし、好中球の浸潤、肺損傷を促進し、心臓保護を減衰させると考えられている(Vaduganathan et al 2020)。最近の研究では、実質的には、ACE阻害剤/ARBの使用とCOVID-19の陽性検査との間に関連性はなく、これらの薬剤を使用しても、致死例や救急ユニットへの入院を含むCOVID-19入院の危険性を拡大させる効果はないことが示唆されている(Abajo et al 2020;Mehta et al 2020;Reynolds et al 2020)。COVID-19管理におけるこれらの薬剤の使用の実際の反映については多くの矛盾した結果があり、臨床的なエビデンスを提供するためにさらなる研究が必要である(Elimination or Prolongation of ACE Inhibitors and ARB in Coronavirus Disease 2019 – Full Text View; Fosbøl er al 2020)。いくつかの国際的な心臓協会は、すでにACE阻害剤/ARBを使用しており、COVID-19に感染している患者には、薬の使用を継続することを推奨している(ACEI/ARB Use in COVID-19 Patients With Hypertension; Czarska-Thorley, 2020)。現在のパンデミックの広がりを制限するための措置としての物理的な遠距離および検疫、およびその後の集団生活様式の変化は、これらの患者の心血管系の状態にも影響を及ぼす可能性がある。これは、他の人との交流が少なくなり、積極的な関係が希薄になったことや、身体活動が低下したことに起因する可能性がある(Jiménez-Pavón et al 2020;Guzik et al 2020)。
環境および職業的リスク要因
COVID-19感染症に最もかかりやすい職業の違い
COVID-19がパンデミックと宣言された後、感染症にかかるリスクが最も高い職業についての懸念が広まっている。COVID-19の高い感染率には業務上の曝露が寄与しており(Koh, 2020)職業病に分類すべきであるとの考えがある(Godderis er al)。 実際、パンデミックのパンデミックの始まりは職場である武漢の魚市場であり、症例の半数以上(55%)はその市場に由来していたのに対し、閉鎖後の関連症例はわずか8.6%であった(Li Q. et al 2020)。シンガポールでは、最初の症例のいくつかは、現地の従業員と海外の従業員が会う仕事の会議に関連しており、その結果、シンガポールから3人、英国から1人、マレーシアから1人、韓国から2人の感染者が出た。国際的な事例は出国後まで発見されなかった(Koh, 2020)ことから、他国への感染拡大の要因になっている可能性がある。シンガポールではこれまでの事例に加えて、ツアーガイド、中国人観光客に接客した宝石店や小売店の労働者、タクシー運転手、建設現場の労働者など、他の初期の事例でも職業曝露が原因となっている可能性が高い(Koh, 2020)。感染した同僚を相手にしたことによる過去のパンデミック時の感染者数を見て、恐怖心が高まった。H1N1パンデミックの後、約800万人の労働者が感染して出勤したと推定されており、これがさらに700万人の同僚への感染につながった可能性がある(Drago and Miller, 2010)。
最近、このパンデミックや今後のパンデミックを食い止めるために、米国における労働者の感染症への曝露頻度を推定するための研究が行われた。この研究では、医療従事者が最も曝露頻度が高いことが明らかになった(Baker er al)。 実際のデータは、職業による感染リスクが最前線の医療従事者の間で最も高いことを裏付けている。中国の研究によると 2020年2月3日までの武漢の病院では、29%の患者が職務遂行中に感染した医療従事者であった。集中治療室の患者1人が少なくとも10人の労働者に感染したとしている(Wang D. et al 2020)。基本的な再生産数(R0)は2.2であることが示唆され、これは1人の感染者が2.2人の他の人に感染することを意味し、これは人から人への感染速度が速いことを示唆している(Li Q. er al)2020; Wang D. er al)2020)。イタリアでは 2020年2月20日から3月中旬近くまでの間に、感染した医療従事者は350人(約20%)に達し、死亡者も出たと報告されている(Remuzzi and Remuzzi, 2020)が 2020年3月末には感染者5000人、死亡者40人に達したと報告されている(Burdorf er al)。 英国の記事によると、SARS-CoV-2の医療従事者スクリーニングの際に 2020年3月10日と11日に5%が陽性となり、この割合は月末には20%にまで増加したという。しかし、論文では、患者から労働者へのCOVID-19の院内感染は、大きな広がり方ではなかったことが示唆されている(Hunter er al)。 過去のパンデミックを振り返ってみると、医療従事者が大きな影響を受けていたことが証明されている。例えば、SARSのパンデミック時には、医療従事者は全世界の症例数の5分の1であった(Chan-Yeung, 2004)。多数の感染者を扱っていることや、高ウイルス負荷にさらされていることから、感染した医療従事者の割合が高いことはもっともらしい(Burdorf et al 2020)。個人用保護具(PPE)の不足により、イタリアの事例のように、感染者や死亡した医療従事者の数が大幅に増加する可能性がある(Ranney et al 2020)。
COVID-19感染の影響を受けやすい職業は他にもある。米国の研究によると、保護サービス従事者とパーソナルケア・サービス従事者は、感染への職業曝露率が最も高いグループの一つであり、次いでコミュニティ・ソーシャルサービス従事者がこれに続いた(Baker er al)。 これは、公共に面した役割を持つ職員、例えば警察官、消防士、教育サービス従事者、保育士、公共交通機関の運転手などが感染する可能性が高いことを示唆する論文と一致している(Sim, 2020)。また、配達員に加えて、例えば、店舗やレストランの従業員など、多くの一般の人々と交流しなければならない労働者の中にも感染率が高い可能性がある。さらに、理学療法士、爪の技術者、美容師など、他人との物理的な近接性を必要とする仕事は、高いリスクがある(Burdorf et al 2020)。もう一つのグループとして、船舶や航空会社の乗務員が挙げられた(Sim, 2020)。乗組員の中で最初の症例を検出してから1週間後に約1.9%のスタッフ(総勢1068名中20名)が陽性と確認されたクルーズ船での発生数は、以前の意見を裏付けるものである(Kakimoto et al 2020)。
COVID-19パンデミックの労働者への影響は、身体的・経済的なものである可能性がある。健康への影響は、ウイルス自体に関連している場合もあれば、ストレスに起因している場合もある(Sim, 2020)。例えば、感染した医療従事者の割合が増加すると、健康な医療従事者の仕事の負担が増加し、仕事の過負荷や、病気に感染したり家族に感染したりすることへの恐怖、あるいは感染した患者や同僚を扱った後の検疫などによる高いストレスにつながる(Sim, 2020; Xiang et al 2020)。保健ワーカーだけがパンデミックで精神疾患に苦しむことができる労働者ではなく、他の労働者も検疫や仕事を失う、あるいはすでに仕事を失っているという考えからストレスを受けることがある(Sim, 2020)。伝染病のために仕事に行くのをやめてしまう人もいれば、病気になりながら仕事をせざるを得なくなる人もいる。欠勤や欠勤の割合が高いと、ストレスを高めたり、病気の労働者の状態を悪化させたり、他の人に感染して仕事の生産性を低下させる可能性がある(Kinman, 2019; OSHA, 2020)。健康問題の他にも、多くの企業が閉鎖され、労働力の減少を招いている。これは従業員、特に日雇い労働者に大きな影響を与える(Sim, 2020)。残念ながら、一部の労働者は在宅勤務をする余裕がない。一方で、パンデミックが職場に有益な効果をもたらすという考えもある。雇用主は従業員を守るために安全対策を講じなければならないし、遠距離恋愛をより頻繁に利用することで、交通量を減らし、燃料消費に起因する大気汚染を減少させることになるだろう(Sim, 2020)。
結論として、この重要な時期に労働者、特に医療従事者を失うわけにはいかないので、車輪を回転させ続けるためには、労働者を保護するための予防措置を講じるべきである。米国の労働安全衛生局(OSHA)は、労働者を安全に保つために安全な作業環境を提供する方法を計画するように助言している。また、資源を有効に利用するために、暴露リスクに応じて職業上のリスクを分類し、従うべき指示を示している(OSHA, 2020)。現在では、労働者に社会的・精神的なサポートを提供することが重要である(Koh, 2020)。適切な病気休暇の規制は、労働者のストレスを軽減するための重要な必要性である(Kinman, 2019; OSHA, 2020)。より多くの労働力を失わないように、ロックダウンを終了する前に計画と訓練を設定すべきである(Agius, 2020)。
ワクチン接種の状況
結核に対するBCG(Bacillus Calmette-Guérin)ワクチン接種が義務化されている国では、COVID-19の死亡率に影響を与えている可能性がある(Miyasaka, 2020)。以下の表2に示す最近のデータは、国ごとの死亡率とBCGワクチン接種の菌株の違いを示したものである。表2に示すように、BCGワクチンを接種していない国や接種を中止した国は、BCGワクチンを接種し続けている国に比べて死亡率が高くなっている。
表2 COVID-19 人口100万人当たりの死亡数とBCGワクチン接種の有無
表2
| 国 | BCGワクチン接種の利用可能性(b) | BCGのひずみ(b) | 100万人あたりの死亡数(a) |
|---|---|---|---|
| 台湾 | まだ利用可能 | 日本 | 0.3 |
| イラク | まだ利用可能 | 日本 | 2 |
| 中国 | まだ利用可能 | ロシア/ブルガリア | 3 |
| 日本 | まだ利用可能 | 日本 | 4 |
| オーストラリア | 1950〜1980年代半ば | コンノート | 4 |
| 韓国 | まだ利用可能 | 異なる株 | 5 |
| ノルウェー | 2009年まで不明 | デンマーク | 39 |
| 七面鳥 | まだ利用可能 | インド | 40 |
| フィンランド | 1941–2006 | デンマーク | 43 |
| イラン | まだ利用可能 | デンマーク | 75 |
| ドイツ | 1961–1998 | パスツール | 82 |
| 米国 | 使用されていない | NA | 207 |
| スウェーデン | 1940〜 1975年 | デンマーク | 274 |
| フランス | 1950〜 2007年 | デンマーク | 381 |
| 英国 | 1953–2005 | デンマーク | 419 |
| イタリア | 使用されていない | NA | 478 |
| スペイン | 1965–1981 | デンマーク | 540 |
a Worldometer(Coronavirus Update (Live): 4,714,317 Cases and 312,298 Deaths from COVID-19 Virus Pandemic)より取得。
bRitz and Curtis(2009)およびZwerling et al 2011)(The BCG World Atlas. A Database of Global BCG Vaccination Policies and Practices; Sharma er al)。)
BCGワクチンは、感染症に対する免疫応答の増加を誘導することにより、様々な病原体から保護されるため、免疫に異種効果がある(Hirve er al)。 また、使用したBCG株によって死亡率が異なることが表2に示されている。すなわち、日本とロシアのBCG株はCOVID-19患者の死亡率が低いのに対し、デンマークのBCG株はCOVID-19患者の死亡率が高いことを示している(Miyasaka, 2020)。これは、初期のBCG株が株数の豊富さから訓練された免疫応答を刺激することができるためと考えられる。しかし、オーストラリアやフィンランドのデータは、数年前にBCGワクチン接種を中止しているため、それとは逆の結果となっているが、それでも死亡率も低いのである。したがって、BCGワクチンがCOVID-19の死亡率を最小化する唯一の要因ではないことは間違いないが、フィンランドとオーストラリアでは、優れた医療施設に加えて人口密度が低いため、社会的距離が有効である可能性がある。
イタリアの高齢者人口は23.3%であり、国連、世界人口展望2019(Dowd er al)。 また、イタリアの家族は、異なる世代間での接触が密に行われている近隣地域に住む傾向がある(Kalmijn and Saraceno, 2008)。したがって、異なる世代間の頻繁な接触と生活の近接性は、イタリアでのCOVID-19の発生を加速させる結果となった(Mossong et al 2008)。そのため、高齢者人口の多い国では、死亡率の高さを防ぐために、そのカーブを平坦にし、医療負担を軽減するために、保護のための厳しい措置が必要であることを助言している(Dowd et al 2020)。
まとめると、社会経済階級が低く、医療へのアクセスが悪い密集した地域に住む高齢者集団は、COVID-19のリスクが高いことがわかる。BCGワクチン接種や特定の酵素遺伝子の発現などの他の要因がCOVID-19の発症に寄与している可能性があるが、これを確認するためにはさらに多くの研究が必要である。
妊娠とCOVID-19
妊婦や新生児がCOVID-19に感染するリスクが高いことが懸念されている。COVID-19については、ここ数ヶ月の間にいくつかの研究が発表されたが、この集団の感染リスクを示すデータはまだ限られている(Novel Coronavirus 2019(COVID-19))。CDCの最近の報告によると、COVID-19を持つ妊婦は、早産のリスクを高めることに加えて、ICUの入院や機械的人工呼吸などの重症化のリスクが高い。これまで死亡率が高いというエビデンスはなかった。このカテゴリーの感染の全体的なリスクはまだ低く、このカテゴリーの他の呼吸器感染症よりも有意に低い(Novel Coronavirus 2019 (COVID-19);CDC, 2020b)。
利用可能なデータによると、分娩の種類、経膣または帝王切開は、ウイルス感染に影響を与えない(Karimi-Zarchi et al 2020; Ryan et al 2020)。さらに、COVID-19が先天性異常や流産を引き起こす可能性があるという証拠はない(ECDC 2020)。パンデミックの初期には、垂直伝播の証拠はなかったが、現在ではその存在が示唆されている(ECDC, 2020; Patanè et al 2020; Fornari, 2020)。ある研究では、COVID-19を持つ母親から生まれた新生児の50%が治癒して退院し、40%が入院し、10%(1例)が死亡したことが示されており、周産期のCOVID-19感染は重篤な副作用をもたらしうると結論づけられている(Zhu er al 2020年)他の研究では新生児は元気で退院したことが明らかになっている(Chen S. et al 2020;COVID-19ウイルス感染と妊娠;Occupational health advice for employers and pregnant women during the COVID-19 pandemic 2020;Wang X. et al 2020)。ほとんどの保健機関は、母親がCOVID-19の軽度の症状を持っているか、または無症状で赤ちゃんに栄養を与えることができる場合は、母乳育児中にフェイスマスクを着用すること、適切な手洗い、赤ちゃんのベッドは母親から2メートル離れた場所に置くことなどの感染予防措置を取りながら、母乳育児を推奨している(Davanzo et al 2020)。母親が赤ちゃんに栄養を与える能力がない場合は、母乳を使用し、頻繁な母乳代用品の使用を避けることが望ましい(Davanzo et al 2020)。
マスク着用文化
COVID-19の発生を受けて,マスク着用に関する様々なアプローチが提起されている.そこで、マスク着用によるコロナウイルスを含む呼吸器ウイルスの感染低減効果を、呼吸器飛沫とエアロゾルの両方から検出することで検討した。マスクを着用していない人では、参加者の30%の呼吸器液滴と40%のエアロゾルからコロナウイルスが検出されたのに対し、マスクを着用している人ではエアロゾルと呼吸器液滴の両方から0%が検出された(Leung N. H. L. et al 2020)。無症状であってもCOVID-19に感染した患者が感染を広げる可能性があるという証拠があるため、フェイスマスクの着用は非常に重要である(Bai er al)。
WHOは、すべての人がマスクを着用することは、安全性の誤った感覚を与え、重要な薬の服用をおろそかにすることになりかねないと主張しており、医療従事者にとっても重要なマスクが不足する原因となり、フェイスマスクの合理的な使用を奨励している(World Health Organization, 2020)。CDCは感染症から自分自身と他の人を守るための指針を示している(CDC, 2020a)が、その中でも特に、他人と接触する際には、誰もが少なくとも鼻と口を覆う顔布を着用すべきであることを念頭に置きながら、約6フィート/~2メートルの距離が必要であることを示している。
社会経済的地位の高い中国人のサンプルでは、98%が外出時にマスクを着用していた(Zhong er al)。 香港の別の研究では、94.8%がマスクを着用していたが、そのうち13%は間違った方法で着用していた(Tam et al 2020)が、中国の他の地域や日本、タイの一部の地域では、使い捨ての代替品を選択している(Feng et al 2020)。韓国、カナダ、チェコ共和国では、市民が公共の場でマスクを使用するように指導している(Cheng et al 2020)。シンガポールでは、保健当局は、健康であればマスクを着用する必要はないとしている(Wang C. et al 2020)。低所得国では、手術用マスクが使用できない場合に限り、布製のマスクを許可するというアプローチも行われている(Sugrue er al)。 一方、一部の研究者は、抗ウイルスナノ材料を含浸させた繊維マスクを試してみて、相乗効果で感染を軽減することを提案している(Livingston et al 2020; Sportelli et al 2020)。
欧州疾病予防管理センターは、パンデミック時にマスクを着用することを推奨しているのは、特に閉鎖された人通りの多い場所で症状のない感染者の割合が高い場合や、リスクの高い人や職業上多くの人と接する必要がある場合である(ECDC, 2020)。特定の集団へのフェイスマスクの着用は好ましくないかもしれない。例えば、CDCでは、2歳未満の子供や、効果的にマスクをコントロールするのが難しいと考えられる人は、フェイスマスクを使用しないことが推奨されている。例えば、支援を受けていない本質的な年齢の若者、または呼吸器疾患を持つ人々(CDC, 2020c)。呼吸器疾患のある人のマスク着用は、呼吸が困難になる可能性があるため推奨されていない(COVID-19と肺疾患Q&A、COVID-19よくある質問)。さらに、息切れのある患者は、暑さを感じたり、息切れが悪化したりすることがあるので、フェイスマスクを拡大して利用することは推奨されていない(Ren er al)。 マスクを着用中の呼吸困難は、スポーツや運動を練習している個人に影響を与える。これらの集団では、患者に最適なマスクを見つけることが非常に重要である。例えば、いくつかのカバーは他のものよりも通気性が良い。患者は単純に深い呼吸を維持し、過呼吸を促す浅い呼吸を避けることができる。一方で、患者は、人が少ないゾーンを発見することができるので、人ごみの中を通り抜けるときだけカバーが重要になる(Nyenhuis et al 2020)。
どのような状況においても、保健当局や政策立案者が、前述の長所と短所に基づいてフェイスマスクの合理的な使用に関する指針を示し、このパンデミックの間にCOVID-19感染に対する脆弱性を可能な限り減少させるために、使い捨ての保護代替品や再使用代替品に関する取り組みや研究を奨励することは非常に重要である(Islam er al)。
結論
COVID-19のゲノム特性化の研究は、このウイルスが前任者(SARS-CoV-1)よりもはるかに進化していることを示している。SARS-CoV-2は、SARS-CoV-1よりもはるかに高い親和性でACE2を結合し、より高い温度に耐え、一般的により溶解性が高い(He et al 2020)。ウイルスゲノムにおける新たな突然変異は、特定のグループの感受性と同様に、ウイルスの伝達および病原性に影響を与える可能性がある(Korber et al 2020)。現在の証拠は、異なる集団間でのCOVID-19感染および重症度に様々な格差があることを示している。
重要な差異には、高齢者では感染率および死亡率が高くなり(Onder et al 2020年)小児では感染率が有意に低くなっている(TezerおよびBedir Demirdağ 2020)など、異なる年齢層間でのばらつきが含まれる。感染率および死亡率の差は、米国のアフリカ系アメリカ人のような異なる民族間でも観察され得る(Fogarty et al 2020)。基礎疾患、特に心血管性の疾患の存在は、COVID-19の症状を悪化させると見られ、そのような疾患を有するグループは、死亡率および罹患率の上昇を示す(Zhou F. et al 2020)。3つの観察は、ACE2,TMPRSS2,またはその両方のいずれかの発現の変動によって引き起こされるという仮説が立てられている。ACE2の調節異常は、COVID-19罹患率の変動と関連していることが見出されており、セリンプロテアーゼであるTMPRSS2は、宿主細胞への侵入に備えたウイルスのプライミングに必要であることが見出されている(Hoffmann et al 2020)。
環境および職業的曝露に関しては、様々な職業でCOVID-19に感染するリスクが高くなることが示されており、特に最前線の医療従事者や対面での交流を必要とする職業では、COVID-19に感染するリスクが高くなることが示されている(Koh, 2020)。パンデミックに関する興味深い指摘としては、BCGワクチンを含むワクチン接種計画がある国では、感染率と死亡率が低下しているようである(宮坂, 2020)。COVID-19の感染拡大を抑制するためのマスク着用の効果については、意見が分かれている。WHOの方針ではフェイスマスクの着用を推奨しているが(世界保健機関 2020年)CDCではフェイスマスクの着用を強く推奨している。CDCはフェイスマスクの着用を推奨しているだけでなく、手の届かない場所では手術用マスクの代わりに自家製の布製マスクを使用することも提案している(CDC, 2020a)。
COVID-19感染の伝播、病原性、死亡率に影響を与える要因が無数にあることは明らかである。現在、治療法や予防法が不足しているため、COVID-19の合併症のリスクが他の人よりも高いグループがあることを明らかにすることに、より多くの関心が寄せられるべきである。注目すべき点は、症例の予後を決定する上でのCOVID-19の分子構造の重要性である。最も重要なことは、環境や職業的な危険因子の同定が最も重要である。最後に、ワクチンや治療薬への反応を予測したり、脆弱なグループの感受性の変化を予測したりするためには、ウイルスゲノムに蓄積された変異を綿密にモニタリングすることが必要である。
略語
SARS、重症急性呼吸器症候群;ARDS、急性呼吸窮迫症候群;α-CoVs、アルファコロナウイルス;β-CoVs、ベータコロナウイルス;γ-CoVs、デルタコロナウイルス;δ-CoVs、ガンマコロナウイルス;CoVs、コロナウイルス;SARS-CoV、重症急性呼吸器症候群関連コロナウイルス;MERS-CoV、中東呼吸器症候群関連コロナウイルス。WHO、世界保健機関、FDA、食品医薬品局、EUA、緊急使用許可、IVCC、国際ウイルス分類委員会、ACE、アンジオテンシン変換酵素、MD、分子動力学、NSPS、非構造タンパク質、PCR、ポリメラーゼ連鎖反応、ADE、抗体依存性増強、ARDS、急性呼吸窮迫症候群。TMPRSS2,膜貫通型プロテアーゼ、セリン2酵素、SNPs、一塩基多型、RBD、受容体結合ドメイン、CXCL、好中球化学乳化因子、CCL20,優勢樹状細胞化学乳化因子、ER、エストロゲン受容体、HDOCK、ハイブリッド蛋白質-蛋白質ドッキングアルゴリズム、RAAS、レニン-アンジオテンシン-アルドステロン系、GISAID、Global Initiative for sharing All Influenza Data。RdRp、RNA依存性RNAポリメラーゼ;cryo-EM、極低温電子顕微鏡;CPT、回復期血漿輸血;SERMs、選択的エストロゲン受容体モジュレーター;心血管疾患、心血管疾患;PPE、個人用保護具;OSHA、労働安全衛生管理局;BCG、Bacillus Calmette-Guérin;ICU、集中治療室。
