Genetic Diversity of SARS-CoV2 and Environmental Settings: Possible Association with Neurological Disorders
2021年1月6日
pubmed.ncbi.nlm.nih.gov/33404977/
シャリファ・ハサナ 医師 ファラッド・ホサイン、マルア・ジャルーリ、MDd. タンヴィール・カビル、ジアシュ・ウッディン、ミール・イマーム・イブネ・ワヘド、タパン・ベオール、メイ・N・ビン Giash Uddin, Mir Imam Ibne Wahed, Tapan Behl, May N. Bin-Jumah, Mohamed M. Abdel-Daim, Lotfi Aleya & Md. サハブ・ウッディン
分子神経生物学 (2021)Cite this article
要旨
2019年末に中国・武漢市の海市で発生した新型コロナウイルス症2019(COVID-19)と呼ばれる新型コロナウイルス(CoV)は、コロナウイルス科に属している。COVID-19と重症急性呼吸器症候群(SARS)は同じ科(Coronaviridae)に属している。COVID-19の現在のアウトブレイクは、世界中で公共の懸念と脅威を生み出し、今では250以上の国と地域に広がっている。世界中の研究者や科学者が、COVID-19パンデミックの罹患率や死亡率を軽減するための治療戦略を見つけようとしている。SARS-CoV2の複製、拡散、および重症度は、環境設定に依存する。特に、COVID-19では、気象パラメータの影響が議論されているが、気象パラメータは呼吸器感染症に影響を与える重要な因子であると考えられている。また、COVID-19は神経疾患の発症を促進する。しかし、COVID-19と神経障害の発症機序については、まだ明らかになっていない。そこで本研究では、SARS-CoV2のゲノムと生態に焦点を当て、COVID-19の進行に及ぼす気候的要因の影響を明らかにした。また、最新の研究データをもとに、COVID-19と神経疾患との間の脆弱性を批判的に明らかにした。
序論
実際、新規コロナウイルス疾患2019(COVID-19)は、世界中の人間の健康を脅かしているパンデミックである。重症急性呼吸器症候群コロナウイルス(SARS-CoV)(2003年に同定)に対して採用された戦略から得られた経験と、スループット分子生物学における最近の開発は、SARS-CoV2の現在のパンデミックと戦うために利用することができる[1, 2]。SARS-CoV2の生態、感染様式、および遺伝学を理解することは、SARS-CoV2の感染に対するより多くの制御および予防策を提供する可能性がある。COVID-19が確認された1人の個人は、約3人の健康な個人に感染する可能性がある[3, 4]。感染後、手は機械的ベクターの供給源となる可能性が高く、体内への侵入を防止し、排除するための潜在的な場所となる。それにもかかわらず、SARS-CoV2がこの段階で減少しない場合、それは、このウイルスがそのスパイクを利用してアンジオテンシン変換酵素2(ACE-2)受容体と結合し、呼吸器上皮の細胞へのアクセスを得るためにその好適部位(すなわち、肺の細胞)に向かって移動することができる。この段階では、SARS-CoV2によって肺の自然免疫が低下する [1]。
いくつかの研究により、季節サイクルがインフルエンザなどの急性感染症に遍在的に存在することが明らかにされているが、これは典型的には呼吸器ウイルス感染症にも見られる[5, 6]。この点では、例えば、温帯地域では毎年冬にインフルエンザのパンデミックが発生している[6]。また、太原、北京、広州、香港の地域での研究では、SARSの発生は気温の変化と有意に関連していることが示されている[7]。環境条件が現在のCOVID-19の発生に影響を与える可能性があることを示す証拠が増えている[8]。Chinらの研究[9]では、SARS-CoV2は4℃でより高い安定性を示したが、熱に対する感受性を示したと報告している。さらに、培養温度を70℃まで上昇させると、SARS-CoV2の生存時間は5分に短縮された。疫学研究では、気象パラメータとCOVID-19との間に相関関係があることが明らかにされているが、その結果には議論の余地がある[10,11,12]。XieとZhuによる研究[10]では、平均気温が3℃以下の場合、1℃の上昇は1日に確認されたCOVID-19症例の4.861%の上昇と関連していることが示された。別の研究では、Maら[12]は、毎日のCOVID-19関連死と日中の気温範囲との間に正の関連性を示し、相対湿度との間に負の関連性が観察された。それにもかかわらず、Yaoら[11]は、中国の都市ではSARS-CoV2感染は気温とは関連していないことを研究で示した。実際、COVID-19は急速に世界的に広がっている。さらに、コロナウイルス(CoV)感染の第二波が発生する可能性がある[13,14]。したがって、今後のシナリオを予測するためには、COVID-19の感染拡大における気象パラメータの役割を明らかにすることが重要である。
一方、最近の知見では、認知症、パーキンソン病(PD)多発性硬化症(MS)などの神経変性疾患とCoVとの強い関連性が明らかにされている[15]。また、SARS-CoV2は嗅神経を介して直接肺に感染することから、脳幹を含む様々な脳領域に感染することが動物モデルやヒトモデルで確認されている[16]。この現象を明らかにするために、ウイルスの糖タンパク質スパイクがACE2受容体と結合することで感染が進行することが考えられる。実際、これらの受容体は、線条体のドーパミン神経細胞や髄質の心電図中枢など、脳の様々な領域に広く存在している[18, 19]。しかし、SARS-CoV2と神経障害との正確な関連は不明である。そこで、本研究では、SARS-CoV2感染に対する脆弱性とCOVID-19と神経障害の重要な相互作用を明らかにすることを目的とした。
COVID-19の疫学
12月30日から 10月18日までの間に、4,000万人以上のCOVID-19の症例と110万人以上の死亡が世界的に報告されている[20,21]。直近の10月18日以降、WHOの6つの地域すべてで、240万人以上のCOVID-19の新規症例と3万6,000人以上の死亡が報告されている(表1)。WHO地域別に見ると、欧州地域ではこの1週間で症例数(92万7433人)と死亡数(8386人)の急増が報告されており、前週に比べて症例数が25%、死亡数が29%増加しており、全世界で報告された全新規症例数の38%、全死亡数の23%に寄与している。新規感染症の発生率が高いのは米州と東南アジア地域で、世界的に観測された新規症例数と死亡数の半分以上を占めていると報告されているが、この2つの地域では死亡数の減少が続いている。また、東地中海、アフリカ、西太平洋地域でも緩やかな増加が見られた。過去7日間で最も多くの新規症例数を報告している国は、インド、米国、フランス、ブラジル、英国であり、7日間で観測されたものと変わらない[20,21]。
表1 WHO地域別に毎週報告されているCOVID-19の症例数と死亡者数、世界の死亡者数(2020年10月18日現在)[21]
SARS-CoV2の分子機構と遺伝的多様性
武漢では、COVID-19関連肺炎患者からSARS-CoV2のゲノム配列が単離され、そのサイズは29.9キロベース(kb)であることが判明した[22]。SARS-CoV2はポジティブセンスの一本鎖RNAを含む[1,23]。武漢SARS-CoV2の最初のゲノムは、ヒトSARS-CoVと82%、アットSARS-CoVと89%のヌクレオチド相同性を示した。他のSARS-CoVとの類似性の高さから、この新しいウイルスによる現在のアウトブレイクは 2020年1月30日に世界保健機関(WHO)と国際ウイルス分類学委員会(International Committee on Taxonomy of Viruses)のCoV研究グループによって正式にSARS-CoV2と宣言された[24]。興味深いことに、SARS-CoV2のオープンリーディングフレーム(ORF)は、コロナウイルス科のメンバー間である程度異なっている[25]。最初のORF内では、SARS-CoV2 RNAのほぼ67%が主に位置し、pp1aおよびpp1abポリタンパク質を翻訳している。実際、それらは16の非構造タンパク質(NSP)をコードしている。ORFの残りの部分は、付属タンパク質と構造タンパク質のコードに関与している。一方、ゲノムの残りの部分は、スパイク(S)糖タンパク質、小エンベロープ(E)タンパク質、マトリックス(M)タンパク質、ヌクレオカプシド(N)タンパク質をコードしている[26]。NおよびEタンパク質と特異的な付属タンパク質は、SARS-CoV2の複製中の初期自然免疫応答の停止に関与している。Angelettiらの研究[27]では、SARS-CoV2のNSP2とNSP3の変異が観察され、SARS-CoV2の分化と病原性に大きく寄与していることが示されている。さらに、Zhangら[28]は、中国のCOVID-19患者において、SARS-CoV2の様々な形態の変異が観察されたことを報告している。
さらに、CoVの病原性は、CoVの構造タンパク質および非構造タンパク質の効果と関連している。CoVのすべての構造タンパク質のうち、S糖タンパク質はCOVID-19の発症に大きな役割を果たしている[28]。S1とS2はS糖タンパク質の2つのサブユニットである。S糖タンパク質のホモ三量体構造は、SARS-CoV2の表面にあるスパイクで構成されており、宿主細胞内の受容体との接着を媒介している。また、SARS-CoV2のS2サブユニットには、膜貫通ドメイン、融合ペプチド、細胞質ドメインが存在しており、これらは高度に保存されており、抗ウイルス薬の新規ターゲットと考えられている[29]。ゲノムレベルでは、SARS-CoV2およびSARS-CoVはRD1,RD2,RD3,RD4,RD5およびRD6を含む6つの領域を含む。これらの領域のうち、RD1〜RD3はORF lab遺伝子の部分コード配列であり、RD4およびRD5はS遺伝子の部分コード配列である。一方、RD6は、ORF7b及びORF8遺伝子の部分的なコーディング配列を形成している。SARS-CoVとSARS-CoV2のタンパク質間には高い相同性(95%以上)があることから、これら、2つのウイルス間には構造的な類似性があると考えられ、ワクチン候補の設計に役立つ可能性があると考えられている[1, 30, 31]。
さらに、SARS-CoV2の病原性と病原性は、宿主の自然免疫応答を阻害し、ウイルスの集合と放出を連続的に仲介することで、非構造タンパク質と構造タンパク質に関連していると考えられている[29, 32]。CoVゲノムの中では、NSP3が最大のタンパク質であり、CoV複製に必須のドメイン活性を有している[31]。また、最近では、COVID-19の発病は主にNSP2とNSP3の変異によって誘導されることが示されている。Eタンパク質以外にも、SARS-CoV2の主要な構造タンパク質および非構造タンパク質のすべてに42の変異が認められた。さらに、Nタンパク質、Mタンパク質、S糖タンパク質、ORF1abポリタンパク質にも変異が確認された[33]。これらの知見から、突然変異が世界的な急速な感染拡大、抗原性の変化、宿主のトロピズムに関与しているのかどうかについて、さらに疑問が生じた[33]。最近、SARS-CoV2が異なる個体で変異していることが実証されており、その変異は6つの遺伝子型に大別されている[28]。そのため、SARS-CoV2のゲノムを厳密に解析し、その正確な発症メカニズムと将来の変異の可能性を明らかにする必要がある。
SARS-CoVのリガンドと受容体
ACE-2 は、肺、腸、動脈、心臓の細胞の形質膜表面に存在し、腎組織にも存在する[34]。ACE-2の血圧調節機能以外にも、SARS-CoV2や他のCoVは、この受容体タンパク質を利用して宿主細胞に侵入し、有害な作用を発揮する[34]。ウイルスの外表面は親水性で、内部には親油性の面があるため、このウイルスは洗浄剤で破壊することができる[35]。S1とS2はSタンパク質の2つの機能的バリアントまたはサブユニットであり、S1バリアントは宿主細胞の受容体との結合に、S2バリアントは宿主細胞の細胞膜とのウイルス融合に関与していることが知られている(図1)。いくつかのCoVにおいて、S糖タンパク質は、融合前の状態で非共有結合で結合しているS1とS2のサブユニットの境界で切断されている[35]。遠位のS1サブユニットには受容体結合ドメインが含まれており、膜に固定されたS2サブユニットの融合コンフォメーションを安定化する役割を果たしていることが明らかになっている[35]。実際、前述のような切断は、広範囲の不可逆的な構造変化を介して膜融合に関与するタンパク質を誘導すると考えられている。したがって、感受性細胞へのCoVの侵入は、特異的な受容体結合活性とSタンパク質のタンパク質分解処理が関与する複雑なメカニズムであり、ウイルスの細胞膜との融合を媒介していると考えられている[35]。異なるCoVがS1サブユニット内の異なるドメインを使用して、様々な付着物や侵入受容体を検出することが明らかになっている。研究の結果、共通のヒトCoVであるHKU1とOC43は、SドメインA(SA)を介してヒト細胞表面の糖脂質や糖タンパク質に見られる5-N-アセチル-9-O-アセチル-シアロシドに結合し、感受性細胞への侵入を媒介していることが明らかになった。
図1 SARS-COV2およびCOVID-19ゲノム配列の模式図
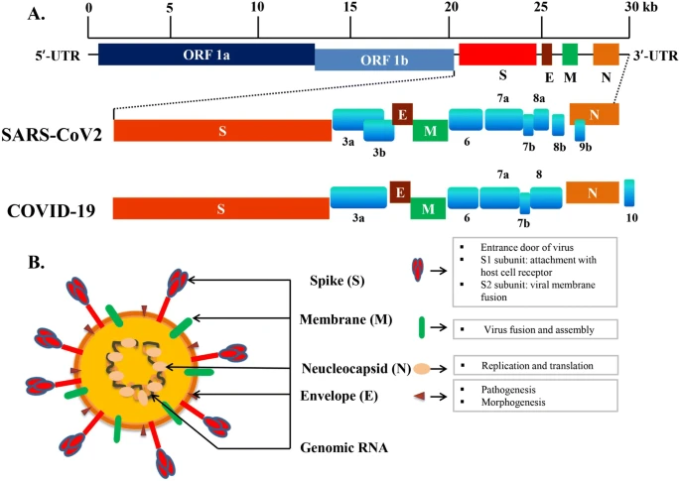
A. ゲノム配列とオープンリーディングフレーム(ORF)との比較について言及している。ゲノム配列の全長は〜30kbである。B. ウイルスRNAはヌクレオカプシド(N)タンパク質と関連している。スパイク(S)エンベロープ(E)膜(M)は脂質二重層に埋め込まれている。
実際、SARS-CoV2およびSARS-CoVは、ドメインB(SB)の結合を介してACE-2と直接相互作用し、宿主細胞に侵入する[36]。CoVのS糖タンパク質は表面に露出しており、ウイルスの宿主細胞への侵入を促進するため、感染後の中和抗体の主な標的であり、ワクチンや治療薬の開発の焦点となっている。Sトリマーは、適切なフォールディングを行い、宿主プロテアーゼや中和免疫マーカーへのアクセスを得るために重要なN-連結糖鎖で広く装飾されていることが観察されている[37]。実際、SARS-CoV2 と SARS-CoV の S 糖タンパク質の構造や配列に顕著な類似性が見られたことから、これらの 2 種に共通する関係を示しており、ヒトが攻撃を受ける ACE-2 受容体との関係を明らかにしている。さらに,S糖タンパク質はACE-2受容体に完全に適合しており,現在のCOVID-19発生との戦いは,下気道に存在する細胞におけるS糖タンパク質とACE-2受容体のメカニズムをよりよく理解することに大きく依存していることを示唆している.SARS-CoV2は、細胞を介してエンドサイトーシスを介して宿主細胞に侵入すると考えられている[37]。したがって、COVID-19の発生に対する戦略は、CoVs上のS糖タンパク質と宿主肺胞細胞のACE-2受容体の関与のメカニズムをよりよく理解することに大きく依存している。
SARS-CoV2のバイオノミクス
ヒトに感受性のあるウイルスとして、これまでに 6 種類の CoV が認識されている。そのうち4つは低病原性CoVとされており、ライノウイルスと同様の軽度の呼吸器疾患を引き起こす[22]。一方、他の2つのCoV、中東呼吸器症候群(MERS-CoV)およびSARS-CoVは、高病原性であり、ヒトに致命的な影響を与える可能性がある。SARS-CoV2を引き起こすCOVID-19は、CoVsファミリーの7番目のメンバーとして同定されている。進化解析やウイルスゲノム配列解析の結果から、コウモリがウイルスのリザーバー宿主であることが疑われている。また、SARS-CoV2はコウモリから未知の中間宿主を経由してヒトに感染する可能性もある。これまでのところ、SARS-CoV2の中間宿主としては、ヘビ、パンゴリン、タケネズミが示唆されている。これらの動物は、コウモリの尿、糞、唾液を介してウイルスに接触した可能性がある[38]。進化するウイルスは、人獣共通感染の連鎖を経て、動物を宿主として利用することが多くなってきていることが観察されている[38]。したがって、パンデミックを制御するためには、SARS-CoV2 の感染源となりうる動物を認識することが不可欠である。
SARS-CoV2の感染
中国からの包括的な研究では、ヒトからヒトへの感染がSARS-CoV2アウトブレイクの主な入手方法であることが確認されている[39]。COVID-19感染者は、SARS-CoV2感染の主要な感染源である[22]。最近の研究では、呼吸器飛沫がSARS-CoV2感染の接触に関連していることが報告されている。また、感染は空気中の飛沫を介して、互いに密接に接触することで起こると述べている[38, 40]。無症候性COVID-19患者も感染過程にあることに言及することが重要である。無症状者は感染後14日以内に病原体を感染させることができる[41]。別の研究では、SARS-CoV2は局所的および/または経口的に感染する可能性があることが示されている[42]。汚染された食品からのSARS-CoV2の食中毒はまだ解明されていない。SARS-CoV2の母子感染も想定されているが、SARS-CoV2の垂直感染を検証するためには、さらに多くの研究が必要である[43]。別の最近の研究では、SARS-CoV2の潜在的な感染様式としてエアロゾルも報告されている。これは、エアロゾルでは5~8時間以内に、感染媒介物表面では5~7日間伝染性を維持することができる。この証拠に基づき、WHOはエアロゾル感染が可能であると報告している[3]。
空気感染
最近のエビデンスでは、無症状のCOVID-19患者が、くしゃみ、咳、近距離の人との会話、不健康な空気の流れによって広がる可能性のあるウイルス感染の潜在的な感染源であることが示されている[44]。しかし、空気汚染はSARS-CoV2の主な感染経路であると考えられている[45]だけでなく、非侵襲的陽圧換気、高流量酸素療法、気管支鏡検査、気管支内挿管、バッグ・マスク換気、吸引・ネブライザー、喀痰誘導、心肺蘇生などの医療処置も、SARS-CoV2のエアロゾルの生成と空気中への放出の主な感染源であると考えられている。2015年に韓国で発生したMERS-CoVのアウトブレイクを受けて、いくつかの病院における環境汚染の役割が評価されているほか、空気や表面上でのMERS-CoVの生存性と安定性が広範囲に研究されている[46]。
水と廃水の伝達
COVID-19パンデミック時には、適切な衛生管理、安全な飲料水の確保、下水道の整備が世界中の人々の健康を守る上で重要な役割を果たしている[47]。SARS-CoV2感染のリスクは感染者の便を介しては少ないように思われるが、腸管感染を引き起こす可能性があり、便サンプルに現れる可能性があるという証拠がある[48]。さらに、SARS-CoV2感染が確認された症例の約2~10%が下痢を伴うことが研究で示されており[49,50,51]、COVID-19患者の便からはSARS-CoV2の残留ウイルスRNAが検出されている[42,52]。しかし、培養便サンプルからSARS-CoV2の曝露が検出された研究は1件のみである[53]。最近、廃水源でSARS-CoV2ウイルスの存在が確認され、また、ウイルスが数日から数週間にわたって下水中で生存することも示されている[54]。この知見は、コミュニティ内でのCoVのライフサイクルを追跡およびモニタリングするための感度の高いツールとなりうる[55,56]。しかし、水資源中でのCoVの生存は、温度、日光、およびウイルスが容易に吸着し、病原性微生物のような悪条件から身を守ることができる有機化合物の存在など、いくつかの環境要因に依存している。WHOによって報告されているように、汚染された飲料水を介したヒト型CoV感染の証拠はない[57]。一般に、コーティングされたウイルスは、環境的にあまり好ましくなく、酸化剤に対してより敏感であり、例えば、SARS-CoV2は、塩素との接触により、ヒトの腸内ウイルスよりも迅速に不活化される可能性が高い[53]。
食品、食品パッケージ、および食品取扱者による感染
SARS-CoV2の食品、食品パッケージ、食品取扱者を介した感染は、COVID-19病の原因とは特定されていない。しかし、利用可能な証拠によると、ウイルスは数時間から数日の間に表面に存在しており、したがって、疾病管理予防センター(CDC(アメリカ疾病予防管理センター))[58]が提案しているように、洗浄と消毒が感染を制御するための最良の方法である。定期的な手洗い、生肉と他の食品の分離、高温調理、冷蔵庫での保管など、食品の収集、移設、準備の際には消毒が厳しく推奨されている[59,60]。食品の準備・配布において調理に携わる者は、エプロン、マスク、手袋、帽子の使用など、完全な個人衛生を維持することを強く推奨する。さらに、くしゃみや咳の際には肘を曲げて鼻や口を覆うこと、COVID-19の症状を持つ従業員やこれらの患者との個人的な接触を隔離すること、人と人との間に最低6フィートの距離を保つことも推奨されている。また、職場での手洗い・消毒のための複数のポイントを設け、希釈次亜塩素酸ナトリウム(0.1%)による接触の多い表面の洗浄・消毒を行うことも推奨される[59]。
実験室調査とSARS-CoV2
COVID-19症例の適切な診断のためには、非常に高感度で正確な実験プロトコルが必要である。確定症例、動物のリザーバー研究、接触者の追跡、感染のコントロールのために重要である。急性診断を開発するためにウイルス培養を使用することは実行可能ではない、なぜなら、SARS-CoV2がVeroE6細胞のような特定の細胞株において明白な細胞病理学的効果を誘導するのに典型的には3日かかるからである。通常、SARS-CoV2の診断は、ほとんどの医療施設では利用できないバイオセーフティレベル3の研究室で行われる。血清抗体抗原迅速検出検査は、陰性の結果が得られる可能性があるため、規制当局は承認していない。このような欠点のため、逆転写ポリメラーゼ連鎖反応(RT-PCR)が世界的に最も成功しているCOVID-19スクリーニングツールとなっている[61]。パンデミックの初期には、完全なSARS-CoV2ゲノムへのアクセスが可能であったため、適切なプライマーとSARS-CoV2の検出のための標準的な実験手順を生産することができた。RT-PCRアッセイは、SARS-CoV2のRdRp、エンベロープ(E)およびヌクレオカプシド(N)遺伝子のいずれかを標的とするように設計されている[61]。汚染物質の混入やサンプリングの不備により、偽陽性や陰性結果が出る可能性が高くなる。世界中のいくつかの研究室でRdRpベースのRT-PCRアッセイの使用が開始されている[61]。
一般的に、SARS-CoV2は、症状の発症前に上気道サンプルから 1~2日以内に検出されることがある[62]。中等度の症例では7~12日、重度の症例では14日までウイルスが存在し続けることもある[62]。ウイルスRNAはまた、COVID-19感染者の約30%の便中に、発症5日目から、中等度の症例では4~5週間まで検出される。糞便ウイルス脱落が感染に重要であるかどうかの検査も実施しなければならない[34]。シンガポールでは、鼻咽頭吸引液からのウイルス脱落の増加が、症状発現から 24日後まで観察されている[63]。ドイツでは、徐々に回復した患者で高喀痰ウイルス負荷を伴う長期的なウイルス脱落が観察された[64]。長期間、体液中にウイルスRNAが存在する場合があるが、これはまだ感染していることを意味するものではない[65]。ウイルスの病原性を実証するためには、ウイルス分離にウイルス培養を用いることが必要である。Hoehlら[65]によると、感染性ウイルスを持つ無症候性の症例が2例見つかっている。SARS-CoV2陰性を確認するためには、上気道検体を用いて24時間以上の時間間隔をおいて2回の連続検査を行うことが推奨されている[66]。症状のある人の検体採取は、発熱がない状態で7日以上3日以上経過した後に行うべきである。しかし、最初に陽性反応が出た後、ウイルス排出を記録するための検査を受ける前に、無症候性の患者では14日間観察する必要がある。SARS-CoV2特異的IgG抗体を報告するための血清学的検査は、適切に検証され標準化されれば有用である[66]。RT-PCRの使用は、別々のイベントで2つの別々の遺伝子を標的にするように設計されるべきであるが、陰性として患者を退院させることが重要である。RT-PCRの使用は、別々の事象で2つの異なる遺伝子(例えば、E-遺伝子およびRdRP)を標的とするように設計されるべきであることは、陰性として患者を退院させるために重要である。
気候要因と SARS-CoV2 感染
感染症の発生と蔓延は、様々な環境条件に依存している。科学者は、この発生に関与するいくつかの要因を発見した。いくつかのウイルスの伝播が気候的要因と関連しているという情報があるが、他の要因については外挿はされていない。インフルエンザウイルスの制御された実験室での実験では、絶対湿度がウイルスの感染に有利であることが示された[67]。この結果は最終的にインフルエンザの疫学的傾向と相関しており、このメカニズムは他の呼吸器ウイルスにも及ぶと考えられている。CoVの感染における湿度の重要性を明らかにした詳細な研究はまだない。研究では、熱帯および亜熱帯地域がウイルス感染に最も適した地域であることが明らかにされている[68]。温帯地域の乾燥した冷気がインフルエンザの感染を阻害していると結論づけるのが妥当である。しかし、CoVsにとってこの因子の重要性はまだ決定されていない。人々は通常、冬の季節には家にいることが多く、夏に比べて換気が少なくなる。
学校は感染症の感染源となる場所である。呼吸器ウイルス感染症の感染は、学校の日中に増加することが観察されている[69]。したがって、学校は水痘、麻疹、インフルエンザなどの感染症のコントロールに影響を与える。学校は限られたエリアに多数の生徒が集まる場所であり、湿度が高い確率が高くなる。いくつかの呼吸器ウイルスの発生率は、興味深いことに年齢層によって変動していた[69]。これまでのところ、COVID-19陽性に分類された子どもはわずかで、これは子どもたちが感染しにくいことを示唆しているかもしれない(欧州疾病予防管理センター)。しかし、COVID-19陽性の小児は感染性もある。したがって、無症状の子供は感染のリスクを高める。学校の閉鎖は、SARS-CoV2の感染を減少させるのに役立つと結論づけることができる。免疫学的には、健康な人の免疫システムは冬よりも夏の方が優れているとされている[70]。また、メラトニンが免疫応答にどのような影響を与えるかという研究も報告されている。主に季節性があり、夏に多くの免疫応答が観察されている[71]。別の研究では、ビタミンDが免疫系を高めることも報告されている[72]。このビタミンの調節には、夏にほとんど利用できる日光が必要である。ビタミンDの補給が呼吸器ウイルス感染症の発生を減少させるのに役立つというのは確固たる信念である[73]。COVID-19回復の重要な研究分野である。季節変動に関係なく、ウイルス感染症のパンデミックは指数関数的に増加し、平準化し、時間の経過とともに減少すると予測されている。しかし、気候変動と季節性は、SARS-CoV2感染に大きく影響する可能性がある。
COVID-19 生存率と予測因子
CoV は通常、消化管および呼吸器管を介して伝播する。これらのウイルスは通常、脆弱な人々に感冒を引き起こし、重篤な影響を及ぼすことなく自然に回復するのに対し、MERS、SARSは慢性肺炎や胃炎を引き起こす可能性がある[74]。体内からのウイルスの流出と伝達は、感染後6日以内に起こり、4日後にピークに達する[75,76]。COVID-19が生き残り、感染するために必要な環境因子は非常に明らかである;しかしながら、動物のCoVとは異なり、COVID-19の感染の自然因子についての情報はほとんどない[77]。温度および湿度とCOVID-19の感染との関係を見いだした先行研究はごくわずかである。
温度と湿度
気温が人の健康に与える影響は、国から国、さらには地域によっても異なる。SARS-CoV2やインフルエンザウイルスの感染は気温の影響を大きく受けることが明らかになっている。また,新型COVID-19やインフルエンザウイルスは温度によっても感染することが明らかになっており,これはSARS-CoV2の感染にも当てはまる.SARS-CoV2は、寒冷地では宿主の免疫力が弱まり、本来の機能を発揮できなくなる可能性が高いため、気温が低くなると急速に感染が拡大する可能性がある。その結果、宿主の中で感染の脆弱性が急速に高まる。逆に、SARS-CoV2は高温(38℃)になると生存率が低くなる。CoVサンプルを用いて、相対湿度と温度の様々な条件で研究を行った。その結果、湿度30%および50%の条件でそれぞれ27時間および67時間の半減期が観察された。また、湿度80%では3時間の半減期が観測された。このシナリオは他の季節性インフルエンザでも報告されている[75]。したがって、湿度の上昇に伴う温度の低下はウイルスの半減期に大きな影響を与える。
いくつかの臨床試験の報告では、適切なマスクを使用することで飛沫感染を回避できることが示唆されているが、エアロゾルの形態での飛散を保護することは非常に困難です[78, 79]。ある研究では 2003年に香港でSARSウイルスがエアロゾルと欠陥のある下水道システムによって拡散し、多くの人が死亡したことが報告されている[80]。同年、3時間のフライトで22/122人の旅行者がSARSに感染したという事件があった[81]。不思議なことに、半径2m圏外の人が、飛沫やエアロゾルでは感染しないウイルスの曝露に巻き込まれた[82]。飛沫やエアロゾルのみで感染したとは断定できないが,航空機内の低相対湿度がSARSウイルスの生存率を高めたと考えられる.その後、別の研究では、航空機内でのCoVの伝播リスクは取るに足らないと報告されている[83]。カナダの研究では、開放型酸素マスクがCoVの感染を促進することが報告されている。ウイルスは空気中の飛沫を介してマスクから拡散する可能性があるため[84]、開放型酸素マスクから吐く空気がウイルスを感染させ、医療サービスへの脅威となる可能性があると考えられる。高温多湿の環境下でSARSおよび関連ウイルスが酸素を含んだ空気中でどのように生存し、感染するかを評価するために、今後の研究が必要とされている。病院で行われた研究では、ウイルスはエアロゾルを介して感染する可能性があることが報告されている。また、適切な換気システムが病気の広がりを緩和できることも報告されている[85]。COVID-19は26℃以上の温度では持続しないが、皮膚には5~10分程度、プラスチック材料には6~12時間、金属には12時間程度留まると考えられている(図2)。
図2
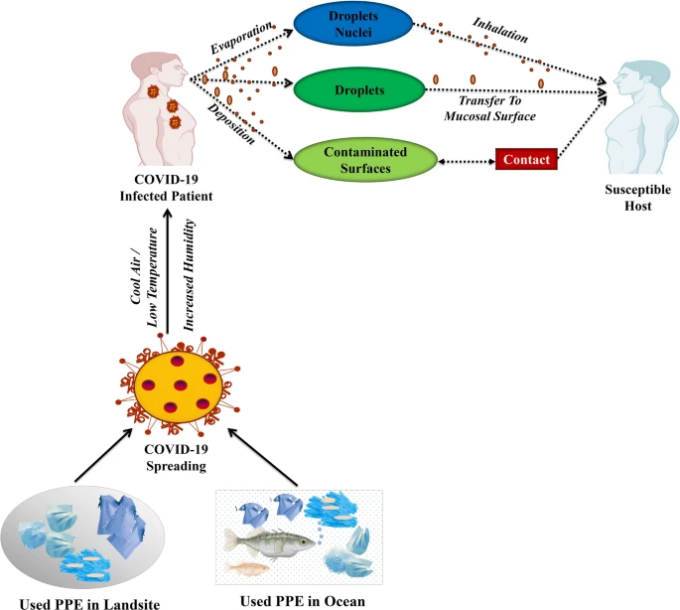
図2 陸上サイトや海洋での使用済みPPEはCOVID-19の伝播を広げる。COVID-19の感染拡大には、低温・高湿度の環境が関係している。また、飛沫の飛散や汚染された場所への接触により、COVID-19の感染が拡大する可能性がある。
皮膚とCOVID-19
研究者は、COVID-19試験にヒト検体の代わりにヒトCoV229E(HCoV-229E)を使用している。最近の研究では、約45%の手感染ウイルスが存在し、1時間後も生存していることが報告されている[86]。このウイルスの生存時間は、わずか10分後に消失するパラインフルエンザウイルス3型よりも長い。別の研究では、ヒトの手指を水とアルコール手指消毒剤で洗浄してウイルス反応を調べている。その結果、HCoV-229Eの濃度は、水を用いた場合は30秒以内に70%減少したのに対し、アルコール手指消毒剤を用いた場合は99.99%減少したことが判明した[87]。この研究は、COVID-19のような感染症の予防と管理のための適切な衛生と消毒の重要性を強調している。
環境表面
このようなウイルスの特徴に関するエビデンスは、特にCOVID-19のみを考慮した場合、まだ限られている。ウイルスの表面生存は、環境や公衆衛生に脅威を与える。病院、手術室、清潔な待合室を考慮に入れれば、特にCOVID診療科でははるかに大きな問題である。様々な表面や消毒剤との接触でウイルスがどのように作用するかを理解するためには、臨床現場の消毒が不可欠かもしれない[88]。病院の手術室では、器具は特定の目的のためだけに使用されているが、移乗物も汚染源となりうる[89]。COVID-19患者の病院におけるCoVの存在は、Ongらによって評価された[90]。存在は便器や流し台にも見られたが、部屋を清掃した後の空気にはCoVは含まれていなかった。表面の特性に応じて、異なることがわかったCoVの生存時間は、プラスチックやスチールなどのあまり多孔質ではなく、彼らは、活性ウイルスを保持し、より迅速に液滴を保持するため、圧倒的に最悪である。また、室内の空気量や湿度は、様々な環境要因の影響を受ける可能性がある[3]。エアロゾルや表面のウイルスは、数時間から数日の間も生存可能な状態を保ち、伝染することがあるため、エアロゾルや表面のウイルスの感染も可能である[3]。Kampfら[4]は、CoVは最大9日間表面に生息し,0.1%次亜塩素酸ナトリウムまたは62-71%エタノールを1分間、表面消毒剤として使用すべきであると報告している。換気の悪い環境では、大きさが0.1μm未満のウイルス粒子が二次エアロゾルとして大気中に残る可能性がある。研究では、くしゃみから最大200万個の飛沫が空気中に放出される可能性があり、咳からは100万個以下、大声で話すことからは約3000個の飛沫が放出されることが示唆されている。100μmを超えると、2mの高さから気道から排出された液滴は、3~6秒で平らな面に落下し、水平方向に約1.5mに衝突した後、容易に蒸発し、乾燥して固形物となる。この物質は2~3μmの大きさになる[88]。SARS-CoV2感染の予防における換気の良い環境の重要性については、まだ十分な検討がなされておらず、ウイルス粒子が限られた環境での距離から危険な濃度に到達する能力については十分な試験が行われていないが、大気中の換気を改善することで、空気感染症の感染伝播を最小限に抑えることができると考えられている。
気候変動
暖かい季節が始まるとCOVID-19が劇的に低下すると結論づけることができる科学的研究はこれまでにない。COVID-19の減少を予測するには、より多くの時間が必要である[91]。いくつかの研究では、COVID-19が最も苦しんできた場所での一般的な気象パターンを想定している[92]。地球の東と西の国々の人口では、COVID-19はあまりパンデミックしていない。一方で,北と南の地域では有病率が高く,病気の発生を予測するパターンを支持していた[93].2020年1月の武漢市の平均気温と相対湿度は 2020年2月の中国の他の被災地とよく似ていることがわかった[94]。気象観測所では、気温は4~9℃であったが、武漢市では5~11℃であった。しかし、気候要因により都市部では 5~11℃であった[95]。COVID-19北半球での夏の始まりとともに、熱帯ではインフルエンザのようになり、南半球でも同時に感染することが予想される[96]。
COVID-19の医療廃棄物と自然生息地
このCOVIDパンデミックの間、WHOは、N95呼吸マスク、手袋、ガウン、フェイスシールド、およびゴーグルを含む個人用保護具(PPE)の使用を強く推奨している[97]。PPEの製造には、ラテックス、ポリウレタン、ニトリルゴム、ネオプレン、ポリ塩化ビニルなどの異なるタイプのポリマーが使用されている[98]。これらのPPEは耐液性があり、長持ちするため、廃棄しても環境から完全に破壊されることはない。2020年1月にOcean Asia NGOが香港で実施した調査によると、COVID-19が原因で、約700万人がマスク(1人または2人組)手袋、手指消毒剤を定期的に使用していることが明らかになった[99]。そのため、使用されるPPEの量は日に日に増加しており、環境が汚染されている。別の研究では、内海と海洋の両方の自然生息地が脅威に直面する可能性があることが確認されており、時には海洋魚が廃棄物を餌として摂取して死に至る可能性があることも確認されている[100]。WHOが明らかにした研究では、COVID-19への対応のために、マスク8,900万枚、手袋7,600万枚、ゴーグル160万枚の月間需要があると予測されている[101]。感染性廃棄物は病院だけに限ったことではなく、症状の軽い人や症状のない人がウイルスを含んだ廃棄物を作ることが多い。ウイルスは、見られるように、段ボール、プラスチック、および金属の中で数時間から数日生存することができるので、このような廃棄物を無差別に捨てたり、無駄にしたりすることは、廃棄物管理に関連する労働者の健康を危険にさらす可能性がある。廃棄物管理の従業員に適切なPPEが提供されていない先進国では、この状態はより深刻になる可能性がある。これらの国々では、雑巾拾いや非公式の廃棄物拾いの作業員は、現在、ウイルスに汚染された廃棄物に汚染される危険性の高い地域にいる。発展途上国の何百万人もの人々は、廃棄物の収集と処理施設を持っていない[102]。発展途上国では、廃棄物の収集、輸送、処分における最低限の健康安全性の問題を確保することが非常に急務である。他の主要な制限は、技術的専門知識の欠如だけでなく、開発途上国で廃棄物を処理するための他の科学的ツールや経済的支援の欠如である。
WHOは、医療機関があらゆる医療行為中に発生する廃棄物をバイオメディカル・ヘルスケア廃棄物(BMW)と表現している[103]。これらの医療行為には、獣医学や人間医学における診断、予防、治癒、緩和治療が含まれる。BMWには、鋭利なもの、伝染性のあるもの、病理学的なもの、化学的なもの、医薬的なもの、放射性廃棄物が含まれる。非有害廃棄物(85%)と有害廃棄物(15%)で構成されており、そのうち10%が感染性廃棄物、5%が化学廃棄物または放射性廃棄物である[104]。接触感染の危険性に加えて、BMWの取り扱い条件の悪さは、土壌や地下水の汚染、浄化システムにおける望ましい微生物の破壊、シャープスアイテムによる身体損傷など、環境への悪影響を引き起こす可能性がある[105]。SARS-CoV、エボラ、およびMERS-CoVの疾病の発生に関する最新の報告は、感染制御の実践のためのバイオメディカルおよびヘルスケア廃棄物の安全な取り扱いの必要性を実証している。意識と知識はCOVID廃棄物をより良く取り扱うための魔法のような解決策となりうるため、政府、地方自治体、廃棄物管理施設は、デジタルおよび印刷媒体を通じて人々と直接つながるための意識向上キャンペーンを開始する必要がある。
COVID-19と神経疾患
SARS-CoV2は脳感染と有意に関連しており、最近の証拠はCOVID-19を神経学的疾患にリンクさせている[106]。新たな研究の文脈では、COVID-19感染は、顕在化した神経学的疾患の臨床スペクトルを悪化させる可能性がある。さらに、アルツハイマー病、PD、およびMSの患者は、CoVの影響を受けることが多く、高リスクのカテゴリーにある[107]。SARS-CoV2感染はまた、インターロイキン(IL)-1,IL-6,IL-10,腫瘍壊死因子α(TNF-α)などの炎症性マーカーの発現を増加させ、ミクログリアの活性化に寄与する。活性化したミクログリアは、最終的にはアルツハイマー病、PD、MSなどの神経変性疾患を進行させる(図3)[108]。
図3 SARS-CoV2が引き金となる神経障害
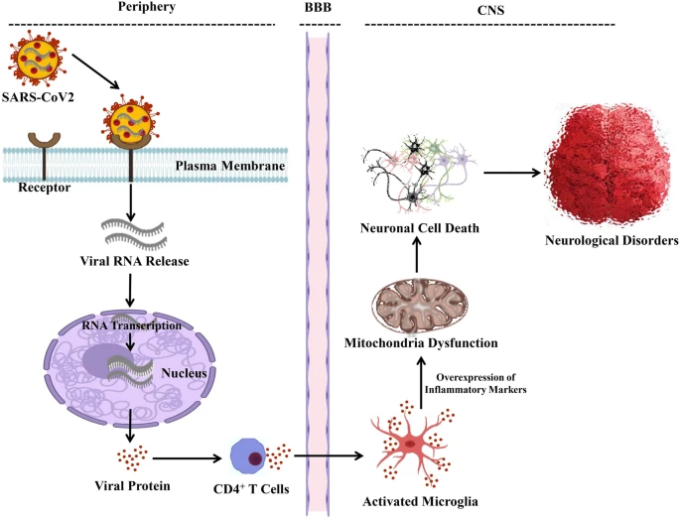
まず、SARS-CoV2は宿主細胞に侵入してウイルスRNAを放出し、そのRNAはタンパク質を凝集させてCD4+ T細胞となる。CD4+ T細胞はミクログリアを活性化し、高レベルのプロ炎症性マーカーを産生し、これらのマーカーはミトコンドリアの機能不全と神経細胞死を加速させ、神経障害の進行をもたらす。BBB、血液脳関門、中枢神経系、中枢神経系
COVID-19と認知症の脆弱性
アルツハイマー病を中心とした認知症は、高齢者の間でパンデミック状態として出現している[109]。そのため,COVID-19パンデミックにおける認知症の管理にはいくつかの懸念がある。第一に、認知症と加齢を含む2つの主要な危険因子の組み合わせがCOVID-19感染者の死亡率に役割を果たしている。第二に、認知症とCOVID-19パンデミックの併用による重篤な影響は、これらの脆弱な患者の神経認知機能への隔離と社会的距離の影響を含めて、さらに研究する必要がある。実際、SARS-CoV2感染後、高齢者は死亡率が高くなりやすい。すべてのCOVID-19関連死の平均年齢は81歳であり、80歳以上の人の症例死亡率は20%以上であると推定されている[110]。それにもかかわらず、特に80歳以上の高齢者に焦点を当てた報告は限られており、高齢者のCOVID-19に関するデータは不十分である[111,112,113]。さらに、これらの研究は認知症のない高齢者を対象に行われた。この集団では、Covinoら[114]は、認知症と年齢という2つの主要な危険因子が共存している場合のリスク層別化を明らかにした[114]。イタリア中部の別の研究では、死亡リスクは年齢に依存しないかもしれないが、重度の認知症がこれらの集団では関連する危険因子である可能性があることが観察された[114]。さらに、Bianchettiら[115]は、SARS-CoV2感染により入院した患者の臨床症状、転帰、認知症の有病率を評価した。北イタリアに入院した627人の調査結果をレトロスペクティブに調査したところ、認知症に罹患した人は、認知症のない人に比べて死亡率(約40%)が高いことが観察された [115]。これらの知見を総合すると、COVID-19患者、特に認知症後期の場合、認知症が死亡率の重要な危険因子である可能性があることが示唆される(図1)。
COVID-19とパーキンソン病の脆弱性
COVID-19とパーキンソン病を含む運動障害との間には関連性がある。20年以上前に、PD個体の脳脊髄液中にCoVに対する抗体が存在することが明らかになった[116]。さらに、CoVは鼻腔を介して脳に到達することがあり、最終的には低汗症/無汗症を引き起こす可能性がある[117]。嗅覚過敏はパーキンソン病の通常の前運動の特徴であり、嗅球は病的なα-シヌクレイン沈着の主要標的である[118]が、これは単なる偶然の一致ではないかもしれない。Stoesslら[119]は、同程度の年齢と併存疾患を持つ患者と比較して、運動障害を持つ患者がCoV感染を起こしやすいという証拠はまだないと報告している[119]。Fasanoら[120]は、イタリアのミラノで行われた別の研究で、パーキンソン病患者におけるCOVID-19感染の予測因子/特徴とその結果について言及している。これらの研究者は105人のパーキンソン病患者を検出し、そのうち73人がCOVID-19感染の可能性があり、32人がCOVID-19感染が確認された。その結果、軽度から中等度のパーキンソン病患者におけるCOVID-19のリスク、死亡率、罹患率は、一般の人と比較して変化していないことがわかった[120]。さらに、日本では、肺炎で入院したパーキンソン病患者は、性別と年齢を一致させた患者と比較して、院内死亡の頻度が低かった[121,122]。対照的に、少数の高齢で疾患期間が延長したパーキンソン病患者では、死亡率が有意に上昇するとともに、COVID-19感染に対して主に脆弱であることが観察された[123]。これらの結果をまとめると、PD個体は年齢に関連した標的、疾患に関連した呼吸筋硬直、および複数の合併症の存在に対して特別に感受性の高い集団である可能性があるにもかかわらず、パーキンソン病はSARS-CoV2を介して感染し、COVID-19を発症するリスクを上昇させないことが示されている。
COVID-19と多発性硬化症の脆弱性
MSは、疾患の免疫学的性質および最終的にCOVID-19の脆弱性を上昇させる免疫応答を変化させることができる疾患修飾療法(DMT)による臨床管理のために、人々に特に関心を示す可能性がある。可能性のある危険因子を一次的に検出することは、COVID-19パンデミック期間中、これらの重要な患者の臨床管理に関する特定のアプローチを選択するために重要である。MSとCOVID-19との関連は複雑である。CoVファミリーはMSとの潜在的な関連性について研究されており、最近ではMSのマウスモデルの開発に利用されている[124]。世界的に見ても、多発性硬化症患者、特に免疫調節療法や免疫抑制療法を受けている患者におけるウイルス感染のリスクを分類することは、神経内科医にとって困難な作業である。仮説的に多発性硬化症患者は一般の人に比べて感染症のリスクが高いと報告されているが、多発性硬化症患者はSARS-CoV2感染症やCOVID-19の発症リスクが高いかどうかについては、まだ議論がある。Willisら[124]は、これらの疑問に答えるために3つの関連論文を検討した。その中で、2つの大規模なデータベースを利用して追跡期間を延長した最初の研究では、MSを持たない患者群と比較して、多発性硬化症患者の感染リスクを区別することに焦点を当てている[124, 125]。その結果、多発性硬化症患者は一般的に感染症のリスクが高く、入院を必要とすることがわかった。
一方、2番目の研究では、一般的に使用されているDMTsとリツキシマブ(すなわち、MSで頻繁に使用されていることが明らかになった)に関連した重篤な感染症のリスクを調べた[124, 126]。興味深いことに、DMTsを投与された多発性硬化症患者は一般的に感染症のリスクが高く、一方でリツキシマブの使用は重症感染症の最も高い割合と関連していた[124]。感染症リスクとMSのDMTsとの関連性は、集団ベースのレトロスペクティブコホート研究で評価されている[127]。さらに、彼らの主な所見では、第二世代のDMTの導入はリスクの上昇と関連していたが、第一世代は関連していなかったことが確認された。Louapreら[128]は、男性性、進行性MS、EDSS、肥満、糖尿病、肺・心血管疾患などの併存疾患が危険因子として認められたことを明らかにした[128]。それにもかかわらず、一変量解析では、DMTsの使用は入院リスクを含むSARS-CoV2感染の重症度とは関連していなかった[128]。これらの結果をまとめると、主に多発性硬化症患者におけるCOVID-19感染のリスクが高いことが明らかになったにもかかわらず、多発性硬化症患者の推定リスクについてはまだ議論があることが示された。
結論
このレビューでは、SARS-COV2の伝播を減少させることに寄与する可能性のある気象パラメータを強調している。COVID-19の発生を抑制するためには、この生命を脅かすウイルスの感染を食い止めるためにさらなる対策を講じる必要がある。しかし、ゲノミクスや感染様式については現在まで議論の余地がある。その結果、COVID-19の発症の背景にある遺伝的多様性と感染様式を明らかにした。すべての人は社会的距離を保ち、PPEを着用すること。他国から来た人やCOVID-19感染地域を旅行する人は、14日間の隔離を維持してほしい。重症者は医師に連絡し、十分な治療を受ける必要がある。さらに、環境因子はCOVID-19の発症や神経障害と有意に関連している。神経障害の発症に関連する正確なメカニズムを理解するためには、さらなる研究が必要である。
