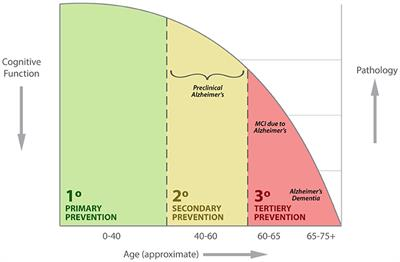
A Population Perspective on Prevention of Dementia
www.ncbi.nlm.nih.gov/pmc/articles/PMC6617301/
要旨
世界の認知症患者数は2050年には1億3,000万人に増加すると予測されている。観察研究から得られた広範なエビデンスに基づいて、認知症患者の約30%は潜在的に修飾可能な危険因子に起因していると推定されている。このことは、これらの因子を標的とした介入が認知症の発症を遅らせたり、予防したりする可能性を示唆している。
認知症患者の大多数は中低所得国に住んでいるため、このような介入は、幅広い医療システムで簡単かつ安価に実施できるものでなければならない。しかし、現在までのところ、認知症予防試験の結果は、これらの危険因子を治療することで認知症のリスクが低下するという説得力のある証拠を示していない。
本論文では、認知症予防の可能性について、利用可能なエビデンスを概観することを目的としている。特に、効果的な認知症予防介入の開発を複雑にする可能性のある方法論的な問題を議論し、今後の認知症予防研究の機会と課題を探る。現在進行中の試験や計画中の試験では、高リスク集団における認知症リスクに対するマルチドメイン介入の効果が検証されている。
将来の認知症戦略は、世界的に増加する認知症の有病率を抑制するためにも、個人、コミュニティ、集団レベルでの介入を通じて、より広範な集団を対象とすることが望ましい。
キーワード
認知症予防、アルツハイマー病、血管リスク因子、マルチドメイン介入、公衆衛生
1. 後期認知症への視点の変化
認知症の臨床像は何世紀にもわたって認識されてきたが、その原因についての説は時代とともに大きく変化してきた。認知症が特に注目されるようになったのは、1907年にアロイス・アルツハイマーが「大脳皮質の特殊な疾患について」という有名な症例報告を発表したときである[1]。進行性の認知障害を持つ51歳の患者の脳内にプラークやもつれが見られたことは、エミール・クレーペリンの代表的な精神医学の教科書に掲載され、「アルツハイマー病」(Alzheimer’s disease)[2]という用語で呼ばれるようになった。それ以来、アルツハイマー病は比較的若い人にプラークやもつれを介して認知症を引き起こす稀な疾患であると考えられてた。人生の最後の数十年での認知機能の低下は、当時は老人性認知症と呼ばれてたが、動脈硬化や脳卒中に起因するものと考えられ、別個の疾患と考えられてた[3]。
70年代初頭以降、老人性認知症の病態は、認知症高齢者の脳内に大量の細胞外アミロイド沈着(プラーク)と高リン酸化タウ蛋白(タウ蛋白)の細胞内沈着が発見されたことに基づいて、血管メカニズムからアルツハイマー病の病態へと変化した[4]。その結果、老年性認知症と老人性認知症の峻別が薄れていた。90年代初頭には、アポリポ蛋白E(APOEε4)の特異的なe4対立遺伝子が早期認知症と後期認知症の両方に関連していることが発見され[5,6]、アルツハイマー病が早期認知症と後期認知症の優勢な原因であるという仮説が支持された。この時点では、血管性認知症はまだ認知症の原因としては別個のものであり、頻度は低いと考えられていた。
後期認知症の発症における血管病理の役割が再び注目されるようになったのは90年代後半で、いくつかの疫学的・放射線学的研究で心血管系の危険因子や疾患と認知機能障害との強い関連性が報告されたからである [7,8]。これらの所見は神経病理学的所見によって裏付けられた。102人の高齢修道女の脳の検査では、アルツハイマー病病理の存在とラクナ梗塞との間の認知機能に対する強い相互作用効果が示唆された[9]。死亡時の年齢の中央値が85歳であった英国の人口ベースのコホートを対象とした大規模な剖検研究では、ほとんどの認知症患者は脳血管障害とアルツハイマー病障害が混在していたのに対し、認知症のない被験者はかなりのレベルの障害を持っていたり、全く障害がなかったりすることが多いことが示された[10]。それ以来、多数の疫学研究で血管リスク因子または血管疾患と脳卒中発症と後期認知症との関係が調査されてきた[11,12,13]。最近のいくつかの研究に基づいて、APOEε4対立遺伝子を持つなどの遺伝的因子と血管因子の存在と相互作用が、アミロイド斑、高リン酸化タウを含むタングル、およびさまざまな血管病変を含む複数の脳疾患の発症に関与していると考えられている[14,15,16]。これらの脳病理はいずれも軽度認知障害(MCI)および認知症を発症する可能性を高めるが[17]、発症、経過、または特定の臨床症状のいずれかを完全に説明するには不十分である。
2. 認知症予防の機会の窓を探る
多面的な脳疾患が原因の認知症という概念は、認知症の予防と治療のための幅広い戦略の可能性を示唆している。このような戦略の必要性は 2015年には4,700万人だった認知症患者が2050年には1億3,000万人以上に増加すると予想される世界的な認知症患者数の多さによって強調されている[18]。認知症患者の90%は75歳以上、75%は80歳以上と推定されている[19]。認知症に罹患していない人でも認知症を予防する戦略をとることで、認知症の発症を遅らせ、認知症の有病率を下げることができるかもしれない[20]。2050年までに認知症患者の68%が中低所得国(LMIC)に居住することが予想されているため[18]、このような戦略は理想的には、さまざまな医療システムで大規模に実施することが容易で安価であるべきである。
観察研究では、認知症リスクに関連する多くの修飾因子が示唆されており、予防の対象となりうる。血圧の上昇、肥満度(BMI)総コレステロール値の上昇 [21,22,23,24,25,26]、糖尿病 [27]、喫煙 [28]、うつ病 [29]、身体活動の低下 [30]、認知活動の低下 [31]、食生活の低下 [32]、教育水準の低下 [33] は、認知症リスクの増加と独立して関連している確立された因子である。修正可能な認知症リスク因子を個人レベルでわずかに改善するだけでも、これらのリスク因子が世界的に高い有病率であることから、人口レベルで認知症患者を大幅に減少させることができる可能性がある[34]。7つの認知症危険因子(糖尿病、中年期高血圧、中年期肥満、運動不足、うつ病、喫煙、低学歴)の集団帰属リスクを計算し、相互関連性を考慮した結果、全世界の認知症患者の30%がこれらの修飾可能性のある危険因子に起因すると推定された[35]。このことは、認知症予防には大きなチャンスがあることを示唆している。
これらの修正可能な因子の高い有病率は、人口ベースの予防戦略が認知症の有病率を減少させることができるかどうかという問題を提起している。長年にわたり、多くのコミュニティプログラムは心血管疾患(心血管疾患)のリスクを減らすために設計されてきた。管理されたビフォーアフター研究では、一般的に、これらのプログラムは心血管疾患の危険因子を改善し、場合によっては心血管疾患の発症と死亡率を減少させる効果があることが示されている[36]。心血管疾患と認知症の危険因子はほぼ同様であるが、地域社会の予防プログラムが認知機能や認知症に及ぼす影響を研究した比較研究は行われていない。しかし、5つの大規模研究では、明確に定義された地理的地域における2つの時点間の認知症発症を比較している。5件の研究のうち4件で認知症の有病率がわずかに減少したことが示されたが、これは教育の改善、血管疾患の予防と治療の改善など、人口レベルの投資に起因する可能性がある[37]。
3. 認知症予防試験
過去20年の間に、ベースラインで認知機能障害のない人を対象に、個々の危険因子や全体的な認知症リスクプロファイルを改善することで認知症を遅らせたり予防したりできるという仮説を検証するために、いくつかの介入研究が行われてきた。我々は、単一の危険因子を標的とした単一領域の介入と、複数の認知症危険因子を同時に標的とした複数領域の介入を区別している。以下では、認知症を一次アウトカムまたは二次アウトカムとしたこれらの研究について述べる。
3.1. 単一ドメイン介入
潜在的な介入のリストは非常に長いが [38] 、臨床試験およびメタアナリシスからの最も確実な証拠が利用可能な介入に我々の概要を限定する。そのため、ここでは網羅的なものにするつもりはない。
高血圧の治療は血圧低下メカニズムを介して認知症のリスクを低下させるが、他の、おそらく降圧クラス特異的な効果を介してもよい [21,39,40,41]。高血圧試験の結果は心強いものであったが、まだ結論は出ていない。認知症を主な転帰とした降圧治療の4つのプラセボ対照試験のメタアナリシスでは、複合リスク比は0.87(95%CI 0.76~1.00;N = 16,595人;N = 786人の認知症症例)であり、治療が有利であることが示された [42]。最近のメタアナリシスでは、2つの生活習慣介入を含む9つの血圧低下試験が含まれており、追跡期間中央値は3.9年であった。プールされた認知症発症リスク比は0.93(95%CI 0.84~1.02;N = 57,682;N = 2131例の認知症)であった[43]。最近発表されたSystolic Blood Pressure Intervention Trial. 最近発表された収縮期血圧介入試験:減少した高血圧における記憶と認知のサブスタディ(SPRINT-MIND)は、高血圧患者9000人以上(50歳以上)を対象に、120mmHg未満を目標とした任意の薬剤による集中的な血圧治療が、140mmHg未満を目標とした標準的な血圧コントロールと比較して、認知症の発症を減少させるかどうかを評価した。この試験は、介入群で心血管イベントと全死亡率に有益な効果があったため、早期に終了した。事前に計画された二次解析では、介入期間中央値が3.3年、追跡期間中央値が5.1年で、推定認知症(HR 0.83;CI 0.67~1.04;N = 8563;n = 325例の認知症)に対する有意な効果は認められなかったが、偶発的MCI(HR 0.81;CI 0.69~0.95;N = 8563;n = 640例の推定MCI)の有意な減少が認められた [44]。観察研究[21]からの有望な結果にもかかわらず、これら2つのメタアナリシスと最近のRCTは、血圧治療によって認知症を遅らせたり予防したりすることができるという説得力のある証拠を提供できなかったが、ポイント推定値は一貫して潜在的な予防効果を示唆している。
2型糖尿病(2TD)は、脳血管障害、インスリン抵抗性、ミトコンドリア機能障害などのさまざまな機序により認知症リスクを増加させる可能性がある[45,46]。最近のシステマティックレビューでは、異なる2型糖尿病治療戦略の認知機能と偶発的な認知症への影響を評価するための7つのランダム化比較試験が同定された[47]。有効性の解析には3つの研究が含まれており、認知機能または認知症の発症をアウトカムの指標としていた。3件の研究はいずれもバイアスのリスクが不明瞭であった。これらの研究のうち2件は、集中的な血糖コントロールと標準的な血糖コントロールを比較したものであった [48,49]。5年間でミニ精神状態検査(MMSE)で3点以上低下した参加者の数に関しては、両群間に有意差はなかった(RR 0.98;CI 0.88~1.08;N = 11,140人)。 08;N = 11,140人;1研究)認知症の発症(RR 1.27;CI 0.87~1.85;N = 11,140人;n = 109人;1研究)[49]、または40ヵ月後のMMSEスコア(MD -0.01;CI -0.18~0.16;N = 2794人;1研究)[48]。3件目の研究では、グリベンクラミドとレパグリニドを比較した。12ヵ月後、MMSEスコアに対するglibenclamideのわずかな優位性が認められた(MD -0.90;CI -1.68~-0.12;N = 156人;1研究)[50]。
観察的証拠 [23,24] にもかかわらず、現在までにコレステロール低下治療が認知症リスクに有益な効果を示した試験はない。システマティックレビューでは、心血管リスクが高い人の認知機能の低下と認知症の発症に対するスタチンとプラセボの効果を比較した2つのRCTが同定された。どちらの研究もバイアスのリスクは低かった。認知症の発症に関しては、シンバスタチンとプラセボの間に差は認められなかった(OR 1.00;CI 0.61~1.65;N = 20,536;認知症症例数62例;1研究)。5つの異なる認知テストで評価された認知機能には、シンバスタチンまたはプラバスタチンの効果は認められなかった[51]。現在のガイドラインによると、心血管疾患の予防を目的としたスタチン処方の対象者は、40歳から75歳までの非常に高い割合である[52]。脳卒中の予防は認知症のリスクを低下させる効果が期待できるが、その効果についての直接的なエビデンスは今のところない。
身体活動は、神経新生、血管新生、シナプス可塑性の亢進や抗炎症作用など複数の機序で認知症リスクを低下させると考えられている[53]。さらに、身体活動は、肥満、脂質異常症、高血圧などの認知症リスクに関連する他の因子にも有益な効果をもたらす可能性がある。最近のシステマティックレビューでは、認知機能障害の診断を受けていない成人の認知機能に対する身体活動介入の有効性を評価するために、6ヵ月以上の追跡調査を行った32の試験が調査された。身体活動のみを対象とした研究には、有酸素運動トレーニング(6件、531人)レジスタンストレーニング(3件、315人)太極拳(1件、93人)が含まれていた。これらの試験からの証拠は、認知機能に対する有益な効果について結論を出すには不十分であった [54]。身体活動が肥満や心血管疾患のリスクに有益な効果をもたらすことから、身体活動を促進するための公衆衛生キャンペーンや公衆衛生の取り組みが広く行われている。現在までのところ、これが認知症リスクを低下させるかどうかは不明のままである。
3.2. マルチドメインの介入
修正可能な認知症リスク因子の組み合わせにさらされることは、認知機能の低下と認知症のリスクに相乗的な効果をもたらす可能性がある [55,56]。したがって、1つ以上の危険因子を標的としたマルチドメイン介入は、認知症予防を研究するためのより適切なアプローチである可能性がある。過去10年の間に、いくつかのマルチドメイン試験が実施され、幅広いサンプルサイズと追跡期間で様々な介入を試験してきた。認知症、MCI、認知機能低下を主要エンドポイントとした主なマルチドメイン介入試験について、サンプルサイズとフォローアップ期間の観点から考察する(表1)。
表1 マルチドメイン認知症予防試験。
| preDIVA | FINGER | MAPT | |
|---|---|---|---|
| サンプルサイズ | 3526 | 1260 | 1680年 |
| 年齢層 | 70〜78 | 60〜77 | 70歳以上 |
| 主な選択基準 | 痴呆ではないb | 認知症リスクスコア≥6平均値または少し低いレベルで認知パフォーマンス | 痴呆ではないb 記憶の不満または日常生活の制限または遅い歩行速度 |
| 介入 | 看護師主導の集中的な血管ケア | ダイエットアドバイス、運動、認知トレーニング、血管ケア | 認知トレーニング、身体活動と栄養に関するアドバイス、血管ケア+/-オメガ3多価不飽和脂肪酸 |
| 介入期間 | 6〜8年 | 2年 | 3年 |
| フォローアップ期間 | 6〜8年 | 2年 | 3年 |
| 主な結果 | 認知症、障害d | 認知機能c | 4つの認知テストの複合zスコアe |
| 主な二次的成果 | 心血管疾患、血管因子、認知機能低下、うつ病 | 血管およびライフスタイルの要因、抑うつ症状、障害 | 身体能力、うつ病 |
FINGER:Finnish Geriatric Intervention Study to Prevent Cognitive Impairment and Disability; MAPT. aは心血管リスク因子・加齢・認知症(CAIDE)リスクスコア、bは臨床診断なしでMini-Mental State Examinationが23以上、cは神経心理学的テスト・バッテリー(NTB)dはAMC Linear Disability Score、eはFree and Cued Selective Remindingテスト、Mini-Mental State Examination、Digit Symbol Substitutionテスト、Category Namingテストの項目で評価した。
オランダの集中的血管ケアによる認知症予防(preDIVA)[57]クラスター無作為化試験では、6年間の看護師主導の集中的多領域心血管ケア介入の認知症および障害の累積発生率に対する通常のケアとの効果が比較された。116の一般診療所がいずれかの条件に無作為に割り付けられた。70~78歳の認知症のない3526人が参加した。中央値6.7年の追跡調査の結果、98%以上の参加者で主要アウトカムデータが得られた。集中的な心血管ケアが認知症の発症(HR 0.92,CI 0.71~1.19,N = 3454人、N = 233人の認知症)と障害に及ぼす有意な効果は認められなかった。
認知障害と障害を予防するためのフィンランド老年医学介入研究(Finnish Geriatric Intervention Study to Prevent Cognitive Impairment and Disability:FINGER)[58]では、栄養指導、身体活動、認知トレーニング、修正可能な認知症リスク因子のモニタリングを含む多領域介入の認知機能に対する効果を、一般的な健康アドバイス(対照群)と、広範な神経心理学的テスト・バッテリー(NTB)で評価した。認知症のない60~77歳の患者1,260人を対象に、心血管リスク因子・加齢・認知症(CAIDE)リスクスコアで認知症リスクが6ポイント以上上昇した患者を無作為にいずれかの治療群に割り付けた。2年後、介入群は対照群と比較して標準化されたNTBでわずかに大きな改善を示した(1年あたりの変化スコアの群間差0.022;CI 0.002~0.042;N=1190人)。
フランスのMultidomain Alzheimer Preventive Trial(MAPT)[59]では、オメガ3多価不飽和脂肪酸の効果と、認知機能に対する認知訓練、身体活動、栄養をターゲットとしたグループセッションからなるマルチドメイン介入の効果を研究した。参加者は70歳以上で、主観的な記憶の不定愁訴、日常生活の1つの道具的活動の制限、または歩行速度の遅さのいずれかを持っていたときに資格があった。1680人の参加者は、4つのグループのいずれかにランダムに割り付けられた:オメガ3多価不飽和脂肪酸と組み合わせたマルチドメイン介入、プラセボとマルチドメイン介入、およびオメガ3多価不飽和脂肪酸と他の介入またはプラセボ単独での介入はない。3年後、治療群とプラセボ単独群のいずれかの間で、4つの認知テストの複合スコアで評価された認知機能に有意差はなかった:グループ間の差は0.093(95%CI 0.001~0.184;N = 1525人)であった。 184;N=1525人)複合介入群では0.079(95%CI -0.012~0.170;N=1525人)マルチドメイン介入+プラセボ群では0.011(95%CI -0.081~0.103;N=1525人)オメガ3多価不飽和脂肪酸群では0.011(95%CI -0.081~0.103;N=1525人)であった。
4. 観察研究と介入研究のギャップを説明する
多くの観察研究から得られた楽観的な結果と、認知症予防試験から得られた悲壮感のある結果との間には、かなりのギャップが存在する。したがって、血管因子は認知症リスクと因果関係ではなく、関連性を持っている可能性がある。しかし、Hillの因果関係の基準である一貫性や妥当性[60]はほとんど満たされている。現在のエビデンスでは、認知症、特に高血圧に対する予防的介入の保護効果を支持するものではないが、予防効果の方向にはむしろ一貫性のあるシグナルがある。さらに、認知症予防試験のデザインに関連した方法論の問題[61,62,63]がタイプIIのエラーを引き起こし、多領域介入の「真の」効果を隠蔽し、観察的証拠との明らかな矛盾を引き起こしていることも考えられる。
4.1. 対象者の年齢とJ字カーブ
認知症予防試験を設計する際の重要な課題は、対象者の最適な年齢範囲である。対象集団が若すぎると、若年層では認知症の発症率が低いため、フォローアップ期間やサンプルサイズが無理なものになる。逆に、年齢が高すぎる対象集団では、いくつかの危険因子と認知症の関係が年齢とともに複雑になるため、介入の有効性が低下する可能性がある[63]。後半生の血圧と認知症との関連はU字型またはJ字型の曲線に沿っていることが示唆されており、高値も低値も認知症リスクの増加につながるとされている[64]。これは血圧と心血管疾患の関係に関する十分な研究と一致している[65]。BMIに関しては、晩年の認知症リスクと同様のJ字型の関係が示唆されており、BMIが高いと認知症リスクが低く、低いと認知症リスクが高くなる[66]ことから、血圧と同様のJ字型曲線が示唆されている。同様に、晩年の総血清コレステロール濃度が高いことは認知症リスクの低下と関連している[24,67]。これらの関連の方向性がいつ変化するかは不明である。それにもかかわらず、上述した3つのマルチドメイン介入の対象集団は、年齢層がそれぞれ60-77歳、70歳以上、70-78歳であり、介入の恩恵を受けるには年齢が高すぎたと考えられる。このような複雑な関係性は、今後の認知症予防試験にとって大きな課題である。明らかに、1つのサイズがすべてに当てはまるわけではないが、年齢に関しては、血圧、BMI、コレステロールの最適な目標値が何であるかは、現在のところ不明である。
4.2. 対象者のリスクプロファイル
対象集団が利用できる標準的な予防ケアの質の高さとアクセスのしやすさは、試験で得られるコントラストの程度に影響する。DIVA以前の研究のサブグループ解析では、未治療の高血圧患者と心血管疾患の既往歴のない患者で介入の効果が最も強かったことが示されている [57]。3つのマルチドメイン介入試験では介入の効果が認められなかったのは、質の高い心血管系リスク管理が介入参加者と対照参加者の両方ですでに利用可能であったからである。そのため、今後の研究では、質の高い予防医療を受けられないリスクの高い集団を対象とする必要があるかもしれない。政策立案者や医療機関は、一般的に臨床試験には参加していないが、最もリスクの高い人々を積極的に対象とする必要があるかもしれない。
4.3. 対照条件におけるホーソン効果と治療効果
もう一つの課題は、いくつかのマルチドメイン介入試験で対照群の主要転帰および副次的転帰の改善が観察されていることである[57,58]。これは、DIVA試験前の両群の血圧の低下で示されている。ベースラインと追跡調査の間の収縮期血圧の平均差は介入群で8.3mmHg、対照群で4.6mmHgであり、開業医または専門医による治療の開始、またはベースラインの測定後の参加者によるライフスタイルの変化を示唆している。さらに、研究の認知に対する反応としての参加者または医療専門家の行動の変化(ホーソン効果)が役割を果たしている可能性が高い [68]。どちらのメカニズムも、介入条件と対照条件の間の「真の」対照を覆い隠し、タイプIIのエラーにつながる可能性がある。
4.4. 競合する死のリスク
認知症の最も重要な危険因子は年齢である。60歳から始まり、年齢が6.3歳上がるごとに認知症の発症率が2倍になる[18]。リスク因子が共有されているため、認知症予防試験は心血管系のエンドポイントに有益な効果をもたらし、結果として死亡率にも影響を及ぼす可能性がある。したがって、効果的な多因子介入は、死亡が遅れると逆説的に認知症発症率を高める可能性がある。このことを考慮しなければ、認知症予防介入の有効性を深刻に過小評価することになりかねない。
5. 今後の方向性
5.1. 限られた統計力に対処するための戦略
認知症予防試験を計画する際には、介入の最適なタイミングと認知症の発症までのタイムラグがあるため、十分なサンプル数と長い追跡期間が統計的な力を得るために最も重要である。したがって、これらの前提条件を考慮すると、認知症予防試験への資金提供は困難な課題であることに変わりはない。
追跡期間を長くするための一つの方法として、Syst-Eur試験[13]のように、オープンラベルでの試験延長が考えられる。しかし、このような観察研究の延長では、選択的な患者数の減少が複雑な要因となる。パワー不足を克服するためのもう一つの戦略は、他の(国際的な)研究グループとの共同研究であり、多国間試験の設計や、可能で適切な場合には過去の試験のデータのプールを可能にすることである。例えば、欧州認知症予防イニシアチブ(EDPI)共同事業は、FINGER試験、MAPT試験、preDIVA試験に参加した3つの研究グループを含む欧州の5つの研究機関の共同研究である[69]。
第三の戦略として、認知症の発症よりも早期に出現する可能性の高い主要アウトカムを選択することが考えられる。例えば、認知機能障害、既存の認知症リスクスコア、最終的に認知症に至る生物学的プロセスを反映していると推定されるバイオマーカーなどである。しかし、バイオマーカーと認知との関連性が不確かであるため、臨床的な関連性という点では最適ではない。
第四の解決策として、認知症リスクが高く、認知機能に障害がない人だけを対象にすることが考えられる。認知症リスクを推定するためには、バイオマーカー、画像診断 [70]、家族歴 [71]、認知症リスクスコア [72,73]など、数多くの戦略が存在する。しかし、家族歴や複数の認知症リスク因子の存在など、単純で容易に利用できるリスクマーカーは、低コストで大規模に適用できる。また、認知症リスクの高さを示すために認知機能低下の兆候を用いる研究者もいる。しかし、後者のアプローチでは、認知症の初期段階にある人を含めるリスクが相対的に高く、介入が効果的ではない可能性がある[74]。
第5のアプローチは、LMIC(低中所得国)のように予防医療の質へのアクセスが悪い集団を対象とすることである。認知症の発症率が比較的高く、高所得国(HIC)に比べて若年での発症がピークであることから、これらの人々は生活習慣の介入の有望なターゲットとなりうる[18]。さらに、これらの国の認知症危険因子の有病率はHICよりも高い[75]。
5.2. 現在進行中および計画されているマルチドメイン認知症予防試験
LMICで認知症予防を成功させるためには、認知症予防の介入は理想的には簡単に利用可能で、アクセス可能で、かつ手頃な価格であるべきである。これらの基準は、電子健康(eHealth)やモバイルヘルス(mHealth)のようなウェブベースの介入によって満たされることが多いが、特に最近では世界人口の大半がインターネットを利用しており、インターネットへのアクセスが限られている国では急速に増加している[76]。現在進行中または計画されている4つのマルチドメイン介入は、このようなデジタル認知症予防介入の有効性を検証するものである(表2)。
表2 計画的かつ進行中のマルチドメイン認知症予防試験
| HATICE | 認知症の予防に対するライフスタイルの変更の影響 | MYB | PRODEMOS | |
|---|---|---|---|---|
| 募集開始 | 2015年3月 | 2016年3月 | 2018年5月 | 2020年1月 |
| サンプルサイズ | 2724 | 3600 | 8500 | 2400 |
| 採用国 | オランダ、フィンランド、フランス | タイ | オーストラリア | イギリス、中国 |
| 年齢層 | 65歳以上 | 45〜75 | 55〜77 | 55〜75 |
| 主な選択基準 | 認知症ではない、2つ以上の心血管危険因子 | タイ国籍、認知症、糖尿病、COPD、癌、CVDの診断なし | 認知症や重度のうつ病の診断はありません | 認知症ではない、2つ以上の認知症の危険因子 |
| 介入 | 心血管リスク因子の自己管理のためのコーチがサポートするインターネットプラットフォーム | 食事、身体活動、飲酒、喫煙に関するコーチ支援のコンピュータープログラム | 身体活動、栄養、安心、脳トレーニングに関するデジタルモジュール | 認知症の危険因子を自己管理するためのコーチがサポートするスマートフォンアプリ |
| 介入期間 | 1。5年 | 3年 | 3年 | 1。5年 |
| フォローアップ期間 | 1。5年 | 10年 | 3年 | 1。5年 |
| 主な結果 | SBP、LDLコレステロール、およびBMIの複合zスコア | インシデント認知症 | グローバル認知複合ドメインスコアb | CAIDEスコア、実装結果 |
| 主な二次的成果 | 複合スコア、インシデントCVDからの個々の要因 | インシデントT2DM、CVD、癌、COPD、死亡率 | インシデント認知症、認知症リスク | CAIDEスコア、障害、費用対効果の個々の要素 |
BMI: body mass index; CAIDE. Cardiovascular Risk Factors, Aging, and Dementia risk score; COPD: chronic obstructive pulmonary disease; 心血管疾患: cardiovascular disease; HATICE: Healthy Aging Through Internet Counselling in the Elderly; Impact of Lifestyle Modification on Prevention of Dementia: Impact of Lifestyle Modification on Prevention of Dementia, Chronic Kidney Disease, Diabetes, Chronic Obstructive Pulmonary Disease, Cancers, and Cardiovascular Disease in a Thai General Population. LDL: 低密度リポ蛋白質; MYB: 脳を維持する; PRODEMOS: 携帯電話アプリを通じた認知症の予防; SBP: 収縮期血圧; 2型糖尿病: 2型糖尿病。
EDPI共同事業によって実施されている多国籍試験Healthy Aging Through Internet Counselling in the Elderly(HATICE)試験では、心血管リスク因子の自己管理を促すコーチがサポートするインタラクティブなインターネット・プラットフォームと、インタラクティブな機能を持たない偽のプラットフォームを18ヶ月間比較している。試験対象者は、65歳以上で心血管リスクが上昇している約2724人。一次エンドポイントは、収縮期血圧、低密度リポ蛋白、BMIを含む複合心血管系リスクスコア。認知機能は副次的転帰である[77]。
タイで現在進行中のクラスターランダム化試験では、3600人の参加者を対象に、4つの領域(食事、身体活動、飲酒、喫煙)について、3年間のデジタル、コーチがサポートする生活習慣改善介入を通常のケアと比較している。参加者は45~75歳で、認知症、慢性腎臓病、糖尿病、慢性閉塞性肺疾患、がん、心血管疾患の診断を受けていない人が対象となる。10年後に測定される主要転帰は、認知症の発症である。MMSEで評価される認知機能は副次的転帰の一つである[78]。
Maintain Your Brain (MYB)試験では、身体活動、食事、メンタルヘルス、認知トレーニングなどのインタラクティブなモジュールを備えたデジタルプラットフォームと、認知症の危険因子に関する静的な情報を備えたデジタルプラットフォームを比較している。本試験の対象者は約8500人で、55歳から77歳までの非認知症のコミュニティ居住者を対象としたオーストラリアの既存のコホートを通じて募集される。主要アウトカムは、3年後に測定される認知機能複合スコアによる認知機能の変化である。副次的転帰は、認知症の発症と認知症リスクの変化である [79]。
EDPI共同事業によって計画されているPrevention Of Dementia Through Mobile Phone Applications(PRODEMOS)試験は、英国(英国)と中国(北京)で実施されている[80]。英国で認知症リスクプロファイルが高く、社会経済的地位が低い55~75歳の総計2400人の患者を対象に、コーチがサポートする対話型のスマートフォンアプリで認知症リスク因子の自己管理を促すものと、対話型の機能を持たない偽アプリの間で無作為に割り付けた。18ヵ月後に測定される主要エンドポイントは、CAIDEの認知症リスクスコアである。
World Wide Fingersは、FINGER試験から生まれた学際的ネットワークである。フィンランドの老人を対象としたマルチドメインのライフスタイル介入は、2年後に認知機能に中程度の有益な効果を示した。同じ介入が米国、中国の農村部、シンガポール、そしてヨーロッパのいくつかの国で試験される予定である [81]。
5.3. 集団ベースのアプローチ
現在進行中の試験のほとんどは、特定の高リスク集団を対象とした個別の介入を試験している。しかし、認知症の大部分は低リスク者や中リスク者に発生している[82]。したがって、将来の認知症予防戦略は、より広範な集団を対象とすることが望ましい。集団全体を対象とした(サブグループを対象とした)介入には、異なる戦略が必要である。個人レベルに加えて、一次予防はコミュニティや集団レベルでも実施できる。喫煙の奨励や健康的なライフスタイルの奨励など、共通の危険因子を対象とした公衆衛生介入は、いくつかのレベルで実施することができ、メディアキャンペーン、法改正、職場やコミュニティでの予防対策などが含まれる場合がある。このような介入の効果を評価することは複雑であり、従来の並行群間無作為化比較試験とは異なるアプローチを必要とする場合がある。有効性を評価するための別の方法論に加えて、実施に関連した対策も考慮しなければならず、そのような研究には代替的な大規模な政府の資金提供が必要になるかもしれない。認知症の危険因子は心血管疾患の危険因子と大きく重複しているため、既存の医療での実施は、認知症、心血管疾患、その他の非伝染性疾患を対象とした統合的なアプローチが有益であろう[83]。
6. 結論
観察研究の結果は楽観的であることを示唆しているが、現在までのところ、認知症予防試験の結果は、これらの危険因子の治療が認知症リスクを低下させるという説得力のある証拠を提供していない。しかし、いくつかの介入、特に集中的な高血圧管理では、認知症リスクと認知機能低下の軽減に有望と思われるものがある。認知症症例の大部分がLMICで発生していることを考慮すると、介入は簡単で安価に実施できるものでなければならない。現在進行中のいくつかの試験では、高リスク者に対するeHealthとmHealthの介入の有効性が検証されている。認知症の有病率に世界的な影響を与えるためには、一般の人々に広く普及している予防的介入のさらなる実施研究が必要である。