コンテンツ
Head Position During Sleep: Potential Implications for Patients with Neurodegenerative Disease
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6398535/
オンラインで公開2019年1月22日
要旨
背景
神経変性疾患(NDD)患者における睡眠の特徴を明らかにすることは、睡眠障害と神経変性疾患の症状や進行との関連性の根底にある潜在的な神経生物学的メカニズムを理解するために不可欠である。
目的
神経変性疾患と年齢、性別、閉塞性睡眠時無呼吸症候群の診断、いびき、仰臥位および非仰臥位での睡眠時間との相互関係を調べる。
方法
ケースコントロールデザインを用いて、神経変性疾患と診断された45人の患者(軽度認知障害24人、アルツハイマー病15人、レビー小体型、パーキンソン病、その他の認知症6人)と、正常な認知力を持つ120人の年齢性別一致対照者(NC)を対象に、複数晩の自宅での睡眠プロファイラー記録から得られた睡眠姿勢の違いを評価した。
結果
1晩2時間以上の仰臥位睡眠の頻度はNC群より神経変性疾患群の方が有意に高く(p<0.001,オッズ比=3.7)年齢、性別、いびき、閉塞性睡眠時無呼吸症候群の診断をコントロールした後も有意であった(p=0.01)。夜間移動性、すなわち頭部位置の変化の回数/hには群間差はなかった。
結論
本研究は、仰臥位と神経変性疾患との関連を定義する上で、家庭内での睡眠測定の有用性を実証している。本研究で得られた知見は、特に睡眠が中枢神経系の神経毒や代謝物を除去する脳の能力に積極的な役割を果たしている可能性を示唆する最近のエビデンスに照らして、さらなる調査の必要性を示している。
キーワード: 頭位、神経変性、閉塞性睡眠時無呼吸、睡眠、仰臥位
はじめに
睡眠異常は神経変性疾患(NDD)患者に非常に多くみられ、認知機能の低下や他の客観的な神経学的欠損が検出されるずっと前の前臨床段階に現れることが多い。睡眠障害と神経変性との関連は双方向性である可能性があり、睡眠障害は脳内の神経変性過程を交互に引き起こしたり、結果として生じたりする可能性がある[1]。臨床的な睡眠障害の存在は、将来の神経変性疾患のリスクの増加と関連しており、例えば、最近の研究では、若年成人で原発性不眠症を発症した患者は、原発性不眠症を発症しなかった患者よりも認知症を発症するリスクが高いことが明らかになった[2]。中年期後期の閉塞性睡眠時無呼吸症候群(OSA)と睡眠時間の短さは、後年の認知症の発症と関連している[3]。
睡眠と神経変性疾患の関係の根底には、可溶性アミロイドβ(アミロイドβ)やその他の神経毒性タンパク質を脳から除去するグリンパティック系があり、睡眠中に選択的に活性化することが示唆されている[4-6]。睡眠時間の減少や夜間の睡眠障害は、非効率的なアミロイドβクリアランスと関連していることが示されており、睡眠障害がアミロイドβや他の有毒タンパク質の脳内蓄積を引き起こし、神経変性のリスクを高める可能性があることを示唆している[7-9]。最近では、一晩の睡眠遮断でも脳のアミロイドβ産生が増加することが示されており、急性睡眠遮断は右海馬と視床におけるアミロイドβ蓄積を増加させ、否定的な気分と相関していることも示されている[7, 8, 10-13]。重力は脳外への血液の移動と分布にも影響を与えるため、特徴的な睡眠姿勢も脳からのタンパク質クリアランスの効率に役割を果たしている可能性がある[14-19]。
この研究の目的は、地域住民の神経変性疾患コホートにおける特徴的な睡眠パターンと、正常な認知機能を有する年齢性別適合対照者との間の潜在的な関係についての探索的調査を行うことであった。
資料および方法
対象者
この研究のために選択された睡眠記録は、IRB承認済みの3つのマルチサイト縦断研究に参加している包括的に特徴づけられた神経変性疾患コホートから取得された。睡眠時間が 4 時間を超え、記録時間の 10%未満がアーチファクトのために拒否された場合、神経変性疾患 の記録が含まれた。2つの研究を除くすべての研究は2晩記録であった。この研究に使用された神経変性疾患コホートには、軽度認知障害(MCI)と診断された24人、アルツハイマー病15人、パーキンソン病(PD)3人、レビー小体型認知症(DLB)2人、特定不能認知症(その他)1人の被験者が含まれていた。全員が自己申告による記憶障害、または家族・介護者による顕著な記憶障害のいずれかを有していた。
アルツハイマー病、PD、DLBの全例とMCIの14例は、大規模なサンディエゴ地域からリクルートされた。患者は、Shiley-Marcos University of California, San Diego (UCSD) Alzheimer’s Disease Research Center (薬物有害反応C) longitudinal projectに登録され、追加研究のために連絡を受けることに同意したか、地域の神経科医からリクルートされたかのいずれかであった。対象となったアルツハイマー病の参加者は、精神障害診断統計マニュアル(DSM-5)に規定された基準に基づき、認知症と運動障害の専門知識を持つ理事会認定の神経内科医によって認知症と診断された。アルツハイマー病の診断基準は、簡単に言えば、a)記憶領域における客観的な認知障害(標準偏差1.5以上)の存在に加えて、少なくとも1つの他の認知領域の存在、b)認知障害による日常生活活動の低下、およびc)本症候群を説明する他の医学的または精神的疾患の欠如であった。MCIの診断基準は、a)記憶領域における客観的な認知障害(標準偏差(SD)1.5以上)の存在、b)日常生活動作の低下の欠如、およびc)本症を説明する医学的または精神的疾患の欠如であった。DLBの可能性がある患者はMcKeith基準[20]に基づいて診断された。その他の認知症」と診断された患者は、DSM-5の大規模な神経認知障害の基準を満たしているが、病因が明らかではない(すなわち、障害がアルツハイマー病やDLBの典型的なものではない)患者であった。
10人のMCI患者は、マサチューセッツ総合病院の脳老化・認知症研究所を通じて本研究に登録され、マサチューセッツ総合病院アルツハイマー病研究センターを通じて紹介されたか、または地元の縦断的コホートに参加した。MCIの指定は、Mini-Mental State Examination(MMSE)スコアが24以上の非認知症参加者に割り当てられた。神経心理学的検査は、以前に定義されたMCIの運用基準を用いて臨床状態を決定するために使用された [21-24]。MCIの指定は、認知領域内の少なくとも2つのパフォーマンスが、公表されている正常値を1SD以上下回るという客観的基準に基づいていた。
神経変性疾患コホートと一致させるために、正常認知(NC)の年齢・性別をマッチさせた対照者が選ばれた。Knight’s Alzheimer’s Disease Research Centerのデータベースからワシントン大学臨床認知症評価が0の被験者100人9人、およびMMSE≧29の健常者のINSPECDSデータベースから11人を選んだ。睡眠時間が4時間以上の2晩が利用できなかった場合、睡眠時間の一晩間の差が1.5時間を超えた場合、アーチファクトのために記録時間の10%以上が拒否された場合は、記録を除外した。
データと削減
複数晩の記録は、額に装着した電池式の装置であるSleep ProfilerTM(Advanced Brain Monitoring, Carlsbad, CA, US)を使用して取得した。この装置は、AF7-AF8,AF7-Fpz、AF8-Fpzの3つの前頭極の脳波信号から、脳波(EEG)電気泳動、筋電図を取得した(図1)。脈拍数の算出には、額から得られた光電図を用いた。いびき音は音響マイクを用いて取得した。頭部の動きと頭部の位置は、信号を360°の角度に変換した後、3軸加速度計から導出した。
図1 睡眠プロファイラを装着した被験者の写真。
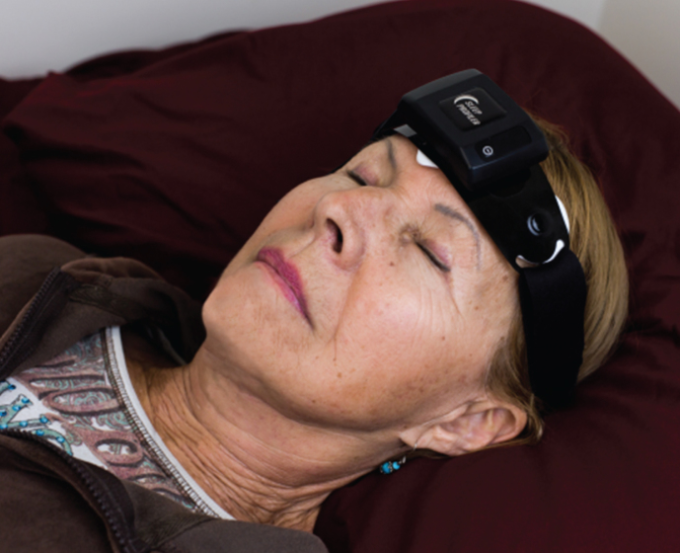
家庭内での研究では、患者は装置を装着する前にアルコールワイプで額を十分に拭くように指示され、皮膚センサーのインピーダンスが許容されるようになった。夜の初めにインピーダンスが高すぎると、音声メッセージが患者に通知された。患者は第2夜の前に額のセンサーを交換した。
睡眠プロファイラ病歴および病歴に関する質問票は、研究時に参加者から取得したものである。質問票は、人口統計学的および擬人化データ、病状の事前診断、薬の使用状況を取得するために使用された。質問票には、Epworth Sleepiness Scale(ESS)Insomnia Severity Index(ISI)Patient Health Questionnaire Depression Test(PHQ9)General Anxiety Disorder(GAD7)を含むスクリーニング質問票の電池が含まれていた。対照コホートに含まれる健康な被験者のうち18人はOSAと診断されたことがあり、16人は一晩のEEG試験中にCPAPによる治療を受けていた。OSAの診断を報告した13人の神経変性疾患患者のうち、8人は研究前にCPAPで治療を受けており、2人は治療を受けておらず、3人のケースでは治療の状況を判断できなかった。
研究が完了すると、記録と質問票の回答がSleep Profilerポータルにアップロードされた。自動睡眠ステージングは、3つのフロントポーラー脳波チャンネルの各30秒エポックから抽出された睡眠マーカーに適用された。0.75 Hzのハイパスフィルタを最初に適用されたアーチファクトで汚染された期間の拒絶の後、次にバンドストップフィルタは、汗のアーチファクトを除去するために使用され、最後に信号のバンドパスは、デルタ、シータ、アルファ、シグマ、ベータ、およびEMGのためのパワー値を得るために16 Hzでフィルタリングした。AF7-FpzおよびAF8-Fpz信号のパターンは、無限インパルス応答フィルタリングされた出力のピアソン相関を計算することにより、ゆっくりとしたローリング眼球運動を特徴づけ、位相的な急速な眼球運動と区別することができた。段階的なレム睡眠と徐波睡眠によるデルタパワーの上昇の区別は、眼球除染前後のデルタパワーの差を用いて行った。パワースペクトル値はまた、スリープスピンドル(すなわち、アルファおよびシグマパワーの両方の短いバースト)皮質覚醒(すなわち、少なくとも3秒間のアルファ上昇)および微小覚醒イベント(すなわち、少なくとも3秒間のアルファ上昇および/またはEMGの組み合わせ)を検出するために使用された。睡眠プロファイラ装置、信号変換、および自動化されたステージングルールの説明、ならびに実験室でのPSGと比較した場合の睡眠メトリクスの精度と信頼性については、以前に記載されている[25-27]。各30秒のエポックについて、パワースペクトル値を平均化し、覚醒、紡錘、動き、いびき、体位、および他のパターンの数を集計した。これらのデータと平均パワースペクトルの比率を組み合わせて、判別関数分析を用いて睡眠段階を割り当てた。1人の評価者が、α、シグマ、β、およびEMGパワーの提示とともに、前頭極の脳波信号波形を目視で検査し、自動ステージングの正確性を確認した。
夜間移動性(すなわち、体位変化)を評価するために、各30秒エポックの開始時の頭部位置を割り当てた。すべてのエポックの頭部位置を含むファイルを編集し、被験者が明らかに寝た姿勢に落ち着いた研究の開始時のエポックと、被験者が起きて研究を完了するために動き始めた研究の終了時のエポックを除外した修正記録時間を確立した。この2つの時点では、夜間移動性の評価に偏りを与える可能性のある頭部位置の変化を除外する努力はしていない。左側臥位から右側臥位への移行では、一般的に2つの体位変化、すなわち、左側臥位から仰臥位、および仰臥位から右側臥位への移行が見られた。左側臥位から右側臥位への移行は、体幹の位置が変化していないにもかかわらず、頭部の位置変化とみなされた。1時間あたりの頭部位置の変化は、頭部位置の変化の総数を変更された記録時間で割ったものである。
データ分析
利用可能な場合には、2晩分のデータを加重平均を用いて結合した(例えば、睡眠効率=第1夜+第2夜の睡眠時間を第1夜+第2夜の記録時間で割ったもの)。連続変数の比較には、等分散を仮定した独立 t 検定を使用した。すべての条件で少なくとも5つの値を持つカテゴリカルデータの比較には、ピアソンカイ二乗分析が使用された。フィッシャー厳密確率検定が、少なくとも1つの条件の合計が5未満のカテゴリカル・データの比較に使用された。すべての統計解析には、両側確率検定が適用された。多変量ロジスティック回帰を用いて、神経変性疾患と独立変数である仰臥位睡眠時間2時間以上/夜、仰臥位時間の割合、いびき、OSA、年齢、性別との関係の強さを評価した。
標準的な重症度スコアリング規則をISI、PHQ9,GAD7に適用した。ESSでは、軽度は11~13,中等度は14~16,重度は16以上であった。
結果
人口統計学、併存疾患、症状
NC群と神経変性疾患群の間には、年齢、性別、BMI、糖尿病や心臓病の有無に基づく有意差はなかった(表1)。NC群は神経変性疾患群に比べて高血圧の診断と降圧薬の処方が有意に多かった。逆に、神経変性疾患患者はNC群に比べてOSAの診断頻度が有意に高かった。全体的に、NC群は神経変性疾患群に比べてESSスコアが高かったが、これはESSが10未満の人の平均スコアがわずかに上昇した結果であった(NC:5.1±2.6,神経変性疾患:3.4±2.5,p=0.001)(表2)。
神経変性疾患群ではNC群に比べてISIスコアが高く、異常ISIスコアを報告する割合が高かった(p=0.01)。神経変性疾患群は有意に高いPHQ7スコアを報告したが、両群間に有意な比例差は認められなかった。抗うつ薬(神経変性疾患=30%対NC=21%、p=0.22)抗不安薬、処方催眠薬(それぞれ7%未満、2.4%)の使用は両群間で差がなかった。
神経変性疾患群では、16人がアセチルコリンエステラーゼ阻害薬(AChEl)を服用しており、11人がセロトニン再取り込み阻害薬(SSRI)を服用していたが、4人が降圧療法を受けており、そのうち2人はアルファブロッカー、2人はベータブロッカーを服用していた。サブクラス別の薬物情報はNC群では得られなかった。
表1 記述的統計
| NC | 神経変性疾患 | P | |
| 人口統計 | |||
| 科目; n | 120 | 45 | – |
| 年齢; y | 71.9±6.8 | 70.9±7.9 | 0.397 |
| 女性; %(n) | 39.2(47) | 33.3(15) | 0.470 |
| ボディ・マス・インデックス; kg / m 2 | 26.9±5.5 | 25.6±4.0 | 0.129 |
| 併存症 | |||
| 高血圧; %(n) | 46.7(56) | 22.7(10) | 0.006 |
| 糖尿病; %(n) | 6.7(8) | 4.5(2) | 0.731 |
| 心臓病; %(n) | 15.0(18) | 13.6(6) | 0.823 |
| OSA; %(n) | 15.0(18) | 29.5(13) | 0.035 |
| 不眠症; %(n) | 5.8(7) | 9.1(4) | 0.488 |
| うつ病; %(n) | 18.3(22) | 25.0(11) | 0.345 |
| むずむず脚; %(n) | 6.7(8) | 2.3(1) | 0.282 |
表2 認知状態別の自己申告症状
| 平均値+ SD | p | 正常 | 軽度 | 中程度 | 重度 | |
| エプワース眠気尺度(ESS) | ||||||
| NC | 6.1±3.7 | 0.034 | 85.9% | 10.8% | 2.5% | 0.8% |
| 神経変性疾患 | 4.7±4.7 | 88.7% | 2.3% | 4.5% | 4.5% | |
| 不眠症重症度指数(ISI) | ||||||
| NC | 4.6±3.8 | 0.011 | 79.0% | 17.6% | 3.4% | 0.0% |
| 神経変性疾患 | 6.5±5.8 | 59.1% | 29.5% | 9.1% | 2.3% | |
| PHQ9うつ病スコア | ||||||
| NC | 2.0±2.2 | 0.032 | 84.2% | 15.0% | 0.8% | 0.0% |
| 神経変性疾患 | 3.0±3.9 | 79.5% | 13.6% | 4.6% | 2.3% | |
| GAD7不安スコア | ||||||
| NC | 1.4±2.2 | 0.159 | 91.7% | 6.6% | 1.7% | 0.0% |
| 神経変性疾患 | 2.0±3.3 | 81.8% | 15.9% | 0.0% | 2.3% | |
睡眠位置の指標
神経変性疾患コホートでは、仰臥位の時間の割合(p<0.0001)および1晩に2時間以上仰臥位で寝ている人の割合(p<0.0001,オッズ比3.7,95%CI 1.8~7.7)に基づいて、頭を仰臥位にした状態での睡眠時間が有意に多かった(表3)。NCノーOSAサブグループと神経変性疾患ノーOSAサブグループを比較すると、仰臥位時間>2 h/nightに有意差が認められた(p<0.001)。MCI、アルツハイマー病、PD/DLB/その他の認知症サブグループでは、仰臥位睡眠時間>2時間/夜の頻度に差は認められなかった(いずれもp>0.60)。多変量ロジスティック分析では、仰臥位睡眠>2時間/夜(p = 0.01)と仰臥位時間の割合(p = 0.001)の両方が神経変性疾患と関連していたが、年齢、性別、閉塞性睡眠時無呼吸症候群、いびきは関連していなかったことが確認された。
表3 認知状態とOSAによる睡眠アーキテクチャの特徴
| 測定する | NCグループ | 神経変性疾患グループ | グループp | ||||
| OSAなし | OSA | p | OSAなし | OSA | p | ||
| 睡眠時間; h | 6.2±1.0 | 6.4±0.8 | 0.35 | 6.2±1.8 | 6.5±0.7 | 0.56 | 0.75 |
| 睡眠効率; % | 79.6±8.9 | 83.1±6.2 | 0.11 | 78.5±13.2 | 82.6±9.4 | 0.32 | 0.79 |
| 時間仰臥位; % | 30.3±27.9 | 31.9±28.8 | 0.83 | 51.7±30.7 | 56.0±30.3 | 0.67 | <0.001 |
| %> 2時間の仰臥位睡眠 | 37.3 | 38.9 | 0.89 | 71.9 | 61.5 | 0.72 | <0.001 |
| 頭の位置が変わります。h | 2.3±1.1 | 1.9±1.2 | 0.32 | 2.1±1.8 | 2.0±0.7 | 0.99 | 0.47 |
頭位変化の回数/hは、群間およびOSAサブグループ間で類似しており、仰臥位時間の差は神経変性疾患群の運動性の低下によるものではない可能性が高いという証拠を提供している。しかし、仰臥位時間の割合と体位変化数/hは神経変性疾患群とNC群の両方で相関していた(神経変性疾患:r = 0.34,p = 0.02 vs NC:r = 0.33,p < 0.001,それぞれ)。
考察
本研究では、複数の機関で実施された縦断的研究に登録された臨床的に特徴的な認知コホートの外来睡眠パターンと優勢な習慣的睡眠姿勢を報告している。本研究は、中枢神経系神経毒および代謝物の濃度上昇に関連する病因を持つ患者において、重症度の範囲で検出可能な可能性のある睡眠バイオマーカーの調査に関する我々の最初の報告である[28]。
仰臥位での睡眠時間と認知症との関係を示したのは本研究が初めてである。我々は、神経変性疾患患者では1晩に2時間を超える仰臥位睡眠の頻度が有意に高く、性別、年齢、OSA診断、いびきを調整した場合、1晩に2時間を超える仰臥位睡眠は独立して神経変性疾患と関連していることを示した。
この所見を説明するために考えられることの1つは、重力が脳外への血液の移動と分布に影響を与えるため、睡眠中の頭部の位置が脳からのタンパク質クリアランスの効率に影響を与える可能性があるということだ[14-18]。
Leeらは、睡眠中のラットでは仰臥位や腹臥位と比較して、横向きの姿勢の方がより効率的にグリンパティック輸送が行われていることを観察している[19]。加齢と睡眠の間の相互作用は、このグリンパティッククリアランスの効率にさらに影響を与える可能性がある。
第一に、睡眠中の呼吸数は加齢とともに増加し、肺の効率が低下した結果である可能性が高い。呼吸が浅くなると、正の胸腔内圧の大きさが減少するため、平均頭蓋内圧が低下する。
第二に、脳内の貫通動脈の脈動の大きさは加齢とともに減少する [29]。
これらの要因により、各呼吸に関連した効率的なクリアランス(すなわちクリアランスサイクル)が低下する可能性がある。睡眠時間の自然な加齢に関連した減少 [30] は、一晩あたりのクリアランス・サイクルの数を減少させることによって、さらに寄与するであろう。
我々は、短時間の研究に結合した仰臥位睡眠の割合の使用に起因する誤解を避けるために、意図的に 神経変性疾患 を長期化した仰臥位睡眠時間(すなわち、1 日 2 時間以上)と関連付けることにした。神経変性疾患の被験者の運動能力の低下が仰臥位での睡眠時間の増加を説明できることは認めるが、1時間あたりの頭位の変化の回数には両群間で差は見られなかった。神経変性疾患群とNC群の両方で、夜間の仰臥位時間と体位変化/時間の間には弱い関連性が見られたが、これはおそらく側臥位間の移行に関連した体位変化の回数によるものと思われる。
本研究の限界の1つは、サンプルサイズが限られていることとレトロスペクティブなケースマッチングのため、OSAの事前診断を除外基準ではなく層別化の目的で使用したことである。神経変性疾患群ではOSAと診断された割合が有意に高かったが、NC群では診断されていないOSAの指標として、神経変性疾患群と比較して2倍の高血圧の有病率や日中の傾眠が有意に多かった。
高齢者におけるOSAの有病率が高いことを考えると、認知的に正常な非OSA患者と神経変性疾患患者の少なくとも10%の記録に、Sleep Profilerの信号に基づく睡眠呼吸障害の証拠が含まれていたことは驚くに値しない。この観察は、クレッシェンドや短いいびきと自律神経の活性化、頭の動き、皮質または微動との重なりのタイミングに基づいて焦点を絞ったレビューの中でなされたものである。
仰臥位での睡眠と睡眠中のラットにおけるグリンパティック・クリアランスの低下との関連性を示唆するデータがあることから、今回の知見は神経変性の分野で興味深い意味合いを持つ可能性がある。ヒトでは、アミロイドβのような可溶性タンパク質のグリンパティック系クリアランスにおける体位に関連した変化を直接測定することは、現在のところ容易ではない。
我々は、MCI、アルツハイマー病、PD、DLBと診断され、脳内にアミロイドβ、αシヌクレイン、タウタンパク質の蓄積に関連する障害を有する神経変性疾患患者を分析した[31]。我々は、1晩に2時間を超える仰臥位睡眠と、これらの神経変性疾患の診断が確定している患者との間に有意な関連があることを発見した。この横断的なデータは、時間的な関連性を評価することができないため、仰臥位睡眠時間が長くなることによる病理学的タンパク質蓄積の因果関係を証明するものではないことは確かだ。
仰臥位の測定や回避が容易で比較的安価であることを考えると、我々の知見は、日常的に臨床評価や画像診断を受けている神経変性疾患患者を対象とした将来の縦断的コホート研究において、家庭での睡眠構造や体位のモニタリングを検討すべきであることを示唆している。
睡眠中の仰臥位での頭部の頻度と持続時間は、これらの神経変性疾患患者でモニターされ、臨床、画像診断、および脳脊髄液神経変性マーカーと相関する可能性がある。今後の研究では、神経変性疾患、OSA、対照群を対象に、仰臥位の睡眠時間を制限するための睡眠体位回避フィードバックトレーニングを含む介入を実施し、神経変性疾患の状態と進行度に関する同様の縦断的なマーカーを測定することも可能である。
結論
我々は、自宅での仰臥位の睡眠姿勢が神経変性疾患と独立して関連していることを発見した。
この結果は、睡眠中の頭部の姿勢が脳からの神経毒性タンパク質のクリアランスに影響を与える可能性を示唆している。
今後、神経変性疾患患者における睡眠姿勢と構造に関するより大規模な前向き縦断的観察コホート研究を実施し、神経認知パフォーマンスや神経変性疾患負荷の臨床、画像診断、脳脊髄液マーカーとの関連性と方向性を明らかにする必要があると考えられる。
