Contents
糖尿病とアミロイド・認知症リスク
概要
アルツハイマー病におけるインスリン
インスリンシグナル伝達と関連するタンパク質は、海馬や側頭葉などアルツハイマー病と関連する多くの脳領域で検出されている。
インスリンシグナル伝達はアルツハイマー病患者の脳組織で損なわれており、インスリン作用の改善がアルツハイマー病の認知機能改善のための治療標的として浮上している。[R][R][R]
糖尿病患者の認知症リスクは56~127%増加
メタアナリシス 糖尿病患者では、全認知症のリスクが73%、アルツハイマー病では56%、血管性認知症では127%増加する。[R]
2型糖尿病患者の認知症発症リスクは60%高い。血管性認知症以外では女性のリスクがより高い。[R]
3型糖尿病と呼ばれるアルツハイマー病
www.ncbi.nlm.nih.gov/pubmed/19885299
脳のインスリン感受性
脳のインスリン抵抗性はドーパミン作動不全を誘発
脳におけるインスリン抵抗性は、ドーパミンの代謝サイクルを変化させ、不安抑うつなどの行動障害を引き起こす。[R]
脳の鉄過剰と関連する脳のインスリン抵抗性
www.ncbi.nlm.nih.gov/pubmed/25125507/
PI3K経路
通常、インスリンのインスリン受容体への結合により、PI3キナーゼ(PI3K)経路と呼ばれる細胞内シグナル伝達カスケードが活性化されることにより、さまざまな生理作用が生じる。
インスリンはインスリン抵抗性であってもインスリン受容体に結合できるが、PI3K経路の伝達に障害があるとインスリン抵抗性による問題が生じる。
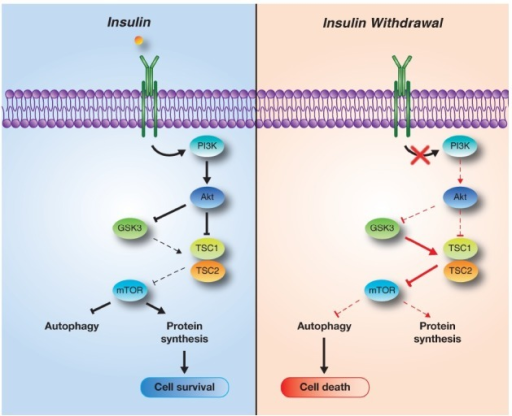
openi.nlm.nih.gov/detailedresult.php?img=PMC4133905_BMB-46-383-g0002&req=4
脳内で合成されるインスリン
海馬、前頭前野、嗅球、嗅内皮質など錐体細胞が存在する脳領域においてインスリン産生[R][R][R]
脳のインスリンシグナル伝達経路
GLUT
インスリンの重要な役割に、インスリン依存性グルコーストランスポーター(GLUT)を細胞膜へ転位させることにより、細胞、特に筋肉、脂肪組織へのグルコース取り込みを増加させることにある。
GLUTには1から7までの分子種が知られており、脳代謝に深く関わるGLUTはGLUT1、GLUT3、GLUT4。
GLUTの機能不全に伴うインスリンシグナル伝達の障害は、GLUTのタイプに依存して異なる脳領域に影響をおよぼす。
TNF-α/ JNK経路
TNF-αシグナル伝達は、-Jun N-terminal kinase(JNK)キナーゼの活性化につながる。
活性化されたJNKはIRS-1をリン酸化し下流のインスリンシグナル伝達をブロックし、抹消インスリン抵抗性を引き起こす。[R]
NMDA受容体
NMDA受容体阻害薬は、インスリン濃度と耐糖能の上昇となる可能性[R]
NMDA受容体活の一時的な活性は抗酸化防御を増強するが、慢性的なNMDA受容体の刺激では抗酸化効果を誘導しない。[R][R]
酸化ストレスによるJNKの活性化は、細胞内のインスリンシグナル伝達経路を阻害する。[R]
NMDA受容体の異常機能によるインスリンシグナル伝達経路の阻害は、酸化ストレスがが要因として提唱されている。
脳内のインスリン
インスリンは特定脳領域の血液脳関門を通過する
インスリンは、視床下部、髄洞、海馬、線条体、頭頂皮質、前頭皮質へといたるBBBは通過するが、中脳、視床および後頭皮質のBBBでは通過させない。[R]
インスリン抵抗性は、BBBを通過するインスリン輸送を損なうことが示唆されている。[R]
インスリンの認知機能への役割
海馬の記憶処理に関わるインスリン
インスリンは海馬の記憶処理に重要な役割を果たしており、中枢でインスリン抵抗性が生じることにより認知機能を損ないえる。[R]
シナプス可塑性と認知機能への影響
インスリンは、海馬および学習と記憶に関与するその他の脳領域のシナプス可塑性か介して、認知機能に影響をおよぼす。[R][R]
アミロイドβクリアランスの促進
インスリンは健康な高齢者の脊髄液中のアミロイドβ42を増加(脳からの排出)させる。[R]
n.neurology.org/content/70/6/440
アルツハイマー病によるインスリンへの影響
インスリンシグナル伝達の阻害
ApoE4はニューロンのインスリンシグナル伝達を阻害
ApoE4は、エンドソーム内のインスリン受容体をトラップすることによってインスリンシグナル伝達を阻害する。
加齢の脳では、ApoE4凝集の増加とエンドソーム機能の低下によりApoE4のインスリンシグナル伝達阻害を悪化させる。[R]
インスリン抵抗性の増加
アミロイドβおよびタウによるインスリン抵抗性の増加
アミロイドβおよび過剰リン酸化タウは、膵臓β細胞の機能不全、肝臓、骨格筋、脂肪組織などの末梢組織におけるインスリン感受性およびグルコースの取り込みの減少に寄与し得る。[R]
Aβオリゴマーによるインスリン受容体の損失
可溶性アミロイドβオリゴマーの神経細胞への暴露は、インスリン受容体の減少を引き起こす。[R]
タウによるインスリン抵抗性の増加
www.ncbi.nlm.nih.gov/pubmed/9930729/
www.ncbi.nlm.nih.gov/pubmed/10938436/
高インスリンに対抗するためのインスリン抵抗性
中枢神経系のインスリン抵抗性は慢性的に上昇したインスリン濃度に対抗するためのホメオスタシス機構である可能性[R]
インスリンの抗認知症効果
インスリンシグナル伝達経路の活性
インスリンシグナル伝達経路はアミロイドβを分解する
アルツハイマー病は、インスリンシグナル伝達の障害に関連している
インスリン処理したアストロサイトは、ERK経路の活性化を介してネプリライシン分泌およびインスリン分解酵素(IDE)発現を誘導する。
インスリンは、アストロサイトにおいてアミロイドβの分解を促進する。in vitro[R]
インスリンシグナル伝達によるシナプス保護
インスリンシグナル伝達はアミロイドβオリゴマー媒介のインスリン受容体の損失とシナプスの劣化を保護することが示されている。[R]
インスリン経路の活性によるBDNF輸送障害の回復
アミロイドβオリゴマーは、プロテインキナーゼB/AKTを損なうことにより、脳内のインスリンシグナル伝達を損い、GSK3βを過剰活性させる。GSK-3βの阻害は、BDNF輸送の障害を改善する。
抗糖尿病であるエキセンディン4(GLP1アゴニスト)は、グルカゴン様ペプチド1受容体(GLP-1受容体)を刺激しインスリン経路を活性化することによって、正常なBDNF軸索輸送を回復させる。[R]
インスリン分泌の促進
インスリン増加によるニューロン内のアミロイドβの減少
インスリンは細胞膜へのアミロイドβの輸送を促進し、アミロイドβの放出を促進することによりニューロン内のβアミロイドを減少させることが示されている。[R]
アルツハイマー病患者では、健常者と比較してインスリンの放出による血漿濃度のアミロイドβ上昇には、より高濃度のインスリンを必要とする。[R]
インスリン改善 標的候補
PI3K経路
PI3K経路の下流のシグナル伝達経路が、神経細胞の生存とシナプス可塑性を促進する主要な役割を果たしていることが示されている。[R]
インスリン受容体 IRS-1
インスリン受容体 IRS-1の調節不全
インスリン受容体IRS-1の調節不全がアルツハイマー病および糖尿病の一般的な病態生理学的メカニズムであることが最近の研究で強調されている。[R]
mTOR活性
mTOR標的によるインスリン分泌の適正化
mTOR活性は、細胞の代謝およびインスリンシグナル伝達にポジティブな影響をおよぼすことができる。(Hamada et al, 2009)
ラパマイシンによるmTOR活性の阻害は、グルコース取り込みを損ない、死亡率を増加させる可能性がある。(Sataranatarajan et al., 2015)
mTORは成長因子(EGF、FGF、EPO、WISP1)を介して機能し、糖尿病において細胞を保護する。
mTORの活性は、幹細胞の増殖および分化に必要であり、幹細胞の維持に影響をおよぼしえる。(Zhang et al., 2015a)
しかし、抑制されたmTORは、幹細胞の増殖と分化を維持するためにSIRT1と関連して自己増殖経路を調節して適応している可能性がある。[R]
PPARγ活性
脂肪細胞の小型化とインスリン感受性の増加
PPARγとは、DNAの転写調節を行う細胞内の受容体(核内受容体)のタンパク質に属し、転写因子としても機能する。
PPARγは主に脂肪組織に分布しており、活性化することによってアディポネクチンの産生が促進される。アディポネクチンは肥大化した脂肪細胞をアポトーシスすることで小型化させる。
小型化した脂肪細胞はインスリン感受性が増強され、炎症性サイトカインの産生、NF-κBの活性も低下する。[R]
チアゾリジンジオン
GLUT-4の発現増加、神経炎症の抑制、アミロイドβクリアランスの増加[R]
GLUT-1発現活性
血液脳関門、内皮細胞のグルコーストランスポーター
グルコースが生体膜を通過するさいに必要な膜輸送タンパク質(グルコーストランスポーター)の一種
赤血球で最も高頻度に発現しているが、脳組織では血液脳関門、関門組織の内皮細胞で発現する主要なグルコーストランスポーター。(GLUT3も関わる)[R]
グルコースは特定のアイソフォームのGLUT1トランスポーター(インスリン非依存性)を媒介して血液脳関門を透過する。
高インスリンによるGLUT-1の低下
末梢性の高インスリン血症は、血液脳関門のインスリントランスポーターのダウンレギュレーションをもたらし、脳に入るインスリン量を減少させる。[R]
GLUT-4発現活性
骨格筋細胞および脂肪細胞で主に発現するが、脳組織でも検出されている。
GLUT-3発現活性
神経細胞グルコーストランスポーター
GLUT-1と同様グルコースが生体膜を通過するさいに必要な膜輸送タンパク質の一種
GLUT-3は神経細胞で最も特異的に発現され、主に軸索、樹状突起に見られ、「神経細胞グルコース輸送体」として知られている。
GLUT1、GLUT2、GLUT4の少なくとも5倍の輸送能力をもち、グルコース輸送に非常に重要な役割を有する。[R]
インクレチン(GLP-1、GIP) の促進
インスリン分泌と膵臓β細胞の増殖
グルコゴン様ペプチド-1/Glucagon-like peptide-1(GLP-1)は、GIP(Glucagon-like peptide-1)インクレチンとも呼ばれ、膵臓からのインスリン分泌を促進し、膵臓β細胞の増殖を促進する。
GLP-1はグルコース以外に脂肪酸、必須アミノ酸、食物繊維などの栄養素による刺激によっても分泌される。分泌量は食事量や栄養組性にも依存して2~3倍増加する。
パーキンソン病患者へのエキセナチド(GLP-1受容体作動薬)の投与[R]
GIP
GIPは、海馬で発現し、GIP受容体は大脳皮質、海馬および嗅球を含む脳の部位で見つかっている。
GIPの外因投与は、ラットの海馬前駆細胞の増殖を誘導する。[R][R]
アミリン/膵島アミロイドポリペプチド(IAPP) 凝集阻害
アミリンの役割
膵島アミロイドポリペプチド(islet amyloid polypeptide)は、アミリンとも呼ばれ、膵臓のβ細胞で産生されインスリンとともに分泌される。
食後のグルカゴン分泌を抑制し、食物の吸収を遅らせることで血糖値を調節する。(血糖値スパイクを防ぐ)
糖尿病患者のアミリン沈着
2型糖尿病患者では、アミリン凝集物が膵島β細胞に沈着しており、膵島β細胞のアポトーシスを誘発する。
また糖尿病患者ではこのアミリンとインスリンの分泌が抑制されることで食後の高血糖が引き起こされる。[R]
アルツハイマー病患者の脳に蓄積するアミリン
アルツハイマー病のβアミロイドと2型糖尿病のアミリンは、共通の毒性メカニズムをもっているという証拠が示されてきている。
このアミリンタンパク質は、アルツハイマー病患者の脳にも蓄積し、アミロイドβと相互作用することで神経変性プロセスを悪化させる可能性がある。[R]
PTP1B 阻害
インスリンシグナル伝達の負の調節因子
プロテインチロシンホスファターゼ(PTP)はアミノ酸のチロシンに付加されているリン酸化を離脱させる機能をもつ酵素。ただし基質特異性は広い。
プロテインチロシンホスファターゼ1B(PTP1B)は、インスリンシグナル伝達を負に調節する制御因子。
PTP1B遺伝子を欠損するマウスでは肥満および糖尿病の発症から保護されていた。
Trodusquemineは、PTP1B阻害剤として創薬研究されている。
ミネラルバランス
ミネラルバランスの不均衡
一部の必須ミネラルのバランスが崩れることで、膵島に悪影響をおよぼし糖尿病の発症を引き起こす可能性がある。[R]
有害金属によるインスリン抵抗性
また一部の毒性金属も、グルコースの取り込みを破壊し糖尿病のリスクを上昇させる可能性がある。
鉛、ニッケル、アルミニウム、銅、クロム、カドミウム、ヒ素[R][R]
鉄高値、マグネシウム低値、マンガン欠乏、銅欠乏、亜鉛欠乏、クロム欠乏 [R]
IGF-1(インスリン様増殖因子)
ja.wikipedia.org/wiki/インスリン様増殖因子
refhub.elsevier.com/S1552-5260(13)02918-X/sref78
血清IGF-1レベルの低下は、アルツハイマー病の発症リスクの増加および脳容積の増加と関連している。低い血清IGF-1を有するヒトではアルツハイマー病発症リスクが51%高い。[R]
空腹時血糖値を高くする要因
慢性疾患
- インスリン抵抗性
- 肥満
- 1型糖尿病
- 2型糖尿病
- 腎臓病
- 脂肪肝、肝疾患
- 甲状腺機能亢進症
- ストレス、外傷、手術
- クッシング症候群(高いコルチゾール)
- 膵炎、ガン
生活環境
- 食べすぎ
- 急性、慢性ストレス
- 質の悪い睡眠、睡眠不足
- 喫煙
ポリ塩化ビニル(PCB)、有機塩素系農薬(OCP)
縦断的分析は、正常血糖コントロールおよび治療を受けた糖尿病患者で40歳(特に48歳以上)に達した後、成人初期の有機塩素系農薬とPCBの血清濃度は、BMIとは無関係にインスリン感受性の低下の測定値と正に関連していることを示す。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4429782/
大気汚染
pubmed.ncbi.nlm.nih.gov/26166095-air-pollution-and-serum-glucose-levels-a-population-based-study/
薬物
ホルモン
- エストロゲン
- 経口避妊薬(75 µg以上)
- プロゲスチン(膵臓β細胞への直接作用)
www.ncbi.nlm.nih.gov/pmc/articles/PMC4135453/
抗うつ薬
- クロミプラミン
- フルボキサミン
- イミプラミン
- ミアンセリン
- ミルタザピン
- パロキセチン
- セルトラリン
改善アプローチ
脳トレ
空間記憶課題が海馬インスリン受容体を増加させる
空間記憶課題の訓練は、海馬インスリン受容体発現を増加させる。[R][R]
鼻腔内インスリン投与
血清グルコースへの影響を緩和
鼻腔内インスリン投与は脳脊髄液のインスリンレベルを上昇させるが、血流には到達しなたいめ血清血糖値の変化を誘発しない。[R]
ApoE4キャリアへの限定的効果
ApoE4キャリアでは、記憶の改善を示さなかった。[R]
鼻腔内インスリンの効果の性差
軽度認知障害患者への鼻腔内インスリン20IU投与では男女とも認知能力を改善を示したが、40IUでは男性のみが改善を示した。
非ApoE4キャリアへのより大きな効果を示したが40IUの投与量では、非ApoE4の女性では悪化を示し、男性では改善を示した。[R]
早期アルツハイマー病患者の認知機能を改善
n.neurology.org/content/70/6/440
膵臓β細胞の標的(特に1型糖尿病)
- EGCG [R] [R][R][R][R][R][R][R][R]
- カプサイシン [R][R][R]
- カリカパパイヤ [R][R]
- クルクミン [R][R][R][R][R][R][R]
- コノフィリン [R][R]
- ゲニステイン(イソフラボン) [R][R][R][R][R][R][R][R]
- 朝鮮人参(ジンセノサイド)
- ベルベリン[R][R][R][R][R]
- ミルクシスル(シリマリン)[R][R][R][R][R]
- レスベラトロール[R][R][R]
- ケルセチン[R]
- ギムネマ酸Wiki[R][R][R]
- ゴーヤ(モルモディシン)[R][R][R][R][R]
- ブラッククミン
- 嗅覚刺激[R]
- 植物による膵臓β細胞の保護と再生[R]


