The association between the use of ivermectin and mortality in patients with COVID-19: a meta-analysis
https://pubmed.ncbi.nlm.nih.gov/33779964/
概要
目的
新型コロナウイルス感染症2019(COVID-19)患者の死亡率に対するイベルメクチンの効果については,多くの研究で検討されている。我々は、無作為化比較試験のメタ解析を行い、COVID-19患者の死亡リスクに対するイベルメクチンの全体的な効果を調べることを目的とした。
方法
PubMed,Cochrane Central Register of Controlled Trials,Google Scholar,およびプレプリントリポジトリのデータベースを系統的に検索した(2021年2月28日まで)。個々の試験のオッズ比をプールするために,ランダム効果および逆分散異質性メタアナリシスを用いた。バイアスのリスクは,無作為化試験のためのコクラン・リスク・オブ・バイアス・ツールのバージョン2を用いて評価した。
結果
6つの無作為化比較試験が本解析に含まれ、イベルメクチンを投与する群に無作為に割り付けられた患者は658人、イベルメクチンを投与しない対照群に無作為に割り付けられた患者は597人であった。6件の試験のうち、4件は全体的にバイアスのリスクが高かった。イベルメクチンの推定効果は、死亡率の改善を示したが(プールされたオッズ比=0.21;95%信頼区間0.11-0.42,n=1255)現在のサンプルサイズでは「有意差なし」という仮説に対するいくつかの証拠があった。
結論
COVID-19患者におけるイベルメクチンの使用に関連して、死亡率に対する有益な効果が予備的に観察されたが、これは適切にデザインされた大規模ランダム化比較試験でのさらなる臨床的証拠が必要である。
はじめに
イベルメクチンは,オンコセルカ症や糞線虫症症など,さまざまな寄生虫症に対する有効性が知られている。最近では,生体内試験および試験管内試験におけるイベルメクチンの研究をまとめたシステマティックレビュー[1]により,さまざまなRNAおよびDNAウイルスに対する幅広い抗ウイルス活性が示された。特に、重症急性呼吸器症候群新型コロナウイルス(SARS-CoV-2)に対して、イベルメクチンは試験管内試験で抗ウイルス作用を示した[2]。このことから、コロナウイルス感染症2019(COVID-19)に対するイベルメクチンの再利用の可能性について、第一線の臨床医の関心が集まっている。そこで我々は、COVID-19患者におけるイベルメクチンの死亡率改善効果を調査するため、無作為化臨床試験のメタ解析を行うことを目的とした。
方法
PubMed、Google Scholar、Cochrane Central Register of Controlled Trials、および言語制限のないプレプリントサーバー(medRxiv、Research Square、SSRN)を含む電子データベースで、2021年2月28日までに発表された適格な研究を対象に、系統的な文献検索を行った。検索戦略は、以下のキーワードとMeSH用語に基づいて構築した。”COVID-19″、”SARS-CoV-2″、および “イベルメクチン”。また,米国(clinicaltrials.gov),中国(chictr.org.cn),世界保健機関(who.int/clinical-trials-registry-platform)の臨床試験登録機関を検索し,COVID-19の治療に対するイベルメクチンの登録臨床試験を調べ,知見が報告されている研究を特定した。2人の研究者(CSKとSSH)が独立して文献のスクリーニングを行い、適格な研究を特定した。また、関連論文の参考文献リストを確認し、追加の研究を検索した。対象とした研究は、COVID-19患者におけるイベルメクチンとその比較対照薬の死亡率を比較した無作為化比較試験であった。観察デザインの研究、シングルアーム試験、非無作為化試験、および臨床結果を報告していない試験は除外した。システマティックレビューは、PRISMA(Preferred reporting Items for Systematic Reviews and Meta-Analyses)ガイドライン[3]に従った。
対象としたアウトカムは、全死亡率であった。対象とした各試験は、2人の研究者(CSKとSSH)が独立して評価し、研究の特徴も抽出した。収集したデータは、著者名、試験デザイン、国、患者の年齢、イベルメクチンの投与方法、比較対照薬の投与方法、死亡率などであった。2人の研究者(CSKとSSH)が,無作為化試験の報告における潜在的なバイアスを評価するための標準化された方法であるCochrane risk-of-bias tool for randomized trials(RoB 2)[4]のバージョン2を用いて,対象となった試験のバイアスのリスクを評価した。RoB 2は,試験のデザイン,実施,報告のさまざまな側面に焦点を当てた,固定のバイアス領域で構成されている.メタ分析では,ランダム効果モデルと逆分散異質性モデルの両方を用いて,プールされたオッズ比を95%信頼区間で推定した。研究間の異質性については,I2統計とχ2検定を用いて,それぞれ50%とP<0.10で検討した。すべての解析はMeta XL, version 5.3 (EpiGear International, Queensland, Australia)を用いて行った。
結果
系統的な文献検索の結果,512件がヒットし,そのうち401件がユニークであった(重複を排除して検索したタイトル)(図1)。スクリーニングの結果、6つの無作為化比較試験[5,6,7,8,9,10]が含まれ、合計658名の患者がイベルメクチン投与群に無作為に割り付けられ、597名の患者がイベルメクチンを投与しない対照群に無作為に割り付けられた。メタアナリシスの対象となった6つの無作為化試験は、それぞれイラク[5]、イラン[6]、バングラデシュ[7]、エジプト[8]、トルコ[9]、インド[10]で行われた。対象となった研究の詳細を表1に示する。6つの無作為化比較試験では、イベルメクチンの投与方法が異なることが確認された(表1)。
図1 PRISMA(Preferred Reporting Items for Systematic Reviews and Meta-analyses)による研究選択プロセスのフロー図
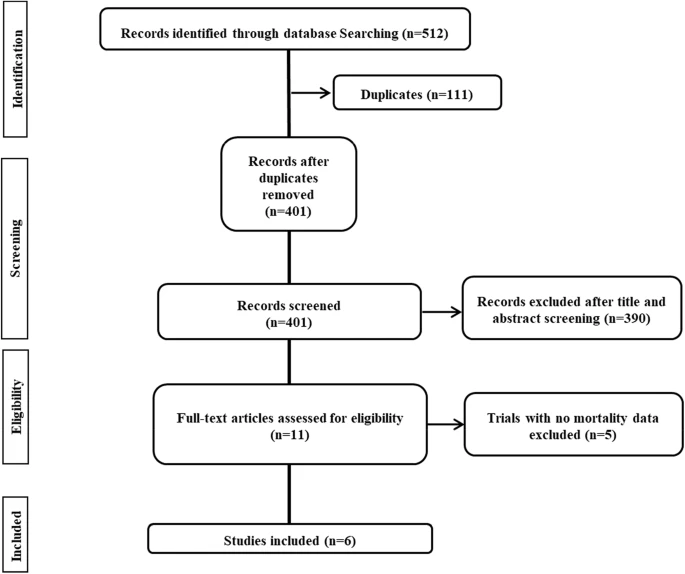
表1 対象となった無作為化試験の特徴
| 調査 | 研究デザイン | 国 | 年齢(中央値/平均) | 介入群におけるイベルメクチンのレジメン | 対照群における比較介入のレジメン | 死亡 | バイアスのリスク1 | |
|---|---|---|---|---|---|---|---|---|
| イベルメクチンユーザー (n / N ;%) |
非イベルメクチンユーザー (n / N ;%) |
|||||||
| Hashim etal。[ 5 ] | ランダム化、シングルブラインド、対照試験 | イラク | イベルメクチンユーザー= 50.1 非イベルメクチンユーザー= 47.2 |
経口イベルメクチン200mcg / kg /日を2日間、回復にさらに時間が必要な患者では、初回投与の7日後に200 mcg / kg /日の3回目の投与 +経口ドキシサイクリン100mgを12時間ごとに5回投与しました。– 10日+標準ケア |
標準治療(必要に応じてアセトアミノフェン500 mg、ビタミンC 1000 mgを1日2回、亜鉛75〜125 mgを1日、ビタミンD3 5000 IUを1日、アジスロマイシン250 mgを1日5日間、デキサメタゾン6 mgを1日、またはメチルプレドニゾロン40 mgを1日2回、必要に応じて) | 2/70; 2.9 | 6/70; 8.6 | 高い |
| Niaee etal。[ 6 ] | ランダム化二重盲検プラセボ対照試験 | イラン | イベルメクチンユーザー= 53–61 非イベルメクチンユーザー= 55–58 |
第1群:単回経口投与イベルメクチン200 mcg / kg 第2群:1、3、および5間隔日での 3回の低間隔経口投与のイベルメクチン(200 mcg / kg)第3群:単回経口投与イベルメクチン400 mcg / kg第4 群: 1、3、および5間隔の日に3回の高間隔のイベルメクチン(400、200、200 mcg / kg)の経口投与 |
プラセボまたは経口ヒドロキシクロロキン200mg /kg1日2回 | 4/120; 3.3 | 11/60; 18.3 | 低 |
| Mahmud etal。(NCT04523831)[ 7 ] | ランダム化二重盲検プラセボ対照試験 | バングラデシュ | イベルメクチンユーザー= 40.7 非イベルメクチンユーザー= 38.5 |
単回投与としての経口イベルメクチン1200mcg +経口ドキシサイクリン100mgを12時間ごとに5日間 | プラセボ+標準治療(アセトアミノフェン、ビタミンD、低分子量ヘパリン、必要に応じてデキサメタゾン) | 0/183; 0 | 3/180; 1.7 | 高い |
| Elgazzar etal。[ 8 ] | ランダム化二重盲検対照試験 | エジプト | イベルメクチンユーザー= 56.7–58.2 非イベルメクチンユーザー= 53.8–59.6 |
経口イベルメクチン400mcg / kg(最大2400mcg)を1日1回4日間+標準治療 | 経口ヒドロキシホロルキン400mgを12時間ごとに1日、続いて200mgを12時間ごとに5日間+標準治療(アジスロマイシン500 mgを5日間、アセトアミノフェン500 mgを必要に応じて、ビタミンC 1 gを毎日、亜鉛50 mgを毎日、ラクトフェリン100 mgを1日2回、アセチルシステイン200 mgを1日3回、D-ダイマーが1000を超える場合は予防的または治療的抗凝固療法) | 2/200; 1.0 | 24/200; 12.0 | 高い |
| オクムシュ他 (NCT04646109)[ 9 ] |
非盲検、ランダム化比較試験 | 七面鳥 | イベルメクチンユーザー= 58.2 非イベルメクチンユーザー= 66.2 |
経口イベルメクチン200mcg / kg /日5日間+標準治療 | 標準治療(経口ヒドロキシクロロキン800mg負荷用量に続いて400mgを5日間、ファビピラビル3200mg負荷用量に続いて1200mgを5日間、アジスロマイシン500mgを初日に続いて250mgを4日間) | 6/30; 20.0 | 9/30; 30% | 高い |
| Ravikirti etal。[ 10 ] | ランダム化二重盲検プラセボ対照試験 | インド | イベルメクチンユーザー= 50.7 非イベルメクチンユーザー= 54.2 |
2日間の経口イベルメクチン1200mcg +標準ケア | プラセボ+標準治療(ヒドロキシクロロキン、コルチコステロイド、抗生物質) | 0/55; 0 | 4/57; 7.0 | 低 |
RoB 2で評価した全体的なバイアスのリスクを表1に示す。Niaeeら[6]とRavikirtiら[10]の試験は、全体的にバイアスのリスクが低かった。その他の試験は全体的にバイアスのリスクが高かった。Mahmudら[7]が主導した試験では、無作為化された参加者のかなりの割合(21%)が解析に含まれていなかったため、結果データの欠落の領域でバイアスのリスクが高かった。Elgazzarら[8]の試験では、無作為化のプロトコルが報告されていなかったため、無作為化の領域でバイアスのリスクが高かった。Hashimら[5]の試験では、単純な無作為化法が用いられ、割付の秘匿に関する情報がないため、無作為化の領域でバイアスのリスクが高く、また、参加者の盲検化が行われていないため、介入からの逸脱の領域でバイアスの懸念があった。Okumuşら[9]の試験では、単純な無作為化法が用いられたため、無作為化の領域でバイアスのリスクが高く、また、試験が非盲検であるため、意図した介入からの逸脱の領域でバイアスのリスクが高くなった。前述の4つの試験[5,7,8,9]は、評価した他の領域ではバイアスのリスクが低かった。
メタ分析の結果、COVID-19患者においてイベルメクチンを使用すると、イベルメクチンを使用しない場合に比べて、死亡率のオッズが有意に低下することが明らかになった。イベルメクチンの推定効果は、死亡率の改善を示し(図2,プールされたオッズ比=0.21,95%信頼区間0.11~0.42,n=1255)現在のサンプル数では「有意差なし」という仮説に対するいくつかの証拠が得られた。
図2COVID-19によるイベルメクチン使用者と非使用者の死亡率のプールされたオッズ比を示すフォレストプロット
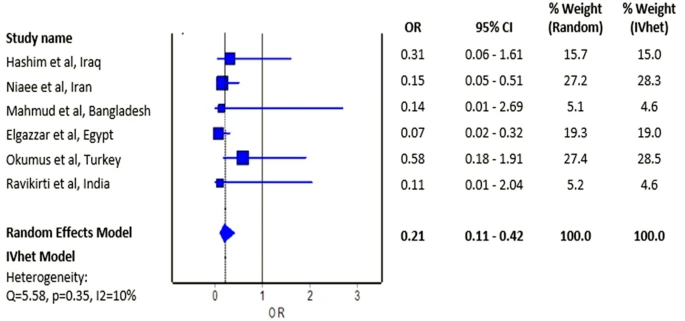
Niaeeらの試験[6]では、かなりの割合の被験者でCOVID-19診断のためのリアルタイム逆転写ポリメラーゼ連鎖反応確認試験が行われていないことを気にする人もいるかもしれないが、この試験をメタアナリシスで除外しても、COVID-19患者においてイベルメクチンを使用することで、イベルメクチンを使用しない場合に比べて、死亡リスクが有意に低下することが観察された(プールされたオッズ比=0.23;95%信頼区間0.09-0.56)。
考察
COVID-19患者におけるイベルメクチンの使用による死亡率の改善は、最近のシステマティックレビュー[1]や、これまでに行われたイベルメクチンに関する最大規模の観察研究[11]で、イベルメクチンの使用に関連して死亡率のオッズが有意に低下することが示された結果と一致している(オッズ比=0.27,95%信頼区間0.09-0.80)。したがって、COVID-19の入院患者におけるイベルメクチンの使用に関連した死亡率へのポジティブな効果は、適切にデザインされた大規模ランダム化比較試験でのさらなる臨床的エビデンスが必要であると、予備的に結論づけている。ただし、今回のメタ分析は対象患者数が少なく、対象となった無作為化比較試験の大部分にバイアスがかかっている可能性があることに留意する必要がある。
COVID-19患者にイベルメクチンを使用することで得られる死亡率の改善は、イベルメクチンの臨床的回復を早める能力に起因すると考えられる。イベルメクチン群では、対照群と比較して臨床的改善(含まれる試験では定義が不一致)を達成した患者の割合が高かった(試験では60. Mahmudら[7]の試験では60.7%対44.4%、Elgazzarら[8]の試験では96.5%対62.0%、Okumuşら[9]の試験では46.7%対36.7%)。) さらに、イベルメクチンはCOVID-19患者の臨床的悪化を防ぐ可能性があり、イベルメクチン投与群では対照群と比較して臨床的に悪化した患者の割合が低かった(Hashimら[5]の試験では4.3%対10.0%、Mahmudら[7]の試験では8.7%対17.8%、Elgazzarら[8]の試験では2.5%対26.0%)ことから、イベルメクチンはCOVID-19患者の臨床的悪化を防ぐ可能性がある。
なお、Niaeeら[6]の試験では、治療群にヒドロキシクロロキンが使用されていたため、試験結果に混乱が生じた可能性がある。Hashimら[5]の試験では、アジスロマイシンとコルチコステロイド(必要に応じてデキサメタゾンまたはメチルプレドニゾロン)を含む標準治療に加えて、介入群にドキシサイクリンとイベルメクチンを併用していた。同様に、Elgazzarらの研究[8]では、被験者がイベルメクチンに加えてアジスロマイシン、ビタミンC、亜鉛、ラクトフェリン、アセチルシステイン、予防的または治療的な抗凝固療法を受けるという複雑な治療レジメンが含まれており、これをヒドロキシクロロキンを投与する対照群と比較した。対照群では心筋梗塞のリスクが高い可能性があり、それが死亡率の高さの原因になっている可能性がある(治療群と対照群の死亡数は、それぞれ2名対24名)。実際、RECOVERY試験では、ヒドロキシクロロキンを投与されたCOVID-19患者において、心臓死のリスクが高いことが示されていた[12]。一方、Okumuşら[9]の試験では、イベルメクチンに加えて、ヒドロキシクロロキン、ファビピラビル(広域抗ウイルス剤)アジスロマイシンを標準治療の一部として採用していた。このメタ分析では、Niaaeeら[6]、Elgazzarら[8]、Okumuşら[9]によるランダム化比較試験が70%以上のウェイトを占めており、したがって、死亡率のベネフィットを確認するためには、より決定的な臨床エビデンスが必要であることは言及しておく。
さらに、対象となった試験では、有害事象の報告が不十分であった。Mahmudら[7]の試験では、治療群(イベルメクチン+ドキシサイクリン)の1人の患者にびらん性食道炎が報告されたが、ドキシサイクリンは薬剤性食道潰瘍の最も一般的な原因の1つであることから、ドキシサイクリンの使用が原因であると考えられた[13]。Okumuşら[9]が主導した試験では、2人の患者に吐き気と嘔吐が、1人の患者に肝酵素の血清レベルの上昇が報告されたが、イベルメクチンによる重篤な有害事象や治療関連の有害事象はなかった。
我々は、この原稿を執筆する時点で、COVID-19の患者にイベルメクチンの使用を推奨するCOVID-19の治療プロトコルを少なくとも1つ知ってた[14]。イベルメクチンによる死亡率改善効果の報告はまだ予備的なものであることから、より決定的な大規模ランダム化比較試験で保証されるまでは、イベルメクチンは臨床試験の場で投与されることが望ましいと考える。
