244,963 回視聴 2024/06/12
モデルナ、RSVワクチンmRESVIA(R)の米国FDA承認を取得
2024年5月31日
モデルナは、本日、米国食品医薬品局(FDA)より、mRNA呼吸器合胞体ワクチン mRESVIA(mRNA-1345)が承認されたことを発表しました、 mRNA呼吸器合胞体ウイルス(RSV)ワクチン、 米国食品医薬品局(FDA)は、mRNA呼吸器合胞体ウイルス(RSV)ワクチンであるmRESVIA 今回の承認は画期的治療薬に指定されたもので、モデルナから承認された2番目のmRNA製剤となります。
ステファン・バンセル、モデルナ最高経営責任者。
FDAによる2番目の製品であるmRESVIAの承認は、当社のmRNAプラットフォームの強みと汎用性を基盤としています。
モデルナは、2024/2025年の呼吸器ウイルスのシーズンまでに、米国内の対象集団にmRESVIAを提供できるようになることを期待しています。
モデルナは、世界の複数の市場においてmRNA-1345の承認を申請しています。
モデルナ、インフルエンザとCovid-19のコンボワクチン開発で第III相試験に勝利
モデルナ注射剤 mRNA-1083
季節性インフルエンザワクチン候補であるmRNA-1010と次世代インフルエンザワクチンCovid-19から構成、 次世代Covid-19ワクチン候補 mRNA-1283から構成されます。
モデルナがmRNAワクチン候補の第III相試験で良好なデータを発表。
現在、mRNA-1083の第III相試験(NCT06097273)においてモデルナは、市販の既存ワクチンと比較して「統計学的に有意に高い免疫応答」を示しました。モデルナは6月10日のプレスリリースで、この試験が主要評価項目を達成したと発表。
免疫応答は3種類のインフルエンザウイルス株(H1N1、H3N2、B/Victoria)とSARS-CoV-2に対して認められました。
モデルナは第III相臨床試験の全データセットを公表していませんが、より多くの臨床試験結果を発表する予定です、 今後開催される医学学会で、より詳細な結果を発表する予定です、 を発表する予定です。
同社は、「次のステップについて規制当局と協力していく」と述べています。
開発中の他のmRNAワクチン
モデルナ、複数のワクチンプログラムを後期臨床試験へ前進
サイトメガロウイルス(CMV)
CMVictory は、16~40 歳の女性を対象とした原発性 CMV 感染に対する mRNA-1647 を評価する重要な第 3 相試験です。
エプスタイン・バーウイルス(EBV) mRNA-1189
無作為化、観察者盲検、プラセボ対照試験。
単純ヘルペスウイルス (HSV) mRNA-1608
フェーズ 1/2 試験
1:1:1:1:1の無作為化、観察者盲検、対照試験は、米国で300人の参加者が完全に登録されています。
水痘帯状疱疹ウイルス(VZV)
モデルナのVZVワクチン候補であるmRNA-1468は、フェーズ1/2試験の初期データが得られています。
ノロウイルス
mRNA-1403 は重要な第3相試験に向けて進行中。
ジョン・キャンベルです。今日は2023年6月11日火曜日のトークへようこそ。mRNAワクチンは世界中で拡大しています。それらを製造するための複数の工場が建設されています。懸念されている副反応の問題は十分に考慮されていないようですが、着々と進められています。
いくつか例を挙げましょう。まずはモデルナ社のウェブサイトからの情報です。モデルナはRSV(respiratory syncytial virus:RS ウイルス)ワクチンの米国FDA承認を取得しました。これはmRNAワクチンで、60歳以上の成人を下気道のRSウイルス感染から保護するために承認されました。一部の人々は、高齢者におけるRSVによるリスクよりもワクチンのリスクの方が大きいと考えているかもしれません。

mRNAプラットフォームの強みと汎用性に基づいて、モデルナの2番目の製品がFDAに承認されたとCEOは述べています。mRNAプラットフォームは非常に汎用性が高く、あらゆる配列を連結して、ほぼ何でも作って人体に注入できます。
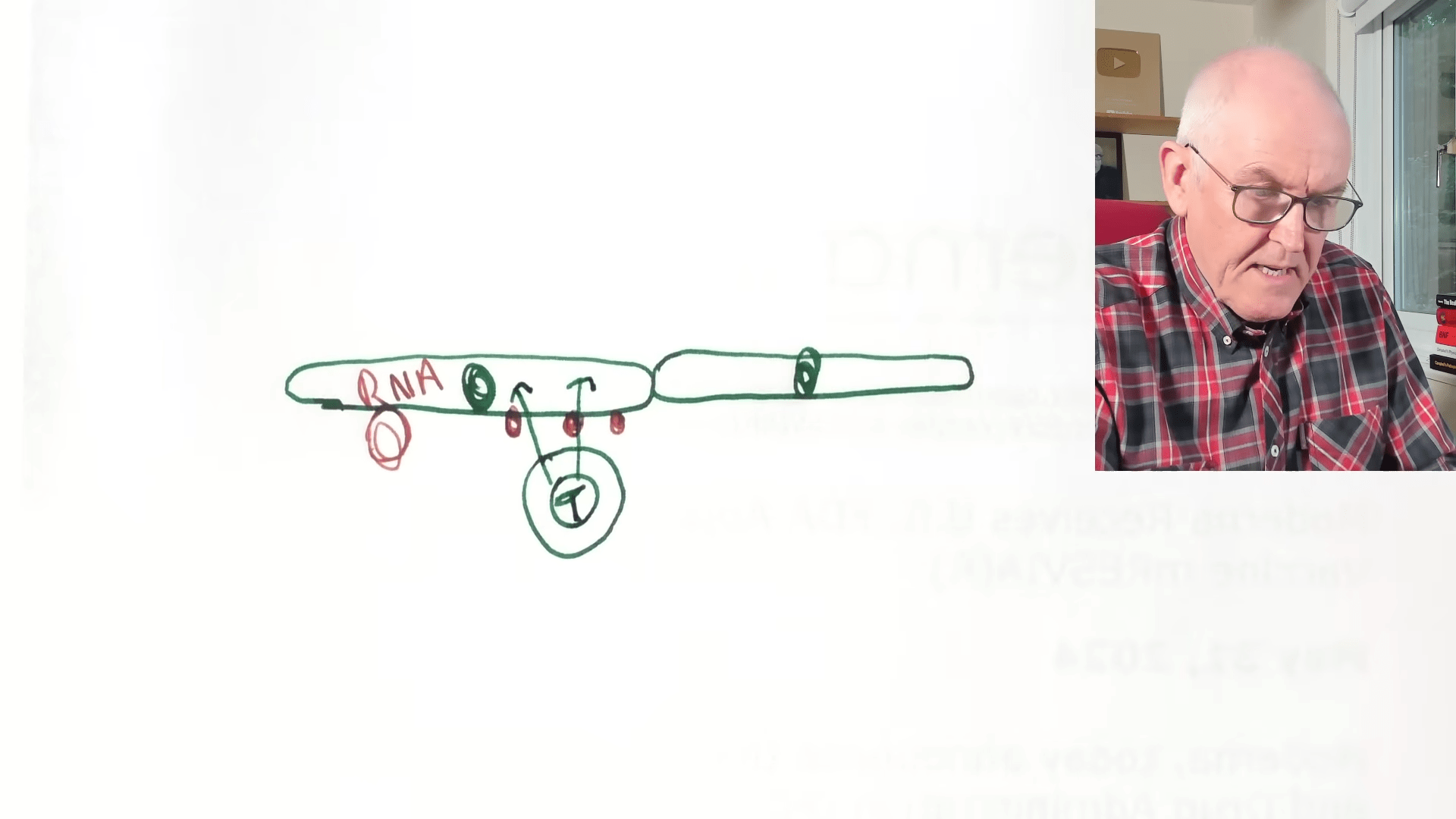
しかし、私が主に懸念しているのは、全身への分布に加えて、これが体内のすべての細胞に潜在的に到達することです。例えば、心筋の血管内皮を裏打ちする細胞があるとしましょう。そこにリポソームナノ粒子が運ばれ、RNAが細胞内に送り込まれると、細胞の遺伝的装置が抗原を生成します。mRNAワクチンを投与すると、少量の抗原が生成される場合もあれば、非常に大量の抗原が生成される場合もあります。投与するRNAの用量は、生成される抗原の量を厳密に決定するものではないと私は理解しています。
これは医薬品投与の基本的な公理の1つに反すると私は考えています。適切な用量の適切な薬を適切な患者に適切なタイミングで適切な経路で投与するべきです。体がどれだけの抗原を生成するかわからないのに、どうやって用量を知ることができるでしょうか。
図に戻りますが、細胞は何であれ抗原を生成します。もしそれがあなたの腕にあり、サイトトキシックT細胞のような白血球が通りかかったとしましょう。これらのサイトトキシックT細胞はこの抗原を異物として認識し、攻撃を開始し、最終的には細胞全体を殺してしまう可能性があります。もしそれがあなたの腕ならば、腕が痛くなるでしょう。心筋であれば、心筋に炎症が起こるでしょう。
スパイクタンパク質は特に病原性が高く、選ばれたのは非常に奇妙だと私は考えています。細胞表面に発現したあらゆる抗原は免疫系によって認識されます。炎症反応が起こり、免疫系はこれらの細胞がウイルスに感染していると考えて攻撃し、細胞を殺します。この懸念は、まだ十分に対処されていないと私は考えていますが、プログラムは着々と進んでいます。
これが私の懸念です。全身への分布と、抗原の不特定量または不確定量の生成、および体細胞によって発現された抗原に対する免疫細胞の反応です。もちろん、これらの細胞は心筋ではなく、精巣や卵巣にあるかもしれません。私が懸念する理由がおわかりいただけたでしょうか。
とにかく、先に進みましょう。それがその発表でした。もう少しこの件について説明しますと、モデルナはこのiRSVワクチンを2024-2025年のウイルスシーズン、つまり次の冬までに、米国の対象集団に提供できるようになると予想しています。モデルナは世界中の複数の市場で規制当局にmRNA承認を申請しています。
これには英国、オーストラリア、カナダ、ニュージーランドが含まれると思います。実際、支払える国は全て含まれると思います。私はこれを受けるつもりはありません。
次の話題に移りましょう。これはClinical Trials Arenaからの情報です。モデルナがインフルエンザとCOVID-19のコンボワクチンレースで第3相試験に勝利し、先行しています。
これはmRNA-1083と呼ばれるもので、季節性インフルエンザワクチンと次世代のCOVID-19ワクチン候補を含んでいます。mRNA-1010がインフルエンザmRNAワクチンです。RNAは配列をコードし、体の細胞がそれを生成して表面に発現します。

もう一つの懸念は、十分に対処されていないことですが、通常、DNAがRNAを作り、RNAがタンパク質を作ります。これはセントラルドグマと呼ばれています。DNAからRNAへの変換は転写と呼ばれ、RNAからタンパク質への変換は翻訳と呼ばれます。RNAが情報をDNAに逆転写することがあれば、それは逆転写と呼ばれます。体内には逆転写酵素と呼ばれる酵素があることがわかっています。それが起こらないことを願っています。
次に、これはインフルエンザワクチンを含んでおり、新しいCOVIDワクチンです。インフルエンザRNAとコロナRNAのコンボです。つまり、2つのRNAワクチンを同じ人に同じ注射器で同じ注射部位に投与することになります。
私はこれを作り上げているのではありません。正直なところ、私が提供した参考文献を見て、自分で確認してください。全てそこにあります。信じられないかもしれませんが、私はこれらの参考文献にあることを報告しているだけです。
モデルナは、mRNAワクチン候補の第3相試験で良好なデータを発表しました。現在、第3相試験が行われています。モデルナによると、市販のワクチンと比較して、統計的に有意に高い免疫応答が見られたそうです。
この試験では、3つのインフルエンザ株(H1N1、H3N2、Bビクトリア)に対する免疫応答が確認されました。おそらく3種類のインフルエンザに対応するRNAが含まれているのでしょう。3種混合のようなものですね。おそらく3種類のRNAが含まれていると思います。そしてコロナのスパイクタンパク質も。スパイクタンパク質のRNAを引き続き使用していると仮定すると、1回の注射で全てが投与されることになります。
モデルナはまだ第3相試験の全データを公開していませんが、今後の医学会議でより詳細な結果を発表し、論文投稿も予定しているとのことです。同社は次のステップについて規制当局と協議するとしています。近くの規制当局に持ち込まれそうですね。
これだけではありません。他にもRNAワクチンがパイプラインにあります。2024年3月27日のプレスリリースによると、モデルナは後期臨床試験で複数のワクチンプログラムを進めています。
サイトメガロウイルス(CMV)ワクチンは、第3相試験で評価中です。これはmRNA-CMVで、おそらくCMVのエピトープをコードしているのでしょう。CMVは非常に一般的ですが、ほとんどの場合は問題を引き起こしません。ただし、母親から感染した子供には問題を引き起こす可能性があります。
エプスタインバーウイルス(EBV)ワクチンも開発中です。EBVは伝染性単核球症(別名:キス病)の原因ウイルスで、成人では非常に厄介な感染症になることがあります。しかし、事実上全ての人がすでにEBVに曝露されています。おそらく95%の人々がすでに抗体を持っているでしょう。無作為化観察者盲検プラセボ対照試験が完全に登録されたようです。このEBV試験も始まる準備ができているようですね。
単純ヘルペスウイルスに対するmRNAワクチンも、現在第1/2相試験中です。また、おたふく風邪に対するmRNA-1468も第1/2相試験のデータが得られています。ノロウイルスに対するmRNAワクチンも積極的に開発されています。
私が知る限り、英国政府はモデルナと契約を結んでいます。前回確認したときは10億ポンドだったと思います。今後10年間でこれらのワクチンを購入することに同意したのだと思います。オーストラリアでも同じで、巨大な新しいmRNA工場が建設されています。カナダでも同じです。mRNAは未来のようですね。
言うまでもなく、私はこれらの試験に参加するつもりはありませんし、これらのワクチンを受け入れるつもりもありません。しかし、それが現在進行中のことなのです。これらは全く巨大な規模で開発されており、FDAはすでに追加のワクチンを承認しました。世界中の規制当局にアプローチが行われています。信じられないことですが、進められているのです。
このチャンネルだけでもワクチン被害者にインタビューしてきましたが、それでもこの全てが進められているのです。私の見解では、安全性の懸念に適切に対処することなく進められています。
とても信じられないことですが、私たちを守るために規制当局が存在しています。彼らがそれを実行してくれることを願っています。確かに、彼らは製薬業界から多額の資金提供を受けていますが、それが彼らの意思決定に影響を与えることはないのでしょう。。
他に言うことはありません。私はこの情報をお伝えしているだけです。興味深い未来が待っていますね。ご視聴ありがとうございました。さようなら。

