コンテンツ
Food Timing, Circadian Rhythm and Chrononutrition: A Systematic Review of Time-Restricted Eating’s Effects on Human Health
https://www.mdpi.com/2072-6643/12/12/3770/htm
Réda Adafer *OrcID,Wassil Messaadi,Mériem Meddahi,Alexia Patey,Abdelmalik HaderbacheOrcID,Sabine Bayen *OrcID,Nassir Messaadi *によって。
リール大学医学部アンリ・ワレンブール総合医学科(フランス・リール市59000)
*
公開:2020年12月8日
要旨
はじめに
最近の観察では、1日の食事時間を長くすることが慢性疾患の発症に寄与する可能性があることが示されている。時間制限食(TRE)は、特にこの1日の食事時間を制限する食事法である。これは、健康マーカーを改善する可能性の高い食事療法の一つであると考えられる。本研究の目的は、時間制限食が人間の健康にどのように影響するかを検討することであった。
方法
5つの一般的なデータベースと6つの栄養ジャーナルをスクリーニングし 2014年1月から 2020年9月の間に発表された、ヒト集団に対するTREの影響を評価するすべての研究を特定した。
結果
収集された494件の論文のうち、最終的に23件が分析の対象となった。TREの全体的なアドヒアランス率は80%であり、意図しないカロリー摂取量の減少は20%であった。TREは平均3%の体重減少と脂肪量の減少を誘導した。この脂肪減少はカロリー制限なしでも観察された。興味深いことに、TREは体重減少とは無関係に有益な代謝効果をもたらし、摂食と概日時計の再調整に基づく内在的な効果を示唆している。
結論
TREは、chrononutritionの原則に基づいて多くの有益な健康効果を生成するシンプルで耐容性の高い食事である。しかし、これらの効果を確認し、そのメカニズムを理解し、人間の健康への適用性を評価するためには、より厳密な研究が必要である。
キーワード:時間制限食、時間制限食、間欠的断食、概日リズム、システマティックレビュー
1. 序論
摂食行動は、慢性疾患の発症に最も影響を及ぼす因子である[1,2]。識別されている主な食物危険因子は、塩分、糖分、加工肉、炭酸飲料の過剰摂取、および果物、野菜、穀物、多価不飽和脂肪の不十分な摂取である[3,4]。
摂食行動に関するデータは、一般的に栄養の質的・量的側面を評価するものである。しかし、食事の時間的特徴や疾患の発生に与える影響については、ほとんど情報が存在しない。
1日の摂食時間は、最初の食事の開始からその日の最後の食事の終了までの期間である。
15,000人の成人を対象としたアメリカのコホートでは、この摂食時間はほとんどの人で12時間と推定され、半数以上の人では15時間に達している[5]。インドの研究でも同様の結果が得られており、1日の食事時間の延長が代謝障害の発症要因である可能性が示唆されている[6]。
このように、最近の観察では、1日の食事時間を短縮することで非伝染性疾患の発症が制限される可能性があることが示されている。例えば、Marinacらは、毎晩の絶食間隔の長さを延長することが乳がん再発リスクを減少させるための戦略である可能性を示唆している[7]。420人のコホートでは、遅食が体重減少に悪影響を及ぼす可能性があることが示されており[8]、2650人の成人女性のコホートを対象とした研究の著者は、夜のエネルギー摂取量を減らし、毎晩の間隔を長くして断食することが全身の炎症を低下させ、その後、乳がんやその他の炎症性および代謝性疾患のリスクを低下させる可能性があることを示唆している[9]。
間欠的断食(IF)は、断食期間と通常の食事期間(週1~3日)を交互に行う食事介入である[10,11]。様々なIFの形態の中で、代替日断食(ADF)は、断食日(すなわち、100%のエネルギー制限)の後に食事日(自由食消費)が続く連続したシーケンスとして定義され、その結果、36時間の断食が行われる [12,13]。IFは、体重減少および健康改善戦略として関心が高まっている食事アプローチである [14,15,16]。
時間制限食事(TRF)はIFの一形態であり、1日の食物消費量を4~12時間に制限し、1日あたり12~20時間の絶食を誘発する [17]。しかし、TRFは2つの点でIFとは異なる。(1) TRFはカロリー制限を必要としないこと、(2) 一貫した毎日の食事窓を必要とすることである[18]。
この食事法は動物において有益な効果を示している。げっ歯類モデルでは、TRFが高脂肪食を与えられたマウスを肥満、高インスリン血症、肝性ステアトーシス、炎症から保護することが実証されている[19]。別の研究では、肥満やII型糖尿病、肝性ステアトーシス、高コレステロール血症などの既往症を持つマウスにおいて、TRFが代謝性疾患の発症を抑制し、代謝性疾患の進行を逆転させることが示された[20]。ショウジョウバエを用いた研究では、TRFが加齢に伴う心臓の衰えを減衰させることが示されている[21]。
時間制限食(TRE)はヒトモデルを指すために用いられる。TREに関するヒト試験やシステマティックレビューでは、動物実験の知見を支持し、心血管代謝に対する有益な効果が示されている[22]。最近のシステマティックレビューと 19 の研究のメタアナリシスでは、TRE は体重減少と無脂肪質量の維持を伴う脂肪質量の減少につながり、血圧、空腹時グル経過濃度、コレステロールプロファイルなどの心血管代謝パラメータにも有益な効果があることが示された[18]。
本研究の目的は、人間の健康に対するTREの効果を探求し、国際的な文献を体系的にレビューすることである。
2. 方法
本研究は、国際的なPRISMA勧告[23]に従って、文献の体系的記述的レビューを行ったものである。
2.1. 項目の収集と選択
https://www.mdpi.com/2072-6643/12/12/3770/htm論文の収集・選定は 2019年9月から 2020年9月まで、3名の独立した研究者により、時間制限付き食事、時間制限付き摂食、時間制限付き栄養をキーワードに実施した。
スクリーニングしたデータベースは、MEDLINE、Web of Science、Scopus、Science Direct、コクランライブラリーであった。さらに、以下の専門誌も分析した。オックスフォード・アカデミーのNutrition Reviews、ワイリー・オンライン・ライブラリーのNutrition Reviews、ワイリー・オンライン・ライブラリーのObesity、アメリカン・ジャーナル・オブ・クリニカル・ニュートリション、Nutrition-Annual Review of Nutrition、クリニカル・ニュートリション。各データベースで使用した研究方程式は、補足方法S1に記載されている。
対象とした論文は 2014年1月から 2020年9月までの間に英語で発表された、成人ヒト集団におけるTREを評価したすべての臨床試験であった。
文献レビュー、メタアナリシス、その他のあらゆるタイプの出版物は、イスラム教徒の断食に関する研究と同様に除外された。
論文が収集されると、3つのステップを含むプロセスを経て論文が選択された。第一に、タイトルを読んで論文を選ぶことであった。残りの論文は要旨
に基づいて選択された。最後に、上記の基準に基づいて含まれたり除外されたりする前に、論文全体が完全に読まれた。
すべての選択ステップは、3人のオペレーターによってブラインドで行われた。意見の相違があった場合には、3 人のオペレーターとスーパーバイザーの間で、コンセンサスが得られるまで議論が行われた。
データベースの構築には、システマティックな文献レビューに特化した Rayyan QCRI Web アプリケーションを使用した [24]。
2.2. データの分析と抽出
データは原著論文から抽出され、論文の参照、研究の種類、参加者の特徴、主なアウトカム、主な結果、エビデンスのレベルなどのテーマに応じて表(補足表 S1)に分類された。そして、これらのデータを表に合成して分析を行った。データの抽出と分析は、レビューの著者である一人の作業者によって行われた。
本論文では、含まれるすべての論文を、XXを番号としてRXXと呼ぶことにする。
2.3. エビデンスレベルの分類
証拠レベルは、臨床試験のすべての方法論的側面を評価する27項目の妥当性スコアであるDowns and Blackチェックリスト[25]に従って分類された。二重盲検法に関する2つの質問(14と15)はカウントされず、スコアは25となった(補足表S2)。
第2の指標は、フランス高等衛生局(HAS)[26]による分類であった(補足表S3-HASのグラデーション)。
これら、2つの指標を組み合わせることで、エビデンスの高、中、低の3つのレベルを決定することができた。
3. 結果と考察
3.1. 厳選された記事と特徴
予備調査では、臨床試験、文献レビュー、その他の関連する研究を含めて、444本の論文を同定した。その中から、重複する論文を 100,6 本除外した結果、最終的には 318 本の論文が残り、22 本が選定された [27,28,29,30,31,32,33,34,35,36,37,38,39,40,41,42,43,44,45,46,47,48,49] 。完全論文読解段階(R15-[41])で論文を追加し、合計 23 本の論文を解析対象とした(図 1 のフローチャート参照)。
図1 論文選択戦略のフローチャート
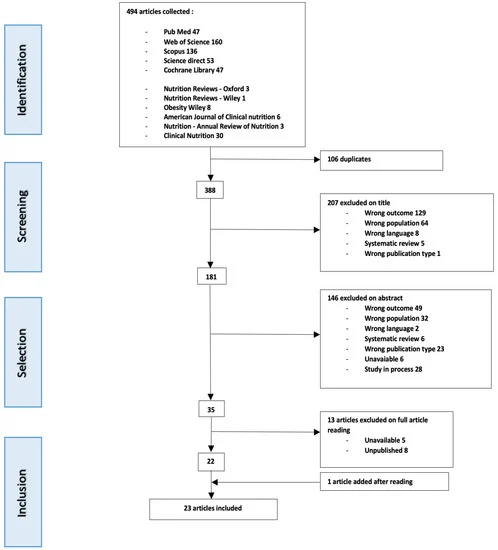
TREに関する文献は限られており、22の試験結果を報告する23の論文しか発表されていない。これらの試験は4日から4ヶ月の期間で実施され、最小サンプルでは8名、最大サンプルでは105名のグループが参加している。全体的なエビデンスのレベルは低~中程度で、中程度のエビデンスの研究では、介入期間が短く(平均33.5日)サンプル数が少ない(平均n=21)対照無作為化試験が10件あった。他の11件の研究は質が低く、3件の非ランダム化対照試験と8件のシングルアーム非対照試験であった。1件の研究はエビデンスのレベルが高く、対照と無作為化のプロトコルが用いられており、レビュー試験の中で最大のサンプル数(105人)であった(R23)。
しかし、TREを評価する28の実験は、収集期間の終了時(2020年3月)にはまだ進行中であったことに注意が必要である。これら、28の試験のうち、26の試験は無作為化されており、より大きなサンプル(平均n=81)が関与しており、この被験者についてより質の高いエビデンスが得られるであろう。これらの観察結果は、TREが関心と知識が高まっている研究対象であることを示している。
3.2. 時間制限食の種類。用語の明確化
時間制限食事は、1日の食事期間を制限することで構成される断続的な断食である [17]。しかし、この制限の定義はヒトを対象とした研究ではまだ不明確であり、情報源によって8時間から 12時間までと様々である。
まず、実践されている時間制限食事の種類を記述するために使用される命名法が標準化されている。TREの後に、24時間の間の食事と絶食の時間数をスラッシュで区切って表示する。例えば、TRE 8/16は、1日の食事時間を8時間に制限し、16時間の断食を行うことを示している。
レビュー中の22件の研究のうち、12時間以下の制限を実施したのは1件のみ(R13)であり、他のすべての研究では10時間以下のウィンドウに毎日の栄養を制限していた。これらのデータは、ヒトにおけるTREの定義を明らかにし、10時間の期間、14時間以上の毎日の断食から始まることを示している。
8/16バリアントはTREの最も一般的な形態であり、レビューの試験の50%(n = 12)であった。1つのTREプロトコル(R1)では、絶食時間を課さなかったが、参加者は最初の食事をずらし、1日の最後の食事の時間を1時間半前倒しすることを要求された。
食事の時間帯もまた、日中に変化しうる。例えば、Suttonら(R4)は、摂食時間が一日のうちでより早く始まった早期TRE(eTRE)の概念を導入した(R2,R4,R5)。その延長で、遅延または遅発性TRE(dTRE)は、最初の食事の摂取を遅らせる(R3,R7,R8,R9,R12,R14およびR23)。Hutchinsonら(R11)は、早期TREと後期TREの両方を評価している。3つの研究(R16,R17およびR18)では、参加者による食物摂取期間の自己選択が認められた。
TREは一般的に毎日(R12およびR13を除く)水(R13を除く)およびアドリビタム断食であり、これは、等カロリープロトコルを使用した4つの研究(R2,R4,R19,R21)を除き、参加者が食物摂取量の質を制限することなく満腹になるまで食事をすることができることを意味している。
これらの特徴は、TREが参加者の食習慣に適応できることを示しており、食事のアドヒアランスにポジティブな影響を与える可能性がある。
3.3. TREへのアドヒアランスとカロリー消費量への影響
TREは全体的に忍容性が高く、アドヒアランスを評価した10試験中8試験(R6,R10,R12,R16,R17,R18,R20,R21)ではアドヒアランス率が80%を超えてた(表1)。しかし、Gabelら(R7)は脱落率が24%と報告しており、別の実施可能性のある研究(R22)では、9/15のTREへのコンプライアンスは72±24%(すなわち、~5日/週)であった。
表1 結果の統合
| 研究[参照] | 証拠のレベル | 人口 | プロトコル | エネルギーバランス | 代謝効果 | その他の結果 |
|---|---|---|---|---|---|---|
| R1 Antoni etal。2018 [ 27 ] |
低 | n = 13人の 健康な成人、 29〜57歳。 |
↓3時間 10週間の非ランダム化比較試験のフードウィンドウ。 |
↓毎日のエネルギー摂取量 | ↓体1.9%脂肪量指数 ↓空腹時血糖 |
フォローアップのために失われたものを含むわずか19%の撤退 |
| R2 Jamshed etal。2019 [ 28 ] |
中 | n = 11 健康な成人、 32±7歳。 |
初期のTRE6 / 18 3〜5週間のウォッシュアウトを伴う4日間のランダム化比較等カロリークロスオーバー試験 |
カロリー摂取量に違いはない(等カロリー) | ↓24時間のブドウ糖と高血糖のエクスカーション ↓インスリン抵抗性 ↑総コレステロール、LDLc、HDLc |
↑BDNF ↓IGF1 概日リズム、寿命、オートファジーに関与する遺伝子発現の修飾 |
| R3 スミス他 2017 [ 29 ] |
低 | n = 20人の 健康な女性、 21.3±1。2歳。 |
遅延TRE8 / 164 週間のシングルアームトライアル |
↓体重0.6±1kg ↓筋力トレーニングを受けた参加者の体脂肪(> 3日/週) |
||
| R4 サットン他 2018 [ 30 ] |
中 | n = 8 糖尿病前症の太りすぎの男性、 59±9歳。 |
初期のTRE6 / 18 5週間の対照、ランダム化、等カロリークロスオーバー試験、7週間のウォッシュアウト |
カロリー摂取量に違いはない(等カロリー) | ↓インスリン(空腹時、平均およびピーク) ↑インスリン感受性 ↓インスリン抵抗性 ↑トリグリセリド ↓血圧 |
↓食べたい ↓8-イソプロスタン |
| R5 Ravussin etal。2019 [ 31 ] |
中 | n = 11 健康な成人、 32歳。 |
初期のTRE6 / 18 4日間の対照、ランダム化、等カロリークロスオーバー試験、3.5〜5週間のウォッシュアウト |
カロリー摂取量に差はない(標準食) エネルギー消費量は変わらない |
↓空腹のいくつかの側面 ↓朝のグレリン、レプチン、GLP-1 ↓平均的なグレリン ↑夕方のPYY(満腹感) |
|
| R6 Gabel etal。2019 [ 32 ] |
低 | n = 23 肥満、 50±2年。 |
TRE 8/1612 週間のシングルアームトライアル。 |
身体活動は変わらない。 カロリー摂取量の測定なし |
↓4%体重 ↓5%脂肪量 |
80%は順守を意味する。 |
| R7および 9Gabel etal。2018年2014年 [ 33、34 ] |
低 | n = 23 肥満、 50±2年。 |
遅延TRE8 / 16 12週間、一致する履歴グループを使用した非ランダム化比較試験。 |
350 kcal /日の↓ 身体活動は変わらない。 |
↓相対体重の2.6% ↓相対BMIの ↓収縮期血圧7±2 mmHg |
74%の順守率。TREグループの誰も食事療法の問題のために中退したと報告しなかった。 |
| R8 モロ他 2016 [ 35 ] |
中 | n = 34 筋力トレーニングを行う成人、 29.21±3。8歳。 |
TRE 8/16 + RT8 週間のランダム化比較試験。 TRE + RT対RT |
グループ間でカロリー摂取量に違いはない トレーニングセッション中の身体活動に違いはない |
↓脂肪量 ↓血糖値 ↓インスリン抵抗性 ↓トリグリセリド |
↓TNF-α ↓IL-1β ↓IGF1 ↑アディポネクチン ↓呼吸比(脂質酸化) 筋肉量と筋力の保存 |
| R10 アントン他 2019 [ 36 ] |
低 | n = 10 太りすぎの高齢者、 77。1歳。 |
TRE 8/164 週間のシングルアームトライアル。 |
平均体重↓2.6kg | ↑歩行速度 心身機能の改善。 84%は順守を意味する。 |
|
| R11 Hutchison etal。2019 [ 37 ] |
中 | n = 15人の 前糖尿病男性、 55±3歳。 |
dTRE 9/15 vs. eTRE 1週間のクロスオーバー、2週間のウォッシュアウトを伴うランダム化試験 |
身体活動に違いは ないカロリー摂取量の測定はない |
↓eTREのグル経過AUCと平均空腹時グル経過 ↓2つのグループのトリグリセリド |
知覚される空腹感、満腹感、または食べたいという欲求に対するTRFの影響はない。 |
| R12 Tinsley etal。2016 [ 38 ] |
中 | n = 18 筋力トレーニングを行う成人、 22±2。4歳。 |
TRE 4/20 + RT対RTのみ。 8週間のランダム化比較試験。 |
↓空腹日と非空腹日の間の650kcal /日の ↓毎週のカロリー摂取量 |
体重と脂肪量に有意な変化はない | 除脂肪体重、筋肉量、筋力の維持。 95%は順守を意味する。 |
| R13 Gasmi etal。2017 [ 39 ] |
中 | n = 40 20年(n = 40)対50年(n = 20) |
TRE 12/12: TRE50年+ 20年 対照50年+ 20年 12週間のランダム化比較試験。 |
カロリー摂取量に違いはない。 | 体組成や筋肉機能に変化はない | ↓免疫老化 |
| R14 Tinsley etal。2019 [ 40 ] |
中 | n = 40 18〜30歳の 筋力トレーニングを行う女性 。 |
遅延TRE8 / 168 週間のランダム化比較試験。 -RT +プラセボ -TRE + RT +プラセボ -TRE + RT + HMB |
↑20〜200 kcal /日のカロリー摂取量 身体活動とREEに違いはない |
↓2つのTREグループのプロトコル分析ごとに4%〜7%の脂肪量 | プロトコル終了時に参加者の90%に副作用はない |
| R15 ギル他 2015 [ 41 ] |
低 | n = 8 肥満の成人、 18歳。 |
TRE 10/14毎日、 3週間のシングルアームトライアル。 スマートフォンベースのカロリー量とタイミング摂取量の評価 |
↓カロリー摂取量20% | ↓重量4% ↓BMI 1.15 kg / m 2 |
↑睡眠の質 ↓空腹 |
| R16 Lee etal。2020 [ 42 ] |
低 | n = 10 太りすぎの座りがちな高齢者、 77。1歳。 |
TRE 8/16毎日、食事の時間枠を自分で選択する。 4週間のシングルアームトライアル。 |
84%の平均遵守率。 | ||
| R17 Kesztyüsら。2019 [ 43 ] |
低 | n = 40 腹部肥満、 49.1±12。4年。 |
TRE 8/16毎日、食物摂取期間の自己選択を伴う 12週間の単群試験。 |
↓1.7±2.5 kgで重量 0.6±0.9キロ/ Mの↓BMI 2 ↓WC -5.3±3.2センチメートル 1.4±3.5ミリモル/モル↓HbAc1 |
86±15%の平均順守 | |
| R18 Wilkinson etal。2020 [ 44 ] |
低 | n = 19人の MetS59 ±11歳の成人。 |
TRE 10/14毎日、食物摂取期間の自己選択。 12週間のシングルアームトライアル。 |
↓8.62%±14.47%。 身体活動に違いはない。 |
↓体重(-3%) ↓BMI(-3%) ↓体脂肪(-3%) ↓内臓脂肪評価(-3%) ↓WC-4.46± 6.72cm ↓ 総コレステロール ↓LDLc、↓非HDLc ↓収縮期および拡張期血圧 |
85±12%の平均アドヒアランス。 63.2%の参加者は、16±4か月で何らかの形でTREに従事していた。 ↑12.45分の睡眠時間。 ↑参加者の84%で睡眠時間と効率が向上した。 |
| R19 マカリスター他 2019 [ 45 ] |
中 | n = 22 身体的に活動的な男性、 22±2。5年。 |
TRE 8/16毎日自由に対等カロリー(ベースラインから↓300 kcal)。 4週間のランダム化比較試験。 |
カロリー摂取量に違いはない | ↓両方のグループの 体重↓両方のグループの体脂肪量 ↓両方のグループの収縮期血圧 ↑両方のグループのHDLc |
↑両方のグループのアディポネクチン。 主観的な結果(覚醒、エネルギー、集中力、気分)の自由な改善。 |
| R20 Chow etal。2020 [ 46 ] |
低 | n = 20 食事期間が長い(15.4±0.9時間/日)太りすぎの成人。 45.5±12年。 |
TRE8 / 16は毎日自由に摂取できる。 12週間の対照非ランダム化試験。 TRE8 / 16グループと非TREグループ。 |
身体活動に違いはない。 カロリー摂取量の測定はない。 |
(1)vs。非TREグループ ↓体重 ↓除 脂肪体重↓内臓脂肪 (2)vs。介入前の対策 ↓体重 ↓脂肪量 ↓除脂肪体重 ↓内臓脂肪 |
非TRE群と比較したTRE群(9.9±2時間)の摂食時間帯の↓。 TREの順守:83.1% 脂肪を伴う食事ウィンドウの制限と内臓の質量減少との相関 |
| R21 パー他 2020 [ 47 ] |
中 | n = 11 太りすぎ/肥満および座りがちな男性。 38±5年。 |
TRE 8/16毎日vs.非TRE(15時間/日)。 10日間のウォッシュアウト期間を伴う5日間のランダム化クロスオーバー試験。 |
カロリー摂取量に違いはない(等カロリー)。 身体活動に違いはない。 |
↓夜間グル経過AUCTREグループ ↓ TREグループの朝食時のピークインスリン濃度↓ TREグループの朝食 時のピークグル経過濃度 |
100%順守。主観的感情(幸福と満足)の改善 ↓TREグループの夕方の空腹 |
| R22 パー他 2020 [ 48 ] |
低 | n = 19人の2型 糖尿病の肥満成人。 50±9年。 |
TRE9 / 15毎日。 4週間の単群非ランダム化試験 |
カロリー摂取量に違いはない。 TREを順守すると、カロリー摂取量が減少する。 |
NS。 | 72±24%の平均コンプライアンス(約5日/週)。 |
| R23 Miguet etal。2020 [ 49 ] |
高い | n = 105 太りすぎおよび肥満の成人。 46.5±10。5年。 |
dTRE8 / 16毎日。 12週間の対照ランダム化試験。 TRE8 / 16対対照群。 |
カロリー摂取量に違いはない。 身体活動の測定はない。 |
↓TRE群(1.17%)の体重は、ベースラインと比較して、対照群(0.75%)と有意差はなかった。 |
☒:測定なし。NS:有意でない変更(p > 0.05)。略語
AUC:曲線下面積。BDNF:脳由来神経栄養因子; BP:血圧; HDLc:HDLコレステロール; HMB:ヒドロキシメチルブチレートサプリメント; IL:インターロイキン; インスリンR:インスリン抵抗性; インスリン-S:インスリン感受性; LDLc:LDLコレステロール; MetS:メタボリックシンドローム; REE:安静時のエネルギー消費量。RT:レジスタンストレーニング; 2型糖尿病:2型糖尿病; WC:ウエスト周り。
それ以外では、食事のタイミングの遵守は、ほとんどの研究で食事日記または面接で参加者が自己申告していた(R1,R3,R6,R7,R10,R11,R12,R13,R14,R16,R17,R19,R22,R23)。また、食物摂取量の測定は、参加者の自己申告に基づいて行われた(R1,R7,R8,R9,R12,R13,R14,R19,R22,R23)。7つの研究(R3,R6,R10,R11,R16,R17,R20)では、食物摂取量の追跡すら行われていなかった。これらの制限は、宣言や混乱バイアスにつながる可能性がある。
この制限は、自由に生活している状態での食物摂取量のような健康行動を測定することの固有の難しさである。GillとPanda(R15)は、写真と参加者が追加したオプションの通知を組み合わせたスマートフォンアプリケーションを開発した(myCircadianClock、mCC-www.mycircadianclock.org)。この方法はWilkinsonら(R18)やChowら(R20)でも使用されており、食品追跡に関わる方法論的な偏りを減らすための興味深い方法である。その結果、モバイルアプリケーションを使用することは、従来の食事日記よりも食事プロトコルへのコンプライアンスをモニタリングするためにより正確であり、また、このプロトコルへのアドヒアランスを向上させることができることが研究によって示されている[50]。
最近の文献レビューでは、食事療法のアドヒアランスの主な決定要因は、食事への欲求を軽減する能力と患者の食習慣に適合する能力であることが示されている[51]。今回のレビューでは、4件の研究(R4,R5,R11,R21)で空腹感は安定しており、Ravussinら(R5)では、空腹時の不快感と食べる意欲を減らすことで食欲のいくつかの要素が改善したと参加者が報告している。さらに、時間制限食は、食事の質や量に制限がなく、参加者の摂食行動への適応性が高いため、古典的な食事療法よりも制限が少ないように見える。
アドヒアランスだけでなく、長期的なアドヒアランスは、全体的な健康上の利益に関するダイエットの成功の最も重要な要因である[52]。今回のレビューで紹介された試験は、4日から4ヶ月という比較的短い期間で結論が出ている。Wilkinsonら(R18)が実施した試験では、12週間の介入終了後16ヵ月後に参加者の63%が何らかの形でTREに従事していた。この結果は、TREが持続可能な食事介入であることを示唆しており、より長い期間(12~24ヵ月)のアドヒアランスを評価することは興味深いことであろう。
授乳時間の制限は摂取カロリーを増加させると予想された。逆に、TREは多量栄養素の分布を変化させることなく、カロリー消費を平均で20%減少させた(表1)。興味深いことに、このカロリー制限は参加者が意図的ではないと記載されており、これは認知的制限から参加者を保護している可能性が高い。ある研究では、10ヶ月間の食事介入の後、認知制限を受けた人は、ベースラインと比較してエネルギー摂取量が増加し、制限を受けていない人と比較して体重が減少することが明らかになった[53]。
さらに、TREは、継続的なカロリー制限などの他の自主的な制限的食事手段と同程度のカロリー制限を提供する。実際、CALERIEは、非肥満の集団における継続的なカロリー制限を評価した史上最大規模の研究であり [54]、その結果は、最も意欲的な被験者でさえも2年間にわたって25%のカロリー制限を維持することができなかったことを示している。これらの知見をまとめると、
(1)TREはカロリー摂取量を減らしたい患者にとってより持続可能な戦略であり、
(2)TREは自発的な食事制限よりも持続可能な体重減少をもたらす可能性があることが示唆される。
3.4. TREの代謝効果
断続的な断食がカロリー制限を介して有益な代謝効果をもたらすことは文献で確立されている[55,56]。この原理はレビューの結果からも確認されており、平均3%の体重減少と脂肪量の減少(表1)体脂肪の減少と空腹時グル経過濃度の低下(R1)体重減少とBMIの低下(R7,R9,R15,R18)収縮期血圧の低下(R7,R9,R18)ウエスト周長の低下とコレステロール濃度の低下(R18)が認められている。
興味深いことに、TREに関する6つの研究では、カロリー制限にかかわらず、有益な代謝効果が示されている(表1)。例えば、eTREを評価した無作為化アイソカロリー研究では、平均血糖値の低下とインスリン抵抗性の低下が示された(R2)。同様に、クロスオーバー無作為化試験(R21)では、短期TREが夜間血糖コントロールを改善することが示された。eTRE 8/16(R4)のアイソカロリック試験では、耐糖能の改善と収縮期血圧の大幅な低下が示され、ACE阻害薬による薬理学的治療で得られた結果に匹敵する結果が得られた[57]。Moroらは、TRE 8/16と定期的な身体活動との併用により、脂肪量が減少し、血糖値が低下し、インスリン抵抗性が改善し、トリグリセリド値が低下したことを報告している(R8)。Grantら(R14)は、グループ間でカロリー摂取量が増加したにもかかわらず、4%~7%の脂肪質量の減少を示したが、プロトコルごとの分析にとどまった。McAllisterらは、8/16 TREを適用した2つのグループで、アドリバイタム条件とアイソカロリー条件で体重と脂肪量の減少、収縮期血圧の低下、HDLコレステロールの増加を示したが、グループ間では差はなかった(R19)。著者らは、この効果はアディポネクチン値の上昇によるものであることを示唆した。アディポネクチンは空腹時に分泌が増加するアディポカインであり[58]、エネルギー消費量の増加[59,60]や、脂肪分解やインスリン感受性を刺激するキナーゼであるAMPKの活性化[61,62,63]により、脂肪量の減少をもたらす可能性がある。Moroらによる無作為化試験(R8)でもアディポネクチンレベルの上昇が観察された。これらの知見は興味深いものであり、TREがエネルギーバランスとは無関係にプラスの代謝効果をもたらす可能性を示唆している。
代謝の変化は、食べた食物のエネルギー量と身体活動を介して部分的に消費されたエネルギーとの間の不均衡の結果であるが[64,65]、前述の6つの研究のうち身体活動を測定したのは3つだけであった(R8,R14,R21)。例えば、Moroらの試験(R8)では、レジスタンストレーニング(RT)に関連した8週間のTREは、筋力トレーニングのみを行った成人のグループと比較して上述の代謝効果をもたらし、食事摂取量と身体活動量に差はなかった。この研究では、身体活動はトレーニングセッション中にしか測定されていないため、上記の効果はトレーニングセッション以外でのエネルギー消費の増加が測定されていないことに起因している可能性がある。Tinsleyらもまた、レジスタンストレーニングに関連したTREの効果を評価した(R4)。彼らはトレーニングセッション中とトレーニングセッション外で身体活動を測定しており、これは潜在的なバイアスを制限するものである。これらの興味深い効果を確認するためには、身体活動の影響を体系的にコントロールするために、TREに関するさらなる研究が必要である。
3.5. TREと概日時計
また、食事療法の有益な代謝効果は、それがもたらす体重および/または脂肪の減少によって誘導されることも確立されている[56]。この主張は、本レビューの7つの研究(R1,R3,R7〜9,R8,R17,R18,R19〜表1)で確認されている。例えば、Wilkinsonらは、メタボリックシンドロームの成人19人を対象に12週間10/14のTREを実施し、LDLおよび非HDLコレステロールの減少、3%の体重減少に伴う収縮期血圧の低下、体脂肪の減少、BMIおよびウエスト周囲長の減少を記録した。他のダイエットとは対照的に、TREは、体重または脂肪の任意の損失に関係なく代謝上の利益を生成する。例えば、Hutchinsonらは、eTREを2週間実践した参加者において、耐糖能の改善およびトリグリセリドの減少を示した(R11)。さらに、Suttonらは耐糖能の改善とインスリン値と血圧の低下を記録した(R4)。これらの有望な結果は、TREが体重減少や脂肪量とは無関係に、内在性代謝効果を生み出すことを示唆している。
この内在性の効果を説明するために仮定されている主なメカニズムは、体の概日リズムへの作用である[66]。サーカディアンシステムは、睡眠/覚醒サイクル、血圧、心拍数、ホルモン分泌、認知能力、気分調節など、24時間周期に関与するすべての生理学的プロセスを表している[66]。このシステムは、食物摂取、光曝露、身体活動などの多くの環境刺激によって調節される[67]。増加している証拠は、サーカディアンシステムの乱れが肥満などの多くの代謝性疾患の原因であることを示している[68,69]。したがって、食事の摂取時間を制限することは、概日時計[70,71,72,73]に合わせて食物摂取量を再調整するようである[70,71,72,73];これは概日時計と食物摂取量の関係の研究であるクロノニュートリションの基本原理であり[74]、食事のタイミングが代謝に影響を与えることを示唆している[75]。
いくつかの結果がこの仮説を支持している。まず、アディポネクチンは、脂肪量の減少[62]、血糖・脂質代謝の促進[60,63]、血圧の低下[76]など、上述したすべての代謝作用において重要な役割を果たすことが確立されている。この分子は、概日系の作用を積極的に調節することが知られている[77,78]。さらに、大規模な遺伝子発現解析を含むランダム化対照アイソカロリック研究では、eTREが概日リズムに関与する6つの遺伝子の発現に影響を与えることが示された(R2)。最後に、TREが睡眠の質の有意かつ持続的な改善をもたらすことを示した研究(R15)や、成人19人を対象に10/14のTREを評価した12週間の単群試験では、参加者の84%で睡眠時間と睡眠効率の増加が記録された。さらに、睡眠の質の改善は、サーカディアンシステムの強化に直結していることが知られている[79,80]。しかし、概日系に対するTREの正確な作用はヒトでは不明のままであり、関与するメカニズムをよりよく理解するための研究が必要である。
動物モデルでの観察の増加は、心血管系マーカーに対する身体活動のプラスの効果も、概日リズムを回復させる能力によるものであるという仮説を立てている[81,82]。Moroら(R8)は、TRE食とRTプログラム(週3回)を組み合わせたグループと、RTのみを8週間実践したグループを比較した。TRE+RT群のみが、総体量と脂肪量の減少、および代謝マーカー(耐血糖能、トリグリセリドの減少)の改善を記録した。しかし、上述したように、身体活動によるエネルギー消費はトレーニングセッション中にのみ記録されており、これは分類の偏りにつながる可能性がある。今後の研究では、この因子を系統的にコントロールし、TRE単独 vs. TRE + RTをテストすることができるはずである。繰り返しになるが、スマートフォンを利用した方法は、通常の生活状態で身体活動とエネルギー消費を測定するための興味深い戦略です[83]。
3.6. TREのその他の効果
その他の有益な効果については、我々のレビューで検討した。断続的な絶食は、動物[84]およびヒト[84]においてIGF-1レベルを低下させることにより、がんを予防することが示されている。この効果は、2つのレビュー研究(R2およびR8)で述べられており、発がんにおけるTREの保護効果を示唆している。さらに、研究者らは、断続的な1ヶ月間の断食がプロ炎症性サイトカインの減少につながることを示している[85]。この結果は、フィジカルトレーニングに関連したTREの8週間後のTNF-αおよびIL-1-βレベルの低下を報告したレビュー研究でも確認されている(R8)。炎症のこれらのメディエーターの減少は、そうでなければ、アディポネクチンの作用を介して概日リズムの改善に役割を果たしているという仮説が立てられている[86]。遺伝子発現解析により、TREはオートファジーと長寿に関与する4つの遺伝子の発現を増加させることが示されている(R2)。また、TREが神経変性疾患の発症に対する保護因子であるBDNFの分泌を増加させることを初めて示した研究でもある[87]。さらに、高齢者におけるTREの効果を検討した2つの研究では、老年期のロバストネスの予測因子である歩行速度の改善[88]や、免疫白化過程の減衰が示されている(R10およびR13)。さらに、Suttonら(R4)は、TREが酸化ストレスのバイオマーカーである8-イソプロスタインを有意に減少させることを示した[89]。これらの観察は有望であるが、これらの観察は生物学的基準に基づいており、臨床的な意味合いは限定的である。これらに関連した罹患率および死亡率に対するTREの影響を評価するためには、縦断的研究が必要である。
4. 結論
我々のレビューでは、1日の食事期間を短縮することは、カロリー制限のための十分に許容できる食事療法であることが明らかになったが、より長期的に評価することが興味深い。興味深いことに、TREはエネルギーバランスに関係なく多くの健康マーカーに有益な効果をもたらすという点で、他の食事介入とは異なる。これらの効果は、栄養が摂取量や質だけでなく、概日時計に従った食品消費のタイミングによっても健康に影響を与えることを示唆している。
より広く、睡眠の質や身体活動のような他の健康行動が、概日時計に従ったタイミングによって健康マーカーに影響を与えるかどうかを評価することは興味深いことであろう。この目的のために、スマートフォンをベースにした方法を用いて、自由に生活している状態での健康行動を測定する研究をさらに進めることができるだろう。実際、スマートフォンはユビキタスで世界中に存在し、一日のうちいつでも利用可能であり、概日時計に従った生活様式の行動に関する詳細な情報を提供するための携帯型モニタリング装置として使用することができる。この情報は、健康行動、タイミング、病気の発生との関係をよりよく理解するのに役立つはずである。
