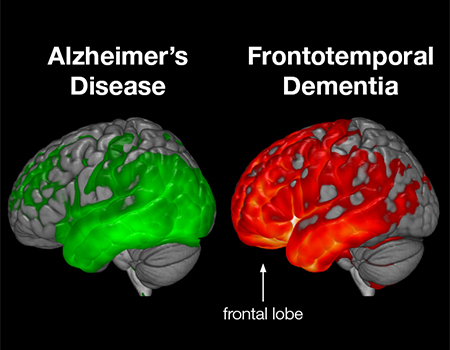
前頭側頭葉変性症/FTLD 臨床分類
概要
FTLD(前頭側頭型認知症)とFTD(前頭側頭型変性症)が混同されがちだが、FTLDは前頭葉や側頭葉の神経変性が目立つ病理学的な広義の概念であるのにたいして、FTDは前頭葉や側頭葉の神経変性による症状で分類されたFTLDのサブクラスとなる臨床学的な概念。
FTLDの下位分類に以下の3つが臨床分類として存在する。
・FTD(前頭側頭型認知症)
・PNFA(進行性非流暢性失語)
・SD(意味性認知症)
前頭側頭葉型認知症/FTD
脳の萎縮パターン、臨床症状により更に以下のサブクラスに分類される
・脱抑制型
・無欲型
・常同型
薬剤投与
・FTDのAchE阻害薬の有効性については見解が一致していない。脱抑制の悪化を示した報告。
・メマリー投与が、異常行動の改善および無感情、興奮、不安に対して有効である報告がある。
・FTLDは、大脳の全領域でセロトニン5HT1A受容体の結合能が有意に低下。SSRIの有用性が示唆されている。
・FTD患者ではセロトニンとドーパミン系の減少が見られるが、アセチルコリン系は比較的保たれている。
・セロトニン系の投与による異常行動の改善例はあるが、認知機能は改善しない。
・無感情に対してはChE阻害薬が有効、
・同じ言葉の繰り返し(保続)に有効な薬剤はない。
・うつ病のはSSRIは興奮を鎮めるのに有効だが、レム睡眠行動障害が誘発する可能性がある。
・幻覚、妄想、興奮が強い時は非定型抗精神病薬の投与を考慮する。
・ハロペリドール等の定型抗精神病薬はパーキンソニズムや遅発性ジスキネジアを誘発しやすい。
進行性非流暢性失語 /PNFA (pro- gressive nonfluent aphasia)
非流暢性、失語、発音の誤りなどの言語症状が優位にたつ症状。
近年のPNFAの患者ではアルツハイマー病病理を有する患者はめったにいない。
大半はタウオパチーを有する。失語や失文法のないPNFA患者ではアルツハイマー病病理またはアルツハイマー病特有のバイオマーカーを有する傾向にある。
海馬硬化症を有するレビー小体
www.ncbi.nlm.nih.gov/pubmed/25367383
www.ncbi.nlm.nih.gov/pubmed/27929803
意味性認知症/SD
側頭葉全部領域に強い萎縮が見られる。社会全般の一般的な知識に関する記憶障害を示す進行性の失語症。
画像や対象物の名付けが困難であり、単語の理解、分類、対象物の用途や特徴の理解も難しくなる。
意味記憶障害に対してエピソード記憶は比較的よく保たれる。
発語は流暢であり音韻性錯誤や文法的な誤りは認められない。
意味性認知症は、TDP-43 type Cと呼ばれるサブタイプのタンパク質と関連しており、遺伝的要因はまれ。
TDP-43については研究の蓄積があるが、TDP-43のサブタイプCについてはまだ基礎的な生物学的知識の研究が不足している。
ただし特異性が高いため、研究対象の標的としては有望とされている。
C型病変を伴う前頭側頭葉変性と皮質脊髄路変性の両者には関連があること。
www.ncbi.nlm.nih.gov/pubmed/23358603
オープンラベルの研究では、アリセプトなどのコリンエステラーゼ阻害剤、メマンチンは症状改善に明確な利益を示していない。
www.ncbi.nlm.nih.gov/pubmed/23358603
ランダム比較科試験 コリンエステラーゼ阻害剤の使用は行動障害を悪化させる可能性がある。
www.ncbi.nlm.nih.gov/pubmed/21157021/
小規模の二重盲検対照試験でトラゾドンによって、行動、症状を穏やかにする効果。
www.ncbi.nlm.nih.gov/pubmed/14666399/
感情へのアプローチとして、鼻腔内オキシトシンが一時的な利益があることが示唆されている。
www.ncbi.nlm.nih.gov/pubmed/21859765/
前頭側頭葉型認知症/FTD
臨床診断基準と神経病理学的診断基準による分類
・ピック型、ピック病(FTD-Pick)
・行動異常型前頭側頭型認知症(bvFTD)
・運動ニューロン疾患型(FTD-MND)
・前頭葉変性症(FTD-FLD )
その他
筋萎縮性側索硬化症/ALS
ALSでは、グルタミン酸トランスポーターEAAT2の発現が減少しており、DexpramipexoleがミトコンドリアのPTP開口を阻害し、ミトコンドリア機能を改善し、フリーラジカルによって損傷したニューロンを保護することが示されている。(Vieira,2014)
神経栄養性成長因子(NTF)がALSの運動ニューロンの生存を伸ばすことが示されている。(Petrou et al,2016)
TDP-43タンパク質の凝集がALSの病因の主要な事象かどうか、または別の病理学的プロセスの副産物であるかどうかも明らかではない。
現時点でALS治療として認可されている薬剤は、高グルタミン酸剤であるRiluzoleのみ。
免疫学的療法では、臨床試験中のアリモクロモールが有望であることが示されている。
FTLDの蓄積タンパクによる分類
過去には臨床像と病理像が対応する、推定できると考えられていたが、そうではない亜型の症例が少なからず存在し分類方法が混沌としていた状態であった。
病理組織のタンパク質、遺伝子の解明が進んだことから、蓄積したタンパク質の種類による分類が行われるようになっている。
FTLD-tau
タウオパチー
FTLDの症例の約半分に異常タウタンパクが含まれる。
FTDの大半はTDP-43プロテノパチーとタウオパチーであり、タウではタウキナーゼ、熱ショックタンパク質、ユビキチンプロテアソーム系、繊維形成の阻害、微小管を安定させる薬剤、神経保護治療、などが薬剤開発の標的となっている。
タウトランスジェニックマウスに関する研究では、メチレンブルーが第三相臨床試験まで通過しており、エンドポイントには達さなかったものの初期の段階ではFTD患者のタウオパチーを減少させた。(Hochgrafe et al,2015)
ピック病/ PiD
ピック病とはピック球、ピック細胞が神経細胞に見られる病理学的な診断名
もともとは、FTLDにはすべてピック球、ピック細胞があると考えられていたため
FTLD ≒ ピック病
となっていたが、後にピック球の存在しないFTLDがあることがわかったことから、現在はピック病はFTLDの一種として病理学的に分類されるようになった。
FTLD全体の95%以上がピック型。
前頭葉変性型の障害部位と類似するが、病変の程度は強く皮質全層におよぶ。
しかしこの定義に含まれない例もあり、FTLDの歴史はピック病の分類の歴史でもある。
大脳皮質基底核変性症/Corticobasal degeneration (CBD)
10万人あたり2~6人 女性に多いとされる
発症年齢は40-80歳代 通常50~70歳代で発症する。
もともとは原発性運動障害と考えられていた、非定形パーキンソン症候群。
現在は、認知障害として認識されており、通常は運動症状前に認知障害を示すが、非典型例が多く症状がまばらであることで悪名高い神経変性疾患。
病理
アルツハイマー型の神経病理学的変化はCBD症例の59%で見られた。
CBDは神経細胞、グリア細胞内への高ハニのタウオパチーが主要な病理学的実態であり、アストロサイトへのタウ蓄積はPSPとCBDを区別する。
PSPおよびCBDは独立した4Rタウオパチー
前頭葉、頭頂葉内に顕著なタウ病理を示す。
- 大脳皮質の限局性萎縮
- 皮質下神経核の変性
- Ballooned neuronの出現
CBD・CBSの鉄沈着
www.ncbi.nlm.nih.gov/pmc/articles/PMC4100470/
微小管関連タンパク質タウ(MAPT)の変異がある場合はFTLD-タウ病理を示す。
プログラニューリン(PGRN)遺伝子変異は頻繁に観察される。PGRN変異を有する場合は、FTLD-TDP病理を有する。
アミロイド症、タウオパチー、TDPノパシー、シヌクレインオパシ-、プリオンパシー
神経画像研究
前頭頭頂部領域の灰白質の萎縮と喪失
前頭葉、頭頂葉領域を含む広範囲の萎縮 TDP-43、AD病理
頭頂葉、前頭葉、基底核のグルコース代謝の低下
症状
皮質基底膜症候群(CBS)いう用語は臨床表現型を表す。
ミオクローヌス、ジストニアの出現頻度は半数以下。
進行すると姿勢保持障害、転倒が出現する。
arh.amegroups.com/article/view/4676/html
治療
リバスチグミンは精神神経症状の改善には役立つが、認知機能へは影響しない。
www.ncbi.nlm.nih.gov/pubmed/17389795
レボドパの治療は効果が認められない。
www.ncbi.nlm.nih.gov/pubmed/21626553
セルトラリン投与は、18人のFTD患者の言語と運動の常同行動を減少させた。
www.ncbi.nlm.nih.gov/pubmed/15786492
セルトラリン50mg/日投与によるCBD患者のうつ病の軽減
MAOIと併用禁忌
www.ncbi.nlm.nih.gov/pubmed/9775711
www.ncbi.nlm.nih.gov/pubmed/22307450
赤線 糸状タウ凝集 黄色線 原繊維タウ凝集
onlinelibrary.wiley.com/doi/full/10.1111/neup.12143
進行性核上性麻痺/PSP
嗜銀顆粒性認知症/AGD
FTLD-TDP
TDP-43
TDP-43は、通常核内に見出されるが、病理学的条件下では細胞質に移行し異常な封入体が形成される。
ほとんどの封入体はニューロン内に見られるが、グリア細胞でも見られる。
Type-A
神経細胞細胞質封入体/neuronal cyto- plasmic inclusion (NCI) 少数
ショートジストロフィー性神経突起 多数
第二層優位
bvFTD (behavioral variant FTD)
進行性非流暢性失語 /PNFA (pro- gressive nonfluent aphasia)
Type-B
・behavioral variant FTD(bvFTD)
・運動ニューロン疾患/MND with FTD
神経細胞細胞質封入体/neuronal cyto- plasmic inclusion (NCI) 中等数
ジストロフィー性神経突起/dystrophic neurites 少数
全層
ALS with dementia
Type-C
・意味性認知症 /semantic dementia(SD)
・behavioral variant FTD(bvFTD)
ロングジストロフィー性神経突起/long dystrophic neurites 多数
神経細胞細胞質封入体/neuronal cyto- plasmic inclusion (NCI) 少数
第二層優位
Type-D
・同一アミノ酸の病原性変異 /inclusion body myopathy with Paget’s disease of
bone and frontotemporal dementiac(IBMPFD)
ショートジストロフィー性神経突起/short dystrophic neurites 多数
レンズ型神経核内封入体 多数
神経細胞細胞質封入体/neuronal cyto- plasmic inclusion (NCI) 少数
全層
用語
ジストロフィー性神経突起/dystrophic neurite(DN)
www.ncbi.nlm.nih.gov/pubmed/26993139
www.ncbi.nlm.nih.gov/pubmed/27018282
カルシンテニン1/Calsyntenin-1の欠乏はAPのからのアミロイドβ産生の促進をもたらし、対照的に、カルシンテニン3の過剰発現は、アミロイドβプラーク周囲の神経突起の変化を引き起こす可能性が示されている。
アミロイドβ斑を取り囲む神経突起の神経毒性Cst-3-CTF(カルシテニン3細胞内C末端断片)の蓄積は、ニューロンプロセスの局所破壊およびジストロフィー性神経突起の発達を導き得る。
さらに、α-およびγ-セクレターゼによるカルシトニン-3のタンパク質分解プロセシングは、Cst-3-CTF蓄積によって引き起こされるアミロイドβプラーク関連神経突起変化から皮質ニューロンを救済するために重要であり得る。
onlinelibrary.wiley.com/doi/full/10.1111/ggi.12737
www.jsbmg.jp/products/pdf/BG35-4/35-4_1-7.pdf
神経細胞細胞質封入体/neuronal cyto- plasmic inclusion(NCI)
www.ncbi.nlm.nih.gov/pubmed/26935872
www.ncbi.nlm.nih.gov/pubmed/28984110
www.ncbi.nlm.nih.gov/pubmed/29128563
SALSのMATR3は運動ニューロンにおけるTDP-43陽性NCIの成分
FTLD-UPS
FTD-3 /Frontotemporal dementia
linked to chromosome 3
FTLD-FUS
aFTLD-U
NIFID / 神経細胞性中間径フィラメント封入体病
onlinelibrary.wiley.com/doi/10.1002/9781444341256.ch42
BIBD / basophilic inclusion body disease
FTLD-ni