Contents
The neuropsychiatric manifestations of COVID-19: Interactions with psychiatric illness and pharmacological treatment
www.sciencedirect.com/science/article/pii/S0753332220313937
ハイライト
- SARS-CoV-2感染と精神疾患に関与する炎症
- SARS-CoV-2は精神疾患の発症リスクがある
- 向精神薬の抗炎症作用がCOVID-19の転帰に悪影響を及ぼす
- 併用療法を選択すると、COVID-19の精神科合併症に役立つ可能性がある
要旨
近年のコロナウイルス感染症(COVID-19)の発生は世界的に大きな影響を与えている。重症急性呼吸器症候群コロナウイルス(SARS-CoV-2)感染と精神疾患との関係は非常に懸念されており、コロナウイルス感染と様々な中枢神経系および末梢神経系の症状との間には明らかな関連性がある。
未感染の神経炎症は、この病気の重篤な呼吸器合併症だけでなく、神経精神疾患の範囲にも存在することが指摘されている。いくつかの神経学的および精神医学的疾患は免疫炎症状態によって特徴づけられるが、これらの疾患に対する治療法には明確な抗炎症性の特性と効果がある。炎症は精神疾患だけでなく、SARS-CoV-2でも共通の寄与因子であるため、いずれかの疾患の治療は、他方の疾患の進行に影響を与えたり、薬理学的治療に対する反応を変化させたりする可能性がある。
このレビューでは、ウイルス感染が既存の精神疾患にどのように影響を与えうるか、また、これらの疾患に対する薬理学的治療がSARS-CoV-2の治療における全体的な進行と転帰にどのように影響を与えうるかを明らかにする。
我々は、根底にある神経炎症過程の調節障害や薬物相互作用の可能性を考慮して、治療によって誘発される利益や潜在的な副作用が最終的に治療アプローチ全体に影響を与えるかどうかを検討している。
最後に,SARS-CoV-2 に関連する神経精神症状に対する補助的な治療法の選択肢を提案する。
グラフィカル・アブストラクト
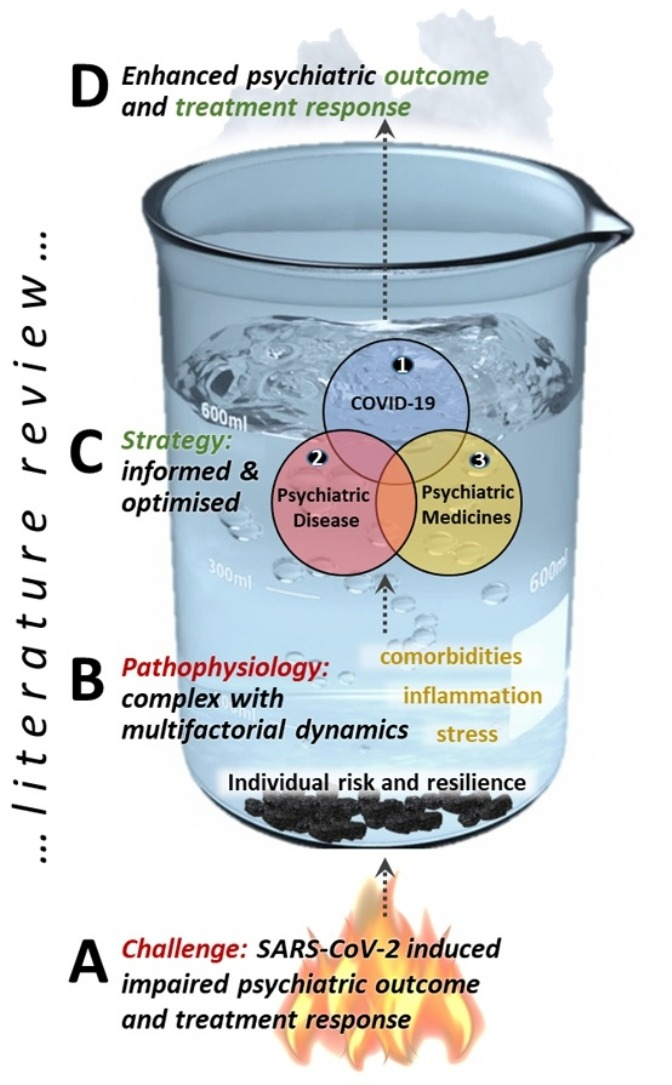
キーワード
SARS-CoV-2COVID-19psychiatric diseasesinflammationpharmacological treatment
1. SARS-CoV-2の概要、精神神経疾患の併存に重点を置いて
1.1.背景
2019年12月に中国・武漢で初めて確認された重症急性呼吸器症候群コロナウイルス2(SARS-CoV-2)[1]は 2020年には世界各地への感染拡大が進んでいる。新型コロナウイルスとして知られるこのウイルスは、「2019年のコロナウイルス病(COVID-19)」と名付けられた病気を引き起こし、人類の活動にかつてない規模で影響を与えている。急速な広がりは、国際的な旅行やグローバル化に煽られ、無症状の初期段階で感染する感染症と相まって、「コロナウイルス感染症」と呼ばれるようになった。この病気は未だに謎に包まれており、私たちはその未知の新しさに戸惑い、時には潜在的な脅威と観察される荒廃に圧倒されている。現在のところ、本疾患に関連するリスク、死亡率、その他の急性および長期の合併症を正確に予測するための過去のデータはない。有望な抗COVID-19ワクチンが開発されているか、承認されようとしている最中であるが、薬理学的に効果的な予防、封じ込め戦略、治療法はない。
一般的には、特に脆弱な人の呼吸器への致死的な影響があることが知られているが、精神疾患への影響など、他の潜在的な合併症が注目されている。実際、コロナウイルス感染症は神経系に親和性のあるウイルスとして定義され、神経向性ウイルス感染症としても知られている[2]。これに関して、Songらは、ヒトの細胞培養および死後の研究において、SARS-CoV-2の神経浸潤を実証した[3]。本レビューでは、このウイルスの発生を背景に精神疾患に焦点を当て、これらの病態の相互作用に関与する可能性のあるメカニズムについて議論する。また、提示された神経精神疾患の治療に関連した治療上の利点と潜在的な副作用、およびそのような治療が罹患者のSARS-CoV-2感染の経過をどのように変化させるかについても論じている。このような知見は、SARS-CoV-2に関連した神経精神医学的合併症に対する新たな治療法を特定するための新たな道筋を明らかにする可能性がある。
1.2. SARS-CoV-2に関連する病態生理と炎症反応
SARS(2002年)中東呼吸器症候群(MERS;2012年~2017年)および最新のSARS-CoV-2(2019)のアウトブレイクを含むコロナウイルス感染症の過去数十年間は、すべて類似した免疫学的特徴および病理学的影響を共有している[4,5]。これらは、(i)自然免疫細胞におけるウイルス複製、(ii)免疫応答の異常、(iii)サイトカインストーム、および(iv)抗体介在性応答という4つの主要な側面に分類できる[4,5]。SARS-CoV-2は、Coronaviridae科Coronavirina亜科Coronavirinaeの一部であり、これらのウイルスは、大型でエンベロープされた一本鎖RNAウイルスである[6]。重要なことに、これらのウイルスは大まかに球形をしており、その名前の由来となっている糖タンパク質[2,6]の顕著な「王冠のような」大きなスパイクを持っている。SARS-CoV-2は、宿主の解剖学的および化学的防御障壁を突破した後、図1に示すように、宿主細胞のアンジオテンシン変換酵素2(ACE-2)受容体に結合することにより、細胞内へのウイルスの侵入を媒介する。受容体の結合ドメインは、ウイルスのスパイクの中に隠され、免疫モニタリングを回避するように配置されている[7]。細胞質に入ると、ウイルスはウイルスエンドリボヌクレアーゼ(RNase)活性を放出するか、宿主細胞膜に複製小器官を形成して、自然免疫センサーによるウイルスRNAの認識を保護することで、自然免疫応答から逃れる[8,9]。培養期間中、ウイルスゲノムは複製され、宿主の自然免疫反応が活性化され、サイトカインの合成と放出が行われる[10](図1)。実際、炎症性マーカー(インターロイキン(IL)-2,IL-6,IL-7,IL-10,IL-18,インターフェロン(IFN)-γ、単球化学吸引性タンパク質(MCP)-1,MCP-3,マクロファージ炎症性タンパク質-1αを含む)は、症状の重症度と正の相関がある[11]。12], [13] 一方、特異的にはIL-6および腫瘍壊死因子(TNF)-αレベルは、感染した患者の症状の重症度および生存率の予測因子として機能する[14]。
図1 SARS-CoV-2感染に伴う病態と炎症反応
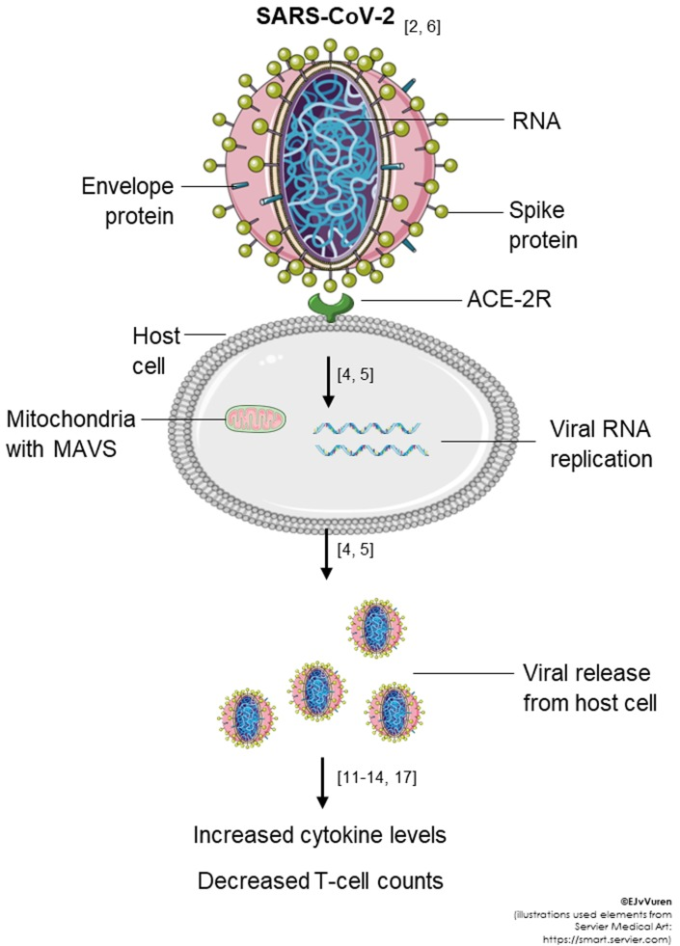
SARS-CoV-2ウイルスはACE-2Rに結合して宿主細胞に入り、ウイルスは宿主細胞の機械を利用して複製した後、ミトコンドリアウイルスのシグナル伝達を調節する。複数の新しいウイルスが宿主細胞から放出され、免疫応答とサイトカインのその後の放出を誘発する(詳細な議論については、サポートされているテキストを参照してほしい)。
略語
ACE-2R;アンジオテンシン変換酵素-2-受容体;MAVS;ミトコンドリア抗ウイルスシグナル;RNA;リボ核酸;SARS-CoV-2;重症急性呼吸器症候群コロナウイルス。
したがって、サイトカインの過剰な産生が急性呼吸窮迫症候群(ARDS)[15]および多臓器不全症候群(MODS)[16]につながるウイルス誘発現象であるサイトカインストームは、この疾患の特徴であるが、他の多くの合併症、特に中枢神経系の合併症を誘発する可能性もある。プロ炎症性サイトカインおよびケモカインの異常な増加を誘発する注目すべきウイルス因子には、ヘマグルチニン(HA)およびポリメラーゼ遺伝子セグメントが含まれる。興味深いことに、SARS-CoV-2に関連したサイトカインストームは、T細胞数の減少を伴うようであり[13,17]、ACE-2受容体はT細胞に発現していないため[18]、前述のT細胞数の減少は、ウイルスの直接的な原因ではなく、おそらくSARS-CoV-2誘導性サイトカインストームの間接的な結果であると考えられる[19], [20], [21]。これらをまとめると、COVID-19に関連した自然免疫系の変化は、二次感染または日和見感染を引き起こし、脳を含む複数の臓器を巻き込んだ深刻な結果をもたらす可能性があり、その場合、適応免疫応答が圧倒される可能性がある。
1.3. SARS-CoV-2に関連する精神的ストレスおよび精神症状
ますます明らかになってきたのは、SARS-CoV-2感染者は、非COVID対照者と比較して、うつ病、不安、心的外傷後ストレス障害(PTSD)症状の発現が高いことである [22]。最近、精神疾患の既往歴のない患者において、躁病様症状がSARS-CoV-2による中枢神経系感染に対する遅延反応である可能性があることが報告された [23]。これは、これらの患者が経験した重大な精神的ストレスによって媒介される可能性があるが [22]、この現象には神経病理学的な裏付けがあるかもしれない。
緊急時のメンタルヘルスおよび心理的サポートに関するガイドラインを提供する省庁間常設委員会は、SARS-CoV-2パンデミックの間、特定のストレス因子が過度に要求されたり、挑戦的であったり、影響を受けやすい患者を脅かしたりしていたことを明らかにした[24]。これらのストレス因子には、感染への恐怖、症状がCOVID-19と間違われること、感染の結果として個人の全身的な健康状態が悪化することへの懸念、経済的・家族的な支援システムや介護の能力などが含まれる[24]。これらのストレス要因が恐怖、心配、不確実性を伴う場合、社会的なスティグマ化や差別という長期的な結果をもたらす可能性があり、その結果、怒りや攻撃性の感情状態が高まる可能性がある [24]。最近の報告によると、COVID-19の心理的影響は、健康状態や職業の点でも異なる地域に住む個人で異なることが示唆されている[25]。中国では、最近の調査では、回答者の35%が心理的苦痛を報告しており[26]、一方で53.8%がパンデミックの心理的影響を中等度または重度と評価している[27]。したがって、特に心理的ストレスはSARS-CoV-2感染に関連した病態生理学的変化に関連する生物学的要素を有するため、心理的ストレスがCOVID-19患者だけでなく一般集団にも及ぼす影響を決定することは極めて重要である[28]。
レニンアンジオテンシン系(RAS)は、あまり研究されていないが、神経免疫学的プロセスや気分障害や不安障害などの精神疾患において重要な役割を果たしている [29]。SARS-CoV-2感染はカルボキシペプチダーゼであるACE-2を肺胞上皮細胞への侵入受容体として関与しているため[30,31]、ACE-2発現のダウンレギュレーションはSARS-CoV-2の発症に重要な役割を果たすだけでなく[32]、SARS-CoV-2誘発のストレス状態への脆弱性との関連を提供する可能性がある。実際、マウスにおけるACE-2発現のダウンレギュレーションは、交感神経活動を亢進させ[33,34]、トリプトファン取り込みを減少させ[35]、脳内5-ヒドロキシトリプタミン(5-HT; セロトニン)レベルの低下をもたらすことが示されており[36]、それによってストレス状態に対する脆弱性が増大する[37](図2)。さらに、視床下部のACE-2受容体は、不安に関連した行動や、生理的ストレス反応に関与する重要なホルモンであるコルチコトロフィン放出ホルモン(CRH)の合成を抑制する[33,38]。この文脈で重要なのは、カプトプリルやリシノプリルを含むACE阻害薬が、特定の患者において迅速に気分を高揚させる効果を有する可能性があるということである[39]。しかしながら、最近の動物研究では、この抗うつ作用はレニン-アンジオテンシン系よりもブラジキニン系に関連しており、哺乳類のラパマイシン標的(mTOR)によって媒介されることが指摘されており[39]、ケタミンの迅速な抗うつ作用に匹敵するものとなっている。SARS-CoV-2誘導性ACE-2ダウンレギュレーションによるCRH合成の減少およびその結果としてのグルココルチコイド産生の減少は、図2に示すように、COVID-19の進行を形成すると思われる動的な免疫応答[40]、特に過剰な炎症を制限するためのグルココルチコイドの負のフィードバック機構を損なうことによっても寄与し得る(SilvermanおよびSternberg[41]によるレビュー)。したがって、脳を含む様々なヒト組織[42]におけるACE-2の発現は、SARS-CoV-2の脳感染が重篤な中枢神経系(CNS)症状[43]をもたらし、SARS-CoV-2感染に関連した免疫炎症作用の悪化に加えて、これらの個体が精神疾患の発症を引き起こしやすいことを示唆している。この程度まで、最近のメタ解析では、SARS-CoV-2陽性患者におけるACE調節薬の継続が支持されており[44], [45], [46]、Songらは、中枢神経系に位置するACE-2受容体を抗体でブロックすることで神経細胞感染を予防することを示唆している[47]。
図2 正常なストレス-炎症カスケード(黒で表示)に対するSARS-CoV-2感染(赤で表示)の可能性のある効果
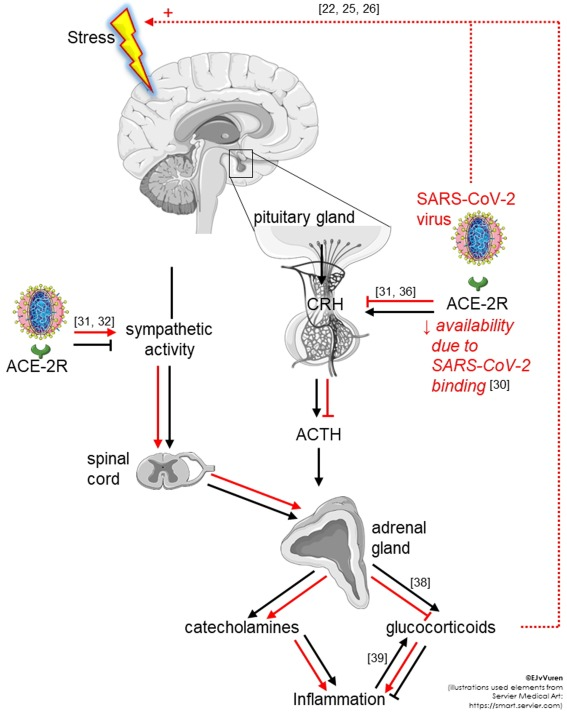
ARS-CoV-2とACE-2Rの結合は、受容体の利用可能性を減少させる。ACR-2Rの利用可能性が低下すると、CRHの下流機構が低下し、結果としてグルココルチコイドの産生が減少する。より少ないグルココルチコイドは、過剰な炎症を制限し、過活動的なストレス応答を防ぎ、永続的なストレス応答を作り出すために利用可能である。この残響ループは、環境条件や併存する精神疾患によってさらに誘発される(詳細な議論については、サポートされたテキストを参照のこと)。
略語
ACE-2R;アンジオテンシン変換酵素-2-受容体;ACTH;副腎皮質刺激ホルモン;CRH;コルチコトロフィン放出ホルモン;SARS-CoV-2;重症急性呼吸器症候群コロナウイルス。
したがって、COVID-19の心理社会的影響は、特に不安およびストレス関連障害の有病率が前例のないほど増加するための基礎を築いており、これにより、気分障害(うつ病および双極性障害)統合失調症、薬物乱用などの多くの他の併存精神疾患の発症を早める可能性がある。したがって、これらの精神疾患とCOVID-19の病理学的経路を共有することは、これらの併存疾患の基礎を理解し、それらを最適に治療する方法を理解する上で鍵となる。
2. 精神疾患におけるストレス、炎症、治療反応の関連性
炎症性機序は、組織の恒常性を維持するための感染または傷害に対する本質的な防御反応である(BennetおよびMolofsky[48]によるレビュー)。これには、サイトカインなどの炎症性メディエーターを放出するマクロファージなどの防御細胞を動員し、病原体の拡散を制限し、組織の修復を開始するプロセスが含まれている。中枢神経系内の炎症に関しては、アストロサイトとともに炎症プロセスの調停および調節に関与するミクログリア細胞の役割に大きな関心が集まっている[49]。ミクログリアは中枢神経系の「マクロファージ」として機能し、プロまたは抗炎症シグナルに反応して活性化されることがある [50]。活性化されると、これらの常駐する自然免疫細胞は、免疫学的刺激によって活性化されると、プロ炎症性サイトカイン、エイコサノイド/プロスタノイド、一酸化窒素(NO)神経栄養因子などの因子を放出し、防御反応を発揮し、組織の修復を促進する [51]。しかし、急性炎症が元々の侮辱が取り除かれた後に収まらない場合、ミクログリアの活性化を悪化させ、プロ炎症性サイトカイン産生および酸化ストレスをさらに増強させ[51]、健康な組織の破壊および最終的には脳機能の障害を引き起こす可能性がある[52,53]。さらに、傷害や毒素によって引き起こされる血液脳関門の障害は、炎症性メディエーターや循環に存在する病原体の浸潤を引き起こし、中枢神経系の炎症をさらに悪化させる可能性がある(レビューは[54]を参照のこと)。
炎症の下流のメカニズムは多因子性であり、図3に示すように、様々な細胞シグナル伝達経路が関与している(BennettとMolofsky[48]によるレビュー)。TNF-α、IL-6およびIFNを含む末梢性および中枢性のプロ炎症性サイトカインの増加は、酸化ストレス(活性酸素および窒素種(ROS; RNS)の産生を介して)につながる。55,56]、アポトーシスの誘発[57,58]、そして最終的には神経伝達物質のシグナル伝達の変化[59], [60], [61]。これらのメカニズムはすべて、精神疾患の発症と進行に役割を果たすことが示されている[56,60,62]。実際、それぞれの健常対照者と比較した場合、精神病性[[63], [64], [65]]、気分障害[66]および不安関連障害[67,68]の患者では、プロ炎症性サイトカインレベルの上昇が観察され、一方でIFNのようなプロ炎症性サイトカインの治療的使用は、抑うつ症状を誘発することが知られている[69]。ここでは、このことについて考察する(図4)。
図3 SARS-CoV-2感染、ストレス、過剰な炎症が精神疾患の発症を促進する川下効果
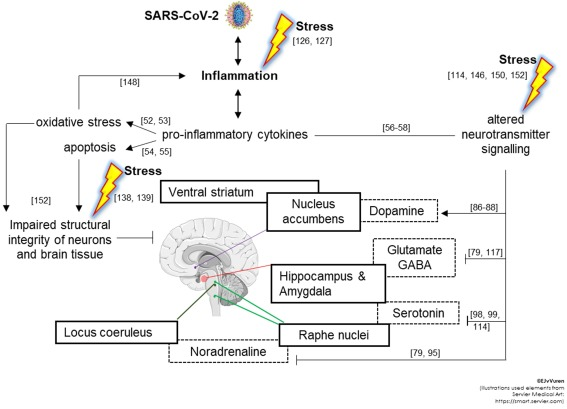
SARS-CoV-2の感染とストレスは過剰な炎症を引き起こし、神経伝達物質のシグナル伝達を変化させ、様々なメカニズムで神経細胞の構造的完全性に悪影響を及す。このような変化は、腹側線条体、海馬、扁桃体、ラッパ核、および脊髄座を含む様々な脳領域において、ドーパミン、グルタミン酸、GABA、セロトニン、およびノルエピネフーリンのレベルに異常をもたらし、精神病性障害、気分障害および不安関連障害の発症に寄与したり、あるいは既往症を悪化させたりする可能性がある(詳細な議論については、添付文書を参照のこと)。
略語
GABA、γ-アミノ酪酸
図4 COVID-19パラダイムにおける基本的なリスク評価と精神疾患の管理を模式的に示したもの
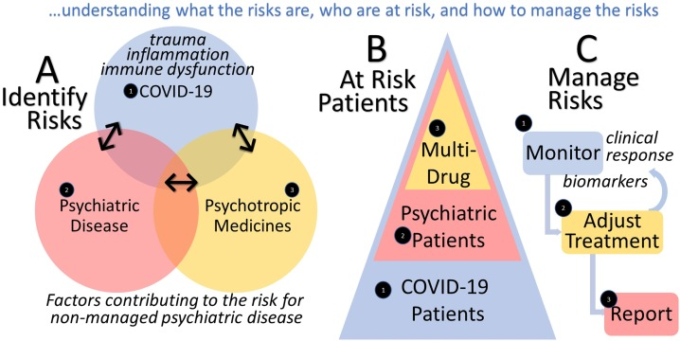
リスク評価の基本的なステップは、(A)リスクを特定すること、(B)最もリスクの高い患者を特定すること、(C)これらのリスクを適切に管理する方法を説明することである。スキーマでは、リスクには炎症や免疫機能障害を引き起こすSARS-CoV-2ウイルスそのものが含まれる。さらに、あらゆる既往の精神疾患や向精神薬(または他の精神活性薬)の使用は、COVID-19に関連する精神疾患のリスクを追加する。リスクのある患者には、SARS-CoV-2感染者、精神疾患の既往、多剤併用の患者が含まれる。リスク管理の重要な要素としては、臨床反応の積極的なモニタリング、炎症のバイオマーカーの同定とモニタリング、反応に応じた治療の調整、モニタリングの継続が挙げられる。最後に、記録を残すために、また、将来の治療戦略、例えば補助的治療などを最適化するために、そのような所見を報告することである(さらなる議論は本文に記載されている)。
略語
COVID-19,コロナウイルス病2019;SARS-CoV-2,重症急性呼吸器症候群コロナウイルス
精神科患者の炎症状態が治療反応に一役買っていることを示唆する証拠がある[70]。例えば、炎症性疾患(関節リウマチ、喘息、狼瘡、潰瘍性大腸炎)と診断された患者では抑うつ症状が頻発しているが、免疫調節薬はこれらの症状を改善する。さらに、ウステキヌマブ(抗IL-12/23抗体)やシルクマブ(抗IL-6抗体)は抗うつ作用を示す[71]。逆に、可溶性IL-2受容体(sIL-2R)の濃度上昇は、治療抵抗性の精神病において記載されている[72]一方で、IL-6およびIFN-γの濃度上昇は、初回エピソードの精神病患者における治療反応不良と関連している[73]。同様に、IL-1β、IL-6およびTNF-αのベースライン遺伝子発現は、治療抵抗性うつ病患者において増加する[74], [75], [76]。したがって、これらの研究は、追加の抗炎症薬が、特にベースラインで炎症状態にある患者において、精神疾患の治療において重要なアプローチである可能性があることを強調している。実際、Areaga-Henríquezら[77]の最近のレビューでは、インフリキシマブ(抗TNF-α薬)ミノサイクリン(テトラサイクリン系抗生物質)またはエイコサペンタエン酸(オメガ3脂肪酸)の使用が、ベースラインのCRP/IL-6値が上昇しているうつ病患者における治療反応を改善することが示されている。同様に、Kohlerら[78]。78]は、セレコキシブ(シクロオキシゲナーゼ(COX)-2阻害剤)ロバスタチンまたはシムバスタチン(ヒドロキシメチルグルタリル(HMG)-コエンザイム(Co)A阻害剤)ミノサイクリン、ピオグリタゾン(チアゾリジンジオン)を投与した場合に、CRP/IL-6値が上昇することを報告している。モダフィニル(精神刺激薬)およびデキサメタゾン(コルチコステロイド)は、うつ病に一般的に使用される選択的セロトニン再取り込み阻害薬(SSRI)の追加治療として同様に有効である。実際、これらの追加治療法は、うつ病症状の軽減においてSSRI単独またはプラセボよりも優れている可能性がある[78]。しかし、統合失調症では、これらの抗炎症薬は陽性症状に対してわずかな効果しかない[79]。一方、トシリズマブ(抗IL-6剤)は認知症状を改善するが、ミノサイクリンとプレグネノロン(内因性ステロイド)はこれらの患者では陰性症状を改善する(Melbourneらによるレビュー[80])。
一方、最近の研究では、プロ炎症状態(リポ多糖(LPS))と抗炎症状態(非ステロイド性抗炎症薬であるイブプロフェン)の両方の後のマウスにおける用量依存的な神経可塑性の障害が記述されている[81]。神経可塑性の障害は多くの精神疾患の中心であるため[82]、このことは、プロ炎症性と免疫抑制性の状態が精神疾患とその治療への反応に影響を与える可能性があることを浮き彫りにしている。さらに、免疫応答を標的とすることに関連した逆説的な作用として、抗酸化化合物は、細胞内の酸化還元炎症状態に応じて抗酸化剤またはプロ酸化剤として作用することがある。このことは、精神疾患の重症度や病態が時間の経過とともに変化する場合に特に関連している。これらの研究は、精神科治療薬が効果を発揮するためには、炎症を注意深く管理する必要があることを明確に示している。
2.1. 精神病性障害
統合失調症などの精神病性障害は、陽性の精神病症状を媒介する脳内の中脳辺縁系ドーパミン(DA)シグナルが異常に高いことを特徴としている[83,84]が、中脳皮質のDAシグナルの低下は認知症状や陰性の精神病症状と関連している[83]。このような変化したドーパミン作動性シグナルは、DA合成、パッケージング、放出および再取り込みに対するサイトカインの負の効果に起因する炎症によって媒介される可能性がある[85](図3)。実際、ヒトにおける母体の炎症は、統合失調症を含む晩年の精神病理と関連している(Depino[86]によるレビュー)。臨床研究では、C反応性蛋白(CRP)やIL-8などの母体のサイトカインレベルの上昇が、成人の子供の統合失調症スペクトラム障害のリスクを高めることが示されている[87,88]。同様に、母親の抗炎症性サイトカイン(すなわちIL-4,IL-5,IL-13)のレベルが上昇した個体は、成人期に精神病を発症する可能性が有意に低かった [89]。実際、TNF-αは統合失調症患者の足底核におけるDAと5-HTの代謝産物を増加させる [90]。また、動物実験では、出生前の炎症が後天核のDAレベルを上昇させ、ラットの成体子孫に統合失調症に特徴的な行動変化を誘発することが明らかにされている[91]。同様に、TNF-αはマウスの後天性核におけるDAと5-HT代謝物を増加させる [92]。このような継続的なストレス因子や感染性ストレス因子は、ミクログリアの活性化、中枢炎症の亢進、および海馬の損傷 [93,94] につながる可能性があり、これは精神病で観察されるドーパミン作動性の過剰駆動を少なくとも部分的に説明することができる [95]。実際、精神的ストレスにさらされた抗精神病薬を服用していない統合失調症患者の線条体ではDA放出が増加していることが報告されている[96]。精神病の病態生理に関与し、炎症の影響を受ける他の神経伝達物質には、図3に示すように、5-HT、ノルエピネフーリン(NE)グルタミン酸がある[83,97]。例えば、トリプトファン-キヌレニン代謝はグルタミン酸シグナルと同様に5-HTを調節している[98]が、トリプトファン-キヌレニン代謝の乱れは炎症促進状態と脳のDAレベルの局所的な変化を伴うことが統合失調症の動物モデルで報告されている[99]。微量アミンは、精神病におけるストレス-炎症カスケード(Gainetdinovらのレビュー[100])を議論する際にも関連しているが、微量アミン関連受容体1(TAAR1)への作用を介してマクロファージにおける炎症性サイトカイン産生を調節する。TAAR1はモノアミン神経伝達を調節し、ドーパミン作動性亢進およびグルタミン酸作動性低下を抑制する [101]。
抗精神病薬は、免疫炎症性カスケードに対する効果が異なるが、前臨床では異なる効果を示す(表1に示すように)。カラギナン誘発性炎症性ラットモデルでは、ハロペリドールは炎症反応を亢進させる[104]が、トリフルオペラジンは抗炎症作用を示す[105]とアリピプラゾールは抗炎症作用を示す[106]。炎症に重要な転写因子であるNF-kBの活性化は、IκBキナーゼ(IKKβ)によるIκBαのリン酸化に依存しており、チオリダジンによって阻害され、抗炎症作用を誘導することが示されている[107]。また、本剤は自己免疫性脳脊髄炎マウス[108]や社会的隔離飼育(SIR)モデル[99]においても抗炎症効果を発揮する。SIRモデルを用いた別の研究では、オランザピンは肝GSH依存性防御の変化を逆転させたが、抗炎症効果は誘導されなかったことが明らかになった[109]。オランザピンはまた、マウスでは大動脈の炎症[110]と関連しており、ラットでは微生物叢の変化(Handら[111]のレビューにあるように慢性炎症性疾患状態と関連している)と関連しており[112]、このように炎症促進作用が示唆されている。リスペリドン[113]やクエチアピン[114]などの他の抗精神病薬も抗炎症作用を有することが報告されている。
表1 向精神薬の抗炎症作用および抗炎症作用
| ドラッグクラス | 抗炎症薬 | 炎症誘発性 |
|---|---|---|
| 抗うつ薬 | ||
| SNRI | ||
| デュロキセチン | ↓IL-6、TNF-α[ 357、358 ] | – |
| ベンラファキシン | ↓IL-1β、IL-6、IL-18、TNF-α; ↑IL-10 [ [359]、[360]、[361]、[362] ] | – |
| SSRI | ||
| シタロプラム | ↓CRP、IL-6、IL-7、IL-8、IFN-γ、TNF-α、TLRの[ 158、350、363 ] | – |
| エスシタロプラム | ↓TNF-α[ 349 ] | – |
| フルオキセチン | ↓TLRの[ 350 ] | – |
| フルボキサミン | ↓COX2; iNOSの、ICAM1、VCAM1 [ 146、363 ] | – |
| パロキセチン | – | ↑IL-6、IFN-γ、TNF-α[ 363 ] |
| セルトラリン | ↓CRP、IL-1βのmRNA、IL-6、IL-7、IL-8、IFN-γ、TNF-α[ 145、158、363 ] | – |
| 三環系および四環系 | ||
| アミトリプチリン | ↑IL-10; ↓IL-1β、IL-18、ICAM-1、MIP-2、MCP-1、TNF-α[ [364]、[365]、[366] ] | – |
| デシプラミン | ↑IL-10 [ 364、366 ] | – |
| イミプラミン | ↓IL-1β、IL-18 [ 367 ] | ↑IL-1 [ 363 ] |
| ミルタザピン | ↓IL-6、IL-7、IL-8、IFN-γ、TNF-α[ 158 ] | – |
| その他 | ||
| アゴメラチン | ↓IL-1β、IL-18、酸化ストレスによる損傷; ↑グルタチオン[ [266] 、[267] 、[268] 、368、369 ] | – |
| ケタミン | ↓IL-1β、IL-6、TNF-α[ 370、371 ] | ↑IL-6、IL-1β、TNF-α[ 153 ] |
| 抗精神病薬 | ||
| 非定型 | ||
| アリピプラゾール | ↑IL-10; ↓CRP、IL-1β、IL-4、IL-6、IL-7、IL-8、IL-12、IL-13、 | – |
| クロザピン | IL-17A、IL-21、IL-23、IFN-γ、TNF-α、STNF-R1 [ 106、116、118 ] | |
| オランザピン | ↓CRP、IL-2 [ 117、372 ] | ↑TNF-α、STNF-Rの[ 121、122、374 ] |
| クエチアピン | ↑IL-10; ↓CRP、IL-1β、IL-6、IFN-γ、TNFα[ 114、117 ] | ↑IL-1β、IL-6、IL-8; TNF-α[ 110、112、 [374]、 [375]、 [376] ] |
| リスペリドン | ↓IL-1β、IL-2、IL-6、IL-7、IL-8、IL-13、IL-17α、IL-21、IL-23、 | – |
| ジプラシドン | TNF-α[ 116、119、373 ] | |
| ↓IL-2、IL-6、IFN-γ、TNF-α[ 373 ] | – | |
| 気分安定薬 | ||
| カルバマゼピン | ↓IL-1β、TNF-α[ 164、165 ] | ↑TNF-α[ 377 ] |
| ラモトリジン | ↓IL-2、IL-6、TNF-α[ 166 ] | – |
| リチウム | – | ↑IL-4、TNF-α[ 167 ] |
前臨床の証拠はハロペリドールの抗炎症性プロファイルを示唆しているが[104]、臨床データは一致していない[115]。抗精神病薬の抗炎症性を支持する臨床研究(表1)には、オランザピンとクエチアピン[[116], [117], [118]やリスペリドン[116,119,120]などがある。しかし、治療抵抗性の統合失調症のために予約されているクロザピンは、治療開始後1ヵ月以内に最大50%の患者に無顆粒球症や心筋炎などの重篤な炎症性副作用を多数誘発することが知られている[121]。clozapineの抗炎症作用を示すより多くの証拠は、6週間の治療後に統合失調症患者で観察されたTNF-αおよび可溶性TNF-α受容体の増加に関連している[122]。しかし、1つの研究では、初回エピソードの妄想性統合失調症患者において、6ヵ月間の治療後にクロザピンの免疫抑制作用が観察された[119]。
上記の証拠を検討すると、抗精神病薬が炎症機序、特にサイトカインレベルに影響を与えることが明らかになるが、研究によって結果は異なる [80,123]。実際、多くの研究で抗炎症作用と抗炎症作用の逆説的な作用が強調されている。このため、各薬剤が異なる病態下でどのように作用するのか、また、どこに神経増悪が関与しているのかを予測することは困難である(表2)。
表2 COVID-19感染時の向精神薬の補助的治療
| ドラッグクラス | 精神医学的影響 | 炎症関連の影響 | 抗ウイルス関連の効果 |
|---|---|---|---|
| 酸化防止剤 | |||
| α-リポ酸 | – | ↓ROS、アポトーシス[ [277]、[278]、[279] ] | ↓gliotoxicity、ウイルス複製およびシグナル[ 277、278 ] |
| マンゴスチン果皮 | 抗うつ薬[ 285 ] | – | ↓ウイルスプロテアーゼ[ 287 ] |
| Sceletium tortuosum | ↓不安、うつ病[ 378 ] | 抗炎症剤[ 283 ] | ↓ウイルス酵素とプロテアーゼ[ 284 ] |
| チモキノン | ↑空間記憶およびアルツハイマー病の合併症の鈍化[ 288、379 ] | ↓NOおよびROS; 調節(阻害)するNF-κB及び抗酸化酵素核因子2ヘムオキシゲナーゼ-1(のNrf2 / HO-1)[ 288、289、380 ] | ↓宿主細胞へのウイルス侵入[ 290 ] |
| Alpha-2-ARモジュレーター | |||
| クロニジン | ↓精神病、不安[ 297、298 ] | – | ↓ウイルス複製[ 296 ] |
| COX-II阻害剤 | |||
| セレコキシブ | ↑気分[ 78 ] | ↓IL-6、TNF-α[ 301 ] | ↓COX-2のウイルストランス[ 299、300 ] |
| 糖質コルチコイド | |||
| デキサメタゾン | ↑うつ病[ 78、304、305 ] | ↑酸化ストレス、炎症[ [306]、[307]、[308] ] | – |
| リチウム | 抗うつ薬[ 309 ] | ↓NF-κB[ 312 ] ↑炎症誘発性活性[ 167 ] ↑NO-cGMP経路活性[ 315 ] |
– |
| MT-1および-2アゴニスト | |||
| アゴメラチン | 抗不安薬、抗うつ薬[ 266、267 ] | ↓CRP、IL-1β、IL-6 [ 263、264、267 ] | |
| テトラサイクリン | |||
| ミノサイクリン | ↑気分[ 77、78 ] | ↓炎症[ 317 ] | ↓ウイルスの複製と再活性化[ 320 ] |
| ミトコンドリアの若返りとモジュレーター | |||
| メチレンブルー | ↑気分[ 147 ] | 抗酸化剤[ 324 ] | RNAウイルスを不活化する[ 325 ] ↑MAVS [ 330 ] |
| N-アセチルシステイン | ↑気分[ 381 ] | 抗酸化剤[ 382 ] | ↑MAVS [ 330 ] |
| mTOR阻害剤 | |||
| ラパマイシン | 抗うつ薬[ 345、346 ] | ↓酸化ストレス、過炎症[ 344 ] | ↑抗ウイルス活性[ 342、343 ] |
| NF-κB阻害剤または拮抗薬 | |||
| ウアバイン | ↑気分障害[ 335 ] | ↓NF-κB[ 333 ] | ↓ウイルス複製[ 334 ] |
| ジゴキシン | – | ↓NF-κB[ 333 ] | ↓ウイルス複製[ 334 ] |
| PDE-4阻害剤 | |||
| ロリプラム | – | ↓サイトカインストーム[ 336 ] | – |
| イブジラスト | – | ↓サイトカインストーム[ 336 ] | – |
| PDE-5阻害剤 | |||
| シルデナフィル | 抗不安薬、↑気分[ 172、237、339 ] | ↓炎症誘発性サイトカイン[ 337 ] | – |
| タダラフィル | – | – | ↓cGMP [ 236 ] |
| PPAR-γアゴニスト | |||
| ピオグリタゾン | ↑気分[ 78 ] | ↓サイトカインストーム[ 341 ] | – |
| トリプトファン-キヌレニンモジュレーター | |||
| アロプリノール | ↓炎症誘発性精神病理学[ 98 ] | ↓炎症[ 98 ] | – |
2.2. 気分障害
モノアミン作動性神経伝達の低下は、気分およびエネルギーの低下、快楽を感じることができない(無気力症)興味および意欲の喪失、および注意力の低下などの抑うつ症状の主な原因として確立されている[83,124]。ここではトリプトファン-キヌレニン経路も関連している。複数の炎症性シグナル伝達経路は、5-HT前駆体であるトリプトファンの分解を引き起こすインドールアミン2,3ジオキシゲナーゼ(IDO)を活性化するようである(Millerらによるレビュー[125])。炎症によって誘発される5-HTの減少は、げっ歯類において抑うつ状態に似た状態を引き起こす [126]が、同様の所見は薬物ナイーブの大うつ病性障害(MDD)患者でも報告されている [127]。炎症はまた、5-HTトランスポーター(SERT)の発現を増加させ、それによって5-HTの再取り込みを増加させ、シナプスの利用可能性を低下させる [128]。この作用は海馬の5-HT受容体の発現をダウンレギュレートし、最終的には抑うつ症状に寄与する[129](図3)。慢性的な予測不可能なストレスは、ラットの前頭前野と線条体において酸化ストレスを増加させ [130]、中枢性炎症を悪化させる可能性があることは注目に値する(Bakuninaらによるレビュー [131])。抗酸化酵素活性(スーパーオキシドディスムターゼなど)の変化と脂質過酸化の増加 [133] は、MDDに関連するサイトカイン誘発性酸化ストレスを引き起こす [132]。その結果、ニューロトロフィンレベルの低下 [134] と、これらの領域の機能と適応可塑性の低下 [135] は、脳が不利な環境条件を克服して学習する可能性が低いことを示唆している。NO-環状グアノシン一リン酸(cGMP)シグナル伝達もMDD患者では障害される [136]一方で、NOシグナル伝達はMDDの病態生理の根底にある炎症性経路を調節することが示唆されている [137,138]。実際、慢性ストレスはストレスに敏感なラットの海馬の構成性NOS活性を増強し、それによって機能不全のグルタミン酸NMDA-NO活性がMDDの脆弱性因子であることを示唆している[139]。重要なことに、ストレスを受けた動物の大脳辺縁部では、nNOSとiNOS由来のNOレベルの両方が変化していた[140]。これらの変化は、ストレスへの適応を阻害し、MDDに対する脆弱性を増大させる行動異常および内分泌異常の発生に寄与している可能性がある。プロスタグランジンE2(PGE2)合成の律速酵素であるCOX-2もまた、慢性的なストレスを受けたラットでは有意に上昇しており、その阻害はグリアの活性化、酸化ストレス、および神経細胞のアポトーシスを抑制することにより、うつ病様の行動を逆転させる[141]。これらの変化した敏感な酸化還元状態が、MDDに関連した行動症状の多くを駆動している[142,143]。
主にMDDにおけるモノアミン作動性レベルの変化を標的とする承認された抗うつ薬は、表1に示すように、臨床改善に寄与する抗炎症特性も示す [144]。ラットの強直間代発作モデルにおいて、セルトラリンは抗炎症特性を示した [145]。同様に、フルボキサミンは、カラギーナン注射によるラットの炎症モデルにおいて、炎症性遺伝子の発現を減少させた[146]。NO および cGMP シグナルのモジュレーターは、MDD 患者または動物実験で抗うつ効果を発揮する[147]。実際、NOおよびcGMPシグナル伝達は、うつ病の動物モデルにおいて、様々な既知の抗うつ薬によって標的化されている[148]。驚くことではないが、COX-2阻害薬は双極性障害において、また治療抵抗性うつ病における補助的治療薬として価値があるかもしれない[149,150]。N-メチル-D-アスパラギン酸(NMDA)受容体の拮抗薬であるケタミンは、抗炎症作用を示す一方で、急速に発症する抗うつ特性を有する[151] [152]。興味深いことに、炎症に対するケタミンの活性は治療期間に関係しているようである[153]。この点で、長期治療は、抗うつ薬抵抗性の遺伝子X環境モデルにおいて、イミプラミンに対する失敗した反応を増強するのに有効である[154]。炎症性の成分が治療抵抗性の臨床例に寄与することが知られており[155]、これはケタミンがどのように反応を再確立するかを部分的に説明することができるかもしれない[156]。
MDDと診断された患者において、Szałach、Lisowska、Cubała [157]は、パロキセチン、ベンラファキシン、デスベンラファキシン、イミプラミン、アミトリプチリン、アゴメラチンが炎症性遺伝子の発現を有意に減少させ、さらにインフラマソーム活性を低下させることを発見した。新たにMDDと診断された患者において、抗うつ剤治療(セルトラリン、ベンラファキシン、シタロプラム、またはミルタザピン)を12週間継続すると、血中サイトカインレベルが有意に低下することが明らかになった[158]。重要なことは、これらのサイトカインの低下は、治療に対して臨床的な反応を示した患者にのみ認められたことである。NOを考慮すると、血漿硝酸塩レベルの上昇は、インターフェロンアルファ療法中のうつ病症状に関与しているだけでなく、うつ病状態でも記述されている[69,159]。虚血性心疾患とうつ病に苦しんでいる患者を対象とした研究では、血清亜硝酸塩および硝酸塩レベルはパロキセチン治療後に有意に減少したが、ノルトリプチリンは減少せず、パロキセチンはノルトリプチリンよりもNOSのより強力な阻害剤であることが示されている[160]。
上記のデータから明らかなことは、抗うつ薬には様々なプロおよび抗炎症作用があり、これは病気の進行と同様に化学的なクラスの機能であるかもしれないということである。
2.3. 双極性障害
双極性障害は慢性的で周期的な精神障害であり、躁・過躁と抑うつの間の異常な気分変動が特徴である[161]。この疾患の経過は、しばしば継続しないため、時間の経過とともに認知障害が生じることが多く、さらに、現在利用可能な薬剤の部分的な有効性により、しばしばポリファーマシーを必要とする。免疫系と神経炎症は、その病態生理、特に疾患経過において中心的な役割を果たしているが、同時に、非ステロイド性抗炎症薬、N-アセチルシステイン、GSK3阻害薬などの新規抗炎症・抗酸化治療の標的を提供している[162]。躁病様症状および炎症は、双極性障害に関連するげっ歯類モデルである躁病のオウアバインモデルで記述されている[163]。ここでは、一般的に使用されている抗炎症剤であるアスピリンが躁病様症状を部分的に逆転させるとともに、双極性障害患者に多く見られる脳由来神経栄養因子、IFN- CORP、Toll様受容体3の発現を低下させた。カルバマゼピンはラットにおいて用量依存的に抗炎症作用を誘導する[164]が、この作用はバルプロ酸塩では観察されなかった[165]。ラモトリギンもまた、LPS曝露後のマウスにおいて抗炎症作用を示す[166]。最近発表された研究[167]では、リチウムまたはバルプロ酸で治療された双極性障害患者のTリンパ球が、増殖活性の低下とアポトーシスに対する感受性の増加を特徴とするプロ炎症活性を示すことが示された。一方、バルプロ酸塩を12週間投与しても、双極性うつ病と診断された患者では、プロ炎症性サイトカインに対する効果は認められなかった[168]。
2.4. 不安関連障害
不安や恐怖は、心配と同様に、すべての不安関連障害に存在する [169,170]。不安症状は主に扁桃体中心回路の機能障害と関連しているのに対し、心配症状はコルチコ・ストライアト・視床皮質(CSTC)ループの機能障害と関連しており、いずれも5-HTとγ-アミノ酪酸(GABA)の障害が関与している [83]。不安に関連する他のメッセンジャーには、5-HT、メラトニン[171]、NO-cGMP経路[172,173]、グルタミン酸[174]、および神経ペプチドであるオキシトシンとバソプレシン[175]がある。興味深いことに、これらの経路はすべて酸化還元プロセスと相互に関連しており、例えば、メラトニンは抗酸化特性を持ち[176]、グルタミン酸-NOS経路は酸化ストレスを刺激し[173]、一方、バソプレシンとオキシトシンは試験管内試験での酸化ストレスの条件下で保護効果を持つ[177]。慢性的なストレスはGABAニューロンの構造的完全性を変化させ [178]、扁桃体 [179]を抑制し、心配性症状の増加の原因となっている可能性が高い(図3)。慢性的な末梢性炎症は、TNF-α発現をさらに増加させ、グルタミン酸興奮性シナプス伝達を増強し、扁桃体におけるGABA受容体媒介の抑制性シナプス伝達を阻害することで、不安の発症に寄与する[180]。炎症誘発性酸化ストレスはストレス曝露中に増加し、PTSDなどの不安状態を悪化させることがわかっている[181,182]。さらに、エンドカンナビノイドレベルの低下は、これらの個体で観察される炎症状態の増加に寄与している可能性がある[183]。NOはまた、不安に関連した中枢性炎症と関連している。急性の激しいストレスは、最初は神経細胞のNOSの活性化を介してNOを増加させ、慢性的なストレス後には構成的な免疫学的NOS(iNOS)を介したNO産生に戻る[185]。これらの作用は海馬NMDA受容体の反応性ダウンレギュレーションと抑制性GABAの減少を伴っており、PTSDなどの重度の不安障害における神経毒性と海馬の変性における炎症性NOの役割を支持している[185]。核因子-ĸB(NF-ĸB)は炎症における重要な転写因子であり、PTSDの動物モデルにおいてNMDA-NO-環状GMPカスケードと相互に関与していることが示されている[186]。
炎症と不安との関連性を示す最も顕著な例は、腸内環境異常である。ここでは、親炎症性種(例えば、EnterobacteriaceaeやDesulfovibrio)がより多く存在することを特徴とする細菌種の違いが、末梢性炎症の脳への伝達を介して不安とうつ病の病態生理を誘発する[187]。蓄積された証拠は、炎症の亢進が心的外傷後ストレス障害(PTSD)などの不安障害の病態生理に寄与していることを示唆しており[173]、抗炎症薬がPTSDの新しい治療戦略である可能性があることを示唆している[188]。臨床的に使用されている様々な抗不安薬には他の作用があり、アゴメラチン[189]やSSRI[190]のように、酸化還元炎症プロセスを間接的に標的としている。これらの薬物は慢性不安関連障害の管理に承認されている[190]。しかし、GABAが不安関連障害で果たす中心的な役割は議論の余地がない[191]。興味深いことに、様々な末梢性ベンゾジアゼピン受容体リガンドは抗炎症作用を発揮する[192]。抗不安薬であるエチフォキシン[193,194]は、GABAA受容体およびミトコンドリア18-kDaトランスロケータータンパク質(TSPO)への作用を介して抗不安作用および抗炎症作用を誘導する[195]が、後者はその抗炎症特性に関与している([196]によるレビュー)。
まとめてみると、心理的ストレスは、図3に示すように、精神疾患のリスクを高め、炎症性経路を介して疾患の経過を形成する可能性さえある[197]。この相互作用は、中枢性炎症を悪化させる可能性のある感染症の存在下で精神疾患の薬理学的治療を検討する際に特に重要である。
3. ウイルス性炎症と精神疾患の経過との相互作用
SARS-CoV-2の心理社会的影響は、特に不安障害の有病率の前例のない増加を促しており、気分障害(うつ病や双極性障害)統合失調症、薬物乱用など、他のいくつかの併存精神疾患の発症を早める可能性がある。この範囲では、インフルエンザ、水痘・帯状疱疹、単純ヘルペス、ヒト免疫不全症、C型肝炎ウイルスなどのウイルス感染症は、うつ病および/または不安症のリスク増加と関連している[[198], [199], [200]]。重要なことに、最近の縦断的研究では、一般的なウイルス感染と精神障害のリスク増加とは関連していなかったが[201]、米国におけるうつ病症状の有病率は、COVID前からCOVID後にかけて3倍に増加しており[202]、他の国でも同様の観察がなされている[203], [204], [205], [206]。そして、この増加の正確なメカニズムは不明であるが、これらの患者は一般的にこれらの精神障害に対する標準的な薬理学的治療、すなわち抗うつ薬、抗精神病薬などを受けることになる。前述したように、これらの薬の副次的な効果は、過剰に活性化した炎症反応を抑制することであり、これは精神疾患の治療という点では良いかもしれないが、この作用はまた、SARS-CoV-2のようなウイルス感染症(新規感染、再感染を問わず)を防御する患者の自然な能力を低下させることにもなる。これらの薬剤はそれ自体は免疫抑制剤ではないが、感受性の高い患者には微妙ではあるが重大な影響を及ぼす可能性がある。このことは、特にCOVID-19に関連しており、SARS-CoV-2ウイルスは伝染性が高く、免疫系が低下している患者では特に病原性が高い。現在の世界的なSARS-CoV-2パンデミック、COVID-19と精神疾患 [207,208] との重要な関連性を念頭に置きながら、SARS-CoV-2によって誘発される炎症反応、ウイルスと精神疾患の経過、およびこの相互作用が向精神薬治療への反応をどのように調節しうるかについて簡単に検討する。
多くのウイルスは中枢神経系に侵入して影響を与えることができる[209]が、その主な理由はまだ完全には解明されていない。1つの作業仮説では、脳には免疫能のある細胞がなく、ウイルスにとって理想的な場所であり、いわゆるウイルスの貯蔵庫を形成していると推測されている[209]。あるいは、ヒト免疫不全ウイルス(HIV)のように神経細胞に感染することが知られていないウイルス感染は、HIV認知症(HIV D)(HIV関連神経認知障害(HAND)としても知られている)のような中枢神経系への影響を誘発する可能性がある。このメカニズムはまだ完全には解明されていないが、特定のHIVタンパク質(gp120およびTat)は中枢神経系に運ばれ、そこで神経細胞の機能障害および/または死を引き起こす細胞のアポトーシスメカニズムを誘発すると推定されている(レビューは[[210], [211], [212], [213]]を参照のこと)。
一般的に、精神科患者は、慢性的に自然免疫系が異常に制御されていること、認知機能や高度な運動機能の変化や障害、ときには個人的な衛生状態の低下など、無数の要因のために、すでにウイルス感染症に感染するリスクが高くなっている可能性がある[[214], [215], [216], [217]]。いずれにしても、免疫系の調節障害は病原性コロナウイルス感染症の重症度の中心である[[218], [219], [220]]。効果的な免疫応答は、ウイルス感染細胞を殺すための細胞傷害性T細胞の活性化に依存するため[20,220]、SARS-CoV-2(および他のウイルス感染者)の患者は、T細胞の数と機能を高めることが有益であろう。これを裏付けるように、SARS-CoV-2陽性患者は、総T細胞数、CD4およびCD8 T細胞の減少を示し、この減少は感染の重症度および年齢と強く関連しており、SARS-CoV-2患者における有意なT細胞の損失を示唆している[17]。
それでも、COVID-19は、誇張された免疫応答、すなわちSARS-CoV-2誘発性サイトカインストームと関連している。これらの患者では、このサイトカインストームはT細胞数と負の関係にあり、高血清サイトカイン濃度(感染期間中に発現する)がSARS-CoV-2感染の過程でT細胞の生存および増殖を負に制御していることを示唆している[17]。実際、T細胞の枯渇はSARS-CoV-2によって誘発されたサイトカインストームの結果であることが示唆されており、重症の感染者では細胞枯渇を示すマーカーが高くなることがわかっている[17]。これは、最初は全般的な改善を示しても、最終的には他の重篤な二次感染のリスクを高めることになる。興味深いことに、最近の研究では、生命を脅かす肺炎を発症したCOVID患者の10%(女性よりも男性の方が多い)に中和性免疫グロブリンG(IgG)自己抗体が存在することが明らかになった[221]。これらの自己抗体はタイプIFNを無効化または中和し、それによって炎症反応を阻害または低減して病原体による炎症を予防する。さらに、生命を脅かす肺炎患者の少なくとも3.5%は遺伝的IFN欠損を有しており[222]、このことは前述の結果と併せて解釈すると、中枢性炎症がCOVID-19の症状において重要な役割を果たしていることを浮き彫りにしている。このようなウイルス誘発性炎症の増加はCOVID-19の特徴ではない。同様の現象はHIV陽性患者において報告されており、これらの患者におけるうつ病の高い有病率の一因となっている[223,224]。このようなサイトカインストームの下流への影響は、先に言及したように、神経炎症の増加、神経可塑性およびモノアミン作動性神経伝達の低下、および神経細胞死の増加を含む可能性がある[223]。
いくつかの精神疾患がウイルス感染と関連しているが、特定のウイルスが原因因子として明確に確立されたことは今日までないが [198,[225], [226], [227]。熱性発作、意識消失、痙攣、運動失調、てんかん状態、脳炎、脊髄炎、神経炎および多発性硬化症を含む肺外症状がインフルエンザに感染した患者で観察されており、それによって神経学的合併症を引き起こすウイルスの能力が強調されている[228]。実際、強迫性障害(OCD)もまた、早期にインフルエンザや他の病原体に感染することと因果関係がある[229]。中枢神経系のウイルス感染に関しては、最近の研究により、統合失調症の神経発達に関与していると考えられるヒト内在性レトロウイルスW env(HERV-W env)が、免疫学的NO合成酵素(NOS)の発現を調節し、それによってNO産生とミクログリアの遊走を増加させることで、神経病理と疾患の進行に寄与している可能性があることが明らかにされた[230]。全体として、これらの神経生物学的変化は酸化ストレスの増加と関連しており、統合失調症に関連した陽性・陰性症状に典型的なモノアミンの変化の多くを促進している[232,233]。
ARDSは罹患率と死亡率が高く、介入が少ない重篤な疾患であり、SARS-CoV-2の致死的な肺症状も同様である。このレビューの焦点を考えると、ARDSの病因における交感神経ストレスの役割は、肺学的および神経心理学的観点から興味深いものである。α2-またはα2A-アドレナリン受容体(α2A-AR)の遮断は、ラットの炎症誘発性肺障害を減衰させる。Congらは最近、α2A-ARの遮断が活性化された肺胞マクロファージにおけるTNF-α、IL-6,およびIL-10産生を阻害することを指摘している[234]。さらに、彼らは NE が NF-κB 活性化をダウンレギュレーションすることを示しており、α2A-AR 欠損は肺組織中の NE 濃度を上昇させ、肺胞マクロファージの活性化を阻害することで肺損傷を改善することを示唆している。α2A-AR の気分調節や抗うつ作用[235]の役割を考えると、ミルタザピンのようなα2 調節薬は、SARS-CoV-2 感染者の ARDS と精神病理学の両方の治療にバイモーダルな作用を示す可能性があると考えられる。以前、精神医学と炎症におけるNO-cGMP経路の役割について述べたが、ホスホジエステラーゼ-5(PDE-5)阻害薬シルデナフィルは、脳組織および末梢レベルのcGMPを増強するため、ARDSにおける適切な介入として提案されていることは注目に値する[236]。さらに、前臨床試験では抗うつ作用が確認されており[237]、SARS-CoV-2に関連した精神病理学療法の補助的な治療選択肢として有用である。
効果的な抗ウイルス薬は、宿主細胞の感染を防ぐだけでなく、ウイルスによる過剰な免疫反応を抑制するか、少なくとも軽減する必要がある。特にSARS-CoV-2に関連して、いくつかの薬剤が研究されており、レムデシビルとクロロキン(およびヒドロキシクロロキン)が最も注目されている[238]。レムデシビルはウイルスの複製を選択的に阻害するのに対し、クロロキンはウイルスの侵入をブロックし、サイトカインの産生を減衰させると考えられている[238]。クロロキンには神経精神医学 [239] を含む重大な副作用があり、有効性の証拠がないため、SARS-CoV-2 の治療薬としてはまだ承認されていない。興味深いことに、世界保健機関(WHO)は最近、COVID-19入院患者に対するレムデシビルの使用について、意味のある有益性がないという理由で、使用を推奨していない[[240], [241], [242]のに対し、米国感染症協会(Infectious Diseases Society of America)は使用を支持している[[243,244]。これらの対照的な発言は、様々な科学者の反応を引きつけ、効果的な治療戦略の探索を再開させた[245]。それにもかかわらず、他の抗ウイルス薬は一般的にウイルスの複製のみを標的としており、付随する炎症には一次的または直接的な影響を及ぼさないため、精神症状の発現に大きな影響を及ぼすことはないはずである。この点では、ソフォスブビルをベースとしたC型肝炎治療薬は、キヌレニン増強作用を介して気分の改善と関連している[246]一方で、NEに影響を与える抗うつ薬は、C型肝炎治療薬であるIFN-αの抗ウイルス特性を低下させることが報告されており[247]、抗ウイルス薬と中枢神経系作用薬の間には、軽微ではあるが敏感な相互作用があることを示唆している。
我々は以前、向精神薬がどのように免疫応答を修飾しうるかを強調した。抗精神病薬は、ウイルス感染や細菌感染のリスクを高める可能性がある [248]。この点では、抗精神病薬の使用により肺炎のリスクが高くなることが観察されている[249]が、これは向精神薬による抗炎症作用が関与している可能性がある。この反応はまた、免疫調節薬(および他の抗ウイルス薬)の併用による免疫活性化作用によっても増強される可能性がある[247]。こうした懸念にもかかわらず、クロルプロマジン(および他の向精神薬)の抗SARS-CoV-2作用が示唆されている [250]。これらの可能性のある保護効果は、特定の向精神薬、特に三環系抗うつ薬、フェノチアジン系抗精神病薬、メチレンブルー、およびクロロカインなどの調査中の抗SARS-CoV-2薬の間の構造的類似性に基づいている。これらの化合物はすべて、イオン化可能なアミン官能基を含む親水性側鎖を有する疎水性芳香環または環系のカチオン性両親媒性薬物であり、宿主細胞の特性を変化させる可能性があり、ウイルスの侵入および複製を減少させる可能性がある[251]。注目すべきは、最近の臨床研究では、抗うつ薬であるフルボキサミン(SSRI)は、15日間の治療期間において、症候性COVID-19患者の臨床的悪化の可能性がプラセボ対照と比較して低いことが示されていることである[252]。今後の研究では、この有望な研究手段を調査すべきである。
逆に、抗ウイルス薬(例:エファビレンツ、マラビロク、オセルタミビルなど)は、気分障害や睡眠障害、幻覚などの中枢神経系に関連した副作用を引き起こすことが知られている[253]。SARS-CoV-2に関連して、クロロキンも同様の中枢神経系関連の副作用を引き起こすことが知られている[239]。これらの中枢神経系の副作用に関与する正確なメカニズムは不明であるが、直接的な(プログラムされた壊死、細胞溶解、および/またはアポトーシスおよび壊死を誘導することによる)神経可塑性の変化 [254] または間接的なメカニズム [257]、例えば、トール様受容体シグナル伝達受容体(TLR)3,7,および8の活性化などが考えられる。後者は、フリーラジカル産生および炎症の増加をもたらし、最終的には神経細胞の損傷をもたらす。最近のレビューでは、エファビレンツのような抗HIV薬の神経精神医学的副作用も取り上げられているが、これはミトコンドリア-免疫-炎症-レドックスカスケードの障害が関与しているとされている[258]。実際、ミトコンドリア機能障害は、酸化ストレスや神経炎症の増加、神経可塑性の低下、およびモノアミンシグナル伝達の障害を引き起こすことにより、多くの薬物誘発性毒性[259,260]や気分障害[261,262]の発症における基本的なメカニズムであると考えられている。
抗SARS-CoV-2と向精神薬との間の薬物動態学的相互作用も存在し、アジスロマイシンによるチトクローム阻害を含む[263]が、前述の向精神薬関連の副作用のリスクを増加させる可能性がある。最後に、抗レトロウイルス治療(ART)の開始に伴う免疫再構成炎症性症候群(IRIS)は、免疫系が回復し始めると過剰な炎症反応を介して不顕性の未治療感染症を悪化させたり、さらには未治療の感染症を悪化させたりする逆説的な現象である[264]。したがって、前述の抗ウイルス薬の中枢神経系への悪影響にもかかわらず、この逆説的な反応自体が、神経炎症を補うことで精神疾患の悪化に寄与している可能性がある。
以上のことから、ウイルス誘発性炎症と基礎となる神経炎症との間には敏感な相互作用が存在しており、敏感な個人においては悪化する効果がある可能性がある。さらに、ある種の抗ウイルス機序が神経炎症や精神症状の面で有益であるにもかかわらず、抗ウイルス剤と抗精神医学的な組み合わせによる拮抗的な純効果も存在する可能性がある。したがって、臨床成績を最適化するためには、補助的な治療戦略が治療上の価値を持つ可能性がある。
4. SARS-CoV-2感染時の向精神薬併用療法
SARS-CoV-2感染の封じ込めを強化するためには、また、いずれの疾患の転帰を悪化させるリスクをもたらさないような精神病理を治療するためには、前節で概説した知識が、新たな補助的治療法を考案し、試験するために必要とされるかもしれない。多数の薬剤がCOVID-19の治療オプションとして調査中であるが(Manhasら[265]によるレビュー)補助的治療オプションが有用であることが証明されうるので、さらなる調査が必要であるにもかかわらず、臨床的に利用可能なオプションを以下に簡単に論じておく。
アゴメラチン(5-HT2C拮抗作用を有するメラトニン(MT)1および2アゴニスト)は、ラットモデルにおいて血漿および脳内IL-1βおよびIL-6レベルを低下させ、微小グリア症およびアストログリア症を予防する [266,267]。臨床的には、12週間のアゴメラチン投与はCRPレベルの低下と関連している[268]。したがって、アゴメラチンは、その抗酸化性、抗炎症性および抗アポトーシス特性のために、COVID-19の治療において有益であることが証明され得る[269]。実際、高用量MTは、SARS-CoV-2誘発性肺炎の治療を受けた患者において、臨床的改善までの時間の短縮、および死亡率の低下の可能性さえあるという点で、有益な役割を果たす可能性がある[270]。その固有の抗不安薬および抗うつ薬の特性を考えると[[271], [272], [273]]、アゴメラチンは、COVID-19に関連する気分障害および不安障害において考慮すべき有用な薬であり得る。
抗酸化剤は、あらゆる意図と目的のために抗炎症剤を含むであろうが、細胞の酸化還元状態に応じて状態依存的な効果を有するようである。α-リポ酸は、SARS-CoV-2感染患者の全死亡率を低下させる可能性のある抗酸化物質である[276]。実際、リポ酸はRNAウイルス誘発性神経毒性[277]から保護し、HIVのウイルス複製を阻害することが示されている[278]。さらに、Dinizらによる最近のレビュー[279]では、天然の抗酸化物質、特にフラボノイドが従来の抗ウイルス療法に補助的な特性をもたらす可能性があることが強調されている。この報告書では、著者らは、観察された抗ウイルス特性に寄与するために、これらの天然抗酸化物質によって標的とされる特定のコロナウイルスタンパク質を同定している。これは、ウイルスのシグナル伝達を阻害し、最終的には複製能力を阻害する活性酸素の減少特性に加えてである。様々な植物種は、中枢神経系の神経伝達を変化させることが既に示されており[280]、抗COVIDに寄与する特性を有しているので、可能性を秘めているかもしれない(詳細なレビューは、Ahmadら[281]およびKhannaら[282]を参照のこと)。例えば、Sceletium tortuosum(カーナ)は、急性免疫課題に対する適切な免疫応答を阻害することなく、穏やかな抗炎症特性を有し[283]、またHIV酵素およびプロテアーゼを阻害することにより抗レトロウイルス効果を発揮することから、関心を持たれているかもしれない[284]。マンゴスチン果皮抽出物は、げっ歯類モデルにおいて抗うつ作用や認知機能を有することが実証されており、ハロペリドールの抗精神病作用を増強することが示されている[285]。興味深いことに、この抽出物の構成成分であるガンママンゴスチンは、C19MP(SARS-CoV-2の主要プロテアーゼ)を阻害し、ロピナビルやリトナビルなどの他の既知の阻害剤と比較して、結合親和性が改善されている[287]。同様に、ニゲラ・サティバ[288]の成分であるチモキノンは、プロ炎症性サイトカインのダウンレギュレーションに寄与する強力な抗酸化特性で最もよく知られており、MODSを回避するための可能性のある候補となっている(Ahmadらによるレビュー[289])。SARS-CoV-2に関しては、チモキノンは、ヒートショックプロテインの細胞表面を調節することにより、ACE2受容体へのウイルスの結合を防ぐことができる[290]。ARDSの重症患者では、ω-3 PUFAを含む経腸食は酸素化を改善し、機械換気と集中治療の滞在時間を短縮した[291]。しかし、マウスへの魚油摂取はインフルエンザに対する免疫反応を変化させ[292]、ウイルスクリアランスを遅らせることが示されているので注意が必要である[293]。もう一つの注目すべき抗酸化物質はメラトニンで、COVID-19患者の心筋損傷や呼吸器合併症の患者に効果があることが示唆されている[294]。抗COVID-19補助療法[270]として以前に述べた(アゴメラチンを参照)その役割を考慮すると、メラトニンはさらなる調査を必要とする強力な候補である。 同様に、オキシトシン-バソプレシンは酸化還元系[177]に作用するが、その微妙なバランスは不安障害[175]に関与している。この点で、オキシトシンはCOVID-19感染症のアジュバント治療薬としての可能性があることが指摘されている[295]。
α2 ARアンタゴニストであるクロニジンは、ウイルスの複製を阻害することでインフルエンザ誘発性肺障害から保護しうる新規な試験管内試験抗インフルエンザ薬として同定されている[296]。クロニジンは、注意欠陥多動性障害[298]だけでなく、統合失調症の患者[297]で示されたように、精神病や不安を治療する可能性があるため、SARS-CoV-2に関連した精神症状の発症の治療にも有益であるかもしれない。
COX-2阻害剤。SARS-CoVのヌクレオカプシドタンパク質がCOX-2発現を活性化すること[299]から、Tomeraら[300]は、COX-2阻害剤であるセレコキシブによるSARS-CoV-2ヌクレオカプシドNタンパク質N2配列の保存が、感染細胞におけるCOX-2発現の直接的なウイルストランザクティベーションの影響を緩和する可能性があることを示唆している。さらに、セレコキシブは、インフルエンザAに感染したマウスにおいて、コントロールと比較してTNF-αおよびIL-6サイトカインレベルを有意に減少させることが示されており[301]、ウイルス感染におけるCOX-2阻害剤の抗炎症的役割をさらに強調している。セレコキシブはまた、補助的な治療法として、SARS-CoV-2感染患者の臨床的改善に寄与する可能性のある有益な気分上昇効果も有している[78]。
デキサメタゾンは高活性のグルココルチコイドである。RECOVERY Collaborative Groupによる予備報告 [302] では、デキサメタゾンの使用により、侵襲的機械換気または酸素療法のみを受けた入院中のSARS-CoV-2患者では28日死亡率が低下したが、呼吸支援を受けていない患者では低下しなかったことが示されている。同様に、標準治療に加えてデキサメタゾンを静脈内投与すると、SARS-CoV-2 患者の無呼吸日数が統計学的に有意に増加した [303]。しかし、デキサメタゾンによる治療はラット[304]およびマウス[305]において抑うつ行動を悪化させ、COVID-19に関連する精神疾患の有病率を考慮すると、これらの患者では問題となる可能性がある。前述の前臨床研究に基づき、デキサメタゾンは酸化ストレス、炎症を増加させ、グルタミン酸神経伝達の異常を誘発することにより、基礎となる精神疾患を悪化させる可能性がある[[306], [307], [308]]。
リチウム塩は抗うつ/抗躁/気分安定化作用を有し、また炎症促進作用を有する[309]。後者は、HIVや全身性エリテマトーデス(SLE)などの免疫学的欠損に関連するいくつかの障害において有益であるようである[310,311]。この点、リチウムは炎症性メディエーターに対して多様な作用を示し、例えば、IκB-α、TRAF3,Tollip、NF-κB1/p50 を含むいくつかの炎症性遺伝子の発現を調節する一方で、LPS 活性化マクロファージにおける NF-κB の核転座を低下させることで NF-κB 活性を阻害する[312]。また、動物実験では、リチウムがNO-cGMP経路の活性を低下させる[313]か、または増加させることが示されている[314,315]。最近、Pietruczukら[167]は、リチウムまたはバルプロ酸で治療された双極性障害患者のTリンパ球が、プロ炎症活性、増殖活性の低下、アポトーシスに対する感受性の増加を特徴としていることを示した。最後に、Spuchらによる症例報告[316]では、重症SARS-CoV-2感染症患者において、炭酸リチウムが炎症活性および免疫応答を改善したことが示されている。
テトラサイクリンの一種であるミノサイクリンは、抗炎症性、免疫調節性、神経保護性を有するタンパク質合成阻害抗菌薬である[317]。ミノサイクリンは、アジスロマイシンに関連したQT延長および心筋梗塞のリスクを軽減する可能性があるため、アジスロマイシンの好ましい代替薬である可能性がある[318]。実際、ミノサイクリンは呼吸器性合胞体ウイルス感染を予防し[319]、細胞環境を変化させることでHIVの複製と再活性化を減少させることが示された[320]。ミノサイクリンはまた、アジスロマイシンの薬物間相互作用の傾向があるため、アジスロマイシンの代替薬となる可能性もある[318]。
ミトコンドリア若返り剤および調節剤。疎水性芳香環または環系、特にメチレンブルーのようなイオン化可能なアミン官能基を含む親水性側鎖を有するカチオン性両親媒性薬物は、ミトコンドリア若返り作用を有しており[147]、これには、マイトファジーの増強[321]、細胞酸素消費量の増加、ミトコンドリア機能不全の遅延[322]などが含まれる。
N-アセチルシステイン(NAC)もまた、強力な抗酸化特性と同様にミトコンドリア機能に有益な効果を持つ[323]。Alamdariらによる症例報告[324]では、SARS-CoV-2患者をメチレンブルー、ビタミンCおよびNACの組み合わせで治療すると、抗炎症作用および抗酸化作用のためか、これらの患者の生存率が向上することが示されている。実際、メチレンブルーはインフルエンザを含む様々なRNAウイルスを不活化するのに有効である[325]。メチレンブルー[147]およびNAC[326]は、有益な気分上昇作用を有することが提案されている。ミトコンドリア調節薬は、最適なミトコンドリア機能(およびその結果として生じる酸化ストレスの減少)が免疫応答において果たす役割のため、抗SARS-CoV-2増強戦略となる可能性がある。ミトコンドリアには、その膜にミトコンドリア抗ウイルスシグナル(MAVS)タンパク質が含まれており、抗炎症反応を調節することで抗ウイルス防御機構に貢献することができる。メラトニンは、そのミトコンドリア増強作用により、最近、抗SARS-CoV-2のアジュバント薬として提案されている[329]。したがって、ミトコンドリア調節因子は、抗ウイルス効果を誘導するための新たな薬物標的を提示する可能性がある[330]。
NF-ĸB阻害剤またはアンタゴニスト。抗ウイルス性病原体によるNF-ĸBの活性化は、アポトーシスに寄与し、炎症を増強する可能性がある(Ludwig & Olivierによるレビュー[331])。NF-ĸB経路の不活性化は、インフルエンザAウイルスの複製を阻害することが示された[332]。ジギタリスアルカロイドであるジゴキシンおよびオウアバインはNF-ĸBアンタゴニストとして認識されている[333]。Choら[334]は、両化合物がSARS-CoV-2複製の99%以上を阻害し、ウイルスのライフサイクルの侵入後の段階でのウイルス阻害につながることを報告した。しかしながら、内因性のオウアバイン様化合物の産生の病理学的増加は、気分障害の病態生理において役割を果たすことが示された(Christo & El-Malakh[335]によるレビュー)。したがって、これらの患者は、これらの化合物によって誘発される可能性のある精神医学的副作用をモニタリングする必要がある。
ホスホジエステラーゼ阻害剤。選択的PDE-4阻害剤(イブディラスト、ロリプラムなど)は、グリアへの作用、特に上流のプロ炎症性分子の阻害およびプロ炎症性/抗炎症性バランスの調節を通じて、SARS-CoV-2のサイトカインストームを減衰させる可能性がある[336]。PDE-5阻害薬(シルデナフィルやタダラフィルなど)は、Ang-IIを介したAT-1受容体のダウンレギュレーションに対抗し、プロ炎症性サイトカインを減少させることで、SARS-CoV-2の補助的な治療薬として有用であると考えられる[337]。実際、シルデナフィルはHIV感染者における致命的なHIV関連肺高血圧症の治療に有望であると考えられる[338]。さらに、これらの薬物は前臨床試験で抗不安作用および気分を高揚させる特性を示している[172,237,339]。
ピオグリタゾンはペルオキシソーム増殖活性化受容体(PPAR)-γアゴニストであり、高病原性でパンデミックなインフルエンザウイルス株に感染したマウスにおいて保護を提供することが示されている[340]。その結果、Carboniら[341]は、ピオグリタゾンが、少なくともメタボリックシンドロームの症状を示す患者において、SARS-CoV-2に関連したサイトカインストームを減少させるために使用される可能性があると仮説を立てた。
mTOR阻害剤であるラパマイシンは、マラビロコ耐性株のHIVに特異的に使用されるアプラビロコおよびビクリビロコの抗ウイルス作用を増強する可能性がある[342,343]。mTOR経路は、細胞傷害、酸化ストレス、ミトコンドリア機能不全、およびCOVID-19に関連する重要な障害である高炎症の発症を制御するための貴重な標的を提供する可能性がある[344]。mTOR経路はまた、抗うつ作用において重要なメッセンジャーであり、ケタミンやラパスチンの迅速な抗うつ作用の標的として認識されており[345,346]、COVID-19に関連した気分障害に関連している可能性がある。
選択的セロトニン標的抗うつ薬。SSRIは最近、COVID-19の治療における補助的な有用性について研究されている。これに関して、フルオキセチンはSARS-CoV-2ウイルスの発現を減少させるのに有効であった[347]一方で、SSRIの治療はSARS-CoV-2感染症の入院患者における死亡または挿管のリスクを低下させることに関連するものもあった[252,348]。有益な効果は、一部ではSSRIの抗炎症作用に起因していると考えられる [145,146,349]。実際、フルオキセチンおよびシタロプラムは、細菌またはウイルス病原体が関連する分子パターン認識受容体の一群であるエンドソームTLRを阻害することにより抗炎症特性を示すことが示されており、この受容体は細菌またはウイルス病原体が関連する分子パターンを認識し、炎症性サイトカインを抑制するための自然免疫応答において重要な役割を果たしている[350]。
アロプリノールなどのトリプトファン-キヌレニン調節薬は、キサンチンオキシダーゼと同様にトリプトファン2,3-ジオキシゲナーゼ(TDO)を阻害し、それによってキヌレニンの形成と5-HT合成のためのトリプトファンの枯渇を調節する。トリプトファン-キヌレニン経路は、炎症誘発性精神病理学において重要な媒介的役割を果たしている [98]。初期の報告では、化学的に修飾されたスーパーオキシドジスムターゼ(O2のスカベンジャー)との組み合わせでアロプリノールを投与すると、インフルエンザウイルス感染マウスの生存率が改善することが示唆されている[351]。
5. SARS-CoV-2パンデミックへの示唆とリスク評価
簡単に言えば、リスクを特定し、リスクにさらされている患者を特定し、リスク管理戦略を示す必要がある(図1参照)。
以上の検討から、SARS-CoV-2は、精神的外傷、神経炎症、免疫系の機能不全を引き起こし、最終的には神経系に影響を及ぼす可能性があることが明らかになった。精神疾患は、疾患修飾因子に対する個人の脆弱性を増大させる。向精神薬の酸化還元炎症作用を考慮すると、SARS-CoV-2の併発感染とその治療により、患者の向精神薬に対する反応が変化し、SARS-CoV-2の疾患、精神疾患、向精神薬の反応の三要素の相互作用が生じる可能性がある。複数の併存疾患を持つ患者や、複数の薬物治療が処方される患者を扱う場合には、状況はより複雑になる。したがって、関連するリスクの可能性と潜在的な大きさを予測し、評価できることが重要になる。
最後に、精神疾患を併存するSARS-CoV-2患者の臨床反応を注意深く観察し、可能であれば炎症および免疫反応の適切なバイオマーカーを測定することにより、リスクを管理することができる。免疫炎症の広範で非特異的なマーカーとしては、CRP、赤血球沈降速度(ESR)血漿粘度、免疫応答のマーカーとしてのプロカルシトニンなどがある[352]。これらは、炎症が亢進してリスクが上昇していることを示す指標として、おそらく最も実用的に実施できるものである。さらに、サイトカインストームの前駆体として、フィブリノゲン、P-セレクチン、D-ダイマー、SARS-CoV-2の進行と炎症に関連していると考えられるフォン・ウィレブランド因子などの血行動態のバイオマーカーも有用であろう[353,354]。コルチゾールおよび副腎皮質刺激ホルモン(ACTH)の上昇は、生物学的ストレスのマーカーであるだけでなく、精神疾患にも関連している[82]。他の実験的でより特異的なバイオマーカーは、臨床的で資源が限られた環境で測定するのが必ずしも現実的ではないかもしれないが、CD4 + T細胞、CD14+、CD16+、炎症性単球、IL-2,IL-7,IL-10,顆粒球コロニー刺激因子(G-脳脊髄液)IP-10,MCP-1,マクロファージ炎症性タンパク質1α(MIP-1α)TNF、およびSタンパク質が含まれる。V483A、L455I、F456 V、G476S [355]。最近では、ACE-2受容体がSAB-CoV-2の潜在的な結合ドメインであることが示唆されている[356]。この点では、ACE-2とドーパ脱炭酸酵素の発現との関連性も提案されており、ドーパ脱炭酸酵素はDAと5-HTの合成に関与している。DAと5-HTの両方のレベルは、いくつかの精神疾患と密接に関連しており、将来的にはSARS-CoV-2の精神合併症の重要なバイオマーカーとなる可能性がある。
モニタリングと臨床反応は、臨床家に反応を記録し、治療を調整し、モニタリングを継続することを促すものである。最終的には、所見を報告することで、より広範な医療コミュニティが学び、治療を強化し、治療成績を最適化することができるようにすべきである。
6. 結語
現在のSARS-CoV-2パンデミックは 2002年~2003年のSARS-CoV 2012年のMERSに続いて、過去20年間で3回目の深刻なコロナウイルスのアウトブレイクである。SARS-CoV-2とそれ以前のSARS-CoV感染症はいずれも、プロ炎症性サイトカインおよびケモカイン(サイトカインストーム)の上昇に関連しているが、MERS-CoVの病原性はインターフェロン(IFN)アンタゴニストタンパク質に基づくものである。進行中の研究は、多くの精神疾患が炎症によって特徴づけられることを示しており、その治療法は可変的な抗炎症特性を有する。SARS-CoV-2の深遠な心理社会的影響は、患者がこれらの障害に対して標準的な抗うつ薬や抗精神病薬を投与されることを意味する。これらの薬剤は、精神疾患がもたらす免疫状態の悪化と相まって、SARS-CoV-2の感染や再感染を撃退するための患者の自然な能力を低下させる可能性がある。このレビューでは、上記の要素をまとめ、この新たなパンデミックの展開に伴って臨床医が遭遇するであろう理論的なリスクと明白なリスクの両方を考慮すると同時に、予防的な治療戦略の可能性を提示している。また、本論文では、SARS-CoV-2に関連する神経精神合併症に対する補助的治療として、既存の治療法や新規の治療法を検討することで、研究の新たな機会を開くことを試みている。
