Reversal of Cognitive Decline: 100 Patients
Dale E Bredesen1*, Kenneth Sharlin2
, David Jenkins3
, Miki Okuno3
, Wes Youngberg4
, Sharon Hausman Cohen5
, Anne Stefani5
, Ronald
L Brown6
, Seth Conger6
, Craig Tanio7
, Ann Hathaway8
, Mikhail Kogan9
, David Hagedorn10, Edwin Amos11, Amylee Amos12, Nathaniel
Bergman13, Carol Diamond14, Jean Lawrence15, Ilene Naomi Rusk16, Patricia Henry16 and Mary Braud16
要旨
アルツハイマー病やアルツハイマー病以前の状態であるMCI(Mild Cognitive Impairment)とSCI(Subjective Cognitive Impairment)の認知機能低下が逆転した最初の例が最近発表された。これら2つの論文では、認知機能の低下の原因となる可能性のある因子(病原体や腸管透過性による自然免疫系の活性化、栄養やホルモンの減少、特定の毒素への暴露、その他の因子など)を特定し、コンピュータベースのアルゴリズムを用いてサブタイプを決定し、認知機能低下の反転のためのReCODEと呼ばれる個別化された標的化された多因子アプローチを用いて各因子に対処する包括的な精密医学的アプローチを用いて、持続的な主観的および客観的な認知機能の改善を示した19人の患者について報告されている。
初期研究の明らかな批判は、報告された患者数が少ないことである。そこで我々は、複数の異なる医師によって治療された100人の患者を報告している。この追加報告は、このプロトコルと全体的なアプローチの無作為化対照臨床試験のさらなる支持を提供するものである。
キーワード
アルツハイマー病; 軽度認知障害; プログラムマティクス; ReCODE; 精密医療; アミロイド前駆体蛋白質; シナプトクラスティック; シナプトクラスティック
はじめに
アルツハイマー病は現在、米国における死因の第3位であり[1-6]、効果的な治療法と予防法の開発は医療の主要な目標である。しかし、アルツハイマー病治療薬候補の臨床試験は、ほぼ一律に不成功に終わっている。このような失敗の繰り返しにはいくつかの理由が考えられる。
(2) アルツハイマー病と呼ばれるものは単一の疾患ではなく、複数のサブタイプが存在すること [3、4] (3) 心血管疾患のような他の複雑な慢性疾患と同様に、アルツハイマー病にも炎症、様々な慢性病原体、栄養失調、インスリン抵抗性、血管障害、外傷、特定の毒素への曝露など、多くの潜在的な要因が存在している可能性がある。
したがって、単剤治療の単相的なアプローチは最適ではなく、各個人の遺伝学および生化学に基づく個別化された多相的なプログラムの方が好ましいかもしれない。実際、このような個別化されたプログラムは、将来の医薬品候補の臨床試験において有利に働く可能性がある。
(4) 薬物標的(例えば、アミロイドβペプチド)をベースにしたアルツハイマー病のモデルは、不正確であったり、不完全であったりする可能性がある。
我々は、アルツハイマー病の認知機能低下の逆転について、根本的に異なる見解を主張してきた。アミロイド前駆体タンパク質であるAPPが統合依存性受容体としての活性により分子スイッチとして機能する疾患[1、2、5、7]である[8-10]。トロフィックシグナルからの十分な支持の存在下では、APPはα部位で切断され、2つのシナプス可塑性ペプチド、sAPPαとαCTFの産生につながる。
対照的に、栄養シグナルからの十分な支持がない場合、APPはβ、γ、カスパーゼ部位で切断され、sAPPβ、Aβ、Jcasp、およびC31の4つのシナプス可塑性ペプチドの産生につながる。このモデルでは、炎症は、NF-κB(B細胞の核因子κ-軽鎖エンハンサー)によるBACE(β-アミロイド切断酵素)誘導およびγ-セクレターゼ活性を介して、少なくとも部分的にはAPPシグナル伝達に対して抗萎縮効果を発揮する。
同様に、二価金属(水銀など)のような毒素もまた、これらが毒素結合ペプチドAβの純増産につながるため、APPシグナル伝達に抗萎縮効果を発揮する。
このモデルは、Aβペプチドが抗菌ペプチドとして機能するという知見と互換性があり[11]、一緒にアルツハイマー病と呼ばれるものは、いくつかのクラスの侮辱に対する保護的、ネットワークのダウンサイジング反応であることを示唆している:病原体/炎症、毒素、および栄養素、ホルモン、または栄養因子の撤退[5]。
このモデルは、アルツハイマー病を発症する確率がシナプス細胞性シグナルとシナプス細胞性シグナルの比率に比例することを示唆している[5]。この考え方は、シナプス芽細胞性シグナルとシナプス細胞破砕性シグナルへの数十の寄与因子を患者ごとに測定し、各寄与因子を標的とするために個別化されたプログラムを生成し、それによってシナプス芽細胞性シグナルを増加させ、同定されたシナプス細胞破砕性シグナルを減少させる治療レジメンにつながっている。
いくつかの例が含まれる。(1) ボレリア、バベシア、またはヘルペスファミリーウイルスなどの病原体を特定して治療すること;(2) 消化管過疎性を特定して、腸を修復して、マイクロバイオームを強化すること;(3) インスリン抵抗性およびタンパク質の糖化を特定して、インスリン感受性を戻して、タンパク質の糖化を減少させること;などが挙げられる。
(4)最適でない栄養、ホルモン、または栄養支持(血管支持を含む)の特定と修正、(5)毒素(メタロトキシンなどの無機物、有機毒素、またはバイオトキシン)の特定、毒素曝露の低減、解毒。患者はそれぞれ、認知機能の低下に寄与する多くの潜在的な因子の組み合わせが異なるため、治療へのアプローチは標的を絞った個別化されたものとなる。
ここでは、このマルチコンポーネント、精密医学的アプローチで治療され、文書化された改善を示している認知機能の低下を持つ100人の患者を説明する。
ケーススタディ
患者1
68歳の専門職の女性は、聞き手に混乱をもたらすほど重度の擬態語の誤りを指摘するようになった。彼女はうつ病も発症しており、抗うつ薬で治療を受けてた。彼女は、買い物、料理、パソコンでの作業などの日常的な仕事に困難を抱え始めた。彼女は孫娘と一緒にジンジャーブレッドマンを完成させるのに苦労した。
彼女は時計の分針と時針を混同していた。彼女はスペルに難があった。症状が進行し、日常の作業を忘れるようになった。孫を学校に迎えに行くのを2週間に2回も忘れたことがあり、とても心配になったそうである。
アポリポ蛋白E(ApoE 3/4)のε4対立遺伝子のヘテロ接合体であることが判明した。アミロイドPETスキャン(フロルベタピル)が陽性であった。MRIでは年齢の割に14%の海馬体積を示した。
高感度C反応性蛋白(hs-CRP)は1.1mg/L,空腹時インスリンは5.6mIU/L,ヘモグロビンA1cは5.5%,ホモシステインは8.4マイクロモル,ビタミンB12は471pg/mL,遊離トリヨードサイロニン(遊離T3)は2.57pg/mL,甲状腺刺激ホルモン(TSH)は0.21mIU/L,アルブミンは0.21mIU/L,アルブミンは1.5mIU/Lであった。
21mIU/L、アルブミン3.7g/dL、グロブリン2.7g/dL、総コレステロール130mg/dL、トリグリセリド29mg/dL、血清亜鉛49mcg/dL、補体因子4a(C4a)7990ng/mL、トランスフォーミング成長因子β1(TGF-β1)4460pg/ml、マトリックスメタロプロテアーゼ9 497ng/mL。
軽度認知障害(MCI)と診断され、抗アミロイド抗体の治験が行われた。しかし,抗アミロイド抗体を投与するたびに3~5日間認知機能が低下し,その後,以前のMCIの状態に戻った。最初の4回の治療で悪化した後、彼女は研究への参加を中止した。彼女は先に述べたプログラム的アプローチで治療を開始した [1]。彼女のMoCAは17ヵ月間で24から30に増加し、18ヵ月間は安定したままであった。
海馬体積は14%から28%に増加した。彼女の症状は著しく改善した:スペル能力の回復、言語能力の改善、買い物、料理、コンピュータでの作業能力のすべてが改善し、追跡調査では安定した状態を維持している。
患者2
73歳の女性医師は、20年近く前から記憶力の低下と単語の検索問題を抱えてたが、過去1年間で加速し、彼女の大切な人は彼女の記憶力を “悲惨なもの “と表現していた。彼女は最近の会話、彼女が見た演劇、または彼女が読んでいた本を覚えていないことができ、人やペットの名前を混同していた。彼女はトラブルをナビゲートしていた、トイレを使用した後、彼女のレストランのテーブルに戻って彼女の方法を見つけることさえ困難。
FDG-PET(Fluorodeoxyglucose-Positron Emission Tomography)スキャンでは,グルコース利用率の低下が両側の前上部前帯と左側頭葉に認められた。MRIでは軽度の二頭身萎縮が認められ、海馬体積の減少が認められた(年齢の16%)。オンライン認知検査では年齢の割に9%であった。
ApoE遺伝子型は3/3,空腹時グルコース90mg/dL,ヘモグロビンA1c 5.3%,空腹時インスリン1.6mIU/L,ホモシステイン14.1マイクロモル,TSH 4.1mIU/mL,遊離T3 2. 6 pg/mL、逆T3 22.6 ng/dL、ビタミンB12 202 pg/mL、ビタミンD 27.4 ng/mL、総コレステロール226 mg/dL、LDL 121 mg/dL、HDL 92 mg/dL、水銀 7 ng/mLであった。
彼女は先に述べたプログラム的アプローチ [1] で治療を受け、12ヵ月間でオンライン認知評価が9%から97%に改善した。
彼女の重要人物は、彼女の記憶力が “悲惨なもの “から “ただのお粗末なもの “に改善され、最終的には “普通のもの “になったことを指摘している。彼女は現在も治療プログラムを継続しており,その改善は持続している.
患者3
62歳の女性は,認知機能の低下,疲労,睡眠不足,抑うつ状態を呈していた。名前を覚えたり、以前に行っていた会計をしたり、ビジネスをしたりする能力を失っていた。体格指数は24、腹部脂肪が増加していた。
MoCAは20であった。ApoE4ヘテロ接合体(3/4)であった。空腹時血清グルコース101mg/dL、ヘモグロビンA1c 6.1%、空腹時インスリン14mIU/L、hs-CRP 1.7mg/L、25-ヒドロキシカルシフェロール24ng/mL、TSH 2.4mIU/L、遊離T3 2.9pg/mL、逆T3 19ng/dL、エストラジオール<6pg/mL、およびプレグネノロン38ng/dLであった。
病原体検査では、ボレリア、他のマダニ媒介感染症、ヘルペスファミリーウイルスは陰性であった。毒素検査では水銀や鉛の毒性は認められなかった。
彼女は以前に記載された個人化されたプログラム[1]で治療されたが、これは彼女の場合、生体同一ホルモンの補充、軽度のケト原性、植物性の食事、定期的な運動、およびストレスの軽減によるインスリン感受性の回復、プロバイオティクスおよびプレバイオティクスによる彼女のマイクロバイオームの強化、オメガ3脂肪による全身の炎症の軽減、ビタミンDおよびビタミンK2の強化、メチル-コバラミンおよびメチル-テトラヒドロ葉酸によるメチル化の強化、および脳のトレーニングを含んでいた。
次の12ヶ月間に彼女は代謝状態を改善した:BMIは21.8、空腹時グルコース87 mg/dL、ヘモグロビンA1c 5.2%、空腹時インスリン5.5 mIU/L、hs-CRP 0.5 mg/L、遊離T3 3.2 pg/mL、TSH 2.1 mIU/L、エストラジオール51 pg/mLにまで低下した。
症状は改善し、営業を再開し、フォローアップのMoCAスコアは20から28に上昇していた。彼女の改善は持続している。
表1
アルツハイマー病、アルツハイマー病以前の状態MCI(Mild Cognitive Impairment)またはSCI(Subjective Cognitive Impairment)による認知機能低下、または確定診断を伴わない認知機能低下を有する100人の患者をリストアップしており、その全員が上記の3人の患者に使用されたのと同じ標的化されたマルチコンポーネントプログラムを使用して文書化された改善を示した。
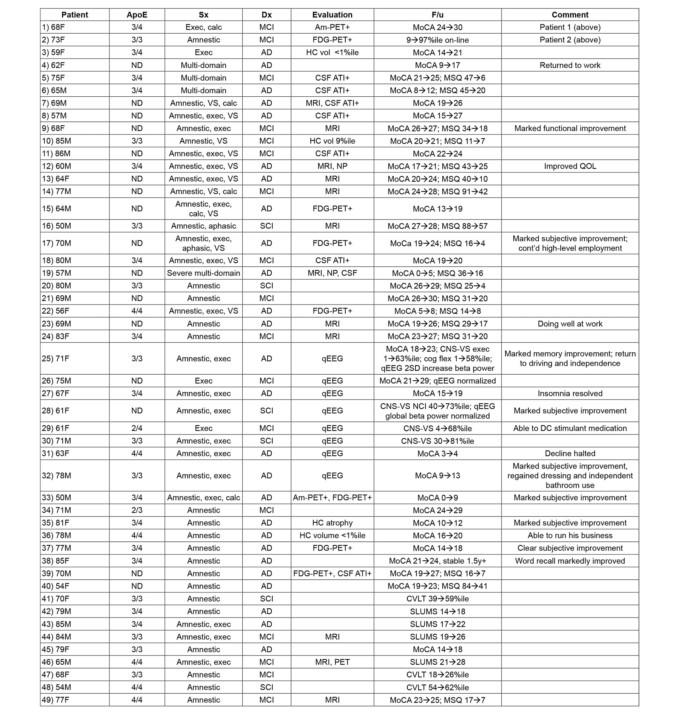
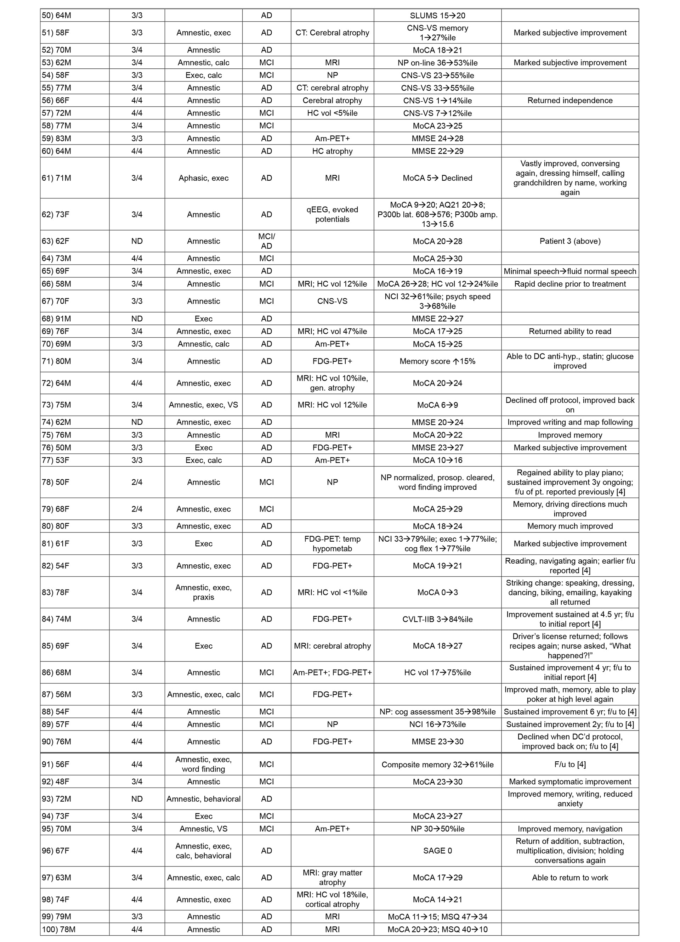
原文参照
考察
アルツハイマー病は大きな医療問題であり、効果的な治療法や予防法の開発ができなければ、国や世界的に悲惨な結果を招くことになり、メディケアの破綻も考えられる。したがって、効果的な治療法の開発は、トランスレーショナルバイオメディシンと公衆衛生プログラムの世界的な優先度が高い。
しかし、神経変性疾患の領域は、アルツハイマー病からパーキンソン病、レビー小体型疾患、筋萎縮性側索硬化症、前頭側頭型認知症、進行性核上麻痺、黄斑変性症などの神経変性疾患に至るまで、生物医学的に最も大きな治療失敗の領域であり、持続的な疾患修飾効果のある有効な治療法が存在しないことは間違いない。
このような一様な不成功の理由はいくつか考えられるが、患者ごとに原因や寄与因子を特定せずに治療を試みたことが一つの理由であると考えられる。単一の原因を仮定すること、単剤療法で治療しようとすること、一様で単相的な治療法で治療しようとすること、すべてが、以前の最適でない、効果のないアプローチに寄与している可能性がある。
さらに、根本原因(例えば、病原体、毒素、およびインスリン抵抗性)ではなく、メディエーター(例えば、Aβペプチド)を標的とすることが、これまで成功しなかったもう一つの理由であるかもしれない。
ここで私たちは、患者ごとに認知機能低下の多くの潜在的な要因を評価し、それに対処するという、まったく異なるアプローチをとってきた。これにより、前例のない認知機能の改善が得られた。
最も重要なことは、プロトコルを中止しない限り、改善は一般的に持続し、2012年に治療を受けた最初の患者でさえ、持続的な改善を示していることである。この効果は、病態生理に影響を与えない単剤治療でその過程を回避するのではなく、変性過程の根本原因が標的とされ、その結果、その過程自体に影響を与えていることを示唆している。
したがって、本プロトコルの持続的な効果は、単剤治療に比べて大きな優位性を示している。今回の研究では、以前に報告された19例の患者 [1、2] の結果を拡張したものであり、ここでは認知機能の低下と改善が認められた100例の患者について報告している。
これらの患者のほとんどはアルツハイマー病または前アルツハイマー病、MCIまたはSCIであることが示された;残りの患者はアルツハイマー病を持っているかもしれないし、持っていないかもしれないが、これらのケースでの評価はアルツハイマー病の決定的な証拠を提供していないので、また、他の特定の変性状態の決定的な証拠を提供していない。
改善した患者の中には、炎症性、萎縮性、糖毒性(インスリン抵抗性)、毒性の各サブタイプ[3、5]を示唆するものも含まれており、この一般的なアプローチの有効性は、アルツハイマー病の単一のサブタイプに制限されていないことを示唆している。
ここで発表された結果は、複数の施設で複数の医師によって得られたものであり、このアプローチは多くの医師にとってスケーラブルで実践可能なものであることを示唆している。また、これらの結果は、無作為化された対照前向き臨床試験をサポートする背景となるはずである。しかし、このような臨床試験の承認を得ることは難しいかもしれない。
さらに、治療反応が線形系として作用する可能性は非常に低く、したがって、プログラム全体の効果が各構成要素の効果の総和と等しくなる可能性は低く、プロトコルの構成要素の解剖は困難である。
しかし、単一の構成要素を系統的に削除する、またはいくつかの構成要素によって異なる多数のプログラム効果を比較するなどの代替的なアプローチは、最も重要な構成要素と最も重要でない構成要素についてのある程度の洞察を提供するかもしれない(もちろん、これらは患者によって異なるかもしれないが)。
100人の患者の現在のセットでは、治療前後(100人中72人)にMoCA、MMSE、またはSLUMSで評価された患者では、平均4.9ポイントの改善があり、標準偏差は2.6、範囲は1-12であった。
自然の歴史は衰退の一つであるので、文書化された改善は、そうでなければ発生していたであろう衰退の予防に加えて考慮されなければならない。もちろん、これらの数値は失敗があった場合には緩和されなければならないので、ランダム化された対照臨床試験の文脈でこれらを見直すことが重要になる。
ここで使用されるプロトコルの利点の一つは、それが強化される可能性があることである。医薬品検査と臨床試験:改善が見られないことを考えると、これまでの大多数の単剤治療試験では、フロア効果、すなわち改善を測定するために必要なしきい値効果があることが問題となる可能性がある。
しかしながら、ここで述べられている陽性効果は、多くの場合、患者を動的な範囲に置くことが考えられ、陽性と陰性の両方のより小さな効果が検出可能であるかもしれない。
より多くの患者がこのアプローチで治療を受ければ、改善のパターンと改善しないパターン、改善のタイミング、どの領域が典型的に改善し、どの領域が改善しないのか、そして関連する知見が得られるであろう。
ここで報告された症例の焦点ではないが、ある種の観察が繰り返し行われた。その一つは、患者の重要な他者が、患者が治療により「より関与している」「より反応している」と典型的に報告していることであった。
顔認識、ナビゲーション、記憶はしばしば改善されたが、計算と失語症は改善されることは少なかった。特定の病原体や毒素が同定された患者では、それらが治療的に標的とされるまで改善がみられなかったか、あるいは標的とされたときにさらなる改善がみられた。
驚くべきことではないが、治療開始時にあまり衰えを示さなかった患者は、病気の経過に沿ってさらに進んだ患者に比べて、より容易に完全に反応した。しかし、MoCAスコアが0という低値であっても改善した例があった。
まとめると、各患者の認知機能低下の原因となる複数の潜在的な要因に対処する標的化された個別化された精密医学的アプローチは、アルツハイマー病やその前兆であるMCIやSCIの治療に有望であることが示されている。
ここに報告された100名の患者の改善は、特にこの一般的で末期的な病気に対する有効な治療法がない現状を考えると、プロスペクティブな無作為化比較臨床試験の実施を支持するものである。