Contents
Replicon mRNA Vaccine: Japan Approves World’s First Self-Amplifying mRNA Vaccine
makismd.substack.com/p/replicon-mrna-vaccine-sa-mrna-japan
グローバルリサーチ、2024年01月03日
自己増幅型mRNAワクチン
2023年11月27日 – CSLとアークトゥルス・セラピューティクスのARCT-154、成人のCOVIDを適応症とする初の自己増幅型mRNAワクチンを厚生労働省が承認
- 「世界初の自己増幅型メッセンジャーRNA(sa-mRNA)COVID-19ワクチンの歴史的承認」
- CSLとアークトゥルス・セラピューティクスは、自己増幅型mRNA(sa-mRNA)COVID-19ワクチンARCT-154について、厚生労働省より18歳以上の成人に対する初回接種および追加接種の承認を取得したと発表した。
- ノーベル賞受賞者のドリュー・ワイズマン博士は、「自己増幅型mRNA技術は、永続的なワクチンの選択肢となる可能性を秘めている」
- 今回の承認は、ベトナムで実施中の16,000人を対象とした有効性試験や、標準的なmRNA COVID-19ワクチンの比較対照と比較して高い免疫原性結果と良好な安全性プロファイルを達成した第3相COVID-19ブースター試験など、複数のARCT-154試験から得られた良好な臨床データに基づいている。 初期試験結果はMedRxivに掲載されており、年内に査読付き学術誌に掲載される予定である。
- CSLのワクチン事業であるCSL Seqirusは、世界最大級のインフルエンザワクチンプロバイダーであり、sa-mRNA コロナワクチンARCT 154の日本における販売について、明治製菓と独占的に提携した。
- アークトゥルス・セラピューティクス(カリフォルニア州サンディエゴ)の最高経営責任者(CEO)であるジョセフ・ペインは、次のように述べています。「世界で初めて承認されたsa-mRNA製剤の開発・検証において、アークトゥルスが果たした役割を誇りに思う」
自己増幅型mRNAワクチンとは何か?
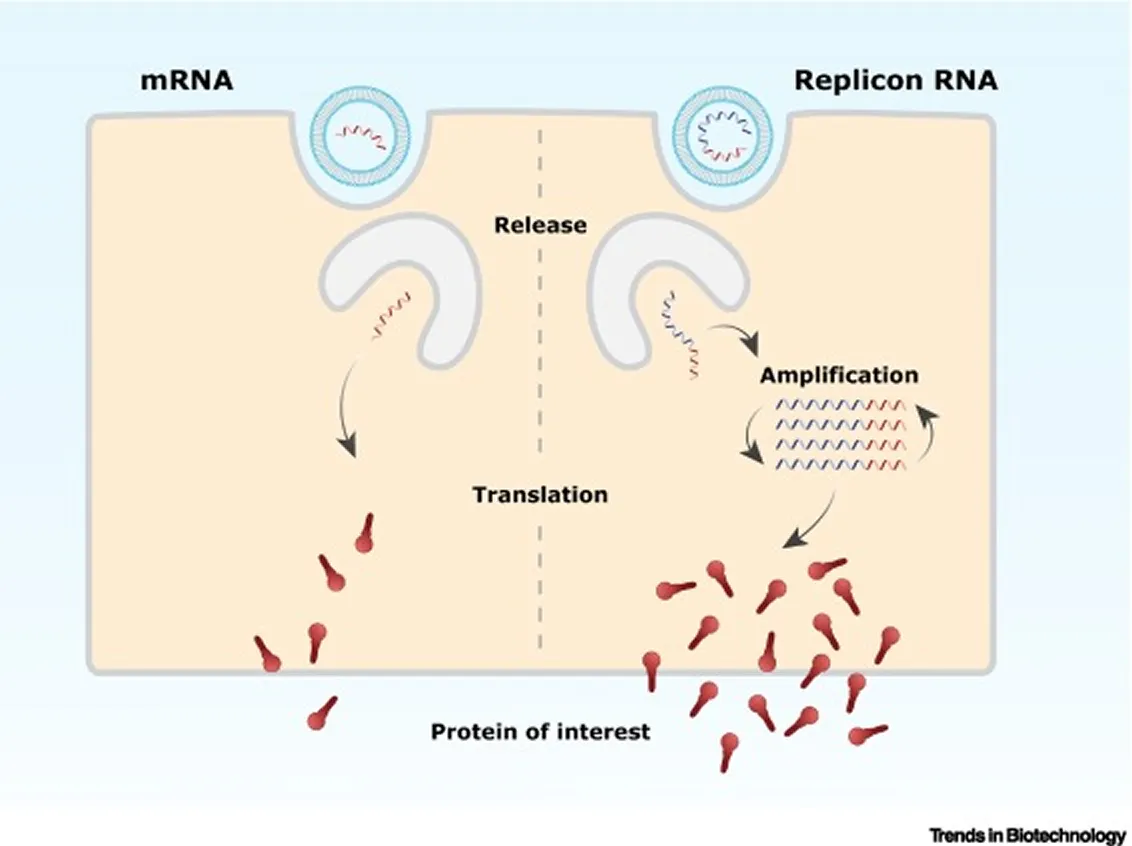
- 「レプリコンは標的細胞に投与後、直接コピー数を増加させるために、自身の複製機械をコード化する」
- 「レプリコンRNAはさらにウイルスレプリカーゼ遺伝子をコードしている。これらの遺伝子はmRNAの迅速な増幅を可能にする。自己増幅ウイルス遺伝子は、例えばアルファウイルスやフラビウイルスなどのウイルスに由来する。
日本政府が承認に利用した16センターのベトナム「安全性調査」
- ワクチン:「ARCT-154は、ベネズエラウマ脳炎ウイルスをベースに、ウイルスの構造タンパク質をコードするRNAを、一点変異を含む祖先株の初期変異型であるSARS-CoV-2 D614Gウイルスの全長スパイク(S)糖タンパク質をコードするRNAに置き換えたレプリコンを、脂質ナノ粒子に封入したものである。バイアルに入れ-20℃以下で保存した100μgの有効成分を、使用直前に10mLの滅菌生理食塩水に溶解し、5μgを含む0.5mLを三角筋に筋肉内注射した」
- 「宿主細胞にワクチンmRNAのコピーを作らせ、より少ない投与量のmRNAで産生されるタンパク質の量を増やす」
- 「加速承認」=ARCT-154の安全性、反応原性、免疫原性、有効性を評価するため、EMA、FDA、WHOのガイダンスに従ってデザインされた現在の加速統合第1/2/3a/3b相試験を開始した。
- 我々は、この新規ワクチンによるヒトボランティアへの最初のワクチン接種から3カ月後までの最初の研究結果を発表する。
- 1回目の投与後、90%に少なくとも1件の有害事象が認められた(ほとんどが軽度)
- 「ARCT-154を接種した患者では、全身性AEと局所反応の頻度が、認可されているmRNAワクチンよりも少なかった。
- 「日本における並行研究では、一次ワクチンとしてBNT162b2を中心とするmRNAワクチンで完全免疫された成人において、中和抗体として測定した場合、ARCT-154のブースター投与に対する免疫応答がBNT162b2のブースター投与に対する免疫応答よりも優れていることが示された」
- 「ARCT-154は、循環変異体に対する免疫レベルを強化し、拡大するために、一次免疫としてではなく、ブースター用量として使用される可能性が最も高い」
小田らによる2023年12月20日の日本研究
- 18歳から64歳までの828人が参加。
- 3倍のmRNAワクチン(ファイザーまたはモデルナ)を接種し、ARCT-154またはファイザーのいずれかを4回目のブースターとして接種した。
- ARCT-154はファイザー社に比べ免疫応答が良好である。
- 「どちらのブースターの忍容性も同等であった」
ローらによる2022年12月13日の研究
- 169人のボランティア、第I/II相
- ARCT-021は、7.5μgの用量までは一般的に良好な忍容性を示した。
- 10μgの用量は、グレード3の重症度を含む、より多くの局所的および全身的な勧誘AEと関連していた。
- グレード2以上のリンパ球減少症については、投与量に関連した傾向がみられ、1.0,3.0,5.0,7.5,10μgの投与量レベルでは、それぞれ0%、25%、26.5%、30.0%、40.0%が罹患した。リンパ球減少は注射後24時間以内に発現し、通常1日以内に問題なく消失した。
メリット
- ARCT-154(5μg)は、他のRNAベースのCOVID-19ブースターに比べ、1人当たり10分の1から6分の1のワクチン量で済む。
- 1回の注射で投与するワクチンの量を減らせば、「製造コストの削減」につながるはずだ。
- ウイルスに似た性質を持つため、saRNAは独特の方法で免疫システムと相互作用する。
- ARCT-154の日本での承認が得られたため、開発者は現在、欧州での承認を求めている。
- 昨年8月、CEPI(Coalition for Epidemic Preparedness Innovations)は、自己増幅型saRNAプラットフォームの開発に最大360万ドルを提供すると発表した。
- 「一度投与すれば、これらの分子の発現は長期間持続する。従って、企業は少量生産によるコスト削減を期待でき、同時に患者への投与量負担も軽減できる。投与量が少なければ、副作用の可能性も少なくなる」
- RNAワクチン候補の製造は迅速で、インフルエンザワクチン候補はわずか8日で製造されたと報告されている[8]。
- 「mRNAは非感染性であり、宿主細胞のRNaseによって分解されるため、細胞内に一時的に存在するだけである」
- 「sa-mRNAワクチンはCOVID-19の持続的免疫を促進する」
- ワクチン接種後12カ月間、免疫反応の上昇を維持する。
問題点
- アクトゥルス、独自の「脂質ナノ粒子」を使用– 詳細は不明だが、ファイザーとモデルナのLNPに類似していると主張
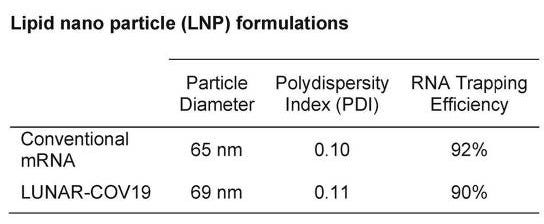
- ArcturusのLNPについては、安全性試験や生体内分布試験は実施されていない。
- sa-mRNAは(複製装置の配列が追加されたため)はるかに大きく、3倍にもなる。
- 「これは、合成中の製品関連不純物の増加や、サイズが大きいことによるクロマトグラフィー工程での結合能の低下など、製造中の課題につながる」
- 一度注入された欠陥のあるsa-mRNAは細胞内で増幅され、欠陥タンパク質の濃度が高くなる。
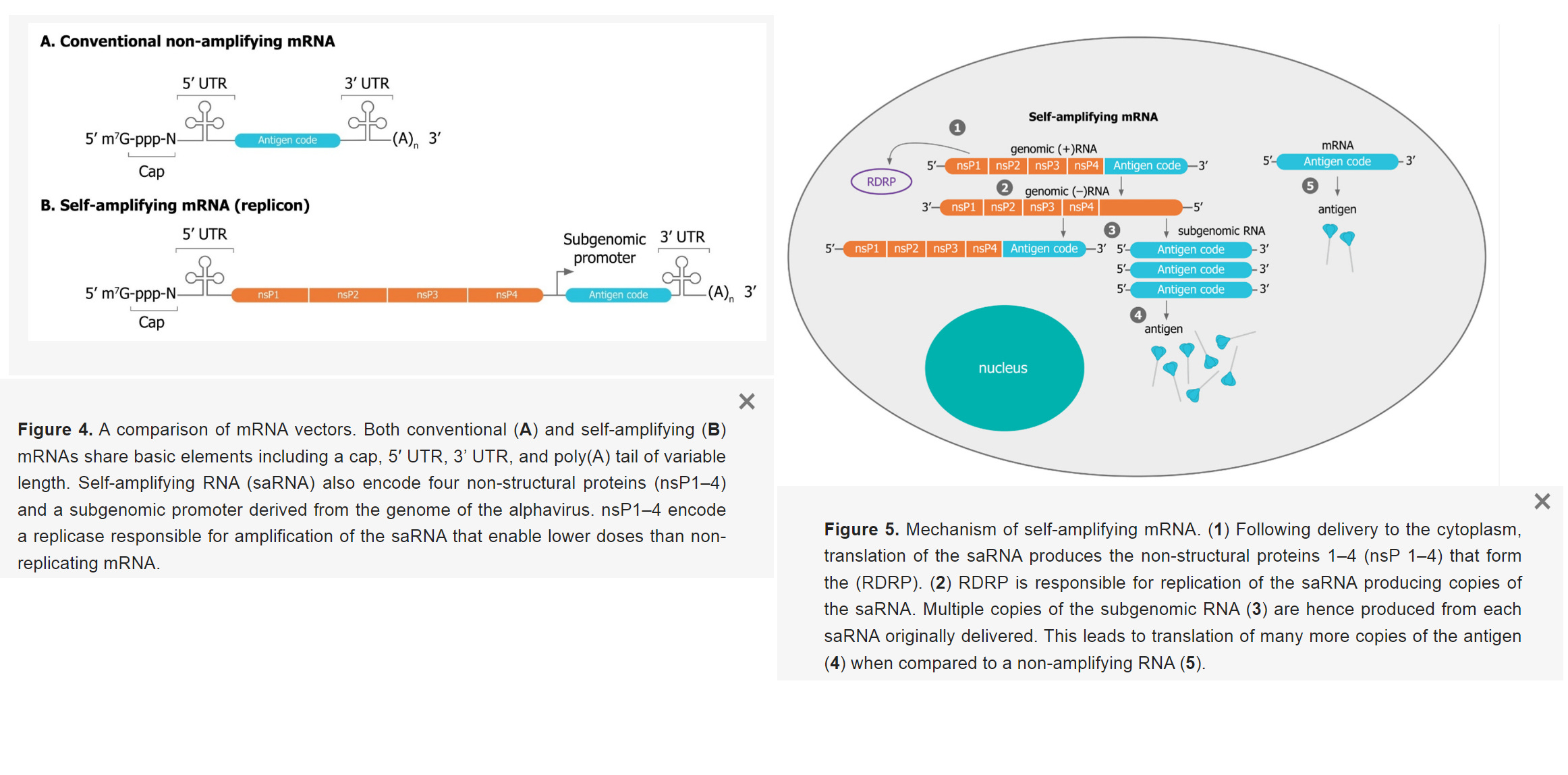
- ほとんどのsaRNAワクチンは、ベネズエラウマ脳炎ウイルス(VEEV)、シンドビスウイルス(SINV)、セムリキフォレストウイルス(SFV)のゲノムをベースにしている。
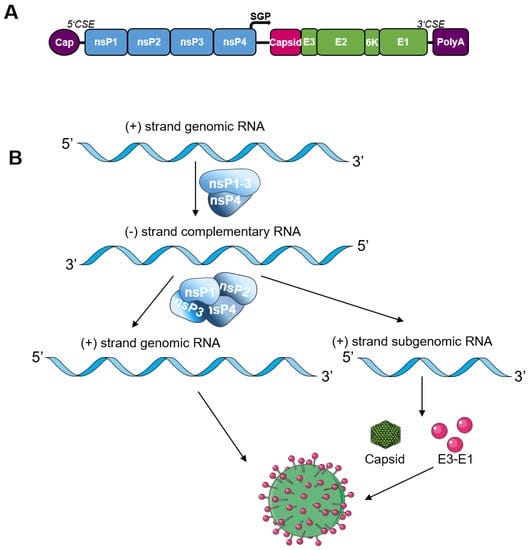
- saRNAワクチンの構築のために、アルファウイルス構造タンパク質は抗原遺伝子(COVID-19ワクチン用スパイクプロテイン)に置き換えられる。
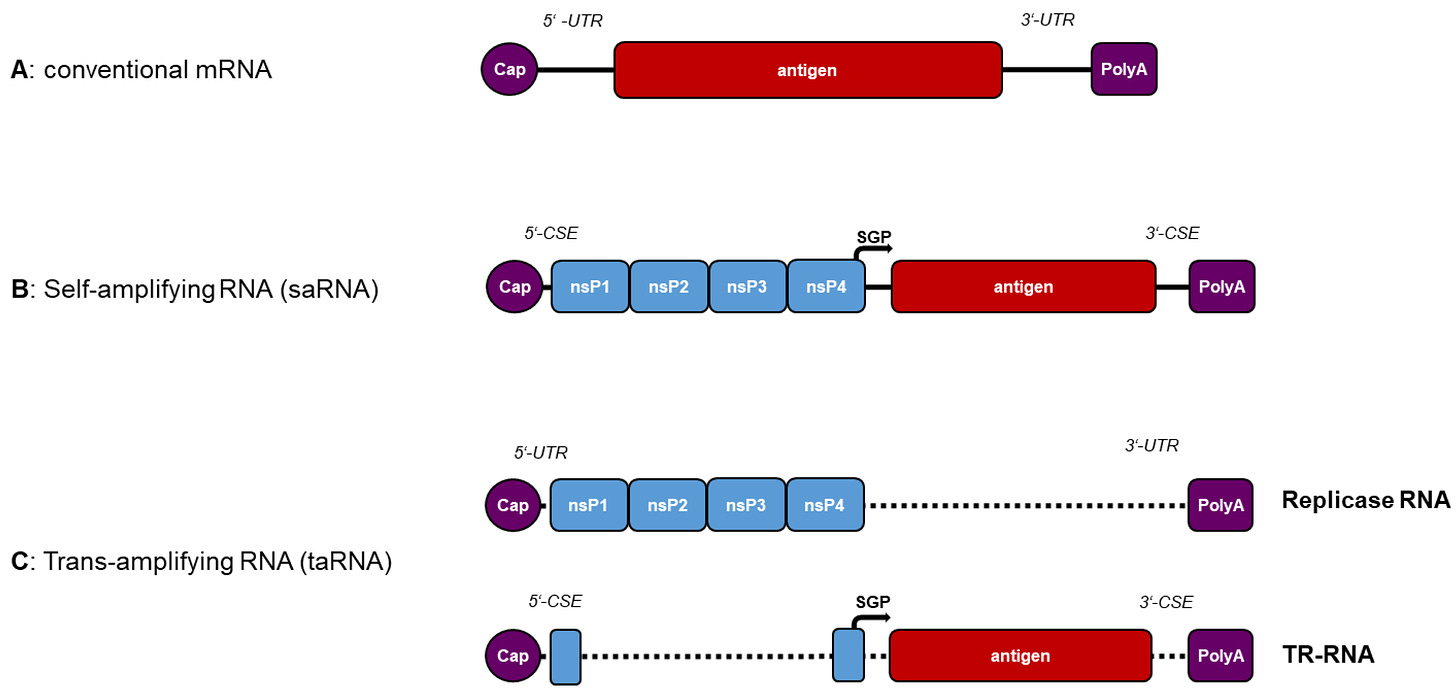
- 「増幅されたmRNA」をどれだけ生産しているかはわからない。
- スパイクプロテインの生産量は不明
- ウイルスレプリカーゼは、まずポジティブセンスゲノムを鋳型として、相補的なネガティブセンスRNAを合成する。
- RNAの増幅と抗原の発現がいつまで続くのかを解明する必要がある。
- DNA汚染?ある
- 「saRNAとtaRNAは、DNAを鋳型として、試験管内試験転写とキャップ構造の付加によってmRNAと同様に作られる」
- 「しかし、sa/taRNAワクチンの場合、ヌクレオシド修飾は増幅の段階で失われ、あまり有益ではない」
- mRNAワクチンとは対照的に、細胞内RNA増幅はdsRNAとなり、自然免疫応答をより強力に活性化する。RNAはTLR3、TLR7など複数のパターン認識受容体によって認識される。
- LNP製剤にはアジュバント効果もある
sa-mRNAをパイプラインに持つ企業:
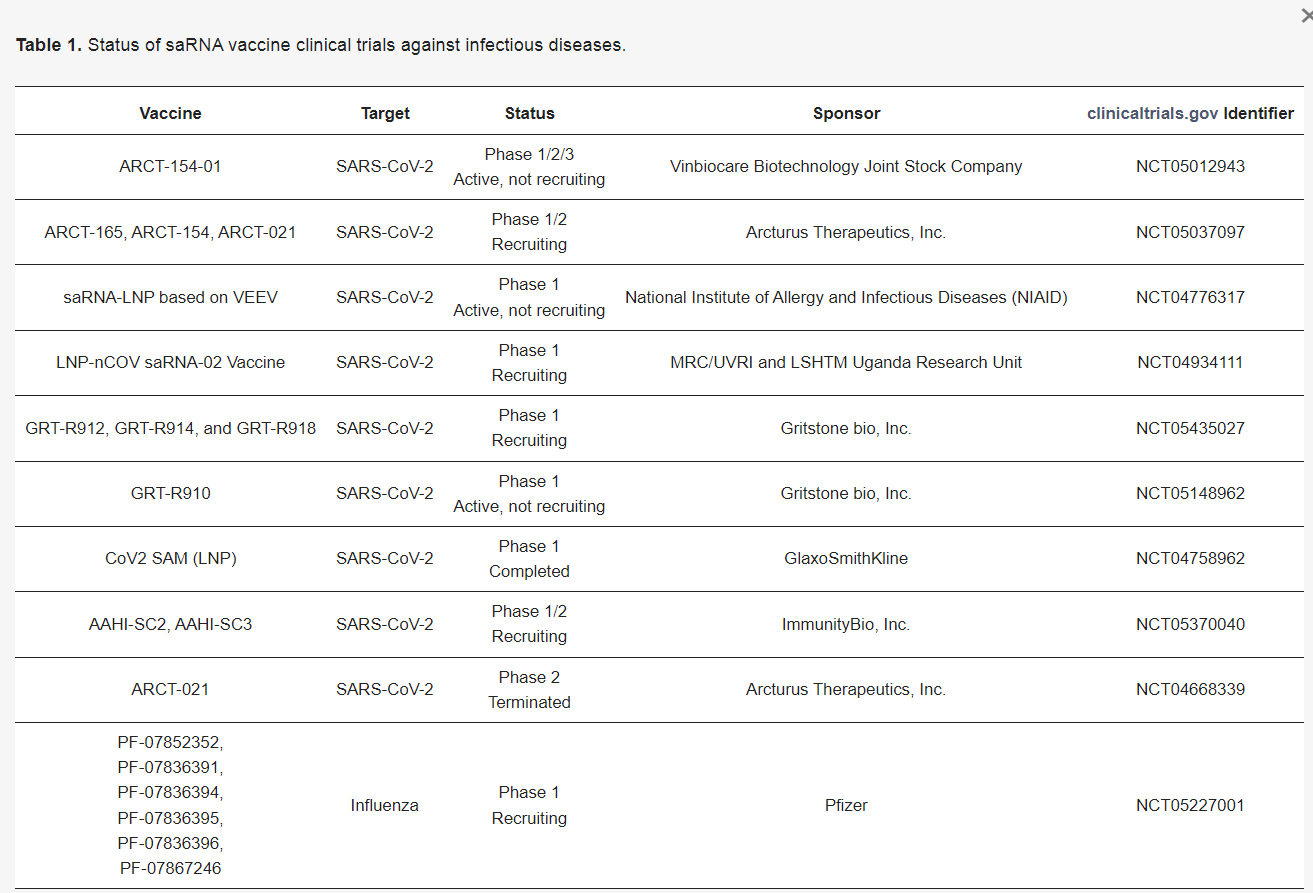
私の懸念…自己複製mRNAの脱落
- ファイザー社は、同社の製品が吸入や皮膚接触による「環境暴露」をもたらすことを認めた。

- しかし、LNP/mRNAやエクソソーム/mRNAを介して、ファイザー社やモデルナ社のCOVID-19 mRNAワクチンを少量でも接種すれば、ワクチン接種にはならない。
- 免疫システムがそれを破壊する。
- しかし、自己複製するmRNAのシェディングにさらされたらどうだろう?
- そうなると、理論的には、そのmRNAはあなたの体内で未知の量のコピーを丸1カ月作ることができ、それは永久的な内部損傷を引き起こすのに十分な期間かもしれない。
- このリスクは研究されていない。

まとめ
日本は世界初の自己増幅型sa-mRNA COVID-19ワクチンを承認した。
この技術の問題点をいくつか挙げてみよう:
- mRNAの投与量は少ないが、スパイクプロテインの量は多く、副作用のプロフィールはファイザー社のmRNAと同じである。利点は?大手製薬会社の製造コストが下がることだ。
- アクトゥルスは、ファイザーと同様の独自の脂質ナノ粒子(LNP)を使用しているが、生体内分布や安全性に関する研究は行われていない。
- これらのLNPは、血液脳関門や胎盤関門を越えて、外来のシュードウリジン修飾sa-mRNAを全身に送達する。
- あなたの体を、単なるスパイク・プロテイン製造工場から、スパイクsa-mRNAとスパイク・プロテイン製造工場に変える。
- DNAプラスミド汚染もまだある。
- sa-mRNAはファイザーmRNAの3倍の長さ(独自の複製機械用の余分なコードのため)であり、これは製造中の不純物のリスクが高いことを意味する。
- 精製がさらに困難になるため、DNA汚染はさらに深刻になる可能性がある。
- ベネズエラウマ脳炎ウイルス(VEEV)のゲノムを複製装置に使用。
- Sa-mRNAの塩基配列に異常が生じ、それが体内で増幅され、未知の結果をもたらす変異タンパク質を生成するリスクが高まる。
- sa-mRNAは細胞内で増幅され、最大で1カ月間、未知の量になる(元のsa-mRNAはシュードウリジン修飾されているが、細胞内で作られるコピーは修飾されていないため)。
- sa-mRNA増幅の忠実度は不明であり、未検証である。
- 未知の量のスパイクプロテインを生成する。
- 未知の変異スパイクプロテインと未知の非スパイクプロテインを大量に生成する。
- 小田による日本の研究では、ファイザーのCOVID-19ブースターと同じ副作用プロファイルを示している(これは悪い兆候である)
- RNAワクチン候補を迅速に製造することができ、インフルエンザワクチン候補はわずか8日で製造されたと報告されている(これも悪い兆候である)。
- mRNAが宿主ゲノムに組み込まれる危険性はないとする研究があるが、それを裏付ける証拠はない。
- 免疫反応を刺激するdsRNA中間体を作り出すが、その効果(および副作用)は完全には解明されていない。
- シェディングは、自己増幅型mRNAではより危険になる。
- 流された人は、1カ月ほど未知の量のsa-mRNAを産生し始めるかもしれない。
- 最後に、もしsa-mRNA全体がゲノムに組み込まれれば、スパイクmRNAを無限に増幅する(そしてスパイクプロテインを産生する)ことになる。
- 長期安全性試験は行われていない。
この自己増幅型mRNA技術は、私たちがファイザーとモデルナのCOVID-19 mRNAワクチンで経験したことよりもさらに大きな災難のように聞こえる。
興味はない。
*
ウィリアム・マキス博士は、放射線学、腫瘍学、免疫学を専門とするカナダ人医師。トロント大学奨学生。100以上の査読付き医学論文の著者。