Contents
Nasal disinfection for the prevention and control of COVID-19: A scoping review on potential chemo-preventive agents
オンラインで公開2020年8月18日
www.ncbi.nlm.nih.gov/pmc/articles/PMC7434367/
要旨
背景
COVID-19を予防するための曝露前・曝露後の化学予防薬は現在のところ使用できない。一方,SARS-CoV-2は発症前後に鼻腔から高負荷で排出される.
目的
SARS-CoV-2に対する健康効果が期待できる忍容性のある経鼻消毒薬、すなわち、SARS-CoV-2以外の少なくとも2種類のウイルスに対して有効な薬剤について、利用可能なエビデンスを対象としたスコープレビューを実施すること。
方法
2010-2020 年に出版された論文を特定するためにオンラインデータベースを検索した。スコーピングレビューに関連する論文を選択した。レビューは、各治療法について、作用機序、忍容性、試験管内試験および生体内試験でのSARS-CoV-2に対する効果のエビデンス、製品の上市の有無を記述した叙述的なものであった。
結果
次亜チオシアナイト,ラクトフェリン,N-クロロタウリン,インターフェロンα,ポビドンヨード,第四級アンモニウム化合物,アルコール系鼻腔消毒薬,ヒドロキシクロロキンの8つの治療法を検討した。エタノール、アルコール系手指消毒剤、ポビドンヨードについては、SARS-CoV-2に対する試験管内試験殺菌効果が報告されている。ラクトフェリン、エタノール、ヒドロキシクロロキンおよび第四級アンモニウム化合物については、他のコロナウイルスに対する阻害効果が報告されている。SARS-CoV-2に対する治療法は、これまでのところランダム化対照臨床試験では試験されていない。しかし、インターフェロン-α、ラクトフェリン、ヒドロキシクロロキンは片腕オープンラベル非対照臨床試験で試験されている。主な作用機序は,酸化活性(ヒポチオシアナイト,N-クロロタウリン,ポビドンヨード),内膜・リソソームpHの亢進(第4級アンモニウム化合物,ヒドロキシクロロキン),ウイルスカプシドの破壊(第4級アンモニウム化合物,アルコール系鼻腔用防腐剤)であった。ラクトフェリンやインターフェロン-αは微妙な生物学的機序を持っている。N-クロロタウリンを除いて、市販されている他のすべての製品がそうであった。
結論
SARS-CoV-2に対する有効かつ安全な化学療法による予防薬はまだ存在しないが,すでにほとんどの候補薬が市場に出回っている。SARS-CoV-2の侵入口は鼻腔であるが、口は呼吸器の飛沫を排出することで出口となる。よく知られている手から鼻から手への感染サイクルは、感染制御のための適切な追加戦略を必要とする。その後の臨床研究を絞り込むために、症例対照法を用いてCOVID-19スワブ陽性者と陰性者の間で候補薬の使用状況を比較することができる。
キーワード
COVID-19,SARS-CoV-2,鼻腔内消毒、ハイポチオシアナイト、ラクトペルオキシダーゼ、ラクトフェリン
1. 背景
1.1. 根拠
新規β型コロナウイルスSARS-CoV-2による現在のコロナウイルス疾患2019(COVID-19)は 2020年8月26日の時点で213カ国に影響を及ぼすパンデミックと宣言されている(Worldometers, 2020)。
SARS-CoV-1とは異なり、SARS-CoV-2は、最大14日間と推定される潜伏期間中に上気道で効率的に複製するようである(Heymann and Shindo, 2020; World Health Organization, 2020a)。この潜伏期には、無症状者および無症状前の個体が感染細胞から大量のウイルスを放出する(世界保健機関 2020a)。その結果、SARS-CoV-2では、SARS-CoV-1よりもウイルス感染が有効であり、逆に活動期/臨界期にのみ伝染した(世界保健機関 2020a)。さらに、感冒を引き起こす可能性のあるヒトコロナウイルスは、既存の体液性免疫に関係なく呼吸器再感染を引き起こすことが知られている(Gorse et al 2020; Cegolon et al 2020)。したがって、COVID-19には、2つの問題がある:ウイルスの高い感染性、および疾患の可変性の臨床パターンであり、これは、重症急性呼吸器症候群(SARS)および高凝固状態を特徴とする生命を脅かす肺炎に至るまでの症状前/症状後の状態からなる(世界保健機関(WHO)2020a、Cegolon et al 2020)。
SARS-CoV-2からの高い感染リスクは、これまでのところ、自己隔離、社会的遠距離、接触者の隔離、個人保護具(PPE)の使用、旅行制限、および個人の移動の自由に対するその他の制限などの感染予防および制御(IPC)対策によって対処されてきた。しかし、SARS-CoV-2の蔓延を抑制する上での各介入の効果はまだ評価されていない(Kucharski and Eggo, 2020)。
現在、世界保健機関(WHO)と欧州疾病予防管理センター(European Center for Disease Prevention and Control)のガイドラインでは、症状のある個人とCOVID-19の確定症例の近親者のみを検査することを推奨している(European Centre for Disease Prevention and Control, 2020;;世界保健機関(WHO)2020b)。パンデミックの初期段階では、症状に基づくスクリーニング戦略は、感染例の治療と分離を目的とした有用なものであったが、ケアホームや病院でのCOVID-19の発生は、現在のIPC対策が不十分であり、いくつかの国で失敗していることを示唆している(Gandhi et al 2020; Arons et al 2020)。さらに、上記のIPC対策は、COVID-19の影響を大きく受ける国々の経済を著しく破壊することになるため、長期的には持続可能ではない。多くの国で実施されているロックダウン措置を緩和/回避する必要性は、薬理学的介入(理想的にはワクチンまたは化学予防薬)がうまくいけば利用可能になるまで、無症候性/前症候性個人からのSARS-CoV-2の感染を減少させるための改訂されたアプローチを促す(Gandhi et al 2020)。上で説明したように、COVID-19の問題は、無症候性/無症候性の個人からの感染であり、ケアホームや病院では特に重要な現象である。ロサンゼルスでは、COVID-19の地域発生の健康リスクを減らすために、家族はケアホームから親族を追い出すよう公衆衛生局から助言を受けている(Dlan and Hamilton, 2020)。
集団検査は、無症候性/無症候性前の個人からのSARS-CoV-2の感染を減少させる可能性のある戦略として、様々な国で検討されている(Gandhi et al 2020)。それにもかかわらず、(韓国で行われているように)定義された集団発生を対象とした大量検査は、現在のパンデミックが進行中の世界的なシナリオでは、賢明なことかもしれない(Balilla, 2020)。言うまでもなく、高所得国においても、大量検査は微生物検査室の能力をはるかに超えている。しかし、大量検査をケアホーム、病院、精神保健施設、刑務所、学校などの高リスクの集合的な環境に限定することは適切かもしれない(Gandhi et al 2020)。ワシントン州のケアホームから報告されたアウトブレイクでは、合計76人の入居者を収容しているケアホームで、リアルタイムPCRでCOVID-19が陽性となった48人の入居者のうち27人は、検査前の14日間に無症状であった(Arons er al)。
SARS-CoV-2の高負荷は、症状の発症前にも鼻腔から環境中に排出され(Heymann and Shindo 2020;Gandhi et al 2020)無症状者からのSARS-CoV-2の感染が報告されている(Rothe et al 2020;Yu et al 2020;Bai et al 2020)。したがって、COVID-19の気付かれていない無症候性症例は、感染の大部分(5人中4人)が完全に無症候性であったと報告した中国国家衛生委員会の最近の証拠によって裏付けられているように、重要な伝染源を構成する可能性がある。特に 2020年4月1日に中国で確認された166件の新規感染のうち130件は、全く症状がなかった(Day, 2020)。
SARS-CoV-2に陽性と判定された無症状者には14日間の隔離が強制されているが、大量検査を行っても、一般集団におけるウイルスの蔓延を解消することはできず、特に寒冷地での発生が繰り返されるリスクがある(Cegolon et al, 2020; Cegolon and Mastrangelo, 2020)。実際、SARS-CoV-2の透過性および生存可能性は、高温多湿の気候によって重要に低下するという証拠がある(Cegolon et al 2020;Matson et al 2020;Wang et al 2020)。2020年)2020年1月から3月の間に中国の都市で観察された相対湿度が23.33%から82.67%に上昇し(p値=0.002)気温が-13.17℃から 19℃に上昇し(p値=0.003)新規コロナウイルスの伝播が減少したことによって確認された(Yao et al 2020)。
ヒトコロナウイルスに対する体液性免疫の保護効果はまだ議論されており、いくつかの証拠は、デング熱、SARS-CoV-1,MERS-CoVおよび西ナイルウイルスなどの他のウイルス性疾患と同様に、COVID-19の重症/重症型を特徴とする二次感染によって引き金となる潜在的な抗体依存性増強(ADE)を指摘してさえいる。Cegolon et al 2020)。上記のIPC対策の緩和に続く、特に寒い時期に、逆行した危険な結果が生じる可能性があること、およびSARS-CoV-2に対する特定の登録された治療法またはワクチンが存在しないことを考えると、ウイルスの複製およびヒトの間でのCOVID-19の拡散を防止および制御するための代替的な解決策を見つけることが明確かつ緊急の必要性である(Yu et al 2020)。
COVID-19は急速に進化するパンデミックである。SARS-CoV-2に陽性と検査され、自宅での自己隔離を強制された無症状の個体は、イタリアではパンデミック開始時には陽性個体全体の約40%であったが、その後、完全なロックダウンの終了後には80%以上になった(GEDI visual, 2020)。図1は、対応する変化をパーセンテージまたはオッズで報告している。後者は、天井効果を克服することができるため、前者よりも指標スコアの改善を検出する。
図1 イタリアでSARS-Cov-2に陽性と判定され、自宅での自己隔離を強制された無症候性の人の 2020年3月1日から6月30日までの1日の傾向
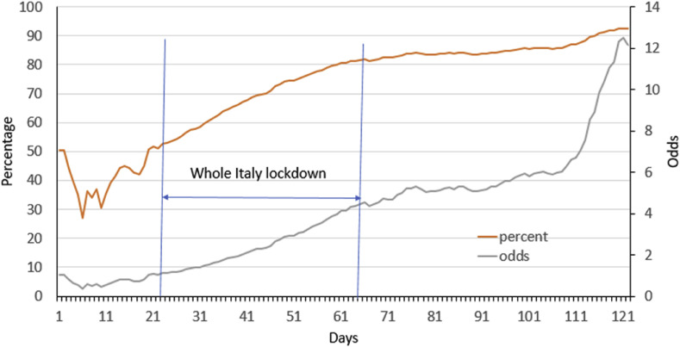
有病率はパーセンテージ(オレンジ色の線と左の縦軸)またはオッズ(灰色の線と右の縦軸)で表される。(この図の凡例の色への参照の解釈については、読者はこの記事のWeb版を参照してほしい)。
したがって、有症者に対する効果的な治療に加えて、コミュニティ内での新型コロナウイルスの感染を抑制するために、無症候性/前症候性の個人のヒト鼻腔内での SARS-CoV-2 の感染を抑制することが緊急に必要とされている。
1.2. 目的
SARS-CoV-2に対して有望な有効性を特徴とする、例えば、類似のウイルス/分子構造を有する、SARS-CoV-2以外の少なくとも2つの異なるウイルスに対して有効な薬剤を特徴とする、忍容性のある外用鼻腔消毒剤を見つけること。
2. 方法
PubMedでは、「抗感染症薬、局所」と「抗感染症薬、鼻腔」をキーワードに、「年齢:19歳以上」、「ヒト」、「英語」のフィルターを適用し 2010年~2020年に発表された論文を対象に調査を行った。返却された255件の論文をタイトルと要旨
で精査した。論文の大部分はメチシリン耐性黄色ブドウ球菌に対する薬剤(一般的にはクロルヘキシジンまたはヘキサクロロフェンの洗体に伴う鼻腔内のムピロシン)を扱ったものであった。今回のスコーピングレビューの対象となった薬理学的薬剤は,ポビドンヨード液(7論文),アルコール系鼻腔消毒薬(2論文),第4級アンモニウム化合物(1論文),N-クロロタウリン(1論文)であった。さらに、検索語として「鼻腔消毒」を使用したのは、査読なしの予備的報告の3つのオンラインリポジトリであった。見つかった治療法は、ポビドンヨード溶液とインターフェロンアルファ(MedRxivからの2論文)次亜チオシアナイト(2論文、うち1論文はSSRNから)アルコール系鼻腔消毒薬(arXivからの1論文)であった。
引用された治療法はすべて、異なる電子データベースからの追加情報を見つけるためのキータームとして使用した。原著論文の要旨は、作用機序、忍容性、毒性効果や耐性菌の選択の証拠、治療法が試験管内試験(特にSARS-CoV-2に対する)で試験されたかどうか、臨床試験段階にあるかどうか、現在販売されているかどうか、販売されているかどうか、などの用語で検索した。
3. 結果
8つの治療法を精査した:次亜チオシアナイト(OSCN-)ラクトフェリン(LF)N-クロロタウリン(NCT)インターフェロン-α(IFN-α)ポリビニルピロリドン-ヨード(PVP-I)ヒドロキシクロロクイン( ヒドロキシクロロキン)第4級アンモニウム化合物およびアルコールベースの鼻腔内消毒薬。
3.1. ハイポチオシアナイト
ラクトペルオキシダーゼ(LPO)は、ヒト気道上皮の界面を含むいくつかの外分泌物中に存在するヘムペルオキシダーゼであり、過酸化水素(H2O2)の存在下で、主にハロゲン化物(ヨウ化物アニオンI-)および擬似ハロゲン化物(チオシアン酸塩、アニオンSCN-としても知られている)基質(Baffort et al 2014)から、異なる抗感染剤を産生する。SCN-およびI-の両方が一電子供与体として作用し、H2O2は比較的特異的な電子アクセプターとして作用し、LPOは触媒酵素である。2つの酸化を受けることで、ネイティブLPOはH2O2に2つの電子を供与し、水に還元される。この時点で、LPOはそのネイティブな状態に還元される。必要な生化学的/環境条件が満たされているかどうかにかかわらず、LPOは、SCN-またはI-の存在下で、それぞれ活性な抗菌分子OSCN-(ハイポチオシアナイト)またはOI-(ハイポオダイト)を生成する(Bafort er al)。
図2において、R-SHは、多数の酵素およびタンパク質の活性に必須のチオール部位を有するペプチドまたはタンパク質である。OSCN-またはOI-によるR-SHのスルフィドリル酸化は、チオシアン酸スルフェニル(R-SCN)またはヨウ化スルフェニル(R-S-I)を生成し、細菌の解糖、呼吸およびグルコース輸送の阻害を決定する。ペントースリン酸経路の阻害もまた、サイクルの最後に形成されるSCN-またはI-と同様にスルフェン酸(R-S-OH)を有するOI-についてのみ観察された。SCN-またはI-のいずれかがネイティブLPOと反応し、サイクルが再開される。システム全体(酵素+基質)の抗微生物活性は、ハイポチオシアナイトまたはハイポオダイト単独よりも効果的であることが知られており、短命で反応性の高い中間体の生成によって説明されてきた(Bafort et al 2014)。さらに、I-ペルオキシダーゼ系の活性は、より低いI-濃度が必要であるという点で、SCN-系よりも大腸菌に対してより効果的である(Bafort et al 2014)。I-ペルオキシダーゼ系は、新しいコロナウイルスに対して試験管内試験で試験されるに値する。
図2 ラクトペルオキシダーゼサイクル[Baffort et al 2014)から、改変された]
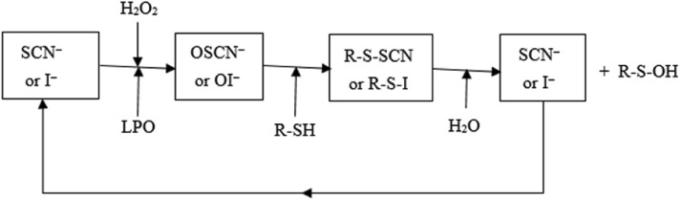
SCN-、チオシアネート;I-、ヨウ化物;H2O2,過酸化水素;LPO、ラクトペルオキシダーゼ;OSCN-、次亜チオシアナイト;OI-次亜ヨウ化物;R-SH、チオール部位を有するペプチドまたはタンパク質;R-S-SCNまたはR-S-I、チオシアネートまたはヨウ化スルフェニル;およびR-SOH、スルフェン酸。
さらに、OSCN-は、おそらく遊離チオールラジカルを酸化してジスルフィド結合を形成することによって、異なる呼吸器ウイルスの表面タンパク質を変化させることができるようである(Alaxia, 2020)ので、ウイルスとヒト気道粘膜との結合とは対照的である。OSCN-はまた、議論の余地なく、ウイルスタンパク質および核酸の合成およびアセンブルを阻害する可能性があり、したがって、感染した細胞からのウイルスの放出を妨害する(Day, 2020; Cegolon et al 2014; Cegolon, 2020)。
LPO細胞外酸化複合体の生成物は、病原体の脅威に対する中心気道のヒト自然保護システムの一部である(Day, 2020; Alaxia, 2020; Cegolon et al 2014; Cegolon, 2020)。ガス交換を最大化する必要性のために、肺胞上皮細胞は強力な保護構造を含むことができない。後者の細胞は、肺腺癌のための外科的切除を受けた2人の患者で発見されたびまん性肺胞損傷によって示されるように、感染剤に対して脆弱であり、後にCOVID-19肺炎にも影響を受けていることが発見された(Tian et al 2020)。気管支は、同じ研究では肺胞ほど脆弱であるとは報告されていなかった(Tian et al 2020)。
ヒトの鼻および眼の分泌物中のLPO/H2O2/SCN-システムの欠如は、結膜および鼻の粘膜における細菌および呼吸器ウイルスの生存および増殖、ならびにその後の環境中でのそれらの脱落を説明し得る(Tenovuo et al 1986;Marcozzi et al 2003;Mastrangelo et al 2005,2009;Schaffer et al 1976;Couche、1995)。マイクロモル濃度で、反応性混合物LPO/H2O2/OSCN-は、細菌(グラム陽性および陰性)真菌(Candida albicansおよびCandida krusei)およびHIV、ヘルペス-シミプレックスウイルス(HSV-1)アデノウイルス、エコーウイルス、呼吸器同期ウイルス(RSV)およびインフルエンザウイルスとしてのウイルスの範囲に対して殺菌活性を証明した(Moskwa et al 2007; Conner et al 2007; Moskwa et al 2009)。2007; Conner et al 2007; Carlsson et al 1984; ThomasおよびAune、1978; Ihalin et al 1998; Reiter et al 1976; Patel et al 2018; Lenander-Lumikari、1992; Mikola et al 1995; Pourtois et al 1990; Gingerich et al 2016)。)
最近の試験管内試験実験では、オキシダーゼ/LPO/H2O2/チオシアネート系によって産生されたOSCN-は、迅速かつ効果的にA/swine/Illinois/02860/09(swH1N2)インフルエンザAウイルスを不活化し、ヒト初代および雄のSprage-Dawleyラットの気管-気管上皮細胞の両方の感染を成功裏に防止した(Gingerich et al 2016)。
より最近の試験管内試験無細胞実験では、インフルエンザAおよびBウイルス(パンデミックを引き起こす主要な循環血清型および種)の12種類のすべての株が、LPO/H2O2/(SCN-/I-)系によって効果的に不活化された(Patel et al 2018)。菌株に依存しない効果を考慮すると、後者の研究の著者は、インフルエンザウイルスのクリアランスに貢献するために、LPO/H2O2/(SCN/I-)系の生体内試験での医薬的応用を奨励した(Patel et al 2018)。
別の実験室実験では、酵素を含まないOSCN-をA/H1N1 2009パンデミックインフルエンザウイルスに対して試験管内試験で挑戦し、細胞毒性を伴わない明らかな用量依存性の殺ウイルス活性を示した(Cegolon et al 2014)。特定のタンパク質を標的としていない広いスペクトルの殺ウイルス効果(CegolonおよびMastrangelo 2020; Patel et al 2018)が実証されたことを考慮すると、OSCN-はSARS-CoV-2に対しても有効である可能性があり、したがって、試験管内試験で試験されるに値すると合理的に論じられ得る(Cegolon et al 2014; Cegolon 2020)。それはすでにヒト気道分泌物中に天然に存在し、その大きな作用スペクトルを考慮すると、OSCN-では、ウイルス変異による抵抗性の低レベルおよび限定的な副作用が予測できる(Cegolon and Mastrangelo, 2020; Cegolon et al 2014; Cegolon, 2020)。SARS-CoV-2に対して試験管内試験で有効であれば、酵素を含まないOSCN-を用いた生体内試験エアロゾル試験は、その後、リアルタイムPCRで任意の個々のCOVID-19陽性をクリアすることにより、SARS-CoV-2の感染性の短期予防を提供することを目的として実施され得る。
OSCN-は、単独またはラクトフェリン(LF)との組み合わせで、健康なボランティアおよび嚢胞性線維症および気管支拡張症に罹患した患者を対象とした第1相臨床試験(RCT02598999)ですでに試験されている(Alaxia, 2020)。
また、LPO/H2O2/SCN-システムは、歯磨き粉や洗口剤として使用されている市販の非処方品(Zendium)である。
3.2. ラクトフェリン
ラクトフェリン(LF)はトランスフェリン科に属する天然の多機能タンパク質である。ラクトフェリンはヒトの乳中に存在し、唾液、涙、牛乳、鼻や気管支の分泌物、消化管液、尿粘膜分泌物などの外部分泌物に含まれている。LFは白血球の好中球顆粒の重要な構成要素である(Farnaud and Evans, 2003)。
LFはトランスフェリンと類似しているため、鉄結合能を持ち、pH3.5でも鉄が放出されない。この性質は、pHが典型的に酸性である感染組織での鉄の隔離を確実にし、病原性細菌による鉄の利用を防ぐ(Kell et al 2020)。
LFはヒトの自然免疫応答の構成要素であり、ウイルス感染時には、LFをコードする遺伝子の発現は、健康なコントロールと比較して、SARS-CoV-1患者において約150倍上昇することが判明した(Reghunathan et al 2005)。LFは、HIV、ジカウイルス、チクングニア、C型肝炎ウイルス、サイトメガロウイルス、ロタウイルスなどの広範なRNAおよびDNAウイルスに対して強力な抗ウイルス活性を有する(Martorellら.2016;Serrano et al 2020;Carvalho et al 2016;Berlutti et al 2011;若林 et al 2004;Wang et al 2018;Wrapp et al 2020;HofmannおよびPohlmann 2004)。)
LFの抗ウイルス活性は、ウイルスが宿主細胞を攻撃したときに特に起こり、LFはウイルスが宿主細胞に定着してから宿主細胞に侵入するのを防ぐので(Lang et al 2011)LFの抗ウイルス活性は、ウイルスが宿主細胞を攻撃したときに特に起こる。LFがヘパラン硫酸プロテオグリカン(HSPG)に結合することが報告されており、これは、共有結合したグリコサミノグリカン鎖で装飾されたコアタンパク質からなる細胞表面および細胞外マトリックス高分子である(Kell et al 2020)。HSPGは、宿主細胞膜上の予備的なドッキングサイトとして機能し、SARS-CoV-1が細胞内に侵入する過程で重要な役割を果たしている可能性がある(Lang et al 2011)。図3に示すように、LFはウイルスとHSPGを競合させることで、SARS-CoV-1の感染を阻害する(Lang et al 2011)。この作用機序により、ウイルスが細胞表面に濃縮されるのを防ぐとともに、特異的な侵入受容体(ACE2)への侵入を防ぐことができると考えられる。しかし、LFがACE2に結合するかどうかはまだわかっていない(Lang et al 2011)。LFは、SARS-CoV-1の場合と同様に、マイクロモル濃度で用量依存的にSARS-CoV-2の浸潤を阻害する可能性がある(Lang et al 2011)。しかし、SARS-CoV-2がHSPGに結合することは確認されておらず、SARS-CoV-2もSARS-CoV-1と同様にHPSGを介して宿主細胞に侵入するのかどうかについては、今後の検討が必要であると考えられる。
図3 SARS-CoV感染におけるラクトフェリン(LF)の保護的役割
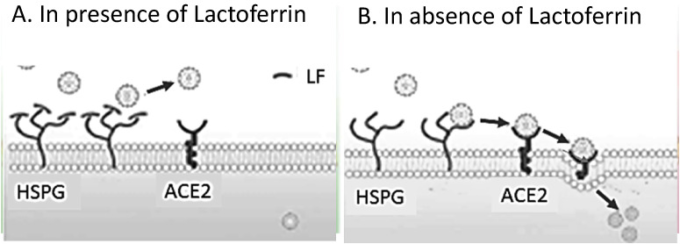
A)LFは細胞表面のヘパラン硫酸プロテオグリカン(HSPG)に結合することでSARS-CoVの感染を阻害する。
B)LFがない場合、HSPGによって提供されるアンカーサイトは、SARS-CoVと宿主細胞の間の初期接触を可能にする。SARS-CoVは特定の侵入受容体をスキャンし、それが後続の細胞侵入につながる。Lang et al 2011)より)改変された]。
LFは経口サプリメントとして入手可能であり、明らかな毒性を伴わない様々な適応症のために、1日100mgから4.5gまでの用量で乳児の栄養添加物として広く使用されている(Peroni, 2020)。LFを含む24の市販品のリストがあり、アメリカの企業アマゾンによって入手可能である。
風邪および/またはインフルエンザ感染症の症状を緩和するためのLFおよびLPO(LF+LPO)を含む吸盤の有効性を調べるために、無作為化非盲検並行群間比較臨床試験が実施された。治療群と非治療群(被験者全体407人)を、習慣的にフェイスマスクを着用している、手洗いをしている、うがいをしているなどのサブグループにさらに分類した(Shin et al 2018)。風邪、インフルエンザ感染症、胃腸症状の発症率と期間は、治療群と非治療群で統計的には差がなかった。(LF+LPO)錠は、保護マスクを着用していないサブグループにおいて、38℃以上の発熱の持続時間を有意に減少させることに中等度の効果があった(Shin et al 2018)。
遊離形態のLFは、塩酸および加水分解酵素の作用により胃内で分解される。カプセル化およびリポソーム化を含むLFの新しい製剤が探索されている。もう一つの興味深い観察は、亜鉛飽和ラクトフェリンがより強力な抗ウイルス効果を発揮することである。亜鉛の補給は、この疾患の治療的介入の可能性として提案されている(Zhang and Liu, 2020)ので、これはCOVID-19に特に関連している。リポソームウシ・ラクトフェリン(LLF)シロップ(LF32mg/10ml+アスコルビン酸12mg)と亜鉛溶液10mg/10mlを組み合わせた経口サプリメントを、IgM/IgG迅速検査陽性で自宅で自己隔離している症状のあるCOVID-19患者75名に10日間投与した。対照群にはLLFのみを投与した。1ヶ月間追跡調査したすべての患者は、治療開始から4~5日以内に症状が消失し、256人の家庭内接触者にLLFを半量投与したところ、SARS-CoV-2感染の予防に効果があった(Serrano et al 2020)。最後になるが、7人の著者のうち6人は、この試験で使用されたすべての治療薬の製造元であるSesderma Laboratoriesに勤務していた(Serrano et al 2020)。
上述したように、LF単独またはOSCN-との併用は、健康なボランティアおよび嚢胞性線維症に罹患した患者を対象とした第1相臨床試験(RCT02598999)で既に試験されている(Alaxia, 2020; Cegolon, 2020)。
3.3. N-クロロタウリン
N-クロロタウリン(NCT)は、毒性の強い次亜塩素酸とアミノ酸タウリンによって体内で生成される(HOCl+タウリン→NCT+H2O)ヒトの防御システムの天然酸化物の一部である(GotttardiおよびNagl 2010)。最近では合成によりNCTが得られ、大量に入手できるようになった。この化合物は、十分な殺菌力と良好な組織耐性との間の最適な妥協点を明らかにした。NCTは低温で長期保存が可能であり、細菌、真菌、寄生虫およびウイルス(単純ヘルペスウイルス1型;単純ヘルペスウイルス2型;アデノウイルス;インフルエンザウイルスAおよびHIV-1)に対して殺傷活性を有する。NCTは、内因性防腐剤として敏感な体の部位に適用することができる。眼、皮膚、粘膜、副鼻腔での忍容性は非常に良好であった。毒性の非常に敏感なパラメータである鼻粘膜の上皮細胞の毛様体拍動頻度は、1%のNCTによってのみ適度にかつ可逆的に減少した(Nagl et al 2018)。NCTの特別な応用分野は、様々な感染症の治療のための吸入である。オーストリアの2つのセンターで、試験群(1%NCTの吸入)と並行対照群(0.9%NaClをプラセボとして投与)を用いた第I相二重盲検無作為化臨床試験が実施された。被験者のうち、1秒目の強制呼気量(FEV1)は低下せず、血液分析ではベースライン値と対照群と比較しても異常は認められなかった(Nagl et al 2018)。全体的に、SARS-CoV-2から鼻咽頭をクリアにするNCTの有効性を示すエビデンスはない。
3.4. インターフェロンα
1957年にウイルス学者によって発見されたインターフェロンは、ヒトの抗ウイルス自然防御の一部であり、細胞代謝の阻害および適応免疫を刺激するサイトカインの分泌のダウンレギュレーションを含む異なるメカニズムでウイルスの複製および拡散を阻害し、抗ウイルス免疫において重要な役割を果たしている(Jakimovski et al 2018)。試験管内試験での調査により、SARS様コロナウイルス感染症に対するIFN-αの有効性が確認された(Zorzitto et al 2006)。動物実験では、IFN-α鼻腔スプレーがサルにおけるSARS-CoV-1感染関連の損傷を効果的にブロックまたは低減できることが確認されている(Enserink 2004;Gao et al 2005)。
SARS-CoV-2は、宿主細胞によるIFNの内因性分泌を阻害することができ、その結果、ウイルス感染を抑制する能力を減少させる(Cegolon et al 2020)。したがって、外因性IFNの使用は、COVID-19の重症型では重要である(Zhou et al 2020)。最近の非盲検プロスペクティブ研究では、組換えヒトインターフェロンα(rhIFN-α)の点鼻薬を、SARS-CoV-2パンデミック期の中国の医療従事者2944人に以下のように試験した(Meng et al 2020)。
- 「低リスク群」に含まれる2415名の被験者(医師997名、看護師1418名、それぞれ平均年齢37.38歳、33.56歳)にrhIFN-αを2~3滴/鼻孔/回、1日4回/日を28日間投与した。
- 529名(医師122名、看護師407名、平均年齢35.24歳、32.16歳)を「ハイリスク群」とし、tymosin-α11.6mgを週1回皮下注射するとともに、rhIFN-αを1日4回、28日間、2~3滴/鼻腔内に投与した。
28日目の時点でCOVID-19陽性の被験者はおらず、呼吸器症状を発症した被験者はいなかった(Meng et al 2020)。後者の研究は、クラスター化された無作為化試験ではなかったが、対照群は医療従事者で構成されていた。使用された対照群は、厳密に平行したプラセボ対照群ではなく、COVID-19肺炎に罹患した医療スタッフで構成され、文献で報告されている同時期のパンデミック地域から募集されたものである。また、現在の形の論文は、ピアレビューで認定されていない速報である。
IFNはCOVID-19からの上気道の消毒に効果があるように見えるが、その使用は、特にその可能性が高いコストを考慮すると、医療スタッフのような最前線の個人にはより適切であるかもしれない。プロトコルでは週1回のチモシンα11.6mgの注射も行われているので、IFNは一般人には実用的ではないように思われる。
3.5. ポリビニルピロリドンヨード
ポビドンヨードとしても知られるヨウ素入りポリビニルピロリドンポリマー(PVP-I)は、1955年に発見され、消毒剤として販売されている。
慢性鼻副鼻腔炎に罹患した患者から採取したヒト鼻上皮細胞培養物の気液界面を、最近、PVP-Iの0.5%溶液(Firebrick Pharma社からライセンスを受けたNasodine®)に試験管内試験で曝露した(Ramezanpour et al 2020年)。細胞毒性は、傍細胞透過性または繊毛ビート周波数には観察されなかった。培養細胞の経上皮電気抵抗は、Nasodine®に30分間曝露した後にのみ有意に減少した(Meng et al 2020)。その結果、PVP-Iは、洗口剤として使用したり、鼻から服用したり、眼科手術中に使用したりすると、安全な治療法と考えられる。
SARS-CoV-2に対する外用および経口PVP-I製品の試験管内試験での殺菌活性が最近報告された(Bidra et al 2020)。4つの製品(防腐液、10%のPVP-I;皮膚洗浄剤、7.5%のPVP-I;うがい薬および口内洗浄剤、1%のPVP-I;およびのどスプレー,0.45%のPVP-I)はすべて、ウイルスと接触してから30秒以内にSARS-CoV-2に対する≧99.99%の殺菌活性を達成した(Bidra et al 2020)。推奨されるIPC対策およびPPEに加えて、COVID-19の拡散リスクを最小化するために、医療従事者およびその患者の間で0.5%のPVP-Iの使用が提案された。PVP-Iを含むマウスウォッシュまたは鼻腔スプレーは、ウイルスの侵入地点での戦いと、口からの飛沫の放出を介したSARS-CoV-2感染の低減の両方に有効な戦略である可能性がある。
ポビドンヨード点鼻スプレー(Nasodine®)のヒトコロナウイルスに起因する可能性のある感冒患者を対象とした安全性と有効性を評価する第Ⅲ相臨床試験(ACTRN12619000764134)が進行中です(Firebrick Pharma Pty Ltd. 1261)。PVP-Iは、SARS-CoV-2に対する有効性が確認された臨床試験データが待たれている。
PVP-Iは有効な防腐剤ではあるが、妊婦や子供には最適ではないかもしれない。実際、ポビドンヨード系防腐剤で新生児の甲状腺機能低下症が報告されている。さらに、無症候性の母親との密接な接触を介した母乳育児中の乳児へのSARS-COV-2の感染が報告されている(Jafari et al 2020)。一過性高チロトロピン血症は、母親が分娩中および分娩後に皮膚消毒剤としてポビドンヨードに曝露された新生児で発生する可能性がある(Casteels et al 2000)。
3.6. ヒドロキシクロロキン
クロロキン(クロロキン)の毒性の低い誘導体であるヒドロキシクロロキン( ヒドロキシクロロキン)は、マイクロモル濃度でSARS-CoV-2に対する抗ウイルス活性が試験管内試験で証明されており(Liu et al 2020)その作用機序は、膜融合に不可欠なエンドソーム/リソソソームなどの細胞内小器官のpH上昇を伴う(Ashfaq et al 2011)。また、クロロキンはACE2受容体やスパイク蛋白質の糖鎖修飾を変化させることで、SARS-CoV-1の侵入を抑制する可能性がある(Savarino er al)。 誘導体 ヒドロキシクロロキンとともに、クロロキンは複数の臨床試験にまで進出している。SARS-CoV-2から鼻咽頭をクリアにする ヒドロキシクロロキンの有効性に関する証拠は比較的低く、1件の小規模なオープンラベル非ランダム化臨床試験のみに基づいているが、COVID-19患者の臨床的改善は確認されていない(Gautret et al 2020)。さらに、 ヒドロキシクロロキンは、グルコース-6-リン酸脱水素酵素の欠乏に関連したQTc延長および溶血という副作用のリスクを特徴としている(Tilangi et al 2020)。これに関連して、メイヨークリニックは、COVID-19患者に ヒドロキシクロロキンによる治療を開始する前にベースラインの心電図モニタリングを推奨している(Giudicessi et al 2020)。アジスロマイシンとの併用でもある ヒドロキシクロロキンの有効性は、ニューヨーク市メトロポリタン地域の25の病院に入院したCOVID-9患者1428人から無作為にサンプリングされた患者1428人の死亡率の有意な減少との関連性が認められなかったため、疑問視されている(Rosenberg et al 2020)。
最後に、 ヒドロキシクロロキンなどの経鼻抗菌薬は、この戦略が細菌/ウイルスの耐性株の開発の増加につながる可能性があるため、ヒトにおける微生物の不顕性コロニー化を減少させるために定期的に使用されないのが一般的である。
3.7. アルコールベースの鼻腔用消毒薬
SARS-CoV-2,SARS-CoV-1およびMERS-CoVは、アルコールへの曝露によって不活化することが比較的容易な親油性エンベロープウイルスである。エタノール62〜71%は、1分以内にSARS-CoV-1およびMERS-CoVからの菌体を殺菌するのに有効であることが既に証明されている試薬の一つである(Kampf et al 2020)。少なくとも60%エタノールを使用した消毒剤は、米国疾病対策予防センター(CDC)により、SARS-CoV-2に対する医療スタッフの手指衛生、および(泡/水が利用できない場合は)一般の人々にも推奨されている(CDC, 2020)。最近の研究では、30%以上の濃度のエタノールは、懸濁液中のSARS-CoV-2を30秒で効率的に不活化した(Kratzel et al, 2020)。さらに別の研究では、米国で販売されている2つの市販のアルコールベースの手指消毒剤(エタノール濃度70%のゲルと泡)で、懸濁液中のSARS-CoV-2を検出可能な閾値以下(3 log10以上の減少)で不活化できることが確認された(Leslie et al, 2020)。生理食塩水鼻水およびエタノール経口洗浄剤は、COVID-19の予防および制御のための潜在的な局所的対策として提案されている(Casale et al 2020)。
都市部の病院センターの医療従事者(Steed et al 2014)またはコロニー化した患者の間で、鼻腔内細菌運搬を減少させるためのアルコールベースの消毒薬の有効性を試験した2つの研究(Kanwar et al 2019)があり、しかしながら相反する結果を提供している。市販の非処方品であるNozin Nasal Sanitizerの防腐剤を、後者の研究で試験薬として使用した。安全性がテストされた製剤は、エタノール活性剤と天然オイルエモリエント剤と防腐剤ベンザルコニウム塩化物の混合物で構成されていた。0.017%のペパーミントオイルをマスキング剤として使用した無菌リン酸緩衝生理食塩水をプラセボ治療の対照として使用した。後者のアルコール系防腐剤を8時間かけて3回鼻腔内に塗布すると、医療従事者のS. aureusの鼻腔内感染が有意に減少した(Steed et al 2014)が、コロニー化した患者のそれぞれの減少は一過性であり、8時間後には有意ではなくなった(Kanwar et al 2019)。新竹は最近、容易に入手可能なアルコール飲料(ウイスキーや日本酒)から得られるエタノール蒸気を制御して吸入し、SARS-CoV-2からヒトの気道を消毒することを提案している(新竹 2020)。SARS-CoV-2に対するアルコール系鼻腔消毒薬の効果を検討するために、臨床研究を行うことが推奨されており、特に妊娠中の女性や小児などの脆弱な集団における忍容性を評価する必要がある。
3.8. 第四級アンモニウム化合物
第四級アンモニウム化合物(QAC)は、米国環境保護庁(EPA)がSARS-CoV-2を不活化するために現在推奨している200種類以上の消毒剤に含まれる有効成分である。家庭環境(パーソナルケア用洗剤、石鹸、液体手洗い洗剤を含む)職場、産業界でのQACの使用量は大幅に増加しており、COVID-19パンデミックの動向を考慮すると、その使用量は今後も増加していくと考えられる(Hora et al 2020)。
配合された洗剤によるSARS-CoV-2の不活性化は、ウイルス性に修飾された宿主細胞由来のリン脂質二重層糖質エンベロープ、および宿主細胞の感染においてACE2受容体と相互作用する関連するスパイク糖タンパク質の破壊の結果として起こると考えられている。別の作用機序は、内分泌細胞およびリソソームのpHの上昇を伴う(Hora et al 2020)。
テキストマイニングアプローチを用いて、Baker(Baker et al 2020)は、コロナウイルスに対する抗ウイルス活性を有する可能性のある以下の3つのクラスのQACを同定した。
- 塩化アンモニウム。代謝性アシドーシスを含む様々な用途。マウスコロナウイルスおよびC型肝炎に対するウイルス活性。
- 塩化セチルピリジニウム。防腐剤、洗口剤、パーソナルケア製品、洗浄剤などに使用されている。食肉や家禽製品の抗菌剤としても使用されているこの製品は、呼吸器感染症に対する治療薬として臨床試験で試験された(Mukherjee et al 2017)。塩化セチルピリジニウムは、インフルエンザ、B型肝炎、ポリオウイルス1に対して抗ウイルス活性を有する。
- ミラミスチン。HIV、インフルエンザ、単純ヘルペスウイルスおよびSARS-CoV-1に対する抗ウイルス活性を有する防腐剤。
塩化セチルピリジニウムやミラミスチンなどのQACは、SARS-CoV-2に対して試験管内試験または臨床試験ではまだ試験されていない。
COVID-19がもたらす明確で深刻な脅威は、感染の拡大を緩和して食い止めるための合理的な戦略としてQACの大規模な使用を促しているが、廃水処理装置の運転の中断、抗生物質耐性の増殖、ニトロサミン消毒副生成物の形成、および表流水の生物相への悪影響など、QACの潜在的な環境への影響も考慮しなければならない。QACの環境への放出を最小化するための潜在的な技術の探索は、大いに期待されている(Hora et al 2020)。
4. 結論
SARS-CoV-2に対する試験管内試験の殺ウイルス効果は,エタノール,アルコール系手指消毒剤,ポビドンヨードについては,これまでのところ報告されていない。他のコロナウイルスに対する試験管内試験阻害効果は、LF、 ヒドロキシクロロキン、エタノールおよびQACについて報告されている。SARS-CoV-2に対する治療法は、無作為化比較臨床試験では試験されていない。SARS-CoV-2に対する有効かつ安全な薬剤がないということは、主にこのトピックに関する関連文献が存在しないことを示唆している。
ほとんどの薬剤候補はすでに市場に出回っている。Bakerらによって指摘されているように、「単純に聞こえるかもしれないが、COVID-19に対する潜在的な治療薬を浴室の戸棚の中で探すべきだ、ということは十分にあり得る」(Baker et al 2020)。
鼻腔がSARS-CoV-2の主な侵入口である一方で、唾液の飛沫を放出することによるウイルスの出口として口も関連している。よく知られている手から鼻から手への感染サイクルは、感染制御のための適切な追加の方法を必要とする。
今回のスコープレビューでは、COVID-19の化学予防に関するトピックについて、利用可能なエビデンス以上に知識のギャップがあることが明らかになった。COVID-19パンデミック(Hurley, 2020)への対応にはスピードが不可欠であるため、特定されたすべての候補薬剤について臨床試験を実施することは、あまりにも過酷で時間がかかりすぎる可能性がある。
すべてを考慮に入れると、これらのデータは、コロナウイルススワブ検査で陽性者と陰性者の間で候補薬剤の使用を比較するケースコントロール研究を用いて、便利な非抗生物質製剤の探索を追求できることを示唆している。このような研究の結果は、その後の研究室や臨床研究の絞り込みに役立つ可能性がある。