SARS-CoV-2 and the next generations: which impact on reproductive tissues?
link.springer.com/article/10.1007%2Fs10815-020-01917-0
要旨
重症急性呼吸器症候群-コロナウイルス2(SARS-CoV-2)によるコロナウイルス疾患2019(COVID-19)は、主に呼吸器系に影響を及ぼす重篤な世界的パンデミックである。泌尿生殖器系にも注目が集まっている。本研究では、Human Protein Atlas, GTEx, FANTOM5などのオンラインリポジトリを用いて、ウイルスの侵入と複製に関与する可能性のある様々な宿主分子の発現パターンをヒトの女性生殖器系および男性生殖器系で調べた。その結果、SARS-CoV-2は、ウイルス侵入に必要な受容体(ACE2)とプロテアーゼ(TMPRSS)を共発現していることから、男性生殖器組織、特に精巣を標的とする可能性があることが明らかになった。我々は、SARS-CoV-2感染が男性個体の受胎状態に影響を及ぼす可能性があると仮説を立てた。 生殖組織におけるSARS-CoV-2の潜在的な感染性は、現在および将来の世代における生殖医療および体外受精の管理において考慮されるべきである。
重症急性呼吸器症候群-コロナウイルス2(SARS-CoV-2)によるコロナウイルス疾患2019(COVID-19)は、劇的な世界的パンデミックと広く考えられている。
COVID-19は、まず、喉の痛み、鼻漏、咳、呼吸困難から、肺炎および病理学的胸部X線特徴を伴う急性呼吸窮迫症候群に至るまでの呼吸器症状を特徴としている[1]。その他の特異的でない症状としては、発熱、筋肉痛、頭痛、リンパ球減少、C反応性蛋白の増加、低汗、および低吐息がある[1]。それにもかかわらず、新たな知見により、他の臓器がSARS-CoV-2に感染する可能性があることが明らかになった;実際、ごく一部の症例では下痢、吐き気、嘔吐が報告されており、消化器系の関与を示唆している[1]。さらに、COVID-19患者における蛋白尿および急性腎尿細管障害は腎障害を示しており[2]、トロポニンTおよびN末端プロB型ナトリウム利尿ペプチドレベルの上昇は心血管障害の可能性を強調している[3]。
科学界は現在、SARS-CoV-2ウイルスの特徴の研究、およびCOVID-19疾患の発症につながるメカニズムの研究に焦点を当てている。さらに、可能性のある治療法やワクチンを発見するための努力が続けられている。そのため、これまでのところ、SARS-CoV-2感染とその後遺症が男性および女性の生殖器系に与える影響を調べた研究はほとんどなく[4, 5]、また、生殖医療の観点からもその結果がどのようなものであるかは不明である。
まず、ヒトの生殖器系に焦点を当て、ウイルスの侵入・増殖に関与することが既に知られている主要なタンパク質(mRNAの発現も)を探し、その関与が試験管内試験(in vitro)実験で実証されている科学的文献をレビューした。アンジオテンシン変換酵素2(ACE2)はウイルス侵入の主要な受容体として広く認識されており[6, 7]、特にACE2とレニン-アンジオテンシン系(RAS)の両方がヒトの妊孕性に基本的な役割を果たすことが知られている[8]が、SARS-CoV-2の病原性を誘発するためには他のアクターが必要である。SARS-CoV-2は、ウイルスエンベロープと細胞膜との融合を可能にするために、タンパク質スパイク(S)プライミングが必要であり、このプロセスは、II型膜セリンプロテアーゼ(TMPRSS)2、4、11A、11D、および11Eなどの宿主プロテアーゼによって媒介される[6、7]。さらに、エンドソーム動態に関与するホスファチジルイノシトール3リン酸5キナーゼ(PIKFYVE)、リソソームに作用する2つの細孔チャネルサブタイプ2(TPCN2)、カテプシンL(CTSL)、カテプシンB(CTSB)などがSARS-CoV-2の侵入に必要な分子として提案されている[6,7]。
上記分子の雌雄生殖組織での発現パターンを調べることを目的として、タンパク質産生と遺伝子発現プロファイルの両方を報告しているヒトタンパク質アトラスデータベース(www.proteinatlas.org)のデータバンク検索とインターログ、トランスクリプトーム所見を記録している遺伝子型-組織発現(GTEx)(www.gtexportal.org)と哺乳類ゲノム5(FANTOM5)(https://fantom.gsc.riken.jp/5/)のリポジトリのインターログを行った。宿主細胞への SARS-CoV-2 の侵入機構に関する先行文献データに基づき、以下の分子を検索した。ACE2;TMPRSS 2、4、11A、11D、および11E;PIKFYVE;TPCN2;CTSL;CTSB、女性(膣、卵巣、卵管、子宮内膜、子宮頸部)および男性(精巣精管、精巣上体、精液小胞、前立腺)の生殖組織における。
我々の観察結果は、補足資料の表1、表2、表3、図1を参照することができる。
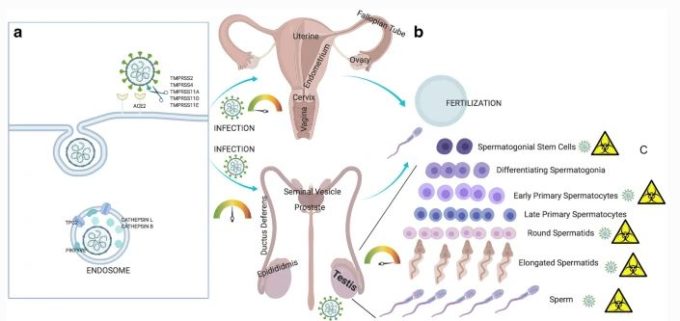
図1
生殖器系における潜在的なSARS-CoV-2感染の模式図。A)細胞内へのウイルスの侵入、関与する可能性のある宿主因子を強調している。B)女性(感染リスクが低い)および男性(感染リスクが高い)生殖器系におけるSARS-CoV-2の潜在的な感染性。C)ACE2とTMPRSSの共発現に基づく精巣細胞の潜在的な感染性(ウイルス画像とハザードアイコンは高リスクの細胞を示している
興味深いことに、ACE2のタンパク質発現は精巣(精管細胞とライディッヒ細胞の両方)で高く、精液小胞の腺細胞では低かった。その代わり、精巣上体、精巣小胞、前立腺ではTMPRSS2が、精巣、精巣上体、前立腺ではTMPRSS4が、精巣小胞ではTMPRSS11Dが発現していることが明らかになった。このことから、精巣や精液小胞には、受容体とほぼ1つのプロテアーゼの共発現が認められ、SARS-CoV-2に感染する可能性があることが示唆された。
女性生殖器では、ACE2タンパク質の存在を示す組織はなく、TMPRSS2についても同様であったため、これらの組織はSARS-CoV-2に感染していないと考えられた。
その他の因子については、PIKFYVEについてはデータがなく、TPCN2とCTSBは雌雄ともにほぼ産生されていたが、CTSLは検出されていないか、低レベルに存在していた。
驚くことではないが、トランスクリプトームデータベース(GTEx, HPA, FANTOM5)を見ると、報告されている情報は異なっていた。
ACE2 RNAの発現は、検査したすべての生殖組織に存在し、精巣では高レベルで、前立腺、膣、卵管、子宮内膜、子宮頸部では低レベルであった。TMPRSS2 RNAもすべての生殖組織で観察されたが、男性組織、すなわち精巣精管、精巣小胞、前立腺で主要な発現を示した。TMPRSS4, 11A, 11D, 11Eの発現量は、各組織ではそれほど目立たなかったが、膣と子宮頸管では多く発現していた。最後に、PIKFYVE、TPCN2、CTSL、CTSBは男女ともに異なる生殖組織に遍在していた。mRNAの発現所見のみを考慮すると、SARS-CoV-2は男性および女性の生殖組織すべてに感染する可能性があることが示唆された。
SARS-CoV-2の好ましい標的であると考えられる肺では、ACE2のmRNA発現が低い(3つのデータセットのコンセンサスは17.9と0.8。精巣では 17.9、肺では 0.8 の正常化発現 NX)。)
ヒトプロテインアトラスの検索に基づいて報告されたタンパク質データは、半定量的な免疫組織化学実験によるものであり、定量的なプロテオミクス(ウエスタンブロットやELISAなど)によるものではないことに注意が必要であり、低分子量に対する感受性の欠如が仮説として考えられる。そのため、タンパク質とRNAのデータに不一致が見られ、転写後の変化も排除できなかったのではないかと推測される。
この問題をさらに調べるために、COVID-19 Cell Atlas (www.covid19cellatlas.org)を用いて、精巣内の異なる細胞集団、すなわち、分化精子母細胞、初期初代精子母細胞、伸長精子母細胞、内皮細胞、後期初代精子母細胞、ライディッヒ細胞、マクロファージ、筋様細胞、丸い精子母細胞、セルトリ細胞、精子、精子、造精幹細胞を調べた。最大発現量のデータは、補足資料の表4および図1に報告されている。
興味深いことに、低レベルでは、すべての細胞でACE2 mRNAの発現が観察されており、具体的には、分化精子母細胞、初期初代精子母細胞、伸長精子母細胞、内皮細胞、後期初代精子母細胞、ライディッヒ細胞、マクロファージ、筋様細胞、円形精子母細胞、セルトリ細胞、精子、造精子幹細胞であった。一方、TMPRSS(2、4、11A、11D、11E)は、伸長精子、精子、および造精幹細胞によってわずかに発現された。最後に、PIKFYVE、TPCN2、CTSL、およびCTSB mRNAは、精巣のすべての異なる細胞タイプで報告されている。これらのデータは、精巣、精子、造精子幹細胞がSARS-CoV-2感染に対する感受性の潜在的なリスクを提示すべきであることを示唆している。
精巣のトランスクリプトームを解析したところ、ACE2陽性精子はACE2陰性精子と比較して精子形成に関連する遺伝子の発現数が多く、ACE2陽性のライディッヒ細胞やセルトリ細胞(TMPRSS遺伝子を発現しない)ではミトコンドリアや生殖に関連する遺伝子のmRNAの発現量が少ないことがわかった。このことから、著者らは、精巣のSARS-CoV-2感染に対する脆弱性が精子形成障害を引き起こす可能性があると推測している[9]。同様に、精巣や精子嚢でもACE2のmRNAやタンパク質の発現が観察された[10,11]。また、精巣幹細胞、分化精巣、レプトテン精子細胞1型、レプトテン精子細胞3型、頬腺精子細胞、ジロテン精子細胞、ディプロテン精子細胞、精子母細胞7、精子嚢1期、セルトーリ細胞もSARS-CoV-2感染の影響を受けやすいと考えられている。精巣はTMPRSS2、CTSL、CSTBも発現しており、脆弱性の仮説を裏付けている可能性がある[12]。
逆に、ヒト精巣組織のscRNAseqデータセットでは、ACE2とTMPRSS2を共発現している精巣幹細胞はごくわずか(0.05%)であった[13]。
COVID-19患者の精液中にSARS-CoV-2が存在することについては、これまでにいくつかの研究が行われている[14]。COVID-19の診断から中央値で31日後の単一射精サンプルのqRT-PCRは陰性であったが、特に19%の感染者は陰嚢の不快感を経験しており、これはウイルス性睾丸炎の徴候である可能性があるが、泌尿器科の精密検査は行われていない[15]。同様に、ある患者の精液からは、鼻咽頭スワブ陽性から9日後にウイルスRNAは検出されなかった[16]。とはいえ、これらは予備的な報告であり、2番目の論文は1人の患者を対象としたものである。また、診断後の精液採取の時期が、患者が急性疾患から回復しかけていたことも、陰性の結果に影響を与えた可能性がある。実際、COVID-19患者6人(15.8%)の精液からSARS-CoV-2が検出されたが、そのうち4人は急性期、2人は回復期であり、ウイルスの存在は男性生殖器周辺の血液バリアの障害によるものである可能性があるが、精液中に検出されたウイルス症につながる装置内に滞留している可能性がある;したがって、著者らはSARS-CoV-2の性感染の可能性と想定される予防策について警告している[17]。
様々なオンラインツールを用いて得られた我々の観察から、男性の生殖組織、特にウイルス侵入に必要な受容体とプロテアーゼを共発現する精巣がSARS-CoV-2の影響を受ける可能性があることが示唆された。これまでのところ、このテーマに関する研究はほとんど行われておらず、試験管内試験(in vitro)や生体内試験(in vivo)の動物モデルで精子へのウイルスの影響を調べた研究はなかった。その後、感染が個体の受胎可能性に与える影響を明らかにし、証明する必要がある。SARS-CoV(2002年発生)は、生殖腺にダメージを与える炎症・免疫学的宿主反応を誘導して睾丸炎を促進したと考えられる[18]が、ACE2がSARS-CoVとSARS-CoVの両方のエントリーレセプターであることを考えると、新型コロナウイルスも同様の作用をする可能性を排除できない[1]。
女性の生殖組織については、女性組織ではACE2の発現が低いことが確認されている。
最近、霊長類の卵巣細胞でACE2とTMPRSS2の共発現が観察されているが、積雲細胞ではACE2が多量に確認されたが、TMPRSS2はわずかに存在していた[13]。子宮内膜では、ACE2 の発現が低く、TMPRSS2 の発現が中程度、TMPRSS4、CTSL、CTSB の発現が高いことが報告されており、さらに、上記のすべての遺伝子は月経周期の分泌期に向かって増加していることが示された[19]。これらの所見は、女性の生殖組織においても、SARS-CoV-2感染に対する感受性は低いものの、潜在的な可能性を示唆している。
一方で、母親から胎児への垂直伝播のリスクについては、議論の余地がある。実際、SARS-CoV-2陽性の新生児は主に無症状であり[20]、免疫グロブリンIgGおよびIgMが陽性であることを示す症例報告は数例のみである[21, 22]。
今回報告された情報は、in silico トランスクリプトーム解析およびプロテオーム解析に基づくものであることを認識し、生殖組織からの細胞への SARS-CoV-2 の潜在的な影響をさらに深める手がかりとなるだろう。精液中にウイルスRNAが検出されたが [17]、ウイルスの複製サイクルが精巣や関連臓器で起こるのか、あるいは、SARS-CoV-2は血液中で定量化されていないので [23]、最後の選択肢は除外できるが、ウイルスの存在が血液バリアの障害の結果だけであるのかは評価されていない。興味深いことに、私たちは、精巣の特定の細胞、すなわち精母細胞幹細胞、精子嚢、精子動物にACE2とTMPRSSsが共発現していることに注目し、SARS-CoV-2の推定標的となることを提案した。おそらく、SARS-CoV-2感染が個人の受胎可能な状態に及ぼす可能性のある影響、特にCOVID-19が受胎可能な対象者に発生した場合には、過小評価されている可能性があり、緊急に再評価される必要がある。生殖医療に携わる医師や研究者は、SARS-CoV-2が男性の生殖組織に感染し、複製する可能性があり、最終的には精液の感染性に影響を及ぼす可能性があることを考慮すべきである。また、生殖医療センターで採取された精液中のSARS-CoV-2の存在を分子的に評価し、体外受精を延期する可能性についても検討することは合理的である。最後に、卵子予備能が低下しており、妊娠の可能性が限られている高齢女性のケースを評価することが重要である。このような女性に対しては、慎重かつ適切な予防・治療法、例えば、女性が陽性の場合には、2003年にSARS-CoVに感染した人の記憶B細胞から分離されたSARS-CoV-2に対するヒトモノクローナル抗体[24]やワクチンの使用が可能になった場合の使用など、慎重かつ適切な予防・治療法の導入を検討すべきである。
