Contents
オンライン公開 2021年1月1日
pubmed.ncbi.nlm.nih.gov/33390779
PMCID:PMC7738953
PMID:33390779
要旨
近赤外(NIR)光治療,すなわち光バイオモジュレーション治療(PBMT)は、眼科における治療応用のための新しい科学的アプローチとして、近年世界的に根強い注目を集めている。このようなNIR療法の治療への応用は、シトクロムcオキシダーゼによる光神経調節の発見や治療生化学的プロセスの解明など、光生物学や生体エネルギー学の分野における著しい進歩が大きな推進力となっている。
経頭蓋照射により、NIR光はチトクロム酸化酵素とスーパーオキシドジスムターゼ活性を著しく増加させることが示されており、代謝と抗酸化の有益な効果を誘導する役割を示唆している。さらに、NIR光はヒトの脳血流と認知機能を副作用なく高める可能性もある。
本総説では、視覚および神経疾患の治療における新たなパラダイムとしてのNIR療法の価値を強調し、眼疾患における分子および細胞メカニズムに重点を置いて、NIR療法の使用を支持する科学的根拠を示す。
キーワード 近赤外光、光バイオモジュレーション療法、メカニズム、眼疾患
はじめに
光は、粒子と波のような性質を持つ電磁放射の一形態である。電磁波は一方向のベクトルを持ち、波長(λ、連続するピークの距離)、周波数(1秒あたりの振動数)、振幅(谷とピークの差)によって特徴づけられる。電磁放射のエネルギー粒子には光子も含まれ、光子は毎秒3×108mで移動する。そのため、混合波にはさまざまな振幅と周波数で移動する光子が散乱・吸収され、生体物質など多くの物体で反射される。このエネルギーをどのように利用するかについて、より多くの研究が行われるにつれて、医療治療への光の応用は世界的に劇的に進歩した。例えば、レーザー治療は現在、特定の専門分野で一般的な治療法となっており、副作用のない多くの慢性疾患に有効であることが示されている。
近年では、遠赤(FR)から近赤外(NIR)のスペクトル範囲(~600~1000nm)の低レベル光治療が、光バイオモジュレーション(PBM)と総称され、様々な病状における実験的治療応用のための新しいツールとして世界的に注目されている。例えば、医学的疾患へのPBMの応用では、細胞保護因子をアップレギュレートし、損傷から保護することによって、損傷したミトコンドリアの機能を回復させることが示されている1。これらの知見は、レーザー治療が炎症を抑制し、さまざまな組織の免疫反応や創傷治癒を促進する可能性を示唆している(総説2)。
本総説では、この治療法の歴史、分子・細胞・神経組織レベルで現在提唱されているNIR光の作用機序、光バイオモジュレーション治療(PBMT)の臨床的適応と応用、臨床研究の結果、眼疾患におけるPBMTのその他の潜在的利益について簡潔に述べる。
近赤外光、LED、PBMT、レーザー
光の明るさと色は、光子の数と各光子のエネルギーによって決まる。近赤外光治療は、赤から近赤外までの波長のレーザーや発光ダイオード(LED)から、指向性のある低出力だが高フルエンスの単色または準単色の光を照射し、生物学的機能を媒介したり、安全な方法で治療効果を促進したりするものである3,4(5にも総説あり)。
レーザーとは、理論的には電磁波放射の刺激による光増幅によって発光する装置と定義される。レーザーの語源は、Light Amplification through Stimulation of Emission Radiationの頭文字からきている。最初のレーザーは、1960年にヒューズ研究所のセオドア・H・マイマンによって発明された。開発後、レーザーは、低照度療法、低レーザー療法、光線療法またはPBMTなどの医療療法としてますます使用されるようになった。
PBMTは、広帯域光、レーザー、可視または赤外スペクトルのLEDなどの非イオン化光源を用いた光治療の一種である。PBMTは、赤色から近赤外領域の波長のLEDによる低出力だが効果的な単色光を使用し、副作用なしに生物学的事象や治療効果を媒介する3,4。PBMTは、光によって誘発されるストレス、炎症、細胞死を軽減することで網膜変性症から保護すること6、黄斑変性症におけるコントラスト感度と視力を促進すること7、貪食作用を高め、活性酸素種の産生を減少させること8、糖尿病性網膜症における構造的・機能的損傷を減少させること9が示されている。
NIRとLEDの光は、光受容体のシトクロムc酸化酵素を活性化し、エネルギー代謝の上昇、創傷治癒の促進、毒性の抑制につながる(総説10)。NIR光の応用は、光エネルギーを代謝エネルギーに変換し、細胞の生物学的機能を修正することである。レーザーによる高エネルギー光子が生体組織や細胞を加熱・破壊するのに比べ、NIR光は電磁放射のエネルギーレベルが波長と負の相関関係にあるため、低レベルである。さらに、NIR光から照射されるエネルギーは、加熱や組織破壊を引き起こさない程度に低いが、細胞や組織の機能を媒介するには十分な高さであるため、通常、組織は低照度でターゲットとされ、副作用を引き起こさない。例えば、光線力学的療法は副作用を伴わずに皮膚症状への応用に使用されており11、神経細胞における電気的光神経調節は熱的影響を伴わずに得られる12。臨床的には、赤色から近赤外波長に対応する治療用光学ウィンドウは、生体内で感受性細胞内分子の励起を促進する光エネルギーと一致する13。そのため、NIR光は近赤外光治療と呼ばれている。これは、生体細胞や組織内の一部の分子が光子を吸収し、光によってシグナル伝達経路が開始されるという理論に基づいている14。その結果、特定の分子が光によって励起され、電子的に励起された状態に達するというエネルギー変換が起こり、その結果、分子のコンフォメーションや機能が変化し、細胞代謝を媒介するシグナル伝達経路が活性化される。従来のレーザーの高エネルギーとは対照的に、甚大な加熱、アブレーションによる組織破壊、凝固、剥離、蒸発などの破壊的効果は起こらない。
近赤外光リソース
地球上では、電磁放射の主な供給源は太陽光による太陽エネルギーである。太陽エネルギーは電磁スペクトルの複数の波を含んでおり、例えば可視スペクトルの波長は多方向で、時間的にも空間的にも同期していない。これに対し、近赤外光は単色であるため、分子バイオモジュレーションにおいて高い特異性を発揮する。近赤外光は、LEDアレイやレーザーによって得ることができ、目のPBMに応用されている。レーザーは、組織への高い浸透を可能にする効率的なコヒーレント光エネルギーを生成することができ、そのような一定のビームは、外接領域にエネルギーを供給する。レーザーからのビーム幅は、光ファイバーに結合することで増強され、より広い範囲にエネルギーを分配することができる。LEDは、波長4~10nmの効率的な光を発生させることができるが、コヒーレントではない。それにもかかわらず、LEDはごくわずかな熱しか発生させないため、熱による損傷は起こりえない15。さらに、LEDは人間工学的な機能を備えたアレイに連結することができ、例えば脳のような広い領域に効率よくエネルギーを供給することができる。実際、LEDは人体実験で評価され、FDAの認可を受けている16。
近赤外光受容体とターゲット
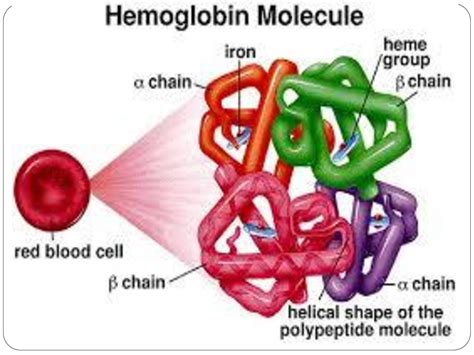
近赤外光は生理学的・病理学的に様々な変化を引き起こすため、光は生きた細胞や組織にある特定の受容体に作用するのではないかと長い間考えられてきた。例えば、動物のオプシンは光を吸収し、光受容体内で光伝達を誘導する。光受容体には、哺乳類の細胞に存在する特殊な光受容体と非特殊な光受容体がある。ヘモグロビン、メラニン、オキシヘモグロビン、水は幅広い波長の光を吸収する。600-1000nmの波長域では、吸収曲線は最小であり、特定の光受容体を活性化するための光の窓を提供している。実際、細胞は遠赤(FR)から近赤外(NIR)までの光に感受性があり、細胞の代謝、増殖、移動の変化によって光線治療を促進することができる。例えば、628nmの光を3日間照射すると、ヒト線維芽細胞では、シトクロムcオキシダーゼ17の活性化により、ミトコンドリア呼吸遺伝子と抗酸化遺伝子がアップレギュレートされ、アポトーシス遺伝子とストレス関連遺伝子がダウンレギュレートされる。問題は、NIR光による効果的な治療のために、細胞内のどの分子が活性化されたかということである。赤色と近赤外領域の波長が効果的な光生物学的治療に関与していることが推測される。もう一つの例は、哺乳類組織のヘモグロビンに存在する光受容体で、酸化還元状態によって光の吸収に差があるため、臨床応用においてヘモグロビンの定量化や酸素化を可能にしている。ヘモグロビン以外の赤色および近赤外域の光受容体は、ヘム含有金属タンパク質、例えばシトクロムcオキシダーゼやミオグロビンである。シトクロムcオキシダーゼは、赤外から近赤外域の光によって活性化され、細胞に変化を引き起こす16,18。さらに、カタラーゼ、クリプトクロムスーパーオキシドジスムターゼ、シトクロムc、シトクロムb、グアニル酸シクラーゼ、一酸化窒素合成酵素などの他の分子も光受容体を持っている15。
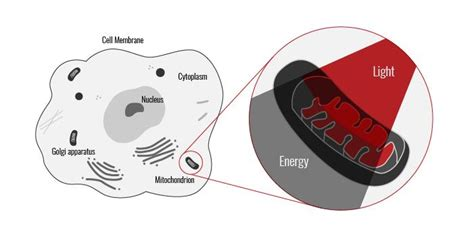
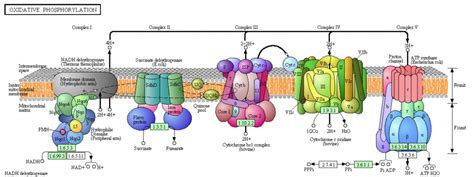
多くの光受容体が発見されているが、多くの分子が光受容体の機能を持つため、近赤外光のメカニズムは未だ不明である。また、特定の有効波長に対する分子標的の反応は複数存在する可能性がある。例えば、フラボタンパク質やNADH-デヒドロゲナーゼは、紫から青だけでなく、赤や近赤外のスペクトル領域にも光受容体を持っている18。さらに、末端オキシダーゼとスーパーオキシドジスムターゼはともに670-680nmの高波長に吸収ピークを持ち、異なる光受容体の吸収スペクトルで重なっている18,19。このことは、ある生物学的効果に対する他の光受容体の影響を排除できないことを示唆している。興味深いことに、NIR光による生物学的効果を媒介する重要な光受容体を特定したのは、神経系に関する研究が初めてである。単離されたミトコンドリアは、赤から近赤外スペクトルの単色光の照射に反応する。光はミトコンドリア膜電位を促進し、ミトコンドリアによるATP交換、RNAおよびタンパク質合成を促進し、酸素20の使用量を増加させる可能性がある。NIR光によるミトコンドリアへの影響は波長特異的であり、生体細胞内でNIR光を吸収する分子は呼吸成分である可能性が高い21。ミトコンドリアの光受容体に関するさらなる研究は、作用スペクトル解析-近赤外光に対する生物学的応答を波長の関数として記述する-によって行われてきた。例えば、HeLa細胞におけるRNA合成は、ある波長では促進されるが、他の波長では促進されない。一般的に言えば、最大効果を誘発する波長は有効波長の範囲に見出すことができ、これはNIR光による光受容体を介したシグナル伝達を特定するのに役立つ。実際、作用スペクトルのバンドはミトコンドリアのチトクロム酸化酵素18の吸収スペクトルにある。シトクロム酸化酵素は、電磁スペクトルの赤色および近赤外領域の光の主要な光受容体として同定されており22,23、網膜や脳の神経細胞における細胞生体エネルギーの重要な酸化酵素である24。シトクロムオキシダーゼは、ミトコンドリアの電子伝達系360の主要酵素であり、シトクロムcから酸素への電子伝達を触媒し、真核細胞が取り込む酸素の約95%を還元する。シトクロム酸化酵素はまた、酸化還元結合型プロトンポンプとして膜貫通電気化学的勾配の形成を促進し、エネルギーを貯蔵するATPを合成する律速段階としても働く25。シトクロム酸化酵素は、神経細胞やフリーラジカル代謝、アポトーシス過程、グルタミン酸作動性調節に関与している26,27。シトクロム酸化酵素活性は神経細胞の機能と強く関連しており、神経細胞内の代謝活性の特異的なマーカーである27。さらに、シトクロム酸化酵素は、逐次照射の分析により、最終形ではなく中間形の一次光受容体のみである可能性がある28,29。酸化状態の異なるチトクロム酸化酵素の吸収スペクトルは、近赤外光の生物学的応答における作用スペクトルと平行である28。
近赤外光の効果と応用
NIR光の線量測定は、低線量では生物学的プロセスが促進され、高線量では生物学的プロセスが抑制されることを特徴とする、ベル型、U字型、または二相性の曲線を持つホルミシス学的線量反応である。ホルミシス曲線は、薬理学的閾値30下での生物学的応答を正確に予測する上で、線形曲線よりも優れている。NIR光による刺激反応は軽度であり、対照を30%~60%上回るため、これは非常に重要である。対照的に、従来の用量反応は通常数倍に増加する。ホルミシスの用量反応は、様々なNIR光応用においてよく知られており、低エネルギー密度(0.001 J/cm2)または高エネルギー密度(0.10 J/cm2)において、それぞれ光刺激性または光抑制性の効果を示すからである31。所望の治療結果を得るための線量範囲で、ポジティブな反応を得ることができる16,32,33。
潜在的な医療用途におけるNIR光の有用性を理解するために、NIR光の効果と応用例を挙げる。例えば、低エネルギーのルビーレーザー34や、685nmや830nmの光を発生するガリウムレーザー35の下では、ラットの皮膚に創傷治癒が現れる可能性がある。脊髄損傷は、ラットの810nmの光で改善された36。NIR光は、歯肉切開37、口腔粘膜炎38、皮膚潰瘍39、創傷治癒40、神経修復41~43、手根管症候群44、45、軟部組織損傷46の治療に有益であった。炎症は光ストレスを受けた網膜に現れる可能性がある47-49。ミクログリア阻害剤ナロキソンによる抗炎症は、網膜の視細胞変性を減少させる可能性がある50,51。LED前処理は、活性酸素合成とアポトーシスを抑制し、エネルギー代謝を促進することで、シアンが誘発するアポトーシスからニューロンを保護する可能性がある52。最近、670nmの赤色光は、多くの研究論文によって、野生の医療応用の可能性があることが明らかになった。例えば、670nmの光は、シアン化合物16の治療下で神経細胞を保護し、ラットの視細胞を保護し、霊長類の網膜の創傷治癒を促進し53、ミトコンドリア代謝を増加させ、網膜の炎症を減少させ、おそらく呼吸鎖複合体I、II、IVによってチトクロムcオキシダーゼを標的として酸化細胞ストレスを軽減し、ミトコンドリアのエネルギー代謝を改善させる54。670nmの赤色光は、光による損傷6や毒素に対する強力な神経保護剤である55。670nmの赤色光を照射すると、ミトコンドリアの膜電位が上昇し、網膜の炎症が抑制される56。670 nmのLEDは、黄斑変性症モデルマウスにおいて、神経網膜の炎症と自然免疫を抑制することができる59。活性化されたシトクロムcオキシダーゼによる酸化の改善を通じて、ミトコンドリアのパフォーマンスが向上し、炎症が抑制されることが実証されたように、老化した網膜ミトコンドリアの呼吸は670nmの光によって改善される。老化した網膜は、わずか5分以内に670nmの光によって酸化が漸増することがある61。670nmの光は、酸化ストレスマーカーの発現を減少させ、高酸素状態での減少を示す62。670nm光の前処理は、脂質過酸化を減少させ、網膜変性における補体伝播を減少させることができる63。低レベルの670nmの光は、酸素誘導による網膜症や過剰な酸素による肺障害を予防し64、炎症、酸化代謝、アポトーシスに関わる遺伝子の発現を調節する65。正確なメカニズムは不明だが、シトクロムcオキシダーゼが主要な光受容体66として働き、酸化的代謝67とATP産生18を促進し、おそらくシトクロムcオキシダーゼの増加とアクロレイン発現68の減少に関連し、修復・保護メカニズムを駆動していることを示唆する強力な証拠がある。実際、網膜疾患33、脳卒中69,70、神経変性5、神経筋障害71、発毛72、記憶73、気分障害74に効果がある可能性が、豊富な研究結果によって裏付けられている。
近赤外光治療で考えられるメカニズム
シトクロム酸化酵素は主要な近赤外光受容体であり、酸化的代謝の鍵となる酵素であるため、眼や脳にとって特に有益である。目と神経細胞は、その代謝をシトクロム酸化酵素に依存している。NIR光の効果には、一次効果(光照射中)と二次効果(光照射後)がある。一次的効果とは、光によって活性化された視細胞における即時的な光化学変化のことである。したがって、これらの効果は光に依存している。例えば、呼吸鎖の酸化還元変化はNIR光によって誘発され、シトクロム酸化酵素による酸化を促進し、ベル型の用量依存的な細胞反応につながる4。
近赤外光はまた、シトクロム酸化酵素によるシトクロムcの酸化を促進し、酸素の使用量の増加、ミトコンドリア膜の感度の上昇、ミトコンドリアの孔の伝染性を誘導することができる18,19。これらの効果は、ミトコンドリアの電子輸送鎖における電子流の増加によって引き起こされる。さらに、NIR光は、光線力学的作用による一重項酸素と電子の自動酸化によるスーパーオキシドイオンによって、フリーラジカルを生成することができる。
さらに、近赤外光は電気振動や光振動によって発色団に一過性の熱を発生させることがある18。このような振動は、標的組織内の様々な分子に影響を与える可能性がある。NIR光はまた、エネルギー移動を促進する水素を強化する可能性がある。
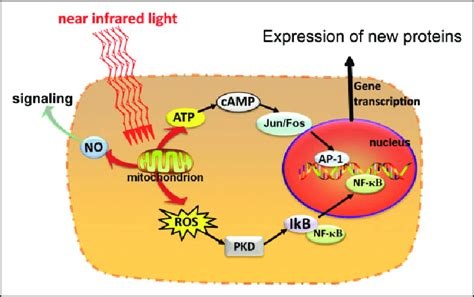
NIR光による二次的な作用は、一次的な作用の結果として現れることがあり、例えば、細胞の恒常性に影響を与える生化学的・生物学的反応などがある。NIR光は、光受容体が活性化され、核に移動し、遺伝子発現が変化するシグナルをミトコンドリアから核に送ることで、ミトコンドリアから核への様々なシグナル伝達経路を開始する可能性がある。詳細には、近赤外光はミトコンドリアのNAD/NADH比の有益な変化を促進し、活性化されたチトクロム酸化酵素による一酸化窒素の放出を誘導し、ATPレベルを媒介する。そして、ATPはP2受容体を活性化し、内向きカルシウム電流をカスケードさせ、細胞内貯蔵庫からのカルシウム放出を促進する77。このようなATPの変化はcAMPのレベルを調節し、様々なキナーゼの活性化を引き起こして遺伝子発現を変化させ、炎症や創傷治癒を制御する可能性がある。
PBM(低照度療法)は、約50年前から認知されている。しかし、その細胞および分子メカニズムはまだあまり明らかではない。近年、PBMにおけるシトクロムc酸化酵素の重要性に関する研究が相互に注目されている。
第一の仮説は、微弱光の刺激により、光子がこの酵素から抑制性一酸化窒素の解離を促進し、電子輸送とATP産生を促進し、ミトコンドリア膜とATP産生を増強し、転写因子の発現を促進し、遺伝子発現、タンパク質合成、様々な細胞および組織機能を促進するというものである(総説13)。
低エネルギーのNIR光による光子照射によるPBMは、数十年前から軟部組織の損傷や創傷治癒の治療に臨床応用されてきた歴史がある。NIR光は、脳、心臓、脊髄などの組織に浸透し78,79、虚血性心損傷の治癒を促進し78、損傷した視神経や網膜の変性を抑制し3,78、脳卒中の回復を促進する79–81。NIR光によるこれらの効果は、チトクロム酸化酵素15の吸収スペクトルと明らかに関連している。近赤外光はチトクロム酸化酵素の酸化還元変化を引き起こし、細胞内シグナル伝達を活性化してミトコンドリア機能を積極的に仲介し、細胞保護因子の過剰発現によって細胞内を保護する3,16,52,79,82-85。NIR光はまた、抗酸化物質や細胞保護因子の発現と蓄積を促進することができる55。例えば、遺伝子プロファイル解析では、NIR光はノンコーディングRNA(ncRNA)を促進することが示されている65。非コード配列の役割を理解することは、今後の研究課題である。
PBMは、ミトコンドリアのチトクロムc酸化酵素を介した電子輸送、光イオンチャネルを改善することで、炎症や痛みを和らげ、骨や腱の創傷治癒を促進する臨床治療に応用することができる(総説86)。PBMの間、NIR光の主要な光受容体であるシトクロム酸化酵素は、ミトコンドリア内の酵素が酸化に重要であるため、傷ついた眼球や脳組織の回復の建設的な役割に重要な役割を果たしている。例えば、NIR光は、ミトコンドリア機能の増加、損傷した神経細胞への血流の改善、細胞生存因子の増加によって、損傷した網膜の改善と機能回復に強力な神経保護効果を発揮する87。
PBMTは近年、ヒトの医療においてますます普及している。最近の研究では、レーザー治療が免疫反応や炎症反応を制御し、特定の組織の創傷治癒を促進する可能性が示されている88。また、PBMTのエネルギーは、加熱や組織破壊の心配がなく、非常に限定的だが、細胞機能を媒介するためには豊富である。例えば、PBMTは皮膚疾患の光線力学療法11や神経細胞疾患の温熱療法12に用いることができる。細胞は試験管内試験では電磁スペクトルの特定の波長に敏感だが、生体内試験では波長に対する有益な観察は優先的に狭い範囲の波長のみである。例えば、可視域(通常400~700nm)の光は、錐体や桿体の特定の光色素を持つ網膜細胞を伝染し、活性化することができる。赤色から近赤外域の波長は、特定の光色素を持たない細胞に有益な効果をもたらすのに最も適している。これはおそらく、ある範囲の波長が組織を伝染する能力によるものだろう。波長が低いほど、例えばバイオレットやウルトラバイオレットの波長は伝染能力が低く、一方、赤外域の赤の波長は伝染能力が高い。さらに、600nm未満の波長のエネルギーは、通常生体内の組織に広く分布している13。医療目的では、赤色と近赤外波長による生体内治療光学領域が存在することを示唆している。この光ウィンドウは、光エネルギーが細胞内の生体分子を活性化する能力にも対応している13。興味深いことに、レッドシフトチャンネルのロドプシンを盲目のrd1マウスに注射すると、マウスの網膜や皮質から、低いオレンジ色の光やヒト網膜の神経節細胞に対する光反応を回復させることができる89。したがって、NIR光は近赤外光治療とも呼ばれる。すなわち、NIR光は、生きた生体分子が光子を吸収し、光によって引き起こされるシグナル伝達経路を活性化させるという概念に基づいている14。この生物学的プロセスは、光によって活性化された生体分子が基底線から電子励起状態に到達し、その結果、コンフォメーションと機能が変化し、細胞代謝と回復を仲介する特定のシグナル伝達経路の活性化を誘導するという理論に基づいて、エネルギー変換と呼ばれている。NIR光の医療分野への応用は目覚ましい進歩を遂げているが、さらなる進歩のためには、そのメカニズムに関する詳細な研究が必要である。
近赤外光による網膜治療の可能性
NIR光は損傷したミトコンドリアの生物学的機能を回復し、細胞保護因子をアップレギュレートし、アポトーシスを抑制する可能性が示唆されている。NIR光の光子は病気の網膜を伝染し、シトクロムcオキシダーゼなどのミトコンドリア光受容体に吸収され、ミトコンドリアのエネルギー有益代謝を促進し、細胞保護因子の産生を上昇させ、アポトーシスを防ぐことができる。
NIR光の医療への応用例を以下に挙げる。NIR光は、メタノールで操作した網膜損傷モデルにより、ミトコンドリアのエネルギー代謝が損傷された網膜を保護することができる。NIR光は、核外層の損傷を減少させ、網膜電図bの波振幅を保護する可能性がある90。驚くべきことに、NIR光による保護効果は損傷から1カ月も持続し、神経保護におけるmRNA発現の増加と関連している。NIRはまた、光受容体を保護し、光損傷によって誘発される複数の遺伝子発現の減少を伴う光毒性による細胞死を回避する可能性がある65。驚くべきことに、NIR光は視細胞の死を70%減少させる可能性がある91。NIR光はまた、ミトコンドリア複合体Iに対する阻害剤ロテノンによって引き起こされる網膜神経節細胞の細胞変性を抑制することができる1。NIR光治療はまた、加齢による黄斑変性による黄色い沈着物であるドルーゼンを促進することができ、数ヶ月間眼圧を下げることができる6。
網膜のミトコンドリア変性と酸化的損傷は、加齢黄斑変性、光刺激網膜損傷、メタノール中毒、網膜色素変性症などの網膜変性やその他の損傷で示されている92–94。NIR光はミトコンドリアのシグナル伝達経路を活性化し、ミトコンドリア機能を促進し、細胞保護因子の発現と活性化を誘導し、酸化ストレスを抑制し、試験管内試験神経細胞や生体内試験神経細胞傷害動物モデルで神経細胞を死から保護する可能性がある5,15,16,18,76。
近赤外光による光治療の可能性
NIR光による光の伝染性は、ターゲット組織、波長、NIR光の光源に依存する。近赤外光は安全だが効果的である。近赤外線の波長の中では、光は最大レベルで眼を伝染できるが、角膜と水晶体による光の吸収は最小レベル(約10%)である95。網膜のニューロンは、組織の要求を満たすために高いエネルギー、すなわちミトコンドリアATPを必要とする96–98。他の神経細胞と同様に、網膜神経細胞もグルコースの枯渇やエネルギー不足、酸化ストレス、ミトコンドリアの機能不全に対して非常に敏感である99,100。ミトコンドリアの機能不全は網膜神経変性において重要な役割を果たしている101。視神経細胞障害は高い罹患率と死亡率を特徴とするが、現在のところ有効な治療法はない102–105。アルツハイマー病患者では、網膜神経節細胞、神経節軸索の数が健常人よりも少ない104,106,107。ミトコンドリア病のひとつであるレーバー視神経症は、全世界の失明患者の約2%を占める108。したがって、網膜神経節細胞からの細胞変性は、この世界における主要な健康問題である。その他の遺伝性疾患には、リー症候群109,110、フリードライヒ失調症111、ボロボロ赤線維によるミオクロニーてんかん112、ミトコンドリアアシドーシスと脳卒中113、痙性対麻痺114、視神経萎縮症候群115などがある。したがって、NIR光は、ミトコンドリア障害の矯正による網膜損傷に対する眼球および神経細胞治療への応用にとって重要である。例えば、有益なNIR光は、ウサギとラットのモデルにおいて、ヘリウムネオンレーザーを使用することで視神経損傷を回復させることができる116,117。総じて、NIR光は眼や神経の中程度の損傷に有効である。

近赤外光による近視治療
示唆されているように、近視の流行は全世界に影響を及ぼしている118-124(125でもレビューされている)。近視が進むと、重度の網膜裂孔や網膜剥離、脈絡膜変性症、緑内障、白内障を引き起こし、米国では多くの失明者が出ている126–130。高次収差とは、網膜像の質に影響を与える目の光学的欠陥のことで、その結果、網膜像の質が低下する。この原理は、オルソケラトロジー、近用追加メガネレンズ、二重焦点・多焦点ソフトコンタクトレンズによる近視制御に応用されており、近視制御における潜在的な意義は非常に大きい131。私たちは、中国の小学生を対象とした大規模臨床調査において、1%アトロピンが中等度近視の進行を遅らせることを報告した132。したがって、このようなレベルの近視有病率は、公衆衛生上非常に深刻な問題である。世界中の人々の高齢化に伴い、近視の有病率は増加の一途をたどっている。
屈折異常の一つである近視は、世界的に失明の原因となることが多くなっているが、これは光によって引き起こされる網膜から強膜への変化によるものと考えられている134。生後の屈折矯正発育において、長波長光は近視と同様の屈折異常を引き起こす可能性がある135。しかし、サルの乳幼児モデルでは、長波長光は近視の発達促進とは密接に関連していない136。動物やヒトの乳幼児は、屈折異常の大きい眼を持っている137-142。近視による屈折異常を軽減するためにガス伝染性コンタクトレンズを使用するオルソケラトロジーは、現在、思春期の近視抑制に広く用いられている(総説143)。近視になったら、できるだけ早くプリズム遠近両用レンズや多焦点コンタクトレンズを使用することで、オルソケラトロジーは近視の進行を遅らせることができる13。屋外での活動を増やすことも、近視の発生を予防し、近視からの屈折異常の移行を遅らせるのに効果的だが、すでに近視になっている眼の進行を抑えることはできない(144に総説あり)。加齢により、軸長は眼球の光学系に合わせて調節され、網膜が焦点面に位置する遠視と呼ばれる状態になる。遠視化の活性化機構は、出生後の眼球では、網膜が焦点面に一致するように眼球の伸長率が設定されると考えられている145-149。動物は白色光よりも単色光で屈折状態を調節することがあり、青色光では相対的に遠視になり、赤色光では相対的に近視になる150。波長の構成は屈折異常、ひいては近視と密接に関連しており、例えば、明滅する青色光は近視などの屈折低下を促進し、コロニー照明に戻ると屈折は遠視に戻る可能性があることから、明滅光はシグナル伝達のデフォーカス151と密接に関連している可能性が示唆される。赤色光は、硝子体室の伸長を減少させ、脈絡膜の厚さを増加させることによって屈折発達を変化させる可能性があることから、帯域の狭い長波長光は、おそらく近視性デフォーカスに関連するシグナルを活性化することによって、遠視性デフォーカスや形態剥奪によって誘発される軸方向の伸長を遅らせる可能性が示唆される131。屈折状態を常に調節することにより、遠視は生後全期間においてほぼ遠視を維持する146,147,152–156。生後早期には、屈折異常はほぼ屈折率に対応している。成熟するにつれて、眼球前面の光学系は徐々に焦点面を網膜に合わせ、軸方向の伸びを遅らせ、水晶体を加えた分を補い、水晶体を装用した場合は遠視、水晶体を外した場合は遠視になる146,148,152,154,157-164。出生後の発達では、遠視に近い不自由な状態に徐々に到達する。遠視化は幼年期から青年期にかけても活動的で、眼軸長の長い成長期が続くが、遠視のままである。高年齢でも、遠視の増大に対してマイナスレンズを装用することで強く反応することは有用である160,165–167。一方、プラスレンズへの屈折矯正能力は、加齢とともに急速に低下する。しかし、プラスレンズを装用した樹上トガリネズミの幼生は、眼の伸長速度を遅らせることはできない。実際、眼球の伸長は続いており、レンズ168を使用しても眼球は近視のままである。プラスレンズの補償がなくても、幼年期から青年期までの若いツリートガリネズミは誘発された近視からすぐに回復できる154。このことは、これらの動物では遠視化が近視の屈折状態に長期間対応する可能性を示唆している154,169。
最近、私たちは多焦点コンタクトレンズによって近視の進行を遅らせることができることを報告した170。実際、明るい光はドーパミンD1受容体を活性化することにより、近視の進行を抑制することができる171。さらに、ニワトリモデルでは、赤色光は近視の進行を促進し、青色光は遠視の進行を引き起こす可能性があり、赤色光と青色光を入れ替えると、このような誘導は遠視と近視に逆転することができることから、色度の操作によって近視に有益な効果が得られる可能性が示唆されている172。

残念なことに、若い動物の加齢において、なぜプラスレンズが軸の伸長や屈折矯正を遅らせないのかはまだわかっていない。近視が誘発された眼が軸伸長から回復する一方で、正常な眼がプラスレンズに反応しない理由はまだ不明である。おそらく正常な眼では、屈折矯正によって軸方向の伸長があらかじめプログラムされた最小値の閾値以下に抑えられることはないのだろう。マイナスレンズ装用により眼球が伸長する状況では、細胞外マトリックスのリモデリング下にある強膜が、mRNAおよびタンパク質レベルで特定の遺伝子発現を変化させたと考えられる173-175。
NIR光治療の展望
NIR光治療は、目や脳などの様々な組織を副作用なく治療する効果的な方法である。世界中の研究者は、NIR光の作用メカニズムを解明し、様々な病気の治療効果に焦点を当て、新たな医学の主要分野として支持する科学的根拠を示すべきである。この治療法は、近い将来、多くの病気を治す「奇跡の薬」になる可能性を秘めている。新しいNIR光機器の開発、NIR光治療による様々な標準治療プロトコルの確立、そしてこの治療法の世界中の様々な医療分野への応用には、さらなる研究が必要である。
結論
近赤外光(PBM)は、赤から近赤外領域にかけての低出力光波長によって生物学的機能を媒介する有望で強力な方法である。眼や神経細胞は、代謝プロセスのエネルギー生成にシトクロムcオキシダーゼを利用している。NIR光はこれらの組織を伝染し、メタノール中毒、視神経外傷と神経障害、網膜損傷と色素変性、黄斑変性症におけるニューロンの回復を助けることができる。
NIR光はまた、アテローム血栓性脳卒中、脳損傷、神経変性からの脳の回復を助けることができる。動物や人間から副作用は観察されていない。従って、NIR光は近い将来、眼科や神経学分野での幅広い応用のための安全で効果的な方法となる可能性がある。

