Low Level Laser Therapy in Primary Raynaud’s Phenomenon — Results of a Placebo Controlled, Double Blind Intervention Study
pubmed.ncbi.nlm.nih.gov/15570642/

概要. 目的
原発性レイノー症候群患者における低レベルレーザー治療の有効性を評価し、臨床的特徴からレーザー治療の成功を予測すること。
方法
48人の患者を無作為化プラセボ対照二重盲検クロスオーバー試験に参加させた。レーザー治療と偽薬治療がそれぞれ週5日、3週間実施された。臨床症状、誘因への暴露、および発作の頻度と強度を日記に記録した。発症前と両照射シーケンスの終了時の赤外線サーモグラフィーの結果を評価した。一次エンドポイントは発作の平均強度であり、二次エンドポイントは発作の平均回数とサーモグラフィー結果であった。年齢、性、症状の持続時間、交感神経症の発症年齢、寒冷以外の誘発条件、寒冷刺激後の最高体温低下、および寒冷刺激後の再暖機時間が潜在的な予測因子として検討された。
結果
レーザー治療では、偽薬治療と比較して発作の回数とその強度が有意に減少した。サーモグラフィーのパラメータは統計的有意差に達しなかった。段階的重回帰分析では、寒さ以外の誘発条件(ストレス、湿潤が追加の引き金となった)再暖機時間、および寒冷刺激後の体温低下が治療効果の有意な予測因子であった。
結論
低レベルのレーザー治療はレイノー発作の頻度と重症度を減少させる。この効果は、血管痙攣の閾値が低下している患者で最も顕著であり、遅発性充血の患者では効果が低い。(J Rheumatol 2004;31:2408-12)
主な索引用語
レイノー病レーザー治療 低レベル
はじめに
疾患の原因療法は、その根底にある病態のメカニズムが分かっている場合にのみ可能である。原発性レイノー現象(RP)では、これは完全には当てはまらない。交感神経系の活動性の変化や内皮依存性の血管調節やプロスタサイクリン、一酸化窒素、エンドセリン-1の役割を含むデジタル血管系の局所的な障害など、いくつかの機序が議論されていたが、カルシトニン遺伝子関連ペプチドや非血管性因子1-5などの他の因子も示唆されている。しかし、その名が示すように、完全な因果関係は不明である。
主に、上記のような病態メカニズムのすべての側面が治療的介入の対象となっている。提案されている治療法は、血管拡張薬の適用から手術6,7まで、広範囲にわたっている。治療法の中には、臨床経験や実験的証拠に基づくものもあるが、作用機序が確立されていないものもある。低レベルレーザー治療(LLLT)は、血管レベルでの生物学的効果が経験的に実証されているが、このカテゴリーに該当する8。
LLLTの臨床的有効性については、エビデンスに基づいたアプローチが検討されているのはわずか数件の報告のみである9-11。以前に行われたプラセボ対照二重盲検試験9に基づいて,臨床試験の延長試験の結果を報告する。この研究では、特に関心のある問題として、レーザー治療の成功がプリマリーRP患者の臨床的特徴やその他の特徴から予測可能であるかどうかも評価した。
材料および方法
患者と診断方法
2001年から 2003年の寒冷期(11月から3月)に登録した。診断カテゴリーに該当し、当院の外来を受診したすべての患者は、所定の患者数(n = 50)に達するまで参加するように求められた。患者はインフォームドコンセントを得た。参加拒否(26%)は主に患者の時間的制約によるものであった。2人の患者はデータセットに不備があり、評価から除外された。
患者は、以下の診断基準に合致する原発性RPと診断され、血管反応を阻害する可能性のある血管活性薬を現在服用していない患者が対象となった。
一次性RPとは、他の疾患と関連していない寒冷曝露や感情的な刺激に反応して皮膚が赤くなる、チアノーゼ、および頻繁に擦れることによって臨床的にchar-acterized指のエピソード性虚血として定義される12。
試験開始前に、二次性RPが疑われる患者を除外するために、標準化された診断手順13が策定された。症状が持続する患者のみを対象とした。この手順により、高確率で二次性RPの症例を除外することが可能となった。この方法は、スクリーニング検査と拡大診断プログラムから構成されている。スクリーニングプログラムは以下のステップで構成されている。(1) 患者の病歴と人口統計学的基準。(2) 臨床検査(手足の触診、Allenテスト、結合組織障害の徴候)。(3) 非侵襲的血管学的検査(ドップラー超音波検査、アクラルオシログラフィー、爪甲毛細血管の顕微鏡検査)。(4) レントゲン検査(胸部、両手)。(5) 臨床検査化学検査(Westergren沈降速度、差動血球数、腎機能、血清学的マーカー)。
スクリーニングの結果、二次性RPが疑われた患者には、大動脈弓部血管造影検査、または基礎疾患を確立するために設計された特定の検査プログラム(臓器スクリーニング)のいずれかで構成される診断プログラムを拡張し、スクリーニングプログラムの期間中の所見に合わせて調整し、拡張プログラムで収集された所見に応じてさらに調整した。
血管痙攣を客観的に評価するために、電子増幅された頭蓋骨オシログラフィが実行された14。オシログラフィは、安静時の両手のすべての指で行われた。オシログラムは、暖かい(37℃の水中で5分)と冷たい挑発(12℃の水中で5分)と1,3,5,7,10,12,15,17,20分後の両方の自発的な痙攣の兆候について検査した冷たい挑発の後。同じ時間点で皮膚温度を測定した。これらのデータをもとに、低温刺激前の温度から直線を引いた温度曲線の交点を求めることで、血管痙攣が消失した時点と再暖機時間を算出した。さらに、低温刺激後の皮膚温度の最大低下量を求めた。
実験手順。同一の外観を持つ2つの装置を使用した(Heltschl GmbH, Schlüsslberg, Austria)。装置Aはダイオードレーザー(出力200mW、波長685nm)であり、装置Bは非コヒーレント発光ダイオード(出力200mW、波長640〜685nm)であった。両方のシステムは同一のパネルで制御された。レーザー装置の焦点は、照射領域の大きさに合わせて露光時間を調整し、2J/cm2に設定した。光源は、この研究の目的のために特別に構築された箱の上側に配置された。患者は、照射部位の位置をスタンダート化し、アレイから発せられる光を隠蔽するために、手を2つのスロットに入れた。照射部位は手の指と手の甲とした。照射時間は30分から40分であった。
各治療シーケンスは、1週間に5回のセッションで3週間の期間を有した。このシーケンスの後、装置を交換し、別の3週間のシーケンスを開始した。最初の装置は無作為に選択された。研究者も臨床スタッフも患者も、AおよびBと表示された装置がレーザーまたは偽露光装置のどちらであるかを知らなかった。実験条件の順序は完全にバランスがとれていた。
照射開始の2週間前、6週間の照射セッション中、および治療後2週間は、患者はレイノー発作を日記に記録するように指示された。これらの日記は、各日ごとに欄が設けられた小さな冊子であった。攻撃を誘発するような状況への暴露の種類と回数、および攻撃の回数は、毎日就寝時に記録されなければならなかった。この情報は、攻撃の相対的な頻度を計算するために使用された。攻撃の平均強度は、5点満点(1=最小、5=重度)のネコゴリー尺度で週ごとに評価した。この方法は、Raynaudダイアリーでの経験に基づいて選択されたもので、就寝時の記入方法がその場での記入よりも優れていることが証明された。後者のタイプの問題の主な理由は以下の通りである。発作の多くは屋外で起こることが多く、雨や雪が降っているときなど、冊子と鉛筆を取りに行って記入するのが困難な状況である。
最初に、最初の3週間後、2回目の3週間後に、局所冷却後に赤外線サーモグラフィー(NEC三栄サーモトレーサー)を行った。赤外線サーモグラフィーは、特に血管性疾患やリウマチ性疾患の患者で効果を評価するのに適しているようである15,16。簡単に言えば、手順は以下の通りであった。腕を脱いだ状態で24℃の室温に15分以上順応した後、ベースラインサーモグラフィーの測定のためにプラスチック製のカバー付きパネルに手のひらを置く。次に、患者はプラスチック製の手袋をはめ、20℃に保たれた水の入った洗面器に1分間手を入れた。回復は、直後および低温曝露後の最初の20分間に測定した。サーモグラフィー評価のために、指先と中手骨の中心にある関心のある円形の領域を選択した。温度勾配は、中手骨から指までの温度測定値の差として、各指について計算した。1℃を超える負の差は病的なものと考えた。冷水に曝露してから 20分後の両手の全指の平均温度勾配を、一般的な血管痙攣状態の指標として用いた。さらに、冷水曝露後20分後に中手骨と指の間に1℃を超える温度差を示した指の数を、病的な温度勾配の指標としてカウントした。
主要エンドポイントは、レーザー治療またはプラセボ治療のいずれかを3週間適用した際のレイノー発作の平均強度と定義した。レーザー治療に対する反応性の潜在的な予測因子を同定するために、レーザー治療中とプラセボ治療中の平均発作強度の、治療前の発作強度に対する相対的な差を基準として用いた。副次評価項目は、平均発作数と赤外線サーモグラフィーの結果とした。
統計的方法
レーザー条件とプラセボ条件の比較は、条件の順序を制御したANOVAによって行った。各週のデータが含まれ、レーザー対プラセボおよび条件の順序に加えて第3の因子を構成した。全期間にわたってデータをプールするのではなく、この手順は、実験条件間の時間傾向の潜在的な違いを評価するために選択された。正規性は、Kolmogorov-Smirnov検定によって評価した。
重回帰分析は、レーザー治療への反応性が患者の特徴によって予測できるかどうかをテストするために適用された。年齢、性別、症状の持続時間、症状発症時の年齢、寒さ以外の症状、寒さ刺激後の最高体温低下、寒さ刺激後の再暖機時間が潜在的な予測因子として検定された。
結果
原発性RP患者48名(女性38名、男性10名)を対象とした。平均年齢(±SD)は46±14歳、発症年齢は26±11歳、症状の持続期間は20±10年であった。症状を誘発する条件は、寒さ(100%)湿潤(63%)ストレス(33%)であった。全例で両手の1本以上の指が罹患しており、23%は足の指も罹患していた。
表1に示すように、喚起条件(寒さ、湿り気など)への曝露頻度は、治療前の段階とレーザーまたはプラセボ治療期間(各3週間)では差がなかった。そのような暴露は1日あたり平均3回報告された。気象気象モニタリングステーションで記録された周囲温度は、偽薬とレーザー照射期間の間で統計的に差がなかった(偽薬3.2±3.6℃、レーザー3.0±3.9℃)。
攻撃の数とその強度は、攻撃の絶対数または攻撃を誘発する曝露の数との関係がテストされたかどうかにかかわらず、偽薬治療と比較して、レーザー治療の期間中に有意に減少した。攻撃のわずかに減少した頻度も偽治療の間に見られた;しかし、減少は、レーザー治療期間中に有意に高かった。発作の強度はプラセボ期(治療前の強度の約96%)ではわずかに減少しただけであったが、レーザー治療では約82%と非常に有意に減少し、3週間の治療期間中に減少傾向がみられた。
表1 レーザーおよびプラセボ治療の各週の1日あたりの平均暴露数、1日あたりの攻撃
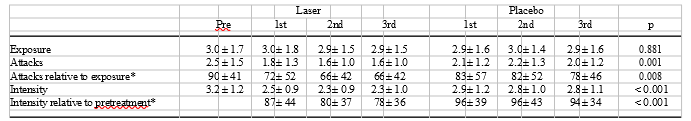
(暴露数に対する絶対値および相対値)攻撃の強度(5ポイントスケール、最小から重度まで、治療段階の前週に対する絶対値および相対値)の平均±SD。
レーザーとプラセボの比較のためのANOVAからのp値。
すべてのサーモグラフィー測定値はレーザー治療に有利に比較されたが、いずれも統計的に有意な値には達しなかった(表2)。
レーザー治療への反応性に関して患者の臨床的およびその他の特性が果たす役割を決定するために、レイノー発作の強度の低下を年齢、性別、症状発現時の年齢、症状の持続時間、誘発条件、患部(手指、足指)低温誘発後の最高温度低下、および低温誘発後の再暖機時間に関して分析した。段階的重回帰により、追加の誘発条件としての湿潤状態、再起温時間、低温刺激後の体温低下のみが攻撃強度低下の基準と有意な関係を示した(表3)。寒さ以外の誘発条件(ストレス、湿潤)を経験した被験者、および/または再起温時間が長い被験者、および/または寒さ刺激後の体温低下が顕著でない被験者は、レーザー治療の効果が低下していることを示した。
考察
原発性RPは原則として良性の疾患であるが、重症化し、生活の質が低下し、患者の職業機能が制限されることがある。平均的なRaynaud発作の持続時間は約25分であり、1日に数回の発作で社会活動が制限され、時には屋内に閉じこもることもある17。診断上の主な課題は、原発性RPと二次性RPの鑑別である。一次性RPに対する治療介入は限られており、主にカウンセリングによる誘発刺激への曝露を予防的に避けることに限られている。しかし、効果と副作用のバランスを考慮した上での治療が必要であることが多い。
この限られた治療スペクトルは、代替治療法のための意識の高まりにつながる。これらの方法の一つがLLLTである。LLLTは血管疾患やリウマチ性疾患の患者に使用されていたが、その効果は明確ではない18,19。
原発性RP患者におけるLLLTの使用を検討した理由は、逸話的な証拠と私たちの外来ユニットでのこの方法の最初の経験でした。これは、彼/彼女自身のコントロールとして各被験者を使用して研究プロトコルの開発につながったため、同時にシャム治療とクロスオーバーアプローチを使用して交絡条件を制御しながら、任意の可能性のある効果を検出するために良い可能性を示している。
本質的には、以前のパイロット研究の結果が再現されている9。発作の頻度は、今回の試験では患者数の3分の1以下であったが、前回の試験ではわずかに減少しただけであった。発作の頻度や強度など、患者のウェルビーイングに関連する臨床指標は、LLLTによって大幅に減少した。発作の頻度は約20%減少した。0.5~1スケールポイントの攻撃強度の平均減少は、15~35パーセンタイルポイント(ベースラインの強度に応じて)の減少に相当するため、臨床的にも重要である。同様の結果がプラセボ対照のRP試験でも得られているが、二次性RP11の患者が優勢でした。本試験で報告された効果はさらに顕著であり、これは試験群の定義(二次性RPの有無)や試験デザインの違いにより、プラセボ効果が異なることに起因していると考えられる。
表2 赤外線サーモグラフィーの結果
全指に平均した指と中手骨の温度差の平均値±SD、最大温度差、および病理学的勾配のある指の数。
ウィルコクソン検定で検定した指の数を除き、レーザーとプラセボの比較のためのANOVAからのp値。
表3 レーザー治療への反応性の予測因子としての寒冷以外の誘発条件
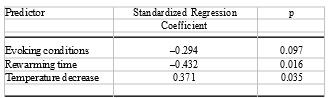
(ストレス、湿潤)再起温時間、および寒冷挑発後の温度低下についての標準化回帰係数(レーザーとプラセボの間の発作の強さの差は治療前の強さに関連していた)。倍数R = 0.51。
最近発表された研究11では、赤外線サーモグラフィーでも有意な改善が示された。我々の研究では取るに足らない変化しか見られなかったが、これはRP20患者における赤外線サーモグラフィーの再現性の低さと、適用された評価方法の違いによるものと考えられる。
LLLTの有効性を予測できる要因を分析したところ、寒さが唯一の引き金となっている患者では、寒さ刺激後の温度低下がより顕著であり、かつ/または再加温時間が短い患者では、LLLTに対する反応がより良好であることが明らかになった。LLLTの効果の違いは、原発性RPの臨床症状の本質的な不均一性を示唆している。低温刺激後のアクラルオシログラムを詳細に評価したところ、2種類の異なる反応が認められた(少数の患者では両方の反応が混在していた)。1つは体温の急激な低下を伴う即時の血管痙攣であるが、その後に体温の急激な上昇がみられた。血管調節の内皮依存性と独立性の経路とRP4-6,21-25における役割に関する議論とLLLTの効果の違いに関する結果を考慮すると、レーザー治療の効果は内皮非依存性のメカニズムに基づいているという仮説を提案する。それはLLLTが細胞膜伝染性を変化させるという仮定に一致して、末梢のアドレナリン神経とポストsy-napticα受容体への影響によって作用することを仮定することができる26。
別に代替療法的アプローチの純粋に科学的な関心から、利用可能なリソースの不足は、客観的にそのような代替的な方法の臨床的有効性を評価することが不可欠になる。このような治療法は、エビデンスに基づいた観点から裏付けられて初めて、臨床現場での重要性を増していくことになる。プラセボ治療のわずかに有益な効果は、患者の前向きな期待を示していると考えられるが、統計的な有意差には至らず、LLLTの差は大きく、レーザー治療の真の治療効果を強調していると考えられる。これはまた、コントロールされた二重盲検試験の重要性を強調するのに役立つ、特にプライマリRPの場合のように主観的な評価を必要とするケースで。
LLLTはレイノー現象の発作の強度と頻度を減少させることが示されている。LLLTの治療効果は、寒冷刺激後の血管痙攣の強さや反応性充血の抑制の程度が異なる患者では、治療効果が異なることが観察された。これが内皮に依存しない因子によるものかどうかは、まだ解明されていない。さらに,LLLTのこの差動効果に基づいたex iuvantibusの議論により,原発性RPの本質的な不均一性が示唆され,今後の研究で立証されれば,原発性RPの病理学的メカニズムの解明に役立つ可能性があると考えられる.
