Will SARS-CoV-2 become endemic?
個人が生涯を通じて同じウイルス種からの複数の異なる感染にさらされる再感染は、多くの呼吸器ウイルスの顕著な特徴である。実際,インフルエンザウイルス,呼吸器同期ウイルス(RSV),ライノウイルス,コロナウイルスなどの一般的な呼吸器ウイルスが人間社会に存続し,普遍的に存在しているのは,主に繰り返し感染を起こす能力に起因している.現在進行中のコロナウイルス疾患2019(COVID-19)のパンデミックの原因となるウイルスである重症急性呼吸器症候群コロナウイルス2(SARS-CoV-2)が出現して以来、ヒトがこの病原体への再感染を経験するかどうかが重大な懸念事項となっており、これによりコロナウイルスがパンデミック性になる可能性がある。
典型的には、初期感染後、ヒトの適応免疫系は、その特定の病原体に結合することを標的とした中和抗体を産生することができるメモリBリンパ球、および免疫応答を調節し、感染細胞の死を誘導するのに役立つメモリTリンパ球を含む一連の防御を開発する。これらの適応免疫構成要素、特にB細胞は、病原体が宿主に再導入された場合、体内での複製を阻止する殺菌免疫を作り出すことができる。
しかしながら、多くのウイルスでは、多くのプロセス、特に不十分な適応免疫応答、免疫の衰え、および免疫の逃避が、免疫の殺菌性を損なうか、または回避し、その後の再感染を可能にする。最初の例では、特定の病原体への初感染では、殺菌免疫を付与するのに十分な適応免疫応答が得られないことがある。血清学的研究では、重症度にかかわらず、ほとんどのSARS-CoV-2感染症では、いくつかの特異的な抗体の発現が誘導されることが示されている(1)。さらに、SARS-CoV-2感染に対する免疫反応は不均一であり、無症状の感染を経験した個体では、重症化した個体に比べて免疫反応が弱くなる(1)。SARS-CoV-2に感染しても殺菌免疫が発現しない個体や、親和性の成熟と長期的な保護の発現には複数回の曝露が必要である可能性がある。
図 SARS-CoV-2のポストパンデミック感染に影響を与える要因
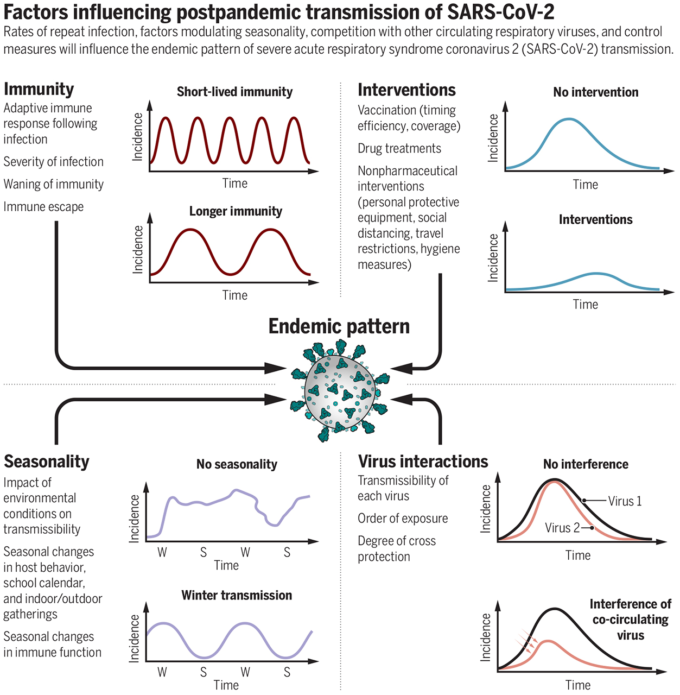
繰り返し感染の割合、季節性を調節する要因、他の循環型呼吸器ウイルスとの競合、および制御手段は、重症急性呼吸器症候群コロナウイルス2(SARS-CoV-2)感染のパンデミックパターンに影響を与える。
初期の適応免疫反応は強固で防御的であったが、時間の経過とともに消失し、宿主は再感染を受けやすい状態になってしまう免疫力の低下も、殺菌免疫力を低下させる可能性がある。免疫逃避は、特にウイルスによる再感染を促進する第三のプロセスである。ここでは、ウイルスが宿主集団を連続的に通過し続ける間に、点突然変異が蓄積される。この蓄積は抗原性ドリフトと呼ばれ、ウイルス表面タンパク質の構造変化を引き起こし、以前に生成された変異体に対する抗体の結合を妨げることがある。免疫逃避は、この抗原性ドリフトの結果として、適応防御の回避による再感染を可能にする。
免疫力の低下と免疫逃避の時間スケールは病原体によって異なり、SARS-CoV-2ではまだ定義されていない。これまでのところ、SARS-CoV-2ゲノムの突然変異率はインフルエンザウイルスよりも遅いようである。これは、RNAウイルスの中でもコロナウイルスに特有の複製時のプルーフリーディングの結果であると考えられる。逆に、ヒトコロナウイルス(HCoV)OC43は、特にスパイク蛋白質のような表面蛋白質をコードする遺伝子において高い変動性を示しており、かなりの多様化が起こりうることを示している。これまでのところ、SARS-CoV-2特異的抗体の消失の証拠が縦断的研究で捉えられており(2)SARS-CoV-2の繰り返し感染が数回確認されている(3)。再感染は起こりうるが、再感染例の数は現在のところ、集団規模での免疫の持続期間や繰り返し感染の重症度を一般化するには十分ではない。再感染が一般的になるのかどうか、再感染の頻度はどうか、再感染者の感染力はどうか、重篤な臨床転帰のリスクはその後の感染によって変化するのかどうかはまだ理解されていない。
他の呼吸器ウイルスからの知見は、SARS-CoV-2との再感染の可能性を示唆している。4種類の常在性HCoV(OC43,HKU1,229E、およびNL63)の自然獲得感染から、同じHCoV型への再感染は1年以内に一般的であることが示されている(4);同じインフルエンザウイルス株への連続感染は2年以内に起こる可能性がある(5);成人のRSVへの1年以内の再感染も記録されている(6)。対照的に、宿主に全身的な影響を及ぼす病原性の高いウイルスの方が、より長く続く適応免疫応答を引き起こす可能性がある。例えば、SARS生存者の縦断的な免疫プロファイルでは、中和抗体が2~5年間持続することで、より強い免疫応答が示されている(7)。しかし、SARSの発生が1年未満であったため、この反応が免疫を付与しているかどうか、また、どのくらいの期間に渡って免疫を付与しているかは確認できなかった。
保護免疫の持続期間に加えて、SARS-CoV-2のヒトに対する長期的な影響は、再感染の重症度に依存する。インフルエンザウイルスとの連続感染は、症状の重症度が低いことと関連している(8)が、繰り返しパンデミックするHCoV感染では、再感染と症状の重症度との関連は認められなかった(4)。さらに、他のウイルス(RSVやデング熱など)では、自然に誘導された抗体やワクチンによって誘導された抗体の結合が不適切であると、その後の曝露時に感染の重症度が増強されることがあり、これは抗体依存性増強(ADE)と呼ばれる現象である(9)。これまでのところ、SARS-CoV-2 再感染が確認された少数の患者の反応は不均一であり、明らかな再感染は1例で入院を必要としている。したがって、SARS-CoV-2感染者にADEが発現しているかどうかを判断するためには、完全な血清学的および前向き研究が必要であり、それは過去の相同感染または他のHCoVからの交差反応性抗体のためである。これはワクチンや回復期の血漿療法に特に関連性がある。
再感染が一般的になり、世界のほとんどの人口に非常に効果的なワクチンが提供されない限り、SARS-CoV-2がパンデミックする可能性が高い(10)。個人が再感染を経験する典型的な時期と季節的な伝播性の違いによって、パンデミックのパターンが決定される。熱帯地域以外では、多くの一般的な呼吸器ウイルス感染症の発生率は、1年の特定の時期に増加する。このような段階的な行動は、免疫の逃避と免疫の衰えにより時間の経過とともに増加する再感染に対する累積的な感受性、および環境条件、行動の変化(例えば、寒い時期に室内での混合)または免疫機能の変化に由来するウイルス透過性の季節的な変調に起因している。例えば、インフルエンザの発生率は、温帯地域では冬の間に最も高くなる。インフルエンザウイルスは、いったん感染性の宿主から排出されると、冬の間、屋内でも屋外でもパンデミックしている低湿度の条件(11)でより安定しているようである。さらに、寒い時期には室内で過ごす時間が長くなり、学校が開かれているため感染が促進され、日照時間が短く、日光への曝露が少ないと、免疫機能が抑制される可能性がある。
固有の HCoV(OC43,HKU1,NL63,および 229E)はすべて、インフルエンザウイルスと同様に温帯地域で季節性を示する(12)。そのため、温度、日照、湿度、オゾン、汚染などの条件が SARS-CoV-2 の生存率と透過性に影響を与えるかどうかを調べる研究が数多く行われていた。日光や湿度などの環境条件がSARS-CoV-2の伝播性を調節する可能性があると考えられるが、その結果は現在のところ決定的なものではなく、免疫力が一般的に低いパンデミックの最初の波の間に伝播を阻止するには十分ではないが、免疫力が上昇すればインフルエンザウイルスと同様、温帯地域の冬の間に季節的に段階的に伝播するのに十分であると考えられる。
2009年のインフルエンザパンデミックと同様に、この最初のパンデミック期間後もSARS-CoV-2による継続的な循環は、再感染率、ワクチンの利用可能性と有効性、およびウイルスの伝播性を調節する社会的、免疫的、自然的要因の機能として現れてくるであろう(図を参照)。さらに、ヒト集団における SARS-CoV-2 の周期的な持続性は、他の呼吸器病原体との相互作用の継続的な機会によって影響を受ける可能性がある。
共循環する呼吸器ウイルスは、同じ資源を奪い合いながら互いに干渉する可能性があり、それらの相互作用は、集団レベルおよび個体レベルで、再構成されたヒト組織および動物モデルにおいて研究されていた。異なるウイルスへの連続曝露を経験した個体における転帰は様々であり、一般的には曝露の順序とタイミングに依存するようである。多くの研究では、最初の感染から誘発される短命(数日)の保護によって引き起こされるウイルス間の負の干渉の証拠が文書化されている。宿主の抗ウイルス性インターフェロン応答は、干渉が発現する主なメカニズムと考えられている;つまり、最近の感染の結果として、宿主細胞はインターフェロンの合成をアップレギュレートし、潜在的に二次感染を阻害する。この効果は短命であるにもかかわらず、集団レベルでは強力であり、ウイルスの有病率を一時的に低下させたり、ウイルスが循環するタイミングをずらしたりすることがある。例えば 2009年夏の大規模なライノウイルス大発生は、ヨーロッパでのパンデミックインフルエンザウイルスの出現を遅らせたという仮説が立てられている(13)。
SARS-CoV-2と他の呼吸器ウイルス、特にインフルエンザウイルスや他のHCoVとの臨床的および集団規模の相互作用については、今後数年の間にモニタリングする必要がある。現在までに、インフルエンザおよびRSVとの感染を含むいくつかのSARS-CoV-2の感染が記録されている(14);しかしながら、複数の病原体の検査は日常的には行われておらず、存在するデータのほとんどは既往症の高い高齢者を対象としたものであり、感染の可能性や重症度の確定的な評価を支持するものではない。パンデミック以前の研究では、複数の呼吸器ウイルスとの同時感染は珍しくないが、重症度の増加とは関連していないことが示されている。
集団規模では、インフルエンザと SARS-CoV-2 の発生が重複する可能性があり、公衆衛生システムに深刻な脅威をもたらしている。季節性インフルエンザは毎年世界中で何百万人もの重症化した感染症を発生させており、この追加の負担は、COVID-19パンデミックによってすでに打撃を受けているシステムに壊滅的な影響を与える可能性がある。逆に、異なる呼吸器ウイルス間の感染様式が類似していることを考えると、SARS-CoV-2の感染を軽減するために採用された非医薬品介入(個人用保護具、社会的距離、衛生状態の改善、屋内での集会の制限)は、季節性インフルエンザの発生の規模を減少させる可能性がある。このような医薬品以外の手段の使用の増加、および可能性のあるウイルス干渉が、最近の南半球の冬の間にインフルエンザの発生率が減少した原因である可能性がある(15)。
多原体システムにおけるさまざまなアウトブレイクの段階と規模は、病原体間の相互作用の力学によって決定される。すなわち、病原体が互いに感染力を高め合う大きな重複段階から、より感染力の強い病原体の相互反応性を中和することによってある株が完全に阻害される段階までです(9)。SARS-CoV-2のポストパンデミックシナリオとして、SARS-CoV-2と他のベータコロナウイルス属(OC43およびHKU1)との間の免疫の持続時間と交差免疫性を想定したモデルがいくつか提案されている(10)。他のベータコロナウイルス属と同様の免疫期間(約40週間)であれば、SARS-CoV-2は1年に1度の大パンデミックを引き起こす可能性があるが、より長い免疫プロファイルは、他のベータコロナウイルス属からの少量の保護的な交差免疫と相まって、ウイルスの見かけ上の消滅につながり、数年後には復活する可能性がある。もちろん、他のシナリオも考えられるが、多くのプロセスが存在し、未解明な点が多いためである。