Vitamin D regulation of the immune system and its implications for COVID-19: A mini review
www.ncbi.nlm.nih.gov/pmc/articles/PMC8135207/
オンラインで2021年5月18日公開
概要
新型コロナウイルスである重症急性呼吸器症候群新型コロナウイルス(SARS-CoV-2)は,現在のパンデミックの発端となったウイルスであり,重篤な呼吸器症状と免疫反応の亢進が主な症状である。SARS-CoV-2の特徴として、急性呼吸困難症候群を引き起こすサイトカインストームを誘発する能力が挙げられる。したがって、ビタミンDのような免疫反応を調整する能力を持つ薬剤は、コロナウイルス感染症2019(COVID-19)の最も深刻な結果を予防または軽減するためのツールとなる可能性がある。ビタミンDは、抗菌作用だけでなく、抗炎症作用も示している。SARS-CoV-2は炎症性サイトカインの放出を促進するが、ビタミンDはこれらの同じ分子の少なくとも一部の放出を弱める。炎症性サイトカインは、COVID-19の臨床現象、特にその最も危険な合併症と関連している。第2に、COVID-19の臨床症状とサイトカインおよび類似の分子との関係について、現在得られているデータを収集し、第3に、コロナウイルスがどのようにして炎症反応を引き起こすかについて、これまでにわかっていることを明らかにし、第4に、COVID-19のリスクと重症度を軽減するためのビタミンDの貢献の可能性について議論する。
キーワード ARDS、カルシジオール、カルシトリオール、サイトカイン・ストーム、パンデミック、炎症、免疫反応、SARS-CoV-2
はじめに
2020年3月11日、世界保健機関(WHO)は、重症急性呼吸器症候群新型コロナウイルス(SARS-CoV-2)を原因とするコロナウイルス感染症2019(COVID-19)を世界的なパンデミックと正式に宣言した1。SARS-CoV-2は、もともと中国の武漢で肺炎患者の集団発生の原因として確認され、瞬く間に世界中に広まった2。2021年1月13日現在、世界中で350万人以上の患者が報告され、約25万人が死亡している3。この憂慮すべき感染症を理解し、その特徴を明らかにし、対策を講じるために、医学界や科学界から多くの努力がなされている。現在、COVID-19に対する治療法が求められているだけでなく、感染を予防したり、少なくとも病気の拡大を抑えたりするための方策を明らかにする必要がある。感染体に対する免疫反応を制御する薬剤は、少なくとも理論的にはCOVID-19の封じ込めに一役買う可能性がある。安価でリスクの低い分子で、免疫反応を調整できるものとして、ビタミンDがある。
ビタミンDは脂溶性のビタミンで、太陽からの紫外線(UV)が皮膚に当たると真皮で合成される。ビタミンDは、葉物野菜、乳製品、魚、人工的に強化された食品からも摂取することができる。内因性に摂取した場合も、食事から摂取した場合も、ビタミンDが生物学的に活性化するためには、さらなる修飾が必要である(図1)。まず、ビタミンDは肝臓で25-水酸化酵素によってカルシジオール、すなわち25-ヒドロキシビタミンD(25(OH)D)に変換される。その後、カルシジオールは腎臓に運ばれ、1α-水酸化酵素によってカルシトリオールとなり、1,25-ジヒドロキシビタミンD(1,25(OH)2D)として知られている4。ビタミンDは代謝活性化されると、血清カルシウムとリン酸レベルのホメオスタシス、骨代謝、免疫系の調節など、体内で多くの役割を果たす。 -7 当然のことながら、ビタミンDの欠乏は、関節リウマチ、1型糖尿病、全身性エリテマトーデス、炎症性腸疾患などの多くの自己免疫疾患と関連しているという研究結果がある。この可能性を探るために、ここでは以下の内容を紹介する。(1)ビタミンDが免疫反応の調節に果たす多くの役割、(2)COVID-19の臨床症状とサイトカインおよび類似の分子との関係についての現在のデータ、(3)コロナウイルスがどのようにして炎症反応を引き起こすかについての知見、(4)COVID-19のリスクおよび重症度の軽減にビタミンDが寄与する可能性。
図1 代謝活性型ビタミンD(1,25(OH)2D)の合成
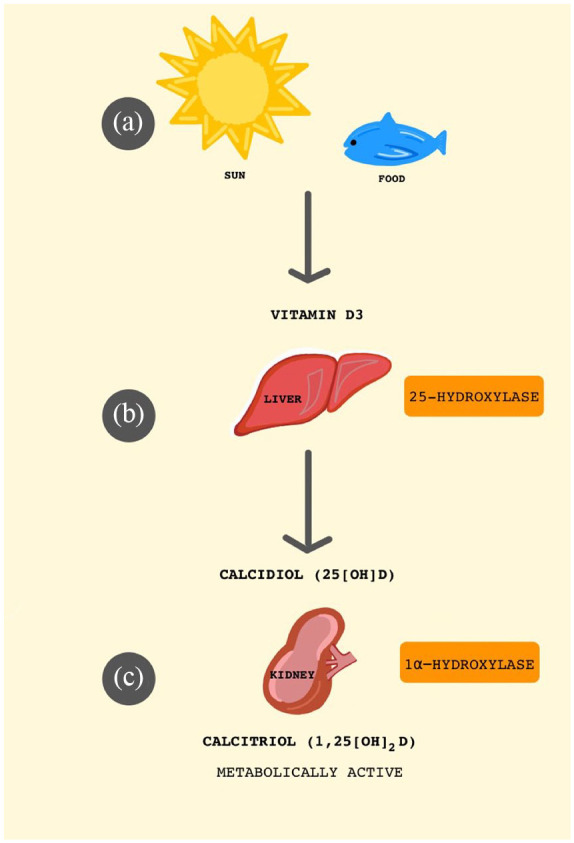
(a) ビタミンDは、太陽からの紫外線(UV)が皮膚に当たると生成されるが、葉物野菜、乳製品、魚、ビタミンD強化食品からも摂取できる。b)ビタミンDは肝臓でカルシジオール、または25-ヒドロキシビタミンD(25(OH)D)に変換される。c)その後、カルシジオールは腎臓に移動し、酵素的にカルシトリオールに変換され、1,25-ジヒドロキシビタミンD(1,25(OH)2D)としても知られている。
方法
MEDLINEおよびGoogle Scholarを用いて、ビタミンD、免疫系、免疫反応、COVID-19,SARS、SARS-Cov-2などの検索語を用いて、最新の文献をレビューした。検索は、英語で発表された研究に限定した。特に、COVID-19の治療にビタミンDが使用されている論文や、ビタミンDレベルが炎症マーカーと関連している論文を見つけることに重点を置いた。ビタミンD、COVID-19,および炎症マーカーに関連する科学論文を見つけたら、このトピックに関するさらなる論文を検索するために、その参考文献を徹底的に調査した。
結果
免疫反応の調節におけるビタミンDの役割
ビタミンDは、免疫系の適応型と自然型の両方を調節するシグナル伝達の役割を担っている。ビタミンDは、BおよびTリンパ球、好中球、単球、樹状細胞(DC)に発現する核内ビタミンD受容体(nVDR)と相互作用することにより、カルシトリオールの形でこのような変化を引き起こす9。さらに、これらの免疫細胞や炎症細胞は、カルシジオールを水酸化して活性型のカルシトリオールに変換する1-α-水酸化酵素(CYP27B1)を発現することにより、カルシジオールをカルシトリオールに変換する能力を持っている9,11。ビタミンDはまた、マクロファージ、単球、ケラチノサイト、上皮細胞、腸管細胞、肺細胞、角膜細胞などにおいて、ディフェンシンβ2およびβ4,カテリシジン抗菌ペプチド(CAMP)などの抗菌ペプチドの産生を誘導する8,9。また、ケラチノサイトや上皮細胞、腸管細胞、肺細胞、角膜細胞では、物理的なバリア機能を強化する。これらの抗微生物作用を総合すると、微生物に対する体の防御力が高まる。8,11
カルシトリオールは、IL-12,IFN-γ、IL-6,IL-8,TNF-α、IL-9などのタイプ1の炎症性サイトカインの産生を抑制することで、Th1免疫反応をダウンレギュレートする。一方、ビタミンDは、IL-4,IL-5,IL-10などのタイプ2の抗炎症性サイトカインの産生を増加させる。8,9 このサイトカインの調節は、主に、NF-kB阻害タンパク質IkBaの増加を介してNF-kB p65の活性化を阻害することによって行われる9。また、ビタミンDは、MHCクラスII分子、共刺激分子、IL-12の発現を低下させることで、DCの分化を抑制する。9 DCの分化・成熟を抑制することは、自己免疫を防ぎ、自己寛容を促進する。9 免疫グロブリンを産生するB細胞において、カルシトリオールはB細胞の分化、増殖を阻害し、アポトーシスを促進する。このことは、抗体が主要な役割を果たす自己免疫疾患の可能性がある場合には、臨床的に重要な意味を持つ。8 これらを総合すると、ビタミンDは少なくともいくつかの免疫反応を制御することができ、その役割はほとんどが抗炎症性であることが明らかになった。
COVID-19の臨床症状
前述のように、SARS-CoV-2(COVID-19)のパンデミックは、世界中の多くの人々の生活に影響を与えている。2019年12月、新規ウイルスによる入院患者3名の不明な呼吸器疾患の最初の症例がWHOに報告され 2020年3月11日までにWHOは新規コロナウイルスの発生をパンデミックと宣言した16,17。SARS-CoV-2がパンデミックと宣言された時点では、ヒトからヒトへの感染により118カ国に広がり、すでに11万8,000人以上の患者が発生していた16。病気の伝染性を判断するためには、主に3つの検討事項を用いて基礎繁殖率(R0)を算出することができる。18 R0の値が1を超える病気はパンデミックする可能性がある。SARS-CoV-2ウイルスのR0は2.2~3.58と推定されており、CoV-2に感染した患者1人につき平均2~4人に病気を広める可能性があることを意味する19,20。
コロナウイルスは、エンベロープ型のポジティブセンスRNAウイルスの一種であり、アルファ、ベータ、ガンマ、デルタの4種類に分類される21。21 SARS-CoVが出現した直後、サイトカインストームが肺の炎症の重症度に大きく関与しているという仮説が立てられた。2005年に発表された論文では、IFN-γがヒト肺上皮細胞株および線維芽細胞株に及ぼす影響を調査し、肺胞上皮細胞は線維芽細胞株よりもIFN-γの影響を受けやすく、IFN-γはFasを介したアポトーシスを促進し、増殖を抑制することを明らかにした22。さらに、どちらの細胞株もT細胞標的サイトカインを分泌することができ、そのサイトカインプロファイルはSARS患者で検出されたものと類似していた。SARS感染後期の急性肺傷害にはIFN-γが関与している可能性が示唆された。MERS-CoV感染者のサイトカインプロファイルは、対照群と比較して、IFN-γ、TNF-α、IL-15,IL-17などの高レベルの炎症性サイトカイン分泌を伴うTh1およびTh17反応を示した23。SARS-CoVとMERS-CoVの両感染症では、免疫系による炎症性サイトカイン反応が亢進し、これが疾患の重症度に関与すると考えられている。
また、CoV-2ウイルスは、SARS-CoVとゲノムの85%を共有していることから、同じウイルスではないものの、両疾患の類似性が示唆されている24。コロナウイルスの感染は人獣共通で、宿主の貯蔵庫となるコウモリが起源であると考えられている25。コロナウイルスは人獣共通感染症であり、宿主であるコウモリに由来すると考えられている25。コウモリからハクビシンやラクダなどの中間宿主動物にウイルスが感染し、SARSやMERSの場合と同様に、牛乳や尿、加熱していない肉などの密接な接触や摂取によって人に感染する25,26。
COVID-19感染症の最も一般的な症状は、発熱、息切れ、乾いた咳などで、通常は5.2日の潜伏期間を経て発症する27。武漢の病院でCOVIDのために入院した41名の患者のうち、32%が基礎疾患(糖尿病、高血圧、心血管疾患)を有していた28。臨床検査の結果、25%の患者で白血球減少(白血球数が4×109/L未満)63%の患者でリンパ球減少(リンパ球数が1. 28 集中治療室(ICU)で治療を受けた患者とそうでない患者の血漿中の炎症マーカー濃度を比較すると、IL-2,IL-7,IL-10,G脳脊髄液、IP10,MCP1,MIPIA、TNFの濃度がICUの患者で高かった28。武漢の 2 つの病院で COVID 患者 191 名を対象に行われたレトロスペクティブ・スタディでは、COVID 患者では IL-6 も上昇しており、COVID 生存者に比べて非生存者では IL-6 の量が約 2 倍になってた29。この研究の著者は、最も一般的な合併症は敗血症(59%)で、次いで呼吸不全(54%)ARDS(31%)であることも観察している。29 その他、COVID-19の重症例では、心筋トロポニンI、乳酸脱水素酵素、リンパ球減少が増加していることが191名の患者で確認された。COVID 患者の胸部 CT 所見では、通常、両側に胸膜下層を含まない ground glass opacity が認められる。30,31 入院中の COVID 患者 138 名を対象としたレトロスペクティブ・スタディでは、下痢や吐き気などの非典型的な症状、高齢であること、重症患者には基礎疾患があること、ARDS、不整脈、ショックを併発する可能性があることなどの知見が得られた。フランスのICUでSARS-CoV-2患者34名を対象とした研究では、炎症反応の亢進と固定化が原因と思われる血栓イベントの増加が観察され、27名の患者に深部静脈血栓症(DVT)が確認されたと報告されている32。COVIDが原因でARDSに罹患した患者150名を対象とした別の研究では、COVIDが原因ではないARDS患者と比較して、血栓イベント(主に肺塞栓症)が有意に多く観察された(11.7%対2.1%、p<0.008)。また、両試験の患者は、フィブリノゲンとDダイマーのレベルが上昇していた32,33。
COVID-19の治療については、現在も精力的な研究が行われている。軽度の症例に対する現在の標準治療は、主に支持療法であり、臨床症状の緩和と合併症の回避に重点が置かれている。コルチコステロイドとレムデシビルは、COVID-19 の中等度および重度の症例において、疾患の進行と死亡率を抑制する34。しかし、ICU への入室を必要としない患者に、インターフェロンα、イトリズマブ、ソホスブビル+ダクラタスビル、アナキンラ、回復期血漿のいずれかを投与すると、死亡率が低下する34。
このパイロット研究では、COVID-19 が確認された患者に 25(OH)D を経口投与することで、ICU 治療の必要性が回避されることがわかった。さらに、ビタミンDを投与しなかった25名の患者のうち2名が死亡したが、投与した50名では死亡例はなかった。著者らは、この分野ではさらなる研究が必要であることを認めつつも、ビタミンDがCOVID-19の重症度を軽減することを示唆している。確立された治療法がないため、現在流通しているワクチンの有効性と安全性に大きな期待が寄せられている37。
COVID-19と免疫反応
38-40 ACE2は、SARS-CoVとSARS-CoV-2の両方の細胞受容体である。38,39 ウイルスが宿主細胞に侵入すると、ウイルスRNAを排出し、複製を開始する。ウイルスが宿主の免疫系に検出されるためには、病原体関連分子パターン(PAMPs)やキャップされていないRNAが、エンドソームRNA受容体、細胞質RNAセンサー、トール様受容体3および7(TLR3,TLR7)レチノイン酸誘導遺伝子1(RIG1)メラノーマ分化関連タンパク質5(MDA5)などのパターン認識受容体(PRRs)によって検出される必要がある。 38-40 PRRが活性化されると、一連の下流シグナルが発生し、NF-κBとI型インターフェロンが活性化され、炎症性サイトカインと抗ウイルスタンパク質がそれぞれ産生されるようになる。 -40 例えば、TLR7は骨髄分化因子88(MyD88)を活性化し、キナーゼ複合体(IKK/IKK)を刺激してNF-κBを誘導し、炎症性サイトカイン(TNF、IL-6,IL-12)の転写を増加させる41。しかし、MERSやSARSなどの高病原性コロナウイルスは、インターフェロンの活性化を阻害し、自然免疫系を阻害しているようである。
コロナウイルスが宿主の自然免疫反応を阻害するもう一つのメカニズムとして、非特異的タンパク質(NSP)1-16が提案されている42,43。NSP1は、ヒトに感染するコロナウイルスの主なグループであるαおよびβコロナウイルスにのみ存在することから、特に注目されている43。SARS-CoVでは、NSP1が宿主の40Sリボソームサブユニットに結合して翻訳を阻害するとともに、末端核酸分解的にmRNAを切断することで、INF-βの発現を阻害する可能性が高い43,44。
レニン-アンジオテンシン系(RAS)は、よく知られているように、血管収縮や血圧に作用するだけでなく、炎症にも関与している45,46。RASが活性化されると、アンジオテンシンIIの濃度が上昇し、NF-κBの活性化を介して炎症が誘発され、さらにTNF、IL-6,IL-12などの炎症性サイトカインが刺激される41,45。SARS-CoV-2によるACE2の低下は、アンジオテンシンIIの蓄積を促進して炎症サイクルを維持し、急性肺障害やARDSを引き起こす可能性がある45,47。状況によっては、ビタミンDがRAS活性化の原因分子の一つであるレニンを低下させることがある45,48,49。
また、SARS-CoVは、重症患者においてIFN-γ、IL-1,IL-6,IL-8,IL-12,IP-10,MCP-1のレベルを上昇させ、肺障害を引き起こすことが知られている50。同様に、SARS-CoV患者では、Th1を介した免疫反応が過剰に活性化され、ナチュラルキラー(NK)細胞や多形核好中球(PMN)が増加することで、肺損傷が引き起こされる50。このようなSARS-CoVによる炎症反応の高まりは、現在知られているSARS-CoV-2と密接に対応している。SARS-CoV-2の重症患者では、IL-2,IL-6,IL-7,IL-10,G脳脊髄液、IP10,MCP1,MIPIA、TNFの濃度が高かった28,29。このようなサイトカインの流入により、炎症反応が亢進し、その結果、実質的な損傷が生じ、最終的にARDSへと進行する。
考察
COVID-19のパンデミックは 2020年8月現在、世界中で2,000万人以上の感染者と80万人近くの死亡者を出している。残念ながら、現時点では、COVID-19の重症例を含めて、治療法の選択肢はほとんど模索中である。
最良の治療法は、他の病気と同様、予防である。現在、流通しているSARS-CoV-2に対するワクチンには大きな期待が寄せられている。しかし、COVID-19を予防するために、あるいは最も深刻な合併症を軽減するために、並行してできる他の手段はないのだろうか?この疑問から、私たちや他の研究者は、ビタミンDの効果を詳しく調べてみた。
ビタミンDは、その安全性や、ビタミンDの補給が呼吸器疾患の予防や改善につながるというデータがあることから、治療の代替手段として注目されている(レビューは、Grantら51を参照)。さらに、最近の文献では、ビタミンDの補給、パーキンソン病、COVID-19の関係が検討されている52。この研究では、ビタミンD3を毎日補給することで、パーキンソン病の進行を遅らせ、COVID-19を予防できる可能性があると結論づけている。 52 驚くことではないが、何人かの著者は、COVID-19による合併症を予防したり、少なくとも弱めたりするための潜在的な代替手段として、ビタミンDの補給を提案している45,51-53。この研究では、25(OH)Dの経口投与により、SARS-CoV-2による感染が確認された患者のICUへの入室回数が減少し、さらには死亡者数も減少したことが報告されている36。また、最近行われた高齢の介護施設入居者を対象とした探索的研究では、COVID-19と診断された前月または直後にビタミンD3を80,000IU経口投与すると、死亡率が有意に低下することがわかった54。その後、同じ研究チームは、研究結果を拡大し、ビタミンD3のボーラス投与を毎月行うか、2~3カ月に1回行うかで、COVID-19の転帰と重症度が改善するかどうかを比較した55 。定期的にビタミンD3のボーラス投与を受けた高齢者は、ボーラス投与を1回しか行わない患者やビタミンD3を全く摂取しない患者に比べて、生存率が高く、COVID-19の重症度も低かったのである。高用量のビタミンD3は、若年層にも有効であることがわかっている。SARS-CoV-2の検査で陽性となった36~51歳のビタミンD3欠乏症の成人を対象に,60,000IUのコレカルシフェロールを1日7日間経口投与する群とプラセボを投与する群に無作為に割り付けた。ビタミンD3の補給を受けた人の60%以上が21日後にSARS-CoV-2を陰性化したのに対し、対照群では20.8%しか陰性化しなかった56。さらに、経口コレカルシフェロールはフィブリノーゲンレベルを有意に低下させたが、Dダイマー、プロカルシトニン、C反応性タンパク質などの他の炎症マーカーは変化しなかった。
ビタミンDがCOVID-19の治療に関連する因子であることを示唆する別の証拠は、関連研究から得られている。複数の独立した研究チームが、血清中のビタミンD濃度の低さがCOVID-19の重症化と関連していることを明らかにしている57-59。一方で、ビタミンD欠乏症の患者では死亡率が高くなることを示すデータも再現されている58-60。実際、27の発表論文のメタアナリシスでは、ビタミンD欠乏症はSARS-CoV-2の感染リスクの上昇とは関連していないものの、ビタミンDの低下はCOVID-19による死亡率を高めると結論づけられている61。
また、ビタミンDの欠乏は、SARS-CoV-2の存在下での炎症反応の増加と関連している。IL-6,TNF-α、フェリチンなどの炎症マーカーは、血清中の25(OH)D濃度が20ng/mL未満のCOVID-19患者では、血清中の25(OH)D濃度が20ng/mL以上のCOVID-19患者に比べて高いことがわかっている58。別の研究では、COVID-19の非生存者は、同じ施設に入院している生存者と比較して、高感度C反応性タンパク質、フェリチン、IL-6,Dダイマー、フィブリノーゲン、プロカルシトニンの値が高く、25(OH)Dの値が低いことが報告されている60。COVID-19の重篤な合併症は、IFN-γ、IL-2,IL-6,IL-8,IL-10,IL-12,TNFなどの炎症性サイトカインの上昇を介した免疫反応の亢進に少なくとも部分的には関係していると考えれば、これは驚くべきことではない。このような状況下で、ビタミンDがこれらのサイトカインをすべてダウンレギュレートするという報告があることから、ビタミンDの免疫調整作用は有用であると考えられる(表1)。さらに、SARS-CoV-2がACE2に結合することも、急性肺障害に関連した炎症の引き金になると提案されている45。臨床データによると、ビタミンDはRASの調節障害に対抗できるため、ACE2のレベル低下による炎症を食い止めることができるとされている45,48,49。
表1 SARS-CoVによって増加したサイトカインと、ビタミンDによって低下したサイトカインの比較
| SARS-CoV によって増加したサイトカイン | 参考資料 | ビタミン D によってダウンレギュレーションされるサイトカイン | 参考資料 |
|---|---|---|---|
| IFN-γ | ウォン他、2004 50 セロン他、2005 22 |
IFN-γ | サッシ他、2018 8 コロッタ他、2017 9 |
| IL-8 | ウォン他、2004 50 セロン他、2005 22 |
IL-8 | コロッタ他、2017 9 |
| IL-6 | ウォン他、2004 50 周他、2020 29 |
IL-6 | サッシ他、2018 8 コロッタ他、2017 9 |
| IL-12 | ウォンら、2004 50 | IL-12 | コロッタ他、2017 9 |
| IL-1 | ウォンら、2004 50 | IL-17 | サッシ他、2018 8 コロッタ他、2017 9 |
| TNF | 黄他、2020 年28 | TNF-α | サッシ他、2018 8 コロッタ他、2017 9 |
| IL-2 | 黄他、2020 年28 | IL-2 | サッシ他、2018 8 |
| IL-18 | セロンら、2005 年22 | IL-9 | コロッタ他、2017 9 |
| ミグ | セロンら、2005 年22 | IL-4 | コロッタ他、2017 9 |
| IL-10 | ウォン他、2004 50 セロン他、2005 22 |
IL-10 | コロッタ他、2017 9 |
| MCP-1 | ウォン他、2004 50 セロン他、2005 22 |
IL-5 | コロッタ他、2017 9 |
SARS-CoV:重症急性呼吸器コロナウイルスのこと
COVID-19におけるビタミンDの潜在的な有用性に関する予備的な証拠があるものの、明確な結論を出すためにはより大規模な臨床対照研究が必要である36。ビタミンDの補給をどのように進めるべきかなど、他にも多くの疑問が残っている。ビタミンDは、ビタミンD欠乏症の人に適応されるべきであると考えるのが妥当だと思われる。ビタミンD欠乏症は、米国医学研究所によって、25(OH)D値が20ng/mL未満と定義されている62。米国医学研究所の2011年のガイドラインによると、血清25(OH)D値が20ng/mL以上になるように、70歳未満の人には1日600IU、70歳以上の人には1日800IUを補給することが推奨されている62。
その結果、高カルシウム血症、高カルシウム尿症、血管石灰化などの副作用が現れる可能性がある。63,64 現在、COVID-19の予防または治療に使用するビタミンDの量については、コンセンサスが得られていない。現在、COVID-19の予防または治療に使用するビタミンDの量については、ほとんどの専門家がビタミンDの補給を推奨しており、いくつかの戦略が提案されている65-67。必要に応じて1日4000IUを処方したり、毎月最大10万IUを3年間補給するなどの他のアプローチをとる場合は、専門家によるモニタリングが必要です66,67。
制限事項
COVID-19患者におけるビタミンDの免疫調節効果に関する直接的な証拠はまだない。ここでは、SARS-CoV-2に感染した患者を対象とした関連研究や、試験管内試験および齧歯類の実験から得られたデータに依拠している。COVID-19の治療法の一環としてビタミンDを検証した臨床試験は、40人から77人の患者を集めただけの小規模なものである。また、使用したビタミンDの用量は試験によって大きく異なっていた。
結論
COVID-19に対する効果的な治療法の探求は依然として続いている。SARS-CoV-2によって引き起こされる免疫反応を調節できる薬剤は、有望な選択肢である。したがって、COVID-19に対するビタミンDの有効性がすでに予備的に証明されていることを考慮すると、ビタミンDの免疫調節能力はさらに検討されるべきである。
