Understanding COVID-19 Pandemic: Molecular Mechanisms and Potential Therapeutic Strategies. An Evidence-Based Review
www.ncbi.nlm.nih.gov/pmc/articles/PMC7802346/
Reem Hanna,1,2 Snehal Dalvi,1,3 Tudor Sălăgean,4 Ioana Delia Pop,4 Ioana Roxana Bordea,#5,* and Stefano Benedicenti#1,*.
要旨
当初、SARS-CoV-2ウイルスは肺炎ウイルスと考えられていたが、過去8ヶ月間に発表された一連の査読付き医学論文によると、このウイルスは脳、心臓、腸、神経系、血管系、さらには血流を攻撃することが示唆されている。未だ不明な点も多いが、COVID-19の最新の進展については、現在の科学的文献を客観的に評価する必要がある。本研究の目的は、SARS-CoV-2の現在の分子構造とCOVID-19の前向きな治療法に焦点を当て、文献の批判的なレビューを行うことであった。主な目的は、現在の科学的根拠に基づいた情報を収集し、精査し、客観的に評価するとともに、現在進行中のトピックの最新の概要を提供することであった。著者らは、ワクチンや光線療法を含む、単剤療法として、あるいは現在の治療モダリティとの併用など、将来性のある治療法の可能性を強調した。著者らは、SARS-CoV-2ウイルスの疫学的、病原性、臨床症状の観点から、SARS-CoV-2ウイルスに関する知識と理解が進化しており、最終的には効果的で安全な治療と信頼性の高い強力なワクチンの製造に向けた戦略的な道筋を示していることから、本レビューは質の高いエビデンスを生み出しており、臨床科学界が将来の参考として活用できると結論づけた。
キーワード:SARS-CoV-2, COV-2, COV-2 SARS-CoV-2,COVID-19,ウイルス病原性、サイトカインストーム、診断法、免疫療法、ワクチン、抗ウイルス、光生体調節療法、PBMT、光力学療法、PDT、臨床試験
まとめ
- SARS-CoV-2 ウイルスの伝播は、人獣共通感染起源の可能性を示している。現在進行中の研究活動の進歩は、COVID-19のさらなる可能性のある動物宿主を特定しようとしている。
- 小児COVID-19で古典的川崎病(KD)が確認されている。
- 新しい疫学的事実、ウイルスの性質、ウイルスに対する免疫応答、ワクチン生産における課題が日々浮上している。
- 前向きな治療法:細胞療法、ACE2(レニン・アンジオテンシン系の重要な構成要素;RAS)をRASの阻害剤で治療したもの;ACEIおよびAT1R。
- 光療法は、堅牢な臨床試験の対象となるCOVID-19管理における潜在的な治療法として考慮することができる。
はじめに
世界保健機関(WHO)が重症急性呼吸器症候群コロナウイルス2(SARS-CoV-2)ウイルス感染症をパンデミックと宣言して以来、研究者や科学者は、コロナウイルスの新規行動、臨床症状、宿主-ウイルス相互作用、宿主免疫応答への影響を理解するとともに、最適な治療法を確立し、安全で効果的なワクチンの製造を試みるために、驚異的な努力を続けていた。2020年10月20日現在、約40,472,505例がコロナウイルス疾患2019(COVID-19)で陽性と判定され、その中には1,119,283人の死亡例が含まれている1.当初、SARS-CoV-2は呼吸器系ウイルスと考えられてたが、過去8ヶ月間に発表された一連の査読付き医学論文から、このウイルスは血流を介して脳、心臓、腸、血管系を攻撃することが示唆されている2. -4 血管内皮を侵す主な原動力はスパイク蛋白質(S)であり、これがアンジオテンシン変換酵素2(ACE2)と結合してサイトカインストームを引き起こす5-8。そのため、ウイルスを早期に発見するための信頼性の高い診断方法や、本疾患の拡大を抑制するための効果的で安全な治療法は、世界中の臨床医や研究者の課題となっている。現在のCOVID-19患者の管理は、緩和治療と臓器機能の回復である。現在までに、3652件以上の研究が clinical trials.govに登録されており、有効な治療法や安全で強力なワクチンの確立を目指して、多数の試験が進行中である12。したがって、最終的な治療法であるCOVID-19ワクチンが開発されるまで、代替療法の発見のための探求は続くだろう。
このレビュー記事の目的は、COVID-19に関する現在の知識と理解を統合することで、病気の進行に関する最新の情報を批判的に評価することである。主な目的は、利用可能な科学的根拠に基づいた情報を収集し、精査し、客観的に評価し、抗ウイルス治療モダリティの概要を提供することであった。
疫学
由来
SARS-CoV-2の起源は完全には解明されていないが、この発生の初期段階では、患者の大多数が華南市の生きた動物または「湿った」市場である華南海鮮市場との関連性を報告しており、人獣共通感染性のウイルス起源を示唆している9,10。さらに最近、SARS-CoV-2の全ゲノムワイドヌクレオチド配列が、中間的なカブトコウモリ(Rhinolophus affinis)CoVから分離されたSARS様CoVと96%同一であること、および中国のカブトコウモリ(Rhinolophus sinicus)から分離された2つのSARS様CoVと89%同一であることから、SARS-CoV-2はおそらくカブトコウモリに見られる株から進化したものであることを示唆するゲノム解析を行った研究がいくつか報告されている。 13,14 一部の研究者は、元の株の突然変異がヒトに対する病原性を直接誘発した可能性があるため、コウモリとヒトの間に増幅する哺乳類宿主の中間体が存在する可能性には疑問が残ると考えている15。相反するように、注目すべき研究では、SARS-CoV-2がパンゴリンから分離され、パンゴリンで発見されたCoVゲノムはSARS-CoV-2と約85.5~92.4%の類似性を示しており、パンゴリンがSARS-CoV-2の中間宿主である可能性を示唆している16。
物理化学的特性
17 このウイルスは、湿度や温度にもよるが、段ボールでは 24 時間、プラスチックやステンレススチールの表面では約 72 時間の半減期を持ち、数時間から数日の間、さまざまな表面で生存し、検出されることがある18,19 。99.99%のウイルス低減を達成するためには、エーテル(75%)エタノール(95%)イソプロピルアルコール(70~100%)次亜塩素酸ナトリウム(0.21%)過酸化水素(0.5%)ポビドンヨード(0.23~7.5%)などの製品(グルコン酸クロルヘキシジンを除く)に1分間曝露することで表面を除染することができる18,20。石鹸や洗剤は泡を形成し、ミセルと呼ばれる泡状構造を形成し、これがウイルスの脂肪保護層を分解し、水で洗い流すことでウイルスを不活性化し、皮膚表面だけでなく他の表面からも分離することがわかっている18 。
臨床症状と疾患の進行
COVID-19の臨床症状に関するエビデンスに基づいた文献によると、疾患のステージや症状の重症度、対応するケアの状況は感染者によって異なることが示されている(図1)2,3,21-23。感染者の約15%に発熱、咳、呼吸困難などの症状が見られた10 が、あまり一般的ではない症状は、喀痰、咽頭痛、消化器症状、胸痛、錯乱、めまい、頭痛、鼻づまり、喀血、結膜炎、皮膚症状、食欲不振などであった10。10 感染者全体の約90%が複数の症状を呈している。今回の所見は、発症時とウイルス感染直後を基準としたもので、感染者は誰もが無症状の状態にあることを明らかにしたものである2 。2,4 鼻咽頭スワブと初期の免疫マーカーが陽性であることから、SARS-CoV-2 の存在が明らかになり、この段階では臨床症状が優勢となる。この場合、患者は自宅で隔離され、多くの場合、自己隔離を求められ、医療従事者による継続的なモニタリングを受けるか、対症療法を受けることになる。この場合、ウイルスが効果的に抑制され、上気道に疾患が封じ込められ、その後回復期に入る3が、残念ながら、残りの20%の人たちは併存疾患があり、免疫抑制症4とみなされ、進行期に入る。重症化すると、胸部CT(Computed Tomography)で低酸素に伴う「グランドグラス」肺浸潤が検出され、急性呼吸窮迫症候群(ARDS)や多臓器不全へと進行していく(図1)2,4。COVID-19の重症患者は軽症患者に比べて感染力が強いが、潜伏期間中の無症候性感染者は感染を拡大させる能力を持っていることが指摘されている2,3。現在、いくつかの横断的研究で無症候性感染症の有病率が高いことが報告されているが、現時点では無症候性患者の検査が日常的に行われていないため、無症候性感染症と症候性感染症の比率は不明確であり、さらなる検討が必要である22。
図1 修正した模式図には、COVID-19の臨床症状、診断検査、重症度の評価、それに応じたケア設定の検討が示されている
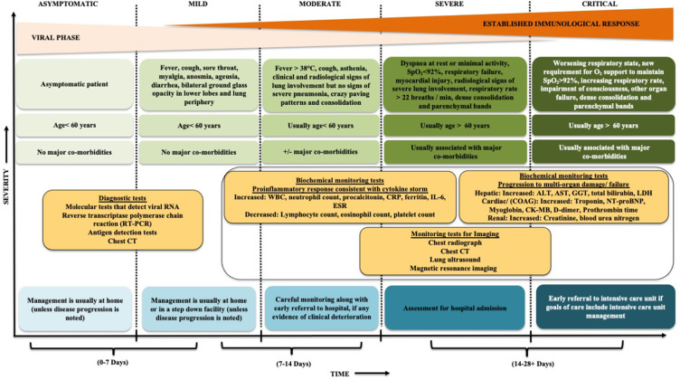
2,3,21-23
影響を受けやすい人口
注目すべき研究では、すべての集団が一般的に SARS-CoV-2 に感染しやすいことが指摘されている。心血管疾患(心血管疾患)糖尿病(DM)肥満などの併存疾患のある高齢者は、免疫機能と反応が低く9-11,損傷した上皮の修復ができず、粘膜のクリアランスが低下しているため、肺ガス交換ユニットへのウイルスの急速な移行、さらには複数の臓器へのウイルスの移行を引き起こす危険性が高いことは事実です24。中国疾病管理センター(CDC(アメリカ疾病予防管理センター)(アメリカ疾病予防管理センター))が発表した報告書によると、30~79歳の年齢層が最も深刻な影響を受けたとされている25。11,26,27 また、SARS-CoV-2 に感染した妊婦や生まれたばかりの赤ちゃんも重症肺炎を発症しやすいことがわかっている。最近まで、幼児の重症例は報告されておらず、強い自然免疫反応が疾患転帰の重要な要因であると考えられてた9 。しかし、COVID-19と川崎病(KD)との関連性を示す驚くべき新たな証拠が報告されている29 。KDとCOVID-19との関連は単なる偶然の一致ではなく、COVID-19と他のヒトCoVとの相関性の報告が過去に確立されているからである30 。この意味で、小児科におけるCOVID-19管理の明確な行動ラインを確立するためには、さらなるエビデンスが重要である。11,26,27 CDC(アメリカ疾病予防管理センター)(アメリカ疾病予防管理センター)は、農村地域に住む人々、ホームレス経験者、新たに定住した難民、介護施設や長期療養型医療施設、障害者グループホームに住む人々はCOVID-19感染のリスクが高いことが示されており、特別な予防措置をとる必要があると述べている。最近のエビデンスでは、Bacille Calmette-Guérin(BCG)ワクチンが、SARS-CoV-2による感染症とその後の重症化を軽減するための潜在的な役割を果たす可能性があることが強調されている32 。
感染経路(疾患スペクトラム)
しかし、感染経路はこれだけではない可能性がある33 。これは、目、口、鼻の粘膜に直接または間接的に接触することで起こる34 。さらに、最近のエビデンスでは、エアロゾルの発生に伴う空気感染経路が本疾患の原因であることが示されている34 。SARS-CoV-2はエアロゾル中で約3時間生存可能であることが明らかになっている24。
潜伏期間
SARS-CoV-2の平均潜伏期間は3~7日(範囲:2~14日)であり、新規コロナウイルスCOVID-19の現在の公式推定潜伏期間を示している35 。 38 2020年1月4日から 2月24日までに報告されたCOVID-19の確定症例のプール分析によると、潜伏期間は5日間であることが米国ジョンズ・ホプキンス大学の研究グループによって示唆されている35。これらの著者らは、SARS-CoV-2の潜伏期間が、カナダの研究グループの知見と一致したSARS-CoV(平均5日、範囲:2~14日)やMERS-CoV(平均5.7日、範囲:2~14日)と一致していることを示唆している39。議論の的となっているのは、24日、41 27日、42,19日と非常に長い潜伏期間を持つ症例が報告されていることである。
病理組織学的特徴
しかし、SARS-CoV-2感染者の肺組織標本の病理組織学的検査では、ヒアリン膜の形成と間質性単核球炎症性浸潤を伴う気胸細胞の脱泡が認められ、ARDSを示唆するものであった44。また、肺胞内腔には多核化した巨大細胞が認められ、ウイルスの細胞病理学的変化を示唆するものであった44。著者らは、COVID-19症例の剖検後に観察されたさまざまな臓器における最新の病理組織学的変化を評価した45の研究を批判的に評価している。その結果、呼吸器系と免疫系が最も影響を受けているが、心血管系、泌尿器系、消化管系、生殖器系、神経系、腸管系などの他の臓器にも病理組織学的に有意な変化が見られ、特に高齢者や併存疾患を有する症例で顕著な変化が見られると結論づけている46。
診断検査と画像診断の特徴(胸部CT提示)
COVID-19の患者は、胸部CTスキャンで以下のような変化を示すことがある:両側の肺実質地ガラスの不透明性、肺の圧密と結節、両側のびまん性分布、時に丸みを帯びた形態と肺末梢の分布。疾患の重症度が進行すると、気管支に変化が観察され、徐々に肺全体に変化が見られるようになり、まれに胸膜の層間肥厚や胸水の貯留が見られるようになる。
SARS-CoV-2の迅速かつ正確な検出は、時間との戦いに勝つために不可欠である。21 SARS-CoV-2 の検出を容易にするために、鼻咽頭および口咽頭スワブ(便、喀痰、血液サンプル)の RT-qPCR またはウイルス遺伝子の配列決定が行われてきた49 。しかし、この検査法には、検体採取が困難であること、医療従事者との密接な接触が必要であり、伝染のリスクを高める可能性があること、出血の開始、嚥下反射などの欠点がある21,50。さらに、COVID-19 の検出はサンプルの部位によって異なることが示されている51 。唾液中のウイルスの検出も証明されており、唾液は、非侵襲的なサイトとして、診断し、感染率をモニタリングするために役立つかもしれないことを示唆している。これらの知見とは対照的に、血清学的検査(抗体検査)を用いることで、COVID-19に感染したことがあり、回復したかどうかを確認することができる54 。診断ツールとしてSARS-CoV-2の合成的に製造されたRNA断片を使用する研究は目覚ましい進歩を見せており、将来的には有望な役割を果たす可能性がある55 。
病態生理と病因発生
SARS-CoV-2の一般的な特徴的特徴と形態
コロナウイルス科(Orthocoronaviridae亜科:Orthocoronaviridae、順序:Nideovirales)は、電子顕微鏡下で観察されるように、エンベロープされた、ノンセグメント、ポジティブセンスの一本鎖RNAウイルスの大規模な家族です15。15,17 このウイルスファミリーは、遺伝子型的にも血清型的にも、α-コロナウイルス(α-CoV)β-コロナウイルス(β-CoV)δ-コロナウイルス(δ-CoV)γ-コロナウイルス(γ-CoV)に分類されている15,17。ヒトの CoV 感染症は、特に α-および β-CoV によって引き起こされる。SARS-CoV-2 は、その前身である重症急性呼吸器症候群コロナウイルス(SARS-CoV)や中東呼吸器症候群(MERS-CoV)と類似したβ-CoVに属している15 。15 ウイルスが保有する数種類のタンパク質のうち、SARS-CoV-2 の構造タンパク質は、スパイク表面糖タンパク質、膜タンパク質、エンベロープタンパク質、ヌクレオカプシドタンパク質の4つで、これらのタンパク質の集合体と感染性の基礎となるものである21 。
スパイク蛋白質の構造と機能
CoVは、エンベロープ上にスパイク表面の糖タンパク質が存在することから、王冠を意味するラテン語の “coronam “に由来する特異的な名前である15 。宿主プロテアーゼは、スパイク蛋白質を、一次接着のためのN末端S1領域とウイルス注入のための膜結合C末端S2領域に切断する可能性を持っている。S1サブユニットのこれら、2つの状態は、ダウンコンフォメーション(受容体のアクセス不可能な状態)とアップコンフォメーション(受容体のアクセス可能な状態)とみなすことができる5,7。これにより、S2サブユニットの高度に安定な融合後のコンフォメーションへの移行が促進される。8 宿主細胞へのすべてのウイルスコンテンツの転送に続いて、ウイルスRNAは複製のために核に入り、ウイルスタンパク質を生合成する。56 研究者らは、スパイク蛋白質の構造と機能を理解することで、様々な抗ウイルス薬の開発や、近い将来のワクチンの直接開発に役立つと楽観視している。
SARS-CoV-2ウイルス相互作用に対する宿主防御
当初、SARS-CoV-2は、ウイルス構造スパイク(S)タンパク質を介して鼻・気管支上皮細胞、肺胞上皮I型・II型肺細胞、毛細血管内皮細胞を標的とし、免疫系の炎症経路を活性化して炎症反応を開始する58,59。宿主細胞内に存在するアンジオテンシン変換酵素2(ACE2)にスパイク蛋白質が結合していることが科学的に証明され、ACE2はSARS-CoVの機能的受容体であることが明らかになった60。61 SARS-CoV-2 の宿主細胞への侵入は、宿主細胞、特に肺胞上皮Ⅱ型肺炎球細胞に存在する 2 型膜貫通型セリンプロテアーゼ(TMPRSS2)による ACE2 の切断によって促進される。 -63 -63 自然免疫と適応免疫(体液性免疫と細胞介在性免疫)の両方からなる炎症反応は、リンパ増殖を阻害し、Tリンパ球細胞のアポトーシスを増加させ、重篤なリンパ球減少症を引き起こす可能性がある。
サイトカインは炎症過程の重要な部分であり、生来のマクロファージ、樹状細胞、ナチュラルキラー細胞、適応性Tリンパ球やBリンパ球を含むいくつかの免疫細胞によって産生される。67 ウイルス負荷が増加すると、誇張された異常な宿主免疫反応が起こり、免疫細胞、リンパ球、マクロファージの継続的な活性化と拡大をもたらし、膨大な量のサイトカインを産生し、結果としてサイトカインストーム(CS)を引き起こし、生命を脅かす重篤な状態になる。CSに関連する臨床所見は、インターロイキン-1(IL-1)IL-6,IL-18,IL-10,IFN-γ、腫瘍壊死因子α(TNF-α)などの炎症性および抗炎症性サイトカインの作用と関連しており、これらはCOVID-19患者の血清中に上昇している68。IL-6とTNF-αは、CSとその結果として起こる一連のイベントの主要な役割を果たしていると認識されている67。
感染の後期になると、ウイルスの複製が促進され、サイトカインレベルが指数関数的に上昇し、マクロファージ、単球、好中球、T細胞などの他の免疫細胞が循環から感染部位に流入してく。次のような様々な破壊的な事象が起こり始める。上皮内皮バリアの不安定化、血管バリアの損傷、毛細血管損傷、肺毛細血管内皮細胞への感染拡大、びまん性肺胞損傷。肺胞壁のびまん性の肥厚、単核細胞やマクロファージの浸潤による空隙への浸潤、ヒアリン膜の形成による肺胞腔内への肺水腫、肺胞-毛細血管酸素伝染の機能不全、および酸素拡散能力の低下(図2)。 44,64 肺損傷は、初期の急性呼吸窮迫症候群(ARDS)またはそのより重篤な形態へと進行する可能性のあるサイトカインストームの結果の一つである。
図2 修正された模式図は、COVID-19の病因および病態生理を示す
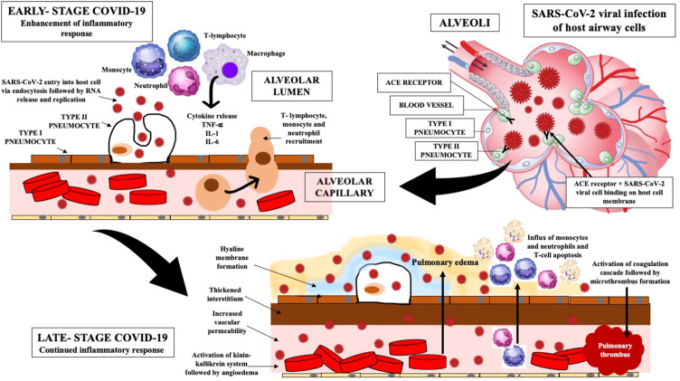
(Wiersinga er al)。64からのデータ
COVID-19の重症度がさらに進行すると、補体系の不均衡な活性化が凝固カスケード、内皮細胞および血小板を刺激し、線溶を阻害し、微小血栓の形成および重症患者における血栓性合併症の高い発生率をもたらす69,70。疾患の進行は、ウイルス性敗血症を媒介とした宿主免疫応答の異常(重篤な臓器機能障害)を引き起こし、多臓器不全の一因となる可能性がある。9,10,71 低酸素飽和度をもたらすARDSは、COVID-19患者の多臓器不全と死亡の主な原因となっている。SARS-CoV-2媒介性CSの治療には,COVID-19患者の罹患率と死亡率を低下させるために,いくつかの抗ウイルス薬と抗炎症薬の治療法が提案されており,本レビューではこれらの治療法の包括的なレビューと批判的な評価を行った。
COVID-19治療の現在のシナリオ
管理全般
現在のところ、COVID-19の管理に関する決定的な治療プロトコルは存在しない。治療の一般的なラインは症状の緩和を確立することを中心に展開される:十分なベッドレスト、良好な水分-電解質バランスの維持、バイタルサイン(体温、心拍数、酸素飽和度、血圧、脈拍、呼吸数)のモニタリング21,73 これらとは別に、疾患の重症度に関係なく、すべての患者が抗酸化物質を豊富に含む食品を十分に摂取し、栄養価の高いバランスのとれた食事を摂取する必要があることに注意することが重要だ。
抗ウイルス療法
特定の抗ウイルス薬や薬物療法は現在までに確立されていないが、COVID-19の症状緩和を得るために、様々な抗ウイルス治療薬が世界中で試行され、変動する結果が得られている17。17,74 COVID-19の管理に利用されている抗ウイルス治療薬の長所と短所を表1に示し、以下に詳細なレビューを示す。
表1 COVID-19管理における治療戦略の利点と欠点
| 治療法 | カテゴリー | 一般名 | 利点 | 欠点 |
|---|---|---|---|---|
| 抗ウイルス療法 | 抗ウイルス性サイトカイン | INFαとINFβ 81 | 幅広い抗ウイルス活性 ウイルス複製に対する直接的な阻害効果を示し、明確なウイルス感染に対する免疫応答をサポートする幅広い抗ウイルス INFβはINFαよりも忍容性が高い 有害な出生結果の兆候はない |
インフルエンザ様症状、吐き気、倦怠感、体重減少、血液毒性、トランスアミナーゼの上昇、精神医学的問題(うつ病や自殺念慮など)。IFNとの最も深刻な薬物間相互作用は、他の免疫調節剤と化学療法剤の併用による追加の毒性の可能性である。 |
| 抗ウイルス薬 | リビバリン89 | 既存の在庫 信頼できるサプライチェーン |
肝障害、ミオパチー、神経障害、骨髄抑制、膵炎 | |
| レムデシビル93 | 短い回復時間 QTc間隔を変更しない 成人の回復までの時間を短縮し、死亡率に影響を与えない |
下痢、発疹、腎不全、低血圧、肝酵素の増加。 | ||
| ロピナビル リトナビル99–101 |
SARS-CoV-2のエンドペプチダーゼC30に結合し、呼吸困難を軽減する能力 | 高脂血症、全身性過敏症症候群、およびアキレス腱障害 | ||
| ネルフィナビル103 | ウイルス抗原のSARS-CoV-2発現の複製を強く阻害した | 吐き気と下痢 | ||
| アルビドール105、106 | 広域スペクトル抗ウイルス薬 SARS-CoVのウイルス複製プロセスをブロック する子供と大人で十分に許容される |
アレルギー反応、吐き気、下痢、めまい、血清トランスアミナーゼの上昇 | ||
| 抗マラリア薬 | クロロキン110、111 | 強力な抗ウイルス効果 広域抗ウイルス薬 安価な薬 優れた患者安全性レポートと耐性レベル ウイルスの侵入を阻止するためのACE2への干渉。ウイルス融合に必要なエンドソームpHの上昇; 軽度の免疫抑制 |
網膜または精神症状 | |
| コルチコステロイド | 糖質コルチコイド | デキサメタゾン115 | サイトカインストームに対する強力な抗炎症作用 抗アレルギー |
食欲増進、神経過敏、睡眠障害(不眠症)足首と足の腫れ(体液貯留)胸焼け、筋力低下、創傷治癒障害、血糖値の上昇 |
| ヒドロコルチゾン115、117 | 抗ショック療法 は、COVID-19で重症の患者を治療するためのデキサメタゾンの代替として使用できる |
創傷治癒が遅い、皮膚が薄くなる、体毛が増える、生理不順、性機能/筋力低下の変化、倦怠感、うつ病、不安、イライラ感 | ||
| 免疫療法 | CPT 120、121 | 過去のパンデミックで使用された、安全で臨床的に効果的で、死亡率を低下させる | 輸血関連急性肺損傷、輸血関連循環過負荷、およびアレルギー/アナフィラキシー反応、感染症の伝播、熱性非溶血性輸血反応、RBC同種免疫、および溶血性輸血反応 | |
| トシリズマブ127–129 アナキンラ131 |
強力な抗炎症作用 | 頭痛やめまい、口内炎、高血圧、高コレステロール血症、アレルギー反応、体重増加や足首の腫れ、胃の炎症や腹痛、免疫系や治癒に影響を与える、好中球減少症、 免疫抑制療法は潜在性結核症やその他の非定型または日和見感染症の再活性化につながる可能性がある感染症 |
||
| 抗体カクテル146、147 | 標的殺害、迅速な症状緩和、迅速な回復、最小限の副作用 | 現在までに遭遇したものはない | ||
| ACE受容体結合戦略169 | 新規SARS-CoV-2受容体として示され、免疫、炎症、ACE2,および心血管疾患の調節に重要な役割を果たす | 現在までに遭遇したものはない | ||
| エキソソーム170、171 | 病気の検出と治療に役立つ 天然ドラッグデリバリービヒクル 高い特異性と効率 |
非効率的な分離方法、特性評価の難しさ、および特定のバイオマーカーの欠如 | ||
| 細胞療法 | MSCは172、173 | 幹細胞は、Chaf1aを介したおよびSumo2を介したエピジェネティックな調節(プロウイルスサイレンシングと呼ばれる)を介してウイルスの活動を抑制することができる ARDSにおける有益な効果 |
MSC送達の最適な用量と経路に関する明確さの欠如、大規模生産と凍結保存の難しさ、および実質的な変動の可能性 | |
| RASブロッカー174 | COVID-19に感染した高血圧患者では、死亡リスクの増加、ICUへの入院、人工呼吸器の必要性、重度または重度の肺炎への進行とは関係なく、子供と大人に安全に使用できる。 | それらの潜在的な害の不十分な証拠とそれらの利益に関する圧倒的な証拠 | ||
| 漢方薬 | 以前のエピデミックで使用され、顕著な症状の緩和、解熱、より速い回復、入院期間の短縮 | 過敏性肺炎、肺損傷、胃腸の不快感を伴う倦怠感 | ||
| 酸化防止剤 | ビタミンCとEが豊富な食品 | 酸化による損傷を予防または軽減 できる心血管疾患のリスクを軽減できる |
皮膚の下にあざ、下痢、めまい、関節痛 | |
| クルクミン | 科学的に証明された健康上の利点 強力な抗炎症作用と抗酸化作用があり、うつ病や関節炎の症状の改善にも役立つ可能性がある |
現在までに遭遇したものはない | ||
| 自然療法 | オメガ3脂肪酸 エイコサペンタエン酸(EPA) ドコサヘキサエン酸(DHA)182 |
抗炎症薬 | EPAとDHAは、活性酸素種によって媒介される非酵素的酸化に対して細胞膜をより感受性にし、潜在的に有毒な酸化生成物の形成をもたらし、酸化ストレスを増加させる可能性がある | |
| マヌカハニー183 | 抗菌 性抗炎症性 創傷治癒を促進する MGOの濃度が高いほど、抗生物質の効果が強くなる。 |
現在までに遭遇したものはない | ||
| 馬鈴薯でんぷん184 | プレバイオティクス効果 | 現在までに遭遇したものはない | ||
| 光線療法 | PDT / a-PDT | 累積的な投与量はない:微生物特異性の欠如と耐性メカニズムの発達212 病原体増殖の不活化を含む食作用プロセスの優れたヘルパー213 咽頭扁桃炎に対する臨床PDTプロトコルは、病気に関連する症状の90%以上を軽減する24時間後に観察された。したがって、PDTはウイルス感染を不活化し、気道内のウイルス量を減らすのに重要だ221 MBを介したPDTは、初期および進行した気管支肺感染症の潜在的な治療法である可能性がある223 ジェットネブライザーデバイスでの3つの光増感剤(ICG、塩素フォトジタジン、およびポルフィリンフォトジェム)の送達は、肺を直接標的にするのに効果的であることが示されている225 効果的、革新的、アクセス可能、費用効果の高い治療法226 死亡率の低下と疾患経過の重症度、COVID-19患者のウイルス量の減少226 安全な輸血を確実にするためのSARS-CoV-2の血漿不活化227 |
現在までに遭遇したものはない | |
| レーザー-PBMT | 抗炎症:サイトカインストームを複数のレベルで軽減し、主要な炎症性代謝物を減少させる189–194 コラーゲンとタンパク質の産生、細胞増殖を増加させ、循環障害を正常化し、浮腫と腫れを減少させ、組織の品質と引張強度を改善する189–194 PBMT肺微小血管漏出、IL-1β、IL-6,および細胞内ROSを低減する。このノートでは、単一または補助治療法としてPBMTは、その抗炎症作用を介してサイトカインストームとARDSを調節することができる196から 199には、 炎症を軽減し、癒しの肺を促進する199、205、206および瘢痕化プロセス最小限に189-194を 免疫機能を改善し、SARS-CoVの-2のサイトカインストームの細胞および分子の活性調節における免疫調節効果を有する200、203、206 それと組み合わせることができる、任意の副作用なしに安全で、効果的な、低コストの様式であるARDSの従来の治療196-199 最小限に人工呼吸器に必要な時間の長さ、COVID-19患者での治癒過程、および短縮回復時間を向上させる199、200 を経由してサイトカインストームとARDSを調節することができる単一または補助治療法としてPBMTその抗炎症作用196–199 酸化防止剤:プロスタグランジンE2,プロスタグランジンエンドペルオキシドシンターゼ-2,IL-1,IL-6,TNFaの用量依存的な減少、ならびに好中球の細胞流入、酸化ストレスを介して炎症に関連する痛みを軽減する201–203 アシドーシスを予防し、 SpOでCOVID-19人の患者の結果における低酸素2 COVID-19肺炎に治癒改善と肺199、205、206、210 、従来の薬物療法と組み合わせPBMTがCOVID-19進行を防止し、症状を改善する可能性を有する200 従来の治療と組み合わせPBMTを重度のCOVID-19および病的肥満の患者では安全で効果的です211COVID-19の進行を防ぎ、症状を改善する可能性がある200 |
現在までに遭遇したものはない | ||
| LED-PBMT | レーザーPBMTと同じ利点がある。しかし、差は、LED-PBMTは、種々の侵入深さを提供する複数の波長のクラスタ化されたプローブを介して非コヒーレント光を送達することである187、188 有用であることができる大きな表面積を照射することができるITISの安全、効率的かつコスト効果的な治療法をCOVID-19管理で。210 |
現在までに遭遇したものはない | ||
抗ウイルス性サイトカイン
抗ウイルスサイトカインは、いくつかのメカニズムを介してウイルスの複製および拡散に対する直接的な抑制効果と、適応免疫を強化し、ウイルス感染に対する宿主の抵抗力を向上させるウイルス感染をクリアするための免疫応答をサポートする両方の効果を示す幅広い抗ウイルス活性を有するタンパク質である75。以前の文献では、SARS-CoVやMERS-CoVの感染を軽減するためにインターフェロンαとβ(INFαとINFβ)を使用することが証明されている75,76。抗ウイルスサイトカイン療法を利用する際によく遭遇する欠点としては、インフルエンザのような症状、吐き気、疲労、体重減少、血液学的毒性、トランスアミナーゼの上昇、精神医学的問題などが挙げられる(表1)。
Zhouらによる非対照の探索的研究では、COVID-19陽性と判定された77名の成人患者に、ネブライザーを用いたIFN-α2b(5ミリ国際単位で1日2回)またはアルビドール(200mgを1日3回投与;tds)またはIFNα2bとアルビドールの併用療法が行われた。著者らは、IFNα2bとアルビドールの併用または非併用でIFNα2bを投与された患者では、IL-6とCRPの血中濃度上昇の持続時間の短縮とともに、上気道における検出可能なウイルスの持続時間が有意に減少したと結論づけている81。同パネルは、以前のコロナウイルス感染症におけるインターフェロンの欠点と、この治療戦略の潜在的な利点を上回る根本的な毒性を強調するための実質的な証拠を提供している82。COVID-19の治療におけるINF1βとレムデシビルの併用は、いくつかの小規模無作為化比較試験(RCT)で評価されているため、今回の試験はより大規模なプラット フォームで行われている83 。
表2 2020年10月20日までにClinicalTrials.govに登録された、COVID-19の治療に抗ウイルス療法を利用した臨床試験を表示
| 研究識別子と引用(上付き文字) | 治療プロトコル | 研究段階; 推定登録数(n) | 主な結果の測定 | 採用状況 |
|---|---|---|---|---|
| NCT04492475 83 | 薬剤:IFNβ1a:rebif(R)は、天然の線維芽細胞由来のヒトIFNβと同一のアミノ酸配列を持つ精製された166アミノ酸のヒトIFNβ糖タンパク質である。0.5 mLのプレフィルドシリンジには、44 µgのIFNβ1a、4 mgのヒトアルブミン、USPが含まれている。27.3 mgマンニトール、USP; 0.4mgの酢酸ナトリウム; 注射用水、USP。 その他:プラセボ:IFNβ1aプラセボには,0.5 mL 0.9%生理食塩水または0.5mL注射用滅菌水が含まれている。 薬物:レムデシビル:修飾アデニンヌクレオシド類似体GS-441,524の細胞内送達用に設計された単一のジアステレオマーモノホスホルアミデートプロドラッグである。有効成分に加えて、レムデシビルの凍結乾燥製剤には、次の不活性成分が含まれている:注射用水、スルホブチルエーテルベータ-シクロデキストリンナトリウム(SBECD)塩酸および/または水酸化ナトリウム |
フェーズ IIIn = 1038 |
回復までの時間(時間枠:1日目から 29日目) 回復の日は、被験者が通常のスケールから次の3つのカテゴリーのいずれかを満たす最初の日として定義される:(1)入院、酸素補給を必要とせず、もはや継続的な医療が必要である。(2)入院していない、活動が制限されている、および/または在宅酸素を必要としている。(3)入院しておらず、活動に制限はない。 |
採用 |
| NCT04343976 84 | 薬剤:ペグ化IFNλペグ化IFNλの 皮下注射180 µg 別名:ラムダ |
フェーズ IIn = 20 |
7日目で検出できないCOVIDPCR(時間枠:1週間) 最初のラムダ投与から7日後の陰性COVIDPCR検査 |
招待による登録 |
| NCT04343768 85 | 実験:ヒドロキシクロロキン+ロピナビル/リトナビル+IFNβ1a 実験:ヒドロキシクロロキン+ロピナビル/リトナビル+IFNβ1b アクティブコンパレータ:コントロールグループ:ヒドロキシクロロキン+ロピナビル/リトナビル |
フェーズ IIn = 60 |
臨床的改善までの時間(時間枠:無作為化の日付から 14日後まで) 7つのカテゴリーの順序スケールで2つのポイントの改善(WHO:コロナウイルス病(COVID-2019)R&D。ジュネーブ:WHOが推奨)または退院病院、どちらか早い方。 |
完了 |
| NCT04280705 95 | プラセボコンパレーター:プラセボ:1日目に200mgのレムデシビルプラセボを静脈内投与し、その後、最大10日間の総コースn = 286で入院している間に100mgのレムデシビルプラセボを1日1回維持投与した。 実験:レムデシビル:1日目に200 mgのレムデシビルを静脈内投与し、その後、最大10日間の合計コースn = 286で入院している間に100mgのレムデシビルを1日1回維持投与した。 |
フェーズ IIIn = 1062 |
7ポイントの序数スケールで各重症度評価を報告している被験者の割合(時間枠:15日目) 序数スケールは、特定の研究日の最初の評価での臨床状態の評価である。スケールは次のとおりである。(1)死亡。(2)侵襲的人工呼吸または体外式膜型人工肺(ECMO)で入院。(3)非侵襲的換気または高流量酸素装置で入院。(4)入院し、酸素補給が必要。(5)入院し、酸素補給を必要としない。(6)入院していない、活動の制限。(7)入院しておらず、活動に制限はない。 |
完了 |
| NCT04292899 96 | 薬物:remdesivir:IV注入として投与(他の名称:GS 5734 TM、Veklury ® 薬剤:ケアの標準:COVID-19感染のためのケア治療の標準 |
フェーズ IIIn = 4891 |
14日目の7ポイントの順序スケールでの改善のオッズ比(時間枠:14日目) オッズ比は、治療群間の順序尺度の改善のオッズを表する。順序尺度は、特定の日の臨床状態の評価である。毎日、前日の最悪のスコアが記録される。スケールは次のとおりです:(1)死亡(2)入院、侵襲的人工呼吸または体外式膜型人工肺(ECMO)(3)入院、非侵襲的換気または高流量酸素装置(4)入院、低流量酸素補給( 5)入院中、酸素補給を必要としない-継続的な医療を必要とする(コロナウイルス(COVID-19)関連またはその他)(6)入院し、酸素補給を必要としない-継続的な医療を必要としない(プロトコルによるレムデシビル投与を除く(7)入院していない |
完了 |
| NCT04292730 97 | 薬物:remdesivir:IV注入(他のnames- GS 5734として投与TM、veklury ® ケアの標準:COVID-19感染のためのケア治療の標準薬は |
フェーズ IIIn = 1113 |
11日目の7ポイントの順序スケールでの改善のオッズ比(時間枠:11日目) オッズ比は、治療群間の順序尺度の改善のオッズを表する。順序尺度は、特定の日の臨床状態の評価である。毎日、前日の最悪のスコアが記録される。スケールは次のとおりです:(1)死亡(2)入院、侵襲的人工呼吸または体外式膜型人工肺(ECMO)(3)入院、非侵襲的換気または高流量酸素装置(4)入院、低流量補助酸素を必要とする( 5)入院中、酸素補給を必要としない-継続的な医療を必要とする(コロナウイルス(COVID-19)関連またはその他)(6)入院し、酸素補給を必要としない-継続的な医療を必要としない(プロトコルによるレムデシビル投与を除く(7)入院していない。 |
完了 |
| NCT04409262 98 | 実験:レムデシビル+トシリズマブ(RDV + TCZ):RDV + TCZアームに割り当てられた参加者は、RDV負荷用量に続いて、1日目にTCZを1回注入し、2〜10日目に1日1回のレムデシビルの維持用量を受け取る。 介入:薬物:レムデシビル; 薬剤:トシリズマブ アクティブコンパレーター:レムデシビル+プラセボ(RDV +プラセボ):RDV +プラセボ群に割り当てられた参加者は、RDV負荷用量を受け取り、1日目にTCZ-プラセボを1回注入し、RDVを1日1回維持する。 2〜10日目から。 介入:薬物:レムデシビル; 薬:プラセボ |
フェーズ IIIn = 450 |
28日目の臨床状態の7つのカテゴリーの順序尺度を使用して研究者によって評価された臨床状態(時間枠:28日目) | 採用 |
| NCT04381936 104 | 薬剤:ロピナビル-リトナビル:ロピナビル400mg-リトナビル100mgを12時間ごとに10日間経口投与(または経鼻胃管挿入)。 薬物:コルチコステロイド:デキサメタゾンの形のコルチコステロイドを経口(液体または錠剤)またはIV製剤として1日1回10日間投与する。妊娠中または授乳中の女性では、デキサメタゾンの代わりにプレドニゾロン40 mgを経口投与(またはIVヒドロコルチゾン80 mgを1日2回)使用する必要がある。ヒドロコルチゾンまたはコハク酸メチルプレドニゾロンナトリウムの形のコルチコステロイド(在胎週数44週以下、またはPIMS-TSのみで在胎週数44週以上)(タイミングと投与量についてはプロトコルを参照) 薬物:ヒドロキシクロロキン:経口でのヒドロキシクロロキン10日(タイミングと投与量についてはプロトコルを参照)。 薬剤:アジスロマイシン:アジスロマイシン500 mgを経口投与(または経鼻胃管)または1日1回10日間静注。 生物:回復期血漿:ABO互換性のある回復期血漿の単一ユニット(275mL±75mL)で試験日に一日あたりIV 1(できるだけ早く無作為化後)および2(第1及び第2ユニット間の12時間の間隔の最小値を有する) 薬剤:トシリズマブ:体重によって決定される用量のIV注入によるトシリズマブ(投与量のプロトコルを参照) 生物学的:免疫グロブリン:妊娠44週以上およびPIMS-TSのみの18歳未満の子供に対するIV免疫グロブリン(IVIg)(投与量のプロトコルを参照) ) 薬剤:合成中和抗体:12歳以上の参加者のみ:ランダム化後できるだけ早く、250 mL 0.9%生理食塩水を点滴静注したREGN10933 + REGN10987 8 g(各モノクローナル抗体4 g)を60in±15分かけて単回投与する(他の名前:REGN-COV2) |
フェーズ:II、III n = 15,000 |
すべての原因による死亡率(時間枠:無作為化後28日以内) 「追加治療なし」群とのペアワイズ比較ごとに、主な目的は、すべての原因による死亡率に対する試験治療の効果の信頼できる推定値を提供することである。 |
採用 |
| NCT04260594 109 | 薬剤:アルビ ドールアルビドール錠:2錠/回、1日3回、14〜20日間服用別名:治験責任医師が 使用した基本治療は患者の状態に基づいた その他:基本治療 基本治療 |
フェーズIVn = 380 |
最初の週のウイルス陰性コンバージョン率(時間枠:最初の週) | まだ募集していない |
| NCT04347980 113 | 薬剤:デキサメタゾンおよびヒドロキシクロロキン:ヒドロキシクロロキン/デキサメタゾングループに含まれる患者は、ヒドロキシクロロキングループと同じ方法で、標準化された換気管理およびヒドロキシクロロキンの投与の恩恵を受ける。彼らは、デキサメタゾンに加えて、20 mg IVの割合で15分間、1日1回5日間(D1からD5)次にD6からD10まで1日あたり10mgの割合で投与される。患者が10日より前に抜管された場合、彼は前に最後のデキサメタゾンを投与される。(別名:標準換気管理) 薬剤:ヒドロキシクロロキン:ヒドロキシクロロキングループに含まれる患者は、標準化された換気管理の恩恵を受ける。ヒドロキシクロロキン群に含まれる患者は、 ヒドロキシクロロキンのJ1から 10日間経腸的に200mg⨰3/日を受け取る。患者が10日より前に抜管された場合、彼は前に最後の ヒドロキシクロロキンを投与される。(別名:標準換気管理) |
フェーズ IIIn = 122 |
28日目の死亡率(時間枠:無作為化後28日) 死亡率は無作為化後28日で評価された |
採用 |
| NCT04334928 114 | 薬剤:エムトリシタビン/テノホビルジソプロキシ ルエムトリシタビン/テノホビルジソプロキシル、200 mg / 245mg錠。1日1回1錠を服用する。 薬:ヒドロキシ クロロキンヒドロキシクロロキン、200mg錠。1日1回1錠を服用する。 薬物:プラセボ:エムトリシタビン/テノホビルジソプロキシルプラセボ プラセボ:外観がエムトリシタビン/テノホビルジソプロキシルに類似した錠剤 薬物:プラセボ:ヒドロキシクロロキン プラセボ:外観がヒドロキシクロロキンに類似した錠剤 |
フェーズ IIIn = 4000 |
SARS-CoV-2(COVID-19)の確認された症候性感染症の数(期間:12週間) | 採用 |
| NCT04513184 118 | 薬剤:IVデキサメタゾン6 mg(ランダム化後1日目から 10日目) 別名:ST 薬剤:鼻デキサメタゾン0.12 mg / kg /日(1日目から3日間)続いて0.06 mg / kg /日(ランダム化後4日目から 10日目)。 他の名前:鼻DXM |
フェーズ IIn = 60 |
臨床的改善の時期(時間枠:無作為化後10日) 無作為化後の患者の臨床状態の評価。WHOの7ポイントの順序尺度での2ポイントの改善として定義される。 |
採用 |
| NCT04509973 119 | 実験:デキサメタゾン12 mg 最大10日間の標準治療に加えて、デキサメタゾン12mgを1日1回静脈内ボーラス注射。デキサメタゾンが利用できない場所では、ベタメタゾン12mgの使用を許可する。 介入:薬剤:デキサメタゾンアクティブコンパレーター:デキサメタゾン6 mg 最大10日間の標準治療に加えて、デキサメタゾン6mgを1日1回静脈内ボーラス注射する。デキサメタゾンが利用できない場所では、ベタメタゾン6mgの使用を許可する。 介入:薬物:デキサメタゾン |
フェーズ IIIn = 1000 |
28日目(時間枠:無作為化後28日目)の 生命維持なしで生存している日数無作為化から 28日目までの生命維持(すなわち、侵襲的人工呼吸、循環補助または腎代替療法)なしで生存している日数 |
採用 |
| NCT04310228 133 | 薬剤:トシリズマブと組み合わせたファビピラビルファビピラビル :初日、毎回1600 mg、1日2回。2日目から7日目まで、1日2回、毎回600mg。経口投与の場合、最大摂取日数は7日以内である。 トシリズマブ:初回投与量は4〜8mg / kg、推奨投与量は400mgである。発熱患者の場合、最初の投与後24時間以内にまだ発熱があり、2つの投薬の間隔が12時間以上である場合は、追加の適用(以前と同じ投与量)が行われる。IV注入、累積数の最大値は2であり、最大単回投与量は800mgを超えない。 薬:ファビピラビル 初日、1日2回、毎回1600mg。2日目から7日目まで、1日2回、毎回600mg。経口投与、最大摂取日数は7日以内である。 薬剤:トシリズマブ 初回投与量は4〜8mg / kg、推奨投与量は400mgである。発熱患者の場合、最初の投与後24時間以内にまだ発熱があり、2つの投薬の間隔が12時間以上である場合は、追加の適用(以前と同じ投与量)が行われる。IV注入、累積数の最大値は2であり、最大単回投与量は800mgを超えない。 |
フェーズ:該当なし n = 150 |
臨床的治癒率(期間:3ヶ月) 臨床的治癒の定義:呼吸器検体のウイルス量が2回連続して陰性であり(2つの検査の間隔が1日以上)肺の画像が改善し、体温は3日以上正常に戻り、臨床症状は改善した。 |
採用 |
| NCT04320615 134 | 薬剤:トシリズマブ(TCZ) 参加者はIVTCZを1回投与される。臨床症状が悪化したり、改善が見られない場合は、1回追加投与することができる。 薬物:プラセボ 参加者は、TCZに適合したIVプラセボを1回投与される。臨床症状が悪化したり、改善が見られない場合は、最大1回の追加投与が可能である。 |
フェーズ:II n = 450 |
研究の主要および副次的評価項目には、臨床状態、死亡率、人工呼吸器、およびICU変数が含まれる。 | 完了 |
| NCT04317092 135 | 薬剤:トシリズマブ注射 トシリズマブ8 mg / kg(1回の投与あたり最大800 mg)12時間間隔。 |
フェーズ:II n = 400 |
2つの主要なアウトカム指標:肺機能の低下の停止と肺機能の改善。 | 採用 |
| NCT04315480 136 | トシリズマブ8mg / kgの単回投与 | フェーズ:II n = 38 |
ウイルス誘発性サイトカインストームにおけるその役割を評価すること、肺機能の悪化を阻止すること、または臨床状態の急速な改善を促進すること、鼻気管挿管および/または死を防ぐこと。 | アクティブ、募集していない |
| NCT04322773 137 | 薬剤: トシリズマブ400 mg IVによるロアクテムラIV単回投与治療 他の名前:トシリズマブ400 mgによる 薬剤:トシリズマブ2⨰162mg皮下 投与によるロアクテムラsc単回投与 他の名前:トシリズマブ2⨰162mg 薬剤: サリルマブ1によるケブザラsc単回投与治療⨰200mg皮下 その他の名称:サリルマブ1⨰200mg その他:通常通りの標準的な医療管理 |
フェーズ:II n = 200 |
重度のSARS-CoV-2肺炎の患者において、3つのIL-6阻害剤投与(すなわち、IVトシリズマブ、皮下トシリズマブ、および皮下サリルマブ)のいずれかの効果を標準治療と比較すること。 | 採用 |
| NCT04331808 138–140 | 薬剤:トシリズマブ トシリズマブ8 mg / kg D1,反応がない場合(酸素必要量の減少なし)D3で2回目の注射。 |
フェーズ:II n = 129 |
トシリズマブ群の患者の有意に低い割合が、14日目に換気または死亡の必要性の主要な結果を達成した | アクティブ、募集していない |
| NCT04315298 141、142 | 薬剤:サリルマブサリルマブの 単回または複数回の静脈内投与。患者がプロトコルで定義された基準を満たしている場合は、追加の用量を投与することができる。 他の名前:kevzara®/ REGN88 / SAR153191 薬剤:プラセボ サリルマブ投与に合わせたプラセボの単回または複数回の静脈内投与 |
フェーズ:II、III n = 1912 |
最初の部分は、米国の複数のサイトで患者を募集することであり、発熱と酸素補給の必要性に対するサリルマブの効果を評価する。試験の2番目のより大きな部分では、死亡率の予防、人工呼吸器、酸素補給、および/または入院の必要性の減少など、長期転帰の改善を評価する。この研究の初期の結果は、その有用性が重症患者のために確保されている可能性があることを示しているようである。 | 完了 |
| NCT04324073 143 | 薬剤:サリルマブ (D1での1時間の注入で400mgのサリルマブのIV用量 |
フェーズ:II、III n = 239 |
募集された参加者は、中等度、重度、または重度の肺炎のCOVID-19患者でした。この試験は、サリルマブ治療を受けた患者の転帰を、標準治療の転帰を受けた患者、および他の免疫調節薬で治療された患者と比較することを目的としている。その後、サリルマブを評価するために、さらに多くの研究が登録または開始された。 | アクティブ、募集していない |
| NCT04329650 144 | 薬剤:シルツキシマブ 11mg / kgのシルツキシマブの単回投与が静脈内注入によって投与される。 薬剤:メチルプレドニゾロン 3日間で250 mg / 24時間のメチルプレドニゾロン、続いて3日間で30 mg / 24時間の用量が静脈内注入によって投与される。 患者がロピナビル/リトナビルを服用している場合、用量は3日間で125 mg / 24時間、続いて3日間で15 mg / 24時間になる。 |
フェーズ:II、III n = 239 |
研究期間内の任意の時点でICU入室を必要とする患者のCOVID19肺炎の割合を持つ入院患者におけるシルツキシマブとコルチコステロイドの有効性と安全性を比較する | 採用 |
| NCT04443881 145 | 薬剤:アナキンラ149 mg / mLプレフィルドシリンジ(キネレット) アナキンラ(100 mg / 6 h)15日間の点滴静注 |
フェーズ:II、III n = 180 |
治療の成功。重度のCOVID-19およびCSS肺炎の患者の機械的換気の必要性に対する標準治療に加えて、アナキンラの効果を評価するために機械的換気を必要としない患者の数として定義される。(時間枠:15日目) 治療の成功。15日目までに人工呼吸器を必要としない患者数として定義される。 患者の人工呼吸器の必要性に対する標準治療に加えて、アナキンラの効果を評価するために人工呼吸器を必要としない患者数。重度のCOVID-19およびCSS肺炎。(時間枠:28日目) 人工呼吸器を必要としない患者の数 重度のCOVID-19およびCSS肺炎の患者における人工呼吸の必要性に対する標準治療に加えて、アナキンラの効果を評価するための人工呼吸までの時間。((時間枠:最大28日) 機械的換気までの 時間重度のCOVID-19およびCSS肺炎の患者の機械的換気の必要性に対する標準治療に加えて、アナキンラの効果を評価するための酸素飽和度の正常化までの時間。(時間枠:最大28日) 酸素飽和度の正常化までの時間 重度のCOVID-19およびCSS肺炎の患者の人工呼吸器の必要性に対する標準治療に加えて、アナキンラの効果を評価するためにICUおよび入院に滞在する。(時間枠:最大28日) ICUに滞在して入院する |
採用 |
抗ウイルス薬
ヌクレオシド類似体は、HIV、B型肝炎ウイルス(HBV)サイトメガロウイルス(CMV)HSV感染症の治療に最も一般的に使用されている重要な抗ウイルス薬である。リバビリンは、過去にSARSの大パンデミック時に広く使用されていたため、COVID-19の潜在的な治療薬として最初に試験された薬剤の1つです87 。過去には、ステロイド薬やIFNβと併用されていた88 。しかし、本剤を使用した場合の副作用としては、肝障害、筋障害、神経障害、骨髄抑制、膵炎などが報告されている(表1)。92 ヌクレオシドアナログはウイルス性肺炎の治療に広く使用されているが,これらの薬剤には下痢,発疹,腎不全,低血圧,肝酵素の増加などの副作用がある(表1)93。患者は10日間、レムデシビルの静脈内投与を2:1の割合で無作為に割り付けられた。投与量は1日目に200mg、2~10日目に100mgを1日1回の単回点滴)または同量のプラセボ点滴とした。94 現在までに、これらのヌクレオシドアナログの COVID-19 管理における有効性を評価するために、いくつかの臨床試験が登録されており、表283,95-98 にその結果を示す。
99 ロピナビルとリトナビルは、事実上同一の分子構造を有しているが、ウイルスの複製と合成に影響を与えるチトクロームP450活性を阻害することにより、HIVプロテアーゼを阻害する(表1)。これらの薬剤は、SARS-CoV-2のエンドペプチダーゼC30に結合し、呼吸器系の苦痛を軽減する能力があることが示唆されている。それにもかかわらず、Khaliliらによる最近のレビュー論文によると、現在進行中の臨床試験がいくつかあり、その多くは中国で実施されており、COVID-19発生におけるリバビリンの役割を評価している。ネルフィナビルは選択的HIVプロテアーゼ阻害剤であり、SARS-CoVに対する抗ウイルス効果が証明されている102。この薬剤は、SARS-CoV-2のウイルス抗原の発現を強力に阻害することができる(表1)103。この薬剤の最も一般的な副作用は、吐き気と下痢である(表1)。
また、広汎な抗ウイルス化合物であるアルビドールの使用は、SARS-CoV-2のウイルス複製過程をブロックする105 。アレルギー反応、吐き気、下痢、めまい、血清トランスアミナーゼ上昇は、本剤に関連する副作用の一部である(表1)106 。本試験の結果は、ロピナビル/リトナビル群と比較して、アルビドール単剤療法の方が、明らかな副作用がなく、短期間で回復した患者さんに有利な結果となった108 。
クロロキンは、その生化学的特性の一つである強力な抗ウイルス効果を示すことから、幅広い抗ウイルス薬として認知されている。Cortegianiらによるシステマティックレビューでは、COVID-19治療におけるクロロキンの有効性と安全性が評価されている。Cortegianiらによるシステマティックレビューでは、COVID-19治療におけるクロロキンの有効性と安全性が評価されている。また、クロロキンのCOVID-19に対する有効性を評価した臨床試験を表2に示す。
すべての抗ウイルス薬がCOVID-19の治療に重要な役割を果たすことができる。それにもかかわらず,現在までに承認されている抗ウイルス薬はない17,74 。これらの薬剤の併用研究では有望な結果が得られており、長期試験による更なる臨床評価が必要とされている。
コルチコステロイド
コルチコステロイドはCOVID-19サイトカインストームに対して強力な抗炎症作用を持つ(表1)115)。臨床的証拠によると、グルココルチコイドはCOVID-19感染症の重要な特徴である炎症を媒介とする肺損傷を調節し、それによって呼吸不全の進行と死亡を減少させる可能性があることが示されている。WHOのRapid Evidence Appraisal for COVID-19 Therapies(REACT)ワーキンググループは、7つの試験のメタアナリシスにおいて、12カ国の重症患者1703人を対象にコルチコステロイド(主にヒドロコルチゾンまたはデキサメタゾン)を評価し、これらの薬剤は対照群と比較して死亡リスクを約3分の1減少させたと報告している117。RECOVERY (Randomized Evaluation of COVID-19 Therapy)共同研究グループは、28 日間の死亡率におけるデキサメタゾン(6 mg od, 経口または静脈内投与)の標準治療と比較して 10 日間までの投与の役割を評価するための対照オープンラベル試験を実施した(表2
)。本試験の主要な結果は、対照群と比較して上記の主要アウトカムを低下させる上でデキサメタゾンが有益な役割を果たしたことを示している(表2)。欠点としては、食欲増進、過敏性、睡眠障害(不眠症)足首や足の腫れ(体液貯留)胸やけ、筋力低下、創傷治癒障害、血糖値の上昇(表1)115,117 が挙げられる。
免疫療法
完治期血漿とは、ウイルスから回復した患者から得られる抗体を豊富に含む血漿のことである。明らかに、この血漿は完全に回復した患者から採取することができ、ウイルスに対する強固な抗体反応を発現させるのに十分な時間が与えられている。120,121 この治療法は安全で臨床的に有効であり、死亡率を低下させる(表1)。120,121 コンバルセッセント血漿療法(CPT)はインフルエンザA,122 エボラ123 やSARS-CoVなどの疾患に広く用いられていた124 。それにもかかわらず、この治療法の有用性は、表2に挙げたような大規模かつ良好に管理された臨床試験によって確立される必要がある。
もう一つの免疫療法は、ウイルス表面タンパク質の脆弱な部位を標的とし、その部位を不活性化して株の伝播を防ぐ保護モノクローナル抗体(mAb)である。最近、SARS-CoV-2スパイク蛋白質の不活性化に有効性を示すヒトmAb 47D11が単離された126 。この点で、COVID-19の管理への保護mABの適用に関する最初の報告は、さらなる研究のための門戸を開くことになる。
現在、IL-6がCOVID-19患者に見られる炎症と関連していることはよく知られており、IL-6およびIL-6受容体(IL-6R)の阻害は、このウイルス感染症の悪影響を軽減するための有望なターゲットであると考えられている。トシリズマブは、アトリズマブとしても知られている抗インターロイキン-6受容体ヒト化mAbである。127-129 Lanらは、トシリズマブの有効性を評価するために、7件のレトロスペクティブ研究のシステマティックレビューとメタアナリシスを実施した(4-8mg/kgを60分以上かけて点滴静注。127-129 Lanらは、トシリズマブ(点滴静注:4-8mg/kgを60分かけて60分間投与;必要に応じて12時間後に最大用量800mgを反復投与)の有効性を評価する7件のレトロスペシフィックレビューとメタ解析を行った。重症COVID-19患者の全死亡率は、トシリズマブ投与群で対照群に比べて低かったが、この差は統計学的に有意ではなかった。集中治療室への入院リスクや機械的人工呼吸の必要性などの因子は両群間で同等であった。以上のことから、著者らは、今後の大規模RCTのデータから質の高いエビデンスが得られれば、COVID-19.130の管理における本剤の潜在的な役割が決まると結論づけた。
Anakinraとして知られる生体内試験での有効性を示す新規のヒト抗インターロイキン-1β中和mAbのCOVID-19管理への使用がここ数ヶ月で明らかになってきた。この組換えIL-1受容体拮抗薬は、COVID-19患者の急性呼吸窮迫の原因の一つと考えられている炎症亢進状態を中和することができると研究者らは考えている(表1)。 Huetらが実施したGroupe Hospitalier Paris Saint-Joseph(フランス、パリ)の前向きコホート研究では、呼吸機能の悪化を示す症状を有する重症COVID-19患者におけるアナキンラの皮下投与(100mgを1日2回、72時間、その後1日100mgを7日間投与)の適応外使用を評価した。132 これらの薬剤の欠点としては、頭痛やめまい、口内炎、高血圧、高コレステロール血症、アレルギー反応、体重増加や足首の腫れ、胃の炎症や腹痛などが挙げられる。アナキンラの免疫抑制作用により、免疫系(好中球減少症)や治癒に悪影響を及ぼし、潜伏結核やその他の非定型・日和見感染症の再活性化につながる可能性がある(表1)127-129,131両剤の有効性を評価するために登録されている臨床試験を表2133-145に示す。
過去数ヶ月間、Regeneron Pharmaceuticals, Inc.は抗体カクテルREGN-COV2を設計し、COVID-19の管理における潜在的な役割について調査を行ってきた。彼らの臨床データは、Regeneronが選択した2つの抗体、REGN10933とREGN10987は、個々の抗体やこれまでに設計された他のカクテルと比較して、エスケープ変異体を生成する可能性が低いことを証明している146。146-148 オックスフォード大学は、Regeneron Pharmaceuticals, Inc.と共同で、COVID-19治療の可能性のある治療法の世界最大級のRCTであるRECOVERYで、Regeneron社の抗ウイルス抗体カクテルであるREGN-COV2を評価することを発表した。これは、入院中のCOVID-19患者を対象とした第3相非盲検試験であり、通常の標準治療と標準治療にREGN-COV2を追加した場合の効果を評価するものである(表2)。他に発表されている抗体カクテル療法としては、イーライリリー社が AbCellera 社と提携した LY-CoV555,アストラゼネカ社が Vanderbilt 大学の研究者と提携したもの、グラクソ・スミスクライン社と Vir Biotechnology 社との共同研究などがあるが、これらの試験はいずれも現在、段階が異なっている147。サイトカインストームの副作用を軽減するためにバリシチニブなどの全身性抗炎症薬を使用することも、その抗炎症作用と抗ウイルス作用のために評価されている。
COVID-19管理のための前向きな治療法
上述した様々な治療法の選択肢とは別に、将来性のある選択肢として浮上してきたモダリティと、それに対応する登録臨床試験を表3149-168に示す。
表3 ClinicalTrials.govに登録された2020年10月20日までのCOVID-19の治療のための前向き治療法を利用した臨床試験
| 治療法 | 研究識別子と引用(上付き文字) | 治療プロトコル | 研究段階; 推定登録数(n) | 主な結果の測定 | 採用状況 |
|---|---|---|---|---|---|
| 組換えACE2受容体 | NCT04375046 149 | 実験:実験:rbACE2グループ 0.4 mg / kg IV BID、7日間(非盲検)+標準治療 介入:薬物:B38-CAPの酵素のような組換え細菌ACE2受容体(rbACE2) 介入なし:介入なし:対照群 標準お手入れ; プラセボなし |
フェーズ In = 24 |
体温(発熱)の経時変化(時間枠:14日) 2つのグループ間の体温(発熱)の経時変化を経時的に比較する。 時間の経過に伴うウイルス量(時間枠:14日) 2つのグループ間のウイルス量を時間の経過とともに比較する。 |
まだ募集していない |
| NCT04382950 150 | 実験:実験:rbACE2グループとエアロゾル化イソトレチノイン rbACE2 0.4 mg / kg IV BID 7日間(非盲検)+エアロゾル化13シスレチノイン酸を2回に分けて段階的に0.2 mg / kg /日から4mg / kg /日に増加14日間の13シスレチノイン酸の吸入療法 介入:組み合わせ製品:B38-CAP(rbACE2)の酵素とエアロゾル化された13シスレチノイン酸のような組換え細菌ACE2受容体 介入なし:介入なし:対照群 標準治療; プラセボなし |
フェーズ In = 24 |
時間の経過に伴うウイルス量(時間枠:14日) 2つのグループ間のウイルス量を時間の経過とともに比較する。 時間の経過に 伴うP / F比(時間枠:14日)PaO 2 / FiO 2比時間の経過に伴う 連続臓器不全評価スコア(SOFAスコア)(時間枠:14日) 呼吸器、血液、肝臓、循環器の評価を含むSOFA神経、腎臓、各システムで0から4のスコア、スコアが高いほど結果が悪いことを意味する。 肺重症度指数(PSI)(時間枠:14日) 経時的な胸部の画像検査(時間枠:14日) 炎症性滲出性疾患の放射線科医の評価に基づいて、以下のカテゴリー:有意な改善、部分的な改善、改善なし、部分的な滲出の増加、滲出の有意な増加、判断できない。 重篤な病気または死亡に進行した被験者の割合(時間枠:14日) 初回投与から正常または軽度の肺炎への転換までの時間(時間枠:14日)時間の経過に伴う Tリンパ球数(時間枠:14日) C -反応性タンパク質レベルの経時 変化(時間枠:14日)アンジオテンシンII(Ang II)の経時変化(時間枠:14日) アンジオテンシン1–7(Ang 1–7)の経時変化(時間枠:14日) アンジオテンシン1–5(Ang 1–5)は時間とともに変化する(時間枠:14日) レニンは時間とともに変化する(時間枠:14日) アルドステロンは時間とともに変化する(時間枠:14日) アンギオテンシン変換酵素(ACE)は時間とともに変化する(時間枠:14日) インターロイキン6(IL-6)は時間とともに変化する(時間枠:14日) 可溶性腫瘍壊死因子受容体II型(sTNFrII)の経時変化(時間枠:14日) プラスミノーゲン活性化因子阻害剤1型(PAI-1)の経時変化(時間枠:14日) フォンウィルブランド因子(VWF)は時間とともに変化する(時間枠:14日) 腫瘍壊死因子-α(TNF-α)は時間とともに変化する(時間枠:14日) 高度な糖化最終産物(sRAGE)の可溶性受容体は時間とともに変化する(時間枠:14日) ) サーファクタントプロテイン-D(SP-D)は時間とともに変化する(時間枠:14日) 有害事象および重篤な有害事象の頻度(期間:14日) |
まだ募集していない | |
| エクソソーム | NCT04491240 151 | 手順: EXO1の吸入3mLの特殊溶液の10日間の吸入中に1日2回、最初のタイプのナノ粒子(エクソソーム)が0.5–2⨰10 ^ 10含まれてた。 手順: EXO2の吸入3mLの特殊溶液の10日間の吸入中に1日2回、2番目のタイプのナノ粒子(エクソソーム)が0.5–2⨰10 ^ 10含まれてた。 手順:プラセボ吸入 ナノ粒子(エクソソーム)を含まない3 mLの特殊溶液の10日間の吸入中に1日2回 |
フェーズIフェーズ IIn = 90 |
試験期間中の非重篤および重篤な有害事象の参加者数(期間:退院後30日) 有害事象などの安全性評価が登録される。有害事象はすべての試験中にモニタリングされる 吸入手順中に非重篤および重篤な有害事象を有する参加者の数(時間枠:10日間の各吸入後) 吸入手順中の有害事象などの安全性評価が登録される |
招待による登録 |
| NCT04389385 152 | 生物学的:COVID-19特異的T細胞由来のエクソソーム(CSTC-Exo) | フェーズ In = 60 |
副作用(AE)および重篤なAE(SAE)(期間:28日) 安全性評価の 有効性評価(期間:28日) 臨床的回復までの時間(TTCR) 人工呼吸器なしの回復率(期間:28日) 有効性評価 |
まだ募集していない | |
| MSC | NCT04384445 153 | ジョフィンは、ヒト羊水(HAF)に由来する、無細胞で最小限の操作による製品である。この製品には、300を超える成長因子、サイトカイン、ケモカインのほか、羊膜幹細胞や上皮細胞に由来する他のアポトーシス小胞/ナノ粒子が含まれている。 生物学的:ゾフィン 生物学的:ゾフィンは、標準的なケアに加えて、2–5⨰10 ^ 11粒子/ mLを含む1mLを静脈内投与される。ゾフィンの投与量は、被験者のベッドサイドで100mLの生理食塩水で希釈される。 このグループの参加者は,0日目、4日目、8日目に標準治療とゾフィンを受け取る。 介入:生物学的:ゾフィン その他:プラセボ その他:プラセボプラセボ(生理食塩水)は、標準治療に加えて1mLを静脈内投与される。プラセボ用量は、被験者のベッドサイドで100mLの滅菌生理食塩水で希釈される。 このグループの参加者は,0日目、4日目、8日目に標準治療とプラセボ(生理食塩水)を受け取る。 |
フェーズI フェーズ IIn = 20 |
注入に関連する有害事象の発生率(時間枠:60日) 安全性は、治療を行う医師によって評価された注入に関連する有害事象の発生率によって定義される 重度の有害事象の発生率(時間枠:60日) 安全性は、治療する医師によって評価された重篤な有害事象の発生率 |
採用 |
| NCT04276987 154 | 実験:MSC由来のエクソソーム治療グループ 従来の治療とMSC由来のエクソソームのエアロゾル吸入治療参加者は、従来の治療とMSC由来のエクソソームの5回のエアロゾル吸入(2.0 * 10E8ナノベシクル/ 3 mL、1,2,3日目、4,および5)。 介入:生物学的:MSC由来のエクソソーム |
フェーズ In = 24 |
副作用(AE)および重度の副作用(SAE)(期間:最大28日) 副作用(AE)および重度の副作用(SAE)の頻度を含む最初の治療後28日以内の安全性評価 臨床的改善までの時間( TTIC)(時間枠:最大28日) 臨床改善までの時間を含む28日以内の効率評価(TTIC) |
完了 | |
| NCT04457609 155 | 薬剤:オセルタミビル COVID-19の現在の標準治療 薬:アジスロマイシンCOVID-19の 現在の標準治療 生物学的:臍帯MSC 現在の標準治療(オセルタミビル+アジスロマイシン)に加えて補助療法 |
フェーズ In = 40 |
臨床的改善:呼吸困難の存在(時間枠:15日) 呼吸数から評価した、COVID-19の主要な症状の1つである呼吸困難がまだ患者にあるかどうかの評価 臨床的改善:喀痰の存在(時間枠:15日) かどうかの評価患者は、肺聴診から評価されたCOVID-19の主要な症状の1つである生産性の咳をまだ持っている 臨床的改善:発熱(時間枠:15日) 体温チェックの測定から発熱の存在を評価し、毎日評価される 臨床的改善:換気状態(時間枠:15日) 換気離脱期の患者の能力から評価された、COVID-19のARDSの主要な症状の1つである換気がまだ必要かどうかの評価 臨床的改善:血圧(時間枠:15日) 毎日の患者の血圧の評価 臨床改善:心拍数(時間枠:15日) 患者の心拍数を毎日評価する 臨床的改善:呼吸数(時間枠:15日) 患者の呼吸数を毎日評価する 臨床的改善:酸素飽和度(時間枠: 15日) 患者の酸素飽和度を毎日評価する |
採用 | |
| RASブロッカー | NCT04331574 156 | 観察モデル:症例のみの 時間的展望: イタリアの病院で募集されたCOVID-19の認定診断を受けた横断的患者 |
フェーズ:該当なし n = 2000 |
ACE阻害薬および/またはアンジオテンシン受容体拮抗薬(ARB)を降圧薬として使用しているCOVID-19患者の登録数(期間:3か月) 病院または一般開業医の健康記録から収集された既往歴データを使用して、カウントするACE阻害薬またはARBで治療された登録済みのCOVID-19患者の数。 降圧薬としてACE阻害薬および/またはアンジオテンシン受容体拮抗薬(ARB)も使用したARDSのWHO仕様に基づく、症状なし、中等度の症状、または重度の肺炎の症状で登録されたCOVID-19患者の数(期間:3か月) この研究は、降圧ACE阻害薬またはARBの仮定がCOVID19の臨床症状の重症度を増加させるかどうかを観察したい |
採用 |
| NCT04329195 157 | 薬剤:1:RAS遮断薬療法の 中止RAS遮断薬療法の中止 薬剤:2:RAS遮断薬療法の 継続RAS遮断薬療法の継続 |
フェーズ IIIn = 554 |
0日目から 28日目までの臨床的改善までの時間(7つのカテゴリーの順序スケールで2ポイントの改善、または退院のいずれか早い方)(時間枠:0日目から 28日目または退院まで) | 採用 | |
| NCT04353596 158 | 薬剤:ACE阻害薬、アンジオテンシン受容体拮抗薬 ACEIまたはARBの中止/交換にランダム化された患者では、RASシステムに直接影響を与えることなく別の薬剤に切り替える必要がある場合がある。継続にランダム化された患者では、研究に関係なく、ACEIまたはARB(例えば、敗血症の開始を伴う低血圧)を停止する必要があるかもしれない。 |
フェーズIVn = 208 |
最大連続臓器不全評価(SOFA)スコアと死亡の組み合わせ(時間枠:30日) SOFAスコアの最小値は0で、最大値は24ポイントになる。すべての死因は最大スコア(24ポイント)として分類される。入院を必要とせずに無症候性疾患が進行した場合、SOFAスコアは0になる。ICUへの入院、 人工呼吸器の使用、または全死因の複合(時間枠:30日) |
採用 | |
| 漢方薬 | NCT04306497 159 | 薬: TCM処方 TCM処方1:煎じ薬または顆粒を1日1回服用する。TCM処方2:煎じ薬または顆粒を1日1回服用する。 |
フェーズ-情報なし n = 340 |
主な症状の軽減/時間の消失速度(時間枠:9日) 発熱、咳および呼吸の短さの三つの主要な症状の軽減/消失の時間の比較 胸部CT吸収(時間枠:9日) を参照してRenyi Yinらによって開発された「肺炎胸部X線吸収評価スケール」では、最終的な吸収判断を使用して、肺炎患者の胸部CT吸収を評価する。これは、吸収の程度に応じて4つのレベルに分けられる。吸収、多数吸収、部分吸収、吸収なし。 |
完了 |
| NCT04251871 160 | 薬物:従来の薬(酸素療法、エアロゾル吸入によるアルファインターフェロン、およびロピナビル/リトナビル)およびTCM顆粒 従来の薬:酸素療法、抗ウイルス療法(エアロゾル吸入によるアルファインターフェロン、およびロピナビル/リトナビル、400 mg / 100 mg、経口、入札)14日間。 TCM顆粒:20 g、経口、1日2回、14日間。 薬剤:従来の薬(酸素療法、エアロゾル吸入によるアルファインターフェロン、およびロピナビル/リトナビル) 従来の薬:酸素療法、抗ウイルス療法(エアロゾル吸入によるアルファインターフェロン、およびロピナビル/リトナビル、400 mg / 100 mg、経口、入札) 14日間。 |
該当なし n = 150 |
急性呼吸窮迫症候群(ARDS) 発症の発生率(期間:14日)急性呼吸窮迫症候群(ARDS)発症の発生率 |
採用 | |
| 酸化防止剤 | NCT04363216 161 | 薬物: アスコル®アスコルビン酸 (6日間)毎日2時間の注入、漸増用量(0.3グラム/ kgで,0.6グラム/ kgで,0.9グラム/キログラム)。 他の名前:ビタミンC |
フェーズ IIn = 66 |
臨床的改善(時間枠:72) •72時間の治療での臨床的改善。72時間の間に最高酸素流量が50%減少し、気管支拡張薬の最も頻繁な使用が50%減少することとして定義される。 72時間以内の12時間のウィンドウ、または退院(どちらか早い方)。 |
まだ募集していない |
| NCT04323514162 | Dietary supplement: vitamin C 10 g of vitamin C IV in addition to conventional therapy. |
Not applicable n=500 |
In-hospital mortality (time frame: 72 h) Change of hospital mortality |
Recruiting | |
| NCT04519034163 | 監査1 2020年1月以降に実施されたすべてのビタミンDの結果(n = 〜15,000)と、年齢、体重、身長、民族性、その他の関連する検査マーカー(Ca、調整済みカルシウム、PTH、Mg、リン酸、肝臓および腎臓のプロファイル、COVID) -19スクリーニング、CRP、ヘマチニクス、FBC) 介入:その他:介入なし 監査2 すべてのCOVID-19スクリーニング結果とビタミンD、民族性、年齢、体重、身長、ICUを含む入院期間(該当する場合)タイプ病気の回復の有無、関連する健康状態、CRP、フェリチン、ヘマチニクス、ビタミンAおよびE、プロカルシトニン、LDH、INR、フィブリノーゲン、FBC、D-ダイマー、CK、トロポニン-T、サイトカイン、腎機能および患者からの電解質GSTTNHS(英国保健医療局)トラストでテスト済み。 介入:その他:介入なし |
フェーズ-該当なし n = 27,000 |
ビタミンDを収集すると、年齢、性別、民族性、BMI、およびその他の関連する検査結果とともに、ロンドン南東部地域の患者が得られる。(時間枠:2020年1月から6月)2020年 1月以降にセントトーマスの栄養補給ユニットによって実施されたすべてのビタミンDの結果(n = 〜15,000)年齢、体重、身長、民族性、その他の関連する検査マーカー(Ca 、調整されたカルシウム、PTH、Mg、リン酸塩、肝臓および腎臓のプロファイル、COVID-19スクリーニング、CRP、造血薬、FBC)が、ビタミンDの測定対象サンプルから 2週間以内にテストされた場合に取得される。この監査の結果は、ロンドン南東部地域の患者の年齢、性別、民族性、BMI(体重kg /身長2)によるビタミンDの状態のスナップショットを提供する。)。相関分析は、他の実験室パラメータでも行われる。 |
まだ募集していない | |
| NCT04323228 164 | 実験的:介入-介入グループは、ビタミンA、C、E、セレン、亜鉛が豊富な経口抗酸化サプリメントを毎日受け取る。介入サプリメントの1カプセルの組成には、1500 µgのビタミンA(β-カロテンとして)250 mgのビタミンC、90 mgのビタミンE、15 µgのセレン、および7.5mgの亜鉛が含まれる。 介入:栄養補助食品:抗酸化物質が豊富な経口サプリメント プラセボコンパレータ:プラセボ プラセボグループは、同じ色と形のセルロース含有ゼラチンカプセルの形で毎日介入を受ける。 介入:栄養補助食品:セルロース含有プラセボカプセル |
フェーズII フェーズ IIIn = 40 |
試験終了時の栄養リスクスクリーニング-2002(NRS-2002)のベースラインスコアからの変化(期間:最大3か月) 試験終了時のCOVID-19患者のNRS-2002スコアの変化0から7のスコアで、スコアが3未満の場合は栄養失調のリスクがないことを意味し、3以上の場合は栄養失調を意味する。 試験終了時のベースライン血清フェリチンレベルからの変化(期間:最大3か月) フェリチンはCOVID-19死亡予測因子と見なされるため、試験終了時の血清フェリチンの変化。 試験終了時のベースライン血清IL-6濃度からの変化(期間:最大3か月) サイトカインストームを表し、COVID-19死亡予測因子と見なされるため、試験終了時のIL-6の変化 試験終了時のベースライン血清C反応性タンパク質濃度からの変化(期間:最大3か月) 急性期を反映する試験終了時の血清中のC反応性タンパク質の 変化ベースライン血清TNF-α濃度からの変化試験終了時(期間:最大3か月) サイトカインストームの重症度を表すため、試験終了時の血清中のTNF aの 変化ベースライン血清単球化学誘引物質タンパク質1(MCP-1)からの変化試験(期間:最大3か月) 血漿MCP-1は、サイトカインストームの重症度を表する |
採用 | |
| ダイエットサプリメント | NCT04382040 165 | ArtemiCは、スプレー投与用のミセル製剤にアルテミシニン(6 mg / mL)クルクミン(20 mg / mL)フランキンセンス(=ボスウェリア)(15 mg / mL)およびビタミンC(60 mg / mL)を含む医療用スプレーである。 薬剤:ArtemiC:治療期間 の最初の2日間は1日2回経口投与される薬剤:プラセボ:治療期間の最初の2日間は1日2回経口投与される |
フェーズ IIn = 50 |
臨床的改善までの時間は、24時間維持≤2の国家早期警告スコア2(NEWS2)として定義されるルーチン処理(時間枠:24時間)と比較して、患者は、臨床徴候の変化をスコア表を用いて評価される の割合治験薬に関連する明確なまたは可能性のある有害事象(期間:14日)のある参加者は、治験薬によって引き起こされた有害事象が評価される |
採用 |
| NCT04347382 166 | 実験:ニゲラサティバとハチミツのグループ 薬:ニゲラサティバシードパウダー80 mg / kg /日をカプセルで最大14日まで粉砕)薬:天然蜂蜜1 mg / kg /日を経口で最大14日まで)標準的な医療 介入と一緒に:薬:蜂蜜; 医薬品:ニゲラ サティバ/黒クミン (呼吸器科医または感染症の専門家による助言場合)抗菌や抗ウイルスの使用に伴い、標準的な症候性のケアが含まれて医師の治療によって処方の標準的な支援医療、ラホール:プラセボcomparator-標準的な医学的ケア 介入:薬物:プラセボ: |
フェーズ IIIn = 313 |
COVID-19 PCRが陽性から陰性になるまでに必要な日数(時間枠:最大14日) RT-PCRは、入院日(0日)に行われ、その後4日ごとに14日間、または症状が解消するまで行われる。 RT-PCRは陰性になる。RT-PCRは、陽性または陰性としてのみ表示される(パキスタンの制限による)。 疾患進行のHRCT / X線所見(時間枠:最大14日) HRCTは入院日(0日)に実施され、合計4回のCTスキャンが4日ごとに実施される。 COVID-19陽性とラベル付けするスコアは、フライシュナー協会の用語集とウイルス性肺炎に関する査読済みの文献に記載されている国際標準の命名法を使用して、それぞれ5と25になる。 症状の進行の重症度(時間枠:最大14日) 臨床的に疾患の進行は、軽度、中等度、重度に分類される症状の重症度に応じて評価される。 入院期間(期間:最大14日) 入院期間は、患者が治療中に病棟に滞在した日数として分類される。入学日と退院日は私たちに総滞在期間を与えるであろう。 30日死亡率(時間枠:30日) 各群の30日死亡率 |
完了 | |
| NCT04323345 167 | 栄養補助食品:天然蜂蜜:天然蜂蜜サプリメント1g / kg /日を2〜3回に分けて14日間経口または経鼻胃管を介して。 その他:標準治療:支持療法およびロピナビル/リトナビル錠またはアルビドールまたはリン酸クロロキンまたはヒドロキシクロロキンまたはオセルタミビル(アジスロマイシンの有無にかかわらず)。 |
フェーズ IIIn = 1000 |
ポジティブからネガティブへのスワップからの回復率(時間枠:14日)14日 目にポジティブからネガティブへのスワップに変わった患者の割合 発熱から常温までの日数(時間枠:14日)発熱がなくなるまでの日数 肺炎の解消CTまたはX線で(時間枠:30日)胸部X線またはCTで肺が回復するまでの日数 |
採用 | |
| NCT04342689 168 | 薬:難消化性澱粉を含む栄養補助食品:大さじ2杯(〜20g)を1日2回14日間服用する(大さじ2杯から 1日1回3日間、その後4日目から 14日目に1日2回)(別名:難消化性澱粉) 栄養補助食品:プラセボ澱粉:大さじ2杯(〜20 g)を1日2回14日間服用する(大さじ2杯から 1日1回3日間、その後4日目から 14日目に1日2回)(別名:難消化性澱粉) |
フェーズ IIIn = 1500 |
COVID-19関連合併症の入院率(期間:治療開始から 1ヶ月) 低酸素性呼吸不全、肺炎の入院診断で、発熱、息切れ、筋痛、咳、または低酸素症の症状を示しながら入院した被験者、または電子健康記録(EHR)のレビューに関するウイルス性肺炎。COVID-19に続発すると考えられる入院前の死亡もイベントとして定義される。すべての入院は、サイトのPIによって審査および裁定される。 |
採用 |
1. Gheblawiらは、そのレビューの中で、新規のSARS-CoV-2受容体としてACE2の役割を強調し、免疫、炎症、ACE2,および心血管疾患との間の重要なリンクを提供している。169著者らは、ACE2の作用は、組換えACE2,ACE2の遺伝子伝達、Ang 1-7アナログ、およびMas受容体アゴニストによって増強されると述べている。
2. エキソソーム(30-120nmの細胞外小胞)の分子機構 エキソソームは、核酸、タンパク質、脂質などの生体分子をレシピエント細胞に送達することで、細胞間のコミュニケーションを助けている(表1)170,171 。170 研究者らは、エキソソームがSARS-CoV-2ウイルスの拡散に役割を果たしており、COVID-19感染との関係を十分に理解することで、ウイルスの侵入、複製、拡散に関する重要な情報を特定し、その悪影響に対抗することができると考えている(表1)170,171。現在、試験されている戦略には、エキソソソームの生合成と取り込みの阻害、エキソソーム療法、エキソソームベースの薬物送達システム、エキソソームベースのワクチン(表3)などがある。
3. 21,172 MSCは、Chaf1a媒介およびSumo2媒介のエピジェネティック制御(プロウイルスサイレンシングと呼ばれる)を介してウイルスの活動を抑制することができ、ARDSにおいて有益な効果が実証されている。172,173 表3は、COVID-19の管理における評価済みMSCの登録された3つの臨床試験のデータを示している。
4. ACE2 はレニン-アンジオテンシン系(RAS)の重要な構成要素であるため、ACE-インヒビター(ACEI)やアンジオテンシン II 受容体 1 型(AT1R)などの RAS 阻害剤を利用することで治療が可能である174 。潜在的な有害性の証拠は不十分であり、その利点を示す圧倒的な証拠のみが存在し、表3156-158に記載された臨床試験においてCOVID-19の管理に利用されることが好ましい。
5. 5. 中国の伝統的な医薬品(TCM)には、例えば、青飛麻黄煎じ薬(QPD) 姜姜姜江煎じ薬(Gancaoganjiang Decoction)羊羹麻黄煎じ薬(Sheganmahuang Decoction)青飛頭渓福正レシピ、グリチルリチン、 ヘスペレチン、バイカリン、ケルセチンなどがあり、天然由来のフラボノイドが豊富に含まれている175,176。しかし、一般的に関連する欠点としては、過敏性肺炎、肺損傷、胃腸の不快感を伴う疲労などが挙げられる(表1)。
6. 6. ビタミンA、C、D、Eを豊富に含む食品の消費 天然に存在する抗酸化物質であるビタミンA、C、D、Eを豊富に含む食品の 消費73 。179,180 COVID-19における抗酸化療法を評価するために登録された臨床試験を表3161-164に示する。
7. クルクミンは、ヒトの様々な臓器における SARS-CoV-2 の付着・内在化に寄与する様々な分子標的、細胞内シグナル伝達経路、RNA 複製を調節する能力や、肺水腫や線維化関連経路を抑制する役割など、 科学的に証明されている利点により、COVID-19 に対する潜在的な役割を持つ可能性がある(表1)。 181 また、NF-κB やいくつかの炎症性サイトカインに対する強い抑制作用を示しており、重症化した COVID-19 患者にみられる致死的な CS を逆転させるための補助薬としても使用できる。クルクミンの知られている欠点がないため、臨床試験で評価されている(表3)。
8. オメガ3脂肪酸、蜂蜜とその様々な成分だけでなく、ジャガイモのデンプンの役割は、COVID-19 infection.182の症状と戦うための新規の自然療法として強調されている。183-185 メチルグリオキサール(MGO)は、エンベロープされたウイルスの増殖を抑制し、SARS-CoV-2の複製を阻害することができるマヌカハニーの成分である184,186 さらに、MGOの濃度が高いほど、より強力な抗生物質の効果がある。蜂蜜とデンプンの既知の欠点はないが、オメガ3脂肪酸すなわち、エイコサペンタエン酸(EPA)とドコサヘキサエン酸(DHA)は、潜在的に有毒な酸化生成物の形成につながり、酸化ストレス(表1)を増加させる、活性酸素によって媒介される非酵素的酸化に細胞膜をより敏感にすることができる。 183-185 研究者は、これらの天然物が宿主の免疫系を強化し、COVID-19患者の共存状態を改善し、抗ウイルス活性を高めるのに役立つと考えており、その結果を評価するためにいくつかの臨床試験が登録されている(表3)166-168
ワクチン
現在、全世界がCOVID-19に対するワクチンを開発するために手を携え、利用可能なすべての資源と人手を費やしている。それは、ワクチン接種がCOVID-19の発生を制御するために割り当てられたすべての既存の救済策の縮図として認められる可能性があると考えられている。73,74 エピトープ、mRNA、Sタンパク質受容体結合ドメイン構造に基づいたワクチンは、現在開始されている最も新しいワクチンの提案である。さらに、一般の人々にワクチンが提供された後は、その有効性と安全性を証明するためにヒト臨床試験が必要となる。この残忍な致死性との闘いにおける全科学者の努力は、ちょうど具体化し始めたところである。疫学的事実、ウイルスの性質、ウイルスに対する免疫反応、ワクチン製造における課題など、新しい疫学的事実が日々明らかになってきている50 。おそらく、このようにして研究が発展し、ワクチンが開発されていくのであろう。
未来の非侵襲的治療
COVID-19は、有効な抗ウイルス薬がなく、現在進行中の研究では、安全で効果的なワクチンが開発されていないため、現在まで深刻な問題となっている。したがって、COVID-19を治療または予防するための治療法として、光治療が考えられている。光療法という用語は、レーザー光およびレーザー放出ダイオード(LED)および光力学的療法(PDT)を含む光生物学的変調療法(PBMT)を包含している。
COVID-19におけるPBMT(レーザーとLED)使用の根拠
190,195 急性気道炎や肺炎のマウスモデルを用いた実験研究では、PBMTが肺微小血管漏出、IL-1β、IL-6,細胞内活性酸素を減少させることが示されている。この点、PBMTは単独または補助的な治療法として、その抗炎症作用を介してサイトカインストームやARDSを調節することができ、COVID-19患者における人工呼吸器の必要性を軽減するPBMTの潜在的な効果が実証されている。
炎症性メディエーターのダウンレギュレーション、好中球流入の活性化の減少、内皮障害の改善、肺のTNF-α、IL-1βの減少だけでなく、肺水腫:いくつかの生体内試験の動物実験では、次のような様々な波長を利用している;λ650 nm、λ660±20 nm201とλ780 nmのPBM照射のためのレーザー。 -204 さらに、呼吸器疾患の生体内試験実験動物モデル研究では、PBMTは炎症を軽減し、肺の治癒を促進することが示唆されている199,205,206。その結果、これは重症化した医療システムを大幅に削減できる可能性がある。207 この声明は、PBMT後の慢性閉塞性肺症候群(COPD)と喘息患者に有意な改善が見られたというエビデンスに基づいた臨床結果によって支持されている。
図3は、PBMがSARS-CoV-2ウイルスの細胞および分子活性を逆転させることができるメカニズムを示している200,203,206このノートでは、標準的な従来のプロトコルへの補助として、PBMTで治療COVID-19肺炎の最初の重症例は、最近Sigmanらによって治療された炎症を軽減し、肺の治癒を促進することを目的としている。この症例の発表は、4日間連続して1日1回、パルスλ808 nm(3 Wのピークパワー、周波数1500 Hz、330マイクロ秒、50%のデューティサイクル)とスーパーパルスλ905 nm(ピークパワー75WSm2A303,周波数1500 Hz、10ナノ秒)で28分間(各肺のための14分間)レーザースキャナーによるPBMTセッションを受けた重度のCOVID-19を持つ57歳のアフリカ系アメリカ人男性に関連している。 210フルエンスは7.2 J/cm2と総エネルギー3600 Jだった。レーザー装置は、ターゲット組織の上に20センチメートルを配置し、各肺の上に250 cm2をスキャンしたスキャナを利用した。患者は、CXR、肺重症度指標、血液検査、酸素要求量、患者アンケートによる肺水腫(RALE)の放射線学的評価を介して治療前後に評価された。その結果、酸素飽和度(SpO2)は93~94%から97~100%に上昇し、一方で酸素要求量は2~4L/minから 1L/minに減少した。RALEスコアは8点から5点に改善した。さらに、肺炎重症度指数(PSI)はクラスV(142)からクラスII(67)に改善した。さらに、肺指標(Brescia-COVID、SMART-COP)はいずれも4から0に低下した。CRPは15.1から 1.23に正常化した。この患者は、市中肺炎評価(CAPA)ツールの大幅な改善を報告している。重要なことは、呼吸指標、放射線所見、酸素要求量、患者の転帰が、人工呼吸器を必要とせずに数日間の治療で改善したことが報告されていることである。本報告では、重症COVID-19肺炎患者における支持的PBMTの意義を示した。COVID-19 肺炎患者の臨床転帰に対する PBMT の効果を評価するためには、大規模なデータを有する今後の無作為化比較臨床試験が必要である。
図3 修正された模式図は、ARDSを予防するためにSARS-CoV-2の細胞および分子活性を予備化するPBMTの細胞および分子カスケードを示している。
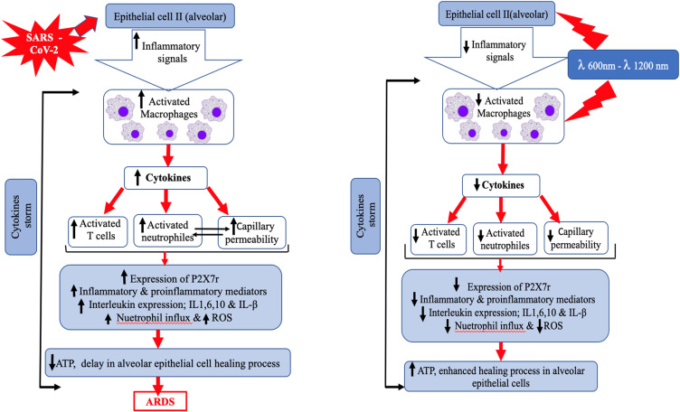
注釈。Mokmeli S、Vetrici M.の許可を得て、複数のレベルでサイトカインストームを減衰させ、回復を強化し、COVID-19における人工呼吸器の使用を減らすためのモダリティとしての低レベルレーザー治療。Can J Respir Ther. 2020;56:1–7.200
今回のレビューでは、SARS-CoV-2ウイルスに感染すると、合併症のリスクが高くなることを強調した9-11。これは、呼吸器系のコンプライアンスの低下、炎症性サイトカインの増加、過剰な脂肪率による二次的な免疫系の活性化によるものである。Sigmanらによる最近の別の症例報告では、先の症例報告と同じプロトコルで照射された重症COVID-19211の病的肥満32歳アジア人女性の治療におけるPBMTの効果が評価されている102。PBMTのアウトカムの評価方法は、重度のCOVID-19と病的肥満の患者を対象に、CXR、肺炎重症度指標(SMART-COPとBrescia-COVID)肺炎重症度指標、血液中の炎症性マーカー(IL-6,フェリチン、CRP)酸素要求量と飽和度を測定した。その結果、パルスオキシメーターによるSpO2が5~6Lの酸素で88~93%であったベースラインと比較して、PBMT後は1~3Lの酸素で97~99%まで上昇した。さらに、PBMT後には、RALEスコアが8から3に、Brescia-COVIDが4から0に、SMART-COPが5から0に、IL-6が45.89から 11.7 pg/mLに、フェリチンが359から 175 ng/mLに、CRPが3.04から 1.43 mg/dLに低下した。この報告は、重度のCOVID-19および病的肥満を有する患者において、従来の治療と併用してPBMTを安全に併用できることを示唆している。このことは、従来の内科的治療にPBMTを併用することでCOVID-19の進行を防ぎ、症状を改善する可能性があることを示したMokmeliらの最近のレビューと一致している。
上記の2つの症例を踏まえると、COVID-19の影響を受けやすい患者では、合併症を最小限に抑えるためにPBMTを利用する傾向が比較的最近見られる。したがって、この有望な非侵襲的治療法を検証するための大規模なデータを有するRCTの実施が急務となっている。
COVID-19におけるPDTの使用の根拠
気道内PDTに最も適した光増感剤(PS)は、様々な臨床治療用途での安全性に優れた性能を持つメチレンブルー(MB、フェノチアジン誘導体)であると考えられている。MBはλ635とλ670nmに吸収ピークを持ち、その完全な吸収スペクトルはλ609nmからλ690nmまでの範囲であり、吸収曲線の上昇部分の低い傾き傾向と下降部分の急激な低下を示している212。COVID-19ウイルスは、そのエネルギーポテンシャルのために感光性分子を蓄積すると推測される。適切に適合した光源(レーザーまたはLED)による光力学的励起は、活性酸素と一重項酸素(1O2)の形成をもたらし、ウイルスの細胞膜を破壊する。ほとんどのウイルスは、DNAまたはRNA(一本鎖または二本鎖)コアと外部タンパク質カバーまたは脂質のいずれかを持っていることを知っているので、それによって、ウイルスの基本的な構造は、ウイルスタンパク質ジスルフィドイソメラーゼ(PDI)と生成された活性酸素との反応のための3つの主要な分子標的を含んでいる:核酸、ウイルスタンパク質、および存在する場合は、ウイルスの脂質:215。216 光力学的損傷は、全体的なPDT用量(PS濃度Sm_2A30ライトフルエンス)などの他の要因と組み合わせて、アポトーシスプロセスにおいて重要な役割を果たしているPSの細胞内位置に非常に近いところで起こる可能性が高いことは注目に値する。
興味深いことに、SARS-CoV-2は、陽性鎖RNAウイルスと同様に、タンパク質のエンベロープやPDT治療の影響を受けやすい脂質など、多くの特徴を持っており、β型CoVのカテゴリーに属している。CoVは円形/楕円形で、しばしば多形で、直径は約60~140nmである。他のCoVと同様に、紫外線や熱に敏感である。重要なことは、発熱、咳、頭痛などの症状の発症時には、口腔粘膜、咽頭、鼻腔粘膜のACE2受容体に多くのウイルスが結合しており、PDTへのアクセスを容易にしていることである。PDTプロセスを介したウイルス負荷の減少は、免疫反応と保護抗体の形成を刺激し、重度の肺機能障害や損傷を伴わない軽度または中等度の疾患経過を促進することができる。これは、口腔咽頭での自然植民地化によるものである。この点で咽頭結節炎PDTは、これらの病原体の減少を促進し、粘膜バリアへの浸透を防ぐためのセーフガードとして機能することができる。このことはBlancoらによって実証されており、咽頭結節炎に対する臨床的PDTプロトコルでは、24時間後に疾患に関連する症状の90%以上が軽減されたことが報告されている。興味深いことに、多くの研究で気道へのPSの送達方法が検討されている。
肺疾患のPDTのためのPS送達のための最も一般的な手段は、静脈内投与によるものである。その結果、PSを直接肺に送達することで、PSの均等な分布の欠如を克服し、副作用を軽減するために、ネブライザーが有用である。微細なカテーテルは、連鎖状甲状腺膜を介して光を送達する別の手段である。この技術は、気管切開のあるCOVIS-19患者に有用である可能性があり、それにより、局所的な設定でのMB-PDTは、予想される罹患率を伴わずに安全である。
Geraldeらによる生体内試験動物研究、224は、PSとしてネブライジングインドシアニングリーン(ICG)を活性化するために60mW/cm2の照度でλ780 nmの単色光を発光し、レーザーダイオードの18クラスターを含むカスタムメイドのレーザー装置を介して体外照明を使用して細菌性肺炎を根絶するためのPDTプロトコルの効率を示している(120 J/cm2)。ICG濃度100μmol/L、15μLのICGをマウスの各鼻孔に注入した。肺炎球菌細胞を持つリクルート感染マウスの数は10匹であった。著者らは、PDT群では死亡は観察されなかったが、対照群では60%であった。また、コロニー形成単位の回収率は、対照群では103〜104/マウスであったが、PDT群では80%の動物で細菌の回収は認められなかった。したがって、著者らは、このプロトコル(肺炎の体外照射型光力学的不活化)を臨床的に実施することは、単独療法として、あるいは抗生物質治療の補助療法としてのPDTの可能性に向けた重要なステップストーンであると結論づけた。Kassabらによる別の生体内試験動物実験では、ジェットネブライザー装置を用いた3種類の光増感剤(ICG、塩素系フォトジタジン、ポルフィリン系フォトジェム)の実行可能性が評価され、肺を直接標的とするのに有効であることが示された。
Schikoraらによる無作為化比較試験/プラセボ試験では、以下の変数に対する抗菌薬PDT(a-PDT)の効果が評価された。感染初期の SARS-CoV-2 ウイルス負荷、肺のウイルス負荷、肺の炎症と重度の損傷、治療の臨床経過、死亡率に対する抗菌薬PDT(a-PDT)の効果が評価された。MB(塩化メチルチオニウム1%溶液を5%グルコース溶液に溶解したもの)を口腔内と喉に塗布し、鼻孔に噴霧した:λ660nmの光エネルギー照射を240mWの出力で5分間、72J/cm2(全照射量360J/cm2)のフルエンスで照射した。PCRリアルタイムテストは、前処理(ベースライン)とa-PDT直後のウイルス負荷を決定するために採用された。さらに、PDTの4週間後には、SARS-CoV-2ウイルスに対する抗体の形成を評価するためにELISAテストを使用して検査を行った。その結果、以下の知見が得られた。(1)死亡率の低下(PDT群0.7%対プラセボ群3.3%)(2)PDT群では重症度の有意な低下(2.6%対19%)COVID-19の進行の減衰(97%対81%)が認められた。その結果、各5段階の治療サイクルの直後にPCR検査で明らかになった咽頭、口腔、鼻腔内のウイルス負荷の低下が認められた。最終的には副作用は報告されなかった。ここで重要なのは、光源を用いた光線力学的励起を行わずにMBだけではウイルス負荷低減効果が得られないことである。著者らは、a-PDTはCOVID-19管理において、副作用のない効果的で革新的な、アクセス可能で費用対効果の高い治療モダリティであると結論づけた。COVID-19パンデミックにおけるPDTのもう一つの重要な応用は、安全な輸血を確保するためのSARS-CoV-2の血漿不活化であることは注目に値する227。
228,229 リボフラビンと紫外線照射は、血小板を含むヒト血漿中のMERS-CoVの力価を検出限界以下に効果的に低下させ、この治療法がMERS-CoVの輸血感染のリスクを減少させる可能性を示唆している。λ405nmの光を採用した研究は、感染リスクを排除するために抗菌性を有することができ、PDTやPDIでは一般的に知られているアプローチにもかかわらず伝播することができることに注意することが重要である。生物戦争を目的とした個人用モバイルデバイスの設計は、特定の波長を照射するためにLEDをプログラムするモバイルアプリケーションのような単純な形態で提案され、使用することができる。さらに、ウイルスの不活化に関しては、λ420 nmからλ430 nmの間の青色波長の範囲の光治療は、白血病ウイルスを不活化することができる200 この文脈では、電磁スペクトルの可視光は、単純ヘルペス(HSV-1)やHIVなどの多くのウイルスを不活化するために血漿のPDTに貢献している213,230,231 最近の報告では、パルス発光モードの青色光は、連続発光モードの場合に比べて、日和見細菌感染症を不活化する効果が20~100倍高いことが示されている232,233。
上述の科学とエビデンスに基づいた実践に基づいて、光治療は、SARS-CoV-2ウイルスを不活化し、そのウイルス負荷を減少させ、宿主の免疫システムを調節するのに役立つサイトカインストームを逆転させるために、単一の治療モダリティとして、または標準的な治療プロトコルの補助として利用することができる。
COVID-19管理のための現在進行中の光線療法登録RCT
上記のすべてのために、光治療は、COVID-19の管理における将来の長期RCTのために、研究者および臨床家から大きな注目を集めるに値する。このことは、Hannaらによる最近の批判的なレビューと一致しており、光線療法はCOVID-19パンデミックにおける有望な治療法であり、その公平な転帰と安全性を評価するために、堅牢で厳格な無作為化二重盲検プラセボ対照臨床試験によって検証される必要があることが示されている。
上述のCOVID-19管理における光線療法の可能性を考慮して、現段階では4つのRCTがclinicaltrials.govに登録されているのみであり、これらのRCTは募集段階にあるか、まだ募集していないか、結果が報告されていないまま終了したかのいずれかである(表4)。これらの試験を以下にハイライトする。
表4 ClinicalTrials.govに登録されている臨床試験を表示している 2020年10月20日まで COVID-19の治療に光治療を利用する臨床試験
| 光線療法 | 研究識別子と引用(上付き文字) | レーザー治療プロトコル | 研究段階; 推定登録数(n) | 主な結果の測定 | 採用状況 |
|---|---|---|---|---|---|
| PDT + PBMT | NCT04416113 | 患者は3つの等しいグループに分けられる。グループIは、レーザーウォッチから低レベルレーザー(ダイオードレーザー980 nm)を30分間、20 Jで3〜5日間、レーザー鍼治療を受ける。グループ2は、メチレンブルーを光増感剤として注入し、レーザーウォッチ(ダイオードレーザー670 nm)を照射することにより、光線力学療法で治療される。グループ3がコントロールとして機能する。評価方法には、臨床検査とCT胸部が含まれる。 | フェーズ:該当なし n = 60 |
WHOによって定義された主要な臨床反応または部分的な臨床反応(PCR)のいずれかを達成した参加者 すべての患者は、完全な個人的および臨床的病歴を伴う徹底的な検査を受け、治療の前後に次のことを行う:PCR、CBC、CRP、ESR、Dダイマー、肝酵素、およびフェリチン、CXR。 1週間経過しても改善が見られない場合、エンドポイント治療は中止される |
アクティブ—まだ募集していない |
| PBMT | NCT04386694 | 侵襲的人工呼吸器を使用してCOVID-19で集中治療室(ICU)に入院した患者の呼吸筋に対する静磁場(sMF)(PBMT / sMF )と組み合わせたPBMT。 このデバイスには、905 nmのダイオードが4つ(各ダイオード1.25 mW、各0.32 cm 2)633 nmのダイオードが8つ(各ダイオード25 mW、各0.85 cm 2)850 nmのダイオードが8つ(各ダイオード40 mW,0.56)ある。センチ2ずつ)。静磁場は110mTである。 PBMT / sMFの適用時間は、サイトごとに60秒になる。下胸部で使用される線量は1部位あたり31.50Jで、合計6部位が照射され、合計で189 Jの線量になる。さらに、首領域(両側)で使用される線量は1部位あたり31.50Jになる。合計1つのサイト(両側)が照射され、合計31.50 J(両側)の線量になる。PBMT / sMFは、皮膚に軽い圧力をかける直接接触法を使用して適用される。 |
フェーズ:該当なし n = 30 |
退院までの時間(時間枠:無作為化の日から退院の日または何らかの原因による死亡の日付のいずれか早い方まで、20日まで評価)退室または死亡までのICUでの入院日数 生存率、横隔膜筋機能 血小板数の ロイコグラムとエリスログラム。 C反応性タンパク質 D-ダイマー 免疫グロブリンGおよびMのレベル、TNF-α、およびビタミンD 呼気終末陽圧(PEEP)のレベル、PO 2、FiO 2 |
採用 |
| NCT04524715 | PBMT:呼吸器系に赤色光PBMTを適用することにより、肺炎の炎症を軽減する。 | フェーズ:該当なし n = 64 |
肺-Oの炎症2 肺-CRPの炎症 肺-IL-6の炎症 |
採用 | |
| NCT04391712 | 肺疾患のCOVID-19陽性患者のためのマルチウェーブロックシステム(MLS)レーザー治療。 レーザー治療は、場合腹臥位で患者、7 J / cmで各肺を横切って10〜25によってCMレーザフィールドを使用して配信された2 1500 Hzで。治療の頻度と期間:1日1回4日間。 |
フェーズ:II n = 10 |
治療後の患者の気質[時間枠:7日]。ベントのICU、換気を必要としないICU、支援を必要とするリハビリのための退院、ADLを実行できない自宅への退院、ADLを実行できる自宅への退院。 酸素化(時間枠; 4日間毎日)。患者のO 2の要件は、前および後処理およびプロトコルの終わりからの変化のための酸素測定評価をパルス IL-6レベル(:試験の最初の4日間の時間枠)。前処理と最終処理の24時間後の変化。 CXRの結果(期間:7日)。RALE CXR評価尺度を使用した、治療前と治療後のCXRの比較。 -ブレシア-COVID呼吸器重症度スケール(BCRSS)(時間枠:7日)。BCRSSで評価された治療前と治療後の変化。 SMART-COPスコア(時間枠:7日)。前処理と後処理を切り替える。 PSIスコア:治療前と治療後の変化。 CRPレベル(時間枠:7日)。 |
完了した (この研究のClinicalTrials。govに投稿された研究結果はまだない)。 |
現在進行中の RCT 臨床試験(まだ募集段階ではない)235 は、COVID-19 患者に対する PBMT と PDT の効果を対照群と比較して評価し、2 週間のタイムフレームで WHO が定義する大規模な臨床的奏効または部分奏効を達成することを目的としている(表 4)。本試験は、発熱、咳、息切れ、悪寒、筋肉痛、新たな味覚・嗅覚の喪失、嘔吐・下痢、喉の痛みなどの症状を有するCOVID-19陽性の入院患者を対象としているが、ICUに入院している重症患者、呼吸困難グレードIIIおよびIVの患者、人工呼吸器を使用している患者は対象外としている。臨床結果を評価するために、臨床検査(分子ベースのアッセイ、血清学と抗原)と胸部CT検査を実施した。60人の募集患者は、次のようにランダム化される:グループIは、30分間、3-5日20 Jとレーザー鍼治療のトリガーポイントの橈骨動脈上の手首に適用されるレーザー時計からλ980nmのPBMを照射し、グループ2は、次のプロトコルに従ってPDTを受信し、670 nmのレーザー時計、光増感剤(PS)としてメチレンブルー(MB)は0.1から0.1の0.1。 2 mL(体重のキログラムあたりの1%溶液)を数分の期間にわたって非常にゆっくりと静脈内に注入し、1時間後に、光フォトニック用量のアプリケーション:100-200 J/cm2,50-100 mW/cm2(50 mW/cm2は、光毒性応答だけでなく、分画光アプリケーションを増加させた)週に2回;一方、グループ3は、コントロール(従来の治療プロトコル)として機能している。
PBMTに関しては、現在進行中の2つのRCTがあり、募集段階にある(表4)236,237。COVID-19と診断され、中等度急性呼吸困難を呈した18歳以上の64名を対象とした。本試験では、PBMTの赤色および赤外域のLED光源を使用している。すべての参加者は、COVID-19の症状に対する標準的な治療を継続して受ける。この試験は、急性ウイルス性肺炎に苦しむ COVID-19 患者の呼吸器系に赤色光 LED 光源を適用した PBMT の後に肺炎の減少が起こるかどうかを決定することを目的としている。PBMTのプロトコルは記録されていない。次の転帰の評価方法は、SpO2,CRP、およびIL-6レベルである。あるいは、COVID-19でICUに入院した患者の呼吸筋に対するLED PBMTと静磁場(sMF)を組み合わせた効果(LED PBMT/sMF)を、侵襲的機械換気を用いて調査するための無作為化三重盲検プラセボ対照試験237が登録されている(まだ募集していない)。表1に記載のレーザープロトコルは、λ850nmの8つのダイオード、λ633nmの8つのダイオード、およびλ905nmの4つのダイオードのクラスター化されたプローブを示している。これは、光が最適な結果を達成するために、浸透の様々な深さで組織と相互作用するであろうことを示している。様々な変数を評価し(表4)この併用療法がCOVID-19の呼吸筋への影響を最小化し、人工呼吸器の離脱プロセスを促進し、関与する筋肉の機能的能力を最適化することに影響を及ぼすかどうかを決定する。
完成したRCT238では、COVID-19感染による肺合併症の治療として、マルチウェーブロックシステム(MLS)レーザー治療の有効性が評価された。レーザー治療は、患者を仰臥位にした状態で、7J/cm2,1500Hzで各肺に10×25cmのレーザー照射場を用いて行われた。治療回数と期間は、1日1回、4日間とした(表4)。しかし、clinicaltrials.govにはまだ研究結果は掲載されていない。
注目すべきは、我々のレビューで強調されているCOVID-19におけるPDTの可能性を一貫して示唆する科学的根拠に基づく研究にもかかわらず、COVID-19の管理におけるPDTとPBMTの併用の効果を評価するRCTは現在までに1件しか登録されていないことである。理想的な光線力学的プロトコルの研究デザインを確認するためには、さらなる研究が必要である。さらに、本レビューの著者らは、COVID-19の各病期(早期・中重症)に対する光線力学的プロトコルが、治療成績の正当性と安全性の確保のために必要であることを指摘している。
おわりに
このレビューは、SARS-CoV-2ウイルスの疫学的および臨床的症状に関する知識と理解が進化しており、最終的には効果的で安全な治療と強力で安全なワクチンの生産に向けた戦略的な道筋を示すものであるため、臨床および科学界が将来の参考として活用できる質の高いエビデンスを生み出した。現在までのところ、COVID-19を治療するために特別に設計された、信頼性の高い安全なワクチンも、効果的で安全な治療法も存在しない。免疫療法および細胞療法のような新しい治療法の革新があり、それらはさらなる研究を必要としている。光療法は、COVID-19の管理において重要な役割を果たすことができる、十分に文書化された治療法である。しかし、この点ではさらなる臨床研究が必須である。
