Contents
The Smoking Syringe: Was evidence withheld from ACIP when they recommended the Pfizer-Vaccine?
ワイズマン Ph.D., M.R.Pharm.S.
2021年9月10日
意見論説 David Wiseman Ph.D., M.R.Pharm.S. (デビッド・ワイズマン博士, M.R.Pharm.S.)

概要
2021年8月30日(月)予防接種実施諮問委員会(ACIP)は、次のような勧告を全会一致で承認した。
ファイザー・バイオエヌテック社のCOVID-19ワクチンは、FDAの生物製剤認可申請(BLA)の承認のもと、16歳以上の人に推奨される。
この勧告は、CDC長官のRochelle Walensky博士によってすぐに承認された。
- この勧告を承認するにあたり、ACIPはファイザー、カイザーパーマネント、CDC、およびその他の科学者からワクチンの安全性と有効性に関する証拠を聞きた。
- しかし、投票後のプレゼンテーションで引用された6つの研究は、この証拠から完全または部分的に除外されていたようである。これらの研究は、CDCやファイザーの科学者によるものも含め、ワクチンの効果、つまりデルタ株に対する効果が90〜95%の範囲から、42%まで低下しているというものである。
- これらの欠落した研究を含めることで、異なるリスク・ベネフィット分析が得られたはずである。
- この勧告がすでにワクチン義務化政策に影響を与えていることを考えると、ACIPに提示された証拠は、科学的整合性と行動に関する最高水準の基準を満たしていないように思われる。
- 例えば、インフルエンザワクチンと比較して、COVID-19ワクチンではワクチン接種者1人当たりの死亡数が177倍になることが報告されているが、そのような他の強力な安全シグナルは考慮されなかった。
- ACIPは、同日にNIHが発表したCOVID-19ワクチンと月経障害との関連性に関する研究への資金提供で示唆された、ワクチンの妊娠や生殖器系への影響の可能性についても考慮しなかった。
- ACIPは、ワクチンがFDAの分類である「遺伝子治療製品」に該当することに関連して、他の長期的影響の可能性(がん、自己免疫疾患)については考慮しておらず、ファイザー社/バイオエヌテック社による「発がん性、遺伝毒性、男性の生殖能力の障害を引き起こす可能性に関する」研究が行われていないことについてもコメントしていない。
- これらのワクチンの使用に起因する短期および長期の心臓、血管、血液、筋骨格、腸、呼吸器、神経学的症状の健康問題は、主要で高価な公衆衛生問題を提起している。この潜在的な公衆衛生危機の認識を具体化し、回避して立ち向かうための行動を促すために、我々は以下の用語を提案した。
ポスト・コビッド・ワクチン・シンドローム – pCoVS
- 必要なことは、以下の通りである。
- pCoVS に対する ICD10 および関連する追跡・償還コードの割り当て。
- 長期および遅延型pCoVSの研究および追跡調査のための資金援助。
- ファイザー社、モデルナ社、ヤンセン社のワクチンを遺伝子治療製品として規制し、長期的な追跡調査を行う。
- FDAとCDCは、2回のワクチン投与の安全性を保証できないのに、3回目(またはそれ以上)のワクチンの安全性をどうやって保証できるのであろうか?
はじめに
2021年8月30日(月)Advisory Committee on Immunization Practices(ACIP)は、以下のような勧告を全会一致で承認した。
ファイザー・バイオエヌテック社のCOVID-19ワクチンは、FDAの生物製剤認可申請(BLA)の承認のもと、16歳以上の人に推奨される。
その後まもなく、米国疾病予防管理センター(CDC)所長のRochelle Walensky博士がこの勧告を支持し、[1]「現在、完全に承認されたCOVID-19ワクチンがあり、ACIPもその勧告を追加した。ワクチンを接種する前にこの承認を待っていた方は、今こそワクチンを接種し、すでに完全に接種している1億7300万人以上のアメリカ人の仲間入りをしよう」と付け加えている。
この勧告がCDCのMorbidity and Mortality Weekly Report (MMWR)に掲載されると、この声明は「米国における予防接種に関するCDCの公式勧告を表す」ことになる[2]。
ACIPの投票に先立って提示された証拠の詳細には、この投票が科学的不正行為の可能性に影響されたことを示唆する内容が含まれている。
何が起こったのか?誰が、なぜ、投票したのか?
CDC[3]は、安全性と有効性が確認された医薬品のみを販売することを使命とするFDAとは異なり、「重要な科学を実施し、国を守るための健康情報を提供する。」ことを目的としている。CDCに助言を与えるのは、非政府機関の科学者、医師、医療専門家、地域社会の代表者などで構成される予防接種実施諮問委員会(ACIP)のような専門家委員会である。
ACIPは、CDCからファイザー・バイオエヌテック社製ワクチンの使用に関する勧告の策定を求められた。ACIPの決定を下すために、ファイザー・バイオエヌテック社とCDCの科学者と医師は、ワクチンの安全性と有効性に関する証拠と、リスク・ベネフィット分析を提供した。
私は同僚とともに、会議の前後にコメントを提出した(1,2) その一部をこの記事に掲載する。
ファイザー・バイオエヌテック社のワクチンの安全性は?
安全性に関する議論では、ACIPの議長であるGrace Lee博士のプレゼンテーションのスライド4に示されている、ワクチンの安全性をモニタリングするために使用されているシステムのいくつかが利用された。
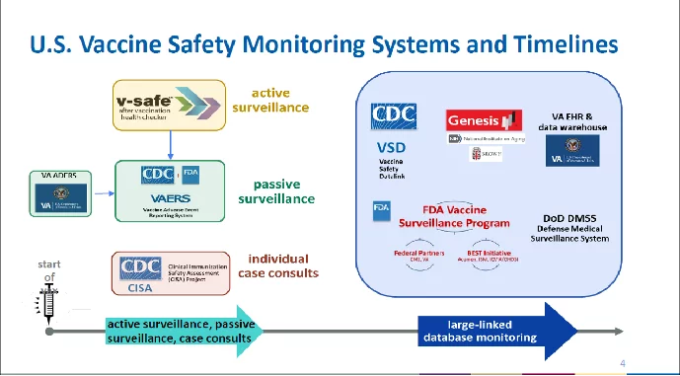
心筋炎に注目
安全性に関する議論では、心筋炎(心筋の炎症)特に若年層における心筋炎に焦点が当てられた。CDCの発表[4]では、NEJM誌に掲載された研究(3)を引用し、ファイザー・バイオエヌテック社のワクチン接種に伴う心筋炎のリスクが3倍であるのに対し、SARS-CoV-2感染に伴うリスクは18倍であると報告している。言い換えれば、COVID-19に感染した場合の心筋炎のリスクは、ワクチンを接種した場合よりも18/3=6倍高いということである。この6という数字は、mRNAワクチンについて調べた査読なしのプレプリント研究(4)と一致している(より高い数字を示したCDCの他の2つの研究が引用されているが、これらの研究は出版されておらず、CDCの内部でのみ利用可能であることを覚えておくこと)。これは、Covidに感染した場合、6倍になるということである。発表では触れられなかったが、そもそもCOVID-19に感染する確率は(せいぜい)8分の1なので、これは相殺されてしまう。

ローゼンブルム博士の発表からのスライド9(脚注4)
安全性の議論から消えた死亡例と心筋梗塞例
他に何が言及されていないのであろうか?私と私の同僚は、会議に先立ってACIPに提出した意見書(1)の中で、COVID-19とインフルエンザワクチンに関連する死亡または心筋梗塞(心臓発作)のVAERSでの報告数を比較した。投与回数で調整すると インフルエンザワクチンと比較して、COVID-19ワクチンでは、死亡が91倍、心筋梗塞が126倍も多かったのである。少なくとも1回の投与を受けた人の数で調整すると、死亡者数は約177人となる(7月30日の数字)。
これは、ワクチンがこれらの事象の原因であることを証明するものではない。しかし、それは問題ではない。これはシグナルと呼ばれるものである。これは非常に激しいもので、剖検を含めて行われた調査の種類と数の包括的な報告を含む透明性のある説明[5]が待たれる。CDCは、COVID-19症例の剖検の実施に関するガイダンスを提供しているが、死亡がワクチンに関連しているかどうかを判断するための剖検の実施に関する前向きなプロトコルはない。これには、ワクチンに起因するスパイクタンパクとCOVID-19感染に由来するスパイクタンパクを区別するための組織病理学的手法の種類についての詳細な説明が含まれる。この分析はどこにあるか?プロトコルはどこにあるのであろうか?同様に、高齢者よりも若年者の方が心臓発作のシグナルが強い(403対88,表1)ことについても調査が必要である。
我々が提出したコメント(1)では、ワクチンによって救われた14万人の命(2021年5月まで)という上限推定値との関連で見るべき、ワクチン関連死の3つの別々のプール、合計45,000~147,000人の死亡を特定した(5)。
- VAERSで過少報告されたCOVID-19以外の死亡者数 – 20,400~62,500人
- ワクチン接種を受けた被験者におけるCOVID-19による死亡 – 25,000-85,000
- ワクチン接種を受けた人からの感染によって貢献したワクチン接種を受けていない人の未知の死亡者数。
これらの3つのプールを区別することが重要だ。最初のプールでは、コービッドに関連しない死亡は、スパイクタンパクの心臓細胞に対する毒性と凝固への影響に関連している可能性がある。コービッド関連の死亡は、ワクチン接種後の免疫抑制が原因である可能性があり、イスラエルの大規模研究(3)で報告された帯状疱疹感染の40%-ワクチン関連の増加が示唆されており、ACIPでのCDCのプレゼンテーションの一つでも言及されている[6]。 コービッド-19は、トイレを共有している被験者の糞便エアロゾル(8)などにより、ワクチン接種者から非接種者に知らず知らずのうちに感染している可能性がある(6,7)。
予防原則に基づき、CDCはこれらの事象とCOVID-19ワクチンとの関連性を説得的に排除する証明責任を負っている。
表1:インフルエンザワクチンと比較したCOVID-19ワクチンのVAERSで報告された死亡または心筋梗塞のシグナル
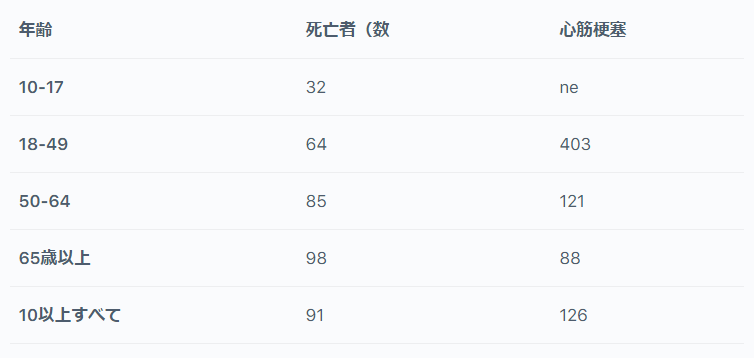
表示されている数字は、各年齢層のインフルエンザワクチン(2015/16-2019/20インフルエンザシーズン)と比較した、COVID-19ワクチンのVAERS報告数(1回あたり)の比率である。COVID-19の報告率は 2021年8月6日時点でのCOVID-19ワクチンのVAERSへのすべての報告を含む。 n.e 推定できない。(1)から抜粋した。
この種の分析に批判的な人たちは、緊急使用許可に基づいて強化された報告義務に関連して、過剰報告があったのではないかと主張している[7]。 CDCの発表の多くは、そのような懸念を表明することなくVAERSのデータを参照している。実際、ある発表では、少なくとも心筋炎・心膜炎については、VAERSとVSD(Vaccine Safety Datalink[8])の発生率データがよく一致しているという指摘があった。
この類似性は、RCA(Rapid Cycle Analysis)と呼ばれるシグナル検出法を用いるVSDシステムにおいて、心筋炎[9]の安全性シグナル(年齢非階層化)を生成するのに十分ではなかった。理論的には、RCAはカイザー・パーマネントのようなシステムで医療記録が作成される際にほぼリアルタイムでシグナルを検出できるはずであるが、この方法はVAERS(9)で規定された方法よりもさらに感度が低く、それ自体に限界があるようである(1)。 VAERSでは、心筋炎はコミナティの添付文書の警告にあるように問題であると認められている(10)。(10)
「市販後のデータでは、特に2回目の投与から7日以内に心筋炎および心膜炎のリスクが高まることが示されている」。
9月3日付のJAMA誌(11)に、VSDシステムのRapid Cycle Analysisの結果を記載した論文が掲載された。それによると、次のように結論づけられている。
「選択された重篤な転帰の発生率は、ワクチン接種後1~21日と22~42日を比較して、有意に高いものではなかった 」と結論づけている。
結論の中にあるVAERSで認められた心筋炎のシグナルの文脈を無視してこの論文を発表することは、非常に誤解を招くことになると思う。
安全性の議論に欠けていた長期的な有害性:遺伝子治療製品、がん
また、これらのワクチンがFDAの遺伝子治療製品の定義を満たしていることから、これらのワクチンの潜在的な長期的影響についても議論されていない。実際 2020年にModernaは「現在、mRNAはFDAによって遺伝子治療製品とみなされている」と認めている(13)。なぜこれが重要なのか?なぜなら、FDAは、遺伝子治療製品が悪性(がん)神経系、自己免疫系、血液系、その他の疾患に及ぼす影響を(適切に)懸念しているからである。この懸念は非常に大きく、FDAは5年から15年の間、試験患者のフォローアップ評価を要求する可能性がある。FDAはいつ自分のガイダンス文書を無視することにしたのか?(12) [10]
8月23日にFDAによって承認されたワクチンのパッケージインサート(10)には、「コミナティは、発がん性、遺伝毒性、男性の生殖能力の障害を引き起こす可能性について評価されていない。」 と記載されている。生物製剤認可申請(BLA)承認書(14)にも、Summary Basis for Regulatory Approval(15)にも、発がん性、遺伝毒性、男性の生殖能力に関する試験を実施することが市販後に求められていない。
安全性の議論に欠けていた生殖器系への影響:月経障害
他に何が欠けていたのか?CDCのスタッフがACIPにファイザーのワクチンの安全性に関する証拠を提出していたまさにその日に、NIHは「COVID-19ワクチン接種と月経の変化との潜在的な関連性を探る」研究に資金提供するという驚くべき発表をした[11]。彼らは詳しく説明している。「一部の女性は、COVID-19ワクチンを接種した後に、月経不順や月経欠落、通常より重い出血、その他の月経変化を経験した」と報告している。CDCはこのことを知らなかったのだろうか?
しかし、ここでは 「一部 」という言葉が重要だ。VAERS(9/3/21)で様々な月経障害[12]を照会したところ、COVID-19ワクチンに関連した報告については、「一部」という意味であることがわかった。
4783件の報告で、7037件の月経障害関連の症状が報告されている。
一部?他のすべてのワクチンと比較すると、すべての年の合算で、798件のユニークイベントで897の症状がある。これらのほとんどは、HPVワクチン(623件の698件の症状)が占めており、季節性インフルエンザワクチンは45件の症状で47件しかない。
私はキャリアの大半を女性の健康の分野で働いてきたが[13]、不本意ながら、この問題は私のレーダースクリーンには映っていなかった。動物実験では、一部のワクチン成分が卵巣に分布していることから、懸念が生じてた。別の分析では月経への影響も指摘されていたが(16)、「月経障害」があまりにも矮小化されていることを知っている。これらの障害の多くは、早期に子宮摘出を行い、癒着、痛み、腸閉塞、心臓病、認知症などの更なる合併症を引き起こしている。このような問題は、リスク・ベネフィット分析で考慮されるのであろうか?
NIHは、報告されている月経の変化について、いくつかの理由を説明している。NIHが「パンデミック関連のストレス」をリストに加えたのは、アメリカ国民に対して透明性を保ち、月経変化の理由をすべて明らかにしたいという強い思いがあったからであろう。しかし、ストレスだけが原因ではない。今回報告された月経変化は、一般的な生殖器系、特に妊娠に対するワクチンの安全性についての未解決の疑問との関連で捉えなければならない。
6月に発表されたCDCの研究(17)では、妊娠中のV-safeサーベイランスシステム参加者35,691人とV-safe妊娠登録者3958人(そのうち妊娠が完了したのは827人のみ)を対象とした予備的な結果として、「mRNA COVID-19ワクチンを接種した妊娠中の人に明らかな安全性のシグナルは見られなかった」としている。この研究では、「妊産婦、妊娠、乳児の転帰を知らせるためには、妊娠初期にワクチンを接種した多数の女性の追跡調査を含む、より長期的な追跡調査が必要である 」と認めている。
このCDCの研究の続報(17)は、9月8日にNEJM誌に掲載され(18)、ACIPの会議の時点では確実に知られてた。この報告書では、無作為化対照群が存在しないという驚くべき事実を踏まえ、次のように結論づけている。
「妊娠前または妊娠中にmRNA COVID-19を接種した後の自然流産のリスクは、予想される自然流産のリスクと一致していることが示唆された;これらの知見は、妊娠中のmRNA COVID-19ワクチン接種の安全性に関する蓄積された証拠に追加される」と結論づけている。
この結論は、コミナティの添付文書(10)に記載されている「リスク概要」という小見出しのガイダンスと矛盾し、軽視しているため、無謀とも言えるほど過剰なものだと私は考えている。
「妊娠中の女性に投与されたコミナティのデータは、妊娠中のワクチン関連のリスクを知らせるには不十分である。
しかし、添付文書全体としては、妊娠に関する明確なガイダンスを提供する点ではるかに優れているというわけではない。と記載されている。「コミナティには妊娠中の暴露登録がある。妊娠前後または妊娠中にコミナティに暴露された方には」
mothertobaby.org/ongoingstudy/covid19-vaccines/
承認書に記載されているように(14)、妊娠中にどのようなリスクがあるかを判断するためにFDAが行った最善の方法は、バイオエヌテック社から4年間の期間で市販後の妊娠・新生児試験を実施することを約束してもらうことであった。
C4591022試験は、「Pfizer-BioNTech COVID-19 Vaccine Exposure during Pregnancy: A Non-Interventional Post-Approval Safety Study of Pregnancy and Infant Outcomes in the Organization of Teratology Information Specialists (OTIS)/MotherToBaby Pregnancy Registry」と題されている。
コミットメントという言葉に注目してほしい。FDAの説明[14]によると
「市販後のコミットメント(PMC)とは、スポンサーが実施することに同意した研究や臨床試験のことであるが、法律や規制で要求されているわけではない。」
これは義務ではない(例えば、心筋炎に関する他の市販後調査のように)。このレベルの規制だけでなく、問題となっている研究の長さと範囲を、7年間[15]の研究が必要とされ、子どもや早期発達への影響を調べることも含まれている、関連性のないヤンセン(J&J)の生物学的製剤と比較してみてほしい。最近(2021)承認されたアストラ・ゼネカ社の生物学的製剤[16]では、妊娠と母体および胎児・新生児のアウトカムに関する9年間の試験が必要とされている。
不十分なリスク・ベネフィット分析
CDCがACIPに提出したエビデンスには、このようなものは一切なかった。実際、リスク-ベネフィット分析(それ自体は16~29歳に焦点を当てたもの)で注目すべき唯一の害は心筋炎であった[17]。

ローゼンブルム博士のプレゼンテーションからのスライド16(脚注4
コービッドワクチン後のシンドローム
VAERSで報告されたコービッド-19ワクチンの死亡やその他のイベントの数の多さ(すべての年の他のワクチンで報告されたすべての死亡やイベントを合わせた数と同程度)は無視できない。この潜在的な公衆衛生上の危機に対する認識を具体化し、回避して立ち向かうための行動を促すために、我々は以下の用語を提案する。
ポスト・コビッド・ワクチン・シンドローム(pCoVS)
定義
SARS-Cov-2ウイルスに対する抗原誘導型の遺伝子治療ワクチンを接種した後に発生する症候群である。この症候群は、心臓、血管、血液、筋骨格系、腸、呼吸器、神経系など様々な症状として現れ、妊娠への影響に加え、長期的な意義は不明であると現在は理解されている。この症候群の発現は、送達された核酸によって誘発されるスパイクタンパク抗原、核酸そのもの、またはワクチンアジュバントが媒介となる可能性がある。より多くのデータが得られるようになると、pCoVSのサブセットや長期的な影響が明らかになり、この定義の見直しが必要になるかもしれない。
我々(1)の提案
- 公衆衛生機関、政府、専門家団体によるpCoVSの認知。
- pCoVS に対する ICD10 および関連する追跡・償還コードの割り当て。
- 長期化・遅延化したpCoVSをモニタリング・追跡するための透明なシステムの確立。
- pCoVSの予防および治療に関する研究のための資金調達の確立。
- ファイザー社、モデルナ社、ヤンセン社のワクチンを遺伝子治療製品として規制すること。
- 遺伝子治療製品に関するFDAガイドラインに沿った、pCoVS用ワクチンの製造業者による長期(15年間)のファーマコビジランスの主張。
- ワクチン接種[18]、または実際の、あるいは潜在的なpCoVSの状態に基づく差別を防止するための法制化。
- 遺伝子治療ワクチンがゲノムや遺伝子発現にどのような影響を与えるかを調べるための資金調達の確立。
ファイザー・バイオエヌテック社のワクチンの効果は?
時代遅れの、非RCT、観察研究、非査読研究の取り込み
複数の発表者による安全性と有効性の分析、およびファイザーワクチンのリスク・ベネフィット分析に大きく貢献したのは、最近、非査読済みプレプリントとして公開された、約4万人の被験者を対象としたファイザー独自のRCT[19]であった(19)。 これらのデータは 2021年3月13日までに収集されたデータについて、ファイザーワクチンの6カ月までの安全性と有効性のデータを報告したに過ぎないことは、議論を通じて広く認識されていた。ファイザー社は3月13日以降に収集されたデータを持っているのであろうか?
再利用医薬品の推進者が観察研究や査読なし(プレプリント)の研究を使用することは、大規模な査読付きRCTによるエビデンスを主張する公衆衛生関係者やメディアから激しく批判されてきた。ACIPの勧告を支持するために提供された重要な分析の1つ(スライド19)[20]に、観察研究や査読なしの研究が含まれていることには疑問を感じたが、7つの査読なしの研究を含む17の観察研究が採用されていた。議論の中で、発表者(Gargano博士)は、観察研究とRCTのデータの間には良好な一致があるという議論者の1人と同意見であった。RCTは1つだけ含まれており19,追加で発表されようとしている(NEJM)研究(覚えておくこと)を参考にした[21]。
これら17件の研究のうち、1件は混合変異株のデータを報告し、1件はデルタ変異株のみ、2件はアルファおよびデルタ変異株、1件のみデルタ変異株のデータを報告した。ファイザー社のワクチンを推奨するというACIPの投票に先立って行われたこの議論では、デルタ変異株の効果や、投票後のプレゼンテーションで説明された免疫力の衰えについての検討は行われなかった[22]。
なぜ投票前に免疫力の低下やデルタに対する有効性を示すデータが省略されたのであろうか?
虫眼鏡を取り出して、スライド6の小さな文字を見てみよう。

ガルガノ博士の発表のスライド6(脚注15)
「8/20/21以前に発表された論文が対象となる」
これは完全に合理的に聞こえるが、ACIPがファイザーのワクチンを推奨することを決議した後に行われたブースター用量、免疫の衰え、デルタ変異株についての議論で提示された証拠(脚注14)を見ると別である。
オリバー博士のプレゼンテーションのスライド15には、ワクチンの効果が40~80%にまで衰えていることが示されている。
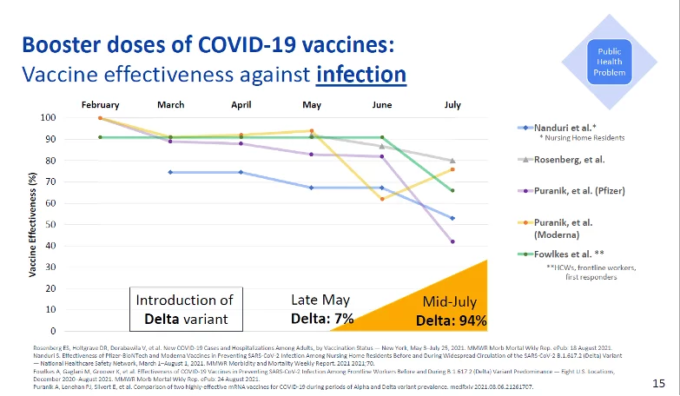
オリバー博士の発表からのスライド15(脚注14)
なぜ投票の前にこのような効果の衰えを考慮しなかったのだろうか?ワクチンの使用を推奨する際には、以前の有効性にかかわらず、現在の有効性のレベルを考慮しなければならないのではないだろうか?あなたは、CDCが投票前の分析を完了するための時間が必要だったので、8月20日を締切日にしたのだと答えるであろう。このスライドで紹介されている4つの研究を見てみよう。
(Nanduri et al 20)これはCDCの論文で、老人ホームの入居者のVEの喪失率が74.7%から53.1%になったというものである。この論文は8月27日にCDCの機関誌「MMWR」(Morbidity and Mortality Weekly Report)に掲載された。この論文は、8月20日の締め切りに間に合わなかったため、投票前の有効性に関するエビデンスには含まれていない。しかし、未発表のデータ(CDCのデータを含む)が投票前の分析に組み込まれていたことは先に見たとおりである。ここでもう一つ問題がある。ナンドゥリ論文にはこう書かれている。「2021年8月18日、この報告書はMMWRのウェブサイトにMMWR Early Releaseとして掲載された」とあり、カットオフ基準を満たしている。
Rosenberg et al (21) これもCDCの報告で、ニューヨークの成人の感染症に対するワクチンの効果が91.7%から79.8%に低下したことを示している。これは8月27日にMMWRに掲載され、8月18日に早期公開された。
Puranikら(22) この査読なしのプレプリントは 2021年7月までにModernaワクチンの有効性が76%に、Pfizerワクチンの有効性が42%に低下したことを示している。この論文はCDCのスタッフが執筆したものではなく、8月8日にmedrxivに掲載された後、8月9日と21日に修正版が掲載された。8月9日と21日に修正版が投稿されたが、これらの修正版でも効果の低下は同じであった。この研究は、投票前のGargano博士のプレゼンテーション(脚注16)で参照されていたが、感染症に対する有効性が42%であるという結果は集計されていないようである。
Fowlkesら(23) CDCの別の論文では、第一線で働く労働者の免疫力が91%から66%に低下していることが示されている。これは8月27日にMMWRに掲載されたが、公開日は8月24日と早まっている。なぜNanduriの論文と一緒に8月18日に発表されなかったのかは不明である。CDCと他の著者による別の論文(24)は、成人での持続的な有効性を示すもので、投票前の分析に含まれており、8月27日にMMWRに掲載されたが、発表日は8月18日と早かったのである。
同プレゼンテーションのスライド52には、上記で引用した4つの論文を含む、デルタ変異株に対するワクチン効果の最近の推定値に関する14の参考文献のリストが掲載されている。

オリバー博士のプレゼンテーションのスライド52 脚注14
このリストには他にも3つの論文があり、デルタ変異株に対するファイザー社のワクチンの免疫力が衰えている、あるいは免疫力が低下していることが書かれてた。
#10. (Sheikh er al)。 (25) この論文自体は2021年6月14日にオンラインで公開されたもので、”Oxford-AstraZeneca社とPfizer-BioNTech社のCOVID-19ワクチンはどちらも、デルタ VOCを持つ人のSARS-CoV-2感染とCOVID-19入院のリスクを減らすのに有効であったが、これらの感染に対する効果はAlpha VOCを持つ人と比較すると低下しているように見えた。”と述べている。
#13. (Tartofら(26) この研究結果は以下の通り
「完全にワクチンを接種した人では、SARS-CoV-2感染症に対する有効性は73%(95%CI:72-74)COVID-19関連の入院に対する有効性は90%(89-92)であった。感染症に対する有効性は,完全接種後1カ月間の88%(86~89)から,5カ月以上経過すると47%(43~51)に低下した。シークエンスされた感染症のうち,デルタに対するVEは他の変異株に対するVEに比べて低かった(75%[71-78]対91%[88-92])。デルタ感染症に対するVEは,完全接種後1カ月間は高かったが(93%[85-97]),4カ月以上経過すると53%[39-65]に低下した。全年齢でのデルタ感染による入院に対するVEは全体的に高かった(93%)。」
このプレプリントは2021年8月23日に掲載された。Pfizer社から資金提供を受けており、15人の著者のうち7人の所属がPfizer社となっている。
Pouwelsらの研究(#7)(6)は、上記の非掲載論文と同様の発表日にもかかわらず、Gargano博士の投票前プレゼンテーション(脚注16)に含まれてた。この研究では、ファイザー社(BNT162b2)モデルナ社、アストラゼネカ社(ChAdOx1)のワクチンのVEを調べ、次のように結論づけている。「SARS-CoV-2ワクチンの接種は依然として新規感染を減少させるが、効果とピークウイルス負荷の減衰はデルタで減少する。」
「重要なのは、デルタ優位の期間における減衰が、ChAdOx1だけでなくBNT162b2でも統計的に有意になったことである(例えば、2回目接種後14日目のCt<30 VE 84%(82-86%)デルタ対94%(91-96%)アルファ(異質性p<0.0001)、ChAdOx1ではそれぞれ70%(65-73%)対86%(71-93%)である(異質性p=0.04))。」
この研究は、8月24日にmedrxivにプレプリントとして掲載された。しかし、CDCが引用しているように、この研究はNuffield Department of Medicine(オックスフォード大学)のウェブサイトに初めて掲載された。ファイル名を見ると、ファイルの日付は2021年8月16日となっている。参照されているリンクのHTMLコードを調べると
したがって、ACIPの投票後に発表されたプレゼンテーションで引用された、デルタに対する免疫の衰えや減少を記述した合計6つの論文は、勧告の投票前にCDCがACIPに提出したファイザーワクチンの有益性と有害性に関する証拠(脚注13)から、完全または部分的(適切な部分)に省略されていることがわかる。この6つのうち、4つ(20-22,25)は明らかに8月20日の掲載締切日を満たしている。これら4件のうち、1件(22)は投票前のDr.Garganoによるプレゼンテーション(脚注16)で参照されていたが、感染症に対する有効性が42%という知見は集計されていなかったようである。
1つの研究(23)は、CDCスタッフによって8月24日にMMWRにアーリーリリースとして掲載された。別の研究(26)は8月23日に掲載されたもので、ファイザーが資金提供し、ファイザーの科学者が参加している。8月20日の締め切りに間に合わなかったにもかかわらず、投票前のCDCのプレゼンテーション(脚注13)に未発表のデータ(脚注14)が含まれていたことや、ACIPに提示された以前のエビデンス(脚注4)にCDCの未発表のデータが含まれていたことを考えると、これら2つの研究が投票前のエビデンスから除外された理由を正当化することは困難である。ファイザーの代表者が提示した証拠(脚注12)から、ファイザーが資金提供した研究(著者にファイザーの科学者が含まれている)(26)が明らかに省略されていることについても説明が必要である。
最後に、ACIPの投票直前に提示された証拠(脚注13)に含まれていた研究を8月20日にカットオフしたことは、投票後に提示された証拠(脚注15)に含まれていたことから、恣意的に見える。
ワクチンの効果が低いことを示すデータを含めることで、リスク・ベネフィット分析はどのように変化するであろうか?
ワクチンの有効性が90~95%の範囲から50%以下に下がれば、リスク・ベネフィット分析は大きく変化し、これらのワクチンは、安全性への懸念がはるかに少なく、さまざまなシナリオでの有効性が30~60%である再利用薬(ヒドロキシクロロキン、(27-29)イベルメクチン、(30,31)フルボキサミン、(32)亜鉛・ビタミンD・その他のビタミン(33,34))と拮抗することになる。ブースター用量の認可に向けての競争の中で、選択肢は尽きつつある。FDA、NIH、CDCは、再利用薬、特にイベルメクチンに対するメディアの攻撃が最近急増していることを支持するかのように見せかけて、自らを窮地に追い込んだのかもしれない。この薬は、「SARS-CoV-2感染の診断が確定しており、入院や死亡につながるような重症化のリスクが高まっていない、入院していない症状のある成人被験者」を治療することを目的としている。(35)
プランAがワクチンに頼り、事後的なプランBがブースター用量に頼るとすると、プランCはPF-07321332の到着をもう1年待つことになるのだろうか。
ブースター投与
投票後に行われたオリバー博士によるブースター投与に関する議論(脚注14)では、主に免疫力の低下とデルタに対する効果の低下に関する既存のデータのみに焦点が当てられた。討議者は、ブースター投与の使用を裏付ける信頼性の高いデータを作成することの難しさを認識しており、9月中旬に予定されているFDAによる承認後にブースター投与に関するACIP勧告を裏付けるデータを得ることができるような計画が概説された。現在、どのようなデータが存在しているのか、また、その時点でどのようなデータが得られるのかは不明である。
オリバー博士は、ブースター投与の安全性と有効性の両方を判断することが重要であると述べている。

オリバー博士のプレゼンテーションからのスライド29(脚注14)
「ブースター」という言葉の使用には疑問があり、「3回目の投与」を他の種類のワクチンと同様に、計画された一連の予防接種経過の中の1つに過ぎないと位置付けるよりも、あまり良い意味合いではないと示唆された。これは明らかにCOVID-19ワクチンの場合ではなかった。もしこれが計画されていたならば、ピボタル試験の中でブースターの効果を調べるための規定を設けることができたであろう。しかし、これらの試験では盲検化が実質的に失われているため、このようなことはほとんどできない。(36)
3回目の投与に関する安全性の評価は、2回目の投与後に残る短期的および長期的な安全性に関する重大な問題と併せて考慮する必要がある。
3回目の投与の有効性については、現在、ほとんどデータがない。最近の研究(37)では、免疫力が低下したり、減少したりした場合には、追加投与によって回復することが示唆されているが、これは部分的なものであり、せいぜい一時的なものである。
ACIPがこの勧告を出す必要があったのはなぜか?
投票に先立ち、プレゼンテーションをもとに幅広い議論が行われた。エビデンス・トゥ・レコメンデーション・フレームワーク」。その議論の中での主要な関心事の1つは、ワクチンをためらうことの問題であった。ある調査では、ワクチンを接種していない人に質問した。
「現在、緊急時の使用が許可されているワクチンの一つが、FDAから完全な承認を受けた場合、あなたはワクチン接種を受ける可能性が高くなるか」(強調)。
その結果、「ワクチン未接種者の31%が、FDAによるワクチンの完全承認後に接種する可能性が高くなると答えた」、つまり「どのワクチンでもよい」ということになる。
これは、FDAが存在しないワクチンを承認するという不可解な行為の根拠となりうるものである。CDCはこれを次の段階に進め、少なくとも31%のワクチン躊躇を克服するためには、あらゆるワクチンのFDA承認が必要であるだけでなく、CDC/ACIPの推奨も必要であると推測している。

Dooling博士によるプレゼンテーションのスライド37と43(脚注18)
したがって、今回承認されたようなACIPからの勧告と、少なくとも1つのワクチンに対するFDAの完全な承認(すなわちBLA)があれば、ワクチンのためらいを減らすための重要なステップになると考えられた。おそらく、8月23日にFDAがバイオエヌテック社(ファイザー社/バイオエヌテック社ではなく)に対して、米国ではまだ入手できないワクチン(コミナティ)の生物製剤認可申請(BLA)を不可解にも発行したときも、このような考え方が優勢であったと思われる。
ACIPの勧告はさらに不可解なものである。その表現は、FDAが説明しているように、法的に異なる2つのワクチンが存在するという法的現実を考慮していない[(38)の脚注8]。この法的区別に意味を持たせるためには、VAERSに2つの法的に異なるワクチンを別々に報告・追跡する機能が必要である。我々は、製造者のリストに、バイオエヌテックとファイザー/バイオエヌテックの両方が表示されることを期待すべきである。そうではない(9/6/21)。勧告の文言は、一方では「ファイザー・バイオエヌテックのCOVID-19ワクチン」(まだEUAの下にある)について述べ、他方では生物製剤認可申請(BLA)承認(コミナティ COVID-19 Vaccine, mRNA)について述べているため、意味をなさないほど誤解を招くものとなっている。
科学的不正行為はあったのか?
本稿の冒頭で指摘したように、ACIPの勧告に対するCDCの承認がMMWRに掲載されると、「米国における予防接種に関するCDCの公式勧告を表す」ことになる[24]。 CDCの承認は、ワクチンの義務化や試験に関する公共政策に、すでに大きな影響を与えている。したがって、ファイザーとCDCの科学者がACIPに提示する証拠は、科学的誠実さと行動に関する最高水準の基準を満たすものでなければならない。有効性が90-95%の範囲から42%まで低下したことを示す主要な研究を含めることで、リスク・ベネフィット分析が異なったものになったことは間違いない。これは、裁判で弁護士が証拠を隠すことに似ていないか?
「科学的不正行為 」はCDC[25]で定義されている。
「42 CFR Part 93(subpart 103 [26] (39)参照)に記載されている該当する連邦規制の下では、研究不正行為は、研究の提案、実施、レビュー、または研究結果の報告における捏造、改ざん、盗用と定義されている。研究不正行為には、誠実な誤り、意見の相違、著者論争は含まれない」。(強調)
8月30日に起きたことが何らかの法律、規制、倫理規定に違反しているかどうかは、倫理学者や弁護士に任せることにする。私は、この記事で指摘された矛盾が、善意の人々の勤勉さを損なうパンデミックの状況によって課せられた要求の結果であることを願うばかりである。もしそれが説明であるならば、問題はまだ修正されなければならない。訂正されていなければ、私にとっては何の問題もない。Has Covidは皆の嗅覚を失わせてしまったのである。
謝辞と資金調達
この問題を解決するために才能と時間を捧げ、刺激的な議論とインスピレーションを与えてくれた、COVID-19のパンデミック中に出会った多くの新しい仲間に感謝している。
また、COVID-19に関連した仕事では、Steve Kirsch氏の寛大な支援に感謝している。私の会社はこれまでに、ジョンソン・エンド・ジョンソンをはじめとするCOVID-19の分野以外の多くの企業からコンサルティング料や研究契約料を受け取っている。
