Contents
- The Scientific Basis of Uncertainty Factors Used in Setting Occupational Exposure Limits
- 要旨
- はじめに
- 不確実性要因の応用と説明
- 不確実性要因の職業曝露限界値導出への応用
- 式(1) 全身性影響のための OEL の計算
- 個別の不確実性要因の根拠
- 表1 OEL設定で使用される不確実性因子とその使用根拠
- 表2 デフォルトの不確実性/労働者の評価要因
- 図1 OEL設定のための非がんリスク評価で一般的に考慮される不確実性を概念的に示したもの
- 科学的根拠に基づく調整因子を用いた不確実性の原因への対応
- 動物から人への不確実性因子
- 個体間(ヒト)変動性不確実性因子(UFH)
- LOAEL-NOAEL不確実性因子(UFL)
- 短期-長期不確実性因子(UFS)
- データベースの不備(不完全なデータ) 不確実性因子(UFD)
- 複合不確実性因子(UFC)について
- 表3 代替的な不確実性因子ドキュメンテーションアプローチのメリットと限界
- トキシコキネティック調整因子
- 修正因子(MF)
- OEL設定における化学物質固有の調整因子(CSAFs)
- 図2 単峰分布からの化学物質特異的調整係数(CSAF)の導出( 73 )
- 図3 バイモーダル分布からの化学物質特異的調整係数(CSAF)の導出( 73 )
- 結論
The Scientific Basis of Uncertainty Factors Used in Setting Occupational Exposure Limits
www.ncbi.nlm.nih.gov/pmc/articles/PMC4643360/
要旨
不確実性因子の概念は、労働暴露限界値を導き出すほとんどの組織を含め、公衆衛生実務のあらゆる側面の健康リスク評価に統合されている。不確実性因子の使用は、有害影響の発生の境界線上にある者からの曝露を十分に減少させれば、脆弱なサブグループを含め、少なくとも曝露された人口の大多数にとって安全な曝露レベルが得られるという前提に基づいている。
職業評価を実施するグループ間では、不確実性因子アプローチの適用に違いがあるが、すべての、あるいはほぼすべての職業暴露限度設定機関が考慮している不確実性の共通領域がある。よく検討される 5 つの主要な不確実性には、
- 動物実験からヒトへの外挿を行う際の反応の種 間変動、
- ヒトにおける反応の変動、
- 影響が観察された用量から無影響レベルを推定する際の不確実性、
- より短い期間の研究から全 生涯暴露への外挿、
- および最も感度の高い有害影響が評価されていない可能性を示す全体的な健康影響デー タベースのその他の不十分さが含まれる。
加えて、いくつかの組織では、その他の不確実性を考慮するために修正因子を使用しているが、これは主に曝露シナリオに関連したものや、上述の 5 つの分野の相互作用を考慮したものである。
作業暴露限度値の導出における不確実性の考慮は、数学的には不正確ではあるが、適用される係数が恣意的なものではないように、体系的なプロセスである。不確実性因子の適用のための科学的根拠が改善されたため、デフォルトの不確実性因子は、化学物質固有のデータがない場合にのみ使用されるようになり、可能な限り化学物質固有の調整因子に置き換える傾向にある。
個々の化学物質の不確かさ因子の開発に科学的データを適用することが増えたことは、作業暴露限度値の導出の透明性を高めるという利点もある。不確実性因子の科学的根拠の特徴付けが改善されたことで、作業暴露限度値の導出プロセス全体の一部としての適用の厳密性と透明性が向上したのである。
キーワード
調整係数、作業暴露、リスク評価、不確実性因子
はじめに
暴露限界値の設定に不確実性因子(UF)を使用することは、少なくとも1954年にまで遡ることができる。不確実性因子の概念は、健康ベースの職業暴露限界値(OEL)の導出を含め、現在の公衆衛生のあらゆる面で健康リスク評価に取り入れられている。不確実性因子の概念は広く普及しているが、不確実性因子の名称は組織によって異なり、安全因子や評価因子などとも呼ばれている( 2 , 3 )。また、不確実性因子の適用に影響を与える労働災害リスク評価の独自の側面もある。( 2 , 4 ・8 ) これらの論文では、制限値設定プロセスにおける不確実性の原因について簡単に説明し、デフォルトの不確実性因子の可能性を示唆しているが、OELを設定するために推奨されている不確実性因子の科学的な裏付けを示すものはなかった。
不確実性因子を適用するための概念的根拠は、化学物質の毒性は通常、有意な影響がなく、生物学的補償の範囲内で最小の影響(必ずしも有害ではない)明らかな毒性の影響、そして最終的には明らかな疾患や死亡に至るまで、用量の増加に伴って予測可能なパターンをたどるというものである( 9 ) 。OEL値を公表している組織は、生物学的閾値の欠如を示唆する毒性作用モード(MOA)を持つ化学物質へのアプローチ方法が異なる。この問題は、遺伝毒性のある発がん性物質や変異原性物質の文脈で最も一般的に遭遇するが、これらの化学物質は、ほとんどの毒性物質に安全な用量が存在するという一般的なルールの例外であると考えられることが多い。このような化学物質は、ゼロ以上の用量であれば、ある程度の過剰リスク(ごくわずかではあるが)をもたらすものとして扱われることが多い。多くの組織では、生物学的閾値を持たない化学物質の許容曝露レベルの開発は、不確実性因子の適用よりも、用量反応モデルと低用量外挿法に基づいている( 10 ) 。その結果、がんと非がんのエンドポイントの統合的なリスク評価アプローチが可能となり、生物学的理解を最も反映した手法が用いられるようになってきている( 11 ) 。
本論文では、不確実性因子アプローチのOEL設定への応用と課題について解説する。この原稿で強調したポイントは以下の通りである。
- リスク評価機関の間では、OEL設定における変動性と不確実性の領域については概ね一致している。しかし、不確実性因子 の定量的な適用や OEL の根拠となる文書のレベルは大きく異なる。
- 現在のOEL設定の基準は、化学物質に特化した調整を行い、不確実性因子選択の文書化と透明性を高める方向へと一般的に変化している。
- リスク管理者がOELを十分に理解した上で使用し、解釈するためには、OELに記載されている変動性や不確実性の原因を理解しておくことが不可欠である。
- また、従来の動物実験にとどまらず、新たな試験戦略の結果を含めた毒性学の進歩は、定量的な不確実性因子適用を含め、作用機序や用量反応評価に大きな影響を与えている。
不確実性要因の応用と説明
不確実性要因の職業曝露限界値導出への応用
不確実性因子は出発点(PoD)が決定された後( 12 )、OELを設定する前にOELプロセスに入る。出発点(PoD)とは、OELへの外挿の出発点となる健康影響試験の用量または濃度のことを指する。PoD が被曝集団又は動物の投与群における無影響レベル(例えば、観察されない逆影響レベル [NOAEL]又は基準線量 [BMD])又は影響レベル(例えば、最も低い観察されない逆影響レベル [LOAEL])を表すかどうかにかかわらず、一般的には、PoD がより広範な作業集団における真の無影響レベルとどのように関係しているかについては、多少の不確実性が存在する。これは特に動物実験データに基づく場合に顕著である。不確実性因子を適用することで、化学物質に関連する全ての有害影響から保護されるOELが得られることを意図している。
計算の目的のために、健康ベースのOELは、臨界影響のPoDを様々な不確実性または調整係数で割って、対象となる労働者集団における「真の」無影響レベルに外挿することで算出される(式(1))。一般的に、OEL は、ヒトボランティアを対象とした質の高い疫学研究または管理された吸入暴露研究から、最も信頼性の高い方法で導出することができる。しかし、PoD は通常、比較的少数の動物またはヒトを対象とした単一の主要な研究から得られるものであり、場合によっては別の経路での曝露の可能性もある( 12 ) 。他の単位(例えば mg/m3 暴露濃度)を使用する場合、あるいは PoD が局所的または部位別の影響に関連する場合には、用量単位の調整が必要となる場合がある( 13 ) 。 一般的に考慮される不確実性の主要な原因のそれぞれについて、不確実性因子 が定義されている。これらの因子を乗算して複合不確かさ因子(UFC)を形成し、健康ベースの限界値を設定するために使用される一般的な式の分母に使用される。
式(1) 全身性影響のための OEL の計算

個別の不確実性要因の根拠
関与する組織にかかわらず、生物学的変動性とデータベースの不確実性に関連して、すべての、あるいはほぼすべての OEL 設定組織が考慮すべき共通の考慮事項がある。表 I は、本稿で使用する EPA( 14 ) の命名法を用いて、共通の考慮事項を強調したものである。使用されている具体的な命名法、具体的な個別要因、およびそれらのデフォルト値は、組織によって異なる(表 II)。ほとんどの専門委員会は、明示的に使用されている場合でも、不確実性因子 に割り当てる値に関する具体的な情報を公表していないことに留意されたい( 15 , 16 )。
表1 OEL設定で使用される不確実性因子とその使用根拠
| 因子 | 不確実性の領域 | 基本的な原則 |
|---|---|---|
| 不確実性因子 A | 動物から人間へ | PoDが動物実験に基づいている場合、動物と平均的な人間の間の感度の違いを調整します |
| フロリダ大学H | 平均的な人間から敏感な人間 | 平均的な人間と最も敏感な適用可能な亜集団の違いに合わせてPoDを調整します |
| 不確実性因子 L | LOAL-to-NOAEL | ベンチマーク線量またはNOAELではなくLOAELに基づいている場合、影響の開始のしきい値の推定値としてPoDの値の不確実性を調整します |
| フロリダ大学S | 短期から長期の曝露 | より短い期間の研究から外挿するときに、慢性毒性のより低いPoDを特定する可能性を調整します |
| フロリダ大学D | データベースの不足 | 追加の研究が利用可能であった場合、より低いPoD(またはより感度の高い効果)を特定する可能性を調整します |
表2 デフォルトの不確実性/労働者の評価要因
| 因子 | ECHA | ECETOC | TNO / RIVM | その他B |
|---|---|---|---|---|
| 不確実性因子 A | AS–BW 0.75 2.5(TD) | AS–BW 0.75 | AS 3(TD) | NS |
| フロリダ大学H | 5 | 3 | 3 | NS |
| 不確実性因子 L | 1 | 3またはBMD | 1〜10またはBMD | NS |
| フロリダ大学S | 2–6 | 2–6 | 10〜100 | NS |
| フロリダ大学D | 1 | NA | 1 | NS |
| MF | NA | NA | NS | NS |
AECHA (2008) Table R.8-19より抜粋。情報要求事項及び化学物質安全性評価に関するガイダンス。第 R.8 章:ヒトの健康に対する用量(濃度)反応の特性化(41) BACGIH-American Conference of Governmental Industrial Hygiists Thresholden Limit Values; American Industrial Hygiene Association Guideline Foundation Workplace Environmental Exposure Levels; SCOEL-Scientific Committee on Occupational Exposure Limits; 略称:ECHA-European Chemicals Agency; ECETOC-European Centre of Ecotoxic and Toxicics Chemicals (ECETOC) ECHA-欧州化学物質庁、ECETOC-欧州化学物質生態毒性学・毒性学センター、TNO/RIVM-国立公衆衛生環境研究所(TNO栄養・食品研究との協力)AS-アロメトリックスケーリング(BW0.75)NS-指定なし、TD-毒性力学
不確実性の各領域を概念的に可視化したものを図 1 に示す。ここでは、不確実性因子は異なる種類のデータの線量反応曲線間で、あるいは同じ線量反応曲線上の異なる点間で、異なる外挿値として表示されている。不確実性因子のうち2つの不確実性因子(UFAとUFH)は、特に生物学的変動性を扱っている。生物学的変動性の場合、より多くの情報を得るための研究は、固有の変動性を特徴づけるのに役立ち、必要とされる因子の値を増減させることができる。例えば、動物のバイオアッセイデータに基づいて PoD が作成されている場合、UFA は実験動物からヒトの毒性に外挿する際の不確実性を考慮している。PoDに対するこの調整は、ヒトの反応が動物の反応よりも低い用量で起こる可能性を可能にする。同様に、UFHではヒトの用量反応関係の動態や動態の変化を考慮することができ、平均的なヒトから感受性の高いヒトや感受性の高いヒトのサブ集団へとPoDの推定値を調整することができる。これらの2つの要因を合わせることで、動物のNOAELを感受性の高いヒトのNOAELに変換する効果がある。多くの場合、PoDの原データには他の不備があり、その結果生じる不確実性は、UFL、UFS、およびUFDの3つの追加要因を用いて対処されている。これらの 3 つの要因は、より完全なデータが利用可能であれば、より低い PoD が発見されていた可能性を説明するものである。より多くのデータを適用することでこれらの不確実性を低減することで、より良いPoDを提供し、全体の不確実性を低減することができる。UFLは、同じ用量反応曲線内のLOAELからNOAELに外挿するために適用される。UFS は、短期間の試験で得られた PoD を、より長期の試験で観察される可能性のあるより低い値にシフトさせる。UFDは、より感度の高いエンドポイントを特定できた可能性のあるデータの欠落(例えば、発生毒性試験や生殖毒性試験の欠落)を調整することを目的としている。これらの不確実性の各領域については、以下に詳述する。
図1 OEL設定のための非がんリスク評価で一般的に考慮される不確実性を概念的に示したもの
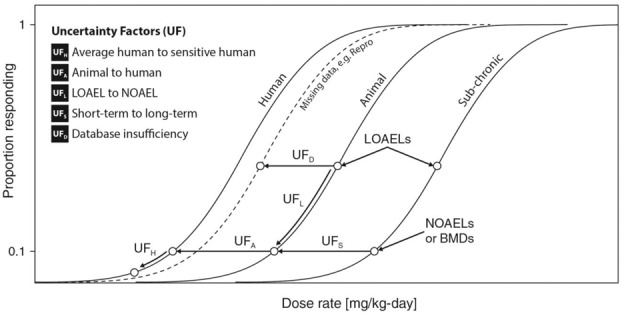
不確実性因子は、実験動物対ヒト(UFA)平均値対感受性の高いヒト(UFH)LOAEL対NOAEL(UFL)短期対長期(UFS)またはデータベースの不十分さを調整するための調整因子(UFD)のいずれかについて、線量反応曲線間で異なる外挿を行ったものと考えられる。
科学的根拠に基づく調整因子を用いた不確実性の原因への対応
Dourson and Stara, (17 ) Naumann and Weideman, (18 ) と Dourson ら (19 ) は、後述する不確実性因子の科学的根拠をまとめたものである。不確実性因子 の使用は、安全な濃度・用量を決定するための政策決定に基づく科学的判断である。この判断は系統的なアプローチに基づくものでなければならない。適用すべき適切な不確実性因子を決定するためには、通常、毒性学的な専門知識が必要であるが、特定の化学物質に関する利用可能なデータと科学的根拠に裏付けられている場合には、代替因子を使用することもできる。このため、OELを確実に導出するためには、各主要な不確実性領域の根本的な根拠と意図を十分に検討し、利用可能なデータに基づいてどのように対処するのが最善かを検討する必要がある。以下に説明する不確実性因子は、ヒトに対する安全な曝露レベルを設定する際の変動性と不確実性の主な原因に対応している。これらの値は、保護対象となる集団のセグメントによって異なる可能性があることに注意してほしい。米国環境保護庁(EPA)によって設定された基準線量(RfD)は、若年者、高齢者、病弱者を含む全人口を生涯にわたって保護することを目的としている。OEL は、一般的に健康な成人と考えられている労働者を生涯にわたって保護することを目的としている。また、労働者の子孫を保護し、就業期間を超えて早すぎる病気や死に至ることがないようにすべきである。
動物から人への不確実性因子
動物-ヒト間の不確実性因子(UFA)は、動物ベースの PoD から外挿して、「平均的な」ヒトの対応する PoD を推定するために使用される。この係数を適用する際には、臨界毒性試験で使用した動物よりも低い用量でヒトが反応する可能性を考慮に入れている。ヒトは、与えられた反応に対して動物よりも同じように感受性が高いか、あるいは低い感受性である可能性があるため、この仮定は予防的なものと考えられる。この係数は、後者の可能性を示すデータがない場合に使用され、可能であればデータで置き換えることが望ましい。化学物質に特異的なデータがない場合には、デフォルトの不確かさ係数を 10 と高く設定するのが一般的である。
UFAはしばしば、種間の毒物動態(TK)の違い(すなわち、毒性のための標的組織への内部線量の違い)のためのサブファクターと、感度(すなわち、与えられた内部線量に対する標的組織の応答の違い)のためのサブファクター(TD)の違いで構成されているように概念化される。このようなUFAのサブファクターへの分割は、各機関によって異なる。特に、WHOは毒物動態学に4,毒物動態学に2.5のサブファクターを適用している( 20 , 21 )が、EPAは一般的に√10の同等のサブファクター、すなわち約3を使用している( 22 ) 。この調整は、個人間の TK サブファクター(後述)にも関連する可能性がある。
種子間の違いが毒物動態と毒物力学の両方を反映していることを認識することで、既知の生理学的な違いを考慮してこの因子を改良する可能性が出てくる。TKの違いに対処するための1つのアプローチは、アロメトリックスケーリングによるものである。アロメトリックスケーリングでは、体重または表面積の比に基づいて生理学的パラメータや基礎代謝(したがって化学物質の代謝や排泄)の違いを推定することができる。初期臨床試験における投与量設定に関する FDA のガイダンス文書には、アロメトリック・スケーリングに基づくヒト換算投与量を推定するための種 類固有の外挿係数が記載されている( 23 ) これらは医薬品の OEL の設定に用いられることもある。体表面積又は体重に基づくアロメトリック尺度を 2/3乗(BW0.67)に使用することで、臨床試験の安全性を向上させるために使用されるヒト当 たりの用量が得られる( 23 ) 。体重を ¾乗(BW0.75)に換算した場合、1.5(イヌ)から7(マウス)までの範囲の種特異的係数が得られる( 26 ) Bokkers and Slob( 27 ) による分析では、アロメトリック外挿係数の 95 パーセンタイルに基づいて、アロメトリックに換算した用量に 3.1 の追加 不確実性因子 を適用すべきであることが示唆されている。Vermeireら(3)も同様の結論に達している。著者らは特に毒性力学に起因するものではないが、この追加の不確実性因子は、数値的には、アロメトリックに尺度化されたTKのサブファクターにTDのサブファクターを追加するのと同様である。Escherら( 28 )による最近の分析では、種間外挿のためのアロメトリックスケーリングの使用を支持しているが、残りの不確実性は毒性力学以外の要因に起因する可能性があると主張している。実際には、これらのアロメトリックスケーリング法に基づいて因子を適用した後に、毒性力学的差異に対処するための追加のサブ因子の必要性についてはコンセンサスが得られていない。
UFA を精緻化するための高度なドジメトリー技術が追加されており、一般的には、この因子の TK 部分を種間の生理学的差異に基づくデータで置き換えることができる( 13 ) 。吸入ドジメトリーを用いて調整された PoD に基づく評価については、その方法が TK の変動性のすべての重要な側面に対応しているかどうかも考慮する必要がある。例えば、予測された沈着率や表面濃度のみに依存する方法では、代謝や排泄に関連する他の動態過程を十分に考慮していない可能性がある。一部では、このような考慮事項は、関連する標的組織の線量を推定する高度なアプローチを使用して対処することができる。最近発表されたジアセチル( 29 ) の PBPK (Physiologically-based pharmacokinetic) モデルは、このようなモデルが、種間スケーリングのためのデフォルトの TK 仮定を置き換える可能性を示している。
個体間(ヒト)変動性不確実性因子(UFH)
個人間(ヒト)変動性不確実性因子(UFH)は、ヒト集団内の一般的な生理学的および代謝学的変動、および年齢、性別、遺伝的感受性、持病などの変動により敏感な部分集団が存在する可能性を考慮したものである。一般的に、OEL はほぼすべての労働者を保護することを意図しているが、母集団の中で最も感受性の高い個人を常に保護できるとは限らない。例えば、Johansson ら( 30 ) は、喘息患者の実験データは一般的に OEL 値を設定する際に明示的に考慮されていないことを示しているが、これは最近の ACGIH TLV® で変化している。UFH の定義を複雑にしているのは、「ほぼすべての」労働者の割合が、これまでに発表された OEL の方法や派生 OEL で十分に文書化されていないことである。考慮すべき重要な点は、影響を受ける可能性のある下位集団の相対的な規模である。第二の考慮事項は、OEL で曝露された場合に、特定の固有の感受性を持つ亜集団で発生する可能性のある影響の重篤さである。重篤な反応の可能性がある場合は、OEL の適用範囲が有利になる。あるいは、影響の重篤度と、感受性の高い部分集団に関する残留不確実性は、修正因子(下記参照)を追加することで対応できる。
個体間変動のための 不確実性因子 は、動物またはヒトのデータから得られた PoD 値を調整するために使用される。ヒトデータの場合は、これが唯一の不確実性因子となる場合がある。化学物質に特化したデータがない場合( 19 )には、一般的には10と高い不確実性因子が使用される( 詳細は以下を参照)。UFAと同様に、UFHは2つのサブファクターで構成されており、1つは個人間のTKの違いを表すサブファクターであり、もう1つは特定の組織線量における感受性の違い(すなわちTDの違い)を表すサブファクターであると考えられている。UFAとは異なり、UFHのTKとTDのサブファクターは一般的に√10の数値、つまり約3.
( 17 ・19 , 31 ・34 ) UFHの科学的根拠についてレビューされている。 ( 17 ・19 , 31 ・34 ) TKサブファクタの√10は、人口のすべてのグループにとって適切ではない可能性があることが指摘されている。 ( 35 ) また、労働者は高齢者や若年者を含まず、生涯にわたって曝露されないため、一般集団よりも異質性が少ないと予想されるという理由から、全体のUFHは10未満がOELの設定には適切であるべきであるという議論もある( 36 , 37 ) 労働者集団の疫学研究では、一般的に、毒性物質への過剰な曝露がない場合には、労働者は一般集団よりも健康であることがわかっている。これは「健康な労働者効果」として知られており、職業疫学では十分に確立されている( 38 , 39 ) しかし、労働者集団には、喘息患者、アトピー患者、妊婦、高齢労働者、および平均的な人口よりも影響を受けやすいその他の人々も含まれている可能性がある。
遺伝的およびエピジェネティックな要因は、化学物質に対する反応の変動性の重要な要因となりうる。これは、医薬品の代謝の変動性という文脈でよく説明されている。また、主要な不確実性因子の1つがヒトの変動性に対処するために割り当てられているため、職業的化学物質曝露に対する同様の考慮への影響もOELの設定において重要な変数となっている。遺伝学とエピジェネティクスを系統的に考慮するアプローチについては、Schulteら( 40 )が詳細に論じている。
欧州化学物質庁は( 41 ) 労働者の個人間ばらつきに対処するために 5 の係数を用い、派生無影響レベル (DNELs) を設定する際には一般集団には 10 の係数を用いることを推奨している ( 表 2 を参照)。この区別の根拠は十分に文書化されていないが、後述する化学物質特異的調整因子(CSAF)に関する文献は、この二分法を支持しているようである。例えば、Naumannら( 42 )とSilvermanら( 43 )が分析した医薬品活性成分(API)のTKデータの再分析によると、高齢者や疾患を持つ集団のバイモーダルCSAFの平均比は、同じAPIの場合、健康な集団と比較して2.2倍高いことが示されている。同様の毒性力学が想定される場合、個人間変動に対するデフォルトの 不確実性因子 値 10 を労働者の場合は 2 倍に削減することが正当化されるようである。
労働者集団の感受性のばらつきを考慮してUFHのデフォルト値を10とすることが適切であるかどうかは科学的な疑問であり、明確な科学的根拠がない場合には、この点については組織によって方針が異なる可能性がある。これを決定する根拠は、研究対象の化学物質によって引き起こされる特定の影響に対する感受性の基礎となる 情報に依存している。UFHの選択には、以下のような考慮事項が含まれる。
- 感受性の基礎となる根拠は、労働者集団では一般集団よりも多かれ少なかれ多いか、少なかれ少ないか。
- 労働者集団が一般集団よりも重度の毒性影響を受けると仮定する根拠があるか?
LOAEL-NOAEL不確実性因子(UFL)
OELを導出するために使用された主要研究にLOAELが含まれているがNOAELが含まれていない場合、外挿のためのPoDとして使用するベンチマーク線量(BMD)を計算するのが好ましい手順である( 12 ) 。 ベンチマーク線量(信頼限界下限値)またはBMDLは、標準的な研究デザインでは通常NOAELに近似しており、NOAELと同様にPoDとして使用される。NOAELまたはBMDLがPoDとして使用される場合、外挿法の目的は副作用と関連しない濃度を推定することであるため、健康リスク評価における不確実性のこの領域には通常1の値が適用される( 14 , 41 )。しかし、いくつかのデータセットはベンチマーク線量の推定には不適 切な場合がある。OEL が LOAEL を基準にして外挿した場合には、線量反応曲線上で影響がないと予想される点を推定するために 不確実性因子(UFL)を追加で適用する必要がある。
適切な UFL の選択には多少の判断が必要である。Dourson and Stara( 17 )は、LOAEL:NOAEL比の経験的分析を行い、検討した症例の96%が10分の1以内に収まっていることを明らかにした。Naumann and Weideman( 18 ) は、多数の良質な毒性試験の分析に基づき、平均的な LOAEL:NOAEL 比は約 3 であることを指摘している( 44 ・46 )。これらの解析では、NOAELとLOAELの比率を解析するという制限があるが、これらは個々の研究の線量間隔によってあらかじめ定義されている。これは PoD 選択における固有の課題であり、BMD 法が一般的に好まれる理由である( 12 )。
デフォルト値以外の値を選択する際には、いくつかの考慮事項が関連している。異なる値を使用する最も一般的な根拠は、LOAELにおける影響の重大性である。さらに、いくつかの OEL 設定プロセスでは、最低観察影響レベル(LOEL)の使用を PoD の基礎としている。例えば、医薬品のばく露ガイドの設定では、最も感受性の高い影響は、しばしば薬理学的効果(これは患者に対 して意図された効果であることが多い)に基づいている。しかし、労働者にとっては、治療以外では意図されていない影響であるため、このような影響は PoD の候補となる。このように考えると、薬理学的効果は一般的に「有害」とみなされるが、臨床試験の文書ではLOAELではなくLOELとして言及されることが多い。臨界効果がLOAELと呼ばれるかLOELと呼ばれるかにかかわらず、UFL選択の重要な決定因子は同じである(効果の重症度および用量反応勾配)。Dourson and Stara, ( 17 ) Naumann and Weideman, ( 18 ) および Dourson ら ( 19 ) は、LOAEL における影響の重症度を UFL の選択に含めるべきであることに同意している。これは、脂肪肝のような毒性学的な重症度が最小の影響は LOAEL が NOAEL に近いことを示唆し、一方、肝壊死のような重症度の高い影響は LOAEL が NOAEL から離れていることを示唆しているからである。その他の考慮事項としては、反応発生率、用量反応曲線の傾き、及び MOA(予想される用量反応挙動)が挙げられる。残存する不確実性は、修正因子(下記参照)で対処することができる。
短期-長期不確実性因子(UFS)
OEL は、動物実験では通常、慢性的なバイオアッセイ(例えば、マウスやラットの場合は 2 )に相当する、全労働寿命に亘って曝露された労働者を保護することを意図している。PoD が亜慢性データに基づいている場合は、OEL が労働寿命を保護することを意図していることを考慮して、適切な慢性曝露データの不足を調整するために UFS が適用される。UFS のデフォルト値は、文献ではいくつかの議論の対象となっている。Dourson and Stara( 17 )は、10倍の係数を用いると、観察された亜慢性対慢性の影響レベルの比率と96%等しいか、それ以上になることを示す研究を引用して、10のデフォルト値を主張している。Naumann and Weideman(18 ) は、多数の高品質な毒性試験のレビューから、より長期の試験を実施した場合、より低い PoD が得られた可能性を考慮するには、通常 3 の係数で十分であることが示唆されていることを指摘し、UFS のデフォルト値を 3 とすることを提唱している( 47 ・52 ) Dourson ら(19 ) は、UFS を 10 とすることを「ゆるやかな上限推定値」とみなすという、より柔軟なアプローチを提唱している。
UFS の適切な値を評価するためには、試験期間を延長した場合に PoD の基礎となる臨界効果が発生率や重症度のいずれかで増加するか、あるいは低用量で発生すると予想されるかどうかを評価する必要がある。重大度の増加なしに、可逆的な急性効果が慢性的に発現する可能性がある。短期試験から長期試験への毒性の進行または進行の欠如、例えば2週間の試験と90日の試験を比較した場合のような、短期試験から長期試験への毒性の進行または進行の欠如は、UFSの評価に関連するデータを提供する可能性がある。MOAもまた、関連する情報を提供する可能性がある。MOAの完全な評価は、その用量が長期の曝露によって蓄積される可能性が高いかどうか(すなわち、TKを考慮した場合)及び影響が長期の曝露によって蓄積し、より重篤になるかどうか(すなわち、TDを考慮した場合)に基づいている。例えば、反応性代謝物(体内に蓄積しない)を介して損傷を生じ、経時的な損傷の進行の証拠を示さない化学物質は、UFS を低減する価値があるかもしれない。感覚刺激性影響は、一般的に暴露期間が長くなると進行するとは考えられず、これらの化学物質の OEL は UFS を 1 とすることが多い。 典型的な 3 ヶ月の亜慢性試験よりも長く、慢性試験よりも短い期間(例えば、6 ヶ月または 1 年の試験)で試験された化学物質も、UFS < 10 とすることができる。特定の化学物質のUFSの選択は、利用可能なデータの質と化学物質のMOAの両方を考慮しなければならない。
データベースの不備(不完全なデータ) 不確実性因子(UFD)
全体的な毒性データベースが不完全であり、データのギャップが大きい場合には、未研究の毒性エンドポイントに対 してより低いPoDが同定される可能性があるため、追加の不確実性因子が必要となる場合がある。このような考慮事項は、データが 1 種のみから得られる場合や、発生・生殖毒性試験がまだ実施されていな い場合にしばしば生じる。すべての OEL 設定機関が明示的な UFD を含んでいるわけではないが、この係数は、追加試験が実施された後に、より低い PoD が発見される可能性を考慮することを意図したものである。Dourson ら( 53 ) は農薬の慢性毒性データをレビューし、適切なデータベースはラットとイヌを対象とした 2 年間の研究と、ラットを対象とした生殖・発達に関する研究で構成されると結論付けている。OEL設定の目的で犬の2年間の試験データを持っているのは珍しく、マウスやラットでの2年間の試験の方が一般的である。利用可能なデータによると、2種の長期試験と生殖・発達試験が不足しているデータセットに基づいてOELを設定する場合には、データベースの不備に対して3-10のUFDが必要であることが示唆されている( 19 )。
UFDを適用するかどうかの決定は、問題となっている化学物質の特定の種類のデータを考慮し、追加の研究で追加の毒性が明らかになる可能性を判断することに基づ くべきである。場合によっては、実施されていない特別な試験デザインでしか確実に試験できない影響の可能性を既存のデータが示唆していることもある。例えば、神経学的影響や免疫系への影響に関連する懸念が標準的な試験デザインから示された場合、特別な機能的試験や終末期に特化した試験の必要性を示唆しているかもしれない。もし実施されていない場合は、そのようなデータのギャップを利用して、より大規模な UFD を支持することが多い。信頼性の高い暴露測定値がないためにOELを確立するには不十分であるが、化学物質に関連する危険性に光を当てることができるかもしれないヒト研究の利点がOELの設定にはあることは珍しくない。例えば、動物を対象とした生殖・発達研究を欠いたデータセットは、利用可能なヒトデータが潜在的な生殖危険性を示唆している場合には不十分であると考えられるが、ヒトデータが生殖・発達毒性の懸念を排除するのに十分である場合には適切(UFD = 1)であると考えられる。
OELの設定における共通のデータギャップは、吸入経路での曝露による毒性データがないことである;多くのOELは経口投与試験に基づいて導出されている。これは、経口投与試験に基づいて作成された多くのOELが、経口投与試験に基づいて作成されていることを反映している。経路から経路への外挿が生物学的に正当化できる状況を支える科学的原則がある( 54 ) が、そのような経路から経路への外挿によって生じる不確実性を検討する必要がある。一般的な考慮事項には、観察された全身毒性効果がどの程度のものであれば、侵入経路の影響よりも敏感になる可能性が高いかということが含まれる。これは、現在の工業用化学物質の OEL のエンドポイントとして非常に一般的なのが気道刺激性であるため、大きな懸念材料である( 55 ) 。経路依存性のバイオアベイラビリティの調整の必要性も検討されている。この考慮のための調整は、投与量の調整を適用したり、OEL 式の吸収係数を使用したりすることで対応できる場合もある( 5 , 13 , 56 )。あるいは、バイオアベイラビリティに関する残留不確実性は、修飾因子を用いて対処することができる。
複合不確実性因子(UFC)について
使用されている代表的なデフォルトの値は、組織によって異なる。一般住民を保護するために米国で環境基準を策定している組織(例:EPA 基準線量[RfDs]、有害物質・疾病登録庁[ATSDR]最小リスクレベル[MRL]など この場合、不確実性因子調整に使用される最小増分値は、その精度を反映させるため、log10単位の2分の1(3.16を3に四捨五入)であることに注意が必要である。多くの欧州機関では、不確実性の全領域を考慮して10の値を使用しているが、計算では2と5の中間値を使用する傾向がある。場合によっては、特定のデータを外挿するために別のデフォルト値が設定されていることもある(例えば、EUの化学物質登録要件における派生無影響レベル[DNEL]に使用される評価係数など)。
様々な不確実性因子の数値が決定された後、それらの数値を乗算して全体の不確実性因子(UFC)を算出する。例えば、デフォルト値のUFAは4,UFHは10とすると、UFCは40となり、これを上述のようにPoDに適用する。デフォルトの不確実性因子の説明では3.16の代わりに3を使用しているが、3つの不確実性因子を掛け合わせる場合は注意が必要である。例えば、2つの不確実性因子を3つ掛け合わせた場合、それぞれの係数が半対数の調整値(例:3.16×3.16)となり、積は9ではなく10となる。これは3つの不確実性因子を3つ掛け合わせた場合にも示されている。
UFA、UFH、UFS、およびUFLのデフォルト値を仮定すると、UFCの数値は非常に大きくなる可能性がある。様々な不確実性因子が互いに独立している場合には、この乗算的なアプローチでUFCを設定するのが正しいのであるが、様々な不確実性因子が完全に独立しているわけではなく、デフォルトのファクタを10倍にするだけでは、いくつかの不確実性の原因を二重にカウントしてしまう可能性があるという議論があった。推定されるダブルカウントを調整するために 不確実性因子 の一部を削減することが提案され( 57 )、Swartout ら( 58 ) によって実証的に検証されている。すなわち、UFA、UFH、UFS、及び UFL はすべて 10 の値が割り当てられている)。) さらに、5 つの完全な不確実性領域が存在する場合には、十分な信頼性を持って曝露限界値を導出するのに十分なデータが得られない可能性が高い。
不確実性因子 の組み合わせを定義するための確率論的アプローチも提案されている( 58 ・60 ) 。最近では、長谷川ら( 61 ) が、経験的に得られた不確実性因子の確率的な組み合わせに基づいて、デフォルト不確実性因子の代替的なセットを提案している。この代替不確実性因子は、通常の10倍のデフォルト不確実性因子よりも大きい場合もあれば、10倍以下の場合もある。これらの確率的な不確実性因子の組み合わせは、現在のところ規制当局に広く受け入れられているとは言えないが、UFC全体を確立するための既存の慣行を改善するための枠組みを提供する可能性がある。職業リスクの解釈における確率論的不確実性因子の影響については、Watersら( 62 ) が詳述している。
不確実性因子アプリケーションでOELを算出する際の文書の性質やレベルは、OELを発行している組織によって大きく異なる。主要な機関が発行しているTLV®、職場環境曝露レベル(WEELs)、EUの職業曝露限界に関する科学委員会(SCOEL)が発行している値のOEL文書には、考慮すべき点や不確実性を考慮したOELの根拠が記載されている。OEL の導出に用いた個々の 不確実性因子 や値については、多くの場合、合成値が記載されているが、明示的な記述は行われていない。対照的に、ほとんどの政府機関によって設定されている環境または緊急空気中限度(例えば、EPA基準濃度[RfC]、急性緊急ガイドラインレベル[AEGL]、米国の州機関によって導出された限度、および職業シナリオを含むEUのDNEL値など)のようなリスク値は、文書化された不確実性因子のアプローチを持っており、与えられた値を導出するために適用される値は通常列挙されている。複合不確実性因子を計算し、特定のデフォルト構成要素のサブファクタを列挙する各アプローチには長所と限界があり( 表Ⅲ) 、ハイブリッドアプローチも提案されている( 63 ) が、全体的な傾向としては、OELの理論的根拠の中で不確実性因子の選択について(少なくとも定性的には)文書化が増加している。
表3 代替的な不確実性因子ドキュメンテーションアプローチのメリットと限界
| 因子の適用と乗算のアプローチ |
| 説明:特定のデフォルト値が、事前に選択された不確実な領域に割り当てられます。複合UFは、評価される特定のデータセットに関連するデフォルト値の積として計算されます。結果として得られる複合UFを変更するためのルールは、重複する不確実性に対処するために指定できます。 |
| 利点: |
| •OEL計算の透明性は、OELとその不確実性を解釈するユーザーの能力を向上させ、労働者のリスクコミュニケーションをサポートします |
| •さまざまな不確実性がOELに与える相対的な影響は明らかであり、不確実性を軽減するために新しいデータを収集することの価値または影響を判断できます。 |
| 短所: |
| •デフォルト値の厳密な適用は、専門家の科学的判断の使用を通じて提供される価値を制限します |
| •デフォルト値を乗算すると、データセットの全体と一致しない複合UFが生成される可能性があり、事前に割り当てられたデフォルトからの逸脱を説明する際に、多くの場合、多大な労力と潜在的なユーザーの混乱が必要になります。 |
| エビデンスアプローチの不確実性の重み |
| 説明:不確実性の領域は統合されたアプローチで考慮され、特に潜在的な重複する考慮事項と、すべての証拠からのデータのバランスをとるときに導き出される最適な保護複合UFに焦点が当てられます。 |
| 利点: |
| •証拠の重みアプローチを使用して、利用可能なデータのすべての側面を考慮に入れた複合UFを導出する際の柔軟性が向上します。 |
| •デフォルトのUF値の誤用または不確実性の重複領域に起因する可能性がある、適切でないOELを設定する際の落とし穴を回避します。 |
| 短所: |
| •特定のデフォルトがないため、OELの基礎となる透明性が制限され、その結果、ユーザーのコミュニケーションとデータ収集が制限されます。 |
| •アプローチは規範的ではないため、OEL開発に関する高度な科学的専門知識が必要です。 |
トキシコキネティック調整因子
投与量モデルを使用して PoD を修正する代わりに( 13 )、OEL 式の分母を修正する追加的な調整があり、これは一部の組織が特定の毒物動態の考慮事項を反映するために使用している。例えば、ECHA は、労働者曝露シナリオのための投与経路や曝露経路の違いを考慮して PoD を修正するための事前定義の評価係数を有している( 41 ) 他にも、一部の組織(特に製薬部門)が適用する 2 つの一般的な調整は、経路固有のバイオアベイラビリティと定常状態の内部投与条件に対処するための外挿法を反映している( 5 ) 特定のケースでは、経路間の外挿法が適切であるかもしれない。経口)で実施された研究から OEL を導出しようとする場合には、経路間外挿が適切であるかもしれない。通常、関連する投与経路を用いた直接試験が期待されるが、特定の状況での適切な保護を確保するためには、追加の調整因子(例えば、バイオアベイラビリティ補正因子)を用いた外挿が有用であろう。
Naumann and Weideman(18)及びNaumannら(56)は、バイオアベイラビリティ補正係数の使用の背景と、OEL開発のためにバイオアベイラビリティ補正係数をいつ、どのように適用すべきかの指針を提供している。検証された TK モデルやリスク評価で既定値の使用が必要な場合を除き、バイオアベイラビリティの調整に最も一般的に採用されている 技術的アプローチは、ルート固有のバイオアベイラビリティデータの比率を反映したものである( 5 , 64 ) 調整係数を OEL 式の分母に入れると、次のように計算できる。

例えば、全身のバイオアベイラビリティーが 10%で吸入経路によるバイオアベイラビリティーが 100%の経口投与試験で得られた臨界効果に基づいて OEL が導出された場合、結果として得られるバイオアベイラビリティー調整係数は 1.0/0.1 または 10 の係数となる。したがって、この調整は、全身投与量ベースでの経口投与量(PoD)に対する吸入換算値の推定値として機能し、すなわち、OELはこの係数によって低下する。
実際には、このようなバイオアベイラビリティーの調整は、ルート固有のバイオアベイラビリティーデータがない場合に行われなければならない単純化された前提条件に基づ いて、多くの場合、重大な制限がある。このような因子の適用に対するいくつかの制限事項には、以下が含まれる。
- この調整は、入口ポータルでの影響に基づく OEL には適用されない-このような場合、ルート間の外挿は推奨されない。
- 調整は全身のバイオアベイラビリティーの信頼できる推定値に依存している。全身線量の代用となるもの(例えば、浸透率)は、局所代謝や肝性一次代謝などの他の毒物動態特性を考慮に入れていないため、全身線量の適切な測定基準とはならない。
- 毒性を引き起こす化学物質の形態(例えば、親または代謝物)が不明な場合、親化合物に基づくバイオアベイラビリティの調整は、毒性の強さの実際の経路特異的な違いを反映していない可能性がある。このような考慮は、経口投与後に大きな肝一次代謝を受ける化学物質に共通している。
- 吸入が化学物質の消費者や環境への曝露が懸念される主な曝露経路でない限り、吸入後の TK データは利用できない可能性が高い。したがって、調整は PoD となった重要試験の投与経路の経験的なバイオアベイラビリティの推定値に基づいて行われるかもしれないが、吸入(OEL の対象経路)のバイオアベイラビリティを推定しなければならない。この限界に対処するための一つの方法として、予防的な仮定として吸入バイオアベイラビリティ(ほとんどの低分子有機分子)を 100%と仮定するか、あるいは分配係数などの特性に基づいて値を推定することがある。
- 大きな分子(例えば、タンパク質治療薬)の吸入バイオアベイラビリティーを推定するには、分子量、上皮輸送を促進する特定の受容体の存在、粘膜クリアランスや嚥下後の消化管からのバイオアベイラビリティーなどの要因を考慮する必要があり、さらに複雑さが増す。
繰り返し曝露による生物蓄積の可能性があるため、OELを調整するためには追加の要因が必要となる場合がある。排泄半減期が長い化学物質の場合、血漿中濃度は定常状態に達するまで繰り返し曝露することで上昇する。短期間の研究から得られた NOAEL を用いて設定された OEL は、短期曝露後の血漿中濃度(PoD の特定に用いた研究に相当する期間)と長期曝露後の定常状態における予想血漿中濃度の比に対応する係数で下方に調整する必要がある。この調整は、単回投与又は短期間の臨床試験が利用可能な場合が多い医薬品の OEL を設定する際に特に有用である。動物毒性試験から導き出された OEL は、通常、OEL が導き出される前に定常状態の動態が適用される反復投与試験が必要である。維持用量での定常状態が達成されるような十分な期間の試験を用いて OEL が確立された場合には、このような条件下では蓄積は既に考慮されているため、このような生物蓄積の調整は必要ではない。
修正因子(MF)
この因子は、上記の不確実性因子では対応できない不確実性を調整するものであり、特に複数のレビュアーがいる場合には、科学的判断を明示的に取り入れることが可能となる。また、他の因子でカバーされていない残留不確実性に対処する必要がある場合には、修正因子を考慮することもできる。この因子はまた、データベースの全体的な質やヒトのリスク評価に対する利用可能な研究の関連性に対 して科学的判断を適用することを可能にする。このような場合には、1~10未満の追加係数を使用してもよい( 19 ) 。 修正係数(MF)を明示的に組み込むことで、意思決定プロセスの透明性を高め、最終的な OEL につながる可能性がある。しかし、現在の EPA の指針は、この因子の特定の使用を見送り、この因子が扱う不確実性を UFD のような別の因子の中に組み込むことである( 22 )。
修正要素は、他の要素では明確に、または十分に対応できない状況をカバーするために、査読者が必要と判断した場合に、さらなる調整を行うために使用することができる。MF を適用する際によく引用される考慮事項には、以下のようなものがある。
- 臨界効果の用量反応曲線の傾き。
- 臨界効果の選択。
- 効果の重症度。
- 経路間外挿。
- 影響を受けやすい亜集団の同定。
- 臨界効果の臨床的意義。
- 臨界効果の可逆性。
- データベースの全体的な質。
- 重大な影響の労働者への関連性。
- 関連する化学物質との類似性または相違。
- 個々の不確実性因子間の独立性の欠如。
OEL設定における化学物質固有の調整因子(CSAFs)
デフォルトの不確かさ因子は、定義上、がない場合にのみ使用されるべきである。化学物質特異的調整係数(CSAFs)は、Renwick(65 ・67 )によって提案され、世界保健機関/国際化学安全計画(WHO/International Programme on Chemical Safety)によって採用されたスキームに従って、TKとTDのデータが利用可能な場合にデフォルト係数を置き換えることを意図している( 21 , 68 )。
CSAF は、十分な化学物質固有のデータが入手可能な場合には、デフォルトの不確実性因子に代えて、安全な曝露レベルを設定するために使用することができる。Renwick スキームは、1 日の許容摂取量、許容摂取量、基準用量/濃度、作業暴露限度など、規制や内部の健康に基づく限度を導出する際に、化学物質固有の TK および TD データを組み込むための枠組みを提供している。Renwick( 67 ) は、化学物質に関連するデータを使用する際に考慮すべき点として、化学物質自体や代謝物が活性種であるかどうか、TK または TD データと臨界エンドポイントとの関連性、ヒト集団の代表的なデータであるかどうかなどを挙げている。Meek er al)。 ( 69 ) はまた、十分な化学物質固有のデータが利用可能な場合に、デフォルトの不確かさ因子の代わりにデータ由来の調整値を使用するガイドラインを提案している。
不確かさと変動性の区別は強調されるべきである。CSAF は、目的とする母集団の関連するサブセットにおける TK と TD の「変動性」を特徴づけるために使用される。このサブセットが母集団全体の代表であり、相違点(または類似点)に関する定量的な情報を 提供する限り、「不確実性」のレベルは大幅に低減されるべきである。リスク評価者/リスク管理者は、自分たちが導き出した健康に基づく限界値が、最も影響を受けやすい人であっても十分な保護を提供することに、より確信を持つべきである。残存する不確実性があるかもしれないが、潜在的に重要な差異に関するデータがない場合に比べれば明らかに少なくなるだろう。潜在的に影響を受けやすい集団のTKおよびTDデータに焦点を当てることで、リスク評価者は保護を最も必要とする集団のセグメントのデータを意識的に評価する。
CSAFスキームでは、評価された化学物質の全身暴露と薬理活性を示すいくつかのTKおよびTDパラメータを用いて個人差を評価している。内部被ばく量の指標として最初に選択されたTKパラメータは、ピーク血漿中濃度(Cmax)時間別血中濃度曲線下面積(AUC)定常状態血漿中濃度(SS)および排泄率またはクリアランス率であった。最初の2つ、CmaxとAUCは、クリアランス率もCSAF法では一般的に使用される指標であるが、血中の化学物質の量を直接測定するものであるため、体への負担と全身被曝の最良の指標と考えられている。
TKおよびTDデータを評価するための一般的なガイドライン( 21 , 69 )には、CSAFを選択するためのいくつかの重要な考慮事項が記載されている。TKの個人差を評価するためには、(1)使用するTKパラメータは臨界効果に直接関連するものでなければならない(例:AUC vs. Cmax)(2)データは推奨される健康基準の限界に最も関連する用量と経路で作成されなければならない、(3)ヒトを対象としたデータは、感受性の高い小集団を含め、保護対象となる集団(労働者、この場合は18~65歳)の予想される変動を代表するものでなければならない。TDの個人差を評価するためには、(1)測定されたエンドポイントが推奨曝露限度の導出に用いられた臨界効果に直接関連していなければならず、(2)データには、平均的なヒトと感受性の高いヒトの同程度の反応レベルの組織における反応の定量的比較が含まれていなければならず、(3)個人間変動を定義するのに十分な数の個体が含まれていなければならない。WHO/IPCSのガイダンス文書 ( 21 , 68 ) には、4つのサブファクターすべてについてCSAFを導出する方法の例が記載されている。
個人間差を推定してCSAFを導出する方法は、関心のあるTKまたはTDパラメータの中心傾向に対する分布の末尾の比率に依存している。このアプローチは、ある部分集団(例えば、分布の尾部)が十分に異なる(すなわち、与えられた線量に対して有意に高いCmaxまたはAUC値に基づいてより感受性が高い)場合には、それらの被曝レベルを正常な(平均的な)健康な個人に適合するように下方に調整する必要があるという前提に基づいている。2つ以上の異なる部分集団が存在する場合、最も感受性の高い部分集団の上端の健康な集団の平均値に対する比率を用いて、適切な調整係数を導き出する。これは、図2(変換された単一モーダル分布)と図3(変換された二峰性分布)に図示されている。
図2 単峰分布からの化学物質特異的調整係数(CSAF)の導出( 73 )

© Taylor & Francis. Taylor & Francisの許可を得て転載。再利用には権利者から許可を得る必要がある。
図3 バイモーダル分布からの化学物質特異的調整係数(CSAF)の導出( 73 )
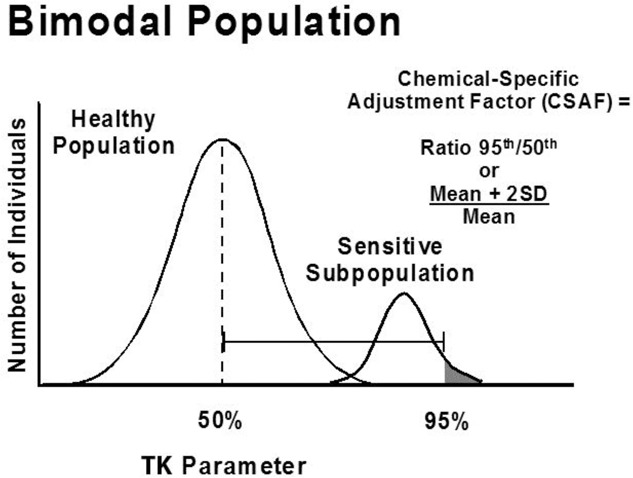
© Taylor & Francis. Taylor & Francisの許可を得て転載。再利用の許可は権利者から得なければならない。
実際には、個人差の評価は、通常、TKおよび/またはTDパラメータの要約統計量(平均や標準偏差など)のみを提示した論文に依存している。CSAFは、平均に2つの標準偏差を加えたものを平均(平均+2SD)/平均で割って計算される。) 時々、標準誤差は、前者に√Nを乗じて標準偏差に変換する必要がある。
この事例研究は、非選択的βアドレナリン遮断薬であるマレイン酸チモロールを対象としており、OELを設定する際にこの潜在的な感受性を考慮に入れるために、2つの異なる表現型(すなわち、代謝不良者と広範な代謝者)を持つCYP2D6による酸化的代謝の多型をどのように評価したかを示している( 70 )。代謝不良者の有病率(選択されたサブ集団の最大9%)は、マレイン酸チモロールのOELを確立する際に、この潜在的な感受性を慎重に考慮することを示すのに十分な高さであった。図 3 に示すように、代謝不良者の平均 AUC 値より 2 つ上の標準偏差に対応する値を、広範な代謝物の平均 AUC (MeanPoor + 2SD)/MeanExt) で除算することにより、この二峰性分布の速度論に対する化学物質特異的調整因子 (CSAF) 9.8 が計算された。ダイナミクスの CSAF 1.2 と組み合わせると、これは、感度における人間のばらつきに対処するために 12 の複合 CSAF を生成する。CSAFは臨床的に有意な心血管系への影響を外挿した無影響レベル(経口バイオアベイラビリティの補正を含む)に適用され、代謝の悪い人を含むほぼすべての労働者を保護すると予想されるマレイン酸チモールの職業暴露限度(OEL)が設定された。
CSAF を使用したからといって、健康ベースの限界値を設定する際に使用される「安全係数」が自動的に低下するわけではないことに注意することが重要である。ある化学物質の利用可能なデータから、個人間のばらつきが大きいことが示唆されることがある。上記の例では、CSAFH-TKと毒性力学(CSAFH-TD)のデフォルト値3.2を組み合わせた複合不確かさ係数は31であり、これはデフォルト値10よりも3倍高いことに注意してほしい。曝露限界値の設定の文脈でCSAFアプローチを適用するための全体的なプロセスは、図4に示されている。
図4 曝露限界値設定のための不確実性因子を追加したCSAFアプローチの適用。
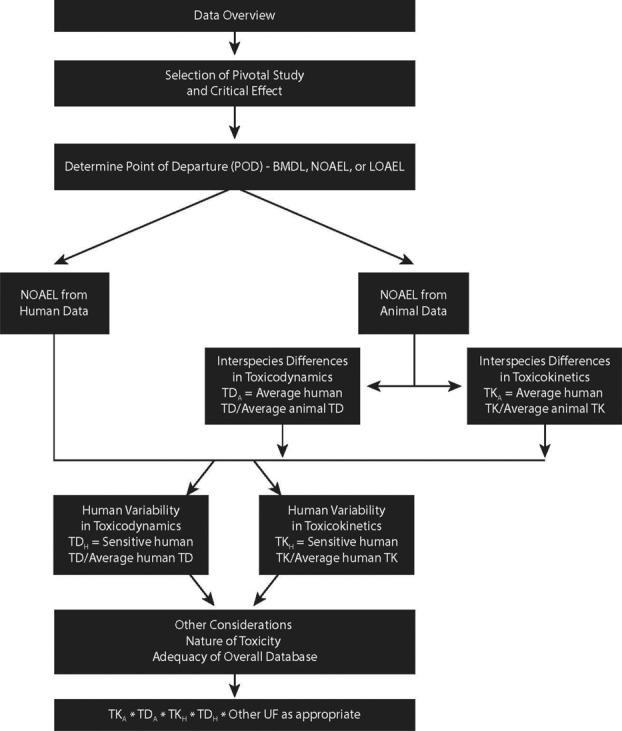
WHO/IPCS (2005)(21)からの引用。
結論
OELの導出における不確実性因子の適用は、ここ数十年で大きく変化してきている。元々は専門家の判断に基づく恣意的な安全係数と考えられていた不確実性因子の適用は、科学的根拠に基づくデフォルト値( 17 , 18 , 31 , 71 )や、最近では化学物質固有の値の開発( 21 , 42 , 43 , 70 , 72 )など、科学的根拠への依存度が高まってきている。このように、不確実性因子アプローチには好ましい階層が存在する(図5)。このような傾向があるにもかかわらず、多くの工業薬品ではCSAF計算をサポートするための詳細なTKデータが入手できない場合がある。
図5 不確実性に対処するためのアプローチの階層構造と、科学的確実性の向上と、リスク評価プロセスに化学物質や種に固有のデータを組み込むための要件の増加との対応。

本論文では、最も一般的に使用されている不確実性因子(動物からヒトへの外挿、個体内変動、短期暴露から長期暴露への外挿、LOAELからNOAELへの外挿、不完全なデータベースの調整のための不確実性因子)の科学的根拠を概説する。OELの設定過程では科学的判断の適用を避けることはできないため、そのような判断はオープンで透明性のあるものでなければならず、不確実性の重要な領域を体系的に評価し、利用可能な場合には化学物質固有のデータを取り入れ、OELで使用される最終決定の根拠を明確に文書化しなければならない。不確実性因子応用の科学的進歩は継続している。不確実性因子申請の科学的発展における進歩には、以下のようなものがある。
- 透明性への期待の高まりと、適用された定量値を含めた不確実性因子選択の根拠の説明。
- ツールの改良、データへのアクセスの向上、手法の理解度の向上により、よりロバストな手法(CSAFやバイオアベイラビリティ補正係数など)の適用や利用が可能になったこと。
- 感度におけるヒトの変動性の基礎(例えば、遺伝学やエピジェネティクス)を理解し、OEL の設定におい てより完全に考慮し、完全にデータに基づいた OEL の導出方法に移行することを目標とする。
- 毒性学の進歩を応用し、不確実性因子値を定量的に精緻化するための計算毒性学的アプローチを含めて、毒性学の進歩を応用する。
