The emerging plasticity of SARS-CoV-2
science.sciencemag.org/content/371/6536/1306.full
Kevin D. McCormick, Jana L. Jacobs, John W. Mellors
サイエンス 2021年3月26日
SARS-CoV-2の変異体のスパイクタンパク質(緑)の変異(赤)が、宿主の受容体(薄灰色)や抗体(濃灰色)の結合に影響を与えると、免疫力が低下する可能性がある。
ウイルスは、突然変異(誤取り込み、挿入・欠失、組み換え)と、ウイルスの複製、感染、宿主の防御の回避など、より効率的な形質を求める自然選択の結果として進化する。新たに選択された形質は、予測できない方法で結びついている可能性があり、ウイルスの拡散と進化により、病原性(病気の重さ)が増すことが懸念される。2020年に報告された重症急性呼吸器症候群新型コロナウイルス(SARS-CoV-2)の限られた多様性は,非構造タンパク質14(nsp14)の3′-5′エキソヌクレアーゼ校正機能に起因すると考えられ,宿主細胞への侵入を媒介するウイルススパイク(S)タンパク質の単一配列に基づくワクチンは,循環するすべての変異体に対する免疫防御を生成する可能性が高いと考えられた(1).しかし、Sに変異を持つSARS-CoV-2の亜種が世界中で出現しており、ワクチンや抗体ベースの治療法の課題となっている。SARS-CoV-2が継続的に拡散していることで、Sやウイルスゲノム全体に、結果的にさらなる変異が蓄積される機会が生まれている。
SARS-CoV-2は 2002年から 2004年にかけて発生したSARSの原因となったSARS-CoVと高い配列相同性を有しているが、コロナウイルスファミリーは、配列と宿主の受容体への嗜好性の両方において多様である。例えば、SARS-CoV-2と「風邪」のヒトコロナウイルスであるHCOV-NL63は、ともにアンジオテンシン変換酵素2(ACE2)を宿主細胞の受容体として認識するが、SARS-CoV-2とHCOV-NL63は異なるコロナウイルス属に属しており、Sの受容体結合ドメイン(RBD)の配列と構造に大きな違いがあり、30%以下の配列相同性しかない(2)。このようなSの多様性は、コロナウイルスが、機能を大きく損なうことなく、配列と構造の両方の変化を許容する幅広い可能性を持っていることを示している。このことは、コロナウイルスが人獣共通感染症を引き起こす理由の一部を説明するものであり、SARS-CoV-2の進化の可能性がまだ完全には解明されていないことを示唆している。
Sタンパク質は、2つのサブユニットから構成されている。Sタンパク質は、RBDを含むS1と、ウイルスと宿主細胞の融合を媒介するS2の2つのサブユニットから構成されている。抗体を中和するエピトープは、Sタンパク質全体に散在しているが、ほとんどがRBDに集中している。可塑性の可能性があるにもかかわらず、1億人以上に約1年間(2019年12月から)広がった後、SARS-CoV-2のSの進化の証拠は限られていた。唯一の注目すべき進化事象は、S1のD614G(Asp614→Gly)置換で、これはACE2親和性を高め、感染力と伝達力の向上につながった。公共のデータベースに登録されているウイルスの配列は、ほとんどが、主要な免疫反応が起こる前の急性感染時に上気道から得られたものである。このような配列では、ウイルスの多様化に対する宿主内の免疫選択の影響を捉えていない可能性がある。
SARS-CoV-2の宿主内での広範な進化は、血液悪性腫瘍の治療や自己免疫のために免疫機能が低下し、感染が長期化した少なくとも5人の患者で報告されている(3-7)。これらの患者は、SARS-CoV-2に平均115日間感染した後、感染が解除されるか、COVID-19に感染した。また、各患者は、少なくとも1回の回復期血漿(CP)療法(COVID-19から回復したドナーからの血漿を静脈内に輸血すること)および/またはモノクローナル抗体療法を受けてた。これらの人の中には、退院時や死亡前にSARS-CoV-2を高力価で排出していた人もおり、感染の可能性を示している。これらの患者のうち2人から得られたSARS-CoV-2の変異体は、CPに対する中和感受性が最大で5倍に低下していた(3, 7)。これらは免疫不全者でのケーススタディであるが、5人の感染者のうち4人にS1のアミノ酸69〜70(Δ69〜70)Δ141〜144,Δ242〜248の欠失が認められたことから、懸念されている(3, 5〜7)。N501T(Asn501→Thr)またはN501Y(Asn501→Tyr)の変異が5つのうち2つの感染症で見られ(5, 6)1つの感染症のRBDにあるE484K(Glu484→Lys)およびQ493K(Gln493→Lys)の変異は、試験管内試験での選択後、抗体耐性ウイルスでも生じた。
これらの報告に先立ち、B.1.1.7,B.1.351,P.1の3つの主要な流通変異体が検出された。これらの変異体はいずれも、RBDのACE2インターフェースにE484K、N501Y、K417N(Lys417→Asn)など、少なくとも8つの単一の非同義のヌクレオチド変化を含んでいる(図参照)。また、B.1.1.7およびB.1.351のS1のアミノ(N)末端ドメイン(NTD)にも様々な欠失がある(図参照)。これらの変異体に含まれる変異のほとんどは、K417N、E484K、N501Yなど、パンデミックの最初の年にSARS-CoV-2のごく一部の配列で観察されたものであるが、これらの変異体が宿主間感染時に各置換基が順次追加されてできたものであることを示唆する証拠はない。
2020年の大半の期間、SARS-CoV-2の変異はわずかしか流通していなかったため、3つの主要な変異体は、長期にわたる個人感染とその後の感染の間にウイルスが選択圧を受けて適応した結果であると考えられる。宿主内でSARS-CoV-2が広範囲に進化した個人の症例報告はすべて、最適ではない中和抗体による治療を受けていたことを示していた(つまり、CP治療ではウイルス集団全体を中和できなかったのである)。抗体治療の効果があったかどうかにかかわらず、宿主内での選択とそれに続く感染の結果として、同じ変異体や新しい変異を含む変異体が異なる地域で出現し続ける可能性が高いと考えられる。実際、S1に複数の変異を持つ他の変種も報告されており、他の変種とは異なるRBDの置換を含むB.1.526(ニューヨークで検出)とB.1.429(カリフォルニアで発生)の系統や、ナイジェリアとウガンダでそれぞれ発生したと考えられているB.1.525とA.23.1などがある(8)(図参照)。
S1の変異の個々の表現型への影響はまだ完全には解明されていないが、いくつかの初期の手がかりが得られつつある。Asn501位をThrまたはPheに置換すると、ACE2との結合親和性が高まり(9)、Tyr501はマウスモデルでの感染力と病原性を高める(10)。流通している変異体の中には、RBDに直接結合する中和抗体に対する感度が低下しているものがあるかもしれない(ACE2結合界面にあるRBDの重要なアミノ酸が3回置換していることに起因する。RBDに直接結合する抗体(ACE2との結合界面にあるRBDの主要アミノ酸であるLys417,Glu484,Asn501の3つの置換に起因)やNTDに結合する抗体(ACE2との結合にはNTDの構造変化が必要)の感度が低下する可能性がある。ウイルスの遺伝子型と表現型を相関させるためのさらなる研究が必要である。
E484Kのように中和抗体の結合力を低下させる変異は、N501Yのように感染力を回復させる代償変異を必要とする可能性がある。2つの異なる系統(B.1.351とP.1)で進化したトリプルRBD変異(Lys417,Glu484,Asn501)などの変異には、収束的な関連性があると思われる。さらに、E484Kは最近、B.1.1.7系統でN501Yとともに検出された(11)。S1のΔ69-70はSARS-CoV-2シュードウイルスの感染力を2倍にしたが、これはウイルスの体力を犠牲にして抗体中和感受性を低下させたD796H(Asp796→His)という変異を補うために欠失が必要であったことを示唆している(7)。代償性変異の役割は、E484K(抗体感受性の低下)とΔ69-70(感染力の代償的増加)の両方を持つB.1.525系統の出現によっても裏付けられている。
スパイクタンパク質の変異と欠失
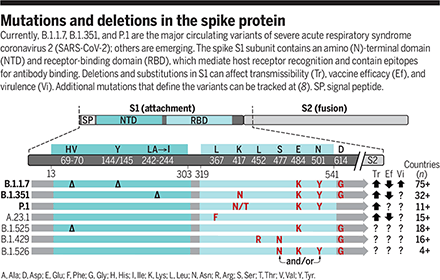
現在、重症急性呼吸器症候群新型コロナウイルス(SARS-CoV-2)には、B.1.1.7,B.1.351,P.1が主な流通変異体として存在しているが、その他の変異体も出現している。スパイクS1サブユニットには、アミノ(N)末端ドメイン(NTD)と受容体結合ドメイン(RBD)があり、これらは宿主の受容体認識を仲介し、抗体結合用のエピトープを含んでいる。S1の欠失や置換は、伝達性(Tr)、ワクチン効果(Ef)、病原性(Vi)に影響を与える。変異体を定義する追加の変異は、(8)で追跡できる。SP、シグナルペプチド。
SARS-CoV-2の変異体に見られる複雑な変異パターンが、同じウイルスゲノム上でつながっているのか、あるいは同じ患者の中で異なる変異体が混在しているのかは、まだわかっていない。個々の変異体の感染性や表現型を正確に評価するためには,HIV-1などのウイルスの遺伝的多様性を明らかにするために用いられているように,単一ゲノム増幅および配列決定を用いて,個々のSARS-CoV-2ゲノムにおけるこれらの変異のつながりを評価する研究が必要である.SARS-CoV-2の宿主内進化の事例報告では、SARS-CoV-2が同一個体内で複数の異なる系統を進化させることが示されている(6)。
いくつかの研究では、循環している主要な変異体は、最近ワクチンを接種した人のCPや血漿に対する中和感受性が低下していることが示唆されている。例えば,B.1系統(D614Gを含むSARS-CoV-2)に感染した人のCPは,B.1.351系統の生ウイルス分離株に対する中和活性がさまざまに低下していた。さらに、ワクチンによって誘発された抗体は、P.1およびB.1.351系統のS1のトリプル変異(K417N、E484K、N501Y)を含むシュードウイルスの中和活性を低下させた(12)。B.1.1.7系統に見られる欠失や変異を持つシュードウイルスも中和感受性の低下を示したが,BNT162b2(Pfizer/BioNTech)を接種した40人の血清中のB.1.1.7を完全に中和するのに十分な抗体価が得られた(13).S1(NTDとRBD)とS2に非同義の変異があるものを含め、急速に普及している新興の変種について、CPとワクチン接種後の血清による中和に対する表現型を継続的に評価し、ワクチンの有効性への影響の可能性をモニタリングすることは、最優先事項である。
単一のS配列に由来するSARS-CoV-2ワクチンの第3相試験では、D614G変異を含むSARS-CoV-2の初期亜種の感染予防に高い効果があることが示されている(14,15)。さらに最近のデータでは、特定のワクチンはB.1.351変異体に対する防御力が低いことが示唆されているが、さらなる研究が必要である。新しい変異体に対する抗体感作性の低下を示す研究は、本質的にワクチンの効果が低いことを証明するものではない。中和抗体を産生するエフェクターB細胞に加えて、自然免疫系と適応免疫系には、感染を防御したり、ウイルスの免疫逃避を促進したりする、ワクチンによって誘発される反応が数多くある。逆に、SARS-CoV-2の免疫逃避を促進する可能性のあるS以外の特徴のない変異も存在する。
長引くSARS-CoV-2感染において、免疫逃避のための変異が出現していることや、急速に広がっている複数の亜種があることを示す証拠が増えていることから、幅広い関心と行動を起こすべきである。SARS-CoV-2の感染拡大を抑制することが、免疫回避変異のさらなる選択を防ぐことにつながる可能性が高い。そのためには、調整された包括的な世界的予防接種・予防戦略が必要である。部分的な展開や不完全な予防接種では、中和抗体価が最適ではないため、ワクチンの効果に悪影響を及ぼす逃避型が選択されてしまう可能性がある。自然免疫反応やワクチンによる免疫反応によって選択される可能性のある、循環するSARS-CoV-2の亜種を検出し、その特徴を明らかにするためには、遺伝子型および表現型の検査能力の向上が世界的に不可欠である。また、ワクチンを接種した人の間で発生した感染症についても、突破口のメカニズムを積極的に評価する必要がある。SARS-CoV-2が爆発的に世界に広がり、壊滅的な被害をもたらしたことは、新しい亜種がパンデミック対策をさらに複雑にする可能性があることを明確に警告している。ワクチンメーカーは現在、循環するSARS-CoV-2の亜種に対するブースターワクチンの可能性を検証しており、また、より広範囲に作用するモノクローナル抗体の治療法の開発も進めている。パンデミックを確実に制御し、撲滅するためには、このような積極的なアプローチが必要となるだろう。
