The Effectiveness of Vitamin E Treatment in Alzheimer’s Disease
www.ncbi.nlm.nih.gov/pmc/articles/PMC6412423/
要旨
ビタミンEは何年も前にアルツハイマー病の治療薬として提案された。しかし、その効果ははっきりとしたものではない。ビタミンEは抗酸化物質や神経保護物質であり、抗炎症作用や低コレステロール作用があり、脳の健康に重要な役割を果たしている。
さらに、アルツハイマー病患者のビタミンEのレベルは、非認知症のコントロールに比べて低い。このことから、ビタミンEはアルツハイマー病に対して有益な効果を発揮する可能性がある。
しかし、ビタミンEの認知症の進行を遅らせる効果は限られており、情報は錯綜しており、結論は出ていない。問題は、なぜビタミンEがアルツハイマー病の治療に効果がないのかということである。
本論文では、アルツハイマー病において肯定的な結果が得られた研究と得られなかった研究をレビューし、治療としてのビタミンEが認知機能に肯定的な結果をもたらす場合もあれば、そうでない場合もある理由を考察する。
キーワード
アルツハイマー病、抗酸化物質、脳の健康、ビタミンEの回答者、非回答者
1. アルツハイマー病とその発症の仮説
アルツハイマー病は、長い進化の末に臨床症状が現れる神経変性疾患である。しかし、ここ数年でアルツハイマー病のパラダイムが変わっていた。以前は、研究者たちは、アルツハイマー病は加齢の過程で始まる加齢性疾患だと考えてた。今日では、臨床症状が現れる前に15年(遺伝性の場合)から 20~30年(散発性の場合)の間に発症することがわかっている[1]。この病気には予防的・治癒的な治療法はなく、いつ発症するかの知識がないことが医師の仕事を非常に複雑にしている。もう一つのハンディキャップは、なぜ病気が始まるのかがわからないことである。
この意味で、アルツハイマー病の始まりを説明しようとする仮説はいくつかある。これらの仮説は排他的なものではなく、重なり合ったり、同時に起こったりする可能性がある。これらの仮説は3つのグループに分けることができる。タンパク質の沈着に基づく仮説。このグループには、βアミロイド(アミロイドβ)カスケード仮説とタウ仮説がある。
主にアミロイドβペプチドによって形成される沈着物は老人斑として知られている[2]。アミロイドβはアミロイド前駆体タンパク質(APP)と呼ばれる膜タンパク質のタンパク質分解に由来する。アミロイドβカスケード理論の賛成では、アミロイドβの発生に関与する遺伝子の変異がアルツハイマー病を引き起こすと言うことができる[3,4];タウタンパク質をコードする遺伝子の変異はアミロイド沈着を引き起こさない[5,6]。ApoE4対立遺伝子は、アミロイドβペプチドのクリアランスの減少につながり、アルツハイマー病のリスクを増加させる[7];アルツハイマー病脳から分離されたアミロイドβオリゴマーは、シナプスの損失、神経細胞密度、および記憶障害を伴う[8];アミロイドβペプチドは、タウの過リン酸化を誘導することができる[9]。
本質的にタウタンパク質によって形成される沈着物は神経原線維のもつれとして知られている。タウは細胞骨格タンパク質であり、その安定性に非常に重要である。タウは高リン酸化状態に変化し、アルツハイマー病の病理学では細胞骨格の崩壊を引き起こす。高リン酸化タウを多く含む神経細胞はアポトーシスを起こし、神経変性が起こる[10]。この理論を支持して、このタイプの認知症の重症度は、脳内の神経原線維のもつれの蓄積の増加とよく相関している[11,12,13];アルツハイマー病患者の脳脊髄液(脳脊髄液)中の高リン酸化タウ種と認知機能障害の程度との間には高い相関がある[14];この治療標的に対する薬剤によるタウフィラメントの減少は認知機能の低下を緩和する[15]。
アルツハイマー病の最初のイベントとして神経炎症を含む反応過程の仮説。アルツハイマー病ではプロ炎症性サイトカインの上昇が見られる [16,17]。高レベルの腫瘍壊死因子α(TNF-α)とインターロイキン6(IL-6)も対照群と比較して患者の血清と脳内で検出される。複数の炎症性マーカーは、IL-1,IL-6,顆粒球-マクロファージコロニー刺激因子(GM-CFSIL-12,IL-26,およびTNFなどのアルツハイマー病動物モデルで見られる。組織学的には、特徴的なアミロイド斑がミクログリアに取り囲まれ、反応性アストロサイトがアルツハイマー病患者の脳に出現している[18]。また、脳アミロイドーシスマウスを用いた研究によると、アストロサイトの活性化は発症過程の非常に早い段階で起こるようである[19]。具体的には、アミロイドβが沈着する前に、細胞と炎症性サイトカインの両方の上昇が現れることが確認されている[20]。
機能喪失に基づく仮説としては、カルシウムミスバランス仮説、血管仮説、酸化ストレス仮説などがある。カルシウム理論の賛成では、若年性アルツハイマー病の各突然変異が細胞内のカルシウムバランスを変化させることが確認されていると言うことができる[21]。散発性アルツハイマー病では、アミロイドβや他の組織学的変化が存在する前に、ニューロンのカルシウムレベルの上昇によるニューロンの過剰興奮性を示唆する証拠がある[22]。
血管理論を支持して、血管危険因子とアルツハイマー病との間には明確な関係があると言える;アルツハイマー病患者では早期の血管損傷が存在する;血管損傷だけで神経変性を引き起こす;アルツハイマー病の初期段階ではアミロイドβの血管内沈着が存在する[23]。
最後に,蓄積された実験的証拠の中で最も重要なものの一つが酸化ストレス説である。
アルツハイマー病の発症については様々な説があるが、全ての説に共通しているのは、加齢に伴う細胞の老化がエネルギー代謝の機能低下を引き起こしているという点である。このスレッドは、酸化ストレスであり、この病気の中心的な役割である。我々 はそれを大まかな方法でこのレビューの次の行で議論し、その役割は、主に、酸化ストレスの影響に取り組んでいるビタミン E の役割と相互に関係する。
2. 酸化ストレス理論とアルツハイマー病
酸化ストレスとは、形成される高酸化種と抗酸化防御が不十分な状態との間のバランスの崩れである[24]。これにより、酸化ストレスの結果として生じる恒常性バランスの変化が引き起こされる[25]。ミトコンドリアにおけるO2からH2Oへの還元。ミトコンドリアにおけるO2からH2Oへの還元は、非常に反応性が高く、近くのいくつかの生体分子と相互作用する活性酸素種(ROSとしても知られている)を産生する。一方、脳は私たちの体の中で最も多くのO2を消費する器官である。全体重の2~3%を占めるにもかかわらず、基礎代謝の約20~25%を消費している。結果として、それは最も高い活性酸素生成器官である。脳の代謝は、アルツハイマー病では早期に低下し、これは代謝調節の低下と増加した活性酸素の発生と関連している可能性がある[26]。
アルツハイマー病では、すべての高分子の酸化は患者の脳で非常に早い段階で見られる。脂質、タンパク質、核酸、多糖類はすべてアルツハイマー病で酸化される。
高度糖化最終生成物(AGE)は、還元された糖とタンパク質の側鎖との反応である糖化によって形成される。糖化産物は非常に安定な分子であり、神経細胞内、老人斑、神経原線維のもつれに蓄積する傾向がある[27]。
脂質過酸化は、不飽和脂質のヒドロキシラジカル攻撃により、反応性カルボニルや反応性アルデヒドなどの反応性の高い二次生成物を生成し、それらの生理的役割を超えて酵素活性部位を不活性化させることができる。さらに、酸化された膜は、移動性が変化している。タンパク質のアルデヒド付加体は、老人斑や神経原線維のもつれによく見られ、脆弱なニューロンの細胞体で最も顕著である[28]。
タンパク質が酸化されると、ペプチド結合が損なわれ、切断される可能性がある。また、反応性カルボニルの生成や、タンパク質のニトロ化も頻繁に起こる。これらのタンパク質修飾はすべて神経細胞体で顕著に起こっている[29]。
最後に、核酸もまた、酸化によって影響を受ける可能性がある。活性酸素はプリン塩基とピリミジン塩基の両方を変異原性、さらには劇症的な結果を伴って変化させる可能性がある。脆弱な神経細胞体は、表向きは酸化された核酸を蓄積する [30]。
したがって、抗酸化療法がアルツハイマー病の治療法として数え切れないほど提案されていることは驚くに値しない。
3. なぜビタミンEがアルツハイマー病の治療薬なのか?
3.1. ビタミンEは抗酸化物質であり神経保護物質である
ビタミンEは8つの化合物のグループを含む用語で、脂溶性ビタミンに属する。このグループにはα-、β-、γ-、δ-トコフェロール、トコトリエノールがあり、その主な特徴は抗酸化力にある。しかし、ビタミンEには神経保護作用、抗炎症作用、コレステロール低下作用[31,32,33]があり、脳の健康に重要な役割を果たしている。
ビタミンEの抗酸化作用は、そのフェノール基のクロマノール環上の水酸基の存在に基づいており、この水酸基は水素原子を供与し、活性酸素種(ROS)を含む様々なフリーラジカルを中和することができる[34]。この反応が起こると、非ラジカル生成物とビタミンEラジカルが得られる。その後、ビタミンEラジカルは別のフリーラジカル脂質と反応したり、ビタミンC [35,36,37,38]によって本来の形に再生されたりする。このプロセスによってビタミンEはペルオキシラジカルを中和し、脂質の過酸化[39]、特に細胞膜の保護に不可欠な多価不飽和脂肪酸の過酸化をブロックする。
[40]。この抗酸化活性は、試験管内試験と生体内試験の両方でいくつかの研究で証明されている。ビタミンEの抗酸化能力を示す最も重要な証拠の一つは、1997年にHamとLieblerによって報告されたもので、彼らはラットにビタミンEの補助的な食事を与えた。彼らは、t-Bu-OOHによる肝細胞の脂質過酸化を誘発するビタミンEの抗酸化特性を評価した。その結果、ビタミンEを投与したラットでは代謝変化が減少することが示された[41]。
さらに、ビタミンEは脳内で最も重要な抗酸化物質の一つと考えられており、特にα-トコフェロールの形態である。これは、さまざまな組織におけるビタミンEのレベルの調節と分配を含む機能を持つトランスポーターα-TP(α-トコフェロール伝達タンパク質)の脳内での高レベルの発見によるものである[42,43]。脳機能におけるα-TTPの重要な役割は、α-TTP遺伝子の突然変異を持つヒトのキャリアは、進行性の脊髄小脳運動失調、運動失調、プロミオセプションの喪失、極端に低いビタミンEレベルを発症するという事実からも明らかになっている[44,45]。脳では、α-TTPの発現は小脳で最も高く、特にアストロサイトでは、隣接するニューロンにビタミンEを供給している [46]。重要なことは、神経変性疾患患者の脳ではα-TTP発現が増加していることである[42,47]。このことから、ビタミンEは抗酸化作用を介して神経保護に重要な役割を果たしていると考えられる。
前述のように、アルツハイマー病では、すべての高分子の酸化を促進する活性酸素の明らかな生産がある。アミロイドβはミトコンドリアと小胞体による活性酸素の生成を伴うので、それ自体が細胞内の酸化ストレスの重要な誘導因子であるという事実は驚くべきことではないかもしれない。アミロイドβはまた、活動電位の伝達に重要な細胞カルシウムの恒常性の崩壊を引き起こす。アミロイドβが凝集して細胞膜の近くに沈着すると、脂質過酸化を促進してマロンジアルデヒド(MDA)や4-ヒドロキシノネナール(4HNE)などのプロオキシダント種を産生する。最後の1つは、その近傍の脂質やタンパク質を共有結合的に修飾することができるアルデヒドであり、これらのタンパク質の1つはタウである[48,49]。
タウの酸化的修飾は、試験管内試験での凝集を促進し[50]、タウの高リン酸化と神経原線維のもつれの形成を誘発する可能性がある[51]。さらに、酸化ストレスもまた、グリコーゲン合成酵素キナーゼ-3β(GSK3β)活性を促進することにより、タウの高リン酸化を促進する。GSK3βはユビキタスに発現するキナーゼであり、ペアらせんフィラメントのほとんどのセリン残基とスレオニン残基でタウをリン酸化する[52]。最後に、4HNEは直接マイトジェン活性化タンパク質(MAP)キナーゼ、p38 [53]を活性化し、タウの過剰リン酸化につながる。正直に言うと、相関関係は、活性化されたp38と凝集したタウ[54]のレベルとの間の高リン酸化タウを示すトランスジェニックマウスで発見された。
最後に、ビタミンEは脳内で最も重要な抗酸化物質の一つと考えられており、特にα-トコフェロールの形態である。これは、トランスポーターα-TP(α-トコフェロール伝達タンパク質)の脳内での高レベルが原因であり、その機能には様々な組織内でのビタミンEのレベルの調節と分布が含まれている[42,43]。脳機能におけるα-TTPの重要な役割は、α-TTP遺伝子の突然変異を持つヒトのキャリアは、進行性の脊髄小脳運動失調、運動失調、プロミオセプションの喪失、極端に低いビタミンEレベルを発症するという事実からも明らかになっている[44,45]。脳では、α-TTPの発現は小脳で最も高く、特にアストロサイトでは、隣接するニューロンにビタミンEを供給している [46]。重要なことは、神経変性疾患患者の脳ではα-TTP発現が増加していることである[42,47]。このことから、ビタミンEは抗酸化作用を介して神経保護に重要な役割を果たしていると考えられる。
3.2. 抗炎症・細胞シグナリングとしてのビタミンE
抗酸化物質としての役割を超えて、ビタミンEは高齢者の免疫応答を強化することができる。加齢やアルツハイマー病などの神経変性疾患では、多くの炎症反応を誘発する免疫系の調節障害が生じる。高齢者が食事のサプリメントとしてビタミンEを摂取すると、ビタミンEの抗炎症作用があることを証明する多くの研究がある。
これらの研究では、試験管内試験でのT細胞の増殖、IL-2の産生、E2プロスタグランジンの阻害などの有益な効果が示されている[32]。Leeと共同研究者らは、毎日233mgのビタミンEを28日間摂取すると、Tリンパ球集団のIL-2受容体レベルが上昇することを発見した[55]。De La Fuenteらは、同様の用量を3ヶ月間摂取した場合、高齢者におけるα-トコフェロールの有益な効果、特にリンパ球の付着能力、IL-2産生の増加、NK活性、リンパ球の増殖に効果があることを示している[56]。
しかし、この有益な効果は、アレルギー性鼻炎などの併存疾患によって消失したり、過敏症反応を引き起こしたり[58]、成人喫煙者では有害な影響を及ぼすことさえある[59,60]。
免疫系に対するビタミンEの作用機序は、シクロオキシゲナーゼ(COXs)および5-リポキシゲナーゼ(5-LOX)活性を阻害することなく、プロスタグランジンE2およびD2を阻害することに関係している[61,62,63]。一方、ビタミンEの疎水性側鎖のω-およびβ-酸化に由来する代謝物は、COX活性を阻害する[62]。一方、ビタミン E は、5-LOX 活性の阻害をもたらすイオノフォアの阻害を介して、カルシウムの流入を遮断する膜の変化を阻害する[63]。両方の阻害は、最終的にプロスタグランジンの阻害を誘導するシグナル伝達経路を活性化する。その後、IL-2産生が生成され、したがって、免疫応答(図1)。
図1 ビタミンEによる5-LOX活性の阻害
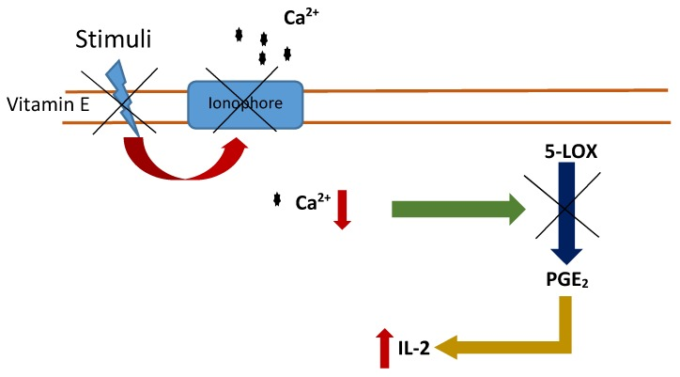
ビタミンEはカルシウムイオノフォアを阻害し、細胞内カルシウムレベルの低下を引き起こし、5-LOX活性の阻害を誘発し、プロスタグランジン(PGE2)の阻害を誘発する。インターロイキン2(IL-2)レベルが上昇し、その結果、免疫反応が起こる。
ビタミンEはプロテインキナーゼC(PKC)の阻害剤であり、この阻害は抗酸化活性とは無関係であることが示されている[64]。ビタミンEは活性型を阻害するホスファターゼ(PP)2Aを活性化することができ[65,66]、ビタミンEはジアシルグリセロールキナーゼ活性を調節することができる[65,66]と、メカニズムは二重になっている。結果はビタミンEのアイソフォームによって異なり、α-トコフェロールは血管平滑筋のPKCを阻害し、細胞の増殖を阻害するのに対し、β-トコフェロールはこの作用を阻止する[64,67,68]。
対照的に、ビタミンEによるPKCの阻害は、アルツハイマー病病理のいくつかの側面において非有益な効果を有する可能性がある。例えば、アミロイドβ1-42に反応性のT細胞亜集団がアルツハイマー病の異なる臨床段階で異なるPKCのアイソフォームを発現するため、PKCは免疫応答において重要な役割を果たしている[69]。さらに、PKCは非アミロイド性APPの処理に不可欠なα-セクレターゼ活性を調節している。したがって、アミロイド原性ビアが減少し、したがって、アミロイドβ毒性ペプチドの形成が抑制される[70]。
ビタミンEはまた、PKCに依存しない方法で転写レベルで遺伝子を制御することができ、これらの遺伝子のいくつかは、CD36 [71]、SRクラスA [72]および細胞内接着分子-1 [73]である。
まとめると、ビタミンEは抗酸化物質として作用するだけでなく、PKC依存性またはPK非依存性の両方の方法で細胞シグナル伝達特性を持っている。したがって、アルツハイマー病におけるビタミンE治療の研究は、その抗酸化特性だけでなく、抗炎症および神経保護効果にも焦点を当てるべきである(図2)。
図2 ビタミンEの効果
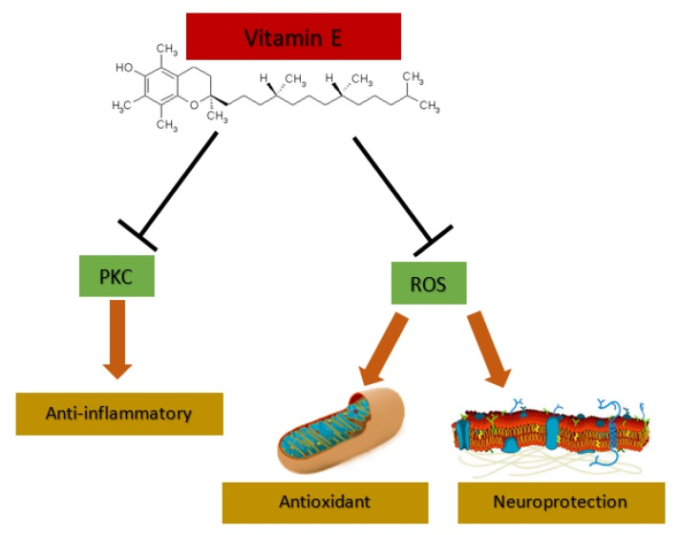
ビタミンEは、プロテインキナーゼC(PKC)の阻害により抗炎症作用を発揮し、活性酸素(ROS)への攻撃により抗酸化作用や神経保護作用を発揮する。
3.3. アルツハイマー病におけるビタミンEのレベルは低い
30年近く前に、アルツハイマー病患者55人において、ビタミンEレベルが非認知症の対照群と比較して低下したことが発表された [74]。それ以来、多くの研究がこれらの結果を裏付けている。患者数が少ない場合もあるが(表1参照常に有意な結果が得られている。2014年に実施されたメタアナリシスでは、微量栄養素とアルツハイマー病に関する80の研究がレビューされた。著者らは、特にビタミンEはアルツハイマー病患者の血漿中濃度が低いことを示したと結論づけた。さらに、著者らはビタミンEのレベルと患者の栄養失調の状態との間に関連性を見いだせず、栄養失調の前に微量栄養素の状態が損なわれている可能性を示唆している[75]。選ばれた116の出版物の最近のメタアナリシスでは、アルツハイマー病患者のビタミンEレベルも脳脊髄液および脳内で有意に低いことが確認されている[76]。904人のアルツハイマー病患者と1153人の対照群を含む17の研究を用いたより最近のメタアナリシスでは、アルツハイマー病患者は健康な高齢の対照群と比較して血清ビタミンEの濃度が低いことが示された[77]。
表1 アルツハイマー病とビタミンE値の低下との関連性に関する研究
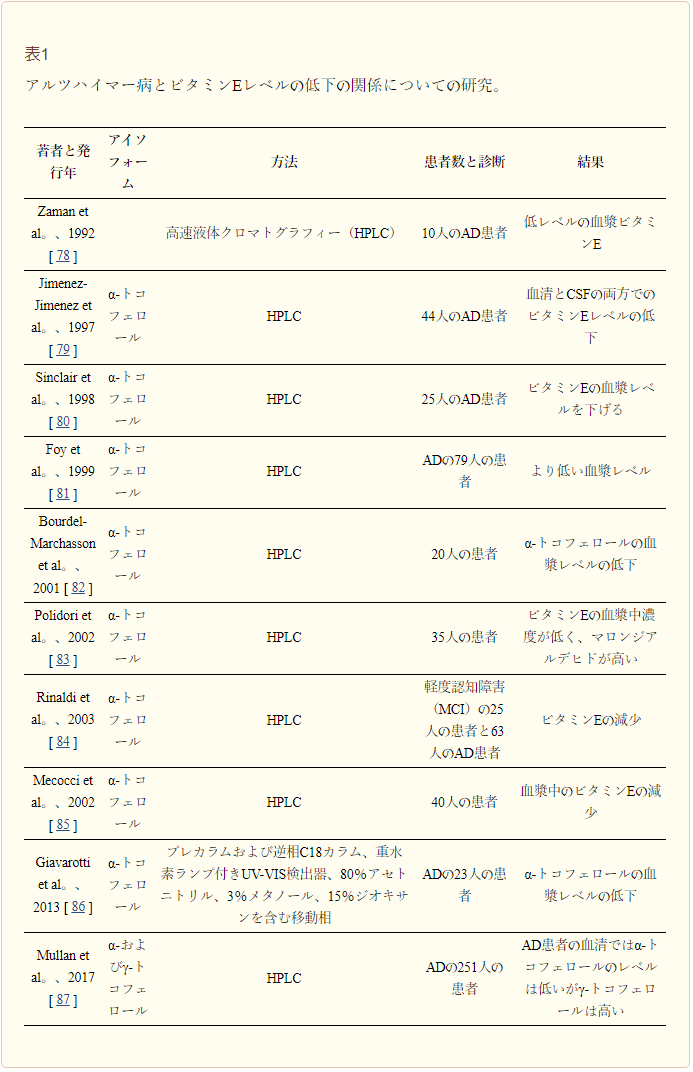
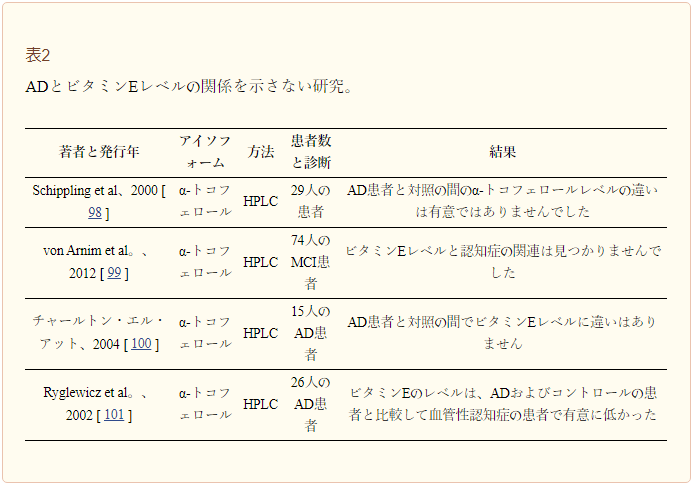
表2 アルツハイマー病とビタミンE値の関連性を示さない研究
3.4. ビタミンEと認知機能低下の予防
疫学研究では、ビタミン E の補給と アルツハイマー病 発症リスクの低下との関連性も明らかにされている。1998年には、633人を対象としたプロスペクティブ研究が発表されており、4.3年間の追跡調査の結果、27人のビタミンEサプリメント利用者のうちアルツハイマー病発症者はいなかった[89]。2002年には、Engerhaltらがオランダの別のコホートで6年間の追跡調査を行い、この結果を裏付けた [90]。1993年から 2000年に実施された65歳以上の住民815人を対象とした別の前向き研究が同年に発表され、ベースラインでアルツハイマー病を認めず、平均3.9年の追跡調査が行われた。この研究では、ビタミンEを含む食品ではなく、他の抗酸化物質を含む食品がアルツハイマー病発症リスクの低下と関連している可能性が示唆された。しかし、この関連はAPOE ɛ4対立遺伝子を持たない個人の間でのみ観察された [91]。別の前向き研究は、ユタ州(米国)からキャッシュカントリー研究は、ビタミンEとビタミンCを含むマルチビタミン複合体を補充した人々の明らかに低いアルツハイマー病リスクを結論づけた興味深いことに、彼らは単独でこれらの化合物の摂取に関連する保護効果の証拠を示していない[92]。
ロッテルダム研究(365人のアルツハイマー病患者)からの分析データもまた、アルツハイマー病の長期リスクの緩やかな減少を示した。重要なことは、肯定的な結果はビタミンEを豊富に含む食品の摂取量が多い参加者のみに見られたことである。しかし、平均的なビタミンE摂取量の参加者では認知症リスクは低下しなかった[93]。560人のアルツハイマー病患者を含む認知症のコホート研究であるCanadian Study of Health and Aging (1991-2002)のデータは、ビタミンEサプリメントの使用が認知機能低下のリスク低下と関連していることを示唆している[94]。
一方、他の3つの研究では、ビタミンEの摂取量とアルツハイマー病のリスクとの関連は示されていない。最初の研究では、2969人の参加者を2年ごとに5.5年間追跡調査し、ビタミンEとビタミンCのサプリメントを単独または併用しても、アルツハイマー病や認知症全体のリスクは低下しないと結論づけた[95]。もう一つは、The Honolulu-Asia Aging Studyの3385人の男性を対象とした研究で、ビタミンEとCのサプリメントは晩年の認知機能を改善する可能性があるが、特にアルツハイマー型認知症に対する保護効果は認められなかった[96]。最後に、ワシントンハイツ-インウッドコロンビア・エイジング・プロジェクトの980人の高齢者を対象とした別の研究では、食事療法、サプリメント、総摂取量のいずれもビタミンEはアルツハイマー病のリスク低下とは関連していないことが明らかになった[97]。
4. ビタミンEはアルツハイマー病の治療薬として有効か?主な試験へのアプローチ
1997年に発表された佐野らによる初期の研究では、アルツハイマー病における治療としてのビタミンEの有効性が初めて示された。この二重盲検無作為化多施設共同臨床試験もプラセボ対照で、主に中等度の重度障害を有するアルツハイマー病患者におけるビタミンE補給に焦点を当てたものであった[102]。310人の患者が募集され、2000IU/dのビタミンEまたはプラセボを2年間投与された[102]。その結果、死亡、施設入所、基本的な日常生活動作の能力喪失、または重度の認知症の発生までの時間を測定した[102]。彼らは、この用量のビタミンEがアルツハイマー病の進行を遅らせると結論づけた。22年後も論争は続いている。表3は、アルツハイマー病治療におけるビタミンEの有効性に関する臨床試験をまとめたものである。
表3 アルツハイマー病治療におけるビタミンEの有効性に関する臨床試験
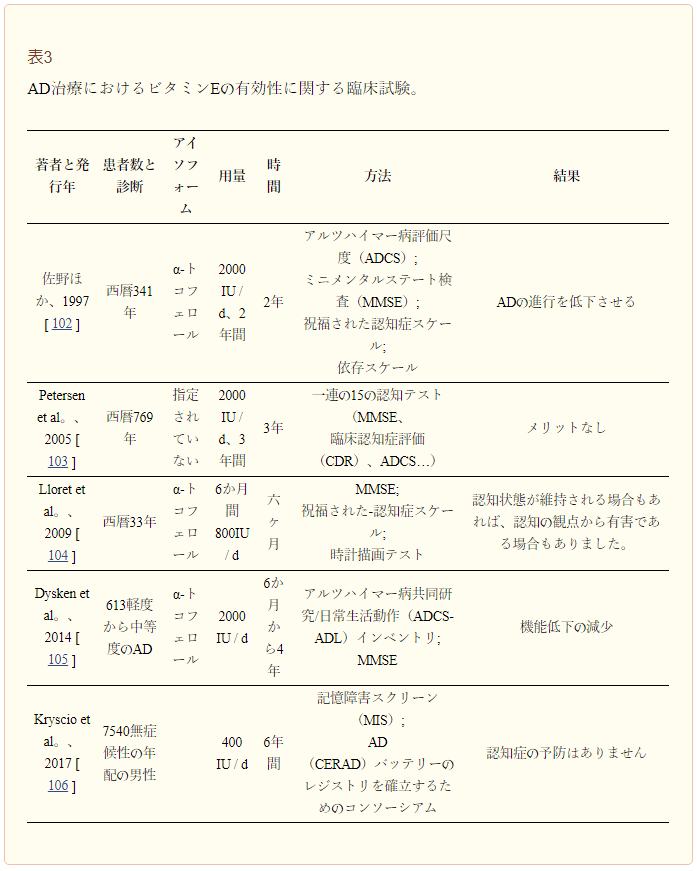
2005年にPetersenらは769人の被験者を選び、二重盲検試験を行った[103]。被験者には2000IU/dのビタミンEまたはプラセボが3年間投与されたが、著者らはビタミンEの補給には効果がないことを明らかにした[103]。興味深いことに、2009年に発表された研究(800 IU/d、6ヵ月)では、ビタミンEを補充したグループに2つの異なるサブグループが認められた。ビタミンEの「回答者」と呼ばれる1つのグループでは、治療後に酸化ストレスパラメータが低下し、認知テストのスコアは維持されていた。しかし、「非反応者」と呼ばれる第二のグループでは、ビタミンEは酸化ストレスを防ぐ効果がなく、認知力はプラセボ群よりもさらに低下していた。ビタミンEが酸化ストレスを低下させると、患者の認知状態は維持されると結論づけた。しかし、ビタミンEが酸化ストレスを防ぐことができない場合は、認知の面で有害であると結論づけている[104]。
それにもかかわらず、2014年に、二重盲検、プラセボ対照、並行群、無作為化臨床試験(The TEAM-アルツハイマー病 VA Cooperative Randomized Trial)でDyskenらは、軽度から中等度のアルツハイマー病患者613人を募集し、同じ用量(2000IU/dのα-トコフェロールまたはプラセボ)でα-トコフェロールの補充が、軽度から中等度のアルツハイマー病患者の機能低下を減少させることを発見した[105]。不思議なことに、これらの結果はメマンチンでも、メマンチンとビタミンE治療の併用でも観察されなかったため、メマンチンがビタミンEの効果を阻害している可能性がある[105]。
2017年のPREアルツハイマー病ViSE試験では、低用量のビタミンE(400 IU/d)を用いたKryscioらが、無症状の高齢男性7540人を選択してビタミンEを補充しても認知症を予防できないことを明らかにした[106]。彼らは、アルツハイマー病の予防におけるビタミンEとセレンの補充の効果を評価し、ビタミンEもセレンも、あるいは両方の組み合わせでさえも認知症を予防しなかったと結論づけた[106]。
しかし、ビタミンEに基づくアルツハイマー病の有効な治療法を得ようとする試みは続いている。ビタミンEの異なる形態の有効性を評価する研究や、認知症の進化に対して有益な効果を持つ可能性がある別の化合物とのビタミンEの組み合わせはまだ多くの研究がある。昨年、戸山郁夫氏のグループは、パーム油からの異なるビタミンE類似体の組み合わせであるトコトリエノールに富んだ画分の有益な効果を、アルツハイマー病のトランスジェニックマウスモデルで評価した[107]。結果は、補充がトランスジェニックマウスの認知機能を救済し、アミロイドβオリゴマーのレベルは変化しなかったが、アミロイドβの沈着を減少させたことを示した[100]。最後に、アルツハイマー病動物モデルを用いた別の研究では、魚油の補充[108]とビタミンEの組み合わせを評価した。彼らの結果は、低ビタミンEの食事と魚油のサプリメントのみがトランスジェニックマウスの認知機能を救済することを示した。ビタミンEの高用量は有益ではなく、高レベルのビタミンEが酸化を引き起こすプロオキシダントとして作用することを示唆している[108]。
5. なぜビタミンEはアルツハイマー病の治療に失敗するのか?
酸化ストレスはアルツハイマー病の初期症状であるため、可能性のある治療法として抗酸化療法を試みるために、科学界では多くの努力がなされていた。しかし、上で述べたように、認知症の進行を遅らせるビタミンEの有効性は限られており、情報は錯綜しており、結論は出ていない。しかし、なぜ他の抗酸化物質とビタミンEは、アルツハイマー病の認知機能低下の経過を改善するために失敗するのであろうか?
これは、酸化ストレスのパラドックスを強調している:酸化防御を高める努力は、「抗酸化パラドックス」と呼ばれている人間の病気[109]のために有益であることが証明されていない。Halliwellは3つの可能性を指摘している:
- 動物で得られた結果をヒトに外挿していること、
- ヒトのコホートではベースラインの栄養状態の測定が行われていないこと、
- 一部の抗酸化物質がプロオキシダント効果を持つ可能性があること[110]。
上で述べたように、患者ではビタミンEの血漿中濃度が低いため、「ベースラインの栄養状態」についてのエビデンスがある。しかし、主な試験では開始前のベースラインのビタミンE値の測定はチェックされていないことが多いのも事実である。
一方で、動物からヒトへの結果の外挿は些細なことではない。酸化ストレスを測定するための正しい方法はまだ議論されておらず、特定の方法や適切な方法ではないこともある[111,112,113,114]。アルツハイマー病における酸化ストレスの研究の多くは古いものであり、方法が最新のものではなかった。酸化ストレスのバイオマーカーを測定して抗酸化反応を追跡することは非常に推奨される。しかし、良い酸化ストレスバイオマーカーを選ぶのは簡単ではない。使用されている酸化ストレスのバイオマーカーの中には、酸化低密度リポ蛋白質抗体のように特異性に疑問があるものもある。この点から、疾患に関与する特定のタンパク質の酸化ストレスの分析が推奨されていた。これらのマーカーは、特定の病理学的経路をよりよく表し、治療のモニタリングや結果の予測のための方法となる可能性がある[115]。患者の酸化をモニタリングすることの重要性の一例として、Lloretら[104]によって発見された非反応群のように、ビタミンEサプリメントが酸化バランスを修正することに効果がないことが挙げられる。この作業では、酸化ストレスが減少していた患者だけが認知機能の改善を示したが、非応答者は、認知テストの結果が悪化したことが判明した。
もう一つの重要なポイントは、ビタミンEのバイオアベイラビリティであるが、これは複雑であり、競合する栄養素の摂取量、吸収の腸内差、年齢、性別、喫煙、肥満、遺伝的多型などのいくつかの重要な要因に影響される。植物由来のステロール、エイコサペンタエン酸やレチノイン酸、さらには食物繊維は、ビタミンEの吸収を低下させる競合栄養素として記述されている[116,117,118,119]。さらに、ヒトでは主に食品の内容物やビタミンEの形態の違いにより、血中への吸収率は20%~80%と異なっており、血中でのビタミンEの輸送はリポタンパク質によって行われている[120]。特に、生体内でのα-トコフェロールの中枢神経系への入り口は、高密度リポタンパク質(HDL)粒子によって提供され、HDLレベルは人によって大きく異なる[121]。細胞内では、ビタミンEは、アルツハイマー病脳で高度に発現している輸送タンパク質であるα-TTPと結合しており、特に酸化ストレス条件下では[47]。
年齢や性別もビタミンEのバイオアベイラビリティに影響を与える。60歳以降のビタミンEの血漿中濃度は上昇するが、80歳以降は低下する[122]。α-トコフェロールの血漿中最大濃度は女性の方が男性よりも高いようであるが、これは男女間のHDLレベルの違いによるものかもしれない。[123].
一方、喫煙者は非喫煙者に比べて血清中のα-トコフェロールのレベルが低いが、この差異は食事パターンの違いに起因する可能性があるが[124,125,126]。また、肥満は血清α-トコフェロールレベルと逆の関係にある[127]。特に、ウエスト対ヒップ比とウエスト周長は、性別に関係なくα-トコフェロールの血清濃度と関連していた[128,129,130]。[128,129,130].
最後に、ビタミンE代謝に関与するタンパク質をコードする遺伝子の遺伝的多型もまた、バイオアベイラビリティの個人差を説明することができた [131,132,133,134]。50種類以上の一塩基多型(SNP)がビタミンEの恒常性に関連している。
もう一つのポイントは、ビタミンEが血液脳関門を通過し、脳内レベルを上昇させる効果があることである。したがって、脳の酸化的損傷を軽減するビタミンEの有効性を示すことは非常に重要である[135]。
他の多くの研究では、ビタミンEの補給形態や、他の抗酸化物質、栄養素、医薬品との組み合わせにより、混乱をきたすことがある[136]。
適度な身体活動と一緒に地中海式食事は、今日ではアルツハイマー病の発症と進行に対する最初の防衛線であると考えられている。しかし、ほとんどの場合、この考えを擁護する研究は観察的であった。結果として、大規模な多施設無作為化臨床試験からの結果は、高齢者の認知に適度な運動、身体活動と健康的な地中海式食事との間の実際の関連性を明らかにすることが待たれている。抗酸化物質が豊富な食事は、バイオアベイラビリティが異なる可能性があるため、純粋な抗酸化物質を医薬品の形で摂取するよりも優れているかもしれない[137]。
もう一つの重要な事実は、脳の複雑さである。酸化ストレスは神経細胞の損傷、さらにはアポトーシス細胞死や神経変性を引き起こすため、神経細胞ネットワークが変化し、代償反応が誘導される。酸化的ストレスではなく、還元的ストレスが、健康な若年者のApoE 4/4で見られた[138]。このシナリオは、抗酸化療法の有効性を非常に複雑にしている。失われたニューロンネットワークを適切に改造したり再生したりすることは非常に困難であり、それが老化脳や代償脳であると考えれば、なおさらである。
6. 結論
現在のところ、ビタミンEのアルツハイマー病発症リスクへの影響については、臨床研究では信頼性の低い知見が得られていない。したがって、ビタミンEのレベルが遺伝的にアルツハイマー病リスクと関連しているのか、あるいはこの化合物の補給が認知症の進行を遅らせるのに有益であるのかは不明である。このレビューでは、アルツハイマー病患者の血漿中ビタミンEレベルの低下を示す研究の数が、反対の結果を示す研究よりも多いことがわかる。しかし、治療としてのビタミンEは認知に良い結果をもたらすこともあれば、そうでないこともある。神経細胞ネットワークの喪失とその置換、ベースライン時の患者の栄養状態の違い、各人の脳の補正時間の幅、その他の中でも各人のビタミンEの抗酸化作用などが治療の失敗の原因と考えられる。

