The changing epidemiology of SARS-CoV-2
www.science.org/doi/10.1126/science.abm4915
SCIENCE – 2022年3月10日
概要
トイレットペーパーを買いだめし、食料品を拭いていた時代から、子供たちを学校に送り出し、何十億人もの人々にワクチンを接種するまでになったのである。この間、疫学者や進化生物学者の世界的コミュニティも、COVID-19の原因ウイルスである重症急性呼吸器症候群新型コロナウイルス(SARS-CoV-2)の複雑で変化する動態を理解する上で大きな進歩を遂げてきた。このレビューでは、パンデミックの展開に伴い、このコミュニティが直面した疑問について、その足跡をたどっている。そして、これらの疑問を解決し、最終的にパンデミックをよりよく理解し制御するために、数理モデリングと実証データの定量的解析が果たした重要な役割に焦点を当てる。
2020年2月までに、世界的なコロナウイルスのパンデミックが始まったことは明らかであった。2020年1月23日に中国の武漢でロックダウン措置が発動される前にCOVID-19患者が急増したことは、重症急性呼吸器症候群新型コロナウイルス(SARS-CoV-2)のヒトからヒトへの感染がいかに効率的であるかを示している。2020年1月までに、中国以外でのSARS-CoV-2の記録された症例数の増加は、このウイルスの地域的封じ込めが極めて困難であることをさらに示していた。この頃、疫学者と感染症モデル研究者は 2019年新型コロナウイルス(2019-nCoV)-その後2020年2月にSARS-CoV-2と改名-の封じ込めの可能性を評価し、様々な地理的規模での広がりを予測するために重要な特徴を明らかにし始めた(図1)。
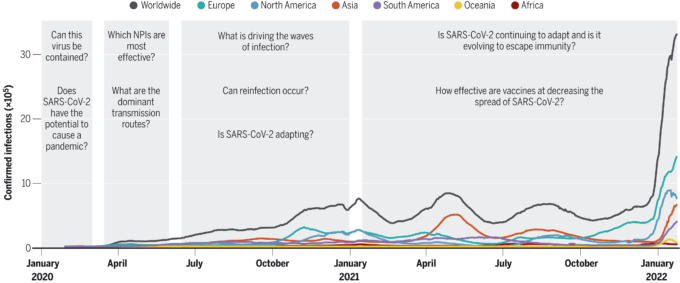
図1 SARS-CoV-2パンデミックの展開に伴い変化した疫学的疑問の年表。確認された感染を大陸別および世界規模で示した。灰色の棒グラフは、本総説で取り上げた期間(パンデミックの発生、曲線の平坦化、波への対応、ワクチンと変異株)を示している。
新興の病原体を封じ込めることができるかどうかは、その基本再生産数R0 (1)に依存する。これは、完全に感受性のある集団において一次感染者から発生する二次感染者の平均数として定義される (2)。R0が1未満であれば、積極的な封じ込めの努力は必要ないが、R0の値が大きくなると封じ込めが困難になる(2)。新興感染症のR0を推定することは容易ではなく、これを頑健に行うには、ウイルスが集団内でどれだけ速く拡散しているかを計算し、ある感染から次の感染までの時間(世代間隔として知られている)を測定することが必要となる(図2)。そのため、初期の疫学解析では、武漢で報告された症例データからウイルスの伝播速度を推定することに焦点を当てた。世代間隔は、過去に発生したコロナウイルス(SARS-CoV-1と中東呼吸器症候群コロナウイルス(MERS-CoV))のデータと、初期のSARS-CoV-2の発生で確認された少数の感染ペアを用いてパラメータ化された。このため、武漢でロックダウン措置が実施される前は、R0は2〜4の間と推定された。これらの推定値の違いは、世代間隔のパラメータ化の違いによるところが大きい(3)。このことは、世代間隔、ひいてはR0の値を正確に推定するための高解像度アウトブレイクデータが重要であると同時に希少であることを強調するものである。
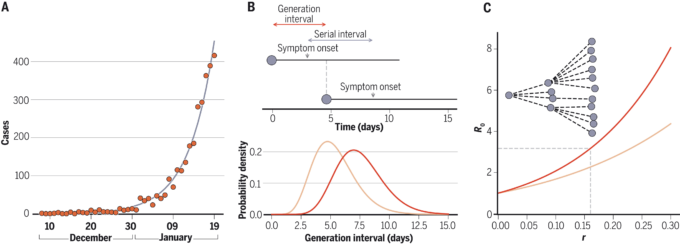
図2 A)観測された症例データに指数関数的成長モデルを当てはめ、ウイルスが集団に広がる速度を推定する。武漢におけるSARS-CoV-2のパンデミックについて、指数関数的成長率rの初期の推定値は1日あたり0.10〜0.20であり(3)パンデミック倍増時間は約3.5〜7日であることがわかった。(B)アウトブレイクデータを用いて、ウイルス連続間隔を推定する。これは、指標となる患者の症状発現から、その患者の接触者の症状発現までの時間として定義される。この連続間隔は、しばしばウイルス発生間隔の近似値として使用される。SARS-CoV-2の場合、武漢の初期の推定では、平均直列間隔は7.5日だった(86)(赤の分布)。平均がより小さい世代間隔分布の例を薄いオレンジ色で示す。(C) 基本再生産数R0は指数関数的成長率rと世代間隔の分布から、人口統計学的解析から導かれた式を用いて算出できる(87)。赤と薄オレンジの曲線は(B)の分布に対応し、R0の推定値が世代間隔にどのように依存するかを示している。上部の感染連鎖はR0=3の病原体のアウトブレイクを示している.
R0を超えると,新興の病原体を封じ込める能力は,感染者を隔離する能力に依存する(1).このことは、無症状または軽度の症状を示す感染者の割合(したがってサーベイランスで見逃されやすい)とその感染可能性に依存することになる。また、症状が出る前に感染している個人からの症状発現前の感染の可能性にも依存する。当初、無症状や軽度の症状の感染がどの程度一般的なのか、つまり、感染「氷山」の底がどの程度の大きさなのかは不明であった。疫学的モデルと中国の感染報告データを組み合わせて 2020年1月23日までに書類に記載されなかったSARS-CoV-2感染者の割合を推測した(86%と推定される)(4)。2020年2月と3月、アウトブレイクが発生したクルーズ船とフライトの乗客の集団スクリーニングとモニタリングにより、無症状のままの感染者の割合の最初の推定値が得られた:18〜31%(5,6)。また、初期のデータから、特に若い年齢層では軽症が一般的であることが明らかになった。さらに、接触者追跡調査により、症状発現時の感染力が高いこと、症状発現前および軽症の人からの感染が多いこと(7-9)完全に無症状の人からの感染も(頻度は低いものの)見られること(10)が明らかになった。これらの知見は、パンデミックの抑制という点で、非常に重要な意味を持つ。SARS-CoV-1やMERS-CoVとは異なり、SARS-CoV-2は最初から、公衆衛生に甚大な影響を与える世界的大パンデミックを引き起こす可能性を持っていることが認識されていた。
…新興の病原体を封じ込める能力は、感染者を隔離する能力にかかっている
曲線の平坦化
SARS-CoV-2は 2020年2月下旬までに中国の多くの地域、そして世界各地に拡散していた。ニュージーランドやベトナムなど、厳重なモニタリング活動によって初期の拡大をほぼ完全に抑えた国もあったが(11,12)他の多くの国ではすぐに地域社会での感染が始まった。数学的なシナリオモデルにより、もし対策が実施されなかった場合の惨状が予測された(13, 14)。北イタリア、ロンドン、ニューヨーク、その他最も早く感染した地域からの報告と相まって、これらのモデルからの予測は、ウイルスの拡散を抑制するために政府が課した制限にすぐにつながった(15)。非薬物的介入 (NPI) には、戸締まり、社会的距離の取り方、そして最終的にはフェイスマスクの使用が含まれるようになった。パンデミックの第一波でNPIが採用されたことで、感染曲線が平坦になり、患者が発生する期間が延長された。感染曲線を平坦にすることは、3つの理由から望ましいことであった。第一に、平坦な曲線では、一度に使用されるベッド数のピークが低くなるため、医療システムが過負荷になるのを防ぐことができる。第二に、発生の勢いを弱め、発生ピーク後の症例のオーバーシュートを抑えることができる(16)。第三に、臨床治療戦略や能力を向上させ、治療薬を評価する時間を確保することができる。
NPI対策がある程度整ったので、モデル化の作業はCOVID-19の将来の動態を予測することに向けられた。2020年の4月と5月に報告された最も公に近い予測のいくつかは、Institute for Health Metrics and Evaluation(IHME)が行った論争の的になる予測であった。これらの予測は統計的モデリングアプローチに依存しており、短期的な予測は正確に行えるが、長期的な予測では感染のプロセスを組み込んでいないため、失敗する可能性が高い(17)。実際、この時のIHME予測では 2020年半ばまでにほとんどウイルスが循環していないと予測されていた。その代わりに、メカニズム疫学的なモデル研究では、厳しいNPI対策が行われている間はウイルスの拡散が遅く、NPI緩和後に患者が再び増えると予測した(14)。
第1波により、疫学者に縦断的なSARS-CoV-2症例データ、COVID-19死亡データ、ウイルス配列データが提供されたため、NPIによるウイルス伝播抑制の効果が定量的に評価されはじめた。これらの分析から、NPIは曲線を平坦にし、循環レベルが低下する程度に一時的に再生産数を減少させるのに有効であることがわかった(18, 19)。これらの知見は、1918年のH1N1インフルエンザのパンデミックのような歴史的なパンデミックに関する研究の結果を反映しており、NPIが病気の伝播を減らすことに成功したことがわかった(20)。また、社会的距離を置くなどの異なる政策によって、どれだけの患者や死亡が回避できたかを定量化するために、反実仮想モデルが用いられた(21)。
NPIは集団レベルでのウイルス伝播の抑制に有効であったが、感染リスクは集団間で均等に減少したわけではない。SARS-CoV-2陽性者と密接に接触していたため 2020年の4月と5月には医療従事者と最前線の労働者(例えば、第一応答者)が特に高い感染リスクを抱えていた。また、タクシーやバスの運転手など公共性の高い職業や、工場や食肉加工工場など換気が悪く混雑した環境での職業など、多くの基幹的職業でリスクが高まることが判明した。また、社会的距離を置くことができないような混雑した生活環境でも、感染リスクが高まることがわかった(22)。NPI を導入していても、老人ホーム、ホームレス・シェルター、刑務所、刑務所などの共同生活施設では、大規模な集団感染が発生した (23)。リスクは、劣悪な衛生環境と不十分な健康管理によって悪化した。また、社会経済的、人種的、民族的なグループ間で、感染率に著しい差があることも明らかになった(24)。
予想されたように、NPIの広範な使用は、実施された場合、かなりの社会的、経済的コストを引き起こした。経済の再開を促進するために、研究者は、効果の高いNPIと廃棄される可能性のあるNPIを区別することを目指した。異なるNPIの効果を評価する鍵は、ウイルスの感染経路を理解することであった。エアロゾルや飛沫による直接感染と比較して、ウイルスが汚染された表面(感染媒介物)を介して個人間でどの程度容易に拡散したのだろうか。2020年4月の初期の研究では、SARS-CoV-2はプラスチックなどの表面で数日間生存し続けることが判明したが(25)その後の研究では、感染は主にフォマットを介してではなく、感染者からの直接感染によって起こることが示唆された(26)。また、コンタクト・トレーシングの研究により、日本の公衆衛生当局が3つのCと呼ぶ、閉鎖的で混雑した場所や密接に接触する環境において、直接感染のリスクが高いことが明らかになった(27)。大規模な集団発生は、ナイトクラブ、カラオケバー、合唱団の練習など、大きな声を出すことが特徴的な屋内環境で発生したことが確認されている。統計解析の結果、集会や職場の閉鎖はSARS-CoV-2の感染拡大の抑制と正の相関があり(28, 29)、SARS-CoV-2の感染を促進する上で閉鎖的な場所での直接感染が重要であることを裏付けている。
コンタクトトレーシングによって検出された大規模なアウトブレイクと、新たに出現したウイルス配列データによって、個人間の実質的な感染の異質性がすぐに認識されるようになった。第一波のデータを用いた研究では、症例の10%程度が二次感染の80%を引き起こしていることが判明し(19,30)これは他のヒト病原体と比較すると比較的高いレベルの異質性であった(31)。超拡散のダイナミクスに関する説明は、個人間の様々な接触パターン(32)拡散を助長する高リスクの環境(23)および高ウイルス量などの生物学的要因(32-34)に及んでいる。注目すべきは、超拡散を行う個人または事象を体系的に特定できれば、より的を絞った方法で蔓延を緩和することに焦点を当てた制御努力が可能になることだ。フェイスマスクの有効性に関する影響力のあるレビューによると、マスク着用は、感染した呼吸器粒子の伝達を減少させることにより、接触あたりの感染率を低下させるという顕著な効果があることが示されている (35)。したがって、特にウイルス量の多い感染者によるマスク着用(すなわち感染源対策)は、集団におけるウイルスの拡散を抑える可能性があると考えられる。
また、疫学的モデルにより、サーベイランスとコントロールの取り組みを改善することで、広く適用されるNPIを緩和できる可能性が指摘された。例えば、モデル研究では、従来のコンタクトトレーシングとデジタルコンタクトトレーシングは、ロックダウン措置が緩和された場合に、ウイルスの拡散を遅らせる可能性があることが示された(36,37)。別の研究では、SARS-CoV-2 の検査頻度と報告速度を上げることは、高感度検査と遅い報告タイムラインだけに頼るよりも、ウイルスの拡散を抑えるのに有効であることが分かった (38, 39)。いくつかのモデル研究では、NPI緩和の異なるタイムラインに伴うトレードオフと、NPI効果の不確実性と実施エラーが、NPIを使用することで疾患の広がりを最適に制御する我々の能力を妨げる可能性があることを強調している(40, 41)。
波を乗り切る
最初の感染の波は、1918年のインフルエンザの大パンデミック後に見られたような、その後の波となった(42)。感染の波が起こる要因としては、ウイルスの進化的変化と宿主の免疫や行動の変化が挙げられる。
理論的には、人獣共通感染症の病原体が持ち込まれた直後は、ウイルスの適応によりヒトの間での感染が増加することが予測される。2020年3月から5月にかけて、D614G変異株(スパイクタンパク質の614位のグリシン残基(G)がアスパラギン酸残基(D)に置き換わったもの)が急速に広がったことは、ウイルス適応が起こった可能性を示唆している(43)(図3A)。この置換がウイルスの適応を反映していることは、この変種がヒト気管支および鼻気道上皮細胞培養において複製を増強し、またハムスターおよびフェレットの生体内感染において複製および感染性を増強したことを示す実験によって裏付けられた(44)。英国における集団レベルのSARS-CoV-2配列データの定量的解析でも、ヒトにおけるD614Gの感染優位性が検出された(45)。
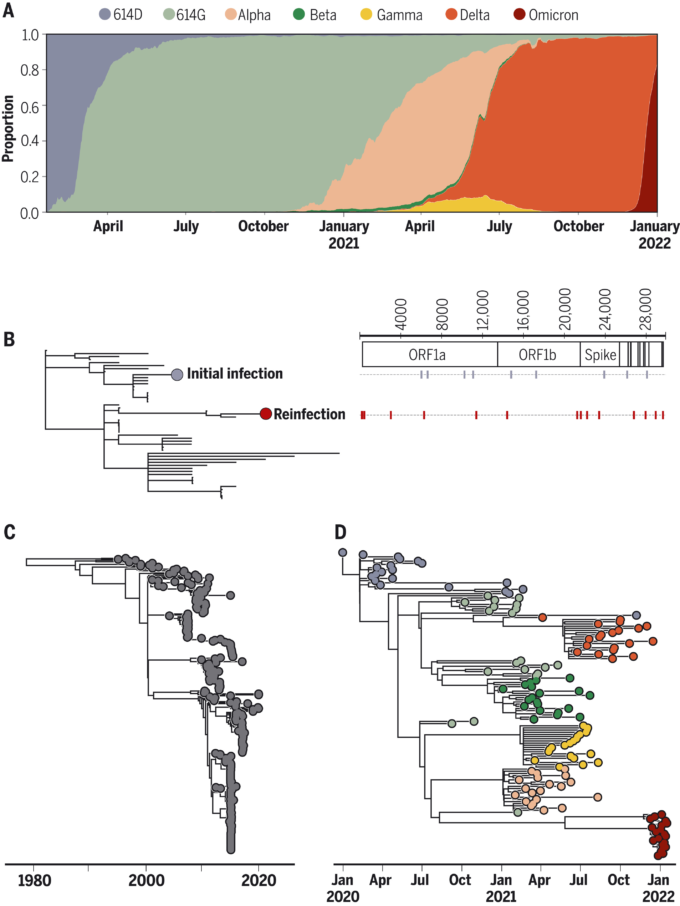
図3 コロナウイルスの配列データは、SARS-CoV-2の疫学的理解に役立っている(A)SARS-CoV-2の懸念される変異株の頻度を経時的に示す。SARS-COV-2がヒトに適応していることを示す最初の兆候は 2020年初頭に614D対立遺伝子が614G対立遺伝子に集団レベルで置き換わったことだ。Y軸の変異株頻度は、GISAID(Global Initiative for Sharing Avian Influenza Data)に寄託されたSARS-CoV-2の配列データに基づいて計算されている。世界的に流通している主要な変異系統のみが示されている。(B)SARS-CoV-2の再感染の証拠となるウイルス配列決定の一例。(48)の許可を得て複製した。循環しているウイルスの遺伝的変異と関連した患者からのサンプルは、観察された二次感染が潜伏感染の再活性化ではなく、再感染であることを示唆している。右の図は、一次感染と二次感染のウイルス試料に存在する置換を示したものである。ORF、オープンリーディングフレーム。(C) 季節性ヒトコロナウイルスOC43(系統A)の系統樹。系統解析により、このウイルス集団の抗原進化が指摘されている。(50)の許可を得て複製した。(D)SARS-CoV-2の配列データから推定した系統樹で、(A)に含まれる変異系統の間の進化的関係を示している。
パンデミック時の時間の経過とともに、自然感染による免疫が集団に蓄積される。SARS-CoV-2の場合、第一波の大きい地域では集団免疫によって今後の感染が大幅に抑制されることが当初期待された。集団を守るために必要な集団免疫のレベルは、およそ1 – 1/R0である(46)。R0を3とすると、SARS-CoV-2の推定値は67%となる。しかし、感染の不均一性により集団免疫の閾値は大幅に下がると理論づけられていた(47)。しかし 2020年8月の時点で、再感染の記録があり、SARS-CoV-2に対する免疫が一過性の感染防御にしかならない可能性が示された(図3B)(48)。この時期のパンデミック性ヒトコロナウイルス(HKU1,OC43,229E、NL63)の研究でも再感染を繰り返す証拠(49)や抗原進化(50,51)が見つかり(図3C)集団免疫によってパンデミックが急速に終息するという期待にはブレーキがかかることになった。
2020年後半にかけて、ウイルスの感染特性や免疫の持続期間について理解が深まる中、SARS-CoV-2感染者は波があり、国や同じ国でも地域によってピークが異なることが判明した。このような発生率の時間的変化の原因は、NPIの変化、行動の変化、天候や休日の影響による季節的変化、自然感染による感染抑制型免疫の発達とその衰退など、様々な要因が複合的に作用した結果であると思われる。これらの要因の相互作用とその相対的な役割を定量化することは、SARS-CoV-2の長期的な動態を予測するために重要な研究分野である(52, 53)。
ワクチンと変異株
2020年12月までに、SARS-CoV-2に対するワクチンが開発され、治験が行われ、緊急用として承認されるという、ワクチン学の歴史上類を見ないタイムラインであった。このような重要な臨床試験が迅速に行われた背景には、疫学的要因があった。SARS-CoV-2に対する獲得免疫はほとんどなく,試験実施中の2020年半ばにはCOVID-19の発生率が高かったため,試験は予定よりも早く,事前に指定したエンドポイントに到達した。現在では広く知られているように、この試験はCOVID-19に対する優れた予防効果を示し、入院や死亡などの重篤な転帰を回避することができた。しかし、ワクチンの使用が許可された後も、疑問は残ったままであった(図4):防御効果はどのくらい続くのか?予防効果はどのくらい持続するのか、新型ウイルスに対する予防効果はあるのか。ワクチンは感染を防ぐことができるのか?無作為化試験は終了後も数カ月間データを収集し続けるが、コホートやケースコントロールデザインを含む観察研究は、これらのさまざまな側面から実際のワクチンの効果をモニタリングするために不可欠であった。
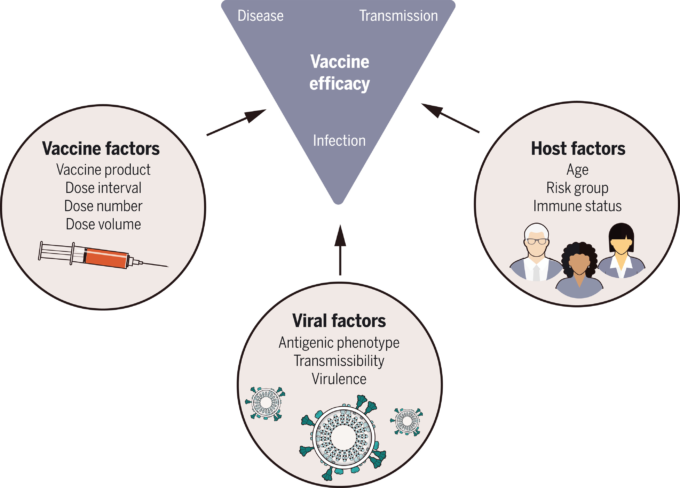
図4 ワクチンの有効性に影響を与えるワクチン,宿主,ウイルスの各因子について,臨床試験および導入後の観察研究において,ワクチン有効性のモデレータとなりうる要因として調査されたものを示す.シナリオモデリングでは,ワクチン接種が感染症や疾病,入院や死亡などの重篤な転帰にどのように影響するか,また,これらの影響が年齢などの宿主因子によってどのように異なるかについて,データに基づく仮定を組み込んで,集団レベルのワクチン効果を予測した。ワクチン接種の集団インパクトの主要な決定要因は、ワクチンの感染阻止効果と感染低減効果の組み合わせである感染に対する効果である。主に観察研究からデータが得られるにつれて、ワクチンによるブレークスルー症例の感染力に関する仮定がモデルに組み込まれるようになった。デルタ、そしてオミクロンの進化に伴い、変異株特有のワクチン効果やウイルスの免疫逃避の可能性を理解することが重要な数量となった。このようにワクチン接種の被接種者への影響に関するワクチン、宿主、ウイルスのデータが揃ったことで、疫学モデルはワクチン接種がSARS-CoV-2の集団レベルの伝播に及ぼす直接的、間接的影響を予測することができるようになった。
どのグループを最初にターゲットにするかなど、政策に関連する問題を含め、ワクチン接種に関する多くの決定は、こうした知識が得られる前に行わなければならなかったため、疫学的モデルは、異なる仮定の下で決定した場合の潜在的影響を調べる上で重要な役割を果たした。最初の疑問の1つは、2回接種シリーズのうち1回分をできるだけ多くの人に接種してカバー率を最大化するか、それとも2回接種(mRNAワクチンでは3~4週間の間隔)という試験プロトコルに忠実であり続けるか、ということであった。初回投与後10~14日目から明らかな防御効果を示した試験データをパラメータとしたモデリング研究では、短期的には、集団レベルで疾患を制限するためには1回投与戦略が望ましいと考えられることが示された(54)。しかし、長期的には、もし1回接種のワクチン効果が2回接種より大幅に低い場合、ウイルスの感染速度やワクチンの展開の早さによっては、2回接種の方が望ましいかもしれない。SARS-CoV-2が1回の接種で不完全な免疫を獲得し、免疫逃避を起こす可能性についての懸念も、定量的モデリングと推論によって解決された(54, 55)。初期の試験データとモデリングの結果に基づいて、英国は2回目の接種を試験間隔より遅らせる戦略を推進した。その結果、50歳以上で高いカバー率が急速に達成され、ワクチン接種後のパンデミックの波では、高い症例数が入院や死亡の傾向を並行させないというデカップリングが明白となった。この観察は、シナリオ・モデリング研究(56)で予測されたもので、重症化を防ぐというワクチンの価値を示している。実際、導入後の評価では、ワクチンは入院や死亡に対して90%程度の予防効果を示した(57, 58)。
ワクチンに関連する疑問は、ワクチン接種によってどの程度感染を減らすことができるのか、ということにまで広がった(図4)。ワクチンは、感染を予防することと、感染が成立した場合の感染力を弱めることの2つのメカニズムによって、感染を回避することができると考えられている。2021年半ばから後半にかけて行われたブレイクスルー観察研究では、疾病や重篤な転帰よりも程度は低いものの、感染に対する防御が証明された(58, 59)。また、いくつかの研究では、破局的感染を経験したワクチン接種者は、ウイルス量が少ないか、またはウイルスがより急速に減少し、その結果、おそらく後方への感染の可能性が少ないことを示した(60-62)[ただし(63,64)参照]。感染に対するワクチンの性能に関する最も包括的な理解は、感染阻止および感染阻止のメカニズムに関する洞察を提供する家庭での研究から得られる。そのような研究の1つは、突破口となる症例の感染力に対するワクチンの有効性を23%と推定している(65)。感染防御と組み合わせた場合、伝播の減少率は92%と推定された。
ワクチンに関する疑問は、ワクチン接種によってどの程度感染を減らすことができるのかという疑問へと広がっていった。
SARS-CoV-2ワクチンの有効性の評価を複雑にしていたのは、ワクチンが展開された時期に懸念される新しい変異株が進化していたことだ。2020年後半、B.1.1.7系統[現在、世界保健機関(WHO)の変種命名法ではアルファとして知られている]が検出され、英国で急速に広まった。この系統が持つ変異のいくつかは、アンジオテンシン変換酵素2(ACE2)への結合を強化するなど、ウイルスの表現型を大きく変え(66)感染性に影響を及ぼした(67)。ウイルスの配列データに基づいてアルファの選択的優位性を定量化すると、当時流通していた他の系統の1.5倍から2倍の再生産数を持つことが分かった(68)。
アルファ系統の出現後すぐに、別のウイルス系統であるB.1.617.2(その子孫系統とともに、懸念されるデルタ変種を構成する)が、インドでSARS-CoV-2の感染の大波を引き起こした(69)。この系統は急速にインドを席巻し、世界的に支配的となった。In vitroの分析では、回復期のヒト血清は祖先の系統よりもデルタに結合する効率が低く、デルタの方が複製効率が高いことが示された(70)。これらの知見と一致するように、あるモデル研究では、集団レベルでのデルタの成長の優位性は、デルタの高い感染性と、過去の感染によって生じた宿主の免疫反応に対する感受性の低下との組み合わせから生じることが分かった(69)。幸いなことに、導入後のワクチン効果調査により、アルファとデルタの両変種に対して、症候性疾患に対する防御がほぼ維持されることが分かった(58, 71, 72)。その後の研究により、感染や症候性疾患に対するワクチンの有効性は時間の経過とともに低下することが明確になり(73)特に高齢者にとってはワクチンの追加接種(ブースター)が有益であることが分かった(74)。
2021年11月、南アフリカの研究者は、∆69-70スパイク遺伝子欠失を保有するウイルス亜集団の拡大を示すS遺伝子標的不全(SGTF)を有するCOVID-19症例数の増加に気づいた。その後まもなく、全ゲノム配列解析により新たな変異型の存在が確認された。その変異プロファイルと南アフリカでの極めて急速な広がりから、WHOはこの変種を懸念すべきものとして指定し、オミクロン(B.1.1.529)と名付けた。2021年12月、この変種は世界中に急速に広がり、これまで以上に多くの感染が確認され(図1)デルタ変種と急速に入れ替わった(図3A)。Wuhan-Hu-1参照遺伝子型に対するオミクロンの変異プロファイルは、スパイク糖タンパク質に30以上の変異があり(75)その多くが免疫逃避を可能にすると予測されている。初期の研究では、オミクロンは過去の感染やワクチン接種による抗体を回避する能力があることが確認され(76)上気道の細胞への感染能力を向上させる別の細胞侵入経路を用いることができることが示された(77)。さらに、動物モデルでは、オミクロンへの感染は、以前の変異株への感染よりも臨床的に重症化しない可能性が示された(78)。実験的な予測は、疫学研究でも実証され、オミクロンはデルタと比較して、既感染者への再感染性に優れ(79)臨床的な重症化も少ないことが示されている(80)。それにもかかわらず、オミクロンの急速な拡大により、多くの国でこれまでに確認されたSARS-CoV-2感染の最大の急増をもたらし、ウイルスに起因する死亡の急増も続いている。しかし、重症化や死亡に対するワクチンの効果は新型でも高く、オミクロンを原因とする死亡はワクチン未接種の人に集中している。
オミクロンとその前のアルファの出現は、遺伝的に異なる新しい変異株の発生源に関する進化上の重要な問題を提起している。SARS-CoV-2がヒトの集団の中で進化する速度を考えると、両変種は出現時に予想されるよりも多くの突然変異を有していた。オミクロンは、他のSARS-CoV-2変異株と進化的に遠い関係にあることが注目される(図3D)。SARS-CoV-2は多くの家畜や野生動物で観察されており(逆人獣共通感染症の結果として)これらの新しい変異株はこれらの代替宿主で進化し、再びヒト集団に流出した可能性がある。あるいは、これらの変種は、慢性的なSARS-CoV-2感染で適応進化が起こりうるという記録的な例から、免疫不全者や免疫抑制者において進化したのかもしれない(81)。このことは、懸念される変異株を早期に特定し、懸念される変異株が蔓延する前に特定し阻止するための、より包括的なモニタリング戦略の必要性を示している。
今後の展望
SARS-CoV-2は、パンデミック開始以来、制御が難しく、最近のオミクロンの広がりは、この課題を増幅させるばかりである。SARS-CoV-2がヒトの間で常在菌として定着することは避けられない。しかし、その健康や日常生活への影響は、時間の経過とともに大きく変化していくだろう(82)。政府や公衆衛生担当者は、SARS-CoV-2に対処する長期的な戦略に移行しなければならない。ワクチンと、病気の進行を防ぐための外来治療を含む治療薬は、非常に価値のある手段である。しかし、ワクチン接種が普及し、過去の感染の波がある地域でも感染レベルが高く、このウイルスの将来の疫学的影響について多くの未解決の問題が残っているため、今後の課題は手ごわいままである。
SARS-CoV-2の最も進化的に成功した変異型は、より祖先的な変異型と比較して、より高い伝播性を持つように進化している。高い感染力はより多くの感染をもたらすが、感染やワクチン接種による集団レベルの免疫の増加は、健康への影響という点ではこれらの感染をそれほど深刻なものにしないかもしれない。しかし、ウイルスが直面する進化的圧力、ひいては適応進化のパターンが変化することになる。オミクロンのように、免疫を回避することで感染優位性を獲得する変異株が、季節性インフルエンザのように主流になる可能性もある。
SARS-CoV-2の病原性の進化は、それがどの程度有害か、あるいは致命的かという点で、パンデミックの初期から議論の的となっている(83)。進化論では、毒性の低い方への進化を期待すべきではないと指摘されており(84)、懸念されていた過去2つの変異型は、SARS-CoV-2の毒性の進化に明確で一貫した傾向がないことを実証している。デルタは以前の変異株よりもやや強毒性であると考えられているが、オミクロンはそれほどでもない。SARS-CoV-2の毒性は時間とともに(容易に予測できない方向に)進化する可能性があるが、感染致死率は人口免疫の上昇など他の理由によって低下すると考えられる。上述のように、利用可能なSARS-CoV-2 mRNAワクチンは、ブレークスルー感染が発生した場合でも、重症化に対する防御を提供する。ワクチンブースターが、重症化からの保護にさらに役立つだろう。モノクローナル抗体と抗ウイルス剤は、症状発現後すぐに服用することで、同様に重症化と死亡のリスクを減らすことができる。長期的には、集団免疫の結果、初感染の年齢が若くなり、感染の平均的な重症度が下がり、後年の感染も軽度になると思われる。季節性コロナウイルスは、通常、人生の非常に早い時期に感染し、既存の免疫のために二次感染は一次感染より軽いという類似点がある(85)。
一歩下がって
このパンデミックの複雑さを反映して、この2年間で最も差し迫った科学的な疑問が変化している(図1)。初期の疑問は、新種の病原体をその病原性と感染性に関して地図上に配置することに焦点が当てられていた。モデリングの前提は、SARS-CoV-1やMERS-CoVの経験、そして限られた数のSARS-CoV-2のデータセットに大きく依存している。時間の経過とともに、我々は広範な仮定を、より深い理解に置き換えていった。ウイルスの急速な拡散と爆発的な感染の波が生じたため、迅速な対応が必要となり、問題は短期的なものから長期的なものへと変化していったのである。安全で効果的なワクチンの開発により、我々は大きな前進を遂げたが、新型インフルエンザや免疫力の低下により、感染の抑制に対する我々の期待も薄れつつある。今後、このウイルスが人類にどのように適応していくのか、また、パンデミックした場合の健康への影響など、重要な問題が残されている。この病原体を研究する科学者としての仕事はまだ終わっていないが、より安全で健康的な世界を目指すという共通の使命のために、これまで達成されたすべての成果を認めるものである。

