The beneficial effects of nutraceuticals and natural products on small dense LDL levels, LDL particle number and LDL particle size: a clinical review
www.ncbi.nlm.nih.gov/pmc/articles/PMC7149933/
要旨
心血管疾患(心血管疾患)は世界的に罹患率と死亡率の主要な原因となっている。SDLDLレベルは独立した危険因子であり、冠動脈疾患やメタボリックシンドロームの評価において総LDL-Cよりも高い予測値を示している。
機能性食品素材は、脂質異常症を管理し、その後の心血管疾患やメタボリックシンドロームを改善するために大きな注目を集めている。しかし、これらの生理活性天然化合物のsdLDL値への影響を検討した研究は現在までにない。そこで、本レビューの目的は、オメガ3系多価不飽和脂肪酸などの特殊な食事成分、栄養補助食品、生薬がsdLDL値、LDL粒子数、LDL粒子径に及ぼす影響について、これまでに得られたエビデンスをまとめることである。
本レビューでは、既存の臨床試験の結果から、薬用植物、栄養補助食品、オメガ3脂肪酸などの天然物を補助的または補完的な治療薬として使用することで、sdLDLレベル、LDL粒子数、LDL粒子径を減少させ、その後、これらの天然物は一般的に安全で、入手しやすく、安価であるという利点を生かして、心血管疾患の予防・治療に利用できる可能性があることを示唆している。
キーワード フィトケミカル、薬用植物、栄養、リポタンパク質、動脈硬化、スモールデンスLDL
序論
心血管疾患(心血管疾患)は世界的な問題であり、罹患率と死亡率の主要な原因である[1]。心血管疾患sによる死亡の有病率は、2030年までに2,360万人を超えると予測されている[2]。不健康な食生活、運動不足、糖尿病、脂質異常症、高血圧など複数の危険因子が心血管疾患の修飾因子と考えられている[3]。心血管疾患の進行とアテローム性動脈硬化リスクの増加は脂質異常症と正の関係があることはよく知られている。したがって、脂質プロファイルの最適なレベルは、アテローム性動脈硬化プロセスを減少させるために重要な役割を果たしている[4]。
LDL-Cは、サイズ、密度、脂質組成および物理的特性が異なる分子の不均一なグループから構成されるリポ蛋白質の一種である。より小さくて密度の高いLDL粒子は酸化されやすく、動脈壁の内皮を透過しやすいため、心血管疾患の動脈原性危険因子と考えられている[5, 6]。大きな浮力のあるLDL粒子(直径25nm以上)は表現型パターンAと考えられ、サイズ19.0~20.5nmの小さくて密度の高いLDL粒子は表現型パターンBと考えられている[7-9]。トリグリセリドが高く、HDL-C濃度が低い個体とLDLパターンBとの間には、メタボリックシンドロームの特徴である正の関連性が確立されている[10]。小密度低密度リポ蛋白質(sdLDL)粒子は、その化学的含量の変化によって特徴づけられるLDLの一部分であり、コレステロールとコレステロールエステルを含まず、リン脂質含量が減少する一方で、トリグリセリド含量は変化しない[11]。VLDL粒子は、最初にリポ蛋白リパーゼ(LPL)酵素によってLDLクラスIIIおよびIVに変換される。その後、肝リパーゼ(HL)の助けを借りてコレステリルエステル転送タンパク質(CETP)の酵素は、sdLDL粒子のレベルの増加につながるsdLDL粒子にTGを転送する。低TGレベルでは、VLDL粒子は中密度リポタンパク質(IDL)および大LDLサブクラスに変換される(図1)[5,12]。これまでの研究では、sdLDLレベルは独立した危険因子であり、冠動脈疾患[13,14]およびメタボリックシンドローム[15]の評価において総LDL-Cよりも予測性が高いことが示されている。Association of Clinical Endocrinologists(AACE)のガイドラインでは、LDL粒子径やsdLDLよりもLDL粒子数の方が心血管疾患イベントを予測するための強力なツールであることが推奨されている[10]。全体的に、脂質プロファイル(LDL-C、トリグリセリド、HDL-C、コレステロール)とともにsdLDLまたはLDL粒子数を測定することは、心血管疾患の評価および管理に有用であると考えられる[10,18]。
図1 内因性脂質代謝の経路と、アテローム性リポ蛋白質と抗アテローム性リポ蛋白質の経路の模式的なまとめ
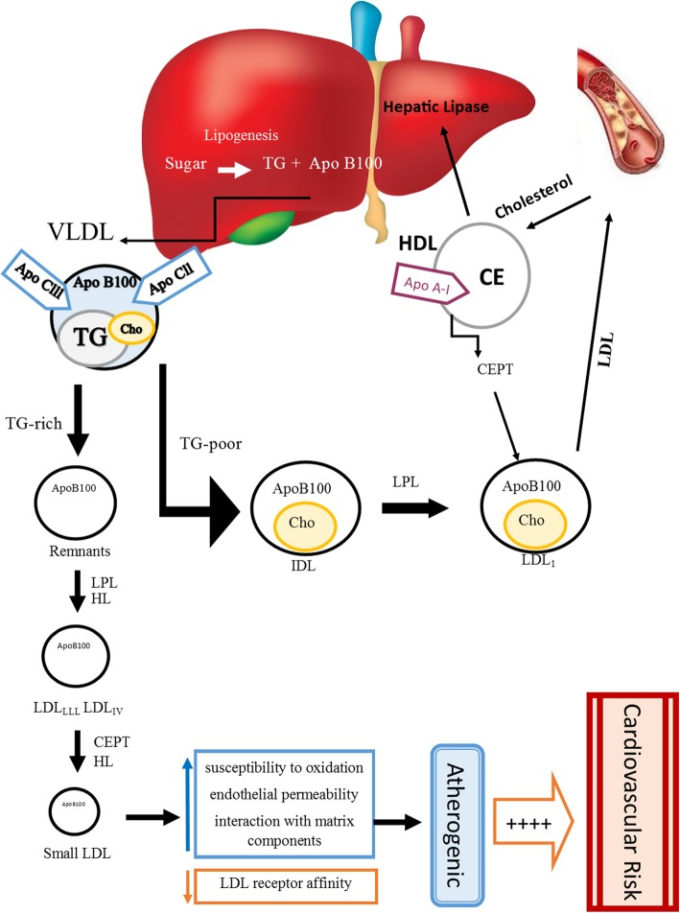
sdLDL:小密度低密度リポ蛋白、Apo:アポリポ蛋白、VLDL:超低密度リポ蛋白、IDL:中間密度リポ蛋白、LDL:低密度リポ蛋白、LDL-R:低密度リポ蛋白受容体、HDL:高密度リポ蛋白、TG:トリグリセリド、CE:コレステリルエステル、+:リスク増加
心血管疾患リスクを低減するための最も重要な治療目標の一つは、sdLDL-Cレベルを改善することである[18]。健康的な食生活を重視した生活習慣の変化は、脂質プロファイルのアテローム性を低下させる上で重要な役割を果たす可能性がある[19-21]。機能性食品素材は、脂質異常症を管理し、その後の循環代謝の健康を高める天然物として注目されている[22-28]。脂質異常症の非薬理学的管理として栄養補助食品や漢方薬が研究されてきたが[29-35]、これらの生理活性天然化合物がSDLDLを改善して心血管疾患の相対リスクを低下させる効果については、より明確な解明が必要である。現在までに、これらの生理活性天然化合物のsdLDL値への影響を検討した研究はない。そこで、本レビューの目的は、n-3多価不飽和脂肪酸、栄養補助食品、生薬などの特殊な食事成分がsdLDLレベル、LDL粒子数、LDL粒子径に及ぼす影響について、これまでに得られたエビデンスをまとめることである。
検索戦略
本ナラティブレビューは、PRISMAガイドラインに基づいて行った。PubMed、Web of Science、Google Scholar、Scopusのデータベースを2019年8月までに検索し、英語に限定した。検索戦略は、タイトル要旨に以下のキーワードを含めた:(薬用植物 OR ハーブバイオアクティブ OR 生物活性天然化合物 OR 栄養補助食品);AND(無作為化 OR ランダム化 OR 無作為化 OR 「無作為化対照試験」 OR 「無作為化試験」 OR 「無作為化試験」 OR 「乱数」 OR プラセボ)AND(小密度低密度リポ蛋白 OR sdLDL OR 「LDL粒子数」 OR 「LDL粒子径」 OR 「LDLサブフラクション」)。
植物ステロールと植物油
フィトステロール(植物ステロールとスタノールエステル)は、がん、心血管疾患、糖尿病などのいくつかの慢性疾患の発症を予防することが報告されている[36-39]。以前のメタアナリシスの結果では、フィトステロールは脂質プロファイルレベルを改善する可能性があることが示されている[40-42]。フィトステロールは酸化LDLを減少させる可能性があり、LDLのアテローム性修飾と考えられる。クロスオーバー対照試験では、25名の健康な男性ボランティアを対象に、2週間のウォッシュアウト期間を挟んで、ポリフェノール含有量の少ないオリーブオイル(LPCOO; 366mg/kg)またはポリフェノール含有量の多いオリーブオイル(HPCOO; 2.7mg/kg)を3週間、25mL/日の生のまま摂取してもらった。試験終了時に、ベースラインおよびLPCOO群と比較して、HPCOO介入により、LDL小粒子の有意な減少が認められた。逆にベースラインと比較して、LPCOOはLDL小粒子を有意に増加させた[43]。試験研究では、メタボリックシンドローム患者108人を、4gのフィトステロールを含む植物ステロール強化ヨーグルトミニ飲料、またはフィトステロールを含まないヨーグルト飲料(コントロール)の2つのうちの1つを受けるように無作為に割り付けた。2ヶ月間の介入後、フィトステロール補給は対照群と比較して介入群のsdLDLレベルを有意に低下させた[44]。別の研究では、4.5~15.9歳の59人の子供を2つのグループに分けた。(i) LDL-C≧130 mg/dlの25人の被験者に、2gの植物ステロールを濃縮したヨーグルトドリンクを6~12ヶ月間摂取させた群(介入群)または(ii) LDL-C<130 mg/dlの34人の被験者(対照群)であった。その結果、介入群では、植物ステロールの摂取により、SDLDLが変化なしの対照群と比較して減少することが示された[45]。以前の研究では、56人の健康な参加者が2週間、飽和脂肪を多く含む食事を摂取し、その後、精製オリーブ油、菜種油、またはヒマワリ油を主な脂肪源として4週間、3つの食事介入群のうちの1つに無作為に割り付けられた。その結果、オイルダイエット段階では、群間の差は有意ではなかったが、LDLサイズが有意に減少し、オイルの消費はLDLサイズの変動を有意に変化させなかったことが示された[46]。最近の報告では、健康な被験者40人を250ml中に2.23gのイノシトールを含むイノシトール富化飲料(IEB)またはショ糖加糖飲料(SB)を1日2回、12週間飲むように無作為に割り付けた。この研究では、IEB群の被験者は、SB群と比較してLDL粒子径が有意に増加したことが示された[42]。Shresthaらは、33人の健康な成人を治療用クッキー(7.68g/dのサイリウムと2.6g/dの植物ステロール)とプラセボクッキー(0gのサイリウムと植物ステロール)に4週間(それぞれ3週間のウォッシュアウト期間で区切られている)割り付けた無作為化クロスオーバー試験を実施した。試験終了時に、サイリウムと植物ステロールのクッキーは中小のLDL粒子を減少させ、プラセボと比較して平均およびピークLDL粒子径を著しく増加させた[47,48]。無作為化二重盲検臨床試験では、LDL-C値≧3.33mmol/Lの成人54人を2群に無作為化し、1日4カプセルのフィトステロールエステル(2.6g/日フィトステロールエステル)またはプラセボ(キャノーラ油)を12週間投与した。試験終了時には、LDLの割合、平均およびピークLDL粒子径はグループ間で差がなかった[49]。Matvienkoらは、中等度高コレステロール血症および高トリグリセリド血症の男性34人を無作為に2群に分け、ステロールエステルを67%、遊離ステロールを33%含むフィトステロールを2.7g含むひき肉を摂取する群と、対照群としてひき肉のみを摂取する群に分けた臨床試験を実施した。介入の4週間後には、対照群と比較してフィトステロール処理群で平均LDL粒子数が減少する傾向があったが、LDL粒子の小粒径およびLDLピーク粒子径に関しては群間で差はなかった[50]。別の試験では、家族性複合高脂血症(FCHL)でトリアシルグリセロールが上昇した28人の参加者が、1日2.5gの植物性スタノールエステルを濃縮したマーガリン、または対照としてスタノールを含まないマーガリンを3週間摂取した。試験の2週間前と期間中、コレステロール低下薬は使用しなかった。スタノール補充後の試験終了時に、総LDL粒子数は減少したが、sdLDL粒子はベースラインと比較して差はなかった[51]。Utarwuthipongら[52]はまた、高脂血症の女性16人を対象とした研究を報告している。この女性は、8週間のベースラインの食事としてNational Cholesterol Expert Panelの食事療法(炭水化物55%、タンパク質15%、脂肪30%、コレステロール300mg/日未満)を推奨されていた。その後、参加者全員を4つの治療群に無作為に割り付け、食事療法+SBO(大豆油、総エネルギーの20%)食事療法+RBO(米ぬか油、総エネルギーの20%)食事療法+PO(パーム油、総エネルギーの20%)食事療法+RBO/PO((3:1)RBO/POの混合物として総エネルギーの20%)のいずれかを摂取させた。10週ごとに別のグループにクロスオーバーさせたので、合計48週参加した。順次超遠心分離法を用いてsdLDL粒子を測定した。その結果、SBOとRBO/POは有意にsdLDL-コレステロール値を低下させたが、POは有意にsdLDL-コレステロール値を上昇させ、RBOは対照食と比較して差がなかった(表1)。全体的に、ここで検討したほぼすべての研究において、植物油と植物ステロールはsdLDLコレステロール値とLDL粒子径に対して有望な効果を示した。6件中4件の研究では、植物油と植物ステロールの介入後にsdLDLが減少し、4件中2件の研究では介入後にLDL粒子径が増加した。sdLDLが減少しなかった2研究と、LDL粒子径が変化しなかった1研究では、LDL粒子数が有意に減少した。
表1 小密度低密度リポ蛋白質(LDL)の血漿中濃度、LDL粒子数、LDL粒子径に及ぼす植物ステロールと植物油の影響
| 著者、年 | 介入 | 1日あたりの用量 | 治療期間 | 科目 | 評価の方法 | 主な成果 | LDLに対する特定の食事成分または栄養補助食品の最終効果(数、サイズ、濃度) |
|---|---|---|---|---|---|---|---|
| Hernáezetal。2015 [ 43 ] | オリーブオイル | 25 mL / d生LPCOO; 366mg / kgまたはHPCOO; 2.7 mg / kg) | 3週間 | 25人の健康なボランティア男性 | NMR分光法 | HPCOOは小さなLDL粒子を大幅に減少させた(-15.3%)LPCOOは小さなLDL粒子を大幅に増加させた(+ 13.6%)グループ間の違いは重要でした | 小さい高密度LDL ↓ |
| Sialvera etal。2010 [ 44 ] | 植物ステロール | 4g /日 | 2ヶ月 | 108人のメタボリックシンドローム患者 |
sLDL e EX 「セイケン」 |
植物ステロールの補給は、対照群と比較して、介入群の小さな高密度LDLレベル(-3.9mg / dl)を有意に減少させた | 小さい高密度LDL ↓ |
| Garoufi etal。2014 [ 45 ] | 植物ステロール | 2g /日 | 6〜12か月 | 59人の高コレステロール血症および正常な子供(4.5〜15.9歳) | キット(sLDL-EX「SEIKEN」 | 植物ステロールの消費は、介入群のsdLDLを大幅に減少させたが、レベルは対照群よりも高いままでした。 | 小さい高密度LDL ↓ |
| Kratz etal。2002 [ 46 ] | 植物油 | 精製オリーブオイル、菜種油、ひまわり油 | 4週間 | 56人の健康な成人 | ページ | 植物油に反応して、LDLサイズは大幅に減少し(-0.36 nm)グループ間の違いは重要ではないと考えられた。さらに、オイル消費量はLDLサイズの変動を大きく変化させませんでした | LDL粒子サイズ— |
| Banuls etal。2015 [ 42 ] | IEB、SB | 4.45g /日 | 12週間 | 40人の健康な成人 | ページ | IEBは、ベースラインおよびSBと比較してLDL粒子サイズ(0.13 nm)の有意な上昇をもたらした。 | LDL粒度↑ |
|
Shrestha etal。2006 [ 48 ] 2007 [ 47 ] |
トリートメントクッキー、 プラセボクッキー |
トリートメントクッキー; 7.68 g / dオオバコと2.6g / d植物ステロール、または プラセボクッキー; 0gのオオバコと植物ステロール |
3ヶ月 | 33人の健康な成人 | 非勾配、高分解能PAGEおよびNMR | オオバコと植物ステロールは、プラセボと比較して、中小LDL粒子(-18.9±0.7 nmol / L)が減少し、LDL平均サイズ(+ 0.11±0.04nm)とLDLピークサイズ(+ 0.2±0.15nm)が大幅に増加した。 。 |
中小LDL粒子↓ LDL粒度↑ |
| アーネストら。2007 [ 49 ] |
植物ステロールエステル、 カノーラオイル(プラセボ) |
2.6g /日 | 12週間 | LDL-Cレベルが3.33mmol / L以上の成人54人 | 既知の直径の4つの血漿標準の相対移動を使用して、LDL粒子サイズを推定した。各スキャンの主要ピークの推定直径は、LDLピーク粒子サイズとして識別された | LDLの割合、平均およびピークLDL粒子サイズは、両方のグループで変化しなかった。 | LDL粒子サイズ— |
| Matvienko etal。2002 [ 50 ] |
牛ひき肉とフィトステロール、 コントロール(牛ひき肉のみ) |
2.7gの植物ステロール | 4週間 | 血漿TCおよびLDLコレステロールが上昇した34人の男性 | 非変性PAGEおよびNMR | 小さなLDL粒子とLDLピーク粒子サイズに大きな変化はない。しかし、平均LDL粒子数は対照よりも減少した。 |
小型高密度LDL— LDL粒子サイズ— LDL粒子数↓ |
| Theuwissen etal。2009 [ 51 ] | スタノールサプリメント | 2.5g /日の植物スタノール | 3週間 | 28 adults with elevated triacylglycerols | NMR by Liposcience | After stanol supplementation the number of total LDL particles decreased, but sdLDL particles did not significantly change compared with baseline. |
Small dense LDL — LDL particle number ↓ |
| Utarwuthipong er al 2009 [52] |
SBO; RBO; PO; mixture of (3:1) RBO/PO |
20% of total energy as SBO; 20% of total energy as RBO; 20% of total energy as PO; 20% of total energy as mixture of (3:1) RBO/PO. |
10 weeks | 16 hypercholesterolemia women | Sequential ultracentrifugation technique | SBO and RBO/PO significantly reduced sdLDL-cholesterol level (− 10%) and (− 5%) respectively, though PO significantly increased sdLDL-cholesterol level (+ 5%) and RBO was not significantly varied, differences between groups were significant. | Small dense LDL ↓ |
sdLDL 小密度低密度リポ蛋白質、LDL-C 低密度リポ蛋白質コレステロール、TC 総コレステロール、LPCOO 低ポリフェノール含有オリーブオイル、HPCOO 高ポリフェノール含有オリーブオイル、PAGE ポリアクリルアミドグラジエントゲル電気泳動。NMR 核磁気共鳴、IEB イノシトール富化飲料、SB スクロース甘味飲料、SBO 大豆油、RBO 米ぬか油、PO パーム油、mg/dl ミリグラム/デシリットル、nmol/l ナノモル/リットル、nm ナノメートル
エイコサペンタエン酸とドコサヘキサエン酸
α-リノレン酸(ALA)由来のエイコサペンタエン酸(EPA)とドコサヘキサエン酸(DHA)は、内因性に作ることができないため、細胞膜の安定性に関与する食事由来の必須脂肪酸ファミリーの一つである[53]。EPAやDHAはNAFLD[54]、糖尿病[55]、心血管疾患[56,57]の治療に有益な効果があることが示唆されている。しかし、n-3脂肪酸がLDLの酸化感受性を高めるかどうかについては、データはまだ確定的ではないが懸念されている[58-60]。比較研究では、1.9~2.2gのEPAと1.1gのDHAを含む5g/日の魚油サプリメントを健康な成人210人に6週間投与した。介入後の時点では、ベースラインと比較してLDL粒子径に有意な変化は見られなかった[61]。Oelrichらは、中等度高トリグリセリド血症の60人の被験者を無作為に4群に分け、大豆油サプリメントを対照群として、3つの製剤((i)90%TG製剤、(ii)60%TG製剤、(iii)0%TGエチルエステル)で4g/日の魚油サプリメントを摂取させた臨床試験を行った。LDL粒子は、勾配ゲル電気泳動により評価した。12週間の介入後、すべての魚油群において、LDL1,LDL2,LDL3の4つの粒子径は、LDL4の濃度に差はなかったが、ベースラインと比較して有意に増加した[62]。二重盲検プラセボ対照試験では、中等度高コレステロール血症の糖尿病患者42人にコーンオイルカプセル(4g/日)を4週間投与した後、無作為に2群に分けて、魚油錠(EPAとDHAを2.6g、ビタミンEを13.4mg加えたもの)またはコーンオイル錠(コーンオイル1g、ビタミンEを13.4mg加えたもの)を1日4回摂取させた。この試験の結果、EPA/DHA介入群では対照群と比較してsdLDL粒子に有意な変化は認められなかった[63]。無作為化クロスオーバー試験では、高血圧の成人20人が魚油4カプセル(1日4g)またはコーン油タブレットをプラセボとして6週間摂取した結果、魚油群でLDLサイズ(+0.16nm)が増加した[64]。別の臨床試験では、脂質プロファイルが正常な健康な121人が、600mg/日のEPA、1800mg/日のEPA、600mg/日のDHA、または比較対照として使用した6g/日のオリーブオイルを摂取するように無作為に割り付けられた。6週間のサプリメント投与後、sdLDLは4つのグループ間およびグループ内で変化しなかった[65]。Satohら[66]は、メタボリックシンドロームの危険因子が2以上の肥満者44人を、食事+1.8g/日EPAを3ヵ月間摂取する群(介入群)と食事のみの群(対照群)の2群に無作為に割り付けた。食事は日本動脈硬化学会ガイドラインに準拠したもので、多価不飽和脂肪酸、一価不飽和脂肪酸、飽和脂肪酸として、それぞれ3:4:3の比率で、総エネルギーの60%を炭水化物、15~20%をタンパク質、20~25%を脂肪として摂取するようにした。また、1日の食事は理想体重25kcal/kgを基準とした。その結果、ベースラインと比較してEPA群ではsdLDLとsdLDLの割合が有意に減少したが、両群間で差はなかった。別の研究では、軽度高コレステロール血症の過体重成人59人を無作為に割り付け、毎日4gのEPAを摂取する群と、比較対照としてDHAまたはオリーブオイルを6週間摂取する群に分けた。LDL粒子径には群間および群内で有意差はなかった;しかしながら、ベースライン値を調整した後、オリーブオイル(プラセボ)と比較して、DHA群ではLDL粒子径が有意に増加した(0.25±0.08nm)[67]。健康な男性または軽度高脂血症の男性34名を対象に、2つのグループに無作為に割り付けた研究では、以下のような結果が得られた。(i) 7.5g/日DHA(~3g/日DHA)(ii) 7.5g/日オリーブオイル(コンパレータ)。介入の90日後、DHAを消費した参加者は、ベースラインと比較して平均LDL粒子の有意な増加があったが、これはコントロールと比較して差はなかったが、密度の小さなLDL粒子が少なかった[68]。別の臨床試験では、HDLの平均値以下の57人の被験者に、DHAカプセル(1日1.52gのDHA)または対照群としてオリーブオイルカプセルを6週間投与した。その結果、DHAは対照群と比較して、小密度LDL中のコレステロールの割合が有意に減少したが、SDLDLには影響がないことが明らかになった[69]。別のクロスオーバー試験では、15名の健康な成人男性を2群に無作為に割り付け、亜麻仁油10g(α-リノレン酸5.49g)またはコーン油10g(α-リノレン酸0.09g)をプラセボとして12週間摂取させた。その結果、介入群では、ベースラインと比較して、亜麻仁油を4週間、12週間摂取した後、sd-LDL濃度が有意に低下した(それぞれ-25.8%、-21.2%)。また、SD-LDL濃度は4週間後に対照群と比較して有意に低下した[70]。冠動脈性心疾患が知られていない56人の患者を対象とした研究では、亜麻仁油5.2g(ALAの3g/d)または対照としてオリーブ油5.2gを1日あたり26週間摂取するように割り付けられた。試験終了時には、亜麻仁油は、アテローム性LDLサブフラクション(LDL3とLDL4)には影響を与えなかったが、アテローム性の低いLDLサブフラクション(LDL1とLDL2)は、対照のオリーブオイルと比較して有意に増加した[71](表2)。全体的に、ここで検討された5つの研究のうち3つの研究では、介入後にLDL粒子径が有意に増加した;しかしながら、6つの研究のうち2つの研究では、他の研究では有意な変化は認められなかったが、sdLDLは有意に減少した。
表2 小密度低密度リポ蛋白質(LDL)の血漿中濃度、LDL粒子数、LDL粒子径に及ぼすエイコサペンタエン酸およびドコサヘキサエン酸(EPA&DHA)の影響
| 著者、年 | 介入 | 1日あたりの用量 | 治療期間 | 科目 | 評価の方法 | 主な成果 | LDLに対する特定の食事成分または栄養補助食品の最終効果(数、サイズ、濃度) |
|---|---|---|---|---|---|---|---|
| Ouellette etal。2014 [ 61 ] | 魚油の補給 | 5g /日 | 6週間 | 210人の健康な成人 | 2〜16%ページ | n-3 PUFA補給は、血漿LDL-C濃度とLDL粒子サイズに影響を与えなかった | LDL粒子サイズ— |
| Oelrich etal。2013 [ 62 ] | 魚油サプリメント、大豆油サプリメント(プラセボ) | 4g /日(800mg EPAおよびDHA) | 12週間 | 60人の高トリグリセリド血症の成人 | 勾配ゲル電気泳動 | ベースラインと比較して、LDL 1(+ 20±5%)LDL 2(+ 64±13%)およびLDL 3(+ 26±6%)の4つの粒子サイズは、すべての魚油グループで大幅に増加した。 | LDL粒度↑ |
| Petersen etal。2002 [ 63 ] | 魚油サプリメント、コーン油サプリメント(プラセボ) | 4g /日(2.6gのEPAとDHA + 13.4mgのビタミンE) | 8週間 | 中等度の高トリグリセリド血症の42人の糖尿病患者 | 超遠心分離 | 小さな高密度LDL粒子は、対照群と比較して有意に変化しなかった。 | 小さな高密度LDL |
| 鈴川ほか 1995 [ 64 ] | 魚油、コーン油(プラセボ) | 4g /日(3.4gのn-3) | 6週間 | 高血圧の成人20人 | ND | 魚油はベースラインと比較してLDLサイズ(+ 0.16 nm)を増加させた。 | LDL粒度↑ |
| Asztalos etal。2016 [ 65 ] | EPA、DHA、オリーブオイル(プラセボ) |
EPA600mg /日 EPA 1800mg /日 DHA 600mg /日 オリーブオイルプラセボ6g /日 |
6週間 | 正常な脂質プロファイルを持つ121人の健康な個人 | デンカ生研株式会社(LDL-CおよびsdLDL-C、東京、日本) | 4つのグループすべてで、sdLDL-Cに有意な変化はない(p = 0.82) | 小型高密度LDL— |
| 佐藤ほか 2007 [ 66 ] | EPA | 1.8g /日 | 3ヶ月 | メタボリックシンドロームの44人の肥満患者 | Quantimetrixリポタンパク質LDLシステム(LDL3–7:sdLDL) | sdLDL(-5 mmol / l)およびsdLDL比率(-1.27%)は、ベースラインと比較してEPAグループで有意に減少したが、2つのグループ間に有意差はなかった。 | 小さい高密度LDL ↓ |
| 森ら 1999 [ 67 ] |
EPA、 DHA、 オリーブオイル(プラセボ) |
4g /日 | 6週間 | 軽度の高コレステロール血症の59人の太りすぎの成人 | 市販の3〜13%非変性ネイティブゲルを使用 | グループ間およびグループ内のLDL粒子サイズに統計的に有意な差はなかった。 | LDL粒子サイズ— |
| ケリー等。2007 [ 68 ] |
DHA、 オリーブオイル(プラセボ) |
7.5 g / d DHAオイル(〜3 g / d DHA)または7.5 g / dオリーブオイル | 90日 | 34人の健康なまたは軽度の高脂血症の男性 | NMR | DHAを摂取した参加者は、小さな高密度LDL粒子の数が少なかった(21%)のに対し、変化はプラセボと比較して統計的に有意ではなかった。平均LDL粒子サイズは、ベースラインと比較して大幅に増加した(0.6 nmまたは3%)。 |
LDL粒度↑ LDL粒子数↓ |
| マキら 2005 [ 69 ] |
DHA、 オリーブオイル(プラセボ) |
1.52g /日DHA | 6週間 | HDLの平均レベルを下回る57人の被験者 | 垂直自動プロファイルII(VAP-II) | DHAは小さな高密度LDLに影響を与えなかった。さらに、小さな高密度LDLのコレステロール濃度のパーセンテージは、コントロールよりもDHAグループで有意に減少した(-9.7対-3.0%)。 |
小型高密度LDL— 小さな高密度LDLのコレステロール濃度↓ |
| 川上ほか 2015 [ 70 ] |
FO、 コーン油(プラセボ) |
10 g FO(5.49 g ALA) コーン油10g(ALA 0.09 g) |
12週間 | 15人の健康な男性 | sd-LDL-EX「SEIKEN」 |
介入群では、sd-LDLの濃度は、ベースラインと比較して、4週間後(-25.8%)および12週間後(-21.2%)に有意に減少した。 さらに、sd-LDL濃度は4週間後にプラセボよりも有意に減少した。 |
小さい高密度LDL ↓ |
| ハーパー等。2006 [ 71 ] | FOサプリメント、オリーブオイルカプセル(プラセボ) |
5.2 g / d FO(3 g / dのALA) または5.2gのオリーブオイル |
26週間 | 既知の冠状動脈性心臓病のない56人の患者 | 400回の連続分光光度測定によるコレステロールの酵素的測定による超遠心分離 | FOは、アテローム性LDLサブフラクション(LDLには効果がなかった3及びLDL 4)。しかし、FOは著しく少ないアテロームLDLサブフラクション(LDLに増加1及びLDL 2オリーブオイル(+ 0.08 + 0.01ミリモル/ L)ベースライン(+ 0.06 + 0.1ミリモル/ L)と比較して)。 |
小型高密度LDL— LDLサブフラクション(LDL1およびLDL2)↓ |
sdLDL小密度低密度リポタンパク質、LDL-C低密度リポタンパク質コレステロール、高密度リポタンパク質コレステロール、PUFA多価不飽和脂肪酸、ALAα-リノレン酸、EPAエイコサペンタエン酸、DHAドコサヘキサエン酸、NMR核磁気共鳴、FO亜麻仁油、mgミリグラム、mmol/lミリモル/リットルあたり、nmナノメートル
果物
果物はフラボノイド、ポリフェノール、食物繊維の豊富な供給源であり、抗酸化特性を有しており、様々な代謝障害に有益な効果があることが報告されている[72-75]。ランダム化3期クロスオーバー試験のデザインでは、ベースラインのLDLを持つ体重過多の45人の参加者が、平均的なアメリカの食事(炭水化物51%、タンパク質16%、脂肪34%、飽和脂肪13%)を摂取して2週間のランイン期間に入った。駆け込み期間後、参加者は、アボカドダイエット(1つの新鮮なHassアボカドに136gの果肉と13gの一価不飽和脂肪酸(MUFA)が含まれている)または低脂肪ダイエット(SFAの代わりに穀物を含む炭水化物59%、タンパク質16%、脂肪24%、飽和脂肪7%)または中等脂肪ダイエット(オレイン酸油、ヒマワリ油、キャノーラ油を多く含む炭水化物49%、タンパク質16%、脂肪34%、飽和脂肪6%)のいずれかを受けるように無作為に割り付けられた。5週間の期間の後、被験者を2週間かけて洗浄し、それぞれの介入についてクロスオーバーさせた。その結果、LDL粒子数と小密LDLコレステロール数は、ベースラインと比較してAV食後に有意に低下した。LDL粒子径はすべての食事で減少したが、LF食事と比較してAV食事はLDL粒子径の有意な上昇をもたらした[76]。対照的な3群クロスオーバー試験では、空腹時グルコースが5.0~6.4 mmol/Lの範囲にある31人の過体重または肥満の被験者が、68g/dの新鮮なアボカドを摂取したハーフアボカド群、または1日あたり136gのアボカドを含むホールアボカド群、または対照群(アボカドなし)のいずれかに無作為に割り付けられた。摂取後6時間後、凍結血漿のNMRスペクトルによりリポタンパク質粒子を測定した。アボカドを丸ごと摂取した群は、対照群と比較してsdLDL粒子の有意な減少を示した[77]。臨床試験では、メタボリックシンドロームの被験者27人をイチゴ群と対照群に分けた。ストロベリー群には2カップのストロベリー飲料と2カップの水が与えられ、対照群には1日4カップの水のみが与えられた。ストロベリーの補給後、対照群と比較してLDL小粒子の濃度が有意に減少したが、LDL平均粒子径は両群間で変化しなかった[78]。最近の研究では、脂質プロファイルが上昇した60人の被験者を、低用量フリーズドライイチゴ(FDS)[LD-FDS;25gのイチゴに2カップの水を加えたもの]または低用量コントロール[LD-C. 4gの食物繊維に20gのサトウキビ糖を加えて2カップの水を加えたもの]または高用量FDS [HD-FDS; 50gのイチゴに2カップの水を加えたもの]、または4)高用量コントロール[HD-C; 8gの食物繊維に36gのサトウキビ糖を加えて2カップの水を加えたもの]のいずれかを12週間摂取させた。その結果、HD-FDS食はHD-C食と比較してLDL小粒子を有意に減少させ、これはLD-FDS食と比較して有意に異なっていたことが示された[79]。無作為化クロスオーバーデザインでは、20人の肥満成人を2つのグループに無作為化し、3週間追跡した。介入群には80gのイチゴパウダーを1日4回、対照群には赤い食用色素で染めたイチゴ風味の製剤を与えた。その結果、介入群では対照群と比較してLDL粒子径が有意に増加した;しかしながら、イチゴ食は小粒LDLの濃度に影響を与えなかった[80]。別のクロスオーバー研究では、24人の肥満成人を介入群(46gのフリーズドライブドウ粉末と1日2回240mlの水)または対照群(46gの果糖、ブドウ糖、有機酸および食物繊維と1日2回240mlの水)のいずれかに無作為に割り付けた。3週間のウォッシュアウト期間で区切られた3週間の介入期間の後、試験群ではLDL粒子径と小粒径LDLの濃度に変化はなかった[81]。脂質異常症患者の治療に対するベルガモットサプリメントの有効性を評価した前向き研究がある。中等度高コレステロール血症の総勢80名の参加者に、Bergavit®(ネオエリオシトリンを16%、ネオヘスペリジンを47%、ナリンジンを37%含有するベルガモットフラボノイド)150mg/日を6ヶ月間投与した。6ヵ月後、Bergavit®サプリメントは、ベースラインと比較してsdLDL-3,-4,および5粒子を有意に減少させた[82]。別の研究では、メタボリックシンドロームとNAFLDを持つ107人の被験者に、ネオエリオシトリン370ppm、ナリン520ppm、ネオヘスペリジン310ppmからなるフラボノイドを含むカプセルに入ったベルガモットポリフェノールフラクション(BPF)1300mg/dを投与した。その結果、BFPによる120日間の介入では、ベースラインと比較してsdLDL粒子が有意に減少することが示された[83](表3)。全体的に、7つの研究のうち6つの研究では果実摂取によりsdLDLが有意に減少し、4つの研究のうち2つの研究ではLDL粒子径が増加した。1つの研究では、sdLDLの有意な減少に加えて、LDL粒子数も減少していた。
表3 小密度低密度リポ蛋白質(LDL)の血漿中濃度、LDL粒子数、LDL粒子径に及ぼす果実の影響
| 著者、年 | 介入 | 1日あたりの用量 | 治療期間 | 科目 | 評価の方法 | 主な成果 | LDLに対する特定の食事成分または栄養補助食品の最終効果(数、サイズ、濃度) |
|---|---|---|---|---|---|---|---|
| Galletti etal。2019 [ 84 ] | Armolipidプラス®(AP) | AP; ベルベリン500mg、紅麹米、モナコリンK 3mg、ポリコサノール10mg | 24週間 | 147人のメタボリックシンドローム患者 | 電気泳動移動度 | ベースラインと比較して、AP錠を服用した後のsdLDL-Cサイズ(+1Å)の有意な上昇。 | LDL粒度↑ |
| 王ら。2015 [ 76 ] |
アボカドダイエット(AV) 低脂肪食(LF) 中脂肪食(MF) |
AV; 新鮮なハスアボカド(136 g / d)またはLF; 59%炭水化物、16%タンパク質、24%脂肪、7%飽和脂肪またはMF; 49%炭水化物、16%タンパク質、34%脂肪、6%飽和脂肪 | 5週間 | ベースラインLDL-Cの45人の太りすぎまたは肥満の被験者 | NMR分光法 |
LDL粒子数(-80.1 nmol / L)小さな高密度LDLコレステロール(-4.1 mg / dL)は、ベースラインと比較してAV食で有意に低かった。 LDL粒子サイズは、LF(-0.24 nm)MF(-0.21 nm)およびAV(-0.12 nm)のすべての食餌で減少したが、LF食餌と比較して、AV食餌はLDL粒子サイズの有意な増加をもたらした(+ 0.12 nm)。 |
小さい高密度LDL ↓ LDL粒子数↓ |
| Park etal。2018 [ 77 ] |
アボカド(ハーフA) アボカド(Whole-A) コントロール |
ハーフA; 68 g、 全体-A; 136 g、 コントロール; 0 g |
食後6時間 | 31人の太りすぎまたは肥満の被験者 | NMR | アボカド全体を消費した後、小さな高密度LDL粒子は、コントロールと比較して大幅に減少した(36.8 nmol / l)。 | 小さい高密度LDL ↓ |
| バス他 2010 [ 78 ] | 苺 | 凍結乾燥したイチゴ50gまたは新鮮なイチゴ3カップ | 8週間 | メタボリックシンドロームの27人の被験者 | NMR |
イチゴの補給は、小さなLDL粒子の濃度の有意な減少(14%)をもたらした。この変化は、対照群と介入群の間の有意差でした。 LDLの平均粒子サイズは2つのグループ間で有意に変化しなかった。 |
小さい高密度LDL ↓ LDL粒子サイズ— |
| バス他 2014 [ 79 ] |
LD-FDS、 LD-C、 HD-FDS、 HD-C |
LD-FDS; 25 g / dイチゴ、 LD-C; 食物繊維4g +サトウキビ20g HD-FDS; 50 g / dイチゴ、 HD-C; 食物繊維8g +サトウキビ36g |
12週間 | 脂質プロファイルが上昇した60人の被験者 | NMR | HD-FDS食は、HD-C食と比較して、小さなLDL粒子(-323±16 nmol / l)を大幅に減少させた。さらに、この変化はLD-FDSと比較して統計的に有意であった。 | 小さい高密度LDL ↓ |
| ズニーノ他 2011 [ 80 ] | いちご粉 | 320g /日の冷凍イチゴ | 3週間 | 20人の肥満被験者 | NMR | LDL粒子サイズは、対照群と比較して介入群で有意に増加した(+ 0.43±0.08nm)。 | LDL粒度↑ |
| ズニーノ他 2014 [ 81 ] | ブドウの粉 | ブドウ粉46g | 3週間 | 24人の肥満被験者 | NMR | ブドウの食事は、小さなLDLおよびLDLサイズに影響を与えなかった。 |
小型高密度LDL— LDL粒子サイズ— |
| Toth etal。2016 [ 82 ] | Bergavit® | 150 mg / dのフラボノイド、16%のネオエリオシトリン、47%のネオヘスペリジン、37%のナリンギン | 6ヶ月 | 中等度の高コレステロール血症の80人の被験者 | ゲル電気泳動 | ベルガビットの補給は、ベースラインよりも小さな高密度LDL-3,-4,および5粒子(それぞれ-38,-53%、-67%)を大幅に減少させた。 | 小さい高密度LDL ↓ |
| Gliozzi etal。2014 [ 83 ] | BPF | 1300mg /日 | 120日 | メタボリックシンドロームとNAFLDの107人の被験者 | NMR分光法 | 小さな高密度LDL粒子は、ベースラインより120日間の介入後に有意に減少した(-374±7 nmol / l)。 | 小さい高密度LDL ↓ |
sdLDL 小密度低密度リポ蛋白、HDL-C 高密度リポ蛋白コレステロール、LDL-C 低密度リポ蛋白コレステロール、NAFLD 非アルコール性脂肪性肝疾患、NMR 核磁気共鳴、FO 亜麻仁油、AP アルモリピッドプラス®。AV アボカドダイエット、LF 低脂肪ダイエット、MF 中脂肪ダイエット、LD-FDS 低用量フリーズドライイチゴ、LD-C 低用量コントロール、HD-FDS 高用量フリーズドライイチゴ、HD-C 高用量コントロール、BPF ベルガモットポリフェノール画分、nmol/l. ナノモル/リットル、nm ナノメートル、Å オングストローム
ナッツ
ナッツには不飽和脂肪、水溶性食物繊維、抗酸化物質、およびフィトステロールが含まれており、これらは血清脂質、血圧、および炎症に有益な影響を及ぼす可能性がある[85]。臨床試験のメタアナリシスでは、ナッツ類の摂取はトリグリセリド、総コレステロール、LDL、およびアポBに対して有意な有益な効果をもたらすと結論づけられている[86]。さらに、以前の系統的レビューでは、ナッツ類、特にアーモンド、ピスタチオ、ブラジルナッツ、ピーナッツ、ヘーゼルナッツは、ナッツ類に含まれる生理活性抗酸化化合物の存在により、酸化LDLからの保護を提供する可能性があることが示された。しかし、クルミのようないくつかのナッツ類では、不飽和脂肪酸の含有量が多いため、酸化に対する感受性を高める可能性がある[87,88]。無作為化クロスオーバー試験では、ピスタチオ補充食(炭水化物50%、脂肪33%、ピスタチオ57g/日を含む)と対照食(炭水化物55%、脂肪30%)を54人の糖尿病予備軍患者に2週間投与し、介入間に2週間のウォッシュアウト期間を設けた。その結果、ピスタチオを添加した食事では対照食事と比較して小粒径のLDL数が有意に減少したが、LDL粒子径は群間で差がなかった[89]。Oliver Chenらは無作為化クロスオーバー介入を実施し、冠動脈疾患患者45人にナッツ類を含まない対照食(National Cholesterol Education Program(NCEP)食)またはNCEP食にアーモンドを1日85g添加した介入食を6週間投与した(それぞれ4週間のウォッシュアウト期間で区切られている)。研究終了時には、アーモンドの消費後の小密度LDL-Cレベルには有意な効果は観察されなかった [90]。単一介入試験デザインでは、21人の健康な成人にヘーゼルナッツを1g/kg/日のヘーゼルナッツ濃縮食を4週間摂取させた。30日後、小LDL値はベースラインと比較して有意に低下した[88]。別の研究では、高脂血症の成人18人(閉経後女性13人、男性5人)を対象に、1)習慣的な食事、2)習慣的な食事にクルミを加えた食事、3)低脂肪の食事、4)低脂肪の食事にクルミを加えた食事の4段階の介入食事療法を順次実施した。それぞれの食事療法を4~6週間実施した。試験終了時には、4つの食事すべてがLDL粒子径に影響を与えなかったが、クルミの補給(48gのクルミ/8460kJのエネルギー摂取量)は、習慣的な食事と比較して小粒LDLのコレステロール分布の有意な減少をもたらした[91]。無作為化4周期クロスオーバー試験では、48人の過体重成人を4群に無作為化し、アーモンド42.5g/d(ALD)ココアパウダー18g/d、ダークチョコレート43g/d(CHOC)アーモンド、ココア、チョコレートの組み合わせ(CHOC+ALD)または対照群として平均的なアメリカ人の食事(AAD)を摂取させた。各介入は4週間で、それぞれの間に2週間のウォッシュアウト期間を設けた。その結果、(CHOC+ALD)群では対照群(AAD)と比較して有意にsdLDL粒子の濃度が低下しており、アーモンド、ココア、チョコレートの組み合わせが冠動脈性心疾患のリスクを改善する効果があることが示唆された[92]。PREDIMED試験では、高脂血症または高血圧の糖尿病患者169人を、地中海食(MeDiet)+エクストラバージンオリーブオイル(EVOO;1L/週)またはMeDiet+クルミ15g、ヘーゼルナッツ7.5g、アーモンド7.5gを含むミックスナッツを1年間摂取する群と、低脂肪食を勧められた対照群に無作為に分けた。試験終了時には、ベースラインと比較して、MeDiet+ナッツは中小LDL(10%)極小LDL(11%)を有意に減少させ、LDLサイズ(+0.2nm)を有意に上昇させた。また、SDLDL粒子量は、MeDiet+ナッツ群では対照群と比較して有意に減少し、LDLサイズの変化の増加は他の群と比較して統計的に有意であった[93]。3期間のクロスオーバー試験では、健康な成人28名を以下の3群に割り付けた。総脂肪(TF)から30%、SFAから8%、ピスタチオから10%のエネルギーを含む1日1食のピスタチオ(1PD)TFから34%、SFAから8%、ピスタチオから 20%のエネルギーを含む2PD(2食のピスタチオ/dまたは63-126 g/d)またはTFから25%、SFAから8%のエネルギーを含む対照食(低脂肪食)の3つのグループに割り付けられた。それぞれの食事は、食事の間に2週間のウォッシュアウト期間を設けて、4週間にわたって実施した。その結果、2PD治療群では、1PD群と対照群の両方と比較してsdLDLが有意に減少していた[94](表4)。全体として、6つの研究のうち5つの研究でナッツ類の消費はsdLDLを有意に減少させた。3つの研究のうち1つの研究でLDLの粒子径が増加し、1つの研究では小さなLDLのコレステロールの分布が減少していた。
表4 ナッツ類の小密度低密度リポ蛋白質(LDL)の血漿中濃度、LDL粒子数、LDL粒子径に及ぼす影響
| 著者、年 | 介入 | 1日あたりの用量 | 治療期間 | 科目 | 評価の方法 | 主な成果 | LDLに対する特定の食事成分または栄養補助食品の最終効果(数、サイズ、濃度) |
|---|---|---|---|---|---|---|---|
| Hernández-Alonsoetal。2015 [ 89 ] |
PD、 コントロールダイエット |
PD; 50%の炭水化物、33%の脂肪、57 g / dのピスタチオを含む コントロールダイエット、55%炭水化物、30%脂肪 |
2週間 | 54人の前糖尿病患者 | NMR | 小さなLDL粒子は、対照食と比較してPDで有意に減少した(変化:-28.07nM対+16.49 nM)が、LDL粒子サイズは2つのグループ間で有意に変化しなかった。 |
小さい高密度LDL ↓ LDL粒子サイズ— |
| Chen etal。2015 [ 90 ] | アーモンド | 85g /日 | 6週間 | 冠状動脈疾患の45人の患者 | オリンパスAU400自動分析装置 | アーモンドの摂取後、低密度LDL-Cに有意な影響は観察されないでした。 | 小型高密度LDL— |
| Yücesanetal。2010 [ 88 ] | ヘーゼルナッツ | 1g / kg /日 | 4週間 | 21人の健康な成人 | ND | 30日後、小さなLDLはベースラインと比較して有意に減少した(-0.04mmol / l)。 | 小さい高密度LDL ↓ |
| Almario etal。2001 [ 91 ] |
HD、 HD + W、 LFD、 LFD + W |
48gのクルミ/ 8460kJのエネルギー摂取量 | 6週間 | 18人の高低血症の成人 | NMR | 4つの食事すべてがLDL粒子サイズに影響を与えなかった。しかし、クルミの補給は、HDと比較して小さなLDLのコレステロールの分布の有意な減少をもたらした(-12.7%)。 |
LDL粒子サイズ— 小さなLDLにおけるコレステロールの分布↓ |
| Lee etal。[ 92 ] |
AAD、 ALD、 CHOC、 CHOC + ALD |
追加; 治療食品なしまたは ALD; 42.5 g / dのアーモンドまたは CHOC; 18g / dのココアパウダーと43g / dのダークチョコレート |
22週間 | 48人の肥満または太りすぎの成人 | ND | ダークチョコレート、ココア、アーモンドを摂取すると、AADと比較して小さなLDL粒子(-6.7 mg / dl)が大幅に減少した。 | 小さい高密度LDL ↓ |
| Damasceno etal。2013 [ 93 ] |
MeDiet + EVOO、 MeDiet +ナッツ、 コントロールダイエット |
(MeDiet + EVOO); 1L /週のエクストラバージンオリーブオイル、または(MeDiet +ナッツ); 30g /日のミックスナッツ(15gのクルミ、7.5gのヘーゼルナッツ、7.5gのアーモンド)またはコントロールダイエット。低脂肪食についてアドバイス | 1年 | 169糖尿病、高脂血症または高血圧 | NMR分光法 |
中小LDL(10%)および非常に小LDL(11%)は、ベースラインと比較して(MeDiet +ナッツ)グループで有意に減少した。ただし、MeDiet +ナッツグループでは、対照グループと比較して、小さな高密度LDL粒子が大幅に減少した。 LDLサイズはベースラインと比較してMeDiet +ナッツグループ(+ 0.2 nm)で有意に増加し、その変化は他のグループと比較して統計的に有意であった。 |
小さい高密度LDL ↓ LDL粒度↑ |
| Holligan etal。2014 [ 94 ] |
1PD、 2PD、 コントロール |
1PD; 1日あたり1サービング(32〜63 g)のピスタチオ(ピスタチオからの10%のエネルギー)(30%の総脂肪と8%の飽和脂肪酸)または 2PD; 1日あたり2サービング(63〜126 g)のピスタチオ(ピスタチオからのエネルギー20%)(総脂肪34%、飽和脂肪酸8%)または コントロール; 低脂肪食(総脂肪25%、飽和脂肪酸8%) |
4週間 | 28人の健康な成人 | ポリアニオンと二価カチオンベースの試薬で凝集体を形成した後、ろ過により血漿から除去し、Cobas6000アナライザーを使用してsdLDLレベルを測定した。 | 2PD治療群は、1PD(-0.14 mmol / l)および対照群(-0.21 mmol / l)と比較して、小さな高密度LDLの有意な減少を明らかにした。 | 小さい高密度LDL ↓ |
sdLDL小密度低密度リポ蛋白、LDL-C低密度リポ蛋白コレステロール、PDピスタチオ補食、HD習慣食、HD+W習慣食+くるみ、LFD低脂肪食、LFD+W低脂肪食+くるみ、AAD平均アメリカ人の食事。ALD アーモンドダイエット、CHOC チョコレートダイエット、MeDiet + EVOO エキストラバージンオリーブオイルを補充した地中海式ダイエット、MeDiet + ナッツを補充した地中海式ダイエット、NMR 核磁気共鳴、mg/dl デシリットル当たりミリグラム、nmol/l。ナノモル/リットル、ミリモル/リットル、ミリモル/リットル、ナノメートル、ND データなし
クルクミン
クルクミンはウコンスパイス(Curcuma longa L.)の有効成分であり、異なる伝統的な医療システムで何世紀にもわたって食品スパイスやハーブレメディとして使用されてきた[95]。その非常に生理活性の高い化合物のため、抗炎症、抗腫瘍、脂質修飾、抗酸化、抗ステアチン、抗線維症、心臓保護、抗血栓作用を含むいくつかの薬理学的効果が報告されている[96-105]。抗動脈硬化作用および心保護作用は、減少したLDL-酸化を介して媒介されると考えられている[106, 107]。最近の報告では、117人のメタボリックシンドローム患者に、1000mg/日のカルクミノイドと5mgのピペリンを8週間摂取させた(介入群)か、5mgのピペリンを比較対照として摂取させた。試験終了時には、ベースラインと比較して介入群でSDLDL値が有意に低下し、両群間でも有意に低下した[97]。無作為化クロスオーバー試験では、治療を受けていない高脂血症の肥満患者30人が、カルクミノイド群(1000mg/日+ピペリン5mg)またはプラセボ群(ピペリン5mg)のいずれかに無作為に4週間割り付けられ、2週間のウォッシュアウト期間を経て、さらに4週間のクロスオーバーが行われた。試験終了時には、クルクミンサプリメントを摂取しても、プラセボと比較してsdLDL濃度に有意な変化は認められなかった[108](表5)。ここでレビューされた2つの研究では、1つの研究でクルクミン補給後にsdLDLが減少した。
表5 小密度低密度リポ蛋白(LDL)の血漿中濃度、LDL粒子数、LDL粒子径に及ぼすクルクミンの影響
| 著者、年 | 介入 | 1日あたりの用量 | 治療期間 | 科目 | 評価の方法 | 主な成果 | LDLに対する特定の食事成分または栄養補助食品の最終効果(数、サイズ、濃度) |
|---|---|---|---|---|---|---|---|
| パナヒ他 2014 [ 97 ] | クルクミノイド-ピペリン | 1000mg /日+ 10mgピペリン | 8週間 | 117人のメタボリックシンドローム患者 | 市販のキットを使用した免疫比濁法(sdLDL) | sdLDLレベルは、ベースラインと比較して介入グループで有意に減少し(-2.73)2つのグループ間で有意差が観察された。 | 小さい高密度LDL ↓ |
| Moohebati etal。2014 [ 108 ] | クルクミノイド-ピペリン | 1000mg /日+ 5mgピペリン | 4週間+2週間のウォッシュアウトフェーズ | 30人の肥満の脂質異常症の被験者 | 免疫比濁アッセイ | プラセボおよびベースラインと比較して、クルクミン補給を受けた後、sdLDL濃度の有意な変化は観察されなかった。 | 小型高密度LDL— |
sdLDL 小密度低密度リポ蛋白質、LDL-C 低密度リポ蛋白質コレステロール、mgミリグラム
その他の栄養補助食品
ウーロン茶
烏龍茶は、ツバキの葉から抽出した部分発酵茶で、ポリフェノール化合物を高レベルで含んでいる。脂質プロファイルを改善することが示されており、特にコレステロールの低下に効果的である[109, 110]。ある臨床試験では、心筋梗塞の既往歴のある患者12名と安定した狭心症の患者10名を2群に分け、対照群として1000ml/日(お茶2袋)のウーロン茶、または水を4週間飲んでもらった。試験終了時には、ベースラインと比較してウーロン茶群で血漿LDL粒子径の有意な増加が認められた[111]。
玄米
玄米は全粒穀物米として、食物繊維、フィチン酸、ビタミンBおよびE、α-トコフェロール、γ-オリザノールおよびγ-アミノ酪酸(GABA)を含む栄養豊富な米である[112]。無作為化比較試験では、42人の糖尿病前体重過多患者を、毎日400gの部分分解玄米(PABR)または白米(WR)に無作為に割り付け、12週間摂取させた。その結果、小粒径LDLと極小粒径LDLの粒子数は、PABR群では有意に減少したが、WR群では増加した[113]。
キトサン
キトサンはキチンの脱アセチル化に由来し、貝類から抽出されたものである。キトサンは抗真菌、抗菌、抗酸化活性を持ち、脂肪吸収を減少させる特性を持っている[114-116]。高コレステロール血症患者を対象としたいくつかのメタアナリシス研究[117]では、キトサンは総コレステロールを減少させるだけであることが示されている。 パイロット研究では、高トリグリセリド血症患者28人に、真菌菌糸体由来のキトサンを1日2錠(125mg/d)を4ヶ月間投与した。その結果、LDL-2サブクラスは4ヶ月間の補給で有意に増加したが、LDLのピーク粒子径とLDLサブクラスは群間で差がなかったことが示された[118]。
L-シトルリン
L-シトルリンはスイカに豊富に含まれる非必須アミノ酸である。心臓・代謝系の健康に対する潜在的な有益な効果[119, 120]が報告されている。最近の研究では、上腕動脈の流量媒介性拡張(5.5%未満)を持つ22人の患者を募集し、800 mg/日のL-シトルリンを8週間服用した。結果は、L-シトルリンの補充はsdLDLレベルに影響を与えなかったことを示した[121]。
アルモリピッドプラス
アルモリピッドプラス®錠には、RYR 200mg(シトリンとアフラトキシンを含まないモナコリンK 3mg)ベルベリン 500mg、ポリコサノール 10mg、葉酸 0.2mg、コエンザイムQ10 2.0mg、アスタキサンチン 0.5mgが配合されている。比較試験では、家族性複合高脂血症患者30名を対象に、4週間のノルマカロリー食(炭水化物54%、タンパク質16%、脂肪30%、食物繊維45~55g/日)のランイン期間を行い、その後、アルモリピドプラス®(1日1錠)群とプラセボ(微結晶セルロース、酸化鉄ブラウン70,コンプリトールE ATO、ステアリン酸マグネシウムを同形状・同味)群に無作為に8週間割り付けた。結果は、Armolipid Plus®が有意にベースラインとプラセボ群と比較してLDLスコアを減少させたことを示した。平均LDLサイズが有意にベースラインからアルモリピッドプラス®グループで増加した一方で、プラセボ[122]と比較して違いはなかった。別のプラセボ対照試験では、メタボリックシンドロームを持つ147人の個人が2つのグループに無作為に割り付けられ、介入グループは24週間の間、対照グループはプラセボのタブレット(微結晶セルロース、酸化鉄茶色)を受け取ったが、Armolipid Plus®の毎日1錠を受け取りました。結果は、Armolipid Plus®を受け取った患者がベースラインと比較して有意に大きいsdLDL-Cサイズを持っていたことを示したが、グループ間の違いは有意ではなかった[84](表6)。
表6 小密度低密度リポ蛋白質(LDL)の血漿中濃度、LDL粒子数、およびLDL粒子径に対する他の特定の食品成分または栄養補助食品の効果
| 著者、年 | 介入 | 1日あたりの用量 | 治療期間 | 科目 | 評価の方法 | 主な成果 | LDLに対する特定の食事成分または栄養補助食品の最終効果(数、サイズ、濃度) |
|---|---|---|---|---|---|---|---|
| 島田ほか 2004 [ 111 ] | ウーロン茶 | 1000ml /日 | 4週間 | 冠状動脈疾患の22人の患者 | 勾配ゲル電気泳動 | 血漿LDL粒子サイズレベルの有意な増加は、ベースラインと比較してウーロン茶群で観察された(25 。 02±0 。 25対67ナノメートル。 31±0 。 60 nm)と | LDL粒度↑ |
| 荒木ほか 2017 [ 113 ] |
PABR、 WR |
400g | 12週間 | 42人の糖尿病前症、太りすぎの患者 | ゲル浸透カラムを備えた高速液体クロマトグラフィー |
PABRグループの小さいLDLと非常に小さいLDLの粒子数の変化は、-13.1±61.7nMと-9.0±26.8nMでしたが、WRグループでは 35.1±60.8nMおよび16.4±32.6nM |
PABR:小さなLDL ↓ PABR:非常に小さいLDL ↓ WR:小さいLDL ↑およびWR:非常に小さいLDL ↑ |
| Rizzo etal。2013 [ 118 ] | キトサン | 125mg /日 | 4ヶ月 | 高トリグリセリド血症の28人の患者 | ページ | LDLピーク粒子サイズとLDLサブクラスは、それぞれ軽度の増加と減少であるが、統計的に有意な変化ではない。 |
LDL粒子サイズ— 小型高密度LDL— |
| 森田ほか 2013 [ 121 ] | L-シトルリン | 800mg /日 | 8週間 | 上腕動脈の血流媒介拡張(FMD)の22人の患者(<5.5%) | リポプリントLDLシステムを使用したLDLサブフラクショネーションの定量的手法 | L-シトルリン補給後のsdLDLレベルに有意な影響は観察されなかった。 | 小型高密度LDL— |
| Gentile etal。2015 [ 122 ] | Armolipidプラス® | 1錠/日 | 4週間 | 家族性複合型高脂血症の30人の患者 | リポプリントシステム(脂質染色血清の電気泳動) |
Armolipidプラス®( ・28%)ベースラインとし、プラセボ群と比較して有意にLDLスコアを減少させた。 大幅Armolipidプラスに増加した平均LDLサイズ®ベースライン(+ 2.7Å)からではなく、グループ間でのグループは有意ではなかった。 |
小さい高密度LDL ↓ LDL粒度↑ |
SDLDL 小密度低密度リポ蛋白質、LDL-C 低密度リポ蛋白質コレステロール、PAGE ポリアクリルアミドグラジエントゲル電気泳動、PABR 部分分解玄米、WR 白米、mg ミリグラム、nm ナノメートル、Å オングストローム
結論
本レビューでは、栄養補助食品および他のダイエット成分のsdLDL、LDL粒子数、およびLDL粒子径に対する効果を、ヒト臨床試験において総合的に評価した。その結果、オメガ3脂肪酸などの上述した栄養補助食品および特定の食事成分のほぼすべてが、LDLバリアントの有益な効果を有することが示された(表1, , 2, 2, , 3, 3, , 4, 4, , , 5, 5, and6)6)。
オリーブオイル、フィトステロール、サイリウム、魚油、EPA、DHA、亜麻仁油、ベルベリン、アボカド、イチゴ、ナッツ類(ピスタチオ、アーモンド、ヘーゼルナッツを含む)クルクミン、ウーロン茶を含むこれらの薬剤のほとんどは、sdLDLレベル、LDL粒子数を減少させたり、LDL粒子径を増加させた(図2)。
しかし、これらの薬剤の多くについては、現在のところ研究が非常に少なく、実施された試験は、試験数、介入期間、またはそのデザインの点で制限されており、無作為化臨床対照試験はほとんど行われていない。LDL粒子が小さく緻密なものほど酸化されやすく,心血管疾患の独立したアテローム性危険因子であることが報告されている。
したがって,sdLDLの低下,LDL粒子数の減少,LDL粒子径の増加に対する有効性を明らかにし,確認し,最適な投与方法を決定するためには,植物由来の治療薬やオメガ3脂肪酸,あるいは他の特定の食品成分を用いたより大規模な臨床試験が必要である。
しかし、本レビューでは、薬用植物、栄養補助食品、オメガ3脂肪酸が、心血管疾患リスクに有益な影響を与えるsdLDLレベル、LDL粒子数、またはLDL粒子径の増加を低下させるための補助的または補完的な治療薬として使用できる天然物としての役割を持っている可能性があることが強調されている。
図2 栄養補助食品や特定の食事成分がsdLDLの減少と心血管疾患(心血管疾患)に及ぼす可能性のある効果を描いた経路の概略
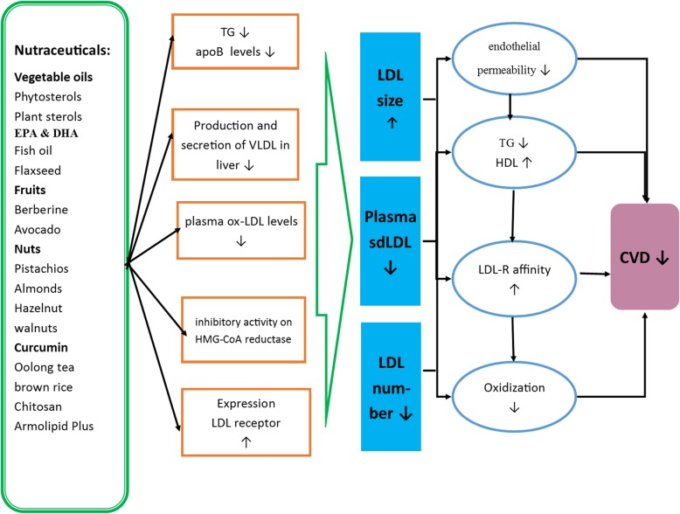
sdLDL:small dense low density lipopoprotein、Apo:apolipoprotein、VLDL:very-low-low-density lipoprotein、LDL-C:low-density lipoprotein chesterolol、心血管疾患:心血管疾患
しかし、本レビューに含まれる研究では、sdLDL値の改善が臨床的影響をもたらすかどうかを評価していないことに注意が必要である。また、sdLDL 値の測定方法が研究間で異なり、結果は直接比較できない可能性がある。したがって、今後、SDLDL値の高い集団における食品素材や栄養補助食品の有効性評価に焦点を当てた研究は、十分なパワーを持ち、確定的な結論を出すことができるようなロバストなデザインで、標準化された方法論を用いてSDLDLを決定することが推奨される。
