Contents
The association between PGC-1α and Alzheimer’s disease
www.ncbi.nlm.nih.gov/pmc/articles/PMC4819073/
要約
アルツハイマー病は神経変性疾患の一つであり、脳内でのアミロイドβペプチドの沈着、慢性炎症、認知機能障害などの病態生理的特徴が報告されている。アルツハイマー病の発症率は世界的に増加しており、研究者は本疾患の理解を深めるために、アルツハイマー病の病態生理の様々な側面について研究を行っていた。これまでのところ、アルツハイマー病の発症機序や予防法は全く知られていない。
ペルオキシソーム増殖因子活性化受容体-γ共活性化因子(PGC-1α)は、下流の遺伝子制御の変化につながる様々な細胞メカニズムに関連するタンパク質である。PGC-1αは、酸化ストレスから細胞を保護し、ミトコンドリア機能障害を軽減することが報告されている。さらに、認知機能に関連する炎症性シグナル伝達やインスリン感受性にも調節的な役割を持つことが実証されている。
ここでは、アルツハイマー病発症におけるPGC-1αの関与についてのさらなるエビデンスを提示する。PGC-1αとアルツハイマー病病態との関係を明らかにすることで、PGC-1αがアルツハイマー病の治療介入のターゲットとなる可能性があることを明らかにした。
キーワード
ペルオキシソーム増殖因子活性化受容体-γ活性化因子(PGC-1α)アルツハイマー病、酸化ストレス、認知機能障害、インスリン抵抗性
序論
アルツハイマー病の発症率は、世界人口の増加に伴い劇的に増加すると予想されている[1,2,3]。ペルオキシソーム増殖因子活性化受容体(PPAR)-γ coactivator-1(PGC-1)ファミリーは、環境ストレスに対する応答を媒介するタンパク質で構成されている[4,5]。
いくつかの研究では、アルツハイマー病患者の脳内でPGC-1αのレベルが明らかに低下していることが報告されている[6,7]。アルツハイマー病脳では、酸化ストレスが核心的な問題とされ、他のアルツハイマー病病態につながると考えられている[8,9]。
PGC-1αは活性酸素種(ROS)の発生に関わる遺伝子の発現を制御し、活性酸素の産生を抑制することで酸化ストレスを予防する[10]。アルツハイマー病では、神経細胞のミトコンドリア生合成の障害は、シナプス機能障害[11]や細胞障害[12]を引き起こし、認知機能の低下に寄与する[13,14]。さらに、アルツハイマー病脳のインスリン抵抗性はアルツハイマー病病態の急速な進行を悪化させる[15,16]。
多くの研究で、PGC-1αがミトコンドリア機能を改善することが示されている[17]と、インスリン感受性を改善することが示されている[18,19]。
本レビューでは、PGC-1αとアルツハイマー病との関連性に関する最近の研究をまとめ、アルツハイマー病病態のメカニズムにおけるPGC-1αの役割について新たな知見を提供する。
PGC-1α
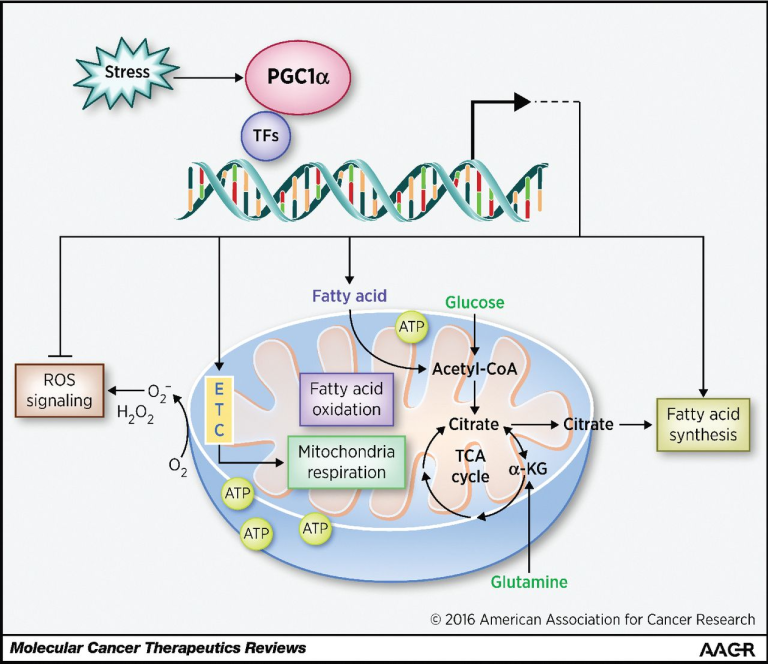
PGC-1αは、温度や栄養状態を含む多くの形態の環境ストレスに高い応答性を示する[4,5]。PGC-1αはまた、多様な環境刺激に応答してミトコンドリアの生合成を制御している[20]。
PGC-1αは、核呼吸因子(NRF)-1,NRF-2,PPARα、PPARδ、PPARγ、エストロゲン関連受容体αを含む様々な転写因子と異性体複合体を形成している[21]。これらのPGC-1α転写活性化複合体は、ヒストン脱アセチラーゼやその小さなヘテロ二量体パートナーなどのリプレッサータンパク質を置換し、それによって遺伝子の活性化を誘導する可能性がある[22]。
PGC-1αは、褐色脂肪組織、骨格筋、脳などのエネルギー需要の高い組織で一般的に発現している[23,24]。脳では、PGC-1αの活性が低下すると、ミトコンドリア機能障害を引き起こして神経細胞の変性を誘発することが知られている[17,25]。PGC-1αノックアウトマウスでは、手足を頻繁につかんでしまうなどの行動異常が見られる[26]。さらに、PGC-1αと、Cre結合タンパク質[27]、cGMP依存性経路[28]、p38-マイトジェン活性化プロテインキナーゼ経路[29]などのシグナル経路との相互作用は、アルツハイマー病における酸化ストレスへの応答において重要な役割を果たしている[30]。
PGC-1αは、活性酸素の解毒を調節する遺伝子に影響を与えることで中心的な役割を果たしている[31]。臨床研究によると、アルツハイマー病患者では健常者に比べてPGC-1αのレベルが低下していることから、PGC-1αはアルツハイマー病における脳機能維持の鍵を握っている可能性があると考えられている[6,7]。このようなエビデンスに基づき、PGC-1αの役割に注目することで、アルツハイマー病病態のメカニズムの理解が深まる可能性がある。
アルツハイマー病におけるPGC-1αと酸化ストレス
アルツハイマー病の顕著な特徴として、酸化ストレス[8]、炎症[32]などの分子異常が挙げられる。これらの特徴のうち、酸化ストレスは、フリーラジカル誘発性細胞障害、DNA酸化、DNA修復異常の引き金になると考えられている[33]。
アルツハイマー病では、酸化ストレスによる神経細胞の損傷が起こる主要な脳領域は海馬と大脳皮質である[34]。対照例と比較して、アルツハイマー病患者はチトクロームcオキシダーゼ[34]などのタンパク質の産生、脂質過酸化[35]の増加など、酸化ストレスの上昇の側面を示している。
したがって、アルツハイマー病のニューロンに設立された酸化的損傷のマーカーは、その病理学の特徴であり、アルツハイマー病の脳の変性の徴候である[36]。アルツハイマー病では、過酸化水素やヒドロキシルラジカルを含む活性酸素のレベルが上昇し、タンパク質を分解することで様々な細胞機能を阻害する[37]。
PGC-1αは、スーパーオキシドジスムターゼ1・2,カタラーゼ、グルタチオンペルオキシダーゼ1などの活性酸素解毒酵素の調節に中心的な役割を果たしている[17]。PGC-1αは、活性酸素形成の直接的な制御因子であるアンカップリングタンパク質2[38]とアンカップリングタンパク質3の発現を調節することが報告されている[39]。さらに、PGC-1αは、活性酸素の発生を減少させるサーチュイン1 [40] およびサーチュイン3 [41] のレベルを制御する [10]。
いくつかの研究では、PGC-1αレベルの上昇は、抗酸化遺伝子の誘導を介して酸化ストレスによるアポトーシスから神経細胞を保護することを実証している[17]。ある研究では、PGC-1α活性の上昇が神経細胞の損失を改善し、神経症状を改善することを示している[42]。
以上のことから、PGC-1αの活性の上昇は、アルツハイマー病における酸化ストレスを減少させることで神経細胞を損傷から保護し、その後、この障害のいくつかの病態生理学的特徴を緩和する可能性があると考えられる。
PGC-1α、ミトコンドリア機能障害、およびアルツハイマー病の認知機能障害
アルツハイマー病では、神経変性とシナプスの劣化は、ミトコンドリアの生合成障害によって引き起こされる[12]。ミトコンドリアは、アルツハイマー病脳における神経細胞のアポトーシスのプロセスにおいて重要な役割を果たしており[43]、活性酸素の生成のための枢要なオルガネラである[44]。ミトコンドリアの機能不全は、アルツハイマー病の中心的な細胞病理の一つと考えられており[45]、様々な経路を通じて認知機能の低下に寄与することが知られている。
アルツハイマー病神経細胞では、ミトコンドリアはアミロイドβ蓄積の部位であり、ミトコンドリアにおけるこれらのアミロイドβ蓄積は最終的に細胞の死をもたらす[46]。障害されたミトコンドリア機能は、エネルギー代謝とATPの生成[47]で深刻な損失につながり、また、アルツハイマー病脳[48,49]で過度の酸化的損傷をトリガするフリーラジカルの消去の欠乏にも。ミトコンドリア機能不全と記憶機能不全との関連は、いくつかのヒトと動物の研究で実証されている[50,51]。
アルツハイマー病では、酸化ストレスの増加[52]やミトコンドリア生合成の障害[53]などのミトコンドリア機能障害が神経変性で起こる[54]。老化した脳では、PGC-1αは老化に関連する因子であるサーチュイン3の発現を調節している[53]。神経変性疾患患者の脳では、PGC-1αの低レベルがミトコンドリア機能不全や酸化ストレスを引き起こすことが観察されている[55,56]。
PGC-1αは神経細胞のミトコンドリア密度を調節しており[57]、PGC-1αノックアウトマウスは脳内のドーパミン作動性神経細胞やグルタミン酸作動性神経細胞の変性に対する感受性の増加を示した[17]。さらに、別の研究では、PGC-1αノックアウトマウスのミトコンドリア遺伝子発現の低下が最終的に神経細胞の機能障害につながることが示されている[26]。
PGC-1αは、認知機能の調節因子として知られているGA結合タンパク質αの発現を細胞培養研究で刺激している[58]。PGC-1αが神経細胞機能において重要な役割を果たしており[59]、ミトコンドリア機能を調節していることを考えると、PGC-1αはミトコンドリア機能障害を改善し、アルツハイマー病における認知機能を改善する可能性があると考えられる。
PGC-1α、インスリン抵抗性、アルツハイマー病における認知機能障害
インスリンは神経伝達物質の放出[60]、神経細胞の生存[61]、シナプス可塑性[62]を調節し、脳の認知と記憶機能を改善する[63,64]。脳内インスリン抵抗性は、脳内へのインスリンの取り込みが低下し、アミロイドβレベルの調節障害や炎症につながると定義されている[65]。
アルツハイマー病では、脳内インスリン抵抗性は疾患の進行に寄与するため、重要な問題である[66]。最近の研究では、アルツハイマー病患者は脳内のインスリンシグナル伝達に欠陥があり[67]、インスリン受容体感受性が低下していることが明らかになった[68]。
PGC-1a遺伝子は、肥満動物[69]や糖尿病マウス[70]では正常動物と比較して高レベルで発現している。PGC-1αは、インスリン抵抗性を打ち消すミトコンドリア生体応答に関与する転写コアクチベーターである[71]。
PGC-1αノックアウトマウスを用いた研究では、高脂肪食にもかかわらず、正常対照動物と比較してインスリン感受性を示した[26]。さらに、PGC-1αは耐糖能、インスリン感受性、糖新生を改善する[18]。PGC-1αがインスリン抵抗性を緩和することを考えると[72]、アルツハイマー病脳のインスリン抵抗性に関連した認知障害を軽減する可能性がある。
おわりに
今回のレビューでは、PGC-1αがアルツハイマー病の病態改善に寄与することを示す最近のエビデンスをまとめた。ここでは、以下の4点に注目している。
- (1)PGC-1αはアルツハイマー病の酸化ストレスから神経細胞を保護し、神経細胞の損傷を防ぐ可能性があること、
- (2)PGC-1αはアルツハイマー病のミトコンドリア機能障害を改善する可能性があること、
- (3)PGC-1αはアルツハイマー病のインスリン抵抗性を低下させる可能性があること、
- (4)最後にPGC-1αはアルツハイマー病に起因する認知機能障害を改善する可能性があること、
の4点を強調した。以上のことから、PGC-1αはアルツハイマー病治療薬として使用できる可能性があると考えられる。