スタチンのベネフィット
スタチンの多面的効果
- 一酸化窒素合成の増加 内皮機能障害の改善
- フリーラジカル放出の阻害
- エンドセリン-1の合成の減少
- LDL-C酸化の阻害
- 内皮前駆細胞のアップレギュレーション
- 炎症細胞数および活性の減少、炎症反応の軽減
- C反応性タンパク質レベルの低下
- マクロファージのコレステロール蓄積の減少
- アテローム性動脈硬化プラークの安定化
- メタロプロテアーゼ産生の減少
- 血小板の接着/凝集の阻害 血栓形成応答の低下
- フィブリノーゲン濃度の低下
- 血液粘度の低下
www.ncbi.nlm.nih.gov/pubmed/15822172/
スタチンのホルミシス効果
スタチンの多面的効果はホルミシス作用によるものか?
スタチンの誘発性のミトホルミシス
CoQ10などの抗酸化剤がスタチン誘発性のミトコンドリア-ホルミシスを妨げる可能性がある。ケルセチンの単独投与では、PGC-1発現、またはミトコンドリアの生合成に影響を及ぼさず、抗酸化物質がミトホルミシスには影響しないことが示唆されている。
www.ncbi.nlm.nih.gov/pmc/articles/PMC3365272/
スタチンによる認知症へ影響
スタチンのアルツハイマー病への保護効果は、コレステロールの低下による脂質代謝の改善だけでは説明できない。マウスの脳ではスタチン投与により、IL-1β、IL-6、およびTNF-αなどの炎症性サイトカインが減少することが示されている。一酸化窒素の合成酵素を促進することにより、血流を改善し保護に働く。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4409455/
高用量スタチンによるsd-LDL、MDA-LDLの減少
高用量スタチン(ロバスタチン)療法は、sd-LDLおよびMDA-LDLを有意に減少させる。
www.ncbi.nlm.nih.gov/pubmed/26162946
スタチンはオートファジーを増加させる?
スタチンはミトコンドリアの生合成を刺激し、断片化を促すが、これはCoq10の補充により妨げられる。スタチンは、ミトコンドリアのオートファジーであるマイトファジーを活性化させことで、損傷したミトコンドリアの排除に役立つ可能性がある。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4208607/
www.ncbi.nlm.nih.gov/pubmed/20135644
www.ncbi.nlm.nih.gov/pubmed/23147595
スタチンはオートファジーを促進して、ヘリコバクター・ピロリ菌を減少させる。
www.ncbi.nlm.nih.gov/pmc/articles/PMC5239775/
スタチンによるアミロイドβクリアランス
スタチンは、、アストロサイトからの細胞外IDE分泌をもたらし、従来のオートファジーと経路とは異なるメカニズムによって細胞外アミロイドβクリアランスを促進する。
www.ncbi.nlm.nih.gov/pubmed/22205103
スタチンによる糖尿病発生率の低下
メタアナリシス スタチン治療による糖尿病患者の冠動脈疾患リスク低減の可能性
www.ncbi.nlm.nih.gov/pubmed/18191683/
www.ncbi.nlm.nih.gov/pubmed/20167359/
スタチンがRAGE受容体を調節に関与している可能性。(RAGEはアルツハイマー病標的候補でもある)
www.ncbi.nlm.nih.gov/pubmed/19485931/
スタチンの糖尿病改善作用がスタチンとアルツハイマー病の交絡因子として作用している可能性がある。
イソプレノイド経路・PPARα
www.pharm.or.jp/dictionary/wiki.cgi?イソプレノイド経路
スタチンの効果は、イソプレノイド経路を介したPPARαの調節による高血圧と関連する全身性の炎症と酸化障害に対する多面的効果の関与が示唆される。
www.ncbi.nlm.nih.gov/pubmed/12065722/
www.ncbi.nlm.nih.gov/pubmed/15337740/
www.ncbi.nlm.nih.gov/pubmed/16397146/
www.ncbi.nlm.nih.gov/pubmed/17309949/
抗炎症性脂質メディエーターSPMの増加
アトルバスタチン・プラバスタチン
アトルバスタチンとプラバスタチンは、n-3DPAをレゾルビンTシリーズに変換する。レゾルビンTシリーズは器官を保護し食作用と細菌の殺傷を強化し、インフラマソームの成分を調節する。
www.ncbi.nlm.nih.gov/pubmed/26236990
www.fasebj.org/doi/full/10.1096/fj.201700268
ロバスタチン
ロバスタチンは、脂質低下作用に加えて、アラキドン酸から15-epi-Lipoxin A4の生成を引き起こし、急性粘膜炎症を減少させた。
www.ncbi.nlm.nih.gov/pubmed/20130564
参考記事:抗炎症性脂質メディエーター(SPM)の神経保護効果/Specialized pro-resolving lipid mediator
スタチンによる認知機能改善 患者特性
プラセボ二重盲検無作為化 軽度から中等度のアルツハイマー病患者(MMSEスコア 12-28)98人 6週間のアトルバスタチン投与(80mg/日)はプラセボと比較して、ADAS-cogスコアの有意な効果が認めれた。以下の特性をもつ患者では、アトルバスタチン治療がより顕著な効果を示した。
- MMSEスコアが高い。
- 200mg/dlを超えるコレステロールレベル
- ApoE4対立遺伝子保有
www.ncbi.nlm.nih.gov/pubmed/16866904
ベースライン時に軽度認知障害(MCI)のない人では認知機能の低下を遅らせる可能性がある。しかしMCIを有する人では、スタチンの認知的保護効果を示さないかもしれない。
www.ncbi.nlm.nih.gov/pubmed/21236699/
メタアナリシス スタチンによる認知症リスク低下
2000年1月から2018年3月に公開された関連研究のメタ分析
916万人の参加者(8万4千人の認知症患者)を含む30件の観察研究
- スタチンを使用した患者は、スタチンを使用しない患者よりも、すべて認知症リスクが低かった。(リスク比[RR] 0.83、95%CI 0.79–0.87、I 2 = 57.73%)。
- アルツハイマー病 RR 0.69(95%CI 0.60〜0.80、p <0.0001)
- 血管性認知症 RR 0.93(95%CI 0.74〜1.16 、p = 0.54)
- スタチンの使用が認知症のリスク低下と有意に関連していることを示唆する。
www.karger.com/Article/Abstract/503105
スタチンBAD 認知機能
スタチン療法は再ミエリン化を阻害する
シンバスタチンが前駆細胞の分化をブロックすることにより、中枢神経系の再ミエリン化を阻害する。中枢神経系における病変の再ミエリン化は、多発性硬化症再発後の神経修復に寄与する。in vivo
www.ncbi.nlm.nih.gov/pubmed/19349355/
スタチンは、ケトン産生を減少する?
スタチンによって阻害されるHMG-CoA還元酵素は、ケトンを生成する酵素でもあることから、ケトンレベルを減少させる可能性が理論的にはある。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4783625/
FDAによるスタチン使用に伴う認知的副作用の警告
コレステロール低下薬であるスタチンの安全情報に、可逆的な認知的副作用(記憶喪失、混乱など)の可能性があることがFDAによって追加された。
www.fda.gov/drugs/drugsafety/ucm293101.htm
スタチンは認知機能を損なうのか? システマチックレビューとメタアナリシス
スタチン治療は、ランダム化比較化試験において、認知障害と関連していなかった。これらの結果から、FDAがスタチンによる認知機能への副作用の警告を継続していくメリットに対して疑問を提起する。
www.ncbi.nlm.nih.gov/pubmed/25575908/
www.ncbi.nlm.nih.gov/pubmed/24095248/
スタチン治療による認知障害の自己報告
スタチンによる認知症的有害事象 スタチンの効果を測定する臨床試験に酸化した170人中128人(75%)の患者が、スタチン療法による記憶または認知障害の自己報告をした。スタチン治療を止めた143人患者のうち128人(90%)が認知障害の改善を報告した。
www.ncbi.nlm.nih.gov/pubmed/19558254/
スタチン関連記憶喪失 60症例の分析および文献のレビュー
患者の50%で認知的副作用
スタチンに関連する記憶喪失を有する60人の患者のうち、36人がシンバスタチン、23人のアトルバスタチン、1人がプラバスタチンを摂取していた。
- 患者の約50%が2ヶ月以内に認知的副作用を認めた。
- 25人の患者のうち14人(56%)が、スタチンの中止に伴って改善を認めた。
- 報告された60の認知試験結果のうち、2件のプラセボ対照試験では、認知症や障害についてスタチンが有益でないことが判明した。
相反する結果
シンバスタチン投与の無作為化比較試験では、脳脊髄アミロイドレベルに影響を与えなかった。
- 小規模の無作為化試験研究において、スタチンを投与された患者は、プラセボを投与された患者よりも低い認知能力を示す傾向を示した。
- 5つの観察研究では、スタチンを投与されている患者の間で認知症のリスクが低いことが分かった。
- 現在の文献では、スタチンが記憶喪失に及ぼす影響に関して、相反した結果が示されている。
- 実験的研究によるとコレステロールの摂取とアミロイド産生との間の関連が支持されており、観察研究では、スタチンを受ける患者が認知症のリスクを低下させることを示している。
- しかし、利用可能な前向き研究では、スタチンによる認知機能改善または抗アミロイド効果は示されていない。
スタチンが認知障害に関連することはまれであるかもしれない症例報告が増加しているが、因果関係は不明なままである。
www.ncbi.nlm.nih.gov/pubmed/12885101/
シンバスタチン誘導性の認知障害
症例報告 シンバスタチンによる認知障害の発症およびスタチン中断による認知障害の逆転
www.ncbi.nlm.nih.gov/pubmed/27048383/
スタチンと認知機能のシステマチックレビュー
公開された文献では、認知機能へのスタチンの有害な効果は示されていない。しかし、高用量スタチンに関して入手可能な強い証拠は限られており、より大規模な質の高い研究設計が必要である。
www.ncbi.nlm.nih.gov/pubmed/24247674/
高齢者へのスタチン投与と認知機能 集団ベース研究
www.ncbi.nlm.nih.gov/pubmed/20413854/
スタチンのリスク
スタチン長期使用は乳がんリスク(2倍)と関連する
症例対照研究 5~10年間スタチンを使用した女性では、侵襲性腺管癌(IDC)のリスクを1.83倍、浸潤性小葉癌(ILC)のリスクを1.97倍の増加と関連していた。親油性スタチンと親水性スタチンの両方の使用者の乳癌リスクが上昇する可能性がある。
スタチン療法による糖尿病のリスクの上昇
しかし心疾患への利益がそれらをうわ回る。
care.diabetesjournals.org/content/early/2014/06/19/dc13-2215
スタチンによるコエンザイムQ10欠乏
より高い用量と効力をもつスタチンによって、必須栄養素であるCoQ10の枯渇による有病率と重症度が用量依存的に高まる。これらはコエンザイムQ10の補充によって、スタチンのコレステロール低下または抗炎症特性に悪影響を与えずに予防が可能。
www.ncbi.nlm.nih.gov/pubmed/14695925/
www.ncbi.nlm.nih.gov/pubmed/22474137/
スタチンはビタミンK2の合成を阻害する
www.ncbi.nlm.nih.gov/pubmed/25655639
www.ncbi.nlm.nih.gov/pubmed/19179058
スタチンによる気分、人格、行動への影響 症例シリーズ
スタチンの使用は暴力的な悪夢、攻撃性、気分、人格の変化、殺人思考、自殺と関連性がある。スタチンは広く許容されている処方薬だが、一部の患者では、深刻な精神病や行動の変化を増加させるリスクの可能性がある処方薬リストに入るかもしれない。
www.ncbi.nlm.nih.gov/pubmed/27747681/
水溶性・脂溶性スタチン
スタチンのBBB透過性の違いによる副作用の差
ロバスタチンおよびシンバスタチンは、睡眠障害などの中枢神経系の副作用を有するが、プラバスタチンはそうではない。スタチンの血液脳関門の透過性の差が、HMG-CoAレダクターゼ阻害剤による中枢神経系副作用と相関することを示している。
www.ncbi.nlm.nih.gov/pubmed/8165193/
横断研究 脂溶性、水溶性スタチン、どちらであるかに関係なくスタチンはアルツハイマー病リスクを低下させる。
www.ncbi.nlm.nih.gov/pubmed/18931004/
スタチンのコレステロール低下強さ
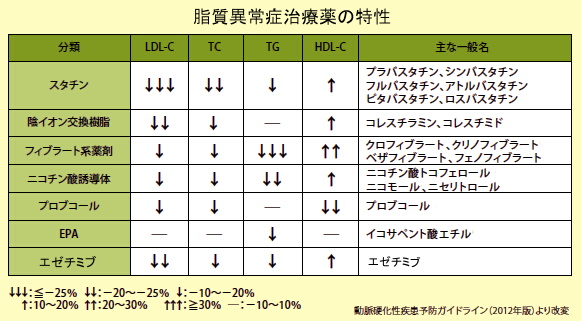
プラバスタチン(水溶性)商品名:メバロチン
スダンダードスタチン 腎排泄、胆汁排出、肝臓への負荷は少ない。薬物相互作用を起こしにくい 最高20mg
副作用:まれ 血清半減期:1.8時間
プラバスタチンの血液脳関門透過性は、スクロースと類似しており、血液脳関門を透過しない。
www.ncbi.nlm.nih.gov/pubmed/8165193/
インビトロでプラバスタチンは内皮細胞機能を増強し、シンバスタチンは内皮細胞のアポトーシスを誘導した。プラバスタチンの神経保護効果は多面的であり、コレステロールレベルの調整とは無関係。
www.sciencedirect.com/science/article/pii/S2452302X17300475
ロスバスタチン(水溶性)商品名:クレストール
- ストロングスタチン 肝排泄、胆汁排泄 最高20mg
- 副作用:肝機能低下 半減期20時間
- 用量反応曲線
www.nature.com/articles/aps2010169
ロスバスタチンはオス、メス両方のマウスのコレステロールレベルを低下させるが、ADマウスのメスのみアミロイドβ産生および老人斑沈着を増強する。
www.ncbi.nlm.nih.gov/pubmed/12885571/
シンバスタチン(脂溶性)商品名:リポバス
スタンダードスタチン 主に肝代謝(主にCYP3A4) 最高20mg
副作用:重篤な肝障害 半減期:2時間
脳のスタチン濃度
シンバスタチン>ロバスタチン>プラバスタチン
www.ncbi.nlm.nih.gov/pubmed/16282522/
シンバスタチン
アミロイドβ42、40レベルを強力に減少させる。in vitro,in vivo
www.ncbi.nlm.nih.gov/pubmed/11296263
ランダム化比較試験 シンバスタチンは軽度のアルツハイマー病患者の脳脊髄液中のアミロイドβ40、42を有意に変化させなかった。
www.ncbi.nlm.nih.gov/pubmed/12205648
アトルバスタチン(脂溶性)商品名:リピトール
ストロングスタチン 肝代謝(主にCYP3A4) 最高20mg
副作用:肝機能低下 半減期13~16時間
メタアナリシス 重篤な副作用および死亡率は、アトルバスタチンとプラセボとの間で統計的に異ならなかった。しかし、副作用および有害事象の数、肝臓機能と関連して、より高い中止率、離脱率および副作用がプラセボ群と比較してアトルバスタチン群で見出された。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4308807/